Гематоэнцефалический барьер это кратко
Обновлено: 05.07.2024
Но диагностика инсульта мозга у новорождённых — лишь первый этап. Главный вопрос — как лечить и как предупредить это заболевание. Детский и взрослый инсульты — разные! Мы знаем, какие факторы провоцируют развитие инсульта у взрослых — к примеру, гипертензия. Но для малышей эти факторы не так актуальны, и даже такие очевидные на первый взгляд причины, как родовые травмы, не вошли в лидирующую десятку провокаторов инсульта у детей.
Почему инсульты мозга у новорождённых и взрослых так различаются? После появления на свет мозг ребёнка ещё продолжает развиваться, причём особенно интенсивно в первые дни после рождения. В настоящий момент не существует тактики лечения инсульта мозга у новорождённых. Мало зная об этом заболевании у младенцев, врачи вынуждены применять к ним терапию, показанную для взрослых. Она оказывается неэффективной, а иногда даже мешает выздоровлению. Успех в лечении таких детей — зачастую случайность, а не результат заранее спланированной тактики врача.
Возникло предположение, что многие препараты, которые существуют в арсенале врача для лечения инсульта, просто не доходят до мозга новорождённого из-за капризного гематоэнцефалического барьера, который закрывается и не даёт поработать препаратам.
В экспериментальной медицине платформа для изучения любых болезней — моделирование патологии на животных. Среди существующих на сегодняшний день моделей инсульта ни одна не пригодна для новорождённых.
Есть два типа инсульта — ишемический, когда сосуды мозга сужаются, что ограничивает его питание и кровоснабжение, и геморрагический, когда сосуды рвутся без явных на то причин. У новорождённых преобладает второй тип инсульта. Однако модели, традиционно применяемые для изучения геморрагического инсульта, работают по принципу механического введения крови в мозг экспериментальных животных, что сильно ограничивает исследовательские возможности.
На биологическом факультете Саратовского государственного университета им. Н. Г. Чернышевского разработали модель инсульта, с помощью которой можно увидеть, как сосуды мозга разрываются самостоятельно, без дополнительных вмешательств. Для этого используется звуковой стресс (120 дБ, 7 Гц). Звуковые волны за счёт способности глубоко проникать в мозг нарушают центры регуляции его кровотока.

Появление голубого окрашивания тканей мозга у взрослой (справа) и у новорождённой (слева) крыс на фоне развития инсульта и введения красителя Evans blue
А теперь посмотрим, как работает гематоэнцефалический барьер при развитии геморрагического инсульта и как эти процессы отличаются друг от друга в первые дни после рождения лабораторного животного и в последующем его развитии.
Оказалось, внутривенное введение красителя крысам на фоне развития инсульта сопровождается появлением голубой окраски тканей мозга только у взрослых, но не у новорождённых особей.
Мы исследовали, какие вещества проходят через гематоэнцефалический барьер в условиях, когда организму необходимо бороться с инсультом. Для этого использовали флуоресцентные метки — лёгкие (декстран 3 кДа) и тяжёлые (декстран 70 кДа), которые своим свечением подсказывают нам их местонахождение и помогают определить путь движения.

Лёгкие флуоресцентные метки (декстран 3 кДа) распределены по-разному: у взрослой крысы (слева) — распределение по всему мозгу, а у новорождённой (справа) — концентрирование в сосуде на фоне развития инсульта мозга
Как оказалось, у взрослых крыс мозг при инсульте как решето: пропускает даже высокомолекулярные соединения (декстран 70 кДа). А у новорождённых декстрановые флуоресцентные метки застревают в сосудах: барьер закрывается так плотно, что даже низкомолекулярные соединения (декстран 3 кДа) остаются в пределах сосудов и не попадают в мозг.

Экспрессия структурных белков гематоэнцефалического барьера — окклудина и клаудина-5 у новорождённых и взрослых крыс (более тёмные полоски отражают более высокую экспрессию)
Исследования проводились на биологическом факультете Саратовского государственного университета им. Н. Г. Чернышевского в рамках проекта Российского научного фонда (№14-15-00128) и гранта Президента РФ (МД-2216.2014.4).
Гематоэнцефалический барьер мозга - гистология, проницаемость, функции
Гематоэнцефалический барьер разграничивает нервную систему от общего кровотока, обеспечивая постоянную и оптимальную по химическому составу среду для ее функционирования.
Межклеточная жидкость занимает 15 % общего объема мозга и окружает нейроны и нейроглию. Схема межклеточных пространств представлена на рисунке ниже. Секретируемая сосудистыми сплетениями спинномозговая жидкость циркулирует в системе желудочков и субарахноидальном пространстве и через пахионовы грануляции проникает в синусы твердой мозговой оболочки.
Единственная составляющая спинномозговой жидкости, которая не проникает через гематоэнцефалический барьер,— метаболическая жидкость. В ее состав входят нейромедиаторы, высвобожденные нейронами и не подвергнувшиеся обратному захвату, что обусловливает наличие неспособных преодолеть гематоэнцефалический барьер медиаторов и их метаболитов в субарахноидальном пространстве.
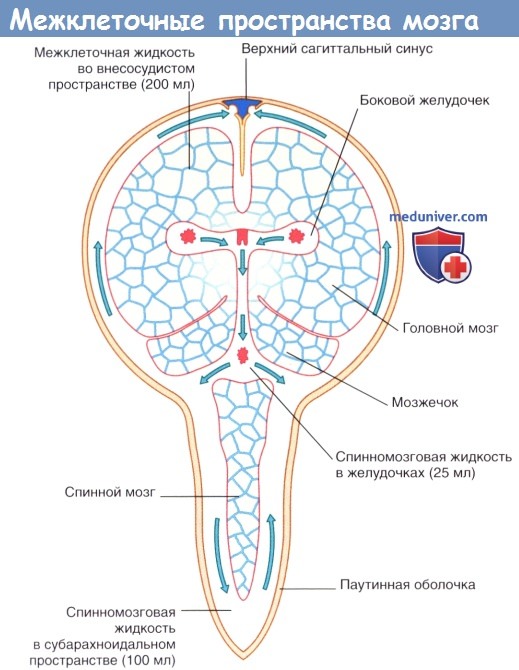
Межклеточные пространства головного мозга.
Стрелками показаны направления циркуляции спинномозговой жидкости.
Компоненты спинномозговой жидкости распределены следующим образом (по результатам поясничной пункции):
• жидкость, продуцированная клетками сосудистых сплетений, — 60 %;
• жидкость, продуцированная клетками капилляров, — 30 %;
• метаболическая жидкость — 10%.
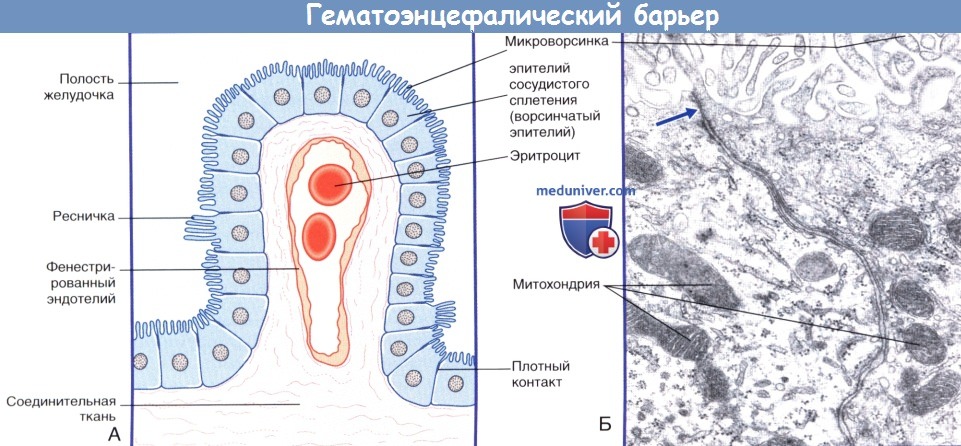
(А) Схематическое изображение барьера между кровью и спинномозговой жидкостью.
(Б) Ультраструктура эпителия сосудистого сплетения. В эпителиальных клетках расположены множество митохондрий и гранулярная эндоплазматическая сеть.
Клетки соединены плотными контактами в апикальной части.
Гематоэнцефалический барьер состоит из двух компонентов. Первый представлен барьером между кровью и спинномозговой жидкостью на уровне сосудистых сплетений, а второй — барьером между кровью и межклеточной жидкостью на уровне капилляров ЦНС.
а) Барьер между кровью и спинномозговой жидкостью. Барьер между кровью и спинномозговой жидкостью представлен эпендимальным эпителием сосудистых сплетений, который характеризуется следующими особенностями строения.
1. Практически все реснички замещены микроворсинками.
2. Клетки образуют плотные контакты. Именно эти места плотного соединения мембран клеток разграничивают кровь и спинномозговую жидкость.
3. Клетки эпителия содержат ферменты, обеспечивающие транспорт ионов и продуктов метаболизма.
б) Барьер между кровью и межклеточной жидкостью. Барьер между кровью и межклеточной жидкостью представлен эндотелием капилляров ЦНС, который характеризуется следующими особенностями строения.
1. Эндотелиоциты образуют плотные контакты.
2. В состав клеток входит небольшое количество пиноцитозных пузырьков, а также отсутствуют фенестрации.
3. Транспортные системы в клетках аналогичны таковым в эпителии сосудистых сплетений.
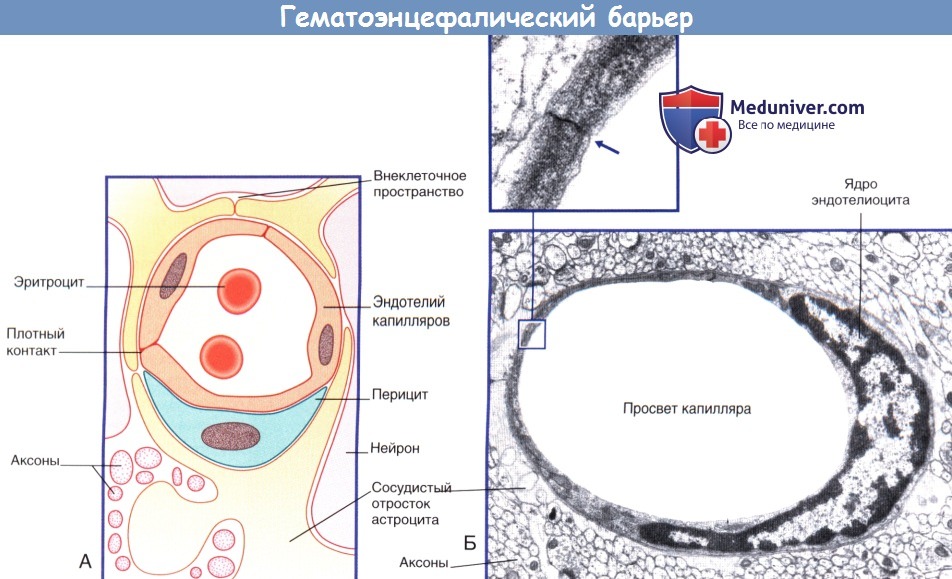
(А) Схема барьера между кровью и межклеточной жидкостью.
(Б) Капилляр центральной нервной системы. На поперечном срезе показан одиночный эндотелиоцит, полностью окружающий просвет сосуда.
Края эндотелиоцитов образуют плотный контакт. Эндотелиоцит окружен базальной мембраной. Капилляр окружен отростками астроцитов.
в) Функции перицитов капиллярного русла. Перициты и клетки эндотелия связаны с помощью щелевидных контактов. В ходе исследований культур клеток было достоверно доказано, что перициты играют ключевую роль в ангиогенезе капилляров, а также в формировании и поддержании плотных контактов между эндотелиоцитами.
Перициты принимают участие в саморегуляции мозгового кровотока за счет того, что на их поверхности экспрессируются рецепторы к вазоактивным медиаторам: норадреналину, вазопрессину, ангиотензину II. При хронической артериальной гипертензии развиваются гипертрофия и гиперплазия перицитов, а также происходит внутриклеточная продукция цитоплазматических сократительных филаментов, что обеспечивает компенсаторное расширение капилляров.
Поверхность клеточной стенки перицитов способна обеспечивать связывание протромбинового комплекса, за счет чего перициты могут принимать участие в процессе свертывания крови.
Кроме того, перициты обладают способностью к фагоцитозу и свойствами иммунорегуляторных цитокинов.
Общая площадь капиллярного русла головного мозга соответствует размерам теннисного корта! Наличие такой огромной поверхности объясняет тот факт, что мозг потребляет 20 % поступающего кислорода. Плотность капилляров коры головного мозга можно оценить на изображении латексного слепк.
г) Функции гематоэнцефалического барьера:
• Контроль проникновения метаболических веществ. Основной источник питания нейронов — глюкоза. При повышении уровня глюкозы в крови специфический белок-переносчик связывает ее, а при низком уровне — обеспечивает более активный захват.
• Контроль транспорта ионов. Nа + /К + -АТФ-аза клеток гематоэнцефалического барьера осуществляет транспорт ионов Na + в спинномозговую жидкость, а ионов К + —в кровь.
• Предотвращение поступления в мозг токсических веществ и периферических нейромедиаторов, выделяемых вегетативными нервными окончаниями в системный кровоток.
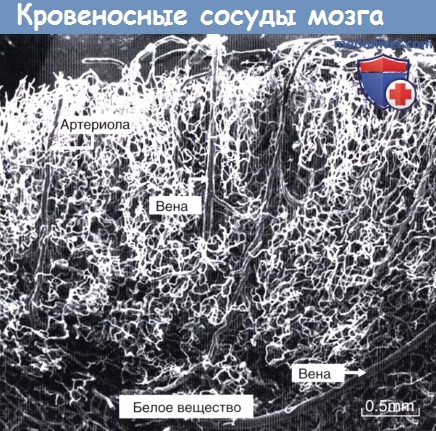
Латексный слепок сосудов препарата мозга.
Корковые капилляры имеют вид извилистых белесоватых нитей.
д) Состояния, связанные с нарушением гематоэнцефалического барьера:
1. Пациенты с артериальной гипертензией подвержены приступам гипертонической энцефалопатии в связи с тем, что степень повышения давления превосходит компенсаторные способности стенок артериол. Вследствие такого повышения давления может произойти нарушение плотных межклеточных контактов эндотелия капилляров, что приводит к отеку мозга за счет быстрого выхода плазмы. Клинически эта ситуация проявляется сильной головной болью, рвотой и, в некоторых случаях, появлением судорог и развитием комы.
2. У пациентов с повышенным содержанием углекислого газа в крови (при заболеваниях дыхательной или сердечно-сосудистой системы, а также после хирургических вмешательств) причиной отека мозга даже при нормальном уровне артериального давления может стать расслабление мышечного слоя артериол. Данная ситуация клинически проявляется спутанностью сознания и сонливостью, в дальнейшем переходящими в кому.
3. Повреждения мозга (травмы или спонтанные кровоизлияния) приводят к отеку мозга вследствие осмотического повреждения тканей мозга (и других факторов).
4. Инфекционные заболевания мозга или его оболочек сопровождаются нарушением гематоэнцефалического барьера, предположительно из-за усиленного перемещения лейкоцитов в капиллярном русле мозга. Несостоятельность гематоэнцефалического барьера играет и положительную роль: стенки капилляров проницаемы для жирорастворимых антибиотиков.
Кроме того, капилляры опухолей мозга характеризуются наличием фенестраций, что позволяет идентифицировать злокачественное новообразование при помощи рентгеноконтрастного вещества, неспособного пройти через капилляры непораженных отделов мозга.
е) Резюме. Гематоэнцефалический барьер - барьер между кровью и спинномозговой жидкостью представлен эпителием сосудистых сплетений (видоизмененным эпендимным эпителием) желудочков мозга. Барьер между кровью и межклеточной жидкостью представлен эндотелием капилляров мозга.
Нормальная деятельность головного мозга возможна лишь в условиях биохимического и электролитного гомеостаза (равновесия). Поэтому жизненно необходимо, чтобы мозг был надежно защищен от попадания веществ, способных изменить работу центральной нервной системы. Для этого и существует гематоэнцефалический барьер, или сокращенно ГЭБ.
Для чего нам нужен ГЭБ
ГЭБ сохраняет специфическую внеклеточную среду вокруг нейронов, поддерживая концентрацию аминокислот, аскорбиновой и фолиевой кислот даже при снижении их концентрации в сыворотке крови.
Кроме того, абсолютно необходимо, чтобы никакие патогенные микробы не могли попасть в головной мозг. Иначе наступает катастрофа. Типичный пример: микроб менингита, так называемый менингококк, вполне мирно может проживать в носоглотке, но при ослаблении защитных сил (и нарушении проницаемости ГЭБ) менингококк попадает в центральную нервную систему, поражая оболочки головного мозга и вызывая потенциально смертельную болезнь — гнойный менингит.

Повышение проницаемости ГЭБ также характерно и для других заболеваний нервной системы. Например, при рассеянном склерозе активированные Т-лимфоциты легко преодолевают ГЭБ и вызывают поражение мозга.
Как ГЭБ работает на практике
Проницаемость гематоэнцефалического барьера напрямую зависит от величины молекул. Маленькие молекулы кислорода, углекислого газа проходят вообще без проблем. Но чем крупнее молекула вещества, тем труднее ей пробраться. Впрочем, существуют способы облегчить эту задачу. Например, давно замечено, что жирорастворимые вещества диффундируют через барьер на ура. Это свойство используется при создании некоторых лекарств, например снотворных барбитуратов.
ГЭБ и фармакология

Антибиотикам желательно добраться до мозга при инфекционных поражениях, противоконвульсивным препаратам — для лечения судорог и, уж конечно, нейролептикам — для купирования острых психозов. Эффективность вышеперечисленных препаратов напрямую зависит от проницаемости ГЭБ.
А вот при болезни Паркинсона, для которой характерен недостаток допамина в мозге, не удастся восполнить этот дефицит ни таблетками, ни уколами, потому что допамин через ГЭБ, к сожалению, не проходит. Хотя, например, предшественник допамина — Л-допа — способен преодолеть ГЭБ. Но все-таки это не совсем то, что нужно.
Кстати, похожая ситуация при депрессиях, в патогенезе которых большую роль играет глютамат. Глютамат также не проникает через через ГЭБ. Поэтому глотать его бессмысленно.
Когда ГЭБ может рухнуть?
Существует ряд ситуаций, при которых страдает ГЭБ и мозг остается незащищенным. Это может случиться при высоком артериальном давлении, поэтому стоит держать его под контролем. Внутривенное введение гиперосмолярных растворов также несет в себе угрозу нарушения барьера. Длительное воздействие микроволнового излучения и радиации доказанно считается причинами нарушений ГЭБ. Инфекции центральной нервной системы типично дают сбои в работе барьера. Также нарушения возможны при травмах мозга, его ишемии, воспалении и инсультах.
А если ГЭБ не пускает, но нам очень нужно?

Маннитол открывает ГЭБ примерно на час, и за это время опухоль подвергается воздействию химиотерапии. С уходом маннитола дверь в мозг закрывается. И правильно — нельзя оставлять мозг без защиты.
Информация для простого пациента

Гематоэнцефалический барьер (ВВВ) является критической границей между центральной нервной системой (ЦНС) и периферией. ВВВ одновременно и "друг", и "враг" врачу - клиницисту. Защищая ЦНС от воздействия потенциально вредных веществ, находящихся в системном кровообращении, ВВВ одновременно представляет собой серьезное препятствие для доставки и поступления лекарств в ЦНС.
Анатомически, BBB представляет собой обширную сеть микрокапилляров протяженностью ~ 650 км, каждый из которых имеет диаметр просвета ~ 6 мм и окружен одиночной, эндотелиальной клеткой, люминесцентная и абламинальная (мозговая оболочка) мембраны разделены на 300-500 нм цитоплазмы. Вещества, пытающиеся перейти из системного кровообращения в ткань мозгуа должны либо пройти через парацеллюлярный путь ( как бы между влеток) или через трансцеллюлярный путь, проходя через микрососудистые эндотелиальные клетки. Парацеллюлярная диффузия водорастворимых веществ и малых ионов строго ограничена плотными соединениями (TJs), которые как бы соединяют мембраны эндотелиальных клеток для , чтобы физически закрыть межэндотелиальный разрыв. Вещества , пытающиеся пройти через мембрану микрососудистых эндотелиальных клеток, активно высвобождаются обратно в капиллярный просвет с помощью встроенных транспортеров оттока или воздействуют на различные метаболизирующие фермент - совокупные усилия "пассивной обструкции" (TJs).
Гематоэнцефалический барьер (BBB) - это не статическая анатомическая граница, а динамический интерфейс, способный быстро реагировать на стрессоры, включая гипоксию, воспаление, травму и боль. Повреждение целостности ВВВ подвергает мозг потенциально опасным концентрациям веществ , находящихся в периферическом кровообращении (например, ионы, аминокислоты, нейротрансмиттеры, белки и другие макромолекулы), которые могут нарушать гомеостаз мозга и отрицательно влиять на активность нейронов. Поврежденный парацеллюлярный проход лекарственных средств, нутрицевтиков или ксенобиотиков в мозг после нарушения "пассивной обструкции" (TJ) может привести к значительным побочным эффектам препарата и / или неблагоприятным взаимодействиям лекарственных средств. Альтернативно, нарушение BBB может включать патологически повышенный "отток" лекарственного средства из тканей мозга через микрососудистую (просветную ) мембрану, что приводит к снижению концентрации и эффективности лекарственного средства, находящегося в тканях мозга.
Учитывая наличие множества типов клеток, внутри- и внеклеточных сигнальных путей и взаимодействующих белков, липидов и углеводов, участвующих в образовании, поддержании и нарушении различных барьерных функций, выполняемых ВВВ, сегодня разработано и множество подходов к диагностике нарушений ВВВ и терапевтическому воздействию на гематоэнцефалический барьер ( BBB) как в области патологии , так и в аспекте терапии болезней с целью оптимизации доставки лекарств в ЦНС. На молекулярном уровне предложен подход, направленный на воздействие на функции конкретного белка, важного для биохимии ВВВ (например, транспортера эффлюка, компонента TJ), что является прямой модуляцией его активности и / или транскрипции генов. Альтернативным подходом улучшения доставки лекарств для ЦНС через ВВВ , является нацеленность на обмен белками и их местоположением , в результате чего изменение местоположения белка используется в качестве средства модуляции его активности. Можно привести два примера с участием P-гликопротеина-транспортера, используемого для "оттока" лекарственного средства и транслюмбронного белка окклюдина TJ, которые демонстрируют потенциал терапевтической модуляции индуцированных патологией изменений в обмене белками BBB с целью оптимизации доставки лекарственного средства в ЦНС в присутствии стрессоров (например, периферическая воспалительная боль, гипоксия).
P-гликопротеин (ABCB1 / MDR1) является выдающимся молекулярным открытием доставки лекарственного средства в ЦНС через ВВВ. Стратегически обогащенный на мембране церебральных микрососудистых эндотелиальных клеток, P-гликопротеин использует энергию от АТФ-гидролиза, чтобы вытеснить лекарства обратно в микрокапиллярный просвет против крутых градиентов концентрации.
P-гликопротеиновые субстраты имеют массу от 300-4000 Да и включают анальгетики, противораковые препараты и иммунодепрессанты, психотропные средства, антибиотики, антиаллергенные средства, противоэпилептические препараты , бета-блокаторы, стероидные гормоны и ингибиторы протеазы ВИЧ-1. Несмотря на интенсивные исследования, усилия сосредоточенные на разработке ингибиторов Р-гликопротеина, а также клинические испытания включающие прямое ингибирование Р-гликопротеина в значительной степени оказались неудачными в плане повышения терапевтической эффективности. Высокие дозы ингибитора, по-видимому, здесь необходимы, но , к сожалению, приводят к системному токсикозу. Более того, полное ингибирование P-гликопротеина может быть опасным для жизни из-за отсутствия защиты от потенциально опасных веществ, передающихся через кровь. В настоящее время усилия ученых направлены на выявление целевых показателей терапии в рамках нескольких сигнальных путей, которые способствуют связанным с болезнями изменениям активности P-гликопротеина.
Исследователями было обнаружено, что начало периферической воспалительной боли (экспериментально вызванное инъекцией λ-каррагинана в задней лапы животного ) наблюдается в течение трех часов за счет увеличения оттока морфина, связанного с P-гликопротеином, через гематоэнцефалический барьер ( BBB). Эти данные показали , что боль, вызванная процессом воспаления, сама по себе препятствует способности клинически значимых антиболевых препаратов , таких как морфин , поступать в ткани мозга. Воспаление, вызванное повреждением ткани, способствует выраженности послеоперационной боли, и поэтому вывод об увеличении оттока морфина с помощью P-гликопротеина через BBB может частично объяснить трудности с достижением послеоперационной опиоидной анальгезии.
Учитывая тот факт , что диета, воздействие окружающей среды или внешние стрессоры могут быстро повышать концентрацию потенциально вредных веществ в системном кровообращении, можно предположить , что по мере развития P-гликопротеина для выполнения столь значимой барьерной роли для ВВВ, этот механизм должен также обеспечить своевременную доставку достаточного количества P-гликопротеина в микрососудистую люминесцентную мембрану для борьбы с какой-либо угрозой.
Трансмембранный протеин - окклюдин является значимым для барьерной функции при TJs между микрососудистыми эндотелиальными клетками гематоэнцефалического барьера (BBB), а изменение концентрации окклюдина от TJs является чувствительным, ранним и надежным признаком открытия TJ и дисфункции ВВВ. Способность быстро закрывать нарушения ВВВ (т. е. его повышенной проницаемости ) при TJs, которые наблюдаются во время окислительного стресса (например, вследствие инсульта), будет препятствовать развитию опасного для жизни отека головного мозга и проникновению в ткани ЦНС нейротоксичных веществ, передающихся через кровь. Периферическая воспалительная боль, индуцированная в трех разных экспериментальных моделях (формалин, каррагенан и полный адъювант Фрейнда), способствовала развитию дисфункции ВВВ, характеризующейся повышенной проницаемостью парацеллюлярных клеток к сосудистым маркерам, таким как сахароза. Было также обнаружено, что периферическая воспалительная боль способствует увеличению проницаемости парацеллюлярной расщелины для опиоидного анальгетического кодеина.
Кодеиновая анальгезия опосредованно централизована, что требует ее накопления в головном мозге, что и происходит при пассивной парацеллюлярной диффузии. Неконтролируемое увеличение потребления мозгом кодеина во время периферической воспалительной боли из-за патологического увеличения парацеллюлярной проницаемости может привести к значительным побочным эффектам ЦНС, связанным с опиоидами, такими как угнетение дыхания, зависимость и повышенная толерантность.
Гематоэнцефалический барьер (ВВВ) представляет собой физический и метаболический барьер, который отделяет ЦНС от периферического кровообращения. Доставка лекарств в ЦНС (CNS) через BBB является сложной задачей, в первую очередь из-за физического ограничения парацеллюлярной диффузии между эндотелиальными клетками, которые содержат микрососуды ВВВ, и активности транспортеров оттока, которые быстро вытесняют обратно в капиллярный просвет широкий спектр ксенобиотиков. В заключении отметим, что терапевтическое манипулирование трафиком P-гликопротеинов представляет собой относительно недорогой и неспецифический подход для усиления доставки лекарств в ЦНС (множества лекарств) и выбора оптимальных комбинаций лекарственных средств. Субстратами, влияющими на активность Р-гликопротеиновой транспортной системы, являются дигоксин, циметидин, такролимус, нифедипин, кетоконазол и амитриптилин.
Нифедипин - селективный блокатор кальциевых каналов II класса, производное дигидропиридина. Тормозит поступление кальция в кардиомиоциты и клетки гладкой мускулатуры сосудов. Оказывает антиангинальное и гипотензивное действие.

Так выглядит строение головного мозга
Гематоэнцефалический барьер в нашем организме — это такая структура, которая защищает наш мозг от всего, что может ему навредить. Иногда этот барьер ломается и уже не может останавливать всё, что в мозг попадать не должно. И в этом случае случается воспаление.
Но воспаление — это штука, которую делает иммунная система. А за ГЭБ иммунной системы нет — ведь мозг функционирует автономно и независимо от остальных систем в организме. Как тогда получается, что люди умирают от менингита и энцефалита?
Дело в том, что иммунитет за ГЭБ всё-таки есть — правда, свой собственный. Поэтому там могут развиваться воспалительные процессы. Медицина уже очень много знает и умеет, но тёмных пятен в истории с иммунной системой в мозге ещё предостаточно — кстати, это перспективное поле для получения Нобелевской, если вы вдруг планировали.
Что такое воспаление
Воспаление — это такой процесс, который запускает иммунная система организма, чтобы защититься от повреждения или от действия патогенного раздражителя, а потом восстановить повреждённую область. Если разложить воспаление по пунктам, то получим такую последовательность:
- Альтерация: когда повреждаются ткани.
- Экссудация: когда жидкость и клетки крови выходят из сосудов и попадают в ткани и органы, формируя отёк.
- Пролиферация: когда клетки начинают размножаться и восстанавливается целостность ткани.
Повреждённые воспалительным процессом клетки начинают выделять эйкозаноиды и цитокины, иммунные клетки получают сигнал, что им пора включаться в работу и тут же устремляются к месту событий.
Если очень коротко про иммунную систему и зачем она нужна: это такая сложная структура, которая защищает организм от инфекций и патогенов. Основа вакцинации — это иммунологическая память, когда организм учится развивать более сильный иммунный ответ после встречи с патогеном.
На этой схеме можно увидеть, где внутри нас живёт иммунная система:

Как видно, здесь не отмечен головной мозг, а статья у нас про его воспаление. Возникает вопрос — а как и почему тогда мозг умеет воспаляться и как там работает иммунная система?
Что такое головной мозг и как в нём работает иммунная система
Чуть отойду от темы, чтобы объяснить, насколько мозг — важная штука. Мне нравится аналогия с компьютером. Мозг — это центральный процессор. Неважно, в каком у нас состоянии мышка и клавиатура, если вдруг с процессором что-то не так. Полетел процессор — летит к чертям всё остальное.
Так же и в организме — от функционирования головного мозга зависит работа вообще всего. Поэтому очень важно, чтобы он был максимально изолирован от лишнего, но при этом, например, имел источник бесперебойного питания — глюкозу. Глюкозу мозгу получать можно и нужно, а вот, например, иммуноглобулины в мозг проникать не должны. Это такие крупные белковые клетки, которые, попав в мозг, начали бы развивать в нём бурную деятельность — аутоиммунные реакции, например. То есть мозг должен быть защищён от разных процессов в иммунной системе, которые распознают его ткань как чужеродную.
Так вот, фейсконтролем, фильтрующим кому можно войти, а кому нельзя, у мозга служит гематоэнцефалический барьер. Это умная структура, которая разделяет кровеносную систему и центральную нервную систему. Главная задача ГЭБ — обеспечить автономность и саморегуляцию головного мозга, выстроив барьер между кровью и спинномозговой жидкостью.
Гематоэнцефалический барьер

Строение ГЭБ
Так как ГЭБ не пропускает антитела и антигены, и у мозга нет своей лимфатической системы, внутри этого автономного государства сформировалась собственная иммунная система.
Кирпичики, из которых она строится:
- Лимфоидные клетки спинномозговой жидкости (Т- и В-лимфоциты и их субпопуляции), естественные киллерные клетки, моноциты и макрофаги.
- Глиальные клетки нервной ткани (клетки микроглии и астроциты) и клетки эндотелия мозговых сосудов.
- Гуморальные факторы, биологически активные вещества.
Первая группа клеток несёт специфические иммунные функции и умеет формировать локальный иммунный ответ в спинномозговой жидкости и ЦНС.
Астроциты и микроглия запускают механизм врождённого иммунитета, что, по сути, и есть основная защита мозга от инфекций. Клетки микроглии первыми реагируют на прямое повреждение ЦНС.
В третью подсистему входят гормоны (тимозин), медиаторы, пептиды, цитокины.
Получается, что внутри ЦНС сформировалась своя автономная иммунная система, которая умеет быть практически независимой от центральной иммунной системы. Тема эта в научном мире на самом деле всё ещё животрепещущая, нейрофизиологи до сих пор выдвигают теории по иммунным реакциям в мозге.
Какие бывают воспалительные процессы в мозге
Технически процесс воспаления в головном мозге начинается так же, как и в любом другом месте. Но так как иммунная система там специфическая, то проходит он по-другому.
Что может воспалиться? Может произойти воспаление оболочек головного мозга — это менингит. А могут воспалиться и внутренние структуры мозга — это энцефалит.
Про менингит

Менингококки — это грамм-отрицательные диплококки (когда две бактерии — кокки — сложены парой). Очень похожи на два зёрнышка внутри ягоды кофейного дерева. На этом снимке менингококки в спинномозговой жидкости.
Менингококк прилично вирулентен, передаётся воздушно-капельным путём и хорошо тропен к мозгу. Поражает такая инфекция преимущественно детей (чаще до 5 лет) и подростков — это больше 70% от общего числа больных. Дети в такой зоне риска находятся потому, что у них ещё несостоятельный иммунитет, и менингококк летит туда, как в удобную мишень. В зоне риска и иммуннокомпрометированные пациенты, это те, кто получает иммуносупрессивную терапию (например, при онкологии). Сюда же пойдут возрастные группы пациентов от 65 лет, с учётом хронических заболеваний.
Основные симптомы менингита: сильная головная боль, высокая лихорадка, изменённое состояние сознания (от ступора до комы), чувствительность к свету и звуку. Появляется специфическая звёздчатая сыпь. Ещё один яркий признак — ригидность затылочных мышц. Это когда они становятся настолько каменно-твёрдыми, что если попытаться пациента поднять за шею, то он поднимется весь, шея не сгибается. По сути, он превращается в одну сплошную доску. Происходит так потому, что вместе с головным мозгом воспаляется спинной.
По этиологии менингиты бывают разные: бактериальный (как раз менингококковый), вирусный (например, краснуха), грибковый, смешанный и другие типы.
Львиная доля менингитов — менингококковые. У нас со статистикой не очень, но вот, например, в США 13 процентов всех менингитов приходятся на менингококковую инфекцию. Это на самом деле колоссальное число.
У бактериального менингита есть разные возбудители, и то, какой именно поразил заболевшего, в основном зависит от возраста. У новорождённых и младенцев, например, бактериальный менингит чаще всего вызывают стрептококки группы B (в частности Streptococcus agalactiae), Escherichia (E.) coli (и другие грамотрицательные бактерии), Listeria monocytogenes.
А младенцев старшего возраста, детей и молодых людей чаще всего атакуют Neisseria meningitidis и Streptococcus pneumoniae. Менингит от последней порой приводит к смерти в течение нескольких часов. Сепсис, который вызван этой бактерией, может стать причиной коагулопатии и двустороннего геморрагического инфаркта надпочечников (синдром Уотерхаус — Фридериксена).
Haemophilus influenzae типа Б — в прошлом главная причина менингита у детей до 6 лет и среди других возрастов. Сегодня же это редкая причина в США и Западной Европе, где от этой бактерии масштабно проводится вакцинация (кроме тех местностей, где население не вакцинируется, — там в группе риска в большой степени дети от 2 месяцев до 6 лет).
Среди взрослых людей среднего возраста и старшего поколения наиболее распространённая причина бактериального менингита — S. Pneumoniae. У людей всех возрастов иногда вызывает менингит Staphylococcus aureus.
Как выявляют менингит?
У пациента берётся спинномозговая пункция. Это когда вводят иглу в полость между мягкой и паутинной мозговыми оболочками головного и спинного мозга и делают забор спинномозговой жидкости. Кстати, пациенту может стать чуть легче от самого процесса забора пункции — мы дренируем часть жидкости, отчего снижается давление и резко отпускает мучительная головная боль.

Забор люмбальной пункции выглядит вот так. Красно-коричневое — это дезинфицирующий раствор йодопирона.
Анализируем клетки, которые в ней содержатся, и понимаем, с чем имеем дело. Иногда может оказаться, что это не воспаление, а, например, опухоль — симптомы бывают очень похожие.
Как лечить?
Если мы видим у пациента все симптомы, которые я перечислил, то в первую очередь назначаем антибиотик широкого спектра. Когда мы берём спинномозговую пункцию, то должны обязательно сделать культуральный посев. Он готовится, к сожалению, несколько суток. Такой роскоши, как ждать несколько дней, у нас точно нет, поэтому антибиотик назначаем, не дожидаясь результата пункции.
Если подтверждается менингит, то пациенту будет назначено минимум три антибиотика. Скорее всего, и что-то противогрибковое. Например, противогрибковый препарат Флюконазол.
Если менингит вирусный, то основное лечение будет направлено на патогенетическую терапию. Это, в первую очередь, инфузионная терапия — когда мы вводим в кровоток определенные растворы, чтобы скорректировать или предотвратить патологические потери организма. Очень важный момент — диуретическая терапия. Мы даём пациенту диуретики, которые дают головному мозгу убирать лишнюю спинномозговую жидкость, потому что там, где воспаление, всегда много жидкости. Диуретики тормозят реабсорбцию воды и солей и делают мощный мочегонный эффект, мы сливаем лишнюю жидкость и восполняем новые жидкости через капельницы.

Так выглядит система для внутривенного вливания
На первое место выходят препараты, которые хорошо проходят через гематоэнцефалический барьер.
Коротко — да. Проницаемость ГЭБ была нарушена и менингококк, который при нормальном функционировании ГЭБ не пройдёт через барьер, проникает в мозг.

Пример того, как лейкоциты проникают через ГЭБ
Точный механизм проникновения менингококков через ГЭБ до конца не изучен, но на это влияют воспалительные процессы. Например, воспаление, вызванное листериями, может привести к тому, что ГЭБ станет для них проницаемым. Пневмококки, например, выделяют особый фермент, который делает эндотелий пористым. Через эти поры и проникает бактериальный агент.
Последствия менингита
При менингите может пострадать абсолютно всё. Слух, зрение, опорно-двигательный аппарат. После менингококка движение ликвора по спинному и головному мозгу может быть затруднено. Это в свою очередь сопровождается гидроцефальным синдромом — повышение внутричерепного давления. Не тот вымышленный синдром, который раньше всем подряд детям ставили, а настоящий гипертензионно-гидроцефальный синдром, который сопровождается головной болью, постоянной астенией и не купируется анальгетиками. Менингит может закончиться инвалидизацией или летальным исходом.
Про энцефалит и энцефалитного клеща
Энцефалит — это когда воспаляются внутренние структуры мозга. Энцефалиты бывают разные: вирусные, микробные, аллергические, инфекционные, токсические.
Вы, наверное, практически все слышали про энцефалитного клеща. Даже Сплин про него пел.
Выглядит он вот так:

Иксодовый клещ, переносчик клещевого энцефалита
В Сибири, например, вообще нет регионов, в которых бы не было эндемичности к энцефалитному клещу. В Московской области есть два эндемичных района: Дмитровский и Талдомский.
Что делать, если укусил клещ? Его нужно аккуратно снять и отнести в лабораторию на микробиологическое исследование. Если вдруг обнаруживается, что вам достался именно энцефалитный клещ, то нужно срочно бежать к врачу-инфекционисту. В этом случае проводится экстренная профилактика иммуноглобулином против клещевого энцефалита, причем важно, чтобы это было сделано не позднее 96 часов с момента присасывания клеща.
Симптомы клещевого энцефалита: лихорадка, интоксикация, поражение серого вещества мозга и его оболочек (а это уже как раз менингит, или менингоэнцефалит). Из последствий могут быть очень стойкие неврологические и психиатрические осложнения, и даже летальный исход.
Носителями вируса, по статистике, являются шесть клещей из ста, а вот заболеть от энцефалитного клеща могут не все — опять же, по статистике, это от 2 до 6% укушенных людей.
Как обезопасить себя от воспалений головного мозга
Чтобы научить организм делать то, что он в заводской комплектации не всегда умеет — например, давать правильный иммунный ответ после встречи с патогеном — мы делаем вакцинацию.
Какие бывают вакцины против клещевого энцефалита:
- Клещ-э-вак — самая популярная отечественная вакцина.
- FSME-IMMUN.
- Энцевир нео.
- Encepur.
Ещё бывает экстренная вакцинация, которая делается, если вы собираетесь ехать в эндемичную зону. Здесь делаются 2 прививки с разницей в 2 недели. Защитный уровень антител появляется в организме спустя 14 дней от введения 2-й вакцины. Ревакцинация тоже делается через 12 месяцев.
После трёх доз вакцинации защитный уровень антител сохраняется в организме приблизительно 3 года — поэтому ревакцинацию нужно делать каждые три года.
Вакцинация против менингококковой инфекции
Вакцины, которые защищают организм от менингококков, называются Менактра и Бексеро. Бексеро не сертифицирована в России, но у нас можно поставить Менактру.
Менактрой можно прививаться в возрасте от 9 месяцев до 55 лет, а Бексеро — для детей от 2 месяцев.
Итого
В головном мозге сформирована своя автономная иммунная система. Гематоэнцефалический барьер, как такая селективная Великая китайская стена, не пропускает к мозгу вещества, которые могут нарушить его работу, и пропускает то, что необходимо для его функционирования — например, глюкозу. Иногда ГЭБ пропускает не то, что хотел бы, а то, что считают нужным врачи. Например, средство для наркоза — пропофол — выключает пациента буквально за несколько ударов сердца с момента введения. Он неполярный и легко проходит через барьер. Часто это, наоборот, становится проблемой, если препарат нужно доставить в мозг, а через ГЭБ он проходит очень плохо. В таких случаях иногда приходится вводить антибиотики или химиотерапевтические препараты сразу в ликвор, с помощью люмбальной пункции, а не внутривенно.
Иногда в работе ГЭБ случаются сбои, что делают этот барьер проницаемым и приводит к развитию воспалительных процессов внутри головного мозга.
Менингиты и энцефалиты могут привести к тяжёлым последствиям, вплоть до инвалидизации и летальных исходов. Чтобы обезопасить себя, нужно вакцинироваться.
Читайте также:

