Физический смысл поверхностного натяжения кратко
Обновлено: 02.07.2024
Поверхностное натяжение – стремление жидкости сократить свою свободную поверхность, т.е. уменьшить избыток своей потенциальной энергии на границе раздела с газообразной фазой.
Опишем механизм возникновения поверхностного натяжения в жидкостях. Жидкость, в отличие от газов, не заполняет весь объем сосуда, в который она налита. Между жидкостью и газом (или паром) образуется граница раздела, которая находится в особых условиях по сравнению с остальной массой жидкости. Рассмотрим две молекулы A и B. Молекула A находится внутри жидкости, молекула B – на ее поверхности (рис. 1). Молекула A окружена другими молекулами жидкости равномерно, поэтому силы, действующие на молекулу A со стороны молекул, попадающих в сферу межмолекулярного взаимодействия, скомпенсированы, или, другими словами, их равнодействующая равна нулю. Молекула B с одной стороны окружена молекулами жидкости, а с другой стороны – молекулами газа, концентрация которых значительно ниже, чем концентрация молекул жидкости. Так как со стороны жидкости на молекулу B действует гораздо больше молекул, чем со стороны газа, равнодействующая всех межмолекулярных сил уже не будет равна нулю и будет направлена внутрь объема жидкости. Таким образом, для того чтобы молекула из глубины жидкости попала в поверхностный слой, нужно совершить работу против не скомпенсированных межмолекулярных сил. А это означает, что молекулы приповерхностного слоя, по сравнению с молекулами внутри жидкости, обладают избыточной потенциальной энергией, которая называется поверхностной энергией.

Очевидно, чем больше площадь поверхности жидкости, тем больше таких молекул, которые обладают избыточной потенциальной энергией, а значит тем больше поверхностная энергия. Этот факт можно записать в виде следующего соотношения:
где поверхностная энергия жидкости, площадь свободной поверхности жидкости и коэффициент пропорциональности, который называется коэффициентом поверхностного натяжения.
Коэффициент поверхностного натяжения
Коэффициент поверхностного натяжения – это физическая величина, которая характеризует данную жидкость и численно равна отношению поверхностной энергии к площади свободной поверхности жидкости:
![]()
![]()
.
Коэффициент поверхностного натяжения жидкости зависит: 1) от природы жидкости (у «летучих жидкостей таких, как эфир, спирт, бензин, коэффициент поверхностного натяжения меньше, чем у «нелетучих – воды, ртути); 2) от температуры жидкости (чем выше температура, тем меньше поверхностное натяжение); 3) от свойств газа, который граничит с данной жидкостью; 4) от наличия поверхностно-активных веществ таких, как мыло или стиральный порошок, которые уменьшают поверхностное натяжение. Также следует отметить, что коэффициент поверхностного натяжения не зависит от площади свободной поверхности жидкости.
Из механики известно, что равновесным состояниям системы соответствует минимальное значение ее потенциальной энергии. Вследствие поверхностного натяжения жидкость всегда принимает форму с минимальной поверхностью. Если на жидкость не действуют другие силы или их действие мало, жидкость будет стремиться принимать форму сферы, как, например, капля воды, мыльный пузырь. Также будет вести себя вода в невесомости. Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, сокращающие (стягивающие) эту поверхность. Эти силы называютсясилами поверхностного натяжения.
Поэтому коэффициент поверхностного натяжения можно также определить как модуль силы поверхностного натяжения, действующей на единицу длины контура, ограничивающего свободную поверхность жидкости:
![]()
Наличие сил поверхностного натяжения делает поверхность жидкости похожей на упругую растянутую пленку, с той только разницей, что упругие силы в пленке зависят от площади ее поверхности (т.е. от того, как пленка деформирована), а силы поверхностного натяженияне зависятот площади поверхности жидкости. Если положить швейную иглу на поверхность воды, поверхность прогнется и не даст ей утонуть. Действием сил поверхностного натяжения можно объяснить скольжение легких насекомых таких, например, как водомерки, по поверхности водоемов (рис.2). Лапка водомерки деформирует водную поверхность, увеличивая тем самым ее площадь. Вследствие этого возникает сила поверхностного натяжения, которая стремится уменьшить подобное изменение площади. Равнодействующая сил поверхностного натяжения будет направлена вверх, компенсируя при этом силу тяжести.

На действии сил поверхностного натяжения основан принцип действия пипетки (рис.3). Капелька, на которую действует сила тяжести, вытягивается вниз, тем самым увеличивая площадь своей поверхности. Естественно, возникают силы поверхностного натяжения, равнодействующая которых противоположна направлению силы тяжести, и которые не дают капельке растягиваться. При нажатии на резиновый колпачок пипетки, создается дополнительное давление, которое помогает силе тяжести, в результате чего капля падает вниз.

Примеры решения задач
| Задание | Тонкое алюминиевое кольцо радиусом 7,8 см соприкасается с мыльным раствором. Каким усилием можно оторвать кольцо от раствора? Температуру раствора считать комнатной. Масса кольца 7 г. |
| Решение | Выполним рисунок. |

На кольцо действуют следующие силы: сила тяжести " width="34" height="22" />
, сила поверхностного натяжения >_s" width="25" height="26" />
и внешняя сила " width="17" height="23" />
.
Так как кольцо соприкасается с раствором и внешней и внутренней сторонами, то сила поверхностного натяжения равна:
Длина контура, ограничивающего поверхность жидкости в данном случае равна длине окружности кольца:
С учетом последнего сила поверхностного натяжения:
Условие отрыва кольца от поверхности раствора имеет вид:
![]()
.
![]()
Переведем единицы в систему СИ: радиус кольца ^\ m;" width="228" height="20" />
масса кольца ^" width="152" height="20" />
кг.
![]()
| Задание | Какое количество энергии освобождается при слиянии мелких водяных капель радиусом мм в одну каплю радиусом 2 мм? |
| Решение | Изменение потенциальной энергии поверхностного слоя капель, обусловленное уменьшением площади поверхности капель при их слиянии в одну каплю равно: |
![]()
где площадь поверхности всех мелких капель, площадь поверхности большой капли, коэффициент поверхностного натяжения воды.
где r — радиус маленькой капли, R — радиус большой капли, n — количество маленьких капель.
Масса маленькой капли:
![]()
масса большой капли:
![]()
Так как маленькие капли сливаются в одну большую каплю, можно записать:
![]()
откуда количество маленьких капель:
![]()
а площадь поверхности всех маленьких капель:
![]()
Теперь найдем количество энергии, которое освобождается при слиянии капель:
![]()
![]()
.
Переведем единицы в систему СИ: радиус маленькой капли ^\ mm=2\cdot ^\ m;" width="247" height="19" />
радиус большой капли ^\ m" width="123" height="17" />
.
![]()
| Задание | Определить коэффициент поверхностного натяжения масла, плотность которого равна , если при пропускании через пипетку масла получено 304 капли. Диаметр шейки пипетки 1,2 мм. |
| Решение | Капля масла отрывается от пипетки, когда сила тяжести равна силе поверхностного натяжения: |
Учитывая, что масса капли
где плотность масла, объем капли,
а сила поверхностного натяжения
откуда объем капли:
![]()
Полный объем масла:
![]()
откуда коэффициент поверхностного натяжения масла:
![]()
![]()
Переведем единицы в систему СИ: плотность масла /^3>=910\ /;" width="247" height="21" />
объем масла ^3=4\cdot ^\ m^3;" width="209" height="19" />
диаметр шейки пипетки \cdot ^m" width="216" height="20" />
.
![]()

Почему мыльные пузыри круглые, а водомерки не тонут? Все это следствия одного и того же физического явления, без которого вода не была бы водой.
О чем эта статья:
Понятие и характеристики поверхностного натяжения
С явлением поверхностного натяжения жидкости мы сталкиваемся каждый день:
- капли воды стремятся принять форму, близкую к шарообразной (а в невесомости они совсем шарообразные);
- струя воды из-под крана стремится к цилиндрической форме;
- булавка не тонет на поверхности воды в стакане;
- многие насекомые могут скользить по поверхности воды.
Силы поверхностного натяжения действуют вдоль поверхности жидкости, стремясь сократить ее площадь. Как будто жидкость заключена в упругую пленку, которая стремится сжать свое содержимое.
Потенциальная энергия взаимного притяжения молекул жидкости примерно равна их кинетической энергии. Это позволяет веществу сохранять объем (но не форму), и этот объем ограничивается поверхностью жидкости.
На молекулу жидкости, которая находится внутри, действуют силы притяжения со стороны других молекул, и они уравновешивают друг друга. А на ту молекулу, что находится на поверхности, действуют силы притяжения не только со стороны других молекул жидкости, но и со стороны газа (внешней среды). Эти вторые значительно меньше первых, поэтому равнодействующая сила притяжения направлена внутрь жидкости, что способствует удержанию молекулы на поверхности.
Поверхностное натяжение — это величина, которая показывает стремление жидкости сократить свою свободную поверхность, то есть уменьшить избыток своей потенциальной энергии на границе раздела с газообразной фазой.
Чем больше площадь поверхности жидкости, тем больше молекул, которые обладают избыточной потенциальной энергией, и тем больше поверхностная энергия. Этот факт можно записать в виде следующего соотношения:
Поверхностная энергия жидкости
W = σS
W — поверхностная энергия жидкости [Дж]
S — площадь свободной поверхности [м 2 ]
σ — коэффициент поверхностного натяжения [Н/м]
Отсюда мы можем вывести формулу коэффициента поверхностного натяжения.
Коэффициент поверхностного натяжения — это физическая величина, которая характеризует данную жидкость и численно равна отношению поверхностной энергии к площади свободной поверхности жидкости.
Коэффициент поверхностного натяжения
σ = W/S
W — поверхностная энергия жидкости [Дж]
S — площадь свободной поверхности [м 2 ]
σ — коэффициент поверхностного натяжения [Н/м]
Коэффициент поверхностного натяжения жидкости зависит:
- от природы жидкости;
- температуры жидкости;
- свойств газа, который граничит с данной жидкостью;
- наличия поверхностно-активных веществ (например, мыло или стиральный порошок), которые уменьшают поверхностное натяжение.
Коэффициент поверхностного натяжения не зависит от площади свободной поверхности жидкости, хотя может быть рассчитан с ее помощью.
Если на жидкость не действуют другие силы или их действие мало, жидкость будет стремиться принимать форму сферы, как капля воды или мыльный пузырь. Так же ведет себя вода в невесомости. Жидкость ведет себя так, как будто по касательной к ее поверхности действуют силы, стягивающие эту поверхность. Эти силы называются силами поверхностного натяжения.
Сила поверхностного натяжения
F = σl
F — сила поверхностного натяжения [Н]
l — длина контура, ограничивающего поверхность жидкости [м]
σ — коэффициент поверхностного натяжения [Н/м]
В химической промышленности в воду часто добавляют специальные реагенты-смачиватели, не дающие ей собираться в капли на какой-либо поверхности. Например, их добавляют в жидкие средства для посудомоечных машин. Попадая в поверхностный слой воды, молекулы таких реагентов заметно ослабляют силы поверхностного натяжения, вода не собирается в капли и не оставляет на поверхности пятен после высыхания.
Поверхностное натяжение некоторых жидкостей на границе с воздухом
Поверхностное натяжение, 10 −3 Н/м
Хлорид натрия (водный раствор)
Азотная кислота 70%
Серная кислота 85%
Пример решения задачи
Тонкое алюминиевое кольцо радиусом 7,8 см соприкасается с мыльным раствором. Каким усилием можно оторвать кольцо от раствора? Температуру раствора считать комнатной. Масса кольца 7 г. Коэффициент поверхностного натяжения мыльного раствора при комнатной температуре равен 4 × 10 -2 Н/м.
Решение

На кольцо действуют сила тяжести, сила поверхностного натяжения и внешняя сила, с которой отрывают кольцо от раствора.
Так как кольцо соприкасается с раствором и внешней и внутренней сторонами, то сила поверхностного натяжения удваивается:
Контур, ограничивающий поверхность жидкости, имеет форму окружности. Значит, его длина будет равна:
Подставляем в формулу силы поверхностного натяжения:
Условие отрыва кольца от поверхности раствора имеет вид второго закона Ньютона для инерциальных систем отсчета:
Подставляем силу поверхностного натяжения:
F = 0,007 × 10 + 4 × 4 × 10 -2 × 3,14 × 7,8 × 10 -2 = 0,11 Н
Ответ: Для того, чтобы оторвать кольцо от раствора, необходимо приложить силу в 0,11 Н.
Важность поверхностного натяжения
Выше мы уже показали, что поверхностное натяжение встречается в повседневной жизни достаточно часто. Но на самом деле оно встречается еще чаще!
В некоторых отраслях промышленности поверхностное натяжение используют как простой показатель загрязнения продуктов. Поскольку оно определяется на молекулярном уровне, любое изменение компонентов вещества может привести к изменению этого показателя. То есть если мы знаем, каким должно быть поверхностное натяжение совершенно чистого вещества, то по отклонению от этой нормы мы можем установить уровень его загрязнения.
Не только человек, но и представители живой природы используют физические явления в своих целях. Например, за счет поверхностного натяжения насекомые водомерки могут перемещаться по водной глади, не промочив лапки. Конечности водомерки отталкивают воду и захватывают воздух, что позволяет насекомым продавливать поверхность воды, не нарушая ее.
За счет поверхностного натяжения возникает такое любопытное явление, как ламинарное течение. Это упорядоченный режим течения вязкой жидкости или газа, при котором соседние слои жидкости не перемешиваются. Выглядит ламинарная струя так, как будто вода застыла.
И это еще не все: поверхностное натяжение позволяет предметам плавать, благодаря ему выживают и развиваются экосистемы, и даже состав воды стабилен только за счет этого явления. Без него вода бы постоянно находилась на границе двух агрегатных состояний: испарялась и вновь конденсировалась, так как молекулы легко выскакивали бы с ее поверхности.
Поверхностное натяжение имеет двойной физический смысл — энергетический (термодинамический) и силовой (механический) . Энергетическое (термодинамическое) определение: поверхностное натяжение — это удельная работа увеличения поверхности при её растяжении при условии постоянства температуры. Силовое (механическое) определение: поверхностное натяжение — это сила, действующая на единицу длины линии, которая ограничивает поверхность жидкости.
молекулы воды притягиваются друг у другу. В поверхностном слое притяжение действует только в одну сторону, из-за чего, возникают забавные штуки
Поверхностное натяжение - это мера сил сцепления поверхностного слоя жидкости: чем прочнее межмолекулярные связи, тем больше поверхностное натяжение, тем прочнее плёнка на поверхности. Например, за счёт водородных связей между молекулами воды плёнка становится столь прочной, что по ней могут бегать насекомые.
Софа! Ты мыльные пузыри пускала ,? В этом смысл натяжения жидкости. Чем плотнее жидкость тем больше поверхность натяжения. Чем круче мыльный раствор тем больше пузыри. А капля глицирина -пузыри будут с твой рост. А попробуй просто из воды выдуть пузырь. Это простой пример.
Поверхностное натяжение относится к числу наиболее важных свойств дисперсных систем и является основной термодинамической характеристикой поверхности раздела. Рассмотрим наиболее простой случай – поверхностное натяжение жидкости на границе с газом (рис. 2.1).
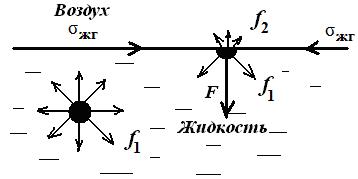
Рис. 2.1. Межмолекулярное взаимодействие
внутри жидкости и на поверхности раздела фаз
На молекулу, находящуюся внутри жидкости, действуют силы взаимного притяжения (силы молекулярного сцепления) со стороны всех окружающих ее соседних молекул. Равнодействующая этих сил равна нулю вследствие симметрии силового поля, и для перемещения молекулы внутри жидкости не требуется затрачивать работу. Это вызвано тем, что в газообразной фазе молекулы удалены друг от друга на большие расстояния, и действующие между ними силы взаимного притяжения очень малы. Молекулы, находящиеся на границе раздела фаз, испытывают действие межмолекулярных сил в большей степени со стороны жидкой фазы f1, чем со стороны газообразной f2(f1 >> f2). Результирующая сила F, пропорциональной разности сил (f1 – f2), направлена внутрь жидкости. Эта сила, отнесенная к единице поверхности (1 м 2 или 1 см 2 ), называется внутренним (молекулярным) давлениемpM:
Молекулярное давление определяется силой сцепления молекул, оно тем выше, чем полярнее вещество, так для H2O величина рМ равна 14000 атм, для C6H6 – 3800 атм. Таким образом, на поверхности любой жидкости существует огромное давление, вызванное нескомпенсированностью молекулярных сил сцепления в поверхностном слое и стремящееся затянуть все молекулы с поверхности внутрь жидкой фазы. Этим объясняется шарообразная форма капель жидкости.
Поверхностный слой вследствие нескомпенсированности молекулярных сил имеет избыточную свободную энергию по сравнению с объемом жидкости. Этот избыток свободной энергии, отнесенный к единице поверхности (1 м 2 или 1 см 2 ), называется удельной свободной поверхностной энергией (поверхностным натяжением). Весь избыток поверхностной энергии заключен в слое толщиной в 1 молекулу. Наличие на поверхности раздела фаз избытка энергии означает, что для образования новой поверхности требуется совершить работу.
Поверхностное натяжение ( ) – работа обратимого изотермического процесса, затраченная на образование единицы площади поверхности раздела фаз (энергетическое определение поверхностного натяжения):
Знак минус говорит о том, что положительная работа совершается при уменьшении или сокращении поверхности.
Силовое определение: поверхностное натяжение– сила, направленная тангенциально (параллельно) к поверхности и приходящаяся на единицу длины периметра, ограничивающего эту поверхность.
Физическая сущность – поверхностные молекулы стремятся уйти вглубь конденсированной фазы, тем самым, сжимая поверхность.
Оба эти определения необходимо рассматривать в единстве. Такое единство энергетического и силового подходов сложилось исторически. Величина поверхностного натяжения была введена в физику задолго до появления понятия энергии и рассматривалась как сила, стягивающая гипотетическую пленку на поверхности жидкости и противодействующая ее растяжению. Силовое определение более справедливо для жидкостей, т.к. у них одновременно с образованием поверхности молекулы и атомы на ней ориентируются, уплотняются, переходя в равновесное состояние и вызывая тем самым тангенциальное натяжение поверхности.
2.2.2. Термодинамическое определение
поверхностного натяжения
При p и Т = const запишем объединенное уравнение первого и второго начал термодинамики для гетерогенной системы относительно изменения энергии Гиббса:
где Т – температура; S – энтропия; р – давление; V – объем; s – площадь поверхности; – поверхностное натяжение; – химический потенциал i-го компонента; ni – число моль i-го компонента; – электрический потенциал; q – количество электричества.
При постоянных Т, р, ni и q имеем
Поверхностное натяжение есть частная производная от энергии Гиббса по площади поверхности раздела фаз при постоянных: давлении, температуре, числе моль компонентов и заряде.
Так как объединенное уравнение первого и второго начал термодинамики может быть записано и относительно других термодинамических потенциалов, а именно внутренней энергии U, энергии Гельмгольца А, и энтальпии H, то при соответствующих постоянных параметрах получим

Поверхностное натяжение– частная производная от любого термодинамического потенциала по площади межфазной поверхности при постоянных соответствующих параметрах.
Наиболее часто поверхностное натяжение выражают через производную от энергии Гиббса, т.к. экспериментальные условия постоянства T и p легко осуществимы экспериментально.
Поверхностное натяжение индивидуальных веществ является в то же время удельной энергией Гиббса поверхности (энергией Гиббса, приходящейся на единицу площади поверхности):
Поверхностное натяжение относится к числу наиболее важных свойств дисперсных систем и является основной термодинамической характеристикой поверхности раздела. Рассмотрим наиболее простой случай – поверхностное натяжение жидкости на границе с газом (рис. 2.1).

Рис. 2.1. Межмолекулярное взаимодействие
внутри жидкости и на поверхности раздела фаз
На молекулу, находящуюся внутри жидкости, действуют силы взаимного притяжения (силы молекулярного сцепления) со стороны всех окружающих ее соседних молекул. Равнодействующая этих сил равна нулю вследствие симметрии силового поля, и для перемещения молекулы внутри жидкости не требуется затрачивать работу. Это вызвано тем, что в газообразной фазе молекулы удалены друг от друга на большие расстояния, и действующие между ними силы взаимного притяжения очень малы. Молекулы, находящиеся на границе раздела фаз, испытывают действие межмолекулярных сил в большей степени со стороны жидкой фазы f1, чем со стороны газообразной f2(f1 >> f2). Результирующая сила F, пропорциональной разности сил (f1 – f2), направлена внутрь жидкости. Эта сила, отнесенная к единице поверхности (1 м 2 или 1 см 2 ), называется внутренним (молекулярным) давлениемpM:
Молекулярное давление определяется силой сцепления молекул, оно тем выше, чем полярнее вещество, так для H2O величина рМ равна 14000 атм, для C6H6 – 3800 атм. Таким образом, на поверхности любой жидкости существует огромное давление, вызванное нескомпенсированностью молекулярных сил сцепления в поверхностном слое и стремящееся затянуть все молекулы с поверхности внутрь жидкой фазы. Этим объясняется шарообразная форма капель жидкости.
Поверхностный слой вследствие нескомпенсированности молекулярных сил имеет избыточную свободную энергию по сравнению с объемом жидкости. Этот избыток свободной энергии, отнесенный к единице поверхности (1 м 2 или 1 см 2 ), называется удельной свободной поверхностной энергией (поверхностным натяжением). Весь избыток поверхностной энергии заключен в слое толщиной в 1 молекулу. Наличие на поверхности раздела фаз избытка энергии означает, что для образования новой поверхности требуется совершить работу.
Поверхностное натяжение ( ) – работа обратимого изотермического процесса, затраченная на образование единицы площади поверхности раздела фаз (энергетическое определение поверхностного натяжения):
Знак минус говорит о том, что положительная работа совершается при уменьшении или сокращении поверхности.
Силовое определение: поверхностное натяжение– сила, направленная тангенциально (параллельно) к поверхности и приходящаяся на единицу длины периметра, ограничивающего эту поверхность.
Физическая сущность – поверхностные молекулы стремятся уйти вглубь конденсированной фазы, тем самым, сжимая поверхность.
Оба эти определения необходимо рассматривать в единстве. Такое единство энергетического и силового подходов сложилось исторически. Величина поверхностного натяжения была введена в физику задолго до появления понятия энергии и рассматривалась как сила, стягивающая гипотетическую пленку на поверхности жидкости и противодействующая ее растяжению. Силовое определение более справедливо для жидкостей, т.к. у них одновременно с образованием поверхности молекулы и атомы на ней ориентируются, уплотняются, переходя в равновесное состояние и вызывая тем самым тангенциальное натяжение поверхности.
2.2.2. Термодинамическое определение
поверхностного натяжения
При p и Т = const запишем объединенное уравнение первого и второго начал термодинамики для гетерогенной системы относительно изменения энергии Гиббса:
где Т – температура; S – энтропия; р – давление; V – объем; s – площадь поверхности; – поверхностное натяжение; – химический потенциал i-го компонента; ni – число моль i-го компонента; – электрический потенциал; q – количество электричества.
При постоянных Т, р, ni и q имеем
Поверхностное натяжение есть частная производная от энергии Гиббса по площади поверхности раздела фаз при постоянных: давлении, температуре, числе моль компонентов и заряде.
Так как объединенное уравнение первого и второго начал термодинамики может быть записано и относительно других термодинамических потенциалов, а именно внутренней энергии U, энергии Гельмгольца А, и энтальпии H, то при соответствующих постоянных параметрах получим
Поверхностное натяжение– частная производная от любого термодинамического потенциала по площади межфазной поверхности при постоянных соответствующих параметрах.
Наиболее часто поверхностное натяжение выражают через производную от энергии Гиббса, т.к. экспериментальные условия постоянства T и p легко осуществимы экспериментально.
Поверхностное натяжение индивидуальных веществ является в то же время удельной энергией Гиббса поверхности (энергией Гиббса, приходящейся на единицу площади поверхности):

Одним из интересных явлений, происходящих в жидкостях, является поверхностное натяжение. Явление это малозаметно, но оно играет важнейшую роль в поведении жидкостей. Рассмотрим поверхностное натяжение более подробно, дадим ему определение.
Проявления поверхностного натяжения
Если сравнить поведение жидкости и газа, то можно отметить сходство этого поведения, если речь идет о внутренних слоях вещества. Существует даже теория гидроаэродинамики, использующее это сходство. Однако, свойства жидкости и газа существенно отличаются, если рассматривать приграничный слой.
Свойство жидкости, заключающееся в том, что ее граница стремится к сокращению, называется поверхностным натяжением.

Рис. 1. Поверхностное натяжение.
Почему возникает поверхностное натяжение ?
Молекулы на границе жидкости
Поскольку в жидкостях молекулы находятся на гораздо более близком расстоянии, чем в газах, на каждую молекулу в жидкости действуют не только силы отталкивания при сближении, но и силы притяжения при взаимном удалении.
Во внутренних слоях это не играет большой роли, молекулы внутренних слоев жидкости ведут себя подобно молекулам газа. Однако, на граничном слое ситуация другая. Молекула граничного слоя испытывает отталкивание со стороны молекул, находящихся глубже, а с внешней стороны сил отталкивания нет.
В результате молекулы в граничном слое жидкости находятся на больших расстояниях, чем молекулы во внутренних слоях. Силы отталкивания на таких расстояниях быстро уменьшаются, и силы притяжения становятся больше.
Можно сказать, что молекулы поверхностного слоя жидкости обладают некоторой избыточной потенциальной энергией по сравнению с молекулами в глубине жидкости. При увеличении площади поверхности эта энергия увеличивается.

Рис. 2. Мыльные пузыри.
Коэффициент поверхностного натяжения
Поскольку силы поверхностного натяжения действуют на молекулы граничного слоя, то общая их энергия зависит от свойств вещества жидкости и прямо пропорционально площади поверхности. Следовательно, для характеристики сил поверхностного натяжения данной жидкости можно ввести специальный параметр – коэффициент поверхностного натяжения $\sigma$, равный отношению поверхностной энергии к площади поверхности:
Из этой формулы можно получить размерность коэффициента. Поскольку энергия в системе СИ измеряется в джоулях, а площадь в квадратных метрах, единицей измерения коэффициента поверхностного натяжения является джоуль на квадратный метр или ньютон на метр.

Рис. 3. Коэффициент поверхностного натяжения.
Что мы узнали?
Поверхность жидкости стремится к сокращению. Это явление называется поверхностным натяжением. Происходит оно потому, что молекулы на поверхности жидкости более разрежены, силы притяжения между ними больше, и эти молекулы имеют большую энергию по сравнению с молекулами в глубине. Для характеристики этой энергии используется коэффициент поверхностного натяжения.
Читайте также:

