Болезнь альцгеймера биохимия кратко
Обновлено: 02.07.2024
Болезнь Альцгеймера – наиболее распространенная форма слабоумия. При ней клетки головного мозга постепенно отмирают, вызывая прогрессирующее ухудшение памяти, мышления и других психических функций.
Риск развития данного заболевания значительно увеличивается после 65 лет.
Синонимы русские
Сенильная деменция альцгеймеровского типа.
Синонимы английские
Alzheimer disease, Alzheimer's disease, AD.
Симптомы
Первые симптомы болезни Альцгеймера проявляются как забывчивость, снижение внимания, скудность речи, небольшие проблемы с координацией движений. Со временем нарушается моторика, значительно ухудшается память, мышление, ориентирование в пространстве, затрудняется речь. Причем больной может не замечать происходящих с ним изменений, несмотря на замечания окружающих.
Болезнь Альцгеймера может проявляться в виде следующих отклонений.
- Нарушение памяти. Забывается расположение предметов в собственном доме, информация о событиях, встречах, на поздних стадиях даже имена членов семьи, названия предметов.
- Нарушение ориентации в пространстве и времени. Больные не способны назвать день, время года. Затрудняется ориентация в пространстве – человек может заблудиться даже в знакомом месте.
- Нарушения устной и письменной речи. Сначала возникают сложности с выбором нужных слов, формулировок, затрудняется обозначение некоторых предметов, со временем пациент вовсе может утратить способность говорить и писать.
- Нарушения мышления. Человек испытывает трудности с концентрацией внимания и мышлением, теряется способность считать, распоряжаться деньгами.
- Сложности в принятии решений. Больной перестает принимать решения адекватно сложившейся ситуации.
- Нарушения в планировании и выполнении привычных действий. Человек затрудняется в выполнении даже таких простых задач, как приготовление еды, самообслуживание.
Изменения личности и поведения:
- депрессия,
- беспокойство,
- нежелание общаться с людьми, выходить из дома,
- перепады настроения,
- недоверие к окружающим, даже к родственникам,
- упрямство,
- раздражительность и агрессивность,
- нарушения сна.
Общая информация о заболевании
Болезнь Альцгеймера – форма слабоумия, которая характеризуется нарушением познавательных функций и расстройствами поведения.
Это неизлечимое заболевание, при котором клетки головного мозга (нейроны) и связи между клетками (синапсы) постепенно атрофируются, вызывая снижение памяти, мышления и других психических функций.
Как правило, болезнь Альцгеймера обнаруживается у людей старше 65 лет, но есть и ранняя болезнь Альцгеймера, которая встречается в 30-40 лет.
Существует две гипотезы механизма повреждения клеток головного мозга при болезни Альцгеймера.
1. Образование бляшек из белка бета-амилоида. В норме он играет важную роль в жизнедеятельности нейронов, но при болезни Альцгеймера в силу неизвестных причин бета-амилоид начинает откладываться в тканях мозга, образуя бляшки, которые уничтожают клетки головного мозга.
2. Нарушение функционирования тау-белка. Для роста и развития клеток мозга необходимо регулярное снабжение их питательными веществами. Если тау-белок, отвечающий за транспортировку этих веществ к клеткам, перестает нормально работать, клетки не получают питания и, как следствие, погибают.
Считается, что развитие болезни Альцгеймера связано с сочетанием таких факторов, как возраст, генетическая предрасположенность, образ жизни, особенности окружающей среды.
Сначала она проявляется как небольшое нарушение познавательных функций больного. Когда она прогрессирует, изменения в головном мозге постепенно сказываются и на физических функциях организма, таких как глотание, баланс кишечника и мочевого пузыря. Эта особенность может увеличить уязвимость по отношению к следующим нарушениям:
- к пневмонии и др. инфекциям (в таких случаях глотание затрудняется, и жидкость или пища попадает в дыхательные пути и в легкие);
- к неспособности контролировать опорожнение мочевого пузыря (недержанию мочи), в связи с чем используется трубка для отвода и сбора мочи (мочевой катетер), что повышает риск инфекции мочевых путей;
- к травмам в результате падения.
Со временем проявления болезни Альцгеймера усиливаются. При тяжелой форме заболевания наблюдается истощение, апатия, отсутствие речи, значительная потеря веса, неспособность к самообслуживанию. Смерть, как правило, наступает в результате развития заболевания – например, из-за пролежневой язвы или пневмонии.
Кто в группе риска?
- Люди пожилого возраста. После 65 лет риск развития болезни Альцгеймера удваивается каждые пять лет. Ею страдает около 50 % людей старше 85.
- Лица с наследственной склонностью к развитию заболевания.
- Люди с незначительными когнитивными (познавательными) расстройствами, вызванными другими причинами (проблемами с памятью, с речью, вниманием).
Факторы, повышающие риск развития болезни Альцгеймера:
- низкая физическая активность;
- курение;
- высокое кровяное давление;
- высокий уровень холестерола;
- плохо контролируемый диабет;
- генетическая предрасположенность.
Диагностика
На данный момент диагноз ставится с помощью исследований, направленных на исключение других причин слабоумия. При подозрении на болезнь Альцгеймера в первую очередь проводится проверка всех психических функций организма.
На сегодняшний день полиморфизм гена ApoE считается ведущим в определении предпасположенности к болезни Альцгеймера. Аллель E4 гена ApoE ассоциирован с наследованием повышенного риска развития данного заболевания.
Анализы крови могут помочь врачу исключить другие возможные причины потери памяти и спутанности сознания.
-
. Снижение гемоглобина и увеличение среднего объема эритроцитов (MCV) характерно для В12-дефицитной анемии. Повышение лейкоцитов может свидетельствовать о воспалении. . Его нехватка также может указывать на В12-дефицитную анемию. . , аланинаминотрансфераза (АЛТ), аспартатаминотранфераза (АСТ). Повышение данных показателей характерно для патологии печени. , антитела к Treponema pallidum. Слабоумие бывает вызвано ВИЧ-инфекцией или сифилисом.
Для исключения других возможных причин, объясняющих симптомы, характерные для болезни Альцгеймера, могут назначаться анализы на электролиты (калий, натрий, хлор), скорость оседания эритроцитов (СОЭ), церулоплазмин.
Другие методы исследования
- Компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) для исключения таких причин слабоумия, как опухоли, атрофия головного мозга, травмы и инсульты.
- Спинномозговая пункция со взятием спинномозговой жидкости (ликвора) для исключения нейроинфекции.
Лечение
К сожалению, болезнь Альцгеймера неизлечима. Терапия предполагает прием препаратов, замедляющих развитие атрофии головного мозга и расстройств познавательной сферы с помощью увеличения количества связей в головном мозге.
Кроме того, пациентам необходима психологическая поддержка. Их родственникам необходимо проявить терпение, потому что общаться с такими больными и ухаживать за ними зачастую непросто.
Что такое болезнь Альцгеймера? Причины возникновения, диагностику и методы лечения разберем в статье доктора Полякова Т. А., невролога со стажем в 13 лет.
Над статьей доктора Полякова Т. А. работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Болезнь Альцгеймера — это хроническое нейродегенеративное заболевание, с медленным началом и значительным ухудшением с течением времени. В 70 % случаев болезнь Альцгеймера приводит к деменции.
Этиология. Факторы риска
Заболевание на данный момент изучено плохо. Предполагается, что в 70% случаев болезнь Альцгеймера объясняется генетическими причинами, среди других факторов риска — черепно-мозговые травмы, депрессия, эндокринные заболевания в анамнезе (гипотиреоз), эстрогенная недостаточность у женщин.
Сопутствующие заболевания
Исследования последних лет показывают, что усиливают предрасположенность к болезни Альцгеймера гипертония, гиперлипидемия, гипергомоцистеинемия, сахарный диабет, метаболический синдром, инсулинорезистентность, заболевания сердца, а также наличие в истории болезни инсульта [1] .
Статистические данные
Болезнь Альцгеймера — наиболее распространённая форма деменции, она встречается в 60–70 % случаев. В мире деменцией страдают около 50 миллионов человек, каждый год выявляется 10 миллионов новых случаев [12] .
В развитых странах болезнь Альцгеймера является одним из наиболее дорогостоящих заболеваний. В России затраты на содержание больных деменцией составляют 74,8 млрд рублей в год [2] .
Распространённость и факторы риска
Заболевание более распространено среди женщин. Предположительно, это связано со следующими факторами:
- продолжительность жизни женщин больше, чем мужчин, а возраст — самый значимый фактор риска развития болезни Альцгеймера;
- риск развития болезни увеличивается на 70 % для людей с депрессией, у женщин она встречается чаще;
- более низкий уровень образования связан с повышенным риском деменции, в некоторых странах у женщин уровень образования ниже, чем у мужчин;
- при беременности часто возникают гипертонические расстройства, они связаны с повышенным риском ухудшения когнитивных функций даже спустя десятилетия после беременности [13] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы болезни Альцгеймера
Признаки болезни Альцгеймера на ранней стадии часто ошибочно принимаются за нормальные признаки старения.
Кратковременная потеря памяти — наиболее распространенный ранний симптом болезни Альцгеймера, который выражается в том, что больному трудно запоминать последние события. В трети случаев заболевание можно распознать по изменениям поведения.
По мере усугубления болезни возникают следующие симптомы:
- проблемы с речью;
- дезориентация;
- перепады настроения;
- потеря мотивации;
- снижение критики;
- больные не в состоянии вспомнить нужное слово, и им приходится заменять его другим (парафазии), однако они хорошо повторяют сказанное.
- со временем возникают затруднения при назывании предметов (аномии).
- уже на ранней стадии возникают трудности с пониманием сложных грамматических структур (семантическая афазия), к которому затем присоединяется отчуждение смысла слова. [3]
Важный признак болезни Альцгеймера — нарушение способности справляться с повседневностью. При заболевании возникают проблемы с самообслуживанием и поведенческие расстройства.
Признаки болезни Альцгеймера у мужчин и женщин
Признаки болезни Альцгеймера у женщин и мужчин схожи, однако у женщин она чаще сопровождается депрессией.
Патогенез болезни Альцгеймера
Существуют отличительные патоморфологические признаки болезни Альцгеймера: амилоидные (сенильные) бляшки — это внеклеточные отложения в виде скопления фрагмента белка, называемые бета-амилоидом; нейрофибриллярные клубочки — скрученные микроскопические нити тау-белка внутриклеточной локализации. Происходит потеря связи между клетками мозга, ответственными за память, обучение и общение. Эти соединения, или синапсы, передают информацию из клетки в клетку. Важная роль в патогенезе принадлежит воспалительному процессу, связанному с активацией микроглии, которая инициируется накоплением амилоида. [1]
Патофизиология болезни Альцгеймера:
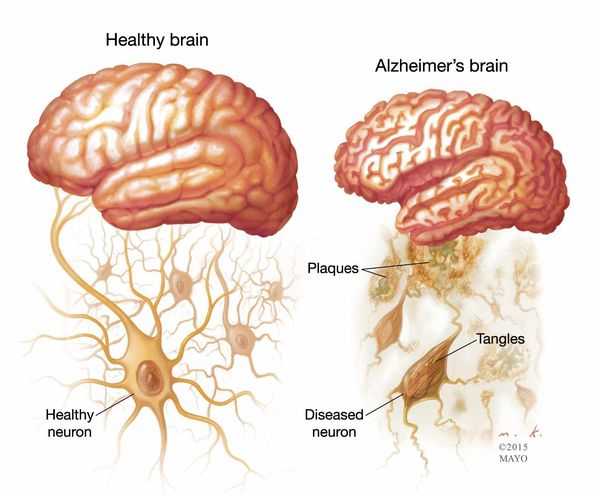
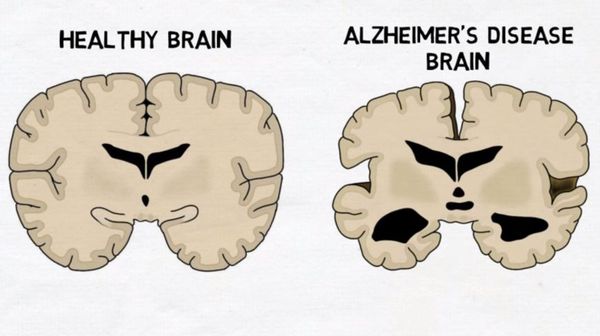
Макроскопически выявляется диффузная атрофия головного мозга с уменьшением объёма извилин и расширением боковых борозд, наиболее выраженная в височно-теменной области.
У значительной части больных цереброваскулярная патология может инициировать или усиливать дегенеративный процесс, связанный с отложением амилоида или другими характерными для заболевания изменениями.
Классификация и стадии развития болезни Альцгеймера
Типичный фенотип болезни Альцгеймера — сочетание выраженных мнестических нарушений гиппокампального типа с акустико-мнестической афазией, зрительно-пространственными нарушениями и апраксией. [3]
Три атипичных фенотипа болезни Альцгеймера (неамнестических):
- с ведущим афатическим дефектом (логопенический вариант первичной прогрессирующей афазии);
- с доминирующими зрительно-пространственными нарушениями (задняя корковая афазия);
- преимущественно с дизрегуляторными нарушениями (лобный вариант болезни Альцгеймера).
Заболевание также подразделяется на формы с ранним началом, зачастую с положительным семейным анамнезом (до 65 лет) и поздним началом (старше 65 лет). Они отличаются патогенезом, генетическими факторами и разной скоростью прогрессирования.
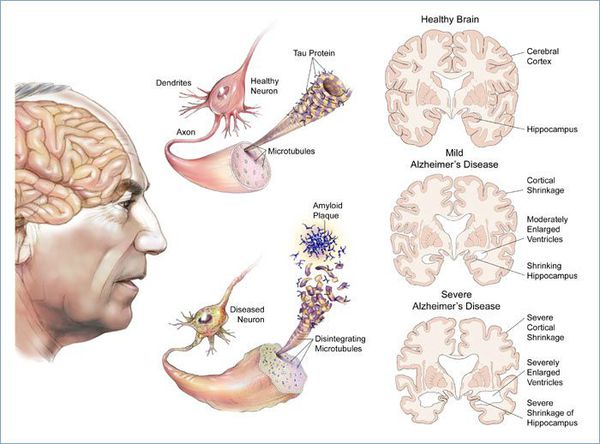
Три стадии болезни Альцгеймера:
Первая (предеменция, ранняя деменция): больные обслуживают себя сами, но им нужна помощь для решения финансовых вопросов, приготовления пищи и т. д.
Вторая (умеренная деменция): зависимость от посторонней помощи растет — больные не способны самостоятельно одеться, осуществить гигиенические процедуры, долго оставаться дома без присмотра.
Третья (тяжёлая деменция): больные не могут выполнить ни одно из привычных повседневных действий без помощи других людей.
Переход от одной стадии к другой коррелирует со снижением оценки по MMSE (Краткая шкала психического статуса), которая является надежным инструментом для отслеживания динамики заболевания.
Осложнения болезни Альцгеймера
Продолжительность жизни людей с болезнью Альцгеймера после установления диагноза обычно колеблется от трех до десяти лет. Более четырнадцати лет после установления диагноза живут менее 3% больных. Уменьшение выживаемости связано с тяжелыми когнитивными нарушениями, снижением уровня физической активности, частыми падениями и нарушениями в неврологическом статусе. Сопутствующие соматические заболевания также влияют на продолжительность и качество жизни при болезни Альцгеймера. Пневмония и обезвоживание — наиболее частые непосредственные причины смерти, вызванной болезнью Альцгеймера. Кроме того, чем старше возраст, тем выше общий возраст выживаемости. У мужчин прогноз менее благоприятен по сравнению с женщинами.
Диагностика болезни Альцгеймера
Трудности ранней диагностики болезни Альцгеймера во многом объясняются "маскированным" характером заболевания в этот период, когда отсутствуют явные внешние признаки деменции. Для постановки диагноза, определения тактики ведения пациента необходимо выявить характер и выраженность когнитивных нарушений.
Нейропсихологический тест
Основной метод оценки когнитивных функций — нейропсихологическое обследование, которое проводит врач, обученный данным методам исследования. В некоторых странах практикуется обследование больных их родственниками с помощью шкал для оценки когнитивных функций: монреальской когнитивной шкалы, Адденбрукской, шкала краткого исследования психических функций MMSE.
Биомаркеры болезни Альцгеймера
Молекулярная диагностика на ранней стадии заболевания также создаёт перспективы для раннего назначения лечения болезни Альцгеймера. Определение биомаркеров в плазме является менее инвазивной альтернативой для диагностики болезни Альцгеймера. Биомаркеры классифицируются на биомаркеры накопления амилоида и биомаркеры нейродегенерации. Основные биомаркеры отражают патологию амилоида (внеклеточное накопление Aβ1-40/1-42) или внутриклеточные включения нейрофибриллярных клубочков (гиперфосфорилированного тау). [4] [5]
Согласно рекомендациям 4-го Канадского консенсуса по диагностике и лечению деменции и рациональному использованию биомаркеров для диагностики болезни Альцгеймера и других деменций (CCCDTD4, 2011): [6]
1. Определение биомаркеров цереброспинальной жидкости не рекомендуются для диагностики болезни Альцгеймера с типичной клинической картиной (2А уровень).
2. Исследование биомаркеров не рекомендуется для скрининга здоровых людей с целью оценки риска развития болезни Альцгеймера в будущем (уровень 1В).
3.Биомаркеры цереброспинальной жидкости можно рассматривать в особых случаях, когда есть атипичные признаки или диагностические трудности при дифференциальной диагностике лобного варианта болезни Альцгеймера от лобно-височной деменции, а также случаи первично прогрессирующей афазии как следствие болезни Альцгеймера или лобно-височной дегенерации (уровень 2В).
МРТ и КТ головного мозга
Современные методы нейровизуализации — магнито-резонансная томография и компьютерная томография головного мозга — позволяют расширить диагностические возможности прижизненной диагностики болезни Альцгеймера.
МРТ и КТ проводят для выявления поддающихся лечению причин деменции и нарушений, которые могут усугубить симптомы. Структурные изменения по данным магнитно-резонансной томографии являются более прогностически значимыми для дальнейших изменений в когнитивной сфере, чем биомаркеры цереброспинальной жидкости. По данным магнитно-резонансной томографии, признаки цереброваскулярного заболевания, такие как лейкоареоз и множественные подкорковые лакунарные инфаркты, чаще наблюдаются у пациентов с болезнью Альцгеймера, чем в контрольной группе. [7] Асимметричная атрофия медиальных отделов височной доли также не исключает сосудистую деменцию.
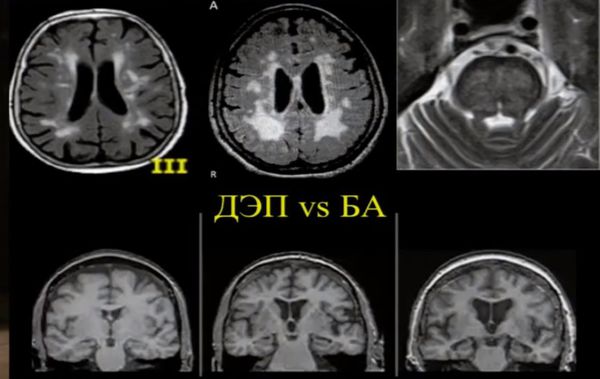
Описана смешанная модель патогенеза болезни Альцгеймера, которая предполагает взаимодействие церебральной амилоидной ангиопатии с сосудистыми факторами на ранних стадиях патологического процесса. Предполагается, что синергия между накоплением амилоида и цереброваскулярной патологией может инициировать дальнейшую дисфункцию нейронов и нейродегенерацию. [8] В этом отношении церебральные микрокровоизлияния, выявляемые в режиме Т2 градиентного эхо на магнитно-резонансной томографии, являются дополнительным и доступным диагностическим маркером, повышающим диагностическую значимость лейкоареоза и свидетельствующим в пользу церебральной амилоидной ангиопатии или гипертонической микроангиопатиии, особенно в случаях смешанной патологии и тяжелого когнитивного дефицита.
Локализация церебральных микрокровоизлияний является дифференциально-диагностическим признаком ведущего патологического процесса. В случае болезни Альцгеймера наблюдается корковая локализация микрокровоизлияний, в случае дисциркуляторной энцефалопатии или сосудистой деменции будут визуализироваться микрокровоизлияния в глубинных отделах мозга. [9] [10]
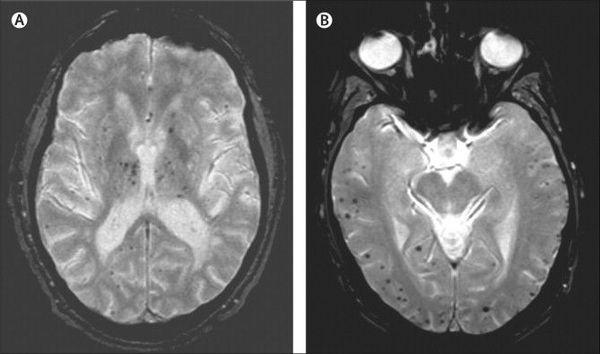
Одним из наиболее перспективных методов диагностики болезни Альцгеймера является позитронно-эмиссионная томография с лигандом, который связывается с амилоидом (PiB), однако накопление амилоида и захват соответствующего лиганда нарастают на стадии умеренных когнитивных нарушений, но после конверсии в деменцию дальнейшего накопления не происходит. [11]
Лечение болезни Альцгеймера
Болезнь Альцгеймера пока не поддается лечению. Но благодаря группе новых препаратов и симптоматическому лечению Альцгеймера можно сделать так, что снижение интеллекта больных будет более постепенным.
Лекарства
К таким средствам относятся:
- ингибиторы холинэстеразы (донепезил, ривастигмин, галантамин)
- блокаторы NMDA-глутаматных рецепторов (акатинол-мемантин).
Облегчение расстройств психики и поведения, сопровождающих болезнь Альцгеймера
С целью лечения сопутствующих расстройств психики и поведения используются также антидепрессанты и нейролептики.
Поддерживающие методы
Существуют и нелекарственные методы воздействия — тренировки интеллектуальных функций. Нейропсихологическая реабилитация позволяет стимулировать к развитию новых нейронный сетей, обучая рабочие нервные клетки.
Специальная диета при болезни Альцгеймера не требуется: питание не влияет на развитие заболевания.
Прекращение лечения
Причиной для прекращения приёма антидементных препаратов может стать выраженная брадикардия, но это осложнение возникает крайне редко.
Рекомендации для ухаживающих за близкими с болезнью Альцгеймера
При уходе за больным человеком важно организовать для него безопасное и удобное пространство.
Также важно внимательно выбирать обувь и одежду.
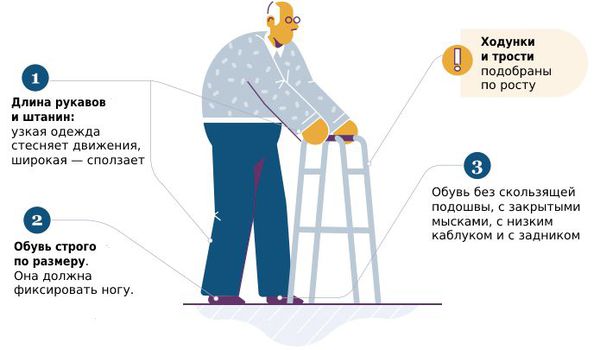
Такими занятиями могут быть:
- прогулки;
- общение с домашними животными;
- уход за растениями;
- наблюдения за рыбками в аквариуме;
- прослушивание радиопередач и музыки;
- творчество, например лепка и живопись;
- чтение книг, при невозможности это могут делать близкие люди вслух.
Ухаживая за больным, не следует игнорировать своё здоровье. Пациенту нужно обеспечить нормальное питание, режим, активный образ жизни — это в полной мере относится и к близким больного человека.
Где обеспечивают уход при болезни Альцгеймера
Государственных специализированных пансионатов по уходу за людьми с болезнью Альцгеймера в нашей стране пока нет.
Прогноз. Профилактика
С увеличением осведомлённости общества о деменции будет расти и потребность в помощи по уходу, понадобятся значительные затраты для её организации. Пока же преобладает в основном неформальная помощь в семьях. Усилия по улучшению качества и доступности помощи потребуют вложений в меры первичной профилактики, и возможно, это позволит контролировать "эпидемии" деменций в разных регионах мира. В качестве основных мишеней первичной профилактики рассматриваются улучшение образования и устранение сосудистых факторов риска.
Профилактика
На сегодняшний день одной из основных целей профилактики является создание различных новых форм внебольничной помощи пациентам пожилого и старческого возраста с целью улучшения диагностики когнитивных нарушений разной степени тяжести, более раннее выявление заболеваний. С такой целью в развитых странах созданы клиники памяти, Альцгеймеровские центры. [2]
Продолжительность жизни
В среднем люди с болезнью Альцгеймера живут 3 – 11 лет после выявления заболевания, но некоторые — 20 лет и более. Продолжительность жизни зависит от степени нарушений при постановке диагноза [14] .
Юридические вопросы
Требования для признания гражданина недееспособным раскрываются в статье 29 Гражданского кодекса РФ. Потеря дееспособности компенсируется больному человеку установлением опёки. Опекун "восполняет" утраченные возможности гражданина, признанного недееспособным, и действует в его интересах.
Процедура признания гражданина недееспособным описана в 31 главе Гражданского процессуального кодекса РФ, в статьях 281–285.
В данной работе приводится анализ результатов исследований последних лет, затрагивающих биохимические аспекты патогенеза болезни Альцгеймера.
Ключевые слова
Статья
Современный взгляд на биохимические механизмы патогенеза альцгеймеровской нейродегенерации
Ващенко И. С., Соколов А. В.
Научный руководитель: к.м.н., доцент Чеботарева Е.Г.
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздрава РФ
Кафедра биологической химии
Введение. Болезнь Альцгеймера (синоним – деменция альцгеймеровского типа) представляет собой наиболее распространенную форму первичных дегенеративных деменций позднего возраста, которая характеризуется постепенным малозаметным началом в пресенильном или старческом возрасте, неуклонным прогрессированием расстройств памяти и высших корковых функций вплоть до тотального распада интеллекта и психической деятельности в целом, а также типичным набором нейропатологических признаков. Изменения в головном мозге, подтверждающие диагноз болезни Альцгеймера, в основном выявляют в наружном слое мозга (коре) и гиппокампе, который залегает в глубине полушарий и играет важную роль в процессах памяти. При микроскопическом исследовании этих областей мозга обнаруживаются нейрофибриллярные клубочки и нейротические бляшки. Клубочки состоят из патологически измененных нейронов, содержащих аномальные белки. Бляшки представляют собой участки отложений в межклеточном пространстве белково-углеводного комплекса – амилоида. Чем больше в мозгу клубочков и бляшек, тем сильнее выражены интеллектуальные нарушения.
Целью нашей работы явилось осветить основные теории, объясняющие патогенез болезни Альцгеймера, существующие в академической науке на сегодняшний день, и проанализировать основные результаты проводимых исследований.
Методы: ознакомление с библиографией, пресс-релизами некоторых фармакологических компаний, анализ методик биохимических исследований, сопоставление результатов экспериментов различных исследовательских групп и их вклада в наши знания о патогенезе альцгеймеровской нейродегенерации.
По данным ВОЗ, в 2005 году деменцией страдали 0.379 % мирового населения, общемировая заболеваемость на 2006 год оценивалась уже в 26,6 млн. человек, а прогноз на 2015 год достигает значения 0.441 % и ещё больший процент населения, 0.556 %, может быть поражён болезнью к 2030 году [1].
Между тем биохимические механизмы патогенеза этого заболевания так и остаются не выясненными до конца. Приводимые в исследованиях оценки общественных затрат на лечение и уход за больными разнятся, но в целом по всему миру затраты на деменцию могут составлять около 160 млрд. долл. [2].
Более 20 лет ведущей гипотезой в области исследования этого заболевания оставалась амилоидная гипотеза, согласно которой фибриллогенез белка амилоид-бетта (Аβ) и образование амилоидных бляшек вызывают нарушение работы синаптической машины мозга и клиническую картину потери памяти. В ее пользу свидетельствуют некоторые факты. Так, строго доказано, что определенные мутации гена, который кодирует белок APP, сильно увеличивают риск развития болезни Альцгеймера [3]. Профессор Селкоу (Selkoe) в своей обзорной статье отметил, что последние нейропатологические, биохимические, генетические и даже терапевтические исследования служили в поддержку гипотезы о постепенном накоплении растворимых и нерастворимых конгломератов белка амилоид-бета в лимбических структурах и ассоциативной коре, и связанных с этим биохимических и клеточных нарушениях, которые дают картину клинических проявлений болезни Альцгеймера [4] .
Профессор биологии Брэдли Хайман (Bradley Hyman) и его коллеги получили весьма любопытные результаты. Гарвардские исследователи выяснили, что амилоидные отложения начинаются с возникновения крошечных зародышей — микробляшек. Хотя их размеры очень малы, они повреждают отростки нервных клеток, аксоны и дендриты, по которым передаются нервные импульсы. Возможно, именно этим объясняется тот печальный факт, что болезнь Альцгеймера повреждает синаптические связи между нейронами [3].
Однако ряд экспериментальных данных говорят об ошибочности положений амилоидной гипотезы, упрощенность. Приведем несколько примеров.
Одной из предложенных форм лечения болезни Альцгеймера была вакцинация антителами против Aβ. Этот метод, показавший свою эффективность в ходе опытов с лабораторными животными на клиническом этапе исследования стал причиной тяжелых форм воспаления мозга у значительного числа пациентов, принявших участие в испытании, усугубление симптомов БА, и даже несколько смертельных исходов [6, 7].
17 августа 2010 года компания Eli Lilly объявила о прекращении международных клинических испытаний третей фазы лекарства семагацестат (ингибитор гамма-секретазы, предотвращающий образование Аβ из его предшественника) с участием 2600 больных болезнью Альцгеймера в 31 стране мира. В пресс-релизе компании подчеркивалось, что у участников клинических испытаний, значительно ухудшалось состояние по сравнению с теми участниками испытаний, кто принимал плацебо, также появлялась склонность к развитию рака кожи [8].
Кроме того, вплоть до сегодняшнего дня Аβ не удалось выделить в достаточном для проведения экспериментов количестве, несмотря на то, что согласно амилоидной гипотезе, его содержание в нервной ткани пациентов с болезнью Альцгеймера. Сами исследования проводят на мышах, трансгенных по редкому мутантному гену предшественника амилоида. Вполне вероятно, что данный вид моделирования не совсем корректно переносить на клиническую практику.
Обоснованные аргументы оппонентов заставили сторонников амилоидной гипотезы изменить ряд ее положений. Последняя версия этой гипотезы гласит, что главной причиной развития БА являются олигомеры Аβ, а не его амилоидные бляшки, как утверждалось ранее [9].
Существуют и другие гипотезы возникновения болезни Альцгеймера, альтернативные амилоидной. Многие исследователи связывают появление нейрофибриллярных клубков и амилоидных бляшек не патологическими, а наоборот, с компенсаторными механизмами. Еще в начале 90х гг. группой отечественных исследователей (Кудинов А.Р., Кудинова Н.В., Кезля Е.В., Козырев К.М., Медведев А.Е., Березов Т.Т.) было доказано, что Аβ- это нормальный физиологичный и водорастворимый апобелок, секретируемый практически всеми изученными на сегодняшний день культурами клеток, содержащийся в плазме крови и ликворе [10]. Липопротеины обеспечивают термодинамически выгодное окружение, необходимое для поддержания Аβ в растворенном состоянии. Аβ так же является важным участником метаболических путей в мозге. В числе выявленных функций Аβ входят модуляция передачи нервного импульса, нейротрансмиссии, синаптической пластичности центральных синапсов ЦНС, защита от избыточных нейротоксических концентраций глутамата, регулирование функций NMDA рецепторов гиппокампа, долговременной потенциации и памяти о пространстве, усиление синтеза фосфатидилхолина, фосфатидилэтаноламина, фосфатидилсерина и синтеза холин-содержащих фосфолипидов в срезах гиппокампа лабораторных крыс. Липопротеины так же необходимы для нейропластичности и для моментальных структурных перестроек мембран нейронов на ранних этапах развития механизмов нейропластичности. Исследования показали важную роль белков из семейства пАβ в онтогенетическом синаптическом созревании нейромышечных соединений, формировании их структуры и обеспечении правильной функции. пАβ важен как регуляторная молекула для пресинаптической экспрессии и активности высоко-афинного транспортера холина, т.е. молекулы, которая опосредует скорость-лимитирующий этап холинэргической синаптической трансмиссии и в нейромышечных соединениях, и в синапсах ЦНС 11.
В норме апоАβ связан с липидами и не взаимодействует с другими белками, что имело место в образцах ЛПВП, выделенных из цереброспинальной жидкости больных с болезни Альцгеймера. Очевидно, что при БА структура липопротеинов изменяется и термодинамически более выгодным становится взаимодействие молекул Аβ друг с другом, что приводит к образованию олигомеров, а также связыванию апоАβ с другими апобелками (аполипопротеинами) с образованием их комлексов.
Первичными причинами возникновения болезни Альцгеймера является вероятно нарушение гомеостаза холестерина [10]. Это приводит к холестерин-зависимому нарушению синаптической пластичности и нейрональной дегенерации. Биохимические изменения белка Аβ способствуют восстановлению обмена холестерина в ткани мозга при патологии.
Вопрос о связи Аβ и tau пока так же остается открытым. Физиологически Аβ и tau могут быть частью биохимической машины обеспечения физико-химических свойств мембран благодаря функциональному влиянию на гомеостаз липидов мозга. Анализ литературных данных свидетельствует о том, что нейродегенеративые изменения нейрохимии белка амилоид-бета (Аβ), чрезмерное фосфолирирование белка tau и связанные с этим модификации нейрального цитоскелета при болезни Альцгеймера и других родственных патологиях ЦНС- это вторичные признаки нейродегенерации. Группа калифорнийских ученых из Стэнфордского и Калифорнийского (Окленд) университетов и Гладстонского института неврологических болезней (Сан-Франциско) высказала предположение, что виной всему нарушение аксонного транспорта. На это указывает тот факт, что при болезни Альцгеймера нарушается внутринейронное распределение некоторых транспортируемых молекул; tau ассоциирован с микротрубочками, необходимыми для транспорта, а Аβ этот транспорт нарушает [9]. Само исследование проводилось на культурах нейронов, нокаутных по tau полностью или частично. В ходе его выяснилось, что Аβ не влияет на транспортировку грузов в нокаутированных клетках, но запускает целый каскад реакций (механизмы которых так до конца и не поняты) в клетках с исходными аллелями, нарушая тем самым нейронный транспорт. Следует отметить, что использование нокаутированных клеток не совсем корректно и требует подтверждений на нокдаунах.
Переходя к выводам, отметим что несмотря на огромную и напряженную работу ученых в этой области, точный механизм нарушений биохимических процессов по-прежнему остается загадкой. Исследования последних лет несколько прояснили картину возникновения амилоидных бляшек, однако до конца взаимосвязь между нейродегенеративными изменениями Аβ и гиперфосфориливанным tau так и не установлена. Сторонники гипотез, альтернативных амилоидной, имеют достаточное количество серьезных оппонентов в научных кругах. При этом положения самой амилоидной гипотезы при появлении новых экспериментальных данных регулярно подвергаются изменениям. Учитывая неудачный опыт крупных фармакологических компаний приостановивших на заключительных фазах ряд исследований, вопрос о правомерности экстраполяции результатов экспериментов с культурами нейронов in vitro или даже лабораторными животными in vivo на клиническую практику также остается открытым. Дело в том, что данные модели либо слишком упрощены и не учитывают всей сложности регуляторных процессов организма, либо наблюдаемые объекты несут крайне редко встречающиеся мутации. Таким образом, говорить о создании единой стройной теории патогенетических механизмов возникновения болезни Альцгеймера на данный момент рано, как рано говорить и о создании лекарства против нее.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Болезнь Альцгеймера: причины появления, симптомы, диагностика и способы лечения.
Определение
Болезнь Альцгеймера — хроническое дегенеративное заболевание головного мозга, характеризующееся резким снижением интеллектуальных способностей вплоть до тотального распада интеллекта и психической деятельности. Болезнь получила свое название по имени доктора Алоиса Альцгеймера, который в 1906 году впервые описал это заболевание.
Заболевание вызывает повреждение нейронов и отмирание клеток коры головного мозга, ответственных за память и формирование эмоций.
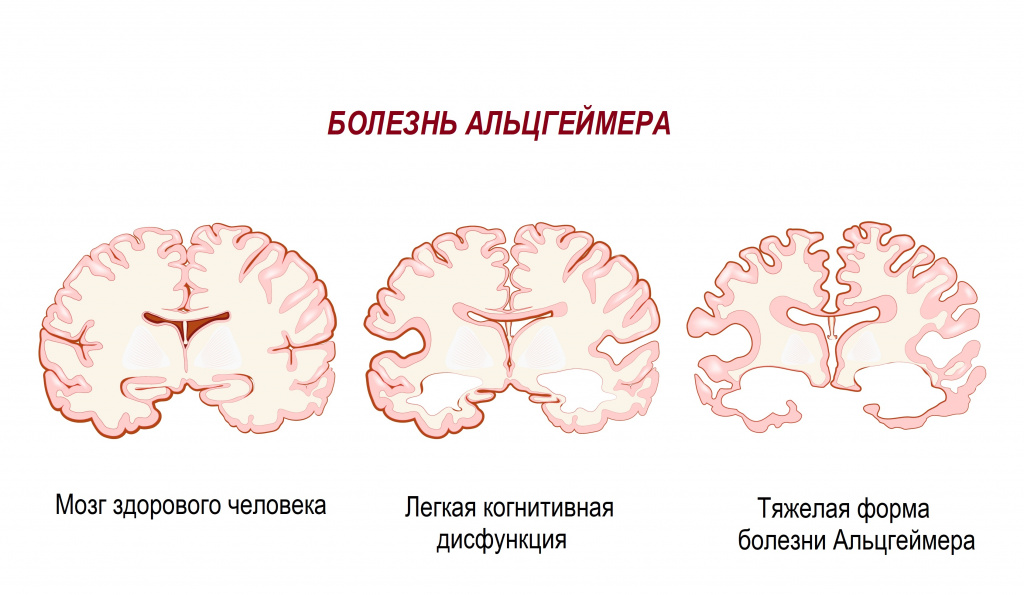
Это приводит к снижению умственных способностей, скорости мышления, реакции, способности справляться с ежедневными делами, ориентироваться в пространстве и критически оценивать свои действия. Происходит значимое нарушение бытовой, профессиональной, социальной самостоятельности и повседневной адаптации.
Причины появления болезни Альцгеймера
Точные причины развития болезни Альцгеймера не до конца понятны. Известно лишь, что в ее основе лежит патологическая активность специфических белков бета-амилоидов и тау-белков:
- бета-амилоиды оказывают токсическое воздействие на нейроны и нарушают межклеточную связь;
- тау-белки нарушают транспортную систему нейронов и токсичны для клеток головного мозга.
Кроме того, при болезни Альцгеймера организм испытывает недостаток фермента, необходимого для образования нейромедиатора ацетилхолина, который является важным участником межклеточной коммуникации.
Патологические формы бета-амилоида образуются у всех людей, но они элиминируются (выводятся) из мозга и проблем не вызывают. Современная гипотеза о развитии заболевания заключается в том, что болезнь возникает именно из-за нарушения элиминации. Белок накапливается в мозге и, превысив определенный порог, запускает болезнь. К нарушению элиминации этого белка причастны разные факторы риска — возраст, вредные привычки (курение, чрезмерное употребление алкоголя), сосудистые патологии, генетическая предрасположенность.
Заболевание вдвое чаще встречается у женщин, чем у мужчин, что отчасти связано с большей продолжительностью жизни женщин. Преобладание количества больных в развитых странах связано с увеличением доли пожилых людей.
Наследственные формы, которые на сегодня четко обозначены, по самым максимальным оценкам составляют до 10% от всех случаев заболевания. Они связаны с мутацией трех генов, которые участвуют в формировании патологических форм белка бета-амилоида.
Другие факторы риска:
- неконтролируемая артериальная гипертензия в среднем и пожилом возрасте;
- атеросклероз крупных артерий головы;
- гиперлипидемия;
- гипергомоцистеинемия;
- сахарный диабет;
- избыточная масса тела;
- гиподинамия;
- хроническая гипоксия;
- черепно-мозговые травмы в анамнезе.
Болезнь Альцгеймера с ранним началом (до 65 лет - так называемый пресенильный вариант) характеризуется быстрым прогрессированием ухудшения памяти, интеллектуальной деятельности и высших корковых функций. Это приводит к раннему развитию тотальной деменции с выраженным распадом речи, жизненных навыков и нарушению различных видов восприятия (зрительного, слухового, тактильного). Для этой формы характерен семейный анамнез заболевания.
Болезнь Альцгеймера с поздним началом (после 65 - сенильный вариант) прогрессирует медленнее, нарушения памяти длительное время остаются главным симптомом. В дальнейшем при неуклонном развитии заболевания наблюдается тотальная деменция по типу амнезии. Относительно редко возникают тяжелые корковые очаговые расстройства, приводящие к параличу.
Кроме того, предусмотрено выделение атипичной формы, или деменции смешанного типа, когда сочетаются симптомы, характерные как для болезни Альцгеймера, так и для сосудистой деменции.
Симптомы болезни Альцгеймера
Для болезни Альцгеймера доминирующим симптомом является нарушение памяти на текущие события, при этом долговременная память сохраняется неплохо. Наиболее частым ранним признаком болезни Альцгеймера является проблема с запоминанием новой информации, поскольку болезнь обычно поражает в первую очередь ту часть мозга, которая связана с обучением.
Гипосмия (снижение обонятельной функции) считается докогнитивным симптомом. То есть прежде чем начнутся первые проблемы с памятью или мышлением, человек перестает четко различать запахи.
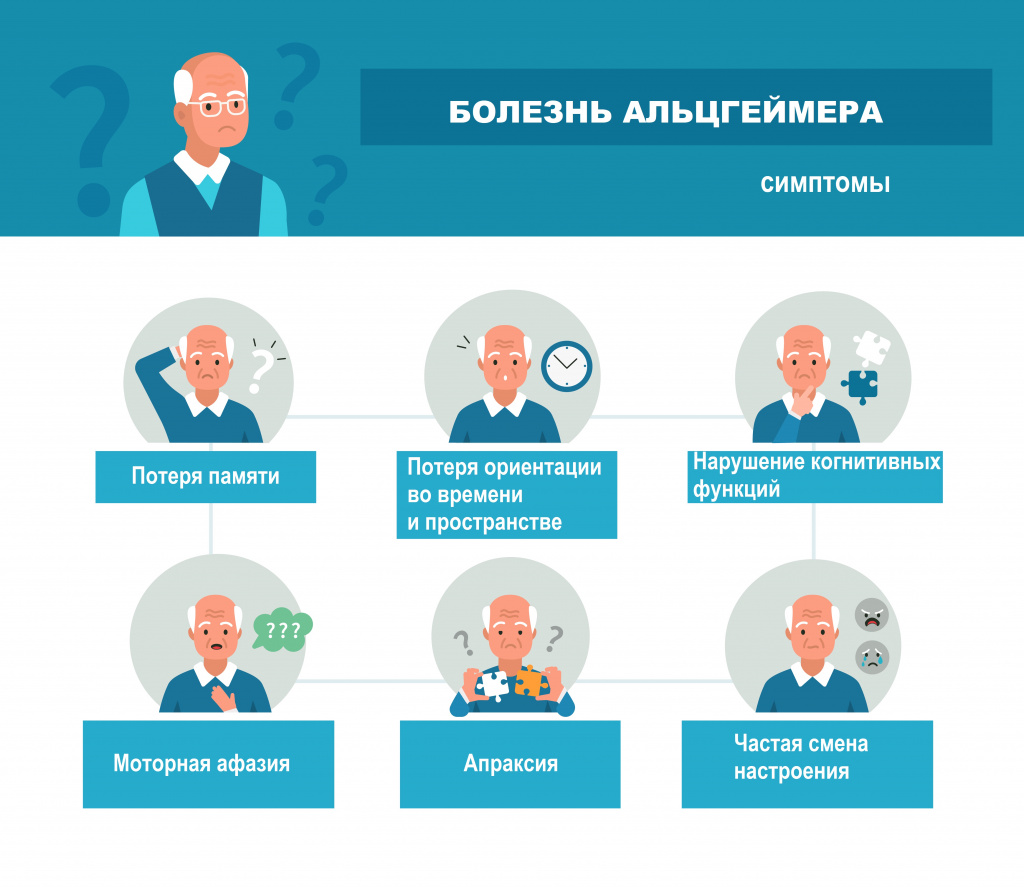
Основные симптомы болезни Альцгеймера:
- амнезия – потеря памяти, забывчивость;
- утрата способности концентрировать внимание;
- апраксия (утрата практических навыков, например, одевания, завязывания шнурков, приготовления кофе и пр.);
- потеря ориентации во времени и пространстве;
- нарушение когнитивных (познавательных) функций;
- агнозия (отсутствие интерпретации воспринимаемой информации);
- моторная афазия (нарушение речи, невнятная речь);
- апатия (отсутствие интереса к жизни, потеря интереса к прежним увлечениям и любимым занятиям);
- проблемы в самообслуживании и общении с другими людьми.
Даже у относительно молодых людей с отчетливыми депрессивными проявлениями возникают органические изменения в мозге, например, атрофия гиппокампа (части мозга, которая участвует в формировании эмоций, регистрации новой информации и пространственной памяти).
Все указанные симптомы проявляются постепенно, на начальных этапах больной может не ощущать серьезных проблем. По мере прогрессирования заболевания способность к критической оценке и внимание снижаются, а ухудшение памяти начинает выражаться сильнее. Люди с болезнью Альцгеймера забывает дату, день недели и год, свой домашний адрес и не узнают место, где находятся в данный момент времени. Потом присоединяются все новые и новые симптомы — речь становится более простой, слова выпадают из памяти и часто заменяются похожими по смыслу, теряется узнавание предметов и их функционального назначения, начинают страдать жизненные навыки – пользование даже обычными бытовыми приборами становится проблемой. В большинстве случаев пациенты не замечают изменения вокруг и в себе, хотя иногда могут быть моменты прояснения, и понимание становится более ясным.
Постепенно уменьшается способность узнавать близких. На поздних стадиях болезни полностью утрачивается способность говорить и понимать речь других. Все прежние навыки человека исчезают, он больше не может встать с постели, одеться, пойти в туалет и самостоятельно поесть.
У пациентов с болезнью Альцгеймера часто наблюдаются расстройства психики и поведения, появляются раздражительность, агрессивность, перепады настроения, необоснованное чувство страха, тревожность, подозрительность, нарушения сна (трудности с засыпанием, нарушение суточного режима, ночные блуждания).
Диагностика болезни Альцгеймера
Как правило, диагностика болезни Альцгеймера схожа с диагностикой других видов деменции. Но несмотря на клинические и специфические лабораторные и визуализационные характеристики, окончательный диагноз может быть подтвержден только гистологическим исследованием ткани мозга.
При наличии у пациента или его близких жалоб на снижение памяти, профессиональную и социальную дезадаптацию проводят:
- объективное обследование для выявления характерных клинических признаков деменции;
- сбор анамнеза и выяснение семейной истории болезни Альцгеймера;
- исследование психического статуса.
Клинические критерии позволяют с 85% точностью установить диагноз и дифференцировать болезнь Альцгеймера от иных вариантов деменции, таких как сосудистая деменция или деменция с тельцами Леви.
Для выявления других поддающихся лечению причин деменции и нарушений, которые могут усугубить симптомы, проводятся лабораторные исследования:
-
генетическая предрасположенность к атеросклерозу и болезни Альцгеймера;
Тест используется для диагностики гиперлипидемии III типа, а также для прогноза развития болезни Альцгеймера Аполипопротеин E (ApoE) – гликопротеин плазмы крови, участвующий в элиминации липопротеинов из циркуляции. Он является структурным белком хиломикронов, липопротеинов.
Болезнь Альцгеймера вызывает прогрессирующую утрату когнитивных способностей и характеризуется накоплением бета-амилоида и образованием нейрофибриллярных клубочков в коре головного мозга и подкорковом сером веществе. Диагноз устанавливается клинически; с целью выявления специфических признаков, предполагающих болезнь Альцгеймера, и для дифференциальной диагностики и выявления других курабельных случаев деменции обычно выполняются лабораторные и нейровизуализационные исследования. Лечение носит поддерживающий характер. В некоторых случаях применение ингибиторов холинэстеразы временно улучшает когнитивные функции.
Возраст от 65 до 74: 3%
Возраст от 75 до 84: 17%
Заболевание вдвое чаще встречается у женщин, чем у мужчин, что отчасти связано с большей продолжительностью жизни женщин. Преобладание количества больных в развитых странах связано с увеличением в них доли пожилых людей.
Общие справочные материалы
Этиология болезни Альцгеймера
Большинство случаев болезни Альцгеймера носит спорадический характер, с поздним началом (старше 65 лет) и неуточненной этиологией. Риск развития заболевания лучше всего предсказывается по возрасту пациентов. Вместе с тем, от 5 до 15% случаев заболевания носит семейный характер, половина из них характеризуется ранним началом (моложе 65 лет) и обычно связана со специфическими генетическими мутациями.
По меньшей мере, 5 различных локусов, расположенных на 1, 12, 14, 19 и 21 хромосомах, оказывают влияние на возникновение и прогрессирование болезни Альцгеймера.
Мутации в генах, кодирующих синтез белков–предшественников амилоида (пресенилина I и пресенилина II), могут приводить к аутосомно-доминантным формам болезни Альцгеймера еще до наступления пожилого возраста. Таким образом, у больных лиц нарушается синтез белков–предшественников амилоида, что приводит к накоплению и отложению фибриллярных агрегатов бета-амилоида, в свою очередь, бета-амилоид является основным компонентом сенильных бляшек, которые состоят из дегенеративно измененных аксонов или дендритов, астроцитов и глиальных клеток, расположенных вокруг амилоидного ядра. Beta -амилоид может также изменить деятельность киназ и фосфатаз, что приводит к гиперфосфорилированию тау (белок, стабилизирующий микроканальцы) и формированию нейрофибриллярных клубков.
Прочие генетические детерминанты включают ε-аллели аполипопротеина (аро) Е (эпсилон). Апо Е протеин влияет на накопление бета-амилоида, целостность цитоскелета и эффективность восстановления нейронов. Риск болезни Альцгеймера в значительной степени повышен у людей, имеющих две эпсилон-4 аллеля, и понижается у людей, имеющих эпсилон-2 аллеля. Для людей с 2 эпсилон-4 аллелью, риск развития болезни Альцгеймера к возрасту 75 лет в 10-30 раз выше, чем для людей без аллели.
Сосудистые факторы риска, такие как гипертония, диабет, дислипидемия и курение, могут увеличить риск болезни Альцгеймера. Появляется все больше данных, свидетельствующих о том, что агрессивное лечение этих факторов риска уже в среднем возрасте может ослабить риск развития когнитивных нарушений в пожилом возрасте.
Взаимосвязь между иными факторами например, низким содержанием гормонов, воздействием металлов и болезнью Альцгеймера четких данных за ее наличие не получено.
Патофизиология болезни Альцгеймера
Два отличительных патологических признака болезни Альцгеймера:
Внеклеточные бета-амилоидные отложения (в сенильных бляшках)
Внутриклеточные нейрофибриллярные клубки (парные спиральные нити)
Отложение бета-амилоидов и нейрофибриллярные клубки приводят к утрате синапсов и нейронов, что, в свою очередь, ведет к грубой атрофии пораженных участков головного мозга, в типичных случаях начинающейся с медиальной височной доли.
Механизм, с помощью которого бета-амилоидный пептид и нейрофибриллярные клубки вызывают это повреждение, не полностью изучен. Существует несколько теорий.
Гипотеза амилоида утверждает, что прогрессивное накопление бета-амилоида в головном мозге вызывает сложный каскад событий, заканчивающийся гибелью нейронов, потерей нейронных синапсов и прогрессирующим дефицитом нейромедиаторов; все вышеизложенное способствует развитию клинических симптомов деменции.
При болезни Альцгеймера были выявлены прионные механизмы. При прионных заболеваниях Обзор прионных заболеваний (Overview of Prion Diseases) Прионные болезни представляют собой прогрессирующие дегенеративные, неизлечимые и в конечном итоге летальные поражения головного мозга. Известные типы включают Болезнь Крейтцфельда–Якоба (БКЯ). Прочитайте дополнительные сведения белок нормальной поверхности клетки, именуемый прионным белком, превращается в патогенную форму, называемую прион. Затем прион вызывает превращение других прионных белков аналогичным образом, в результате заметно увеличивается количество аномальных белков, что приводит к повреждению мозга. Пологают, что при болезни Альцгеймера бета-амилоид в церебральных амилоидных отложениях и тау в нейрофибриллярных клубках имеют прионный тип со свойством самовоспроизведения.
Справочные материалы по патофизиологии
1. Kinney JW, Bemiller SM, Murtishaw AS, et al: Inflammation as a central mechanism in Alzheimer's disease. Alzheimers Dement (NY) 4:575–590, 2018. doi: 10.1016/j.trci.2018.06.014
Симптомы и признаки болезни Альцгеймера
Наиболее распространенными первыми проявлениями болезни Альцгеймера являются
Потеря кратковременной памяти (например, больные задают повторяющиеся вопросы, часто кладут предметы не на их место или забывают их назначение)
Другие когнитивные расстройства имеют тенденцию вовлекать множество функций, включая следующие:
Нарушение хода рассуждений и решения сложных задач, недальновидность (например, больные могут быть не в состоянии управлять банковским счетом, принимают плохие финансовые решения)
Лингвистическая дисфункция (например, трудности мышления при помощи общеизвестных слов, ошибки речи и/или письма)
Дисфункция зрительно-пространственной ориентации (например, невозможность узнавать лица или обычные объекты)
Болезнь Альцгеймера постепенно прогрессирует, но может также иметь и периоды стабильного непрогрессирующего течения (плато).
Диагностика болезни Альцгеймера
Схожа с диагностикой иных деменций
Требуется формальная оценка психического статуса
Сбор анамнеза и физикальное обследование
Как правило, диагностика болезни Альцгеймера схожа с диагностикой других видов деменции Диагностика Деменция – это хроническое, общее, как правило, необратимое снижение когнитивных функций, затрагивающее все аспекты познавательной деятельности. Диагноз деменции устанавливается клинически;. Прочитайте дополнительные сведения . Однако, несмотря на клинические и специфические лабораторные и визуализационные характеристики, окончательный диагноз болезни Альцгеймера может быть подтвержден только гистологическим исследованием ткани мозга.
Рекомендации по диагностике деменции, включая болезнь Альцгеймера, доступны на: National Institute for Health and Care Excellence.
Традиционные диагностические критерии болезни Альцгеймера включают следующие пункты:
Клинически установленная деменция, подтвержденная исследованием психического статуса
Нарушения, выявляемые в 2 и более когнитивных сферах
Постепенное начало (от месяцев до нескольких лет более вероятно, чем дни или недели) и прогрессирующее ухудшение памяти, а также прочих когнитивных функций
Отсутствие нарушений сознания
Начало после 40 лет, но чаще всего после 65 лет
Отсутствие системных заболеваний и заболеваний головного мозга (таких, как опухоль, инсульт), которые могут способствовать прогрессирующему снижению памяти и когнитивных функций
Тем не менее, определенные отклонения от перечисленных критериев не исключают диагноз болезни Альцгеймера, например, вследствие наличия у пациента смешанной деменции.
Низкий уровень бета-амилоида в спинномозговой жидкости (СМЖ)
Бета-амилоидные отложения в головном мозге, обнаруженные с помощью позитронно-эмиссионной томографии (ПЭТ) с использованием радиоактивного индикатора, который связывается специфически с бета-амилоидными бляшками (например, Питтсбург соединение B [PiB], флорбетапир)
Другие биомаркеры показывают нисходящую дегенерацию нейронов или повреждение:
Повышенные уровни тау-белка в СМЖ или его депозиты в головном мозге, обнаруженные с помощью ПЭТ с использованием радиоактивного индикатора, который специфически связывается с тау-белком
Снижение мозгового метаболизма височно-теменной коры измеряется с помощью ПЭТ с использованием фтор-18 (18F)-меченой дезоксиглюкозы (фтордезоксиглюкозы, или ФДГ)
Локальная атрофия медиальных, базальных и боковых височных долей и медиальной теменной коры определяется на МРТ
Для выявления других поддающихся лечению причин деменции и нарушений, которые могут усугубить симптомы, проводятся лабораторные исследования (определение уровня тиреотропного гормона, уровня витамина B12) и нейровизуализация (МРТ или КТ). Если клиническое обследование позволяет заподозрить наличие другого основного заболевания (например, ВИЧ-инфекции или сифилиса), показано проведение анализов на эти заболевания.
Дифференциальная диагностика
Пациенты с болезнью Альцгеймера, в отличие от пациентов с иными вариантами деменций, чаще выглядят более ухоженными и опрятными.
Справочные материалы по диагностике
1. Jack CR Jr, Albert MS, Knopman DS, et al: Introduction to the revised criteria for the diagnosis of Alzheimer’s disease: National Institute on Aging and Alzheimer's Association workgroups. Alzheimers Dement 7 (3):257–262, 2011. doi: 10.1016/j.jalz.2011.03.004
2. McKhann GM, Knopman DS, Chertkow H, et al: The diagnosis of dementia due to Alzheimer's disease: Recommendations from the National Institute on Aging-Alzheimer's Association workgroups on diagnostic guidelines for Alzheimer's disease. Alzheimers Dement 7 (3):263–269, 2011. doi: 10.1016/j.jalz.2011.03.005
3. Chételat G, Arbizu J, Barthel H, et al: Amyloid-PET and 18 F-FDG-PET in the diagnostic investigation of Alzheimer's disease and other dementias. Lancet Neurol 19:951–962, 2020. doi: 10.1016/S1474-4422(20)30314-8
Прогноз при болезни Альцгеймера
Несмотря на то, что темпы прогрессирования болезни Альцгеймера варьируют, снижение когнитивных функций является неизбежным. Средняя выживаемость от времени установления диагноза составляет 7 лет, однако подобный прогноз обсуждается. Средняя выживаемость от момента, когда пациент перестает передвигаться, составляет около 6 месяцев.
Лечение болезни Альцгеймера
Меры безопасности и поддерживающая терапия
Возможно применение ингибиторов холинэстеразы и мемантина
Меры безопасности и поддерживающие меры Лечение Деменция – это хроническое, общее, как правило, необратимое снижение когнитивных функций, затрагивающее все аспекты познавательной деятельности. Диагноз деменции устанавливается клинически;. Прочитайте дополнительные сведения при болезни Альцгеймера такие же, как и при всех остальных видах деменции. Например, окружение должно быть ярким, веселым и знакомым, и оно должно быть направлено на укрепление ориентации (например, размещение больших часов и календарей в комнате). Меры по обеспечению безопасности пациентов (например, системы мониторинга сигналов для пациентов, которые могут заблудиться) должны быть реализованы.
Также важным аспектом является обеспечение помощи для опекунов Помощь ухаживающих лиц Деменция – это хроническое, общее, как правило, необратимое снижение когнитивных функций, затрагивающее все аспекты познавательной деятельности. Диагноз деменции устанавливается клинически;. Прочитайте дополнительные сведения , которые могут испытывать значительный стресс. Медсестры и социальные работники могут научить ухаживающих, как наилучшим образом удовлетворить потребности пациента. Необходимо, чтобы врачи обращали внимание на ранние симптомы проявления у сиделок стресса и синдрома выгорания и, если это необходимо, давали рекомендации по модификации порядка осуществления ухода.
Препараты для лечения болезни Альцгеймера
Ингибиторы холинэстеразы умеренно улучшают когнитивные функции и память у некоторых пациентов. Доступно четыри таких препарата. Как правило, донепезил, ривастигмин и галантамин одинаково эффективны; такрин применяется реже, поскольку обладает гепатотоксичностью.
Донепезил – препарат 1-ой линии терапии, так как суточная доза принимается однократно, а сам препарат хорошо переносится больными. Рекомендуемая доза составляет 5 мг перорально 1 раз в день в течение 4–6 недель, затем доза увеличивается до 10 мг 1 раз в день. Доза донепезила ─ 23 мг 1 раз в день может быть более эффективной, чем традиционная доза ─ 10 мг один раз в день ─ для умеренной или тяжелой форм болезни Альцгеймера. Лечение необходимо продолжить, если спустя несколько месяцев от начала приема появилось функциональное улучшение, в противном случае его следует прекратить. Наибольшее количество нежелательных реакций отмечено со стороны желудочно-кишечного тракта (в том числе, тошнота, диарея). Реже, возникают головокружение и нарушения сердечного ритма (аритмии). Побочные реакции могут быть минимизированы путем постепенного наращивания дозировки (см. таблицу Препараты для лечения болезни Альцгеймера Препараты для лечения болезни Альцгеймера Болезнь Альцгеймера вызывает прогрессирующую утрату когнитивных способностей и характеризуется накоплением бета-амилоида и образованием нейрофибриллярных клубочков в коре головного мозга и подкорковом. Прочитайте дополнительные сведения ).
Мемантин, антагонист N-метил- d -аспартат (NMDA) рецепторов, похоже, восстанавливает когнитивные и функциональные возможности у пациентов с умеренной и тяжелой стадиями болезни Альцгеймера. Доза составляет 5 мг перорально за один прием, а затем в течение 4 недель повышается до 10 мг перорально 2 раза в день. При наличии у пациентов почечной недостаточности необходимо уменьшить дозу или не назначать данный препарат. Мемантин может применяться совместно с ингибиторами холинэстеразы.
Нет точных данных касательно эффективности высоких доз витамина Е (1000 ME перорально 1–2 раза в день), селегилина, нестероидных противовоспалительных средств (НПВС), экстрактов гинкго билоба и статинов. Терапия эстрогенами не подтвердила положительного эффекта в превентивном лечении и может быть небезопасной. Клинические испытания с исследуемыми препаратами, которые нацелены на накопление и очищение от бета-амилоидного белка, не были успешными, хотя некоторые исследования все еще продолжаются.
Читайте также:

