Аллостерическая регуляция цтк кратко
Обновлено: 30.06.2024
Окислительное декарбоксилирование пирувата — необратимый процесс, приводящий к образованию ацетил-КоА. Регуляция этого процесса крайне важна для клеток и организма в целом. Она осуществляется с помощью двух механизмов:
1. Аллостерическая регуляция :
а. АТФ , NADH и ацетил-КоА ингибируют пируватдегидрогеназный комплекс. Они конкурируют с молекулами NAD+ и КоА за активные центры. Кроме этого, они меняют направление реакций, катализируемых E 2 и E 3 (в обратную сторону). Высокие показатели соотношений [NADH] / [NAD + ] и [Ацетил-КоА] / [КоА] поддерживают E 2 в ацетилированной форме, что препятствует передаче на
Регуляция ЦТК и окислительного декарбоксилирования пирувата 73
него гидроксиэтильной группы от E 1 • тиамин-пирофосфата. В результате тиаминпирофосфат так и остаётся связанным с гидроксиэтильной группой, и скорость декарбоксилирования пирувата снижается.
б. NAD + и Кофермент А оказывают обратный эффект — активируют мультиферментный комплекс.
2. Ковалентная модификация E 1 (фосфорилирование/дефосфорилирование):
а. У эукариот продукты окислительного декарбоксилирования пи-
рувата — NADH и ацетил-КоА — активируют киназу пируватде-
гидрогеназы 1 . Киназа фосфорилирует пируватдегидрогеназный комплекс по остаткам серина и выключает его. Биохимический смысл такой регуляции заключается в том, что при достаточном количестве энергии в клетке нет необходимости окислять пируват до ацетил-КоА и направлять его в ЦТК.
б. Молекулы пирувата и АДФ оказывают прямо противоположный эффект на киназу пируватдегидрогеназы , ингибируя её. Ионы
Ca 2+ не только ингибируют киназу, но и активируют фосфатазу пируватдегидрогеназы , которая дефосфорилирует пируватдегидрогеназный комплекс и включает его. Такой же эффект оказы-
вает инсулин : он активирует фосфатазу пируватдегидроге-
назы . Таким образом, инсулин и кальций ускоряют процесс окисления пирувата до ацетил-КоА, а значит, и весь процесс накопления энергии в виде АТФ.
Б Регуляция ЦТК
В регуляции ЦТК участвуют 3 ключевых фермента: цитратсинтаза , изоцит-
ратдегидрогеназа и α-кетоглутаратдегидрогеназный комплекс . Эти ферменты исполь-
зуют три простых механизма регуляции:
1. Регуляция с помощью количества субстрата (его доступности).
2. Ингибирование метаболитами цикла по механизму отрицательной обратной связи.
Регуляция с помощью количества субстрата
Самыми главными регуляторами ЦТК являются его субстраты — ацетил-КоА и оксалоацетат — и его продукт — NADH . Ацетил-КоА и оксалоацетат находятся в митохондриях в тех концентрациях, которые не насыщают цитратсинтазу. Поэтому скорость работы этого фермента повышается, когда возрастает и концентрация его субстратов.
1 Обычно киназа пируватдегидрогеназы связана с пируватдегидрогеназным комплексом (входит в состав мультиферментной частицы).
Цикл трикарбоновых кислот
Проиллюстрируем на примере. Концентрация оксалоацетата уравновешена с концентрацией малата и зависит от соотношения [NADH] / [NAD + ] (последняя реакция ЦТК). Запишем константу равновесия для этой реакции:
При интенсивной работе мышц и дыхательной системы концентрация NADH снижается. При снижении NADH равновесие последней реакции сдвигается в сторону образования оксалоацетата (по принципу Ле Шателье). Повышение концентрации оксалоацетата стимулирует цитратсинтазную реакцию и повышает скорость образования цитрата из оксалоацетата и ацетил-КоА.
Ингибирование метаболитами цикла
Цитратсинтаза ингибируется целым рядом соединений: цитрат (продукт реакции), NADH, АТФ, сукцинил-КоА (конкурирует с ацетил-КоА за активный центр), ацетил-КоА (сигнал о достаточном количестве энергии в клетке).
Изоцитратдегидрогеназа активируется ионами Ca 2+ и молекулами АДФ (сигнал о снижении доступной энергии в клекте), ингибируется молекулами NADH и АТФ.
α -Кетоглутаратдегидрогеназный комплекс активируется ионами Ca 2+ и мо-
лекулами АМФ и АДФ (это говорит об увеличении потребности клетки в энергии АТФ), ингибируется сукцинил-КоА и NADH (см. Рис. 22 ).
Основным ингибитором всех трёх ферментов ЦТК является восстановленный NADH. Его избыток в митохондриях сигнализирует о достаточном количестве энергии (и молекул АТФ).
Образующийся в ПВК-дегидрогеназной реакции ацетил-SКоА далее вступает в цикл трикарбоновых кислот (ЦТК, цикл лимонной кислоты, цикл Кребса). Кроме пирувата, в цикл вовлекаются кетокислоты, поступающие из катаболизма аминокислот или каких-либо иных веществ.
Цикл трикарбоновых кислот
Цикл протекает в матриксе митохондрий и представляет собой окисление молекулы ацетил-SКоА в восьми последовательных реакциях.
В первой реакции связываются ацетил и оксалоацетат (щавелевоуксусная кислота) с образованием цитрата (лимонной кислоты), далее происходит изомеризация лимонной кислоты до изоцитрата и две реакции дегидрирования с сопутствующим выделением СО2 и восстановлением НАД.
В пятой реакции образуется ГТФ, это реакция субстратного фосфорилирования. Далее последовательно происходит ФАД-зависимое дегидрирование сукцината (янтарной кислоты), гидратация фумаровой кислоты до малата (яблочная кислота), далее НАД-зависимое дегидрирование с образованием оксалоацетата.
В итоге после восьми реакций цикла вновь образуется оксалоацетат.
Последние три реакции составляют так называемый биохимический мотив (ФАД-зависимое дегидрирование, гидратация и НАД-зависимое дегидрирование, он используется для введения кетогруппы в структуру сукцината. Этот мотив также присутствует в реакциях β-окисления жирных кислот. В обратной последовательности (восстановление, дегидратация и восстановление) этот мотив наблюдается в реакциях синтеза жирных кислот.
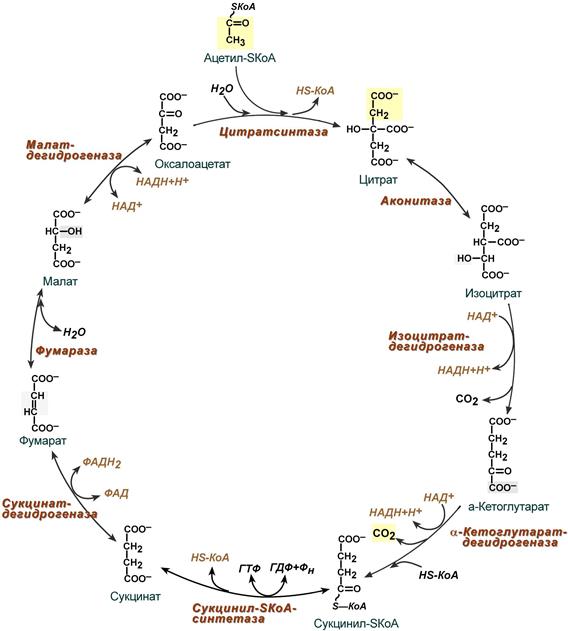
Реакции цикла трикарбоновых кислот
Функции ЦТК
- генерация атомов водорода для работы дыхательной цепи, а именно трех молекул НАДН и одной молекулы ФАДН 2 ,
- синтез одной молекулы ГТФ (эквивалентна АТФ).
2. Анаболическая . В ЦТК образуются
- предшественник гема – сукцинил-SКоА,
- кетокислоты, способные превращаться в аминокислоты – α-кетоглутарат для глутаминовой кислоты, оксалоацетат для аспарагиновой,
- лимонная кислота, используемая для синтеза жирных кислот,
- оксалоацетат, используемый для синтеза глюкозы.

Анаболические реакции ЦТК
Регуляция цикла трикарбоновых кислот
Аллостерическая регуляция
Ферменты, катализирующие 1-ю, 3-ю и 4-ю реакции ЦТК, являются чувствительными к аллостерической регуляции метаболитами:
| Ингибиторы | Активаторы | |
| Цитратсинтаза | АТФ, цитрат, НАДН, ацил-SКоА | |
| Изоцитрат-дегидрогеназа | АТФ, НАДН | АМФ, АДФ |
| α-Кетоглутарат-дегидрогеназа | Сукцинил-SКоА, НАДН |
Регуляция доступностью оксалоацетата
Главным и основным регулятором ЦТК является оксалоацетат , а точнее его доступность. Наличие оксалоацетата вовлекает в ЦТК ацетил-SКоА и запускает процесс.
Обычно в клетке имеется баланс между образованием ацетил-SКоА (из глюкозы, жирных кислот или аминокислот) и количеством оксалоацетата. Источником оксалоацетата являются
1) Пировиноградная кислота, образуемая из глюкозы или аланина,
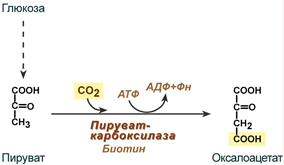
Синтез оксалоацетата из пирувата
Регуляция активности фермента пируваткарбоксилазы осуществляется при участии ацетил-SКоА. Он является аллостерическим активатором фермента, и без него пируваткарбоксилаза практически неактивна. Когда ацетил-SКоА накапливается, то фермент начинает работать и образуется оксалоацетат, но, естественно, только при наличии пирувата.
2) Получение из аспарагиновой кислоты в результате трансаминирования или из цикла АМФ-ИМФ,
3) Поступление из фруктовых кислот самого цикла (янтарной, α-кетоглутаровой, яблочной, лимонной), образуемых при катаболизме аминокислот или в других процессах. Большинство аминокислот при своем катаболизме способны превращаться в метаболиты ЦТК, которые далее идут в оксалоацетат, чем также поддерживается активность цикла.

Пополнение пула метаболитов ЦТК из аминокислот
Реакции пополнения цикла новыми метаболитами (оксалоацетат, цитрат, α-кетоглутарат и т.п) называются анаплеротическими .
Роль оксалоацетата в метаболизме
Примером существенной роли оксалоацетата служит активация синтеза кетоновых тел и кетоацидоз плазмы крови при недостаточном количестве оксалоацетата в печени. Такое состояние наблюдается при декомпенсации инсулинзависимого сахарного диабета (СД 1 типа) и при длительном голодании. При указанных нарушениях в печени активирован процесс глюконеогенеза, т.е. образования глюкозы из оксалоацетата и других метаболитов, что влечет за собой снижение количества оксалоацетата. Одновременная активация окисления жирных кислот и накопление ацетил-SКоА запускает резервный путь утилизации ацетильной группы – синтез кетоновых тел. В организме при этом развивается закисление крови (кетоацидоз) с характерной клинической картиной: слабость, головная боль, сонливость, снижение мышечного тонуса, температуры тела и артериального давления.

Изменение скорости реакций ЦТК и причины накопления кетоновых тел при некоторых состояниях
Описанный способ регуляции при участии оксалоацетата является иллюстрацией к красивой формулировке " Жиры сгорают в пламени углеводов ". В ней подразумевается, что "пламень сгорания" глюкозы приводит к появлению пирувата, а пируват превращается не только в ацетил-SКоА, но и в оксалоацетат. Наличие оксалоацетата гарантирует включение ацетильной группы, образуемой из жирных кислот в виде ацетил-SКоА, в первую реакцию ЦТК.
В случае масштабного "сгорания" жирных кислот, которое наблюдается в мышцах при физической работе и в печени при голодании, скорость поступления ацетил-SКоА в реакции ЦТК будет напрямую зависеть от количества оксалоацетата (или окисленной глюкозы).
Если количество оксалоацетата в гепатоците недостаточно (нет глюкозы или она не окисляется до пирувата), то ацетильная группа будет уходить на синтез кетоновых тел. Такое происходит при длительном голодании и сахарном диабете 1 типа.
Автор текста – Анисимова Елена Сергеевна.
Авторские права защищены. Продавать текст нельзя.
Курсив не зубрить.
Содержание параграфа 21:
21. 1. Цикл трикарбоновых кислот:
реакции,
ферменты и их коферменты,
витамины, необходимые для их работы.
21. 2. Субстратное фосфорилирование в 4-й и 5-й реакции ЦТК.
21. 3. Регуляция ЦТК.
21. 4. Биологические функции цтк.
21. 4. 1. Катаболически-энергетическая функция ЦТК:
21. 4. 2. Анаболическая функция ЦТК.
21. 4. 3. Регуляторная функция ЦТК.
21. 1. ЦИКЛ трикарбоновых кислот:
реакции, ферменты и их коферменты,
витамины, необходимые для их работы.
Необратимые реакции катализируются ключевыми ферментами,
а обратимые реакции – не ключевыми ферментами.
Знать названия ферментов, если они не являются ключевыми или ДГ, не обязательно.
Ключевыми ферментами ЦТК являются все ДГ,
кроме последней –
то есть ИЦДГ, КГДГ, СДГ ключевые, а МДГ – не ключевой.
Еще один ключевой фермент ЦТК – цитрат/синтаза, то есть самый 1 фермент.
Всего ключевых – 4.
Порядок основных метаболитов ЦТК:
ацетилКоА + оксалоацетат ;
цитрат ; изоцитрат ; кетоглутарат ;
сукцинилКоА ; сукцинат ;
фумарат ; малат ; оксалоацетат.
Формулы этих метаболитов нужно знать очень хорошо.
В формуле ацетилКоА 2 С,
в формуле цитрата и (его изомера) изоцитрата по 6 С,
в формуле кетоглутарата 5 С,
а в остальных формулах – по 4 С.
Оксалоацетат – это (почти) сукцинат с кетогруппой (=О),
малат – это сукцинат с гидроксильной группой (ОН),
фумарат – это сукцинат без 2-х атомов водорода и с двойной связью.
1-я реакция ЦТК (необратимая).
Образование цитрата
при взаимодействии ацетилКоА и оксалоацетата.
Схема 1-й реакции ЦТК:
ацетилКоА + оксалоацетат + Н2О ;
цитрат + КоА.
Катализируется ферментом цитрат/синтазой*
(фермент регуляторный = ключевой,
как часто и бывает у первых ферментов метаболических путей – п.7).
Источник энергии для реакции –
расщепление макроэргической связи ацетилКоА.
Нужно знать, но не нужно учить, так как все это легко вычисляется
при сравнении формул субстратов и продуктов:
1) из двух углеродов ацетилКоА
и 4-х углеродов оксалоацетата
образуется шести-углеродный скелет цитрата (2+4=6),
2) второй углерод ацетилКоА
присоединяется ко второму углероду оксалоацетата,
3) в реакцию вступает также молекула воды,
а среди продуктов есть КоА.
2-я реакция ЦТК (обратимая).
Превращение цитрата в изоцитрат (путем изомеризации).
Схема 2-й реакции ЦТК:
цитрат ; изоцитрат.
Сравнение формул цитрата и изоцитрата показывает,
что формула изоцитрата отличается от формулы цитрата
только расположением -ОН группы.
Превращение происходит путем отщепления от цитрата воды
(ОН от 3-го С и Н – от 2-го С)
и последующего присоединения воды обратно,
но при этом ОН присоединяется ко 2-му С, а Н – к 3-му С.
Фермент – цитрат/изомераза (аконитаза).
3-я реакция ЦТК (необратимая).
Превращение изоцитрата в кетоглутарат
путем окислительного декарбоксилирования
под действием фермента изоцитрат/ДГ* (ключевой фермент).
Схема 3-й реакции ЦТК:
изоцитрат + НАД+ ;
кетоглутарат + СО2 + НАДН и Н+.
Сравнение формул изоцитрата и кетоглутарата показывает,
что формула кетоглутарата отличается от формулы изоцитрата
отсутствием атомов СОО карбоксильной группы при 3-м атоме С
и пары атомов водорода во втором положении (при С и при О).
Это подсказывает следующее:
происходит отщепление от изоцитрата (от 3-го С)
карбоксильной группы
(в виде СО2 – это декароксилирование)
и отщепление пары атомов водорода (2-х протонов и 2х электронов –
это окисление).
Поэтому процесс называется окислительным декарбоксилированием.
Фермент называется дегидрогеназой
потому, что катализирует дегидрирование –
отщепление атомов водорода.
Отщепленный СО2 в основном попадет в легкие для выдоха – п.122.
Отщепленный водород переносится на кофермент
для переноса в ДЦ и выработки АТФ (2,5 молекул АТФ).
В данном случае водород переносится на кофермент НАД+,
который превращается при этом в НАДН и Н+
(восстановленную форму кофермента).
В этой реакции происходит укорочение углеродного скелета изоцитрата на 1С.
Это один из двух атомов углерода, которые входили в состав ацетилКоА.
В следующей реакции происходит отщепление еще одного атома углерода.
И в итоге оба атома молекулы ацетил КоА превращаются в СО2.
А углеродный скелет из двух атомов углерода молекулы ацетил КлА
распадается на две одноуглеродных молекулы СО2.
Тем самым завершается разрушение углеродных скелетов, начатое ранее – п.20.3.
Для этой реакции нужен витамин РР в составе кофермента НАД.
4-я реакция ЦТК (необратимая).
Превращение кетоглутарата в сукцинилКоА
под действием фермента кетоглутарат/ДГ*
(кетоглутарат/дегидрогеназного комплекса),
путем окислительного декарбоксилирования.
Схема 4-й реакции ЦТК:
кетоглутарат + НАД+ + КоА ;
сукцинилКоА + СО2 + НАДН и Н+.
Отщепленная карбоксильная группа выделяется в виде СО2,
а отщепленные атомы водорода переносятся на кофермент НАД+,
в результате чего он превращается в НАДН
и далее отдаст атомы водорода в ДЦ.
В этой реакции происходит укорочение углеродного скелета кетоглутарата на 1С. Это еще один из двух атомов углерода, которые входили в состав ацетилКоА (укорочение на один атом С происходит и в предыдущей реакции).
Для этой реакции нужен витамин В2 в составе кофермента ФАД.
А также – витамин РР в составе кофермента НАД,
Витамин пантотенат в составе кофермента А и витамин В1.
Точно такой же набор витаминов и коферментов нужен
и для превращения пирувата в ацетилКоА
(для окислительного декарбоксилирования пирувата) – п.32.
При этом роль НАД и КоА ясна уже из схемы реакции,
а про В1 и В2 нужно просто запомнить,
что они нужны в тех же реакциях ЦТК, где участвует КоА.
5-я реакция ЦТК (обратимая).
Превращение сукцинилаКоА в сукцинат
(под действием фермента сукцинилКоА/синТЕтазы).
Схема 5-й реакции ЦТК:
сукцинилКоА + ГДФ + фосфат ;
сукцинат + ГТФ;
Далее:
ГТФ + (АДФ + фосфат) ;
(ГДФ + фосфат) + АТФ.
Из названий субстрата и продукта понятно,
что КоА отщепляется от сукцинила,
сравнение формул сукцинилКоА и сукцината показывает,
что на месте КоА появляются ОН атомы.
При отщеплении КоА происходит разрушение макроэргической связи,
что сопровождается выделением энергии.
За счет этой энергии происходит образование другой макроэргической связи –
связи между ГДФ и фосфатом.
В результате присоединения фосфата к ГДФ образуется ГТФ.
ГТФ может расщепляться на ГДФ и фосфат,
что сопровождается выделением энергии.
За счет этой энергии (которая выделяется при расщеплении ГТФ на ГДФ и фосфат)
может синтезироваться АТФ из АДФ и фосфата.
В результате пятая реакция ЦТК приводит к образованию 1 молекулы АТФ.
При расщеплении сукцинилКоА происходит присоединение воды, но это обычно не отмечают,
так как вода выделяется при образовании ГТФ.
6-я реакция ЦТК (необратимая)
Превращение сукцината в фумарат
под действием фермента сукцинат/дегидрогеназа*.
Схема 6-й реакции ЦТК:
сукцинат + ФАД ;
фумарат + ФАДН2.
Сравнение формул сукцината и фумарата показывает,
что формула фумарата отличается от формулы сукцината
отсутствием двух атомов водорода.
То есть при превращении сукцината в фумарат
происходит отщепление двух атомов водорода – дегидрирование.
Поэтому фермент называется сукцинат/дегидрогеназой*.
Отщепленные от сукцината атомы водорода
присоединяются к коферменту ФАД
(который превращается при этом в ФАДН2),
для передачи атомов водорода в ДЦ и выработки 1,5 АТФ.
Для этой реакции нужен витамин В2 в составе кофермента ФАД.
7-я реакция ЦТК (обратимая):
Превращение фумарата в малат.
Схема 7-й реакции ЦТК:
фумарат + НОН ;
малат.
Сравнение формул фумарата и малата показывает,
что формула малата отличается от формулы фумарата
наличием атомов Н и ОН.
Это подсказывает, что при превращении фумарата в малат
происходит присоединение НОН, то есть гидратация.
Катализируется ферментом гидратазой (фумарат-гидратазой = фумаразой). Название фермента можно не учить.
Превращение малата в оксалоацетат
под действием фермента малат/дегидрогеназа.
Сравнение формул малата и оксалоацетата показывает,
что формула оксалоацетата отличается от формулы малата
отсутствием двух атомов водорода.
Из этого следует, что при превращении малата в оксалоацетат
происходит отщепление двух атомов водорода – дегидрирование.
Поэтому фермент называется малат/дегидрогеназой.
Отщепленные от малата атомы водорода
присоединяются к коферменту НАД+
для передачи атомов водорода в ДЦ и выработки 2,5 АТФ.
Для этой реакции нужен витамин РР в составе кофермента НАД.
21. 2. Субстратное фосфорилирование в 4-й и 5-й реакции ЦТК.
См.п.23.
В этом примере происходит синтез ГТФ (а в итоге и АТФ)
способом, который называется субстратным фосфорилированием (СФ).
Имеется в виду фосфорилирование ГДФ
(то есть присоединение фосфата к ГДФ)
за счет энергии, которая выделяется
при расщеплении макроэргической связи сукцинилКоА
(который называется первичным макроэргом).
Макроэргическая связь сукцинилКоА
образована за счет энергии,
которая выделилась при окислении кетоглутарата;
кетоглутарат называют субстратом
в этом примере субстратного фосфорилирования.
ГТФ и АТФ называют вторичными макроэргами.
Другие примеры (два) субстратного фосфорилирования встречаются в гликолизе.
Кроме субстратного фосфорилирования,
есть окислительное фосфорилирование (ОФ).
При окислительном фосфорилировании
синтез АТФ происходит за счет энергии,
которая выделяется при работе ДЦ.
Поэтому ОФ может происходить только при наличии кислорода, то есть в аэробных условиях.
Субстратное фосфорилирование не требует наличия кислорода,
то есть может происходить в анаэробных условиях.
Но что касается СФ в ЦТК,
то это СФ не происходит в анаэробных условиях,
потому что в анаэробных условиях не работает ЦТК.
ЦТК не работает в анаэробных условиях потому,
что без кислорода не работает ДЦ.
Без работы ДЦ, освобождающей коферменты НАДН и ФАДН2
от переносимых ими атомов водорода,
эти коферменты не могут передавать водород в ДЦ,
молекулы этих коферментов находятся в восстановленном состоянии
(то есть нагружены переносимыми ими атомами водорода),
а для работы ЦТК нужны окисленные коферменты.
21. 3. Регуляция ЦТК. См. таблицы в п.22.
1). Регуляция работы ЦТК осуществляется путем регуляции активности ключевых ферментов:
ЦТК – цитрат/синтазы, ИЦДГ, КГДГ, СДГ.
Ускорение активности ферментов приводит к ускорению реакций и наоборот.
Увеличивают активность ЦТК:
- гормоны
- - катехоламины (адреналин и норадреналин)
- и глюкагон,
- - вторые посредники (п.92) цАМФ и ионы кальция
- и метаболиты АДФ, НАД+.
Инсулин поддерживает ЦТК (п.102).
Уменьшают активность ЦТК:
метаболиты АТФ, НАДН,
главные продукты ЦТК –
это аллостеричекое ингибирование (п.6)
по принципу отрицательной обратной связи.
Значение регуляции ЦТК –
приспособление работы ЦТК к потребностям организма.
Например, адреналин и норадреналин (катехоламины) –
это гормоны стресса,
при котором увеличивается потребность в выработке АТФ
(так как увеличиваются затраты АТФ).
ЦТК необходим для выработки АТФ
(так как ЦТК поставляет для ДЦ восстановленные коферменты),
поэтому катехоламины увеличивают активность ЦТК.
цАМФ и ионы кальция (п.95)
участвуют в передаче сигнала катехоламинов и глюкагона в клетку
(эти гормоны связываются со своими рецепторами на поверхности клетки).
НАДН и АТФ снижают активность ЦТК потому,
что при наличии этих веществ в клетке в достаточных количествах
необходимость в работе ЦТК снижается,
так как эти вещества образуются за счет работы ЦТК,
то есть эти вещества являются продуктами ЦТК.
Если НАДН в клетке достаточно,
то ДЦ получит достаточно водорода
и сможет работать достаточно активно для того, чтобы был синтезирован АТФ.
НАД+ и АДФ повышают активность ЦТК,
когда их много в клетке.
Потому что накопление в клетке АДФ
означает дефицит в клетке АТФ
(АДФ образуется при расходе, использовании АТФ).
Накопление в клетке НАД+ означает, что НАДН в клетке мало,
ДЦ не получает достаточного количества водорода
и не может работать достаточно активно для того, чтобы был синтезирован АТФ.
И ингибиторы ЦТК (АТФ и НАДН),
и активаторы ЦТК (НАД+ и АДФ) являются (по механизму)
аллостерическими регуляторами ЦТК.
21. 4. Биологические ФУНКЦИИ ЦТК.
21. 4. 1. Катаболически-энергетическая функция ЦТК:
21. 4. 2. Анаболическая функция ЦТК.
21. 4. 3. Регуляторная функция ЦТК:
ЦТК необходим для выработки основного количества АТФ
(в большинстве клеток: кроме ЭЦ, в которых нет ЦТК).
Один оборот ЦТК, в котором происходит катаболизм одной молекулы АцетилКоА,
дает 10 молекул АТФ:
1 молекула АТФ образуется путем СФ
при превращении сукцинилКоА в сукцинат (реакции ЦТК 4 и 5).
9 молекул АТФ образуются путем ОФ с помощью ДЦ
1) в ЦТК от метаболитов отщепляются атомы водорода
(дегидрирование метаболитов),
2) атомы Н переносятся на 3 НАД+ и 1 ФАД,
образуя 3 НАДН (Н+) и 1 ФАДН2,
3) которые отдают водород в ДЦ для переноса на О2 и образования НОН.
В ЦТК АцетилКоА превращается в 2 молекулы СО2,
при этом происходит распад углеродного (катаболизм) скелета ацетилКоА:
двух/углеродная молекула ацетилКоА
превращается в две одноуглеродных молекулы СО2.
Поскольку ацетилКоА образуется
при катаболизме углеводов (гликолиз и ПДГ), жиров и белков,
то, превращая ацетилКоА в СО2,
ЦТК завершает катаболизм веществ разных классов.
Эта функция ЦТК, связанная с разрушением ацетилКоА
и выработкой АТФ, называется КАТАБОЛИЧЕСКИ-ЭНЕРГЕТИЧЕСКОЙ.
21. 4. 2. Анаболическая функция ЦТК.
Метаболиты ЦТК могут использоваться
для синтеза ряда веществ, для анаболизма.
Эта функция ЦТК называется анаболической.
Примеры:
1). Из ОА синтезируется ГЛЮКОЗА (в процессе ГНГ, п.33) –
это позволяет жить без пищи более 12 часов.
2). Из ОА и кетоглутарата
синтезируются заменимые аминокислоты
(Асп, АсН, Глу, ГлН, аргинин и др.) для синтеза белков
(Глу является еще нейромедиатором
и субстратом для синтеза другого медиатора – ГАМК). П.67.
3). Из сукцинилКоА
синтезируется порфирин для синтеза ГЕМА
для синтеза гемоглобина, цитохрома и ряда других белков. П.121.
4). П.46 и 48.
Из цитрата образуется ацетилКоА
для синтеза жирных кислот
(для синтеза липидов МЕМБРАН, жира),
кетоновых тел (питание тканей при голоде стрессе и др.)
и холестерина (для мембран, гормонов и др.).
Снижение работы ЦТК
из-за дефицита его витаминов, приема алкоголя (п.26) и т.д.
- приводит к снижению всех перечисленных синтезов,
- к гипогликемии при перерыве в питании или при голоде (риск обморока),
- к снижению деления клеток
(т.к. мало материала для мембран,
особенно при дефиците в питании жиров и белков,
а главное – мало АТФ),
- дистрофии (снижен синтез белка,
особенно при дефиците аминокислот в пище).
21. 4. 3. Регуляторная функция ЦТК:
метаболиты ЦТК регулируют активность других процессов.
Цитрат
ингибирует гликолиз
и активирует синтез жирных кислот.
АцетилКоА
ингибирует ПДГ
и активирует ГНГ (облигатный активатор).
НАДН ингибирует многие катаболические процессы (но не ДЦ).
Не путайте регуляторную роль ЦТК с регуляцией самого ЦТК.
Свидетельство и скидка на обучение каждому участнику
Зарегистрироваться 15–17 марта 2022 г.
ЦЕНТРАЛЬНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ:
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА,
ЦИКЛ ТИКАРБОНОВЫХ КИСЛОТ
ЦЕНТРАЛЬНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ
Основными поставщиками восстановленных субстратов являются центральные метаболические пути, а именно, окислительное декарбоксилирование пировиноградной кислоты и цикл лимонной кислоты. Они локализованы в матриксе митохондрий, в ходе этих процессов происходят реакции декарбоксилирования (большая часть всей углекислоты, образующейся в клетках, образуется именно здесь). Кроме того, в ходе этих процессов происходят реакции дегидрирования субстратов, образуются восстановленные коферментные формы НАДН·Н + и ФАДН2, водород которых поступает в дыхательную цепь внутренней мембраны митохондрий, где происходит его окисление кислородом до воды и синтез АТФ.

ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА
Пировиноградная кислота (ПВК, пируват) является продуктом окисления глюкозы и некоторых аминокислот. Ее судьба различна в зависимости от доступности кислорода в клетке. В анаэробных условиях она восстанавливается до молочной кислоты. В аэробных условиях происходит ее окислительное декарбоксилирование до уксусной кислоты, переносчиком которой служит коэнзим А.


Суммарное уравнение реакции отражает декарбоксилирование пирувата, восстановление НАД до НАДН Н + и образование ацетил-SKoA.
Окислительное декарбоксилирование пирувата состоит из пяти последовательных реакций и осуществляется при участии набора ферментов, объединенных в пируватдегидрогеназный комплекс (ПВДГК). Это мультиферментная система, которая включает 3 фермента и 5 коферментов (все они являются водорастворимыми витаминами).
Е1 — пируватдекарбоксилаза. Коферментом является активная форма витамина В1, тиамина — ТПФ (тиаминпирофосфат).
Е2 — дигидролипоилацетилтрансфераза. Коферментом является витаминоподобное вещество — липоевая кислота (липоил), которая может временно превращаться в дигидролипоил, присоединив 2 атома водорода. Липоил может также переносить ацетильные остатки.
С этим ферментом также работает активная форма пантотеновой кислоты — КоА-SH, которая принимает ацетильный остаток от липоевой кислоты.
Е3 — дигидролипоилдегидрогеназа. Коферментом является ФАД — активная форма витамина В2, рибофлавина. С работой этого фермента связан также кофермент НАД + — активная форма витамина РР, никотиновой кислоты.
Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется Е1), окислению пирувата до ацетила и переносу ацетила на коэнзим А (катализируется Е2).

Оставшиеся 2 реакции необходимы для возвращения липоевой кислоты и ФАД в окисленное состояние (катализируются Е3). При этом образуется


Таким образом, в результате образуются конечные продукты — СО2, атомы водорода для дыхательной цепи в составе НАДН·Н + и макроэргическое соединение ацетил- S КоА.
Лимитирующей реакцией в этом процессе является пируватдекарбоксилазная реакция. Поскольку фермент
Е1- пируватдекарбоксилаза в качестве кофермента использует ТПФ, при недостатке тиамина в пище нарушается окисление пирувата — процесса, который поставляет клеткам энергию. Возникает энергодефицит, что требует коррекции нарушения метаболизма с помощью тиамина. Схема регуляции работы пиуватдегидогеназного комплекса предствалена на рисунке (слайде).

ЛИМОННОКИСЛЫЙ ЦИКЛ КРЕБСА,
ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ (ЦТК)
Цикл лимонной кислоты локализован в матриксе митохондрий. Это циклический процесс из восьми последовательных реакций, в результате которых происходит декарбоксилирование и дегидрирование ацетил-КоА (универсального клеточного топлива).
Цикл начинается с конденсации ацетил-КоА с 4-углеродной кетокислотой — щавелевоуксусной (ЩУК). В результате образуется трикарбоновая кислота – лимонная, или цитрат. Изомеризация цитрата ведет к образованию изоцитрата. В ходе последовательных реакций изоцитрат де-карбоксилируется и одновременно дегидрируется (фермент изоцитратДГ). Образовавшийся альфа-кетоглутарат также декарбоксилируется и дегидрируется. Образовавшийся макроэрг сукцинил-КоА служит источником энергии для синтеза АТФ (субстратное фосфорилирование в цикле Кребса). В результате еще двух дегидрирований (ферменты сукцинатДГ и малатДГ) ЩУК регенерирует и запускает новый оборот цикла Кребса.
Таким образом, наряду с конечным продуктом обмена — СО2, в четырех дегидрогеназных реакциях трижды восстанавливается НАД+ (изоцитратДГ, альфа-кетоглутаратДГ, малатДГ) и один раз восстанавливается ФАД (сукцинатДГ). Чтобы цикл мог функционировать, необходимо окислить эти коферменты, т. е. передать атомы водорода в дыхательную цепь, где происходит их окисление кислородом до воды.


Функции цикла Кребса
1. Интегративная функция. Цикл Кребса является связующим звеном между реакциями катаболизма и анаболизма.
2. Катаболическая функция. В ходе ЦТК окисляются до конечных продуктов обмена ацетильные остатки, образовавшиеся из топливных молекул (глюкоза, жирные кислоты, глицерол, аминокислоты).
3. Анаболическая функция. Субстраты ЦТК являются основой для синтеза многих молекул (кетокислоты — α-кетоглутарат и ЩУК — могут превращаться в аминокислоты глутамин и аспарагин; ЩУК может превращаться в глюкозу, сукцинил-КоА используется на синтез гема).
4. Водороддонорная функция. Цикл Кребса поставляет субстраты для дыхательной цепи (НАД-зависимые субстраты: изоцитрат, альфа-кетоглутарат, малат; ФАД-зависимый субстрат – сукцинат).
5. Энергетическая функция. На уровне сукцинил-КоА происходит субстратное фосфорилирование с образованием 1 молекулы макроэрга. Помимо этого, 4 дегидрогеназные реакции в цикле Кребса создают мощный поток электронов, богатых энергией. Эти электроны поступают в дыхательную цепь внутренней мембраны митохондрий. Конечным акцептором электронов является кислород. При последовательном переносе электронов на кислород выделяется энергия, достаточная для образования 9 молекул АТФ путем окислительного фосфорилирования.
Несмотря на постоянную убыль субстратов в результате анаболической функции, цикл Кребса не прерывается благодаря анаплеротическим реакциям, которые пополняют фонд его субстратов. Важнейшей анаплеротической реакцией является образование ЩУК (молекулы, запускающей цикл) путем карбоксилирования ПВК.
Регуляция ЦТК
1. Главным и основным регулятором ЦТК является доступность оксалоацетата. Наличие оксалоацетата вовлекает в ЦТК ацетил-SКоА и запускает процесс.
В клетке имеется баланс между образованием ацетил-SКоА (из глюкозы, жирных кислот или аминокислот) и количеством оксалоацетата. Источником оксалоацетата является синтез из пирувата (анаплеротическая или пополняющая реакция), поступление из фруктовых кислот самого ЦТК (яблочной, лимонной), образование из аспарагиновой кислоты.

2. Ферменты ЦТК являются чувствительными к аллостерической регуляции метаболитами.
Например, первый фермент цитратсинтаза ингибируется АТФ, жирными кислотами. Лимитирующим ферментом (катализирует самую медленную реакцию) является изоцитратДГ. Он активируется АДФ, НАД+, ингибируется АТФ, НАДН·Н+. Когда в клетке достаточно АТФ (покой), скорость цикла снижается, при распаде же АТФ образуется АДФ, который активирует самую медленную реакцию и, следовательно, скорость всего цикла в целом.
Читайте также:

