Закон объемных отношений в химии кратко
Обновлено: 03.07.2024
1. Закон сохранения массы и энергии . Это объединенный закон. В него входят два закона.
Масса веществ, вступивших в реакцию, равна массе продуктов реакции.
Этот закон был открыт М.В. Ломоносовым (1748 г.) и дополнен А.Л.Лавуазье в 1789 г.
В процессе реакции сохраняется масса каждого элемента
Этот закон позволяет составлять уравнения химических реакций и осуществлять расчеты на их основе. Он не является абсолютным. Абсолютным является закон сохранения энергии.
Закон сохранения энергии
Энергия не возникает из ничего и не исчезает, а только переходит из одного вида в другой.
Этот закон – результат работ А. Эйнштейна. Он установил связь между энергией и массой вещества (1905 г.):
Е = mc 2 ,
где с – скорость света в вакууме, равная ~ 300 000 км/с.
Поскольку в результате химической реакции выделяется или поглощается энергия, то, в соответствии с уравнением Эйнштейна, изменяется и масса веществ. Однако это изменение столь мало, что на практике не учитывается (так называемый дефект массы).
Следующие законы справедливы только для соединений с постоянным составом молекул (дальтонидов). Они отличаются от соединений, имеющих переменный состав молекул – бертоллидов.
2. Закон постоянства состава (Ж. Пруст, 1801).
Соотношение между массами химических элементов, входящих в состав данного соединения, есть величина постоянная, не зависящая от способа его получения.
Например, как бы не получали воду – при сгорании водорода (2Н2 + О2 = 2Н2О) или при разложении гидроксида кальция (Са(ОН)2 = СаО + Н2О) – отношение масс атомов водорода и кислорода в реакции равно ~ 1:8.
3. Закон кратных отношений (Дж. Дальтон, 1803).
Если два элемента образуют друг с другом несколько химических соединений, то массы одного из элементов, приходящееся на определенную массу другого, относятся друг к другу как небольшие целые числа.
Этот закон подтвердил атомистическое представление о структуре материи: раз элементы соединяются в кратных отношениях, то химические соединения распадаются на целые атомы. Например, на 1 г азота в его оксидах N2O, NO, N2O3, NO2 и N2O5 приходится 0,57; 1,14; 1,71; 2,28 и 2,85 г кислорода, что соответствует отношению 1:2:3:4:5. Однако в случае соединений переменного состава этот закон неприменим.
4. Закон простых объемных отношений (Ж. Гей-Люссак, 1808).
При равных условиях объем вступающих в реакцию газов относятся друг к другу и к объемам образовавшихся газообразных продуктов как небольшие целые числа.
так, например, в реакции образования аммиака из простых веществ
отношение объемов азота (N), водорода (H) и аммиака (NH3) составляет 1:3:2.
5. Закон Авогадро (1811).
В равных объемах различных газов при одинаковых условиях (р и Т) содержится одинаковое число молекул.
Этот закон вытекает из анализа уравнения состояния идеального газа Клапейрона–Менделеева:
рV = nRT.
Это уравнение можно записать для двух газов:
p1V1 = n1RT1;
p2V2 = n2RT2.
При равенстве р1 = р2, Т1 = Т2 и V1 = V2 будут равны и количества вещества газов: n1 = n2 или, с учетом числа Авогадро:
n1 · NA = n2 · NA,
т.е. будет равно и число молекул газов.
Закон Авогадро имеет следствия :
- Одинаковое число молекул любого газа при одинаковых условиях занимает один и тот же объем.
- Массы газов, взятых в одинаковых объемах при одинаковых условиях (р, Т), относятся друг к другу как их молярные массы:
Это следствие вытекает из равенства количеств веществ этих газов n1 = n2.
Подставляя вместо количества вещества отношения его массы к молярной массе n = m/M получим:
m1/ M1= m2/M2 или m1/m2 = M1/M2.
Второе следствие позволяет вывести уравнение для определения молярной массы неизвестного газа по известной величине относительно плотности этого газа по другому известному газу.
После подстановки в числитель и знаменатель левой части уравнения (1) объемов первого и второго газов, которые равны, получаем:
m1 · V2 /m2 · V1 = M1/M2.
Отношение массы вещества к объему заменяем на плотность (ρ = m/V): ρ1/ ρ2 = M1/M2
и получим уравнение для расчета молекулярной массы первого газа по второму:
M1 = (ρ1/ρ2) M2 = D1/2M2 (2)
Или в общем виде:
где Dг – относительная плотность первого газа по второму.
Если известна плотность данного газа по водороду, то используется уравнение:
Законов в химии большое множество. В этой статье собраны и объяснены наиболее важные, для того, чтобы вы понимали основы химии и могли успешно решать задачи.
Вы увидите множество примеров по ходу данной статьи, обратите внимание на то, что все реакции уравнены. Это необходимое условие для решения задач.
Закон сохранения массы веществ
Гласит о том, что масса веществ, вступающих в реакцию, равна массе веществ, образующихся в результате реакции. Бесспорно, данный закон служит фундаментом решения любой химической задачи.

Массы исходных веществ и продуктов всегда будут одинаковы. Если в результате реакции образуется газ, вы можете найти количества вещества газа и посчитать его массу. Этот закон не имеет исключений.
Объем газа легко перевести в массу, например, найдем массу 32 литров кислорода:
ν (O2) = V(O2) : VM = 32 литра : 22.4 литра/моль = 1.43 моль
m (O2) = ν(O2) × M(O2) = 1.43 моль × 32 грамм/моль = 45.76 грамм
Очевидно, что выделение газа не нарушает закон сохранения масс, напротив - является его подтверждением. Моль в химии - замечательный посредник, который помогает переводить литры в граммы, или наоборот.
Иногда, только вспомнив про закон сохранения масс, вы можете найти массу нужного вещества для решения задачи. Представим такое задание:
Неизвестное вещество массой 124 грамма полностью прореагировало с водой, при этом образовалась соль массой 140 грамм и спирт массой 30 грамм. . здесь много-много текста. Найдите неизвестное вещество.
Это сильно сокращенный пример задания :) Решение это задачи основано на законе сохранения масс. Нам известно все необходимое, чтобы посчитать массу воды.
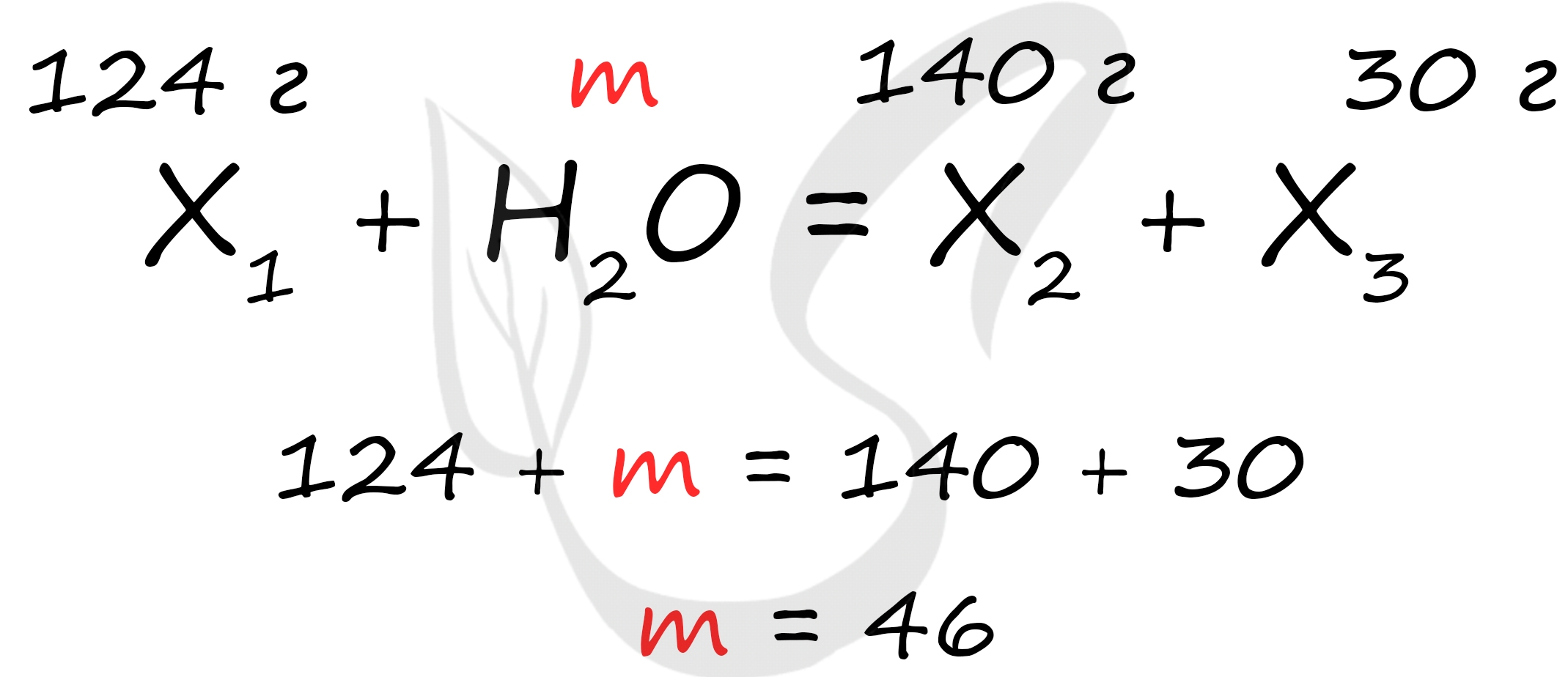
Посчитав массу воды, в дальнейшем мы найдем количество вещества воды и сможем перейти к остальным веществам в задачке (не пытайтесь ее решить до конца, она составлена мной для примера экспромтом :)
Мне доводилось видеть, как в сложных задачках ученики забывали об этом законе, ведь он кажется таким очевидным и простым. Не забывайте про него, будьте уверены - он вам пригодится ;-)
Закон объемных отношений газов
Установлен Ж. Л. Гей-Люссаком в 1808 году. Закон гласит о том, что при постоянном давлении и температуре объемы газов, вступающих в химическую реакцию, находятся в простых отношениях друг к другу и к объемам газообразных продуктов реакции, то есть отношение объемов, в которых газы участвуют в реакции, соответствует отношению небольших целых чисел.
Попытаемся быть чуть проще в трактовке закона, его суть в том, что объемы вступающих в реакцию газов относятся друг к другу как стехиометрические коэффициенты (простые числа).
Наглядно посмотрим на примеры, которые демонстрируют данный закон:

Объемы газов могут быть не равны между собой, как в реакции выше: 3 газа слева и 2 газа справа. Не существует "закона равности объемов газов", существует только закон сохранения массы, который не противоречит разности объемов газов, наоборот только подтверждает ее, так как данный закон выполняется.
Самостоятельно посчитайте, какое количество аммиака может образоваться при участии 15 литров азота в реакции: N2 + 3H2 = 2NH3. Решение найдете ниже.
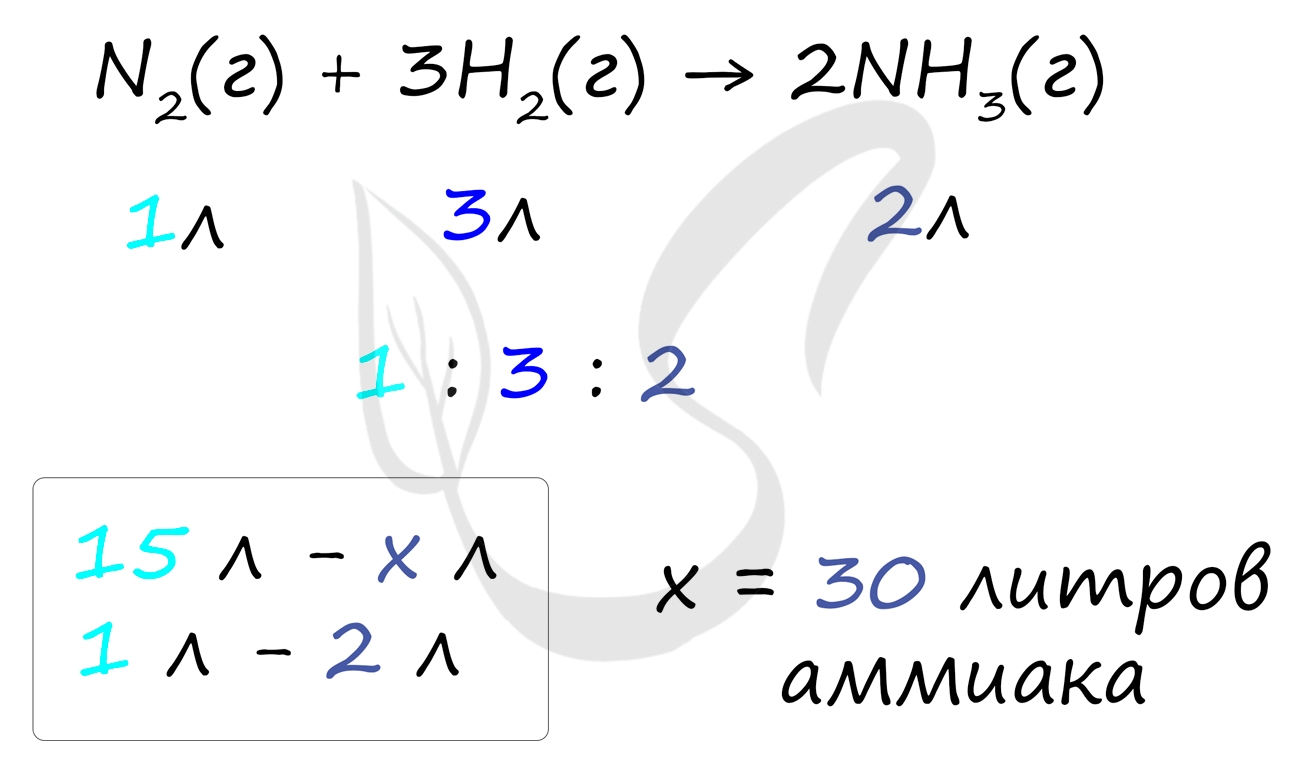
Иногда газов в реакции бывает избыточно, и не все они реагирую полностью. Представим следующую задачу: в синтезе аммиака участвовало 10 литров водорода и 20 литров азота. Найдите объем образующегося аммиака и избыток газа, который не вступит в реакцию.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Основные законы химии
1. В реакции A + B = C + D, известна масса A (22 грамма) и B (42 грамма). Известна масса вещества C (18 грамм). Вычислите, чему равна масса D.
В соответствии с законом сохранения масс, сумма C + D равна сумме A + B = 64 г. Теперь нужно из 64 вычесть массу известного C, после чего получить массу D: 64 - 18 = 46 грамм.
Следствие. Стехиометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объемных отношениях реагируют или получаются газообразные вещества.
V 1 : V 2 : V 3 = ν 1 : ν 2 : ν 3 .
При окислении двух объемов оксида углерода (II) одним объемом кислорода образуется 2 объема углекислого газа, т.е. объем исходной реакционной смеси уменьшается на 1 объем.
Например, при синтезе аммиака из элементов:
Один объем азота реагирует с тремя объемами водорода; образуется при этом 2 объема аммиака - объем исходной газообразной реакционной массы уменьшится в 2 раза.
Решите задачу по образцу:
Вычислите объём кислорода, который потребуется для сжигания 5 м 3 метана СН 4 н.у.?
Закон объёмных отношений впервые сформулировал в 1802 г французский учёный-химик Жозеф Луи Гей-Люссак .
Закон объёмных отношений впервые сформулировал в 1802 г французский учёный-химик Жозеф Луи Гей-Люссак.
Закон объёмных отношений формулируется так:
Объёмы вступающих в реакцию газов относятся друг к другу и к объёмам образующихся продуктов реакции как небольшие целые числа.
При этом подразумевается, что давление и температура неизменны.
Другими словами, стехиометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объёмных отношениях реагируют и получаются газообразные вещества.
При взаимодействии 2 объёмов водорода и 1 объёма кислорода образуются 2 объёма водяного пара.
Один из фундаментальных и общих законов природы — закон сохранения массы — был открыт М.В.Ломоносовым и Л.Лавуазье независимо друг от друга:
Общая масса веществ, вступающих в химическую реакцию, равна общей массе веществ, образующихся в результате реакции.
Из закона сохранения массы веществ следует важный следствие закона сохранения массы: количество атомов каждого элемента до и после реакции остается постоянным.
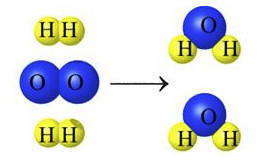
Реакция между Н 2 и О 2 с образованием Н 2 О — подтверждение следствия из закона сохранения массы: количество атомов каждого элемента, которые содержатся в исходных веществах, равно числу атомов этого элемента в продуктах реакции.
Сам Ломоносов считал, что закон сохранения массы веществ является частью более общего закона природы и может быть распространен на другие формы движения материи. Он утверждал, что тело, которое своим толчком возбуждает другое тело к движению, теряет от своего движения столько же, сколько отдает другому. Согласно гипотезе Ломоносова изменения в природе происходят так, что если к чему-то несколько прибавилось, то это отнимется у чего-то другого.
Эта гипотеза была развита только после открытия второй части универсального закона природы — закона сохранения энергии (Майер, 1842 г.):
Энергия не возникает и не исчезает бесследно, а лишь превращается из одной формы в другую в эквивалентных количествах.
Законы сохранения массы и энергии отражают принцип сохранения материи и движения , сущность которого заключается в современном виде формулируется так:
В изолированной системе сумма масс и энергий является постоянной, то есть суммарные массы и энергии веществ, вступающих в реакцию, равны суммарным массам и энергиям продуктов реакции.
Закон сохранения энергии как философский принцип не выводится из более общих постулатов. С физической точки зрения он является следствием однородности времени, то есть тот факт, что законы природы в течение времени не изменяются.
Энергия — это мера движения и взаимодействия различных видов материи. При любых процессах в изолированной системе энергия не возникает и не уничтожается, она может только переходить из одной формы в другую. Например, энергия химического взаимодействия может превращаться в тепловую энергию излучения.
Закон постоянства состава
Сущность закона постоянства состава (Пруст, 1801 г.) заключается в том, что каждое химическое соединение независимо от способа и условий ее добычи имеет определенный массовый состав.
Соотношение между массами элементов, входящих в состав определенной соединения, являются постоянными и не зависят от способа получения этого соединения.
Этот закон не имеет абсолютного обобщенного характера, поскольку в природе существует два типа соединений — с постоянным и с переменным составом.
Соединения, которые имеют постоянный состав и целочисленное атомное соотношение компонентов, называются Дальтониды .
К ним относятся вещества, которые в обычных условиях находятся в газообразном (СО2 , NH3 , NO, HCl) или жидком (Н2О, С6Н6) состоянии или могут быть легко переведены в них, а также кристаллические вещества с молекулярной структурой (I2 , лед).
Соединения переменного состава, в которых стехиометрические соотношения компонентов не соответствуют целым числам, называются бертоллидами .
Бертоллиды не имеют молекулярной структуры. К ним относится подавляющее большинство кристаллических соединений переходных d- и f- элементов: оксиды, гидриды, нитриды, сульфиды, карбиды и другие бинарные соединения. Следует заметить, что на постоянство состава влияет и изотопный состав, например, в обычной воде Н2О и в тяжелой воде D2О массовые доли кислорода различаются.
Итак, состав химических соединений зависит от типа химической связи, агрегатного состояния веществ, изотопного состава и условий их добычи и может быть как постоянным, так и переменным. Поэтому в настоящее формулировки закона постоянства состава внесены некоторые уточнения:
Если химическое соединение имеет молекулярную структуру, то независимо от условий добычи состав ее остается постоянным. Состав химического соединения, не имеющего молекулярной структуры, может изменяться в определенных пределах в зависимости от условий добычи.
Закон объемных соотношений Гей-Люссака
В химических реакциях с участием газов очень часто наблюдается изменение объема реакционной системы. В отличие от постоянства массы веществ, участвующих в реакции и образуются вследствие нее, при взаимодействии газов объем реакционной системы может увеличиваться, уменьшаться или оставаться неизменным. Соотношение между объемами газов устанавливает закон объемных соотношений Гей-Люссака (1808 г.):
Соотношение объемов газов, вступающих в реакцию и образующихся в результате нее, представляет собой соотношение простых чисел, которые являются кратными стехиометрических коэффициентов, стоящих в уравнении реакции перед формулами соответствующих газов.
Этот закон справедлив только в том случае, когда объемы газов измерены при одинаковых условиях.
Из закона Гей-Люссака следует, что стехиометрические коэффициенты в уравнении реакции являются кратными к объемам газов, которые взаимодействуют и образуются.
С помощью закона объемных соотношений можно рассчитать объемы газов или устанавливать состав исходного газа.
Закон Авогадро
Одним из важнейших газовых законов является закон Авогадро:
В равных объемах различных газов при одинаковых условиях содержится одинаковое количество молекул:
N=const, если P,V,T=const, где NN — количество молекул; P, V, T — давление, объем, температура соответственно.
Но поскольку число молекул в реальных образцах вещества очень велико, то была введена универсальная количественная характеристика, которая описывает численный состояние веществ:
Количество вещества ν (или n ) — это физическая величина, определяемая числом частиц — структурных элементов вещества: молекул, атомов, ионов, ионных ассоциатов и тому подобное.
Единицей ее измерения является [ моль ] — одна из основных единиц системы СИ.
Моль — это количество вещества, содержащее столько же структурных элементов вещества, сколько атомов содержится в изотопе углерода-12 массой 12 · 10 -3 кг.
Установлено, что масса одного атома изотопа углерода-12 составляет 19,92 · 10 -27 кг. Тогда число атомов N в 12 · 10 -3 кг равна:
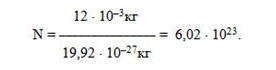
Число, равное 6,02 · 10 23 моль -1 , называется постоянной Авогадро.
Постоянная Авогадро обозначается NA и указывает на число частиц — структурных элементов веществе, количество которой составляет 1 моль и поэтому имеет размерность моль -1 .
Итак, моль любых структурных элементов — это такое количество вещества, которое содержит 6,02 · 10 23 частиц. Например, 1 моль Н2О состоит из 6,02 · 10 23 молекул Н2О и содержит 2 моль (или 2 · 6,02 · 10 23 ) атомов Н и 1 моль (или 6,02 · 10 23 ) атомов В ; 1 моль SO4 2- содержит 6,02 · 10 23 ионов SO4 2- , в том числе 1 моль (6,02 · 10 23 ) атомов S и 4 моль (4 * 6,02 · 10 23 ) атомов О .
Количество вещества связано с числом частиц N и постоянной Авогадро NA зависимостью ν=N/NA.
Масса одного моля вещества называется молярной массой этого вещества, она обозначается через М .
Молярная масса — это физическая величина, определяемая отношением массы вещества к количеству вещества, которое ей отвечает: M=m/ν.
Единицей измерения молярной массы в системе СИ является [кг / моль], но в химии чаще пользуются внесистемной величиной [г / моль], или [г × моль -1 ].
Молярная масса М связана с относительной молекулярной массой Mr и постоянной Авогадро NA зависимостью M=Mr⋅NA⋅1а.в.м.
Например, относительная молекулярная масса оксида углерода равна Mr(CO2)=12+2⋅16=44, а атомная единица массы составляет 1 а.о.м. = 1,66 × 10 -24 г, тогда молярная масса будет М (СО2 ) = 44 × 6,02 · 10 23 · 1,66 · 10 -24 = 44г / моль.
То есть молярная масса численно равна относительной молекулярной массе, но имеет совсем другой физический смысл: Мr характеризует массу одной молекулы, а М — массу одного моля, то есть 6,02 · 10 23 молекул .
Закону Авогадро подлежат все газы независимо от размеров их молекул. Не подлежат ему газы в условиях низких температур и высокого давления, а также вещества в жидком или твердом состоянии. Это объясняется так. Как известно, объем, занимает определенное количество вещества, определяется тремя параметрами: числом составляющих частиц, расстояниями между ними и их размерами. В газах в условиях высоких температур и низкого давления расстояния между молекулами в тысячи раз больше их размеры, поэтому размерами молекул можно пренебречь. В результате объем газа будет оговариваться уже только двумя параметрами: числом молекул и расстояниями между ними. Но при одинаковых условиях (давление и температура) расстояния между молекулами в различных газах одинаковы, поэтому в этом случае равные объемы различных газов содержат одно и то же число молекул.
При низких температурах и под высоким давлением расстояния между молекулами в газах уменьшаются и становятся соизмеримыми с размерами самих молекул, поэтому объем газа зависит от размеров молекул, а газы перестают подлежать закону Авогадро.
Очень часто бывает необходимым знать молярную массу воздуха, которая исчисляется как и молярная масса любой смеси газов с учетом объемной доли φφ каждого газа.
Объемные доли кислорода и азота в воздухе примерно составляют φ(O2)≈0,2 (или 20%), φ(N2)≈0,8 (или 80%). Тогда молярная масса воздуха:
М воздуха =φ(O2)× М (О 2 ) + φ(N2) × М (N2 ) = 0,2 × 32 + 0,8 × 28 = 29г / моль.
1-е следствие закона Авогадро
Один моль любого газа при нормальных условиях (н.у.) занимает объем примерно 22,4 л (0,0224 м 3 ).
Эта величина называется молярным объемом , обозначается V M и измеряется в [л / моль] или [м 3 / моль].
Нормальными условиями считаются: Р = 101325Па (~ 10 5 Па) = 1 атм = 760мм рт.ст., Т = 273,15К или t = 0 0 С.
Молярный объем — это эмпирически установленная величина на основе соотношений:
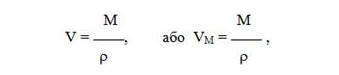
где ρρ — плотность газа, [г / л], или [кг / м 3 ].

Молярный oбьем газов: при н.у. V M = 22,4л / моль
Молярный объем в отличие от молярной массы не является постоянной величиной, а зависит от условий (Р, Т), поэтому VM как понятие употребляют обычно для газов при н.у. Молярный объем связан с другими величинами (объемом V , количеством вещества ν , молярной массой М , плотностью ρ, Числом Авогадро NA и количеством частиц N ) соотношениями:
2-е следствие закона Авогадро
Отношение плотности одного газа в плотности другого газа при одинаковых условиях равна отношению их молярных масс М или относительных молекулярных масс Мr .
Эта величина называется плотностью одного газа по другому и обозначается буквой d или D:
ρ1= ρ2⋅ d2ρ1=ρ2⋅d2 (газа 1), ρ2= ρ1/ d2ρ2=ρ1/d2 (газа 1)
М (газа 1) = d 2 (1) × M (газа 2) M (газа 2) = M (газа 1) / d 2 (газа 1).
Относительная плотность d — это величина безразмерная, она показывает, насколько один газ тяжелее другого.
Основные газовые законы
Состояние газа характеризуется его объемом, давлением и температурой. Между этими величинами экспериментально были установлены следующие законы:
- Закон Бойля-Мариотта (изотермический) сокращенно записывается так:
- при Т = const
- Р 1 · V 1 = Р 2 · V 2 , или Р · V = const;
- Закон Гей-Люссака (Изобарный)
- при Р = const
- V 1 / T 1 = V 2 / T 2 , или V / T = const.
- Закон Шарля (Изохорный)
- при V = const
- Р 1 / T 1 = Р 2 / T 2 , или Р / T = const.
Все три закона можно объединить в один универсальный газовый закон , который описывается уравнением Клапейрона:
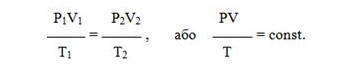
Зависимость для одного моля газа была выведена Менделеевым, поэтому называется уравнением Менделеева-Клапейрона. Оно содержит постоянную величину -универсальную газовую постоянную R.
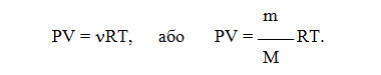
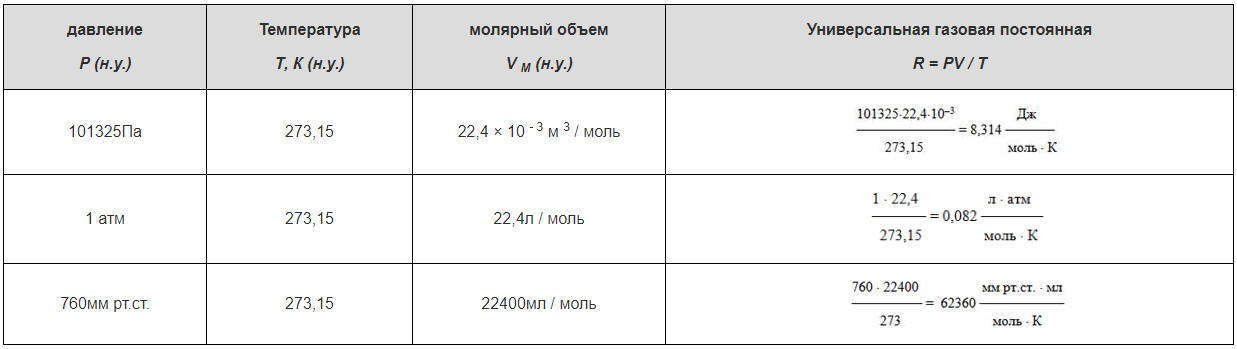
Расчеты значений универсальной газовой постоянной R
Закон эквивалентов
Из закона постоянства состава следует, что элементы сочетаются друг с другом в определенных количественных соотношениях, для характеристики которых было введено понятие эквивалента и эквивалентной массы (слово эквивалентный в переводе означает равноценный ).
Эквивалентом называется условная или реальная частица вещества, которая может присоединять, замещать, отдавать или взаимодействовать иным образом с одним ионом водорода Н + или гидроксила ОН — в кислотно-основных (или ионообменных) реакциях или одному электрону в окислительно-восстановительных реакциях.
Например, эквивалентом азотной (азотной) кислоты реальная частица — молекула HNO3 , содержащей один ион Н + ; эквивалентом ортофосфатной (фосфорной) кислоты — условная частица, соответствует 1/3 молекуле Н3РО4 , в состав которой входят три иона Н + .
Но эквиваленты одного элемента могут быть разными — в зависимости от валентности элемента. Так же сложное соединение может иметь разные эквиваленты, что обусловлено характером ее химического взаимодействия. Например, в реакции нейтрализации ортофосфорная кислота калий гидроксидом
только два атома Н кислоты замещаются атомами К (то есть кислота показывает основность 2). Тогда согласно определению, эквивалентом H3PO4 будет условная частица, которая составляет 1 / 2H3PO4 , поскольку на один атом Н приходится именно половина молекулы H3PO4.
Итак, эквивалент — это фактически один вид молекулы, которая соответствует одному атому Н или иона Н + .
Число, показывающее, какая часть молекулы или иной частицы вещества соответствует эквиваленту, называется фактором эквивалентности fЕ .
Эквивалент и фактор эквивалентности: а) fЕ (HCl) = 1; б) fЕ (CaCl2 ) = 1/2; в) fЕ (AlCl3 ) = 1/3; г) fЕ (CCl4 ) = 1/4; д) fЕ (PCl5 ) = 1/5; е) fЕ (SCl6 ) = 1/6. (Эквиваленты соединений окрашенные темным оттенком):
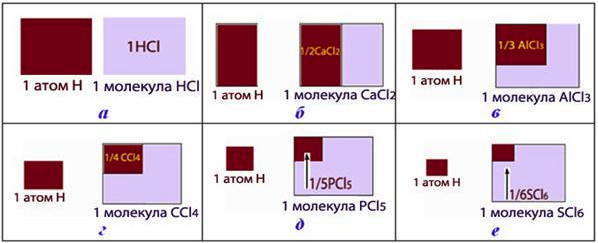
Поскольку эквиваленты элемента и эквиваленты сложного соединения могут быть разными, то как следствие, и фактор эквивалентности тоже будет иметь разные значения, для вычисления которого существуют простые формулы:
Читайте также:

