Правила заполнения орбиталей электронами кратко
Обновлено: 05.07.2024
Наборы значений квантовых чисел для различных атомных орбиталей:
Квантовое число
Атомные орбитали
Количество
Обозначение
При заполнении электронами атомных орбиталей соблюдаются следующие три правила:
1. Принцип устойчивости (принцип минимальной энергии). Орбитали заполняются начиная с имеющих самую низкую энергию и далее в порядке её повышения. В этом случае энергия атома является минимальной, а устойчивость – максимальной.
энергетическая последовательность легко может быть описана при помощи правила суммы двух первых квантовых чисел n+l. Это правило носит название правила Клечковского (1951 г.):
При заполнении орбитальных оболочек атома более предпочтительны (более энергетически выгодны), и, значит, заполняются раньше те состояния, для которых сумма главного квантового числа n и побочного (орбитального) квантового числа l, т.е. n+l, имеет меньшее значение.
Например, орбиталь 4s, для которой n+l = 4+0 = 4, заполняется раньше, чем орбиталь 3d, где сумма n+l = 3+2 = 5.
При равенстве сумм ниже по энергии находится орбиталь с меньшим значением главного кантового числа. Так, орбиталь 3d имеет более низкую энергию, чем 4р.
Большинство из нас думает, что знает об атомах достаточно много. Мы знаем какие они маленькие и даже можем дать определение атому. Но как же человечество пришло к пониманию, что такое атом и каковы основы строения атомов?
Модель атома Томпсона (пудинг с изюмом)
Эти лучи он назвал катодными лучами, позднее их стали называть электронными лучами. С помощью магнита, Томпсон определил, что эти лучи содержат частицы с отрицательным зарядом. После большой серии опытов ему удалось установить, что отрицательные частицы (электроны) очень малы, по сравнению с тем, что дает положительный заряд атому.


Модель атома Томпсона
Модель атома Резерфорда (ядерная модель)

Опыт резерфорда
Но вот произошло то, что он никак не ожидал увидеть: хотя большинство частиц летели прямо, некоторые отклонялись на большой угол, а некоторые летели назад в сторону источника. Этот эксперимент позволил предположить, что весь положительный заряд находится в ядре атома, а отрицательно заряженные электроны плавают вокруг него. Согласно ядерной модели строения атома по Резерфорду, большую часть атома занимает пустое пространство.
Модель атома Резерфорда
Модель атома Бора (планетарная модель)
Пока другие ученые ставили эксперименты с катодными лучами, Нильс Бор был озадачен теми линиями, которые давал водород при добавлении ему энергии. И вот возникла планетарная модель атома, в которой Бор предположил, что электроны движутся вокруг ядра по круговым орбитам, подобно планетам, вращающихся вокруг Солнца.
Также он полагал, что чем дальше электрон находится от ядра, тем большей энергией он обладает. При получении атомом дополнительной энергии, электроны с ближних орбит могут перескакивать на более отдаленные. Начальная орбиталь называется основной, а конечная – возбужденной. Энергия, полученная атомом должна куда-то уйти, и она высвобождается в виде квантов электромагнитного излучения. Т.к. существует несколько возбужденных состояний, то испускаются кванты различных энергий. Этим он объяснил полученный спектр водорода.

Опыт Нильса Бора
Современная модель атома (квантовая модель)
Во что мы верим сейчас? Из предыдущего раздела Основные понятия и законы химии, мы знаем, что Атом состоит из ядра и электронов. Атомное ядро имеет положительный заряд и состоит из протонов (Z) и нейтронов (N), а сумма масс протонов (Z) и нейтронов (N) атомного ядра называется массовым числом A = Z + N. Электроны атома расположены вокруг ядра на своих орбиталях.
Основные принципы заполнения электронной оболочки атомов представлены тремя принципами:
1. Принцип минимальной энергии требует, чтобы электроны заселяли АО в порядке увеличения энергии электронов на этих орбиталях (в основном состоянии каждый электрон располагается так, чтобы энергия системы была минимальной). Это отражает общее правило– максимуму устойчивости системы соответствует минимум ее энергии. Энергия атомных орбиталей возрастает по мере увеличения суммы n + l (первое правило Клечковского); при одинаковой сумме сначала заполняется уровень с меньшим n и большим l (второе правило Клечковского) Энергия атомных орбиталей возрастает согласно ряду Клечковского:
Основные принципы заполнения электронной оболочки атомов представлены тремя принципами:
1. Принцип минимальной энергии требует, чтобы электроны заселяли АО в порядке увеличения энергии электронов на этих орбиталях (в основном состоянии каждый электрон располагается так, чтобы энергия системы была минимальной). Это отражает общее правило– максимуму устойчивости системы соответствует минимум ее энергии. Энергия атомных орбиталей возрастает по мере увеличения суммы n + l (первое правило Клечковского); при одинаковой сумме сначала заполняется уровень с меньшим n и большим l (второе правило Клечковского) Энергия атомных орбиталей возрастает согласно ряду Клечковского:
3. Правило Хунда: наименьшей энергией обладает электронная конфигурация с максимальным спином (то есть при заселении орбиталей с одинаковой энергией (например, трех p-орбиталей px, py и pz) электроны в первую очередь располагаются поодиночке на каждой орбитали и лишь потом начинается заполнение вторыми электронами.). Это означает, что если на p-орбитали три электрона, то они располагаются так: , и суммарный спин = 3/2, а не так: , = 1/2. Объясняется данный факт тем, что в соседних ячейках электроны меньше отталкиваются друг от друга, как одноименно заряженные частицы.

Современные представления о строении атома
Элемент ЕГЭ: 1.1 Современные представления о строении атома. 1.1.1 Строение электронных оболочек атомов элементов первых четырех периодов: s-, р- и d-элементы. Электронная конфигурация атома. Основное и возбуждённое состояние атомов.
Современные представления о строении атома

Атом – химически неделимая электронейтральная частица, которая состоит из положительно заряженного ядра и движущихся вокруг него отрицательно заряженных электронов.
Атомы не имеют заряда (нейтральны). Если атом присоединяет один или несколько электронов, он приобретает отрицательный заряд и превращается в анион. Если атом теряет один или несколько электронов, он приобретает положительный заряд и превращается в катион. Заряд иона указывают арабской цифрой и знаком после символа атома.
Состав ядра: А = Z + N, где А — массовое число; Z — протонное число (число протонов); N — число нейтронов.
Элементарные частицы
Порядковый номер элемента в периодической системе:
- Заряд ядра атома
- Число протонов в ядре атома
- Число электронов в атоме

Нуклиды – разновидности атомов с фиксированным массовым числом А, числом протонов Z и нейтронов N в ядре.

Основные положения квантовой теории строения атома:
- Дискретность энергии электрона
- Двойственная (корпускулярно-волновая) природа электрона
- Невозможность определения траектории электрона (принцип неопределенности)
Относительная атомная масса элемента (Ar)
Физическая величина, показывающая, во сколько раз средняя масса атомов данного элемента больше 1/12 части массы изотопа углерода 12 С.

Атомные орбитали
Орбиталь — пространство вокруг ядра, в котором нахождение электрона наиболее вероятно (вероятность более 90%)

Порядок заполнения орбиталей в основном состоянии
1) Принцип наименьшей энергии. Электроны занимают в первую очередь орбитали, имеющие наименьшую энергию.


2) Принцип Паули. На каждой орбитали могут находиться не более двух электронов, причём спины их противоположны.
Спин электрона — свойство электрона, характеризующее его способность взаимодействовать с магнитным полем. Может принимать два значения (положительное и отрицательное).

Последовательность заполнения орбиталей электронами в основном состоянии:
Энергетические уровни и подуровни

Элементы, у которых идет заполнение s-подуровня, называют s-элементами.
Элементы, у которых заполняется р-подуровень, называют р-элементами.
Элементы, у которых заполняется d-подуровень, называют d-элементами.
Элементы, у которых заполняется f-подуровень, называют f-элементами.
Распределение электронов в атоме по энергетическим уровням (электронным слоям) и подуровням
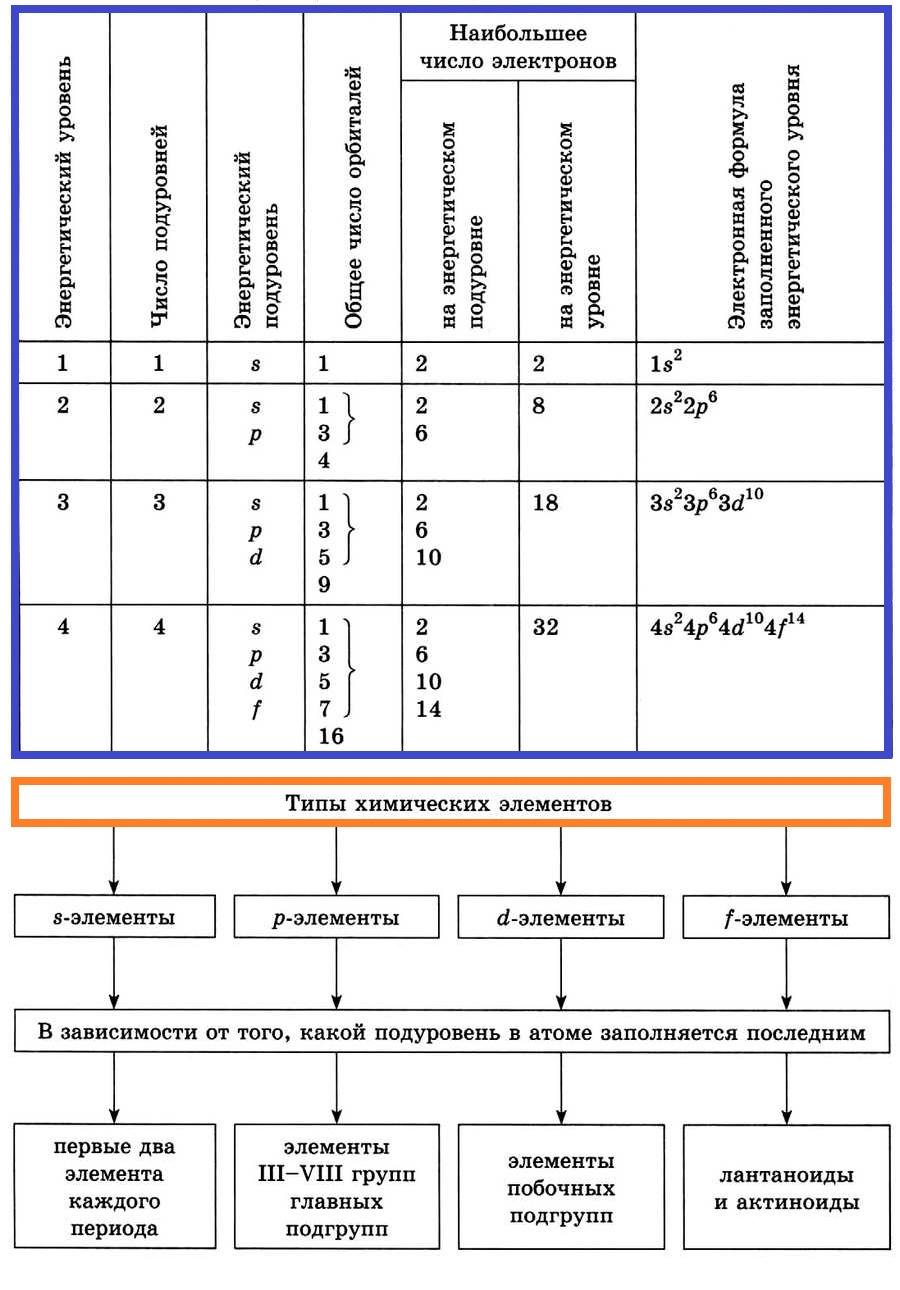
Электроны, относящиеся к последнему энергетическому уровню, называют внешними (валентными) электронами.
Строение электронных оболочек атомов первых четырёх периодов
Распределение электронов по орбиталям атома называют электронной конфигурацией атома, или электронной формулой.
Строение элементов первого периода

Строение элементов второго периода

Строение элементов третьего периода

Строение элементов четвёртого периода

Основное и возбуждённое состояние атомов
Наиболее устойчивое состояние атома, в котором энергия его электронной оболочки минимальна, называется основным состоянием атома. Любые другие состояния атома называют возбужденными состояниями.

Для возможности перехода атома в возбуждённое состояние необходимо выполнение одновременно двух условий:
- наличие спаренных электронов;
- наличие вакантных орбиталей.

Читайте также:

