Опыт лавуазье по определению состава воздуха кратко
Обновлено: 03.07.2024
3. Как опытным путем А. Лавуазье доказал состав воздуха?
Вопрос 3.
Лавуазье нагревал металлическую ртуть в ре-
торте на жаровне в течение 12 суток. Конец
реторты был подведен под колокол, поставлен-
ный в сосуд с ртутью. В результате уровень
ртути в колоколе поднялся примерно на 1/5.
На поверхности ртути в реторте образовалось
вещество оранжевого цвета — оксид ртути.
Оставшийся под колоколом газ был неприго-
ден для дыхания. Этим опытом было доказано,
что в воздухе содержится примерно 4/5 азота
и 1/5 кислорода (по объему).
Лавуазье нагрел ртуть в определенном объеме воздуха, объем воздуха сократился и ртуть покрылась налетом оранжевого цвета. оставшийся газ не поддерживал ни горения ни дыхания. тогда Лавуазье собрал с поверхности ртути оранжевые чешуйки поместил их в пробирку сильно нагрел и собрал выделившийся при этом газ. смешав получившийся газ с остатками от первого опыта он получил смесь газов ничем не отличавшихся от воздуха.
С помощью точного взвешивания Лавуазье показал, что масса оксида ртути равна массе металла и соединившегося с ним кислорода, и наоборот – образовавшийся оксид ртути разлагается с выделением тех же самых количеств ртути и кислорода. Лавуазье не ограничился взвешиванием сосудов, а проанализировал изменения происходящие с воздухом, находящимся в контакте с металлом. Было известно, что при этом из воздуха исчезает 1/5 часть, но никто не знал, что собой представляет эта израсходованная часть воздуха и чем она отличается от оставшейся. Как показали эксперименты, остаток воздуха не поддерживает горения и дыхания лабораторных животных.
Он объяснил какие изменения происходят с воздухом и при горении в нем свечи, и при дыхании мыши в замкнутом пространстве. Лавуазье показал, что дыхание – это по сути медленное горение, дающее животному энергию. При этом поглощается кислород и выделяется углекислый газ. Он также установил состав углекислого газа. Для этого в одном из опытов он сжег алмаз. Эти опыты были исключительно важны для развития не только химии, но и физиологии.
Изначально в колбе (ну или где там еще) :
N2 + O2 + 2Hg
После реакции (индикатор - оранжевый налет) :
N2 + 2HgO
Инертный газ - азот, не поддерживает горения и дыхания (хотя там кроме азота еще аргон и др. )
Потом собранный оксид ртути разлагается:
2HgO = 2Hg + O2
Получили обратно кислород. Если проводить опыты количественно, то по закону сохранения массы смесь полученных газов равна смеси исходных.
Химия дает два пути для определения природы составных частей какого-нибудь тела: синтез и разложение. Когда, например, смешивают воду и винный спирт, или алкоголь, и в результате этого получают известную жидкость, которую в продаже называют водкой, то имеют право заключить, что водка представляет собой соединение спирта и воды; но к тому же самому заключению можно прийти и путем разложения. Вообще в химии нельзя считать себя вполне удовлетворенным, пока не объединены эти два рода доказательств.
А.Л.Лавуазье рассказывает
о своих опытах ученым-друзьям
А.Л.Лавуазье проводит опыт
с ретортой
В течение всего первого дня не произошло ничего примечательного: ртуть, хотя и не кипевшая, находилась в состоянии непрерывного испарения и покрывала внутренние стенки реторты капельками, сначала очень мелкими, но постепенно увеличивающимися и, при достижении известного объема, падавшими от собственной тяжести на дно реторты и соединявшимися с остальной ртутью. На второй день я начал замечать плавающие на поверхности ртути небольшие красные частички, которые в течение четырех или пяти дней увеличивались в количестве и объеме, после чего и перестали увеличиваться и оставались в неизменном виде. По прошествии 12 дней, видя, что окаливание ртути нисколько больше не прогрессирует, я потушил огонь и дал остыть прибору. Объем воздуха, содержавшегося как в реторте, так и в ее шейке и в свободной части колокола, приведенный к 28 дюймам 3 давления и 10 градусам температуры, был до опыта равен приблизительно 50 куб. дюймам. По окончании операции тот же объем, при том же давлении и той же температуре оказался равным всего лишь 42–43 дюймам; следовательно, произошло уменьшение приблизительно на одну шестую. С другой стороны, тщательно собрав образовавшиеся на поверхности красные частицы и отделив их, насколько было возможно, от жидкой ртути, в которой они плавали, я нашел их вес равным 45 гранам 4 .
Мне пришлось повторить несколько раз это прокаливание ртути в замкнутых сосудах, потому что очень трудно в одном и том же опыте собрать и сохранить и воздух, в котором производился опыт, и красные частицы образовавшейся ртутной окалины.
Мне придется часто соединять таким образом в одном описании результаты двух или трех однородных опытов.
Воздух, оставшийся после этой операции и уменьшавшийся вследствие прокаливания в нем ртути до пяти шестых своего объема, не был годен больше ни для дыхания, ни для горения; животные, вводимые в него, умирали в короткое время, горящие же предметы потухали в одно мгновение, как если бы их погружали в воду. С другой стороны, я взял 45 гранов образовавшегося во время опыта красного вещества и поместил их в маленькую стеклянную реторту, к которой был присоединен прибор, приспособленный для приема жидких и воздухообразных продуктов, которые могут выделиться. Когда я зажег огонь в печке, заметил, что по мере того, как красное вещество нагревалось, его цвет становился все более интенсивным. Когда затем реторта начала накаляться, красное вещество начало мало-помалу уменьшаться в объеме и через несколько минут оно совершенно исчезло, в то же время в небольшом приемнике собралось 41,5 грана жидкой ртути, а под колокол прошло 7–8 куб. дюймов упругой жидкости (так Лавуазье называет газ. – П.К.), гораздо более способной поддерживать горение и дыхание животных, чем атмосферный воздух.
Когда, переведя некоторое количество этого воздуха в стеклянный цилиндр диаметром в один дюйм, я опустил туда свечу, она загорелась ослепительным светом; уголь, вместо того чтобы спокойно тлеть, как в обыкновенном воздухе, горел сильным пламенем и с некоторым треском, подобно фосфору, притом с такой яркостью, которую глаза с трудом переносили. Этот воздух, который был открыт почти в одно время Пристли, Шееле и мною, был назван первым дефлогистированным воздухом, вторым — огненным воздухом. Я ему дал сначала название в высшей степени легко вдыхаемого или весьма удобовдыхаемого воздуха; впоследствии это название было заменено названием жизненный, или живительный, воздух. Мы увидим сейчас, что надо понимать под этими названиями.
Исследование состава воздуха
при помощи свечи в цилиндре
1 1 куб. дюйм = 16,4 куб. см, 1 линия = 2,5 мм.
2 1 унция = 28,35 г.
3 1 дюйм = 249 Па.
4 1 гран = 0,065 г.

Наука сегодня превратилась в настоящую индустрию. Исследования стоят миллионы долларов, в экспериментах участвуют сотни ученых.
Однако совсем недавно самые потрясающие научные открытия делались учеными в одиночку, а великие эксперименты, вошедшие в историю науки, ставились на лабораторном столе. …
Глава 4. Антуан Лоран Лавуазье
Флогистон и кислород
Только представьте, что это значит — понять, что дает листу его
цвет и что заставляет пламя гореть!
Карл Джерасси, Роальд Хоффман. Кислород 1

Весьма далеко от современной науки. В алхимии, даже в записях самого Ньютона, многое напоминает магию. В одном из своих дневников он добросовестно переписал несколько абзацев из книги алхимика Джорджа Старки, который сам себя называл Филалетом.
Считалось, что предметы горят потому, что в них много флогистона. По мере того как предметы поглощаются огнем, они выделяют эту горючую субстанцию в воздух. Если поджечь кусочек дерева, то он перестанет гореть, оставив после себя всего лишь кучку пепла, только когда израсходует весь свой флогистон. Поэтому считалось, что дерево состоит из пепла и флогистона. Аналогичным образом после прокаливания, т.е. сильного нагрева, металла остается белая хрупкая субстанция, известная как окалина. Стало быть, металл состоит из флогистона и окалины. Процесс ржавления — это медленное горение, наподобие дыхания, т.е. реакции, возникающие тогда, когда флогистон выделяется в воздух.
С помощью флогистона ученые могли логично объяснить горение, прокаливание, восстановление и даже дыхание. Химия неожиданно становилась осмысленной.
Лавуазье, как и ученые того времни, был уверен в том, что флогистон — одна из основных составляющих вещества. Но к началу экспериментов с алмазами он стал задумываться: а может ли нечто весить меньше нуля?

Два года спустя, в 1771 году, Лавуазье исполнилось двадцать восемь лет. В том же году он женился. Его избранницей стала Мария-Анна Пьеретт Пользе, тринадцатилетняя дочь еще одного откупщика. (Эта достаточно миловидная девушка к тому времени была помолвлена, и ее второму потенциальному жениху было пятьдесят.) Марии-Анне так понравились научные занятия мужа, что она быстро освоила химию и помогала чем могла: делала записи, переводила английскую научную литературу на французский и выполняла сложнейшие чертежи эксперимента, который оказался настолько элегантен, что ему, как философскому камню, суждено было преобразовать алхимию в химию.

С трудом сдерживая скептицизм, Лавуазье повторил некоторые эксперименты своих коллег. Он подтвердил, что сжигание фосфора с целью получения фосфорной кислоты или сжигание серы с целью получения серной кислоты приводит к получению веществ, вес которых превышает вес использованных веществ, т.е. как и при прокаливании металлов. Но почему происходит указанное изменение? Ему показалось, что он нашел ответ на этот вопрос. Используя увеличительное стекло для нагрева олова, заключенного в герметичный стеклянный сосуд, он обнаружил, что и до опыта, и после вся установка весила одинаково. Медленно открывая сосуд, он слышал, как с шумом воздух врывался внутрь, после чего вес вновь увеличивался. Может быть, предметы горят не потому, что испускают флогистон, а потому, что поглощают какую-то часть воздуха?
Сжигание оксида свинца в стеклянном сосуде с помощью увеличительного стекла
Рисунок Марии-Анны Лавуазье

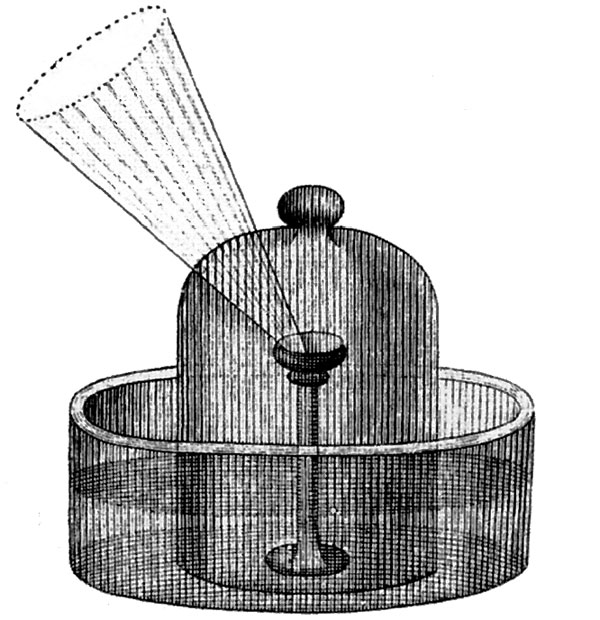
Прояснить все можно было только одним способом. Лавуазье взял с полки сосуд, который назывался плоской колбой. Нижняя часть его была круглой, а высокое горлышко Лавуазье нагрел и изогнул так, что оно сначала выгибалось книзу, а затем снова вверх.
Если в его эксперименте 1769 года сосуд напоминал пеликана, то нынешний был похож на фламинго. Лавуазье налил четыре унции чистой ртути в круглую нижнюю камеру сосуда (обозначена буквой А на рисунке). Сосуд был установлен на печи так, чтобы его горлышко оказалось в открытый емкости, также заполненной ртутью, а затем поднималось в стеклянный колокол. Эта часть установки использовалась для определения количества воздуха, который будет потреблен во время эксперимента. Отметив бумажной полоской уровень (LL), он разжег печь и довел ртуть в камере А почти до кипения.
Можно считать, что в первый день не произошло ничего особенного. Небольшое количество ртути испарилось и осело на стенках плоской колбы. Образовавшиеся шарики были достаточно тяжелы для того, чтобы вновь стечь вниз. Но на второй день на поверхности ртути стали образовываться красные точки — окалина. В течение нескольких последующих дней красная корочка увеличивалась в размерах, пока не достигла максимальных. На двенадцатый день Лавуазье остановил эксперимент и сделал некоторые измерения.
Год за годом коллеги Лавуазье, особенно Пристли, ворчали по поводу того, что тот якобы присвоил себе первенство в экспериментах, которые они тоже осуществили.Пристли однажды отобедал в доме супругов Лавуазье и рассказал им о своем лишенном флогистона воздухе, а шведский аптекарь Шееле отправил Лавуазье письмо с рассказом о своих опытах. Но при всем при этом они продолжали думать, что кислород — это воздух, лишенный флогистона.
Он заглянул намного глубже и сформулировал закон сохранения массы. В результате химической реакции вещество — в данном случае горящая ртуть и воздух — меняет форму. Но масса при этом не создается и не исчезает. Сколько веществ вступает в реакцию, столько же должно получиться на выходе. Как сказал бы сборщик налогов, баланс должен в любом случае сходиться.
Читайте также:
- Система высшего юридического образования в россии на современном этапе кратко
- Сделайте вывод о значении образования единого русского государства кратко
- Каковы взгляды и главные достижения линкольна в политике кратко
- Проблемы профессионального образования и переподготовки кадров кратко
- Исследование и описание экосистемы своей школьной территории лабораторная работа

