Минеральные вещества и их роль в клетке 10 класс кратко
Обновлено: 02.07.2024
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам
Описание презентации по отдельным слайдам:
К макроэлементам относят натрий, калий, кальций, магний, хлор, кремний, серу, железо и др.
К микроэлементам относятся вещества, содержание которых в продуктах ничтожно мало — это йод, цинк, медь, фтор, бром, марганец и др. Несмотря на малое содержание, микроэлементы исключительно важны для питания человека.
Наряду с органическими веществами — белками, углеводами, жирами — в клетках живых организмов содержатся соединения, составляющие обширную группу минеральных веществ. К ним относятся вода и различные соли, которые, находясь в растворенном состоянии, диссоциируют (распадаются) с образованием ионов: катионов (положительно заряженных) и анионов (отрицательно заряженных).
Минеральные вещества входят в состав всех клеток, тканей, костей; они поддерживают кислотно-щелочное равновесие в организме и оказывают большое влияние на обмен веществ.
Минеральные вещества в зависимости от их содержания в продуктах или организме человека условно подразделяют на макроэлементы и микроэлементы.
Многие минеральные вещества являются незаменимыми структурными элементами организма – кальция и фосфор слагают основную массу минерального вещества костей и зубов, натрий и хлор являются основными ионами плазмы, а калий, в больших количествах содержится внутри живых клеток.
Поддержание постоянства внутренней среды (гомеостаза) организма и осмотического давления на мембранах клетки, предусматривает в первую очередь поддержание качественного и количественного содержания минеральных веществ в тканях органах на физиологическом уровне. Даже небольшие отклонения от нормы могут повлечь самые тяжелые последствия для здоровья организма или отдельно взятой клетки
Вся совокупность макро и микроэлементов обеспечивает процессы роста и развития организма. Минеральные вещества играют важную роль в регуляции иммунных процессов, поддерживают целостность клеточных мембран, обеспечивают дыхание тканей.
Неорганические ионы: катионы и анионы
Катионы – калий, натрий, магний и кальций.
Анионы – хлорид анион, гидрокарбонат анион, гидрофосфат анион, дигидрофосфат анион, карбонат анион, фосфат анион и нитрат анион.
Рассмотрим значение ионов.
Ионы, располагаясь по разные стороны клеточных мембран, образуют так называемый трансмембранный потенциал. Многие ионы неравномерно распределены между клеткой и окружающей средой. Так, концентрация ионов калия (К+) в клетке в 20–30 раз выше, чем в окружающей среде; а концентрация ионов натрия (Na+) в десять раз ниже в клетке, чем в окружающей среде.
Благодаря существованию градиентов концентрации, осуществляются многие жизненно важные процессы, такие как сокращение мышечных волокон, возбуждение нервных клеток, перенос веществ через мембрану.
Катионы влияют на вязкость и текучесть цитоплазмы. Ионы калия уменьшают вязкость и увеличивают текучесть, ионы кальция (Са2+) обладают противоположным действием на цитоплазму клетки.
Анионы слабых кислот – гидрокарбонат анион (НСО3-), гидрофосфат анион (НРО42-) – участвуют в поддержании кислотно-щелочного баланса клетки, то есть pH среды. По своей реакции растворы могут быть кислыми, нейтральными и основными.
рН среды и роль ионов в его поддержании
Значение pH в клетке примерно равняется 7.
Изменение pH в ту или иную сторону губительно действует на клетку, поскольку сразу же изменяются биохимические процессы, проходящие в клетке.
Постоянство pH клетки поддерживается благодаря буферным свойствам её содержимого. Буферным называют раствор, который поддерживает постоянное значение pH среды. Обычно буферная система состоит из сильного и слабого электролита: соли и слабого основания или слабой кислоты, которые её образуют
Действие буферного раствора заключается в том, что он противостоит изменениям pH среды. Изменение pH среды может возникнуть вследствие концентрирования раствора или разбавления его водой, кислотой или щелочью. Когда кислотность, то есть концентрация ионов водорода возрастает, свободные анионы, источником которых служит соль, взаимодействуют с протонами и удаляют их из раствора.
рН среды и роль ионов в его поддержании
Когда кислотность снижается, то усиливается тенденция к освобождению протонов. Таким образом поддерживается pH на определенном уровне, то есть поддерживается концентрация протонов на определенном постоянном уровне.
Некоторые органические соединения, в частности белки, также обладают буферными свойствами.
Катионы магния, кальция, железа, цинка, кобальта, марганца входят в состав ферментов и витаминов
Катионы металлов входят в состав гормонов.
Цинк входит в состав инсулина. Инсулин – это гормон поджелудочной железы, который регулирует уровень глюкозы в крови.
Магний входит в состав хлорофилла.
Железо входит в состав гемоглобина.
При недостатке этих катионов нарушается процессы жизнедеятельности клетки
Буферная система крови
В организме человека всегда имеются определенные условия для сдвига нормальной реакции среды ткани, например, крови, в сторону ацидоза (закисления) или алкалоза (раскисления – смещения рН в большую сторону).
В кровь поступают различные продукты, например, молочная кислота, фосфорная кислота, сернистая кислота, образующиеся в результате окисления фосфорорганических соединений либо серосодержащих белков. При этом реакция крови, может сдвигаться в сторону кислых продуктов.
При употреблении мясных продуктов, в кровь поступают кислые соединения. При употреблении растительной пищи, в кровь поступают основания.
Тем не менее, pH крови остается на определенном постоянном уровне.
В крови имеются буферные системы, которые поддерживают pH на определенном уровне.
К буферным системам крови относятся:
- карбонатная буферная система,
- фосфатная буферная система,
- буферная система гемоглобина,
- буферная система белков плазмы
Для нормальной жизнедеятельности организмов требуются минеральные соли. В клетке они находятся в твёрдом или в растворённом виде. Растворённые соли диссоциированы на ионы. Наиболее важными являются катионы металлов: калия K + , натрия Na + , кальция Ca 2 + , магния Mg 2 + , и анионы: Cl − , H 2 PO 4 − , HPO 4 2 − , HCO 3 − , CO 3 2 − .
Роль минеральных солей в клетке разная. Так, ионы калия и натрия обеспечивают возбудимость клеток. Внутри клетки больше ионов K + , а снаружи всегда больше содержание Na + , что приводит к возникновению разности потенциалов на клеточной мембране, обеспечивает раздражимость клеток и передачу возбуждения по нервам или мышцам. Перенос ионов через мембрану клетки осуществляется натрий-калиевым насосом и происходит с затратами АТФ (активный транспорт).

Ионы кальция участвуют в регуляции мышечных сокращений, необходимы для процесса свёртывания крови. Твёрдые соли кальция входят в состав костной ткани, содержатся в раковинах моллюсков и панцирях ракообразных.
Катионы многих металлов (магния, кальция, железа, меди, кобальта, цинка, марганца и др.) необходимы для синтеза некоторых ферментов, гормонов и витаминов.
Анионы фосфорной и угольной кислот образуют буферные системы, поддерживающие на постоянном уровне содержание ионов водорода в клетке (рН среды). Анионы HPO 4 2 − и H 2 PO 4 − (фосфатная буферная система) обеспечивают рН цитоплазмы клеток в пределах \(6,9\)–\(7,4\). Анионы H CO 3 − и CO 3 2 − (бикарбонатная буферная система) поддерживают значение рН плазмы крови \(7,4\).
Фосфаты входят в состав костной и зубной ткани. Хлорид-ионы необходимы для образования соляной кислоты, содержащейся в желудочном соке, а сульфат ионы — для синтеза некоторых аминокислот.
Недостаток минеральных солей приводит к нарушению процессов обмена веществ и негативно сказывается на жизнедеятельности клетки.
Минеральные вещества составляют от 1 до 1,5% от сырой массы клетки, и находятся в клетке в виде солей диссоциированных на ионы, либо в твердом состоянии (рис. 1).

Рис. 1. Химический состав клеток живых организмов
В цитоплазме любой клетки находятся кристаллические включения, которые представлены слаборастворимыми солями кальция и фосфора; кроме них могут находиться оксид кремния и другие неорганические соединения, которые участвуют в образовании опорных структур клетки – в случае минерального скелета радиолярий – и организма, то есть образуют минеральное вещество костной ткани.
2. Неорганические ионы: катионы и анионы
Неорганические ионы, имеющие значение для жизнедеятельности клетки (рис. 2).

Рис. 2. Формулы основных ионов клетки
Катионы – калий, натрий, магний и кальций.
Анионы – хлорид анион, гидрокарбонат анион, гидрофосфат анион, дигидрофосфат анион, карбонат анион, фосфат анион и нитрат анион.
Рассмотрим значение ионов.
Ионы, располагаясь по разные стороны клеточных мембран, образуют так называемый трансмембранный потенциал. Многие ионы неравномерно распределены между клеткой и окружающей средой. Так, концентрация ионов калия (К+) в клетке в 20–30 раз выше, чем в окружающей среде; а концентрация ионов натрия (Na+) в десять раз ниже в клетке, чем в окружающей среде.
Благодаря существованию градиентов концентрации, осуществляются многие жизненно важные процессы, такие как сокращение мышечных волокон, возбуждение нервных клеток, перенос веществ через мембрану.
Катионы влияют на вязкость и текучесть цитоплазмы. Ионы калия уменьшают вязкость и увеличивают текучесть, ионы кальция (Са2+) обладают противоположным действием на цитоплазму клетки.
Анионы слабых кислот – гидрокарбонат анион (НСО3-), гидрофосфат анион (НРО42-) – участвуют в поддержании кислотно-щелочного баланса клетки, то есть pH среды. По своей реакции растворы могут быть кислыми, нейтральными и основными.
Кислотность или основность раствора определяется концентрацией в нем ионов водорода (рис. 3).

Рис. 3. Определение кислотности раствора при помощи универсального индикатора
Эту концентрацию выражают с помощью водородного показателя pH, протяженность шкалы от 0 до 14. Нейтральная среда pH – около 7. Кислая – меньше 7. Основная – больше 7. Быстро определить pH среды можно с помощью индикаторных бумажек, или полосок (см. видео).
Мы опускаем индикаторную бумажку в раствор, затем полоску вынимаем и сразу же сравниваем окрашивание индикаторной зоны полоски с цветами стандартной шкалы сравнения, которая входит в комплект, оценивая схожесть окрашивания и определяя значение pH (см. видео).
3. рН среды и роль ионов в его поддержании
Значение pH в клетке примерно равняется 7.
Изменение pH в ту или иную сторону губительно действует на клетку, поскольку сразу же изменяются биохимические процессы, проходящие в клетке.
Постоянство pH клетки поддерживается благодаря буферным свойствам её содержимого. Буферным называют раствор, который поддерживает постоянное значение pH среды. Обычно буферная система состоит из сильного и слабого электролита: соли и слабого основания или слабой кислоты, которые её образуют (Источник).
Действие буферного раствора заключается в том, что он противостоит изменениям pH среды. Изменение pH среды может возникнуть вследствие концентрирования раствора или разбавления его водой, кислотой или щелочью. Когда кислотность, то есть концентрация ионов водорода возрастает, свободные анионы, источником которых служит соль, взаимодействуют с протонами и удаляют их из раствора. Когда кислотность снижается, то усиливается тенденция к освобождению протонов. Таким образом поддерживается pH на определенном уровне, то есть поддерживается концентрация протонов на определенном постоянном уровне.
Некоторые органические соединения, в частности белки, также обладают буферными свойствами.
Катионы магния, кальция, железа, цинка, кобальта, марганца входят в состав ферментов и витаминов (см. видео).
Катионы металлов входят в состав гормонов.
Цинк входит в состав инсулина. Инсулин – это гормон поджелудочной железы, который регулирует уровень глюкозы в крови.
Магний входит в состав хлорофилла.
Железо входит в состав гемоглобина.
При недостатке этих катионов нарушается процессы жизнедеятельности клетки.
4. Ионы металлов как кофакторы
Значение ионов натрия и калия
Ионы натрия и калия распределены по всему объему организма, при этом ионы натрия входят, в основном, в состав межклеточной жидкости, а ионы калия содержатся внутри клеток: 95% ионов калия содержатся внутри клеток, а 95% ионов натрия содержатся в межклеточных жидкостях (рис. 4).

С ионами натрия связано осмотическое давление жидкостей, удержание воды тканями, а также перенос, или транспорт таких веществ как аминокислоты и сахара через мембрану.
Значение кальция в организме человека
Кальций является одним из самых распространенных элементов в организме человека. Основная масса кальция входит в состав костей и зубов. Фракция внекостного кальция составляет 1% от общего количества кальция в организме. Внекостный кальций влияет на свертываемость крови, а также нервно-мышечную возбудимость и сокращение мышечных волокон.
Фосфатная буферная система
Фосфатная буферная система играет роль в поддержании кислотно-щелочного баланса организма, кроме этого она поддерживает баланс в просвете канальцев почек, а также внутриклеточной жидкости.
Фосфатная буферная система состоит из дигидрофосфата и гидрофосфата. Гидрофосфат связывает, то есть нейтрализует протон. Дигидрофосфат высвобождает протон и взаимодействует с поступившими в кровь щелочными продуктами.
Фосфатная буферная система входит в буферную систему крови (Рис. 5).

Буферная система крови
В организме человека всегда имеются определенные условия для сдвига нормальной реакции среды ткани, например, крови, в сторону ацидоза (закисления) или алкалоза (раскисления – смещения рН в большую сторону).
В кровь поступают различные продукты, например, молочная кислота, фосфорная кислота, сернистая кислота, образующиеся в результате окисления фосфорорганических соединений либо серосодержащих белков. При этом реакция крови, может сдвигаться в сторону кислых продуктов.
При употреблении мясных продуктов, в кровь поступают кислые соединения. При употреблении растительной пищи, в кровь поступают основания.
Тем не менее, pH крови остается на определенном постоянном уровне.
В крови имеются буферные системы, которые поддерживают pH на определенном уровне.
К буферным системам крови относятся:
- карбонатная буферная система,
- фосфатная буферная система,
- буферная система гемоглобина,
- буферная система белков плазмы (Рис. 6).
Взаимодействие этих буферных систем создает определенное постоянное pH крови.

Таким образом, сегодня мы с вами рассмотрели минеральные вещества и их роль в жизнедеятельности клетки.

Анионы – хлорид анион, гидрокарбонат анион, гидрофосфат анион, дигидрофосфат анион, карбонат анион, фосфат анион и нитрат анион.
Рассмотрим значение ионов.
Ионы, располагаясь по разные стороны клеточных мембран, образуют так называемый трансмембранный потенциал . Многие ионы неравномерно распределены между клеткой и окружающей средой. Так, концентрация ионов калия (К + ) в клетке в 20–30 раз выше, чем в окружающей среде; а концентрация ионов натрия (Na + ) в десять раз ниже в клетке, чем в окружающей среде.

- Катионы влияют на вязкость и текучесть цитоплазмы.
Ионы калия(К ) уменьшают вязкость и увеличивают текучесть,
ионы кальция (Са 2+ ) обладают противоположным действием на цитоплазму клетки.
рН среды и роль ионов в его поддержании
Значение pH в клетке примерно равняется 7.
Изменение pH в ту или иную сторону губительно действует на клетку, поскольку сразу же изменяются биохимические процессы, проходящие в клетке.
Постоянство pH клетки поддерживается благодаря буферным свойствам её содержимого.
Буферным называют раствор, который поддерживает постоянное значение pH среды . Обычно буферная система состоит из сильного и слабого электролита: соли и слабого основания или слабой кислоты, которые её образуют
Действие буферного раствора заключается в том, что он противостоит изменениям pH среды. Изменение pH среды может возникнуть вследствие концентрирования раствора или разбавления его водой, кислотой или щелочью.

рН среды и роль ионов в его поддержании
рН среды и роль ионов в его поддержании
Некоторые органические соединения, в частности белки, также обладают буферными свойствами.
Катионы магния, кальция, железа, цинка, кобальта, марганца входят в состав ферментов и витаминов
Катионы металлов входят в состав гормонов.
Цинк входит в состав инсулина. Инсулин – это гормон поджелудочной железы, который регулирует уровень глюкозы в крови.
Магний входит в состав хлорофилла.
Железо входит в состав гемоглобина.
При недостатке этих катионов нарушается процессы жизнедеятельности клетки
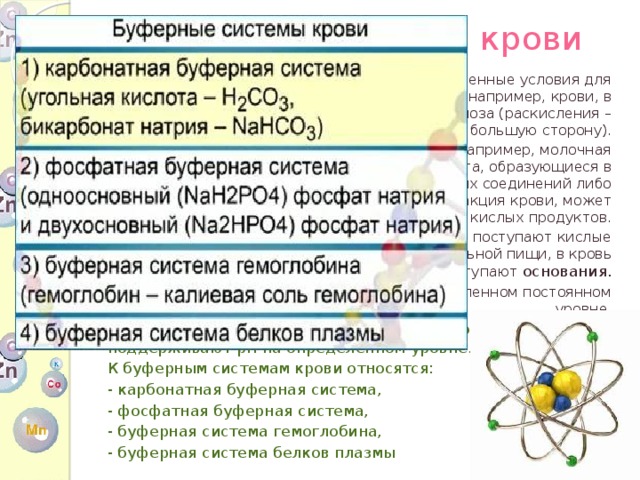
Буферная система крови
В организме человека всегда имеются определенные условия для сдвига нормальной реакции среды ткани, например, крови, в сторону ацидоза (закисления) или алкалоза (раскисления – смещения рН в большую сторону).
В кровь поступают различные продукты, например, молочная кислота, фосфорная кислота, сернистая кислота, образующиеся в результате окисления фосфорорганических соединений либо серосодержащих белков. При этом реакция крови, может сдвигаться в сторону кислых продуктов.
При употреблении мясных продуктов, в кровь поступают кислые соединения. При употреблении растительной пищи, в кровь поступают основания.
Тем не менее, pH крови остается на определенном постоянном уровне.
В крови имеются буферные системы , которые поддерживают pH на определенном уровне.
К буферным системам крови относятся:
- карбонатная буферная система,
- фосфатная буферная система,
- буферная система гемоглобина,
- буферная система белков плазмы

Спасибо за внимание

-75%
Минеральные вещества и их роль в клетке
1. Какие вещества называются минеральными?
2. Какой процесс называется диссоциацией?
3. Что такое ионы?
Минеральные вещества клетки.
Большая часть минеральных веществ клетки находится в виде солей, диссоциированных на ионы, либо в твердом состоянии.
В цитоплазме практически любой клетки имеются кристаллические включения, состоящие, как правило, из слаборастворимых солей кальция и фосфора. Кроме них могут содержаться двуокись кремния и другие неорганические вещества.
Они используются для образования опорных структур клетки (например, минеральный скелет радиолярий) и организма: минерального вещества костной ткани (соли кальция и фосфора), раковин моллюсков (соли кальция), хитина (соли кальция) и др.
Неорганические ионы, имеющие немаловажное значение для обеспечения процессов жизнедеятельности клетки, представлены катионами (К+, Na+Са2+-, Mgг2+, NH3+ и анионами (С1-, НРО42- , Н2РО4-, НСО3-, N03-, РО43-, СО32-|) минеральных солей. Концентрация катионов и анионов в клетке и в окружающей ее среде различна. В результате образуется разность потенциалов между содержимым клетки и окружающей ее средой, обеспечивающая такие важные процессы, как раздражимость и передача возбуждения по нерву или мышце.
Значение рН в клетках примерно равно 7,0. Изменение его на одну-две единицы губительно для клетки.
Постоянство рН в клетках поддерживается благодаря буферным свойствам их содержимого.
Буферным называют раствор, содержащий смесь какой-либо слабой кислоты и ее растворимой соли. Когда кислотность (концентрация ионов Н+) увеличивается, свободные анионы, источником которых является соль, легко соединяются со свободными ионами Н+ и удаляют их из раствора. Когда кислотность снижается, высвобождаются дополнительные ионы Н+. Так в буферном растворе поддерживается относительно постоянная концентрация ионов Н+.
Некоторые органические соединения, в частности белки, также имеют буферные свойства.
Являясь компонентами буферных систем организма, ионы определяют их свойства — способность поддерживать рН на постоянном уровне (близко к нейтральной реакции), несмотря на то что в процессе обмена веществ непрерывно образуются кислые и щелочные продукты. Так, фосфатная буферная система млекопитающих, состоящая из НРО|42- и Н2РО-4, поддерживает рН внутриклеточной жидкости в пределах 6,9—7,4, Главной буферной системой внеклеточной среды (плазмы крови) служит бикарбонатная система, состоящая из Н2С03 и НСО4- и поддерживающая рН на уровне 7,4.
Соединения азота, фосфора, кальция и другие неорганические вещества используются для синтеза органических молекул (аминокислот, белков, нуклеиновых кислот и др.).
Ионы некоторых металлов (Мg, Са, Zе, Си, Мn, Мо, Вr, Со) являются компонентами многих ферментов, гормонов и витаминов или активируют их. Например, ион Fе входит в состав гемоглобина крови, ион Zn — гормона инсулина. При их недостатке нарушаются важнейшие процессы жизнедеятельности клетки.
Буферная система.
1. В каком виде минеральные вещества представлены в живых организмах?
2. Какова роль неорганических ионов в клетке?
3. Какова роль ионов в буферных системах организма?
4. Почему недостаток или отсутствие ионов некоторых металлов приводит к нарушению жизнедеятельности клеток?
Важную роль для жизнедеятельности организмов играют неорганические кислоты и их соли. Так, соляная кислота входит в состав желудочного сока и создает условия для переваривания белков пищи. Остатки серной кислоты способствуют выведению из организма нерастворимых в воде веществ.
Онлайн библиотека с учениками и книгами, плани-конспекти уроковс Биологии 10 класса, книги и учебники согласно календарного плана планирование Биологии 10 класса
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
Читайте также:

