Протонно нейтронная модель строения ядра атома доклад
Обновлено: 07.05.2024
Протонно-нейтронная модель атома ( реферат , курсовая , диплом , контрольная )
Эту модель предложили в 1932 г. советские физики Д. Иваненко, Е. Гапон и немецкий физик В. Гейзенберг. Согласно этой модели ядро атома состоит из протонов и нейтронов, за исключением ядра водорода, которое состоит из одного протона. В этой модели было непонятно, каким образом достигается физическое единство атома на уровне его ядра и электронных оболочек: в ядре на чрезвычайно малом расстоянии находятся одинаково заряженные протоны, которые должны взаимно отталкиваться друг от друга, но этого не наблюдается. Следовательно, этому процессу отталкивания должна препятствовать сила притяжения между протонами, поскольку протоны имеют массу, но масса их чрезвычайно мала. Предлагалось множество моделей физического единства атома, среди которых особенно привлекательной оказалась модель японского физика Юкава (1907—1961), которая была предложена им все в том же 1932 г. Но прежде чем рассматривать эту модель, раскроем физическую суть протонно-нейтронной модели атома.
Строение атома, искусственная и естественная радиация. Все материальные тела состоят из химических элементов. Химический элемент — это простое вещество, состоящее из одного и того же вида атомов. Современной науке известно более ста химических элементов, некоторые химические элементы созданы самим человеком. Атом химического элемента можно представить как сферическую пульсирующую каплю концентрации энергии. Размеры атома — приблизительно 10−8 см. Атом состоит из ядра размером в 10−13 см и вращающихся вокруг него электронов (или одного электрона в случае атома водорода). Между ядром атома и границей атома находится огромное пространство по масштабам в микромире. Ядра атомов состоят из положительно заряженных протонов и нейтральных нейтронов. Плотность в ядре атома огромна, приблизительно 150 * 10б т/см3.
Заряд ядра определяется количеством в нем протонов и обозначается символом Z Вся масса атома заключена в массе его ядра и определяется массой входящих в ядро протонов и нейтронов.
Например, 23892Ur — указывает, что уран-238 имеет в ядре 92 протона и 146 нейтронов (238 — 92 = 146). Химические элементы с массовым числом, А > 50 называются легкими, а с А > 50 — тяжелыми.
Радиоактивностью называется самопроизвольное или искусственное (сознательное воздействие на ядра атомов) превращение ядер одних химических элементов в ядра других химических элементов.
Естественная и искусственная радиоактивность сопровождается, но не обязательно, тремя видами излучения: альфа-излучение, бета-излучение и гаммаизлучение; последнее не является, строго говоря, самостоятельным видом излучения и всегда присутствует при альфаи бетта-излучениях. Искусственная радиация, позитронное бета-излучение, аннигиляция, распад частиц были открыты французскими физиками Ф. Жолио-Кюри (1900—1958) и И. Жолио-Кюри (1897—1956). Законы как естественного, так и искусственного распада ядер атомов одинаковы. Период времени, за который распадается половина ядер радиоактивного химического элемента, называется периодом полураспада. Период полураспада у известных сегодня радиоактивных элементов колеблется от 3 * 10-7 с до 5 * 1012 лет.
Например, уран-238 имеет 12 этапов превращения в другие химические элементы, которые имеют свои периоды полураспада и соответствующие альфаи бетаизлучения. Период полураспада урана-238 оценивается в 4,47 млрд лет. В конечном итоге распад урана-238 заканчивается появлением стабильного химического элемента (свинец-206). Зная, какое количество урана-238 необходимо для появления определенного количества свинца-206, можно вычислить возраст Земли, отталкиваясь от количества содержания свинца-206 в земных породах.
Наряду с реакцией ядерного деления существует реакция ядерного синтеза:
не деление ядер, а сближение, соединение ядер. Реакция синтеза ядер существует реально внутри звезд (например, она происходит во внутренних слоях нашего Солнца). Внутри Солнца температура достигает 15 млн градусов Цельсия. При такой температуре ядра теряют электроны, образуется агрегатное состояние, которое называется плазмой. Поскольку ядра имеют положительный заряд, то при их сближении электростатическая сила их отталкивания резко увеличивается. Для того чтобы преодолеть этот барьер, необходима большая скорость движения ядер. При очень высоких температурах ядра теряют свои электроны. Плазма, с учетом бесконечного количества наблюдаемых звезд, является самым типичным агрегатным состоянием во Вселенной.
§ 35. Протонно-нейтронная модель строения ядра атома
Вы уже знаете, что вещества состоят из мельчайших частиц – атомов, взаимодействующих между собой. Изучая строение и свойства атома, можно создавать новые источники энергии, вещества с заранее заданными свойствами, использовать новые возможности в медицине, технологии производства. В этой связи необходимо ответить на вопросы: как устроен атом? Каким закономерностям он подчиняется?

В физике за атомную единицу массы (1 а.е.м.) принимается величина, равная массы изотопа углерода :

В экспериментах Резерфорда по изучению рассеяния α-частиц веществом было установлено, что в центральной части атома, размеры которого , находится положительно заряженное ядро, имеющее размер , в котором сосредоточено 99,96 % от массы атома (рис. 208).
Для завершения построения модели атома необходимо было ответить на вопрос: обладает ли атомное ядро структурой, и если обладает, то какой?
Наличие в ядре положительно заряженных частиц — протонов было экспериментально доказано Резерфордом с его учениками в 1919 г. Протон, обозначаемый латинской буквой p, представляет собой ядро атома водорода. Он обладает массой и зарядом, равным по абсолютной величине заряду электрона .
В 1930 г. немецкие ученые Вальтер Боте и Ганс Беккер, изучая реакции, происходящие при облучении бериллия α-частицами, обнаружили новое излучение, обладающее очень большой проникающей способностью, первоначально названное бериллиевыми лучами. В 1932 г. английский физик Джеймс Чедвик провел эксперименты по изучению свойств этого излучения и установил, что бериллиевые лучи состоят из электрически нейтральных частиц с массой, сравнимой с массой протона. Эти частицы он назвал нейтронами (от англ. neutral — нейтральный).

Нейтрон — еще одна частица наряду с электроном, протоном и фотоном. Эта частица обозначена латинской буквой n. Она имеет массу , совпадающую с массой протона, электрически нейтральна. Из-за отсутствия электрического заряда у нейтрона взаимодействие с веществом очень слабо. Вследствие этого нейтрон движется в веществе прямолинейно до тех пор, пока не столкнется с каким-либо атомным ядром. При столкновениях с тяжелыми атомами нейтрон почти не теряет энергию, как упругий мячик, отскакивающий от стены. При столкновении же с легкими атомами (водород, бериллий, углерод) нейтрон передает им часть своей энергии и начинает двигаться медленнее. Вещества, содержащие легкие атомы, называют замедлителями нейтронов. Наиболее эффективными замедлителями нейтронов являются вещества, содержащие водород (например, вода), вследствие того, что масса атома водорода близка к массе нейтрона. Со временем кинетическая энергия нейтрона становится такой же, как кинетическая энергия теплового движения частиц окружающей среды. Такие относительно медленно движущиеся нейтроны называются тепловыми.
Нейтроны устойчивы только в составе стабильных ядер. Нейтрон в свободном состоянии, т. е. находящийся вне ядра, является нестабильной частицей. Его среднее время жизни t = 886 c.
После открытия нейтронов в 1932 г. физики — советский Дмитрий Дмитриевич Иваненко и немецкий Вернер Гейзенберг — предложили протонно-нейтронную модель строения ядра. Согласно этой модели ядро состоит из частиц двух типов — протонов и нейтронов (рис. 209).

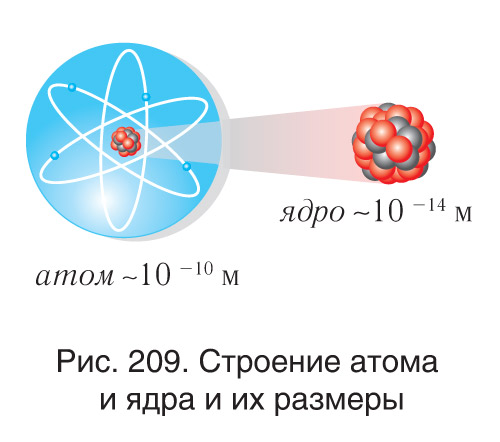
В соответствии с современными физическими представлениями протон и нейтрон являются двумя разными зарядовыми состояниями одной и той же частицы — нуклона (от лат. nucleus — ядро). В состоянии без электрического заряда нуклон является нейтроном, а в состоянии с положительным электрическим зарядом — протоном.
Число протонов в ядре называется зарядовым числом (атомным номером) и обозначается буквой Z (число протонов в ядре равно количеству электронов в нейтральном атоме). Зарядовое число совпадает с порядковым номером химического элемента в периодической системе элементов Менделеева. Общее число нуклонов называется массовым числом и обозначается буквой A. Массовое число совпадает с округленной до целого числа атомной массой элемента. Протон и нейтрон имеют массовое число А = 1, а электрон A = 0. Число нейтронов в ядре равно N = A − Z.
Для характеристики ядра достаточно знать зарядовое Z и массовое A числа. Для обозначения атомного ядра применяется такой же символ, как для соответствующего химического элемента. Слева внизу символа ставится зарядовое число ядра Z, а вверху — массовое число A. Например, символ обозначает ядро углерода, содержащего 12 нуклонов, 6 из которых протоны, а 6 других — нейтроны.
Атом с определенными значениями зарядового числа Z и массового числа A называется нуклидом.

В ядрах одного химического элемента всегда содержится одно и то же количество протонов, а число нейтронов может быть различным. Например, в ядрах углерода число протонов всегда 6, а число нейтронов может быть 5, 6, 7, 8, 9 или 10.
Атомы, ядра которых содержат одинаковое число протонов, но различное число нейтронов, называются изотопами (от греч. (изос) — одинаковый и τοπος (топос) — место) данного химического элемента. Например, хорошо известны изотопы водорода — дейтерий и тритий , которые содержат, соответственно, один и два нейтрона в ядре (рис. 210).
Массы некоторых атомов приведены в таблице 10.
Таблица 10. Массы атомов некоторых химических элементов
| Элемент | Изотоп | Масса атома, а.е.м | Элемент | Изотоп | Масса атома, а.е.м |
| Водород | 1,00783 | Углерод | 11,01143 | ||
| Водород | 2,01410 | Углерод | 12,00000 | ||
| Водород | 3,01605 | Азот | 14,00307 | ||
| Гелий | 4,00260 | Кислород | 15,99491 | ||
| Литий | 6,01513 | Фтор | 18,99840 | ||
| Литий | 7,01601 | Алюминий | 26,98146 | ||
| Берилий | 8,00531 | Кремний | 27,98154 | ||
| Берилий | 9,01218 | Уран | 235,04393 | ||
| Бор | 10,01296 | Уран | 238,05079 | ||
| Бор | 11,00931 | Плутоний | 239,05216 |
Химические свойства элементов определяются не атомной массой, а зарядовым числом ядра, т. е. числом электронов в электрически нейтральном атоме элемента и их распределением по энергетическим уровням. Действительно, атомные массы изотопов различаются, а их химические свойства одинаковы. Например, атомы нуклидов водорода и гелия имеют близкие по величине атомные массы, но принципиально разные химические свойства.
В рамках протонно-нейтронной модели ядра возникает вопрос о его устойчивости. Действительно, между протонами, находящимися в ядре, действуют силы электростатического отталкивания огромной величины. Если считать расстояние между протонами , то модуль силы отталкивания , а гравитационная сила их притяжения составляет всего .
Чем же объясняется устойчивость ядра, если внутри него действуют такие огромные силы кулоновского отталкивания между протонами?
Причина устойчивости ядра кроется в существовании, кроме сил электростатического отталкивания между протонами (нуклонами), ядерных сил притяжения между нуклонами. Ядерные силы отличаются по своей природе как от сил электромагнитных, так и сил гравитационных. Они представляют новый вид взаимодействия между нуклонами, который называют сильным взаимодействием.
Ядерные силы обладают рядом отличительных свойств:
1) являются силами притяжения и отталкивания;
2) на расстояниях порядка размера ядра примерно в 100 раз превосходят по величине кулоновские силы отталкивания в ядре;
3) проявляются только на расстояниях между частицами порядка размера ядра , т. е. являются короткодействующими силами. На расстояниях, больших , они не проявляются;
4) не зависят от электрического заряда взаимодействующих нуклонов (ядерные силы между двумя протонами, нейтронами или протоном и нейтроном одинаковы). Это свойство называется зарядовой независимостью;
5) обладают свойством насыщения. Это означает, что находящиеся внутри ядра нуклоны могут взаимодействовать только со своими ближайшими соседями;
6) не являются центральными, т. е. они не направлены по линии, соединяющей центры взаимодействующих нуклонов.
Эксперименты показали, что многие ядра имеют примерно сферическую форму, а объем ядра пропорционален массовому числу А. Согласно экспериментальным данным радиус ядер возрастает в зависимости от массового числа в соответствии с формулой:
Так как объем шара , то объем ядра пропорционален массовому числу А. Вычислим плотность ядерного вещества:
Все ядра имеют плотность , а один кубический сантиметр ядерного вещества имеет массу 180 млн тонн.
Если бы можно было изготовить спичечную головку из ядерного вещества объемом несколько кубических миллиметров, то она имела бы массу около миллиона тонн. Это соответствует массе воды в кубическом резервуаре со стороной 100 м.
Так как массы и энергии ядерных величин в единицах СИ имеют очень малые значения, для удобства вычислений все массы в ядерной физике выражают в атомных единицах массы (а.е.м.), а энергии — в электронвольтах (эВ). Используя формулу Эйнштейна , массу также можно выразить в единицах энергии — электронвольтах: . Например, в атомных единицах массы масса электрона , масса протона , масса нейтрона , масса атома водорода , а в энергетических единицах , , .
Связь между различными единицами массы определяется следующими соотношениями:
Изотопы применяются в биологии для изучения фотосинтеза, для исследования использования растениями фосфора, азота, калия и микроэлементов, при исследовании процессов обмена веществ и биосинтеза; в медицине — при диагностике заболеваний, для радиоиммунного анализа и томографии; в экологии — для исследования переноса, накопления и распада различных загрязнителей в воздухе, воде и почве.
Дж. Чедвик за открытие нейтрона получил Нобелевскую премию по физике в 1935 г
Ядро (атомное)– это положительно заряженная центральная часть атома, в которой сосредоточено 99,96% его массы. Радиус ядра ~10 –15 м, что приблизительно в сто тысяч раз меньше радиуса всего атома, определяемого размерами его электронной оболочки.
Атомное ядро состоит из протонов и нейтронов. Их общее количество в ядре обозначают буквой А и называют массовым числом. Число протонов в ядре Z определяет электрический заряд ядра и совпадает с атомным номером элемента в периодической системе элементов Д.И. Менделеева. Число нейтронов в ядре может быть определено как разность между массовым числом ядра и числом протонов в нем. Массовое число – это число нуклонов в ядре.
Строение атома
Конкретные представления о строении атома развивались по мере накопления физикой фактов о свойствах вещества. Открыли электрон, измерили его массу. Мысль об электронном строении атома, впервые высказанную В. Вебером в 1896 г., развил Х. Лоренц. Именно он создал электронную теорию: электроны входят в состав атома.
Опираясь на эти открытия, Дж. Томсон в 1898 г. предложил модель атома в виде положительно заряженного шара радиусом 10 -10 м, в котором плавают электроны, нейтрализующие положительный заряд:

Экспериментальная проверка модели атома Томсона была осуществлена в 1911 г. английским физиком Э. Резерфордом:


Пропуская пучок Альфа - частиц через тонкую золотую фольгу, Э. Резерфорд обнаружил, что какая-то часть частиц отклоняется на довольно значительный угол от своего первоначального направления, а небольшая часть – отражается от фольги. Но согласно модели атома Томсона, частицы могли отклоняться только на углы около 200, но появлялись частицы, угол отклонения которых был больше 90 0 (рисунок выше)
Резерфорд показал, что модель Томсона находится в противоречии с его опытами. Обобщая результаты своих опытов.
Резерфорд предложил ядерную (планетарную) модель строения атома:
Атом имеет ядро, размеры которого малы по сравнению с размерами самого атома.
В ядре сконцентрирована почти вся масса атома.
Отрицательный заряд всех электронов распределен по всему объему:


Открытие нейтрона
Идея о существовании тяжелой нейтральной частицы казалась Резерфорду настолько привлекательной, что он незамедлительно предложил группе своих учеников во главе с Дж. Чедвиком заняться поиском такой частицы.
Через 12 лет в 1932 г. Чедвик экспериментально исследовал излучение, возникающее при облучении бериллия? - частицами, и обнаружил, что это излучение представляет собой поток нейтральных частиц с массой, примерно равной массе протона. Так был открыт нейтрон. На рисунке приведена упрощенная схема установки для обнаружения нейтронов.

Это не протон-электронная пара, как первоначально предполагал Резерфорд. По современным измерениям масса нейтрона mn = 1,67493·10 –27 кг = 1,008665 а.е.м.
В энергетических единицах масса нейтрона равна 939,56563 МэВ.
Масса нейтрона приблизительно на две электронные массы превосходит массу протона.
Протонно-нейтронная модель ядра
Сразу же после открытия нейтрона российский ученый Д. Д. Иваненко и немецкий физик В. Гейзенберг выдвинули гипотезу о протонно-нейтронном строении атомных ядер, которая полностью подтвердилась последующими исследованиями.
По современным измерениям, положительный заряд протона в точности равен элементарному заряду e = 1,60217733·10 –19 Кл, то есть равен по модулю отрицательному заряду электрона. В настоящее время равенство зарядов протона и электрона проверено с точностью 10–22. Такое совпадение зарядов двух непохожих друг на друга частиц вызывает удивление и остается одной из фундаментальных загадок современной физики.
Масса протона, по современным измерениям, равна mp = 1,67262·10 -27 кг.
Протоны и нейтроны в ядре принято называть нуклонами.

Символическое обозначение ядра атома
А - число нуклонов, т.е. протонов + нейтронов (или атомная масса)
Z - число протонов (равно числу электронов)
N - число нейтронов (или атомный номер )
Для того, чтобы атомные ядра были устойчивыми, протоны и нейтроны должны удерживаться внутри ядер огромными силами, во много раз превосходящими силы нуклоновского отталкивания протонов.
Силы, удерживающие нуклоны в ядре, называются ядерными.
Особенности ядерных сил:
Ядерные силы примерно в 100 раз превосходят электростатические силы и на десятки порядков превосходят силы гравитационного взаимодействия нуклонов.
Важной особенностью ядерных сил является их короткодействующий характер. Ядерные силы заметно проявляются, как показали опыты Резерфорда по рассеянию a-частиц, лишь на расстояниях порядка размеров ядра (10–14–10–15 м). Ядерные силы очень быстро спадают с расстоянием.
Радиус их действия порядка 0,000 000 000 000 001 метра.
Для этой сверхмалой длины, характеризующей размеры атомных ядер, ввели специальное обозначение Фм (в честь итальянского физика Э. Ферми, 1901-1954).
Все ядра имеют размеры нескольких Ферми.
Радиус действия ядерных сил равен размеру нуклона, поэтому ядра - концентрация очень плотной материи. Возможно, самой плотной в земных условиях. Ядерные силы - сильные взаимодействия.
На больших расстояниях проявляется действие сравнительно медленно убывающих кулоновских сил.
На основании опытных данных можно заключить, что протоны и нейтроны в ядре притягиваются не зависимо от наличия заряда т. е. ядерные силы не зависят электрического заряда.
ЯДЕРНЫЕ СИЛЫ
действуют между всеми нуклонами в ядре;

В середине XX века теория ядра предсказала существование стабильных элементов с порядковыми номерами Z = 110 - 114.
В Дубне был получен 114-й элемент с атомной массой А = 289, который "жил" всего 30 секунд, что невероятно долго для атома с ядром такого размера. Сегодня теоретики уже обсуждают свойства сверхтяжелых ядер массой 300 и даже 500.
Атомы с одинаковыми атомными номерами называют изотопами: в таблице Менделеева
они расположены в одной клеточке (по-гречески изос - равный, топос - место).
Химические свойства изотопов почти одинаковы. Если элементов всего в природе - около 100, то изотопов - более 2000.
Многие из них неустойчивы, то есть радиоактивны, и распадаются, испуская различные виды излучений.
Изотопы одного и того же элемента по составу отличаются лишь количеством нейтронов в ядре.

Решение задач:
1. Сколько нуклонов, протонов и нейтронов содержится в ядрах следующих элементов:
11 23 Na A = 23 N = 23 – 11 = 12 Z = 11
11 21 Na A = 21 N = 21 – 11 = 9 Z = 11
4 9 B A = 9 N = 9 – 4 = 5 Z = 4
Самостоятельно: 8 16 O 3 7 Li 6 12 C 7 14 N 13 27 Al 92 235 U 82 207 Pb
2. Чем отличаются следующие элементы:
Самостоятельная работа. Вариант первый выполняют студенты с нечетным порядковым номером (по списку в журнале), второй – с четным.
Вариант 1
1. Напишите уравнения следующих ядерных реакций:
- алюминий ( 27 13Al) захватывает нейтрон и испускает α-частицу;
- азот ( 14 7N) бомбардируется α-частицами и испускает протон.
2. Закончите уравнение ядерных реакций:
3. Определите энергетический выход реакций:
Вариант 2
1. Напишите уравнения следующих ядерных реакций:
- фосфор( 31 15Р) захватывает нейтрон и испускает протон;
- алюминий ( 27 13Al) бомбардируется протонами и испускает α-частицу.
2. Закончите уравнение ядерных реакций:
3. Определите энергетический выход реакций:
1. Кто открыл явление радиоактивности?
А) М. Кюри;
Б) Дж. Томсон;
В) Беккерель;
Г) Э. Резерфорд
2. Изменяется ли атом в результате радиоактивного распада?
А) не изменяется;
Б) изменяется запас энергии атома, но атом остается того же химического элемента;
В) атом изменяется, превращается в атом другого химического элемента;
Г) в результате радиоактивного распада атом полностью исчезает.
3. Что такое - излучение?
А) поток быстрых двухзарядных ионов гелия;
Б) поток быстрых электронов;
В) поток квантов электромагнитного излучения высокой энергии;
Г) поток нейтральных частиц.
4. Какой прибор позволяет наблюдать следы заряженных частиц в виде полосы из капель воды в газе?
А) фотопластинка;
Б) счетчик Гейгера-Мюллера;
В) камера Вильсона;
Г) электронный микроскоп.
5. В атомном ядре содержится 25 протонов и 30 нейтронов. Каким положительным зарядом, выраженным в элементарных электрических зарядах +е, обладает это атомное ядро?
6. Из каких частиц состоят ядра атомов?
А) из протонов;
Б) из нейтронов;
В) из протонов, нейтронов и электронов;
Г) из протонов и нейтронов.
7. Сколько электронов содержится в электронной оболочке нейтрального атома, у которого ядро состоит из 6 протонов и 8 нейтронов?
8. Какие частицы из перечисленных ниже легче других способны проникать в атомное ядро и вызывать ядерные реакции?
А) электроны;
Б) нейтроны;
В) -частицы;
Г) все перечисленные в выше.
9. Какая частица Х образуется в результате реакции Li + ?
А) гамма-квант;
Б) электрон;
В) позитрон;
Г) нейтрон.
10. Массовое число – это:
А) число протонов в ядре;
Б) число нейтронов в ядре;
В) число электронов в электронной оболочке;
Г) число нуклонов в ядре.
Вариант.
1. По какому действию было открыто явление радиоактивности?
А) по действию на фотопластинку;
Б) по ионизирующему действию;
В) по следам в камере Вильсона;
Г) по вспышкам света, вызываемым в кристаллах ударами частиц.
2. Что такое -излучение?
А) поток быстрых двухзарядных ионов гелия;
Б) поток быстрых электронов;
В) поток квантов электромагнитного излучения высокой энергии;
Г) поток нейтральных частиц.
3. Что такое -излучение?
А) поток быстрых двухзарядных ионов гелия;
Б) поток быстрых электронов;
В) поток квантов электромагнитного излучения высокой энергии;
Г) поток нейтральных частиц.
4. Что одинаково у атомов разных изотопов одного химического элемента и что у них различно?
А) одинаковы заряды и массы атомных ядер, различны химические свойства атомов;
Б) одинаковы заряды, различны массы ядер и химические свойства;
В) одинаковы заряды ядер и химические свойства, различны массы ядер;
Г) одинаковы массы ядер, различны химические свойства и заряды ядер.
5. Какой прибор при прохождении через него ионизирующей частицы выдает сигнал в виде кратковременного импульса электрического тока:
А) счетчик Гейгера;
Б) фотоэлемент;
В) динамик;
Г) камера Вильсона.
6. В атомном ядре содержится Z протонов и N нейтронов. Чему равно массовое число М этого ядра?
7. Энергия связи рассчитывается по формуле:
А) Е= m·c;
Б) Е= m·c 2 ;
В) Е=m·c 2 ;
Г) Е= m·V 2 .
8. Для вычисления энергии связи ядра в СИ в каких единицах нужно выразить значение дефекта массы?
МОДЕЛЬ: АНСАМБЛЬ ПУЗЫРЬКОВ
МОДЕЛЬ: АНСАМБЛЬ ПУЗЫРЬКОВ Поговорим в начале главы об одной мудрой и красивой модели кристалла. По пути к концу книги она нам понадобится много раз.О модели мертвого кристалла или, быть может, правильнее о мертвой модели кристалла мы недавно вспоминали: деревянные
МОДЕЛЬ: РЕЗИНОВАЯ ТРУБКА
МОДЕЛЬ: РЕЗИНОВАЯ ТРУБКА В истории науки подобных примеров множество: появляется новая идея, или обнаруживается новое явление природы, и при этом вдруг оказывается, что ранее, в связи с совсем иными задачами и ввиду совсем иных целей, ученые высказали соображения или
МОДЕЛЬ: ЛУННАЯ ДОРОЖКА
МОДЕЛЬ: ЛУННАЯ ДОРОЖКА В этом очерке лунная дорожка — та, которую все видели на поверхности воды, — лишь удобная модель. А рассказывать я намерен о строении поверхности кристалла, о том, как она рассеивает свет, как на ней образуется световая дорожка, подобная той, какую мы
Стандартная модель
Стандартная модель Сегодня поле Янга-Миллса открыло возможность всеобъемлющей теории материи. Мы настолько уверены в этой теории, что ласково называем ее Стандартной моделью.Стандартная модель способна объяснить все экспериментальные данные, касающиеся субатомных
Строение ядра
Строение ядра Хотя вопрос об излучении ?-частицы казался окончательно выясненным, поскольку закон сохранения электрического заряда выполнялся, физики продолжали свои исследования. Для них оставалось загадкой, как положительно заряженное ядро способно испускать
Внутри ядра
Внутри ядра Это небывалое путешествие пройдет для пассажиров Жюль-Вернова ядра далеко не так мирно и благополучно, как описано в романе. Не думайте, однако, что опасность грозит им во время путешествия от Земли до Луны. Ничуть! Если бы им удалось остаться живыми к моменту,
Глава 4. СТАНДАРТНАЯ МОДЕЛЬ
Глава 4. СТАНДАРТНАЯ МОДЕЛЬ Если к моменту публикации книги БАК действительно уничтожит Землю, мы принесем свои искренние извинения и будем готовы возместить все затраты на эту книгу.21 марта 2008 года Уолтер Вагнер и Луис Санчо начали процесс в Федеральном суде США с
Открытие атомного ядра
Открытие атомного ядра Рассмотрим несколько подробнее одно из фундаментальных открытий Резерфорда —открытие атомного ядра и планетарной модели атома. Мы видели, что уподобление атома планетной системе делалось еще в самом начале XX в. Но эту модель было трудно
Расщепление ядра
Расщепление ядра Открытие изотопов стабильных элементов, уточнение измерений элементарного заряда были первыми достижениями послевоенной физики (1917-1918). В 1919 г. было сделано новое сенсационное открытие — искусственное расщепление ядра. Открытие это было сделано
Модель атома водорода
Модель атома водорода В 1913 году датский физик Нильс Бор (1885—1962) попытался нарисовать наглядную картину: как может быть построен атом из положительного ядра и электронов и при каких условиях он излучает свет. Физики называют такую наглядную картину моделью атома.Задача
4.9. Корпускулярная модель света
4.9. Корпускулярная модель света В описанных выше экспериментах и наблюдениях доказано, что движение объекта природы, называемого светом, как и всех остальных объектов природы, подчиняется классическому закону сложения скоростей. Изучены и другие его свойства, по которым
Модель горячей Вселенной
Стандартная модель
Стандартная модель К середине 1970-х все теоретические и опытные наработки СЛИЛИСЬ в единую теорию, названную стандартной моделью. В ее основе лежат математические выкладки, не являющиеся предметом настоящей книги, так что не следует забывать, что модель опирается на
Первая модель атома
Первая модель атома В заключение, мы можем сказать, что в первые годы XX в. был дан первый, может быть не полный, ответ на вопрос как излучается свет, а атомы с их электрическими зарядами были сочтены ответственными за это. Однако, как устроены атомы и, соответственно, каковы
Глава 4 Стандартная модель
Глава 4 Стандартная модель Почему Большой адронный коллайдер не уничтожил Землю?[56] 21 марта 2008 года Уолтер Вагнер и Луис Санчо начали процесс в Федеральном суде США с единственной простой целью – спасти человечество. Истцы утверждали, что в ближайшие несколько месяцев
Нейтронная звезда на орбите вокруг черной дыры
Нейтронная звезда на орбите вокруг черной дыры Волны исходили от нейтронной звезды, вращающейся вокруг черной дыры. Звезда весила в 1,5 раза больше Солнца, а черная дыра – в 4,5 раза больше Солнца, при этом дыра быстро вращалась. Образованный этим вращением
При изучении строения атома и атомных ядер физикам приходится обращаться с частицами очень малых масс. Поэтому для измерения массы частиц стали использовать новую единицу измерения массы — атомную единицу массы.
Опыты Резерфорда привели к возникновению новой модели строения атома — ядерной модели. Согласно этой модели внутри атома находится маленькое положительно заряженное ядро, вокруг которого по круговым орбитам вращаются электроны. Так как атом заряжен нейтрально, то заряд ядра должен быть равен заряду всех электронов, которые вращаются вокруг ядра. Эрнест Резерфорд обнаружил, что при соударении альфа-частиц с атомами некоторых химических элементов появляются положительно заряженные частицы, заряд которых равен элементарному, а масса равна массе атома водорода. Эти частицы были названы протонами .
Было очевидно, что протоны могли вылетать только из ядер атомов. А следовательно, внутри ядра находилось столько же протонов, сколько и электронов вращается вокруг ядра. Однако масса атомов была больше, чем масса протонов и электронов. Это означало, что внутри ядра должны находиться ещё какие-то частички, заряженные нейтрально. Такие частички — нейтроны — были открыты в \(1932\) г. английским физиком Джеймсом Чедвиком.
Частицы, из которых состоит ядро атома, называются нуклонами . Такая модель строения ядра получила название — протонно-нейтронная модель (рис. \(1\)).
Согласно протонно-нейтронной модели строения атомного ядра, в очень маленьком объёме должно находиться несколько положительно заряженных протонов. Возникали очевидные вопросы. Почему Кулоновские силы отталкивания не разрывают ядро? Какие силы удерживают протоны и нейтроны вместе? Очевидно, что эти силы действуют только на малых расстояниях (порядка 10 − 15 м) и должны быть значительно больше сил Кулоновского отталкивания. Такие силы были названы ядерным и силами.
Взаимодействие между протонами и нейтронами одинаковое, поэтому протон и нейтрон можно рассматривать как одну и ту же частицу — нуклон — в разных состояниях.
Ядерные силы действуют одинаково между протоном и нейтроном, между двумя протонами и между двумя нейтронами.
Читайте также:

