Маркерная и геномная селекция в свиноводстве доклад
Обновлено: 08.07.2024
Основы маркерной селекции. Важные ДНК-маркеры: полиморфные, полимеразные и мономорфные. Значение маркерной селекции в животноводстве. Влияние генов на свойства продукции. Повышение эффекта гетерозиса. Повышение эффективности оценки племенной ценности.
| Рубрика | Биология и естествознание |
| Вид | курсовая работа |
| Язык | русский |
| Дата добавления | 15.12.2012 |
| Размер файла | 479,6 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Российский государственный аграрный университет
Московская сельскохозяйственная академия имени К. А. Тимирязева
Кафедра разведения и племенного дела
Курсовая работа
Выполнила: студентка 3го курса
Москва 2011 год
Содержание
1. Основы маркерной селекции
2. Наиболее важные ДНК-маркеры
3. Значение маркерной селекции в животноводстве
Список использованной литературы
Введение
Основной задачей современного животноводства является получение высокопродуктивных животных, дающих высококачественную продукцию. Большинство показателей продуктивности имеет полигенную природу и определяется многими генами при взаимодействии с окружающей средой. Повышение эффективности селекции будет зависеть от подбора генотипов к конкретным условиям среды.
С целью выявления наиболее успешных генотипов используют генетические маркеры. В конце 70-х появилась возможность идентифицировать большое количество маркеров. Они позволяют получать информацию о разных состояниях генов и исследовать, как их варианты имеют преимущественное распространение у животных с наиболее желательными комплексами признаков.
Использование большого количества генетических маркеров позволяет более достоверно оценить генетический потенциал пород, популяций и отдельно взятых особей, более точно контролировать селекционные процессы.
Особую актуальность, как считает Е.И. Кийко, имеет нахождение локализации гена на хромосоме количественных признаков (QTL) с целью оценки генетических параметров и аддитивного генетического влияния.
Для решения этой проблемы существует направление в племенном деле - селекция с помощью маркеров. Целью ее является замена селекции по фенотипу на селекцию на уровне ДНК.
Основой маркерной селекции является нахождение локусов количественных признаков, которые отвечают за экономически важные продуктивные признаки. Достаточно идентифицировать маркер с неизвестной функцией, связанный с QTL и определить сцепление между аллелями в маркерном локусе.
Одним из самых важных направлений является поиск маркеров, которые позволяют выявить генотипы животных, обладающих хозяйственно-полезными признаками. Еще одно направление - поиск новых систем генетического маркирования.
В основу берут ДНК-маркеры, так как они имеют ряд преимуществ:
? наследование происходит по законам Менделя, что делает возможным непосредственный анализ генотипа;
- путем подбора зондов может быть идентифицировано множество вариантов ДНК;
- информативные зонды распределяются по всему геному;
- возможность оценки генотипа не зависит от возраста и пола животного.
1. Основы маркерной селекции
Идея маркеров в том, считает Джулия ван де Веф, что существуют гены со значительным влиянием на признаки, информацию о которых можно использовать в селекции. За проявление экономически важных признаков отвечает довольно большое количество генов. Некоторые из этих генов имеют наиболее значимое влияние. Их называют основными, локализованными в QTL. Хоть QTL относят ко всем генам, отвечающим за признак, на практике получается так, что к QTL относят только основные, наиболее значимые гены.
На рисунке показано, что из QTL только некоторые гены влияют на фенотип животного. Остальные гены вместе с ними определяют полную наследственную изменчивость. Хоть QTL объясняет только часть генотипа животного, информация, которую можно почерпнуть, добавляет точность к оценке истинного генотипа животного.
На рисунке изображено три быка с различными фенотипами. Верхняя часть показывает истинные аллельные ценности генов, отвечающих за массу тела. Нижний рисунок показывает, что наблюдается, если бы QTL был бы распознан в дополнение к фенотипу. маркерный селекция ген гетерозис
На рисунке предполагается, что племенная ценность и аллельные формы QTL известны. Но на практике это встречается не всегда. Фактически нельзя наблюдать непосредственное наследование QTL, но наблюдается наследование маркеров, которые схожи с QTL. Генетические маркеры как ориентиры, которые выбираются на основе схожести с QTL.
Генетические маркеры дают возможность к наиболее быстрому и точному генетическому анализу. Маркеры не оказывают влияния на организм животного, но они могут быть легко идентифицированы в лабораториях, поэтом можно определить какую разновидность маркера несет животное. Как и гены, генетические маркеры расположены в хромосомах последовательно.
Экспериментально можно определить генетические маркеры, которые располагаются на хромосоме близко к интересующим нас генам.
Нужно вести родословную и делать специальные измерения для того чтобы работать с кроссоверными генами. Если маркер расположен в пределах гена, то кроссинговер не является проблемой.
При выборе маркера надо учитывать какую информацию можно от него получить. При использовании прямых маркеров не возникает никаких проблем с определение генов QTL. Проблемы начинаются при использовании косвенных маркеров.
Ценность генотипа маркера зависит от трех вещей: влияния QTL, частота аллели и вероятность того, что животное унаследовало эту аллель.
Маркерные гены используются для выявления важных для животноводства генов. Маркерные гены особенно важны, дли признаков, которые фенотипически проявляются относительно поздно или только у одного пола, а также для признаков, на проявление которых оказывают влияние негенетические факторы (факторы окружающей среды). Примерами такого рода признаков являются резистентность к болезням, предрасположенность к болезням, плодовитость, молочная продуктивность. Целью маркирования является установление сцепления между основным геном и маркерным геном у животного. Так, к примеру, длина хромосомы крупного рогатого скота в среднем составляет 100 сМ, достаточно иметь три удачно расположенных маркера на хромосому: два маркера, удаленных на расстояние около 20 сМ от центромеры или теломеры, и один -- в центре. Следовательно, 90 расположенных данным образом маркерных локусов достаточно для полного картирования генома крупного рогатого скота.
В генетике животноводства большое значение для дальнейших разработок имеет тщательный выбор генотипов и структуры семьи, а также наличие банков ДНК и банков данных.
Среди множества генов, контролирующих продуктивность, можно выделить группу мажорных генов, вносящих наибольший вклад в формирование и функционирование данного количественного признака. К таким генам, например, относятся гены, кодирующие белки молока. Интерес исследователей к изучению генетического полиморфизма белков молока связан с тем, что их генетически детерминированные варианты оказывают значительное влияние на конкретные черты молочной продуктивности и, соответственно, могут быть использованы в качестве прямых генетических маркеров хозяйственно-полезных признаков. Внедрение генетических маркеров в качестве дополнительных критериев при отборе сельскохозяйственных животных ускоряет селекционный процесс и повышает его эффективность.
2. Наиболее важные ДНК-маркеры
Ценность информации о генотипе зависит от способности маркера предсказывать генотип животного.
- Возможность тестирования любых последовательностей генома.
- Возможность анализа материнского типа наследования (митохондриальная ДНК).
- Возможность анализа отцовского типа наследования (Y-хромосома).
- Отсутствие плейотропного эффекта.
- Информативность о природе генетических изменений. - Возможность проведения ретроспективных исследований.
- Возможность определения в любых тканях.
- Возможность определения на любых стадиях развития.
- Длительность хранения образцов ДНК.
- Возможность использования гербарного материала, ископаемых остатков и т.п.
Полиморфные ДНК-маркеры
Открытие и выделение рестрицирующих эндонуклеаз , расщепляющих ДНК в участках со строго определенной последовательностью, позволило разработать маркеры на основе анализа рестрикционного полиморфизма ДНК (ПДРФ, англ. RFLP - Restriction Fragment Length Polymorphism). Впервые ПДРФ был использован как генетический маркер в 1974 г. при идентификации термочувствительной мутации в геноме аденовируса. Однако широкое применение вариантов полиморфизма ДНК в качестве генетических маркеров началось с 1980 г. после выхода работы Ботштейна, в которой изучены свойства ПДРФ как генетического маркера, дано теоретическое обоснование его использования и предложен метод оценки уровня информативности. ПДРФ используют для анализа полиморфизма конкретных локусов (генов). С использованием ПДРФ-маркеров были получены первые успешные результаты по построению молекулярно-генетических карт многих видов растений и животных, накоплены обширные сведения о генетическом полиморфизме различных организмов, выявлены ассоциации с хозяйственно-полезными признаками. Важным достоинством данного типа маркеров является высокая воспроизводимость результатов, а также кодоминантный тип наследования. ПДРФ-локусы могут обладать множественными аллелями, что повышает их информативность.
Полимеразные ДНК-маркеры
Были изобретены в 1983 году, основаны на методе увеличения числа копий определенных участков ДНК. в процессе повторяющихся температурных циклов полимеразной реакции (ПЦР - полимеразная цепная реакция, англ. PCR - Polymerase Chain Reaction).
Метод ПЦР позволяет быстро и с небольшими затратами материальных ресурсов и времени получить более 10 миллионов копий определенной последовательности ДНК, первоначально представленной одной или несколькими молекулами. Различные модификации метода ПЦР легли в основу создания разнообразных типов ДНК-маркеров, широко используемых в настоящее время в различных областях биологии и медицины.
Мономорфные ДНК-маркеры
STSs-маркеры - в 1989 году Ольсоном с соавторами была сформулирована идея создания системы STS-маркеров, которая была призвана стандартизовать все обозначения маркированных последовательностей ДНК в геноме и включить в себя все типы картированных последовательностей.
3. Значение маркерной селекции в животноводстве
-Использование в возвратном скрещивании
Маркерная селекция после каждого возвратного скрещивания позволяет вести наблюдение за дальнейшим распространением желательного генотипа и на основании этого вести селекцию. Посредством маркерной селекции может быть значительно сокращено число необходимых возвратных скрещиваний, не препятствуя при этом симультативной селекции по признакам продуктивности в исходной популяции.
- Нахождение влияния генов на свойства продукции
Путем генной диагностики можно выяснить влияние генов на животноводческую продукцию. Например, влияние казеиновых генов на качество молока.
- Повышение эффективности оценки племенной ценности
При маркерной селекции можно не дожидаться фенотипического проявления, селекция может проводиться уже на эмбриональных стадиях, а для признаков, ограниченных полом, выполняться у обоих полов. Маркерная селекция делает возможным предселекцию индивидуумов, при которой, исходя из продуктивности родоначальниц и продуктивности сибсов, теоретически рассчитывается племенная ценность, и способствует усилению интенсивности селекции и к избеганию нежелательных эффектов селекции.
-Повышение эффекта гетерозиса
Эффект гетерозиса взаимосвязан с долей гетерозиготных генотипов в скрещиваемой популяции. Если известно достаточно полиморфных маркерных генов, то возможна относительно надежная оценка различных скрещиваний по ожидаемой степени гетерозиготности. Эти данные могут быть использованы для отбора пород или линий в программы по скрещиванию. Благоприятные комбинации аллелей могут быть достигнуты посредством соответствующих спариваний. Таким путем впервые удалось предсказать специфическую комбинативную изменчивость. При разведении популяций может использоваться прогнозирование средней степени гетерозиготности потомства от запланированных спариваний.
Маркерная селекция - перспективная отрасль в разведении, позволяющая более достоверно определить генотип интересующих нас животных.
Это позволяет улучшить и ускорить племенную работу, направленную на улучшение хозяйственно-полезных признаков.
Маркерная селекция включает в себя экономические соображения, основы фенотипической селекции, текущее состояние маркеров, состояние генетических карт, методы обнаружения QTL.
Список использованной литературы
1.Кийко Е.И. Принципы маркерной селекции в молочном скотоводств // Вестник ТГУ, т.15, вып. 1, 2010
2. Julius van der Werf. Identifying and incorporating genetic marker and major genes in animal breeding programs. Belo Horizonte - Brasil: 2000
3. Зиновьева Н.А. Молекулярно-генетичсекие методы и их использование в свиноводстве// Достижения науки и техники АПК, № 10, 2008
4. Шендаков А.И, Т.А. Шендакова Генетические аспекты модернизации молочного скотоводства// Вестник ОрегГАУ, №2, 2009
5. Храброва Л.А. Маркер-вспомогательная селекция в коневодстве // Loshadi Creative Team, 2002
7. Аржанкова Ю.В. Использование ДНК-маркеров и дерматологлифического полиморфизма носогубного зеркала в селекции молочных пород скота// диссертация на соискание ученой степени, 2010
8. Elcio P. Guimaraes, John Ruane, Beate D. Scherf, Andrea Sonnino, James D. Dargie Marker-assisted selection, food and agriculture organization of the united nations Rome: 2007
9. Брем Г., Кройслих Х., Штранцингер Г., Экспериментальная генетика в животноводстве. М.:1995.
Подобные документы
Создание Н.И. Вавиловым коллекции семян различных растений. Массовый и индивидуальный отбор растений, явление гетерозиса. Изменение свойств гемозиготных линий. Управление доминированием признаков у гибридов. Значение племенной книги в животноводстве.
презентация [1,8 M], добавлен 27.03.2012
Виды селекции и ее значение. Методы селекции микроорганизмов и животных. Биотехнология, генетическая и клеточная инженерия. Цели и задачи селекции как науки. Процесс одомашнивания новых видов растений и животных для удовлетворения потребностей человека.
курсовая работа [389,3 K], добавлен 10.09.2010
Создания и совершенствования сортов культурных растений и пород домашних животных, применение этих методов в растениеводстве (селекция растений) и животноводстве (селекция животных). Сорта растений и породы животных с нужными биологическими свойствами.
презентация [598,9 K], добавлен 25.10.2011
Задачи современной селекции, породы животных и сорта растений. Центры многообразия и происхождения культурных растений. Основные методы селекции растений: гибридизация и отбор. Самоопыление перекрестноопылителей (инбридинг), сущность явления гетерозиса.
реферат [17,6 K], добавлен 13.10.2009
Отличия животных от растений. Особенности отбора животных для селекции. Что такое гибридизация, ее классификация. Современные разновидности селекции животных. Сферы использования микроорганизмов, их полезные свойства, методы и особенности селекции.
презентация [1022,0 K], добавлен 26.05.2010
Селекция как наука об улучшении уже существующих и о выведении новых сортов растений, пород животных и штаммов микроорганизмов с нужными человеку свойствами, ее цели и задачи, направления развития на сегодня. Сферы использования методов селекции.
презентация [2,4 M], добавлен 18.04.2013
Создание устойчивых к болезням сортов пшеницы, обеспечение длительного сохранения их свойств как актуальная задача селекции. Изучение биохимических механизмов, ответственных за устойчивость; генно-молекулярные технологии, ускоряющие процесс селекции.
В племенном свиноводстве в Европе и Америке начинают применять геномную селекцию. Ее технологии позволяют расшифровать генотип свиней уже при рождении и отбирать для разведения лучших животных. Эта новейшая технология призвана в дальнейшем увеличивать селекционную точность и надежность племенной ценности свиней.
Родоначальником геномной селекции является маркерная селекция.
Маркерная селекция – это использование маркеров для маркирования генов количественного признака, что дает возможность установить наличие или отсутствие в геноме определенных генов (аллелей генов).
Ген - это участок ДНК, определенная последовательность нуклеотидов, в которой закодирована информация о синтезе одной молекулы белка (или РНК), и как следствие, обеспечивающая формирование какого-либо признака и передачу его по наследству.
Гены, представленные в популяции несколькими формами – аллелями – это полиморфные гены. Аллели генов разделяются на доминантные и рецессивные. Полиморфизм генов обеспечивает разнообразие признаков внутри вида.
Однако лишь некоторые признаки находятся под контролем отдельных генов (например, цвет волос). Показатели продуктивности, как правило, являются количественными признаками, за развитие и проявление которых отвечают многие гены. Некоторые из этих генов могут иметь более выраженный эффект. Такие гены называются основными генами локусов количественных признаков (QTL). Локусы количественных признаков (QTL) - участки ДНК, содержащие гены либо сцепленные с генами, лежащими в основе количественного признака.
Первоначально в качестве генетических маркеров использовались морфологические (фенотипические) признаки. Однако очень часто количественные признаки имеют сложный характер наследования, их проявление детерминируется условиями среды и количество маркеров, в качестве которых используются фенотипические признаки, ограниченно. Затем в качестве маркеров использовались продукты генов (белки). Но наиболее эффективно тестировать генетический полиморфизм не на уровне продуктов генов, а непосредственно на уровне генов, то есть использовать в качестве маркеров полиморфные нуклеотидные последовательности ДНК.
Обычно фрагменты ДНК, которые лежат близко друг к другу на хромосоме, передаются по наследству вместе. Это свойство позволяет использовать маркер для определения точной картины наследования гена, который еще не был точно локализован.
Таким образом, маркеры – это полиморфные участки ДНК с известной позицией на хромосоме, но неизвестными функциями, по которым можно выявлять другие гены. Генетические маркеры должны быть легко идентифицируемы, связаны с конкретным локусом и очень полиморфны, потому что гомозиготы не дают никакой информации.
Широкое применение вариантов полиморфизма ДНК в качестве генетических маркеров началось с 1980 г. Молекулярно-генетические маркеры использовались для программ сохранения генофондов пород сельскохозяйственных животных, с их помощью решались задачи происхождения и распространения пород, установления родства, картирования основных локусов количественных признаков, изучения генетических причин наследственных заболеваний, ускорения селекции по отдельным признакам – устойчивости к определенным факторам, по продуктивным показателям. В Европе генетические маркеры начали применяться в селекции свиней еще с начала 1990 гг. для освобождения популяции от гена галотана, который вызывает синдром стресса у свиней.
Очень удобным видом генетических маркеров является SNP (Single Nucleotide Polymorphisms) — снип или однонуклеотидный полиморфизм — это отличия последовательности ДНК размером в один нуклеотид в геноме представителей одного вида или между гомологичными участками гомологичных хромосом индивида. SNP - это точечные мутации, которые могут происходить в результате спонтанных мутаций и действия мутагенов. Различие даже в одну пару оснований может быть причиной изменения признака. SNP широко распространены в геноме (у человека около 1 SNP на 1000 пар оснований). Геном свиньи имеет миллионы точечных мутаций. Никакой другой тип геномных различий не способен обеспечить такую плотность маркеров. Кроме того, SNP имеют низкий уровень мутаций на поколение (~10-8) в отличие от микросателлит, что делает их удобными маркерами для популяционно-генетического анализа. Основным достоинством SNP является возможность использования автоматических методов их детекции, например, использование ДНК-матриц.
Для увеличения количества SNP-маркеров в последнее время ряд зарубежных компаний объединяют свои усилия, создавая единую базу данных, чтобы иметь возможность, протестировав большое количество животных, проверенных по продуктивности на полиморфизм, выявить наличие связей между известными точечными мутациями и продуктивностью.
В настоящее время определено большое количество полиморфных вариантов генов и их взаимовлияние на продуктивные признаки свиней. Некоторые генетические тесты с использованием маркеров, определяющих продуктивные качества, публично доступны и используются в программах разведения. Используя такие маркеры, можно улучшить некоторые продуктивные показатели.
Примеры маркеров продуктивности:
- маркеры плодовитости: ESR – ген эстрогенного рецептора, EPOR – ген рецептора эритропоэтина;
- маркеры устойчивости к заболеваниям – ген рецептора ECR F18;
- маркеры эффективности роста, мясной продуктивности - MC4R, HMGA1, CCKAR, POU1F1.
MC4R - ген рецептора меланокортина 4 у свиней локализован на хромосоме 1 (SSC1) q22-q27. Замена одного нуклеотида А на G приводит к изменению аминокислотного состава МС4-рецептора. В результате происходит нарушение регуляции секреции клеток жировой ткани, что приводит к нарушению липидного обмена и непосредственно влияет на процесс формирования признаков, характеризующих откормочные и мясные качества свиней. Аллель А определяет быстрый рост и большую толщину шпика, а аллель G отвечает за эффективность роста и большой процент постного мяса. Гомозиготные свиньи с генотипом AA достигают рыночного веса на три дня быстрее, чем свиньи гомозиготные по аллелю G (GG), зато у свиней с генотипом GG на 8% меньше сала и отличаются они более высокой конверсией корма.
Также на мясную и откормочную продуктивность влияют и другие гены, контролирующие комплекс сопряженных физиологических процессов. Ген POU1F1 - гипофизарный фактор транскрипции, является регулирующим транскрипционным фактором, детерминирующим экспрессию гормона роста и пролактина. У свиней локус POU1F1 картирован на хромосоме 13. Его полиморфизм обусловлен точечной мутацией, приводящей к образованию двух аллелей – С и D. Наличие в генотипе свиней аллеля С связывают с повышенными среднесуточными привесами и большей скороспелостью.
Также маркеры позволяют тестировать генотип хряков на признаки, ограниченные полом, проявляющиеся только у свиноматок. Это, к примеру, плодовитость (количество поросят на опорос), которые хряк передает потомству. Например, тестирование генотипа хряка по маркерам эстрогенового рецептора (ESR) позволит отбирать тех хряков для разведения, которые передадут дочерям более высокие воспроизводительные качества.
С помощью результатов маркерной селекции можно оценить частоту встречаемости желательных и нежелательных аллелей для породы или линии, проводить в дальнейшем селекцию, чтобы все животные в породе имели только предпочтительные аллели генов.
Перечень маркеров, рекомендованных к использованию, постоянно расширяется.
Рис. 1. Принцип действия олигонуклеотидного биочипа
ДНК-чип представляет собой подложку с нанеcенными на нее ячейками с веществом-реагентом. Исследуемый материал помечают различными метками (чаще флуоресцентными красителями) и наносят на биочип. Как показано на картинке, вещество-реагент - олигонуклеотид - связывает в исследуемом материале - флуоресцентно меченых фрагментах ДНК - только комплементарный фрагмент. В результате наблюдается свечение на этом элементе биочипа.
В 2009 году был расшифрован геном свиньи. Разработан SNP чип ( вариант ДНК-микрочипа ), содержащий 60 000 генетических маркеров генома. Для ускорения исследований были даже созданы специальные роботы для считывания снипов. Образец ДНК свиньи можно тестировать на наличие или отсутствие практически всех важных точечных мутаций, определяющих продуктивные признаки. Таким образом, отбор лучших животных может быть основан на генетических маркерах без измерения фенотипических показателей.
Эти достижения привели к внедрению новой технологии - геномной селекции. Геномная селекция - это тестирование генома сразу по большому количеству маркеров, покрывающих весь геном, так что локусы количественных признаков (QTL) находятся в неравновесном сцеплении хотя бы с одним маркером. В геномной селекции сканирование генома происходит с использованием чипов (матриц) с 50-60 тысячами SNP (которые маркируют основные гены количественных признаков) для выявления однонуклеотидных полиморфизмов вдоль генома животного, определения генотипов с желательным проявлением совокупности продуктивных признаков и оценки племенной ценности животного.
Впервые термин "геномная селекция" был введен Хейли и Вишером в 1998 году. Meuwissen с соавторами в 2001 году разработал и представил методологию аналитической оценки племенной ценности с помощью карты маркеров, охватывающих весь геном.
Практическое применение геномной селекции началось с 2009 года.
С 2009 года крупнейшие компании США (Cooperative Resources International), Нидерландов, Германии, Австралии начали внедрять геномную селекцию в программы разведения КРС. Быки разных пород были генотипированы по более 50 000 SNP.
Генетическая компания Hypor начала использовать геномную селекцию с 2010 года, действуя в тесном сотрудничестве с Центром научных исследований и новых технологий группы Hendrix Genetics (Хендрикс Дженетикс). Hendrix Genetics тестирует более 60 000 SNP маркеров и использует эту информацию для исследования ДНК. Геномный индекс генетического потенциала свиней рассчитывается после анализа 60 000 маркеров генов (снипов) по животному. В теории, если достаточно генетических маркеров, чтобы охватить все ДНК свиньи (ее генома), возможно описать все генетические вариации для всех измеряемых признаков. Готовится современное математико-генетическое программное обеспечение для обработки данных.
Геномная селекция – это мощный инструмент для использования в будущем. В настоящее время эффективность геномной селекции ограниченна различным характером взаимодействия между локусами количественных признаков, изменчивостью количественных признаков у разных пород, влиянием на проявление признака факторов внешней среды. Но результаты исследований во многих странах подтвердили, что использование статистических методов совместно с геномным сканированием увеличивает надежность прогноза племенной ценности.
Селекция свиней с помощью статистических методов по некоторым показателям (например сопротивляемости заболеваниям, качеству мяса, плодовитости) характеризуется низкой эффективностью. Это происходит вследствие следующих факторов:
- низкой наследуемости признаков,
- большого влияния на этот признак факторов внешней среды,
- из-за проявления, ограниченного полом,
- проявления признака только под действием определенных факторов,
- когда проявление признака происходит относительно поздно,
- вследствие того, что характеристики трудно измерить (например, особенности здоровья),
- наличие скрытых носителей-признаков.
Например, такой порок свиней как стресс-чувствительность трудно поддается диагностике и проявляется в повышенной смертности поросят под воздействием стресса (перевозки и др.) и ухудшении качества мяса. ДНК-тестирование с использованием маркеров генов дает возможность выявить всех носителей этого порока, в том числе скрытых, и с учетом этого проводить селекцию.
Для оценки показателей продуктивности трудно поддающихся прогнозу статистическими методами для более достоверной их оценки нужен анализ потомства, то есть необходимо дождаться приплода и проанализировать его племенною ценность. А использование ДНК-маркеров дает возможность проанализировать генотип сразу при рождении, не дожидаясь проявления признака или появления потомства, что значительно ускоряет селекцию.
Индексная оценка животных осуществляется по экстерьеру и по продуктивным качествам (скороспелость поросят и т.д.). В обоих случаях пользуются фенотипическими показателями, поэтому для использования этих признаков в расчётах необходимо знать их коэффициент наследуемости. Однако даже в таком случае мы будем иметь дело с вероятностью генетического обоснования любого признака, усредненными показателями его предков и потомков (нет возможности определить, какие гены унаследовало молодое животное: лучшие или худшие этого среднего). С помощью анализа генотипа можно точно установить факт наследования определенных генов уже при рождении, оценивать генотипы напрямую, а не через фенотипические проявления.
Однако если отбор свиней идет по показателям, характеризующимся высокой наследуемостью, как например, легко исчисляемое количество сосков, геномная селекция не принесет существенной выгоды.
Маркерная селекция не отрицает традиционных подходов к определению племенной ценности. Статистический анализ и технологии геномной селекции взаимно дополняют друг друга. Использование генетических маркеров позволяет ускорить процесс отбора животных, а индексные методы - точнее оценить эффективность этого отбора.
Геномная селекция – это возможность сделать свиноводство точным производством. Использование технологий геномной селекции позволит производить разнообразные мясные продукты, соответствующие запросу потребителей.
Перепубликация материалов данного сайта разрешена только при указании гиперсcылки на источник информации!
В условиях перехода экономики России на рыночные отношения первостепенное значение должно приобретать производство качественной продукции свиноводства, что возможно при наличии животных с высоким генетическим потенциалом, который формируется целенаправленной селекционной работой. Как показал опыт отечественных и зарубежных ученых, эффективность племенной работы с животными можно повысить путем совершенствования ее методов на основе использования различных генетических маркеро
Содержание
Работа состоит из 1 файл
Свиньи.doc
Содержание:
1. Введение…………………………………………………. ….…… 3
2. Генетические маркеры в селекции свиней………………….…… 4
3. Типы маркеров..……………………. ……………………… ……. 7
4. Заключение…………………………….…………………… ……. 12
Библиографический список……….…………………………. ……. 13
В условиях перехода экономики России на рыночные отношения первостепенное значение должно приобретать производство качественной продукции свиноводства, что возможно при наличии животных с высоким генетическим потенциалом, который формируется целенаправленной селекционной работой. Как показал опыт отечественных и зарубежных ученых, эффективность племенной работы с животными можно повысить путем совершенствования ее методов на основе использования различных генетических маркеров. Выявление таких маркеров на основе экспериментальных исследований, мониторинг различных пород свиней, их популяционно-генетический анализ, изучение роли генетических маркеров в микроэволюционных процессах с целью совершенствования селекционного процесса являются важными условиями в работе с этим видом животных. Эффект селекции во многом зависит от рационального использования имеющихся в той или иной стране генетических ресурсов.
Столетиями методами народной селекции создавались генетически разнообразные породы свиней. В течение последних столетий эти породы были отселекционированы с учетом различных национальных культур, внешних условий среды, задач и потребностей человеческого общества. На основе биоразнообразия, существующего в пределах вида, в большинстве стран мира были созданы уникальные породы свиней. Так например, по данным ФАО, в мире существует 350 пород свиней, при этом только в одном Китае насчитывается 66 пород, из которых 48 – местной популяции, 12 выведены недавно с использованием западных пород и 6 импортированы из Европы и Америки.
2. Генетические маркеры в селекции свиней.
История интенсивного изучения и использования генетических маркеров в популяциях свиней насчитывает более 35 лет. В развитых странах мира в области свиноводства данные системы с целью получения качественной конечной продукции или искоренения наследственных болезней используются достаточно широко.
В настоящее время все генетические маркеры принято классифицировать на 3 большие группы.
Генетические маркеры I порядка (группы крови, полиморфизм белков и ферментов крови, полиморфизм белков молока, антигены главного комплекса гистосовместимости I класса - SLA класс 1, антигены тромбоцитов, аллотипы белков сыворотки крови).
К генетическим маркерам II порядка или анонимным генетическим маркерам относятся полиморфные системы ДНК – это микросателлиты и антигены главного комплекса гистосовместимости II класса – SLA класс II.
К генетическим маркерам III порядка относится группа маркирующих систем, выявляющих такие гены, которое связаны с хозяйственно полезными признаками или наследственными заболеваниями: ген злокачественного гипертермического синдрома – MNS-ген; ген, ответственный за вкусовые качества мяса – RN-ген, или ген Наполи; гены, ответственные за высокую плодовитость – ESR и PRLR-гены; гены внутримышечного жира – HFABP и AFABP-гены и др.
Из генетических маркеров I порядка хорошо изучены группы крови у свиней. В настоящее время к ним относятся 16 систем групп крови, объединяющих 77 антигенов и 81 простых и сложных аллелей. По полиморфным белкам описано 58 локусов, из них 24 в плазме крови, 18 в эритроцитах и лейкоцитах, 7 в молоке и 9 в других биологических жидкостях и тканях организма. Локусы полиморфных систем кодируют белки, выполняющие определенные функции в организме свиней и в большинстве случаев существует их гомология по расположению с другими видами млекопитающих, что имеет немаловажное значение при характеристике картированных генов. Большинство полиморфных систем является ди- и триаллельными локусами.
В селекционной практике применение этих маркеров носит ограниченный характер из-за низкой степени биохимического полиморфизма у большинства пород и видов сельскохозяйственных животных или в силу трудоемкости их исследования. Проведенный анализы показали, что средний уровень гетерозигощости в популяциях на основе 30 локусов белков составил 6%. Такую цифру можно считать существенно заниженной по сравнению с истинной гетерозиготностью популяций.
Начало нового этапа генетических исследований наступило с введением в практику полиморфизма ДНК-маркеров, что было связано с выходом основополагающей работы Д.Ботштейна и др. (1980). Авторы описали применение полиморфизма длин рестриктных фрагментов (ПДРФ) для построения генетической карты человека. Данная работа положила основу создания молекулярно-генетической карты томата, кукурузы, многих видов животных. Но большинство ПДРФ-маркеров является диаллельными, основанными на наличии или отсутствии рестрикционного сайта. Оказалось, что ПДРФ-маркеры включают около 1 % вариабельной ДНК животных. Наиболее информативными оказались открытые в последнее десятилетие маркеры, принадлежащие к повторяющейся фракции геномной ДНК – мини- и микросателлиты, составляющие 30 % эукариотического материала и демонстрирующие необычайно высокий уровень полиморфизма благодаря вариациям в количестве повторенных единиц. Они как раз составляют генетические маркеры II порядка. В настоящее время у свиней открыто около 750 генов микросателлитов, однако для характеристики пород в практике по рекомендации рабочей группы ФАО используют 27 локусов.
С учетом мирового опыта применительно к индустрии свиноводства Российской Федерации с точки зрения научных и прикладных исследований наиболее желательным для диагностики считается ряд генов, ответственных за количественные и качественные признаки.
Например, у свиней к ним относится MHS-ген, вызывающий дряблость, эксудативность получаемой свинины. Вместе с тем правильное использование этого гена позволит получать от гетерозигот нежную свинину. Поэтому такую работу необходимо проводить под жестким генетическим контролем. Другим геном, способным оказать влияние на качество мяса, является RN-ген или Наполи-ген, использование которого позволит своевременно исключать получение "кислой" свинины.
В современных условиях ведения свиноводческой отрасли особое значение приобретают гены, ответственные за нормальную плодовитость (ESR и PRLR) и наличие внутримышечного жира (HFABP и AFABP). Учитывая высокую заболеваемость и отход молодняка до 30 % из-за кишечной инфекции, диагностика генов рецепторов К88АВ, К88АС, а также ЕCF18R позволит вести селекцию на устойчивость к антигену К88 кишечной палочки и диарее, а следовательно – целенаправленно создавать популяции свиней, устойчивых к определенным заболеваниям.
3. Типы маркеров.
Полиморфизм длин рестрикционных фрагментов (ПДРФ). Впервые ПДРФ был использован как генетический маркер в 1974 г. при идентификации термо-чувствительной мутации в геноме аденовируса. Однако широкое применение вариантов полиморфизма ДНК в качестве генетических маркеров началось с 1980 г. после выхода основополагающей работы Ботштейна с соавт. [22], в которой были изучены свойства ПДРФ как генетического маркера, дано теоретическое обоснование его использования и предложен метод оценки уровня информативности. ПДРФ используют для анализа полиморфизма конкретных локусов (генов). Способ анализа ПДРФ сводится к обработке ДНК рестриктазами с последующим электрофоретическим разделением полученной смеси и определением длин рестрикционных фрагментов после блот-гибридизации со специфическим меченым зондом. Так как рестрицирующие эндонуклеазы имеют строго специфические места расщепления, то генетические различия в нуклеотидной последовательности ДНК между индивидуумами (т.е. полиморфизм на уровне ДНК) приведут к различному распределению сайтов рестрикции вдоль соответствующих молекул ДНК и получению продуктов рестрикции, в которых длина гомологичных фрагментов будет различаться. Таким образом, полиморфизм ДНК будет тестироваться как ПДРФ.
Основной причиной, приводящей к возникновению полиморфизма ДНК, первоначально считались точковые мутации (а также микроделеции и инсерции), затрагивающие сайты узнавания тех или иных эндонуклеаз рестрикции. В последующих работах спектр возможных причин был расширен, и в настоящее время основная роль отводится таким факторам, как крупные делеции и вставки, трансверсии, транслокации, транспозиции мобильных генетических элементов и т.п. Кроме того, некоторые рестриктазы не способны расщеплять ДНК, если сайт узнавания содержит один или несколько метилированных цитозиновых остатков.
С использованием ПДРФ-маркеров были получены первые успешные результаты по построению молекулярно-генетических карт многих видов растений и животных, накоплены обширные сведения о генетическом полиморфизме различных организмов, выявлены ассоциации с хозяйственно-полезными признакам. Важным достоинством данного типа маркеров является высокая воспроизводимость результатов, а также кодоминантный тип наследования. ПДРФ-локусы могут обладать множественными аллелями, что повышает их информативность. ПДРФ-анализ митохондриальной ДНК и кластера генов, кодирующих рибосомные РНК (рДНК), широко используется в популяционной генетике, биогеографических и филогенетических исследованиях.
Полиморфизм длин продуктов амплификации (AFLP-маркеры). Для исследования вариабельности генома в целом может быть также использован метод анализа AFLP. Этот метод также не требует ни предварительного клонирования, ни секвенирования ДНК. Особености этого подхода заключаются в использовании в качестве матрицы рестрицированных фрагментов ДНК, лигированных со специфическими олигонуклеотидными адаптерами, и проведении избирательной амплификации со специально сконструированными праймерами. Этот тип полиморфизма ДНК также имеет доминантный тип наследования. AFLP-маркеры часто наследуются как тесно сцепленные кластеры в районе центромеры или теломеры хромосом, но наблюдается и случайное распределение маркеров вне этих кластеров, что позволяет, используя этот подход, быстро генерировать сотни высоковоспроизводимых маркеров. AFLP-маркеры были успешно использованы для геномного картирования в популяционных и филогенетических исследованиях. В последние годы эти маркеры получают все более широкое распространение для исследования мало изученных таксономических групп.
ISSR. Для создания ISSR-маркеров используют праймеры, комплементарные микросателлитным повторам (4-12 единицам повтора) и несущие на одном из концов последовательность из двух-четырех произвольных нуклеотидов (так называемый "якорь"). Такие праймеры позволяют амплифицировать фрагменты ДНК, которые находятся между двумя достаточно близко расположенными микросателлитными последовательностями (как правило, это уникальная ДНК). В результате амплифицируется большое число фрагментов, представленных на электрофореграмме дискретными полосами (ISSR-фингерпринтинг). ISSR-маркеры также относятся к маркерам доминантного типа наследования, полиморфизм которых тестируется по наличию/отсутствию полосы. Метод обладает хорошей воспроизводимостью и наряду с AFLP может быть с успехом использован для выявления межвидовой и внутривидовой генетической изменчивости, идентификации видов, популяций, линий, а в ряде случаев и для индивидуального генотипирования. ISSR-маркеры могут быть использованы также для картирования геномов и маркирования хозяйственно-полезных признаков.
Микросателлиты – первые, полученные с использованием ПЦР, высокополиморфные маркеры для индивидуальных локусов. Подобно минисателлитам, микросателлиты относятся к диспергированным тандемно повторяющимся последовательностям, но единицы повторов (ди-, три- и тетрануклеотиды) и общий размер повторяющейся области существенно короче (как правило, не более 100 п.н.). Эти маркеры известны под несколькими названиями: микросателлиты, STMS, STR, SSR. По аналогии с системой STS была предложена система STMS, которая фактически является частью системы STS. Для создания STR подбираются праймеры к уникальным последовательностям ДНК, фланкирующим микросателлитный повтор, что требует предварительного знания их нуклеотидной последовательности. Полиморфизм STR определяется различной копийностью мономерных единиц в кластере, что приводит к существованию множественных аллельных вариантов. Гетерозиготность их очень высока (часто более 75%). При создании новых полиморфных маркеров, кроме динуклеотидов, используются микросателлиты три- и тетрамерных мотивов, значительная часть которых также высокогетерозиготна. Благодаря большей длине звена, применение тримеров и тетрамеров позволяет упростить методику анализа аллельного полиморфизма.
Несмотря на высокую популярность микросателлитов, они имеют и некоторые недостатки. Неравномерность скорости мутирования разных микросателлитов создает определенные сложности для популяционно-генетического анализа. Имеются и технические проблемы, такие как артефакты при проведении ПЦР (за счет эффекта "проскальзывания"), сложности в разработке технологий для автоматического скрининга микросателлитных аллелей. Кроме того, несмотря на высокую плотность микросателлитных локусов в геноме, их бывает недостаточно для тонкого картирования отдельных областей геномов, создания маркеров для локусов количественных признаков (QTL) и решения многих других задач.
Полиморфные маркеры, основанные на тестировании однонуклеотидных замен (SNPs) – это однонуклеотидные позиции в геномной ДНК, для которых в популяции имеются различные варианты последовательностей (аллели) с частотой редкого аллеля не менее 1%. Основным достоинством SNPs является возможность использования автоматических методов их детекции, например, использование ДНК-микропанелей. Существующие способы тестирования SNPs можно условно разделить на несколько групп, но разделение условно, поскольку в большинстве случаев используются сочетания различных подходов.
STSs-маркеры. Первая попытка систематизации ДНК-маркеров была предложена в 1989 году Ольсоном с соавторами. Им была сформулирована идея создания системы STS-маркеров, которая была призвана стандартизовать все обозначения маркированных последовательностей ДНК в геноме и включить в себя все типы картированных последовательностей. Первоначально STS-маркеры создавались на основе различных технологий, но впоследствии был осуществлен перевод практически всех STSs на основу ПЦР для более удобного использования. Основные требования к STSs - знание их нуклеотидной последовательности и уникальность в геноме. STSs можно рассматривать как мономорфные ДНК-маркеры, поскольку их используют в экспериментах, где наличие полиморфизма не требуется, в таких, например, как построение физических карт геномов или выявление тестируемых последовательностей в рекомбинантных клонах или генетически модифицированных организмах.
Любая специализирующаяся на племенном свиноводстве компания стремится к совершенствованию животных путем улучшения показателей в каждом новом поколении, тем самым ужесточая отбор и требования к генетике. При существующем темпе развития производства и численности поголовья эта задача невыполнима без внедрения современных методов ведения селекции.
- Необходимость подавляющего использования импортных хряков-производителей для поддержания генетического потенциала продуктивности маточного стада
- Необходимость использования зарубежных систем сопровождения селекционно-племенной работы без доступа к базам данных и без раскрытия сути используемых алгоритмов (BLUP-AM)
- Ведение племенного учета на современном уровне
- Использование хряков собственного воспроизводства
- Внедрение BLUP-оценки племенной ценности
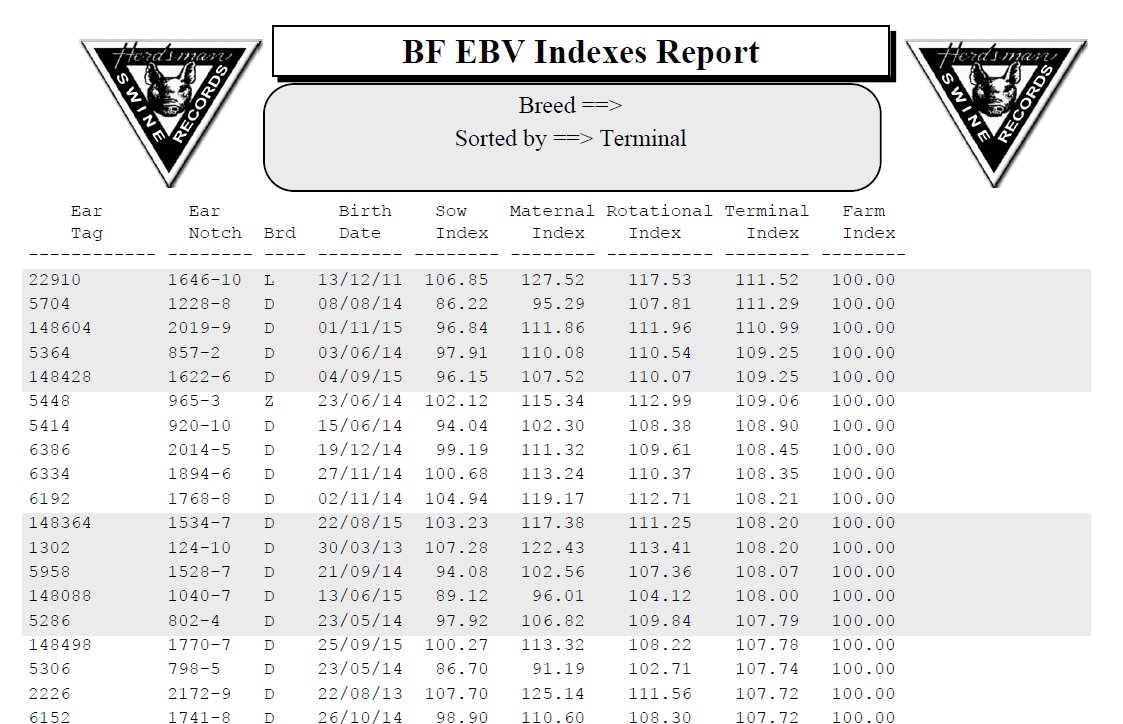
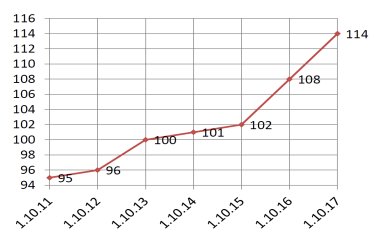
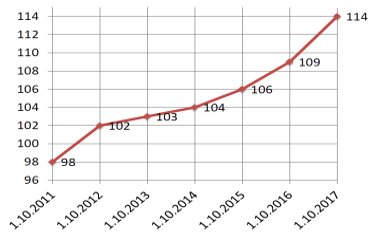
Первоначально ООО СГЦ использовал для племенного учета программу FIAS (Федеральная информационно-аналитическая система управления селекционно-племенной работой), которая предусматривает линейное разведение. Так как её возможностей оказалось недостаточно для четкой оценки генетического потенциала животных, в дальнейшем была приобретена программа Herdsman-2000, работающая по методу построения математических моделей и рассчитывающая индексы племенной ценности каждого животного. Одновременно с внедрением новой программы, началось формирование базы ДНК поголовья в ФГБНУ ФНЦВИЖ им. Л.К.Эрнста.
Одним из главных преимуществ программы Herdsman-2000 является возможность самостоятельной работы с ней без поддержки зарубежных компаний. Для нашей компании было важно совместить линейное разведение по FIAS и индексную оценку животных с помощью BLUP, отбирая из веток животных с высоким генетическим потенциалом. Кроме того, для осуществления грамотного ведения племенного учета на каждой площадке установлена программа FARM, в которой отображены все технологические процессы индивидуально по каждому животному, а также все основные формы бухгалтерского учета.
Использование хряков собственного воспроизводства – одна из главных предпосылок для работы с геномной селекцией. Такой подход позволяет избежать зависимости от поставляющих племенных животных зарубежных компаний. При ежемесячном тестировании 600 голов ремонтных хрячков для отправки на ПИО отбираются 1-2% самых лучших, которые будут обеспечивать генетический рост и гарантируют увеличение показателей, а полученное от них потомство даст дополнительный материал для исследований.
В начале 1970-х годов профессором К.Р. Хендерсоном из Корнельского университета был разработан метод BLUP (Best Linear Unbiased Prediction — наилучший линейный несмещенный прогноз). Изначально речь шла только о теоретической модели, абсолютно неприемлемой для практического применения. Использование BLUP в селекционной практике началось после корректировки методов расчета и разработки моделей, позволяющих наилучшим образом осуществлять разделение изменчивости продуктивных признаков на генетическую и средовую составляющие.
Следует различать статистический метод BLUP и модель, которая используется для описания данных. Метод представляет собой способ расчета, учитывающий в оцениваемых значениях влияние причинных факторов. Модель описывает, какие причинные факторы оказывают влияние на продуктивность.
Для расчета племенной ценности животного на основе BLUP используются различные модели. Наиболее современной и эффективной формой BLUP-оценки племенной ценности является так называемая модель животного. В такой модели для каждого хряка, свиноматки или потомка решается уравнение. Так как каждое животное представлено своим собственным уравнением, то не происходит потери информации, а уровень спаривания перестает играть какую-либо роль.
Главная / Технологии животноводства / Технологии будущего: маркерная и геномная селекция в животноводстве
В 1983 году американский ученый Кэри Муллисон изобрел технологию полимеразной цепной реакции. Она позволяла из небольших участков ДНК клонировать заданное число их копий. С помощью этой технологии ученые смогли изучать непосредственно ДНК живых организмов. Это дало толчок развитию маркерной и геномной селекции, которые с недавних пор внедряются в сельское хозяйство.

В России эту технологию изучают в научно-исследовательском центре геномной селекции, созданном на базе Белгородского государственного национально-исследовательского университета в 2017 году.
Руководитель центра Эдуард Снегин рассказал, какое практическое применение нашли маркерная и геномная селекция в сельском хозяйстве, и как построено сотрудничество центра с сельхозпроизводителями.
Эдуард Анатольевич, что такое маркерная технология и геномная селекция? В чем их различие?
- Маркерная селекция подразумевает отбор животных по отдельно взятым генам-маркерам, контролирующим различные значимые признаки: рост, вес, скорость роста, плодовитость и устойчивость к заболеваниям. Но геном — очень сложная скоординированная система, где все гены связаны между собой. Поэтому отбор по отдельно взятым генам-маркерам всегда сопровождался сложностью оценки их взаимодействия. Из-за этого маркерная селекция перестала удовлетворять запросы современных аграриев и науки в целом, что дало толчок развитию геномной селекции.
Она по своей сути похожа на маркерную, но если маркерная технология позволяет вести селекционный отбор только по отдельным генам, то геномная – по их комплексам, включающим сотни, тысячи и даже десятки тысяч генов.
Давно ли эти технологии пришли в Россию и как они развиваются сейчас?
- В мире развитие маркерной и геномной технологии началось в 90-е годы, после изобретения полимеразной цепной реакции Кэри
Муллисоном. Тогда же технология появилась и в России. На первых порах реактивы и оборудование нужно было завозить исключительно из-за рубежа, и в силу финансовых трудностей многие отечественные генетические лаборатории не могли позволить себе заниматься ДНК-технологиями в полной мере, как это происходило в США и странах Европы.
Тем не менее постепенно в России стали открываться собственные предприятия по производству реактивов и других расходных материалов, были налажены поставки относительно недорогих и качественных приборов и комплектующих из других стран и система грантовой поддержки научных лабораторий и институтов. Поэтому технология ПЦР стала вполне доступной даже для малобюджетных лабораторий.
Еще одним препятствием к интенсивному внедрению геномных технологий в России стало интенсивное освоение нашего сельхозрынка западными компаниями. Многие предприятия закупают скот за рубежом. При этом контракты составляются таким образом, что российский сельхозпроизводитель не имеет право проводить собственные селекционные мероприятия с закупленным поголовьем. Если он и проводит селекционную работу, то только по прямым указаниям зарубежных специалистов, которые крайне не заинтересованы в развитии этих технологий у нас в стране и всячески этому противодействуют.
Впрочем, сейчас эти технологии активно развиваются. Мы, например, сотрудничаем с более чем 50 хозяйствами со всей страны: от Бурятии до Калининграда.
Одинаковыми ли темпами развиваются маркерная и геномная селекция в животноводстве и растениеводстве?
- На сколько мне известно, геномные технологии активно развиваются в обоих направлениях. Однако в связи с довольно сложным геномом растений работа там идет чуть медленнее. Например, размер генома пшеницы - 17 миллиардов пар нуклеотидов, а коровы - около 3 миллиардов. Но в связи с интенсивным развитием приборной базы и компьютерных технологий эти различия постепенно нивелируются.
Как эти технологии применяются на практике? Какую пользу от них могут получить аграрии в животноводстве.
- Наша работа заключается в расшифровке генов животных. Ген, как мы знаем, это участок ДНК, определенная последовательность нуклеотидов, в которой закодирована информация о синтезе одной молекулы белка (или РНК), и которая обеспечивает формирование какого-либо признака и передачу его по наследству.
Гены в популяции, если говорить простым языком, имеют несколько форм – аллелей, от которых зависит, какой именно признак передается. Такие гены называются полиморфными, и именно они обеспечивают разнообразие внутри вида. Однако лишь некоторые признаки находятся под контролем отдельных генов (например, окрас). Показатели продуктивности, как правило, являются количественными признаками, за развитие и проявление которых отвечают сразу несколько генов.
Для работы мы используем специальное устройство – секвенатор, с помощью которого автоматически определяется последовательность нуклеотидов в цепи ДНК. То есть, мы можем расшифровать ДНК конкретного животного, определить те самые аллели, которые отвечают за разные признаки.
Затем проводим отбор животных, у которых проявляются положительные признаки, например, высокая продуктивность, и отбраковываем тех, кто не удовлетворяет нас по характеристикам. На основе этих исследований мы рассчитываем индекс генетической племенной ценности – крайне важный показатель для хозяйств.
Соответственно, животные с хорошим индексом оставляются на фермах, с низким – отбраковываются.
Это очень важно, поскольку имеет экономический эффект. Представьте, что целый год в хозяйстве кормят и поят корову, а она потом рождает теленка с плохой мутацией. Это – деньги на ветер.
Мы также советуем хозяйствам, как проводить скрещивание так, чтобы мутация, даже если она есть у животного, не проявилась в потомстве. То есть, подбирается, например, бык, у которого нет точно такой же мутации, как и у коровы. Получается, что племенные хозяйства с нашей помощью могут проводить мониторинг и отбирать костяк для создания здорового, высокопродуктивного стада.
Я считаю, что традиционные методы селекции экономически неэффективны и требуют существенных временных и денежных затрат для получения нужного результата. Опыт десятков отечественных агрохолдингов показал, что сохранение высокой продуктивности животных даже импортной селекции в последующих поколениях невозможно из-за несовершенных методов оценки генотипа и ошибок при выборе из общего массива стада особей для чистопородного разведения.
С помощью геномных технологий сроки выведения новых пород, да и просто создания высокопродуктивных стад сокращается в разы, а затраты уменьшаются на 90 %. Именно поэтому в западных странах геномные технологии развиваются очень интенсивно.
Не встретят ли эти технологии сопротивления со стороны общественности, как, например, в случае с генно-модифицированными продуктами?
- Хочу подчеркнуть, что геномная селекция никоим образом не связана с какими-то искусственными манипуляциями с генами. В ходе геномной
селекции не происходят вставки чужеродных генов в организмы (создание ГМО), а также не осуществляется процедура редактирования генома (технологии CRISPR). В методах геномной селекции генетик-селекционер работает с тем материалом, который дала природа. На основе современных технологий анализа ДНК и методов биоинформационной обработки полученных данных ведется более грамотный подбор производителей для скрещивания и эффективный отбор наиболее ценных животных. Поэтому людям опасаться за свое здоровье в данном случае не стоит.
Кроме того, сейчас для многих стало очевидным, что для сохранения продовольственной безопасности страны технологии геномной селекции необходимо активно продвигать не только в научном сообществе, но и на законодательном уровне. Например, в поощрении государством тех предприятий, которые решаться на использование этих технологий.
За консультацией по вопросам генетической селекции в сфере животноводства можно обращаться к специалистам НИЦ геномной селекции НИУ "БелГУ":
Читайте также:

