Доклад по биологии 5 класс кислород
Обновлено: 17.05.2024
Кислород — самый распространённый в земной коре элемент, на его долю (в составе различных соединений, главным образом силикатов) приходится около 47 % массы твёрдой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 85,82 % (по массе). Более 1500 соединений земной коры в своём составе содержат кислород.
| Вложение | Размер |
|---|---|
| biologicheskaya_rol_kisloroda1.docx | 30.78 КБ |
Предварительный просмотр:
Кафедра аналитической химии
студент 1 курса
104 группы специальность
Кандидат химических наук
Гурвич Людмила Говсеевна
Саранск 2015-2016 год
Введение
Кислоро́д — элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 8. Обозначается символом O (лат. Oxygenium). Кислород — химически активный неметалл, является самым лёгким элементом из группы халькогенов. Простое вещество кислород (CAS-номер: 7782-44-7) при нормальных условиях — газ без цвета, вкуса и запаха, молекула которого состоит из двух атомов кислорода (формула O2), в связи с чем его также называют дикислород. Жидкий кислород имеет светло-голубой цвет, а твёрдый представляет собой кристаллы светло-синего цвета.
История открытия кислорода.
Официально считается, что кислород был открыт английским химиком Джозефом Пристли 1 августа 1774 года путём разложения оксида ртути в герметично закрытом сосуде (Пристли направлял на это соединение солнечные лучи с помощью мощной линзы).
2HgO (t) → 2Hg + O 2 ↑
Важным этапом, который способствовал открытию кислорода, были работы французского химика Петра Байена, который опубликовал работы по окислению ртути и последующему разложению её оксида.
Наконец, окончательно разобрался в природе полученного газа А. Лавуазье, воспользовавшийся информацией от Пристли и Шееле. Его работа имела громадное значение, потому что благодаря ей была ниспровергнута господствовавшая в то время и тормозившая развитие химии флогистонная теория. Лавуазье провел опыт по сжиганию различных веществ и опроверг теорию флогистона, опубликовав результаты по весу сожженных элементов. Вес золы превышал первоначальный вес элемента, что дало Лавуазье право утверждать, что при горении происходит химическая реакция (окисление) вещества, в связи с этим масса исходного вещества увеличивается, что опровергает теорию флогистона.
Таким образом, заслугу открытия кислорода фактически делят между собой Пристли, Шееле и Лавуазье.
Нахождение в природе
Кислород — самый распространённый в земной коре элемент, на его долю (в составе различных соединений, главным образом силикатов ) приходится около 47 % массы твёрдой земной коры . Морские и пресные воды содержат огромное количество связанного кислорода — 85,82 % (по массе). Более 1500 соединений земной коры в своём составе содержат кислород.
В атмосфере содержание свободного кислорода составляет 20,95 % по объёму и 23,10 % по массе (около 10 15 тонн). Однако до появления первых фотосинтезирующих архей 3,5 млрд лет назад в атмосфере его практически не было. Свободный кислород в больших количествах начал появляться в палеопротерозое (3-2,3 млрд лет назад) в результате глобального изменения состава атмосферы ( кислородной катастрофы ). Первый миллиард лет практически весь кислород поглощался растворённым в океанах железом и формировал залежи джеспилита . 3—2,7 млрд лет назад он начал выделяться в атмосферу и 1,7 млрд лет назад достиг 10 % от нынешнего уровня.
Наличие большого количества растворённого и свободного кислорода в океанах и атмосфере привело к вымиранию большинства анаэробных организмов. Тем не менее, клеточное дыхание с помощью кислорода позволило аэробным организмам производить гораздо больше АТФ, чем анаэробным, сделав их доминирующими.
С начала кембрия 540 млн лет назад содержание кислорода колебалось от 15 % до 30 % по объёму. К концу каменноугольного периода (около 300 миллионов лет назад) его уровень достиг максимума в 35 % по объёму, который, возможно, способствовал большому размеру насекомых и земноводных в это время.
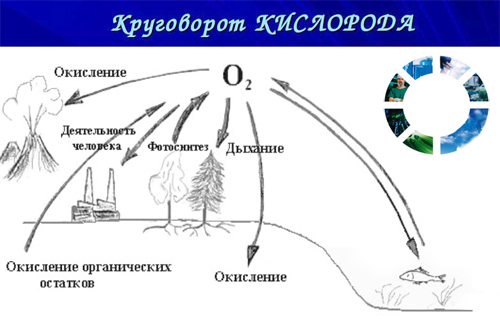
Основная часть кислорода на Земле выделяется фитопланктоном Мирового океана. При этом, около 60 % кислорода, производимого лесами и зелёными растениями, расходуется на процессы гниения и разложения в самих лесах и растительных зонах.
Деятельность человека очень мало влияет на количество свободного кислорода в атмосфере. При нынешних темпах фотосинтеза понадобится около 2000 лет, чтобы восстановить весь кислород в атмосфере.
Кислород входит в состав многих органических веществ и присутствует во всех живых клетках. По числу атомов в живых клетках он составляет около 25 %, по массовой доле — около 65 %.
Биологическая роль кислорода
Кислород — самый распространенный на Земле элемент, на его долю (в
составе различных соединений, главным образом силикатов), приходится около 47,4% массы твердой земной коры. Морские и пресные воды содержат огромное количество связанного кислорода — 88,8% (по массе), в атмосфере содержание свободного кислорода составляет 20,95 % (по объему). Элемент кислород входит в состав более 1 500 соединений земной коры.
Кислород в атмосфере Земли начал накапливаться в результате деятельности первичных фотосинтезирующих организмов, появившихся, вероятно, около 2,8 млрд. лет назад. Полагают, что 2 млрд. лет назад атмосфера уже содержала около 1% кислорода; постепенно из восстановительной она превращалась в окислительную и примерно 400 млн. лет назад приобрела современный состав.Наличие в атмосфере кислорода в значительной степени определило характер биологической эволюции. Аэробный (с участием О2) обмен веществ возник позже анаэробного (без участия О2), но именно реакции биологического окисления,более эффективные, чем древние энергетические процессы брожения и гликолиза, снабжают живые организмы большей частью необходимой им энергии. Исключение составляют облигатные анаэробы, например, некоторые паразиты, для которых кислород является ядом. Использование кислорода, обладающего высоким окислительно-восстановительным потенциалом, в качестве конечного акцептора электронов в цепи дыхательных ферментов, привело к возникновению биохимического механизма дыхания современного типа. Этот механизм и обеспечивает энергией аэробные организмы.
Кислород — основной биогенный элемент, входящий в состав молекул всех важнейших веществ, обеспечивающих структуру и функции клеток — белков, нуклеиновых кислот, углеводов, липидов, а также множества низкомолекулярных соединений. В каждом растении или животном кислорода гораздо больше, чем любого другого элемента (в среднем около 70%). Мышечная ткань человека содержит 16% кислорода, костная ткань — 28.5%; всего в организме среднего человека (масса тела 70 кг) содержится 43 кг кислорода. В организм животных и человека кислород поступает в основном через органы дыхания (свободный
кислород) и с водой (связанный кислород). Потребность организма в кислороде определяется уровнем (интенсивностью) обмена веществ, который зависит от массы и поверхности тела, возраста, пола, характера питания, внешних условий и др. В экологии как важную энергетическую характеристику определяют отношение суммарного дыхания (то есть суммарных окислительных процессов) сообщества организмов к его суммарной биомассе.
Небольшие количества кислорода используют в медицине: кислородом (из так называемых кислородных подушек) дают некоторое время дышать больным, у которых затруднено дыхание. Нужно, однако, иметь в виду, что длительное вдыхание воздуха, обогащенного кислородом, опасно для здоровья человека. Высокие концентрации кислорода вызывают в тканях образование свободных радикалов, нарушающих структуру и функции биополимеров. Сходным действием на организм обладают и ионизирующие излучения. Поэтому понижение содержания кислорода (гипоксия) в тканях и клетках при облучении организма ионизирующей радиацией обладает защитным действием — так называемый кислородный эффект. Этот эффект используют в лучевой терапии: повышая содержание кислорода в опухоли и понижая его содержание в окружающих тканях усиливают лучевое поражение опухолевых клеток и уменьшают повреждение
здоровых. При некоторых заболеваниях применяют насыщение организма кислородом под повышенным давлением — гипербарическую оксигенацию. Аварийный запас кислорода в бомбоубежище.
Общая характеристика кислорода
Кислород является элементом XVI группы II периода периодической системы химических элементов Д.И. Менделеева, имеет атомный номер 8 и атомную массу 15,9994. Принято обозначать кислород символом О (от латинского Oxygenium – порождающий кислоту). В русском языке название кислород стало производным от кислоты, термина, который был введён М.В. Ломоносовым.

Нахождение в природе
Кислород является самым распространённым элементом по нахождению в земной коре и Мировом океане. Соединения кислорода (в основном – силикаты) составляют не менее 47% массы земной коры, кислород вырабатывается в процессе фотосинтеза лесами и всеми зелёными растениями, большая часть приходится на фитопланктон морских и пресных вод. Кислород – обязательная составная часть любых живых клеток, также находится в большинстве веществ органического происхождения.
Физические и химические свойства
Кислород – лёгкий неметалл, состоит в группе халькогенов, имеет высокую химическую активность. Кислород, как простое вещество, представляет собой газ без цвета, запаха и вкуса, имеет жидкое состояние – светло-голубая прозрачная жидкость и твёрдое – светло-синие кристаллы. Состоит из двух атомов кислорода (обозначается формулой О₂).
Полезные свойства кислорода и его влияние на организм

Биологическая роль кислорода
Кислород – основа основ жизнедеятельности всех живых организмов на Земле, является основным биогенным элементом. Находится в составе молекул всех важнейших веществ, которые отвечают за структуру и функции клеток (липиды, белки, углеводы, нуклеиновые кислоты). Каждый живой организм содержит гораздо больше кислорода, чем какого-либо элемента (до 70%). Для примера, организм взрослого среднестатического человека массой 70 кг содержит 43 кг кислорода.
Кислород поступает в живые организмы (растения, животные и человек) благодаря органам дыхания и поступлению воды. Помня о том, что в организме человека самый главный орган дыхания – это кожа, становится понятно, сколько кислорода может получать человек, особенно летом на берегу водоёма. Определить потребность человека в кислороде достаточно сложно, ведь она зависит от многих факторов – возраст, пол, масса и поверхность тела, система питания, внешняя среда и т.д.
Применение кислорода в жизни
Кислород применяется практически повсеместно – от металлургии до производства ракетного топлива и взрывчатых веществ, применяемых для дорожных работах в горах; от медицины до пищевой промышленности.

Научные доклады
Когда и кто открыл кислород?
Химические и физические свойства кислорода
В химии элемент образовывает 2 простых вещества — кислород О2 и О3. Газ О2 не имеет ни запаха, ни цвета. Его молекула притягивается магнитом, так как содержит 2 неспаренных электрона. Атмосферный кислород состоит из двухатомных молекул. В каждой молекуле имеются 2 неспаренных электрона. Молекула инертна и устойчива к высокой энергии активации.
Существуют модификации кислорода: жидкий голубой кислород, твердый кислород. Высокая химическая прочность связи между атомами приводит к тому, что газообразный кислород при комнатной температуре становится малоактивным. В природе он является важным участником процессов превращения и гниения. Интересно, что данный элемент при комнатной температуре реагирует с кровяным гемоглобином. Это обеспечивает транспортабельность кислорода ко всем органам организма.
Со многими веществами может вступать в связь без предварительного нагревания (с щелочноземельными и щелочными металлами, белым фосфором и альдегидами). При этом на поверхности изделий образуется ржавчина. При малейшем нагревании кислород повышает свою химическую активность. С водородом, горючими газами, метаном, простыми и сложными веществами кислород реагирует взрывом.
Изотопный состав элемента изменяется в зависимости от природных условий – он либо обогащается тяжелыми металлами, либо обедняется ими. Очень часто кислород выступает в роли окислителя. В процессе реакции выделяется свет и тепло. Из кислорода в естественных условиях на высоте 10—30 км, при грозовых разрядах, образуется озон (03). Он защищает планету от ультрафиолетового излучения и используется для очищения питьевой воды.
Как мы уже упоминали, кислород – это окислитель. Если окисляемый металл характеризуется высокой летучестью, то процесс происходит как горение с образованием оксида. Эффективность реакции зависит от восстановительной активности. При этом оксиды, выделяемые в процессе, могут быть кислотными, амфотерными и основными. Иногда при горении образуются пероксиды и надпероксиды.
Где применяется кислород?
Кислород используется в черной и цветной металлургии. Он интенсифицирует пирометаллургические и гидрометаллургические процессы. Благодаря элементу научились извлекать из руд золото. Это трудоемкая операция, но благодаря кислороду она протекает значительно быстрее. Также он применяется в химической промышленности, на нужды которой расходуется 30% производящего кислорода. Элемент берет участие в термоокислительном крекинге, когда получается ацетилен – вещество для сварки и резки металлов, для синтезов органических веществ.
Кислород применяется в космосе. Он выступает окислителем в двигателях космических кораблей второй ступени и в ракетах высотных исследований. В составе взрывчатых веществ находится жидкий кислород. Также он применяется в авиации и медицине. Когда затруднительное дыхание, при сердечных и легочных заболеваниях, то больным из кислородных подушек подают кислород.

Бесплатное участие. Свидетельство СМИ сразу.
До 500 000 руб. ежемесячно и 10 документов.
Кислород слово заимствованное из французской терминологии, а точнее берет свое начало от первичного (ошибочного) представления о том, что кислород находится во всех кислотах. В связи с этим выдающийся химик Франции А. Л. Лавуазье предложил термин "оксиген" (на франц. oxygene), который, в свою очередь, происходит от древнегреческого слова "oxygenium" и означает "рождающий кислоту" (oxys кислый, genos рождение). В русском языке элемент первоначально именовался "кислотвором", позднее образовалось и "прижилось" слово "кислород". Вся зелень планеты за один только год образует приблизительно 3 триллиона тонн кислорода. Однако его содержание в атмосфере составляет на сегодняшний день 21% (в городахмегаполисах и вовсе 18%), в то время как несколько миллионов лет назад концентрация была почти в 2 раза выше 3740%. Количество кислорода в воздухе ниже 8% считается угрозой для жизни. В год одно дерево может вырабатывать до 125 кг. кислорода. Этого вполне достаточно, чтобы обеспечить свежим воздухом 2х человек. Если наша планета лишится кислорода хотя бы на несколько секунд, то произойдет множество страшных явлений: дневное небо сразу потемнеет; земная кора начнет лопаться; вода превратится в пар (водород попросту станет газообразным); бетонные сооружения превратятся в руины. А все потому, что кислород важная составляющая всего перечисленного. Рыбам не требуется большого количества кислорода. Но мало кто знает, что и среди них есть привереды, например, карп. Ему нужна кислородная концентрация минимум 4 мг/л. Карась же, наоборот, считается наименее придирчивым, поэтому он хорошо приживается даже в заросших и заиленных водоемах. Кислород получил признание в медицине и косметологии. С ним оказывают помощь больным сердечнососудистыми заболеваниями, гипоксией различного происхождения, бронхиальной астмой, при шоке и удушье. Также для укрепления иммунной системы и профилактики многих недугов могут применяться кислородные коктейли. Косметическая направленность кислорода заключается в омолаживающем эффекте, улучшении состояния кожи, повышении ее эластичности и тонуса. Достигается результат разными способами, к примеру, с использованием кремов, масок, обогащенных кислородом, мезотерапией на основе того же элемента. Кислород (O2) нестабилен в атмосфере нашей планеты и регулярно исчезает, поэтому его запас должен постоянно пополняться фотосинтезом. Без растительности и водорослей наша атмосфера почти не содержала бы O2. Кстати, говоря о водорослях, зеленые морские водоросли обеспечивают приблизительно 70 % кислорода, произведенного на Земле посредством фотосинтеза, остальные 30 % произведены оставшимися зелеными растениями. Озон Озон (O3) – аллотропная форма кислорода, которая реагирует лучше, чем обычный кислород. Озон выделяется в природе во время крупных электрических выбросов (штормы и грозы с молниями) или ультрафиолетовым излучением в верхних слоях атмосферы Земли. Озон действует как защитный слой, предохраняющий нас от вредного воздействия ультрафиолетовых лучей. Иногда озон вместо хлора используется в обработке питьевой воды. Кислород используется в черной и цветной металлургии. Он интенсифицирует пирометаллургические и гидрометаллургические процессы. Благодаря элементу научились извлекать из руд золото. Это трудоемкая операция, но благодаря кислороду она протекает значительно быстрее. Также он применяется в химической промышленности, на нужды которой расходуется 30% производящего кислорода. Элемент берет участие в термоокислительном крекинге, когда получается ацетилен – вещество для сварки и резки металлов, для синтезов органических веществ. Кислород применяется в космосе. Он выступает окислителем в двигателях космических кораблей второй ступени и в ракетах высотных исследований. В составе взрывчатых веществ находится жидкий кислород. Также он применяется в авиации и медицине. Когда затруднительное дыхание, при сердечных и легочных заболеваниях, то больным из кислородных подушек подают кислород. Список группы 1. 2. 3. 4. 5. 6. 7. 8. 1. Что означает слово "oxygenium" в переводе на русский язык? 2. Какое количество кислорода считается смертельным? 3. Сколько кислорода вырабатывает в год одно дерево? 4. Почему может потемнеть дневное небо? 5. Какая рыба самая привередливая? 6. Зачем применяют кислородные коктейли? 7. Для чего используют кислородные кремы и маски? 8. Как пополняется запас кислорода в атмосфере? 9. От чего спасает нас озон? 10.Для чего используют кислород в космосе? 1.1.1. 3.4.1. 1ш2п 3о 305.2.1 305да Са Ко1 Кса Кр 2.1.2. 5в 2ш1п 4о 2.2.1. 5б 2о Да 305.3.2. 305дь 305.3.3. 305дь Са Ко2 Кса Кр Са Ко3 Кса Оь 1. Распечатать задания на синей, желтой и красной бумаге 2. Распечатать шифры 3. Спрятать задания согласно координатам
Читайте также:

