Аккумулятор доклад по химии
Обновлено: 04.07.2024
Аккумуляторами называют химические источники тока, в которых в последствии обратимых химических реакций внутренняя энергия превращается в электрическую. Именно из-за обратимости данной реакции, аккумуляторы можно заряжать и разряжать. Аккумуляторы созданы для накопления электрического тока и нашли широкое применение в самых разных областях.
Содержание
Введение Ошибка! Закладка не определена.
Характеристики аккумуляторов 4
Различные виды аккумуляторов 6
Виды аккумуляторов и их применение 7
Вывод 23
Прикрепленные файлы: 1 файл
Аккумуляторами называют химические источники тока.docx
Введение
Аккумуляторами называют химические источники тока, в которых в последствии обратимых химических реакций внутренняя энергия превращается в электрическую. Именно из-за обратимости данной реакции, аккумуляторы можно заряжать и разряжать. Аккумуляторы созданы для накопления электрического тока и нашли широкое применение в самых разных областях. Без них трудно представить нашу жизнь, они везде окружают нас. Аккумуляторы предназначен ы для многократного использования и имеют достаточно большой срок службы. Простейший аккумулятор - это два электрода, которые сделаны из разных металлов и поглощены в раствор электролита (кислоты). Один из электродов называют катодом, а другой анодом.
Применение аккумуляторов в какой-либо области зависит не только от их видов, но и от емкости устройств. И у обычной батарейки, и у автоаккумулятора этот основной параметр рассчитывается в одинаковых единицах, ампер-часах. Так, емкость 800 мА*ч означает, что данная батарея за час отдает 800 мА электроэнергии. Еще один немаловажный параметр аккумуляторной батареи – число циклов перезарядки. Чем больше это число, тем дольше прослужит устройство.
В практике чаще всего применяют свинцовые и литиевые аккумуляторы. Свинцовый аккумулятор выполнен из двух свинцовых пластинок которые поглощены в серную кислоту. Аккумулятор имеют разное напряжение, например один блок (банка) свинцового аккумулятора дает напряжение 2 вольта, один блок литий-ионного аккумулятора - 3,7 вольт, щёлочный - 1,2 вольт. Создателем первого аккумулятора считают Алессандро Вольту (от его фамилии образовалось значение величины напряжения - вольт). Вольтов столб имел простую конструкцию - медные и циньковые кружки, а между ними кусок ватты смоченный в растворе воды и поваренной соли. Сегодня существует огромное количество разновидностей аккумуляторов тока.
В последние годы было изобретено еще два вида аккумуляторных батарей. В литиево-полимерном элементе вместо жидкого электролита используется полимерная пленка. Как правило, подобные батареи отличаются высокой плотностью заряда и очень небольшими размерами. Благодаря этим качествам подобные батареи используются в малогабаритных устройствах, например, в телефонах. Вторым новым видом стали аккумуляторы гелевые. Роль электролита в них играет силикагель. Эта желеобразная, чуть подсушенная прослойка между электролитами пронизана сотнями микроскопичесих трещин. Вещества, испаряемые электролитами, впитываются в гель и превращаются в жидкость. Таким образом, большая часть вредных испарений остается внутри аккумулятора.
Характеристики аккумуляторов
Среднее разрядное напряжение аккумуляторов находится в широком диапазоне от 1,25В у никель-кадмиевых аккумуляторов до 3,5В у литиевых аккумуляторов. С повышением скорости разряда емкость аккумуляторов уменьшается, причем в минимальной степени у Ni-Cd и Ni-MH аккумуляторов.
Емкость также снижается при понижении температуры. Наибольшее снижение емкости при низких температурах наблюдается у никель-железных аккумуляторов и минимальное снижение - у никель-кадмиевых со спеченными электродами и у свинцовых аккумуляторов.
Высокую удельную мощность можно получить от никель- кадмиевых аккумуляторов, свинцовых (стартерных и герметизированных), никель-цинковых и серебряно-цинковых аккумуляторов. Невысокую удельную мощность имеют никель-железные аккумуляторы.
Удельная массовая энергия минимальна у свинцовых аккумуляторов и максимальна у литиевых аккумуляторов. Наибольшую наработку имеют никель-водородные аккумуляторы, низким ресурсом характеризуются серебряно-цинковые и никель-цинковые аккумуляторы.
Следует отметить, что по мере циклирования уменьшаются емкость, напряжение и соответственно удельная энергия аккумуляторов, причем скорости понижения удельной энергии у разных аккумуляторов существенно различаются. В наименьшей степени снижаются емкость и энергия при циклировании Ni-Cd аккумуляторов.
Наработка зависит от многих причин и прежде всего от глубины разряда. Наиболее высокая скорость саморазряда отмечается у никель-водородных и никель-железных аккумуляторов, наименьшая - у серебряно-кадмиевых и серебряно-цинковых аккумуляторов. К наиболее дешевым принадлежат свинцовые аккумуляторы, к наиболее дорогим - никель-водородные, серебряно-кадмиевые и серебряно-цинковые аккумуляторы.
Влияние тока разряда на емкость отдаваемую аккумулятором:
1-никель-кадмиевые аккумуляторы со спеченным электродом и никель-металлгидридные аккумуляторы, 2-серебрянно-цинковые аккумуляторы, 3- никель-кадмиевые аккумуляторы с ламельным электродом, 4-никель-цинковые аккумуляторы, 5-литий-инные аккумуляторы, 6-свинцовые аккумуляторы, 7-никель-железные аккумуляторы.
Различные виды аккумуляторов:
Железно-воздушный аккумулятор
Железно-никелевый аккумулятор
Лантано-фторидный аккумулятор
Литиево-железно-сульфидный аккумулятор
Литиево-железно-фосфатный аккумулятор
Литиево-ионный аккумулятор
Литиево-полимерный аккумулятор
Литиево-фторный аккумулятор
Литиево-хлорный аккумулятор
Литиево-серный аккумулятор
Натриево-никелево-хлоридный аккумулятор
Натриево-серный аккумулятор
Никелево-кадмиевый аккумулятор
Никелево-металлогидридный аккумулятор
Никелево-цинковый аккумулятор
Свинцово-водородный аккумулятор
Свинцово-кислотный аккумулятор
Серебряно-кадмиевый аккумулятор
Серебряно-цинковый аккумулятор
Цинково-бромный аккумулятор
Цинково-воздушный аккумулятор
Цинково-хлорный аккумулятор
Никель-водородный аккумулятор
Виды аккумуляторов и их применение
Данный тип аккумуляторов, изобретен в 1859 году французским физиком Гастоном Планте. Основные области применения: стартерные батареи в автомобильном транспорте, аварийные источники электроэнергии.
Свинцовые аккумуляторы являются наиболее распространенными среди всех существующих в настоящее время химических источников тока. Их масштабное производство определяется как относительно низкой ценой, обусловленной сравнительной не дефицитностью исходных материалов, так и разработкой разных вариантов этих аккумуляторов, отвечающих требованиям широкого круга потребителей.
Реагентами в свинцовых аккумуляторах служат диоксид свинца (PbO2) и свинец (Pb), электролитом - раствор серной кислоты. Они также называются свинцово-кислотными аккумуляторами. Их разделяют на четыре основные группы; стартерные, стационарные, тяговые и портативные (герметизированные). Наиболее распространенные из свинцовых аккумуляторов - стартерные аккумуляторы, предназначены для запуска двигателей внутреннего сгорания и энергообеспечения устройств машин. В последние годы в основном используются аккумуляторы, не требующие ухода. К недостаткам относят невысокие удельную энергию и наработку, плохую сохранность заряда, выделение водорода.
Стационарные аккумуляторы используются в энергетике, на телефонных станциях, в телекоммуникационных системах, в качестве аварийного источника тока и т.д. Обычно они работают в режиме непрерывного подзаряда. Относятся к недорогим аккумуляторам.
Тяговые аккумуляторы предназначены для электроснабжения электрокаров, подъемников, шахтных электровозов, электромобилей и других машин. Действуют в режимах глубокого разряда, имеют большой ресурс и низкую стоимость.
Портативные (герметизированные) свинцовые аккумуляторы используются для питания приборов, инструмента, аварийного освещения. К их достоинствам относятся более низкая стоимость по сравнению со стоимостью других портативных аккумуляторов, широкий интервал рабочих температур. Недостатками кислотных аккумуляторов являются невозможность хранения в разряженном состоянии, трудность изготовления аккумуляторов малых размеров.
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в сернокислотной среде. Во время разряда происходит восстановление диоксида свинца на катоде и окисление свинца на аноде. При заряде протекают обратные реакции, к которым в конце заряда добавляется реакция электролиза воды, сопровождающаяся выделением кислорода на положительном электроде и водорода — на отрицательном.
Щелочные аккумуляторы - аккумуляторы, в которых в качестве электролита используют раствор щелочи в воде.
Главная особенность щелочных аккумуляторных батарей - способность постепенно отдавать накопленный заряд за достаточно длительный промежуток времени. Это свойство способствует обеспечению бесперебойного питания огромному количеству различных устройств.
Применяются данные аккумуляторы в качестве:
- основных источников электроэнергии на электрокарах и в мобильных устройствах (фотоаппараты, видеокамеры, телефоны, карманные и переносные фонари и т.д.);
- дополнительных источников энергии в трамваях и троллейбусах, тепловозах и электровозах;
- источников энергии для питания аварийных устройств, таких как аварийное освещение, охранно-пожарные сигнализации, источники бесперебойного питания персональных компьютеров и т. п.
Сегодня щелочные аккумуляторы применяются только на машинах, работа которых осуществляется в тяжелых условиях эксплуатации, или там, где необходима долговечность и надежность (строительная и сельскохозяйственная техника).
Наиболее распространены никель-железные и никель-кадмиевые щелочные аккумуляторы. Их широко применяют на тепловозах и пассажирских вагонах.
Данный тип аккумулятора выпускается в разных странах мира примерно с 1950 года. На сегодняшний день более 50% всех аккумуляторов для портативного оборудования являются никелево-кадмиевыми.
Реагентами в никель-кадмиевых аккумуляторах служат гидроксид никеля и кадмий, электролитом - раствор КОН, поэтому они именуются щелочными аккумуляторами. Существуют три основных вида никель-кадмиевых аккумуляторов: негерметичные с ламельными (ламельные аккумуляторы) и спеченными электродами (безламельные аккумуляторы) и герметичные. Наиболее дешевые ламельные никель-кадмиевые аккумуляторы характеризуются плоской разрядной кривой, высокими ресурсом и прочностью, но не низкой удельной энергией. Удельная энергия, скорость разряда Ni-Cd аккумуляторов со спеченными электродами выше, они работоспособны при низких температурах, но дороже, характеризуются эффектом памяти и способностью к тепловому разгону.
Применяются никель-кадмиевые аккумуляторы для питания шахтных электровозов, подъемников, стационарного оборудования, средств связи и электронных приборов, для запуска дизелей и авиационных двигателей и т.п.
Герметичные Ni-Cd аккумуляторы характеризуются горизонтальной разрядной кривой, высокими скоростями разряда и способностью действовать при низких температурах, но они дороже герметизированных свинцовых аккумуляторов и характеризуются эффектом памяти. Применялись для питания портативной аппаратуры (сотовых телефонов, магнитофонов, компьютеров и т.д.), бытовых приборов, игрушек и т.д. Недостатком никель-кадмиевых аккумуляторов является применение токсичного кадмия.
Вместо кадмия в этих аккумуляторах используется железо. Из-за выделения водорода с самого начала заряда аккумуляторы производят только в негерметичном варианте. Они дешевле никель-кадмиевых аккумуляторов, не содержат токсичный кадмий, имеют длинный срок службы и высокую механическую прочность. Однако они характеризуются высоким саморазрядом, низкой отдачей по энергии, практически неработоспособны при температуре ниже -10 °С. Выпускаются в призматическом виде и используются в основном как тяговые источники тока в шахтных электровозах, электрокарах и промышленных подъемниках.
Электрохимические преобразователи энергии: общие сведения и область применения. Физико-химические процессы в электрохимических генераторах (ЭХГ). Аккумулятор как прибор для накопления электрической энергии. Электроэнергетические установки на базе ЭХГ.
| Рубрика | Физика и энергетика |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 01.06.2010 |
| Размер файла | 106,9 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
1. Аккумуляторы
Первым кто открыл возможность получения тока иным, чем электризация трением, способом был итальянский ученный Луиджи Гальвани (1737-1798). Однажды он заметил, что лапка мёртвой лягушки пришла в движение при соприкосновении с её нервом стального скальпеля. Это открытие заставило Гальвани поставить ряд опытов для обнаружения причины возникновения электрического тока.
В основе принципа действия различных типов аккумуляторов лежит явление электролиза, где используется его важное свойство - обратимость. Электролиз - изменение химического состава раствора при прохождении через него электрического тока, обусловленное потерей или присоединением электронов ионами.
Аккумулятор - прибор для накопления электрической энергии с целью её дальнейшего использования.
Аккумулятор можно изготовить аналогично гальваническому элементу, использовав для этой цели две свинцовые пластины, погруженные в раствор содержащий одну часть серной кислоты на пять частей воды. Для зарядки аккумулятора соединяют последовательно два таких элемента и амперметр и пропускают через них ток.
Как только через аккумулятор начинает идти ток, возле катода возникают пузырьки водорода. На аноде, как следовало ожидать, освобождается кислород. Однако его выделением дело не ограничивается. Пластина анода постепенно приобретает темно-коричневый цвет вследствие образования на ее поверхности перекиси свинца (PbO2) за счет того, что некоторое количество кислорода соединяется химически с материалом пластины. При образовании PbO2 ток зарядки падает, указывая на возрастание сопротивления аккумулятора. Когда аккумулятор зарядится полностью, присоединяемый к нему вольтметр покажет напряжение несколько более 2 вольт.
В сущности, процесс зарядки состоит в том, что две одинаковые вначале пластины аккумулятора вследствие электролиза становятся разными; одна из них, по-прежнему остаётся свинцовой (-), а материал другой превращается в перекись свинца (+).
Химические реакции в аккумуляторе протекают следующим образом (в процессе зарядки реакции идут слева направо, при разрядке - в обратном направлении):
200 кДж/кг, но их долговечность мала. Повышение долговечности достигается в газодиффузионных никель-водородных АБ, в которых W*>250 кДж/кг. Еще более высокий показатель (W*>500 кДж/кг) имеют серно-натриевые АБ, но их ресурс составляет 100 - 200 циклов "заряд - разряд". Дальнейшее повышение W* теоретически до значений 103 кДж/кг возможно в литиевых АБ, но их недостаток - малый ресурс вследствие высокой коррозионной активности Li.
Запас энергии в химической АБ принято характеризовать зарядной емкостью (в Ач или Кл), необходимое значение которой зависит от мощности и времени работы потребителей электроэнергии. Химические АБ получили широкое распространение на транспорте, в системах электростартерного запуска авиационных и автомобильных двигателей, в судовых установках, на электромобилях, во внутризаводском электротранспорте, на электропогрузчиках и т.д.
В условиях КЛА всегда реализуется параллельная работа химической АБ с ФЭП. Последние производят подзарядку АБ в "дневные" часы. Для автономных установок, в том числе на КЛА, целесообразно также сочетание ФЭП с системой "электролизер - ЭХГ". Часть энергии ФЭП в "дневные" часы затрачивается на разложение воды, а в "ночные" часы полученные H2 и O2 обеспечивают работу ЭХГ.
2.3 Физико-химические процессы в ЭХГ
Как и в реакции горения (активируемого, например, зажиганием), стадии токообразующей электрохимической реакции также протекают одновременно, но локализованы в различных областях внутреннего пространства ТЭ..\ В качестве типового примера рассмотрим работу водород - кислородного ТЭ. Стехиометрическое уравнение суммарной реакции:
имеет такой же вид, как при горении. Поясним устройство и принцип действия ТЭ, в котором электрохимическая реакция происходит на стыках трех фаз состояния веществ: газообразной (восстановителя H2 и окислителя O2), жидкостной (щелочного электролита - раствора KOH) и твердой (пористых металлокерамических электродов). Схема ТЭ показана на рис. 1а. Электроды анод 1 и катод 2 выполнены из композитного материала (например, из графитовой керамики с платиновым катализатором). Электроды 1 и 2 отделены слоем электролита - раствора щелочи KOH, который не пропускает нейтральные молекулы или атомы газов водорода и кислорода. Ионизированные газы, например, ионы H+, могут дрейфовать сквозь электролит. Корпус ТЭ выполняется из титанового сплава 4, химически не взаимодействующего с KOH. Внешняя цепь ТЭ замкнута сопротивлением Rн нагрузки, которое подключено к металлическим наплавкам на электродах.
Газообразные компоненты химического топлива - отдающий свои электроны восстановитель H2 и присоединяющий электроны окислитель O2 - - непрерывно подводятся под избыточным давлением к порам анода и катода (рис. 1а) из резервуаров с запасом реагентов.
1. На поверхностях анода, смоченных р-ром KOH, в электролите растворяется газообразный водород и абсорбируется на стенках пор электрода. В растворе гидроксид калия находится в диссоциированном состоянии:
Водород в присутствии ионов OH- он легко отдает электроны (окисляется), образуя воду:
Рис . 1. Схемы водородно-кислородных топливных элементов:
а - с жидким электролитом (раствором КОН); б - с ионообменной мембраной
2. На поверхности катода аналогичные явления приводят к реакции восстановления кислорода, который в присутствии воды отбирает у этого электрода образовавшиеся свободные электроны:
В итоге этих первой и второй стадий "холодного горения" на аноде образуется избыток электронов, а в примыкающем растворе - недостаток ионов гидроксила OH-. На катоде же имеется недостаток электронов, а в окружающем его электролите - избыток ионов H+. Вследствие этого протекают следующие две стадии реакции.
3. По внешнему участку цепи от анода к катоду через сопротивление Rн проходят электроны 4e-, совершая полезную электрическую работу (направление тока I противоположно перемещению электронов).
4. В электролите происходит диффузия ионов 4OH- с катода на анод и посредством ионного тока замыкается электрическая цепь (согласно уравнению непрерывности полного тока div J = 0).
Если сложить реакции для первой и второй стадии, получится результирующее уравнение реакции , конечным продуктом которой является вода. Избыточное количество паров воды 2H2O удаляют из ТЭ, например, с помощью продувки с последующей сепарацией или выпариванием. Очищенная от паров электролита, вода может направляться для дальнейшей утилизации (рис. 1а).
Сбалансированный ход реакций на указанных стадиях у поверхностей электродов определяется равновесием давлений газовой и жидкостной фаз: pr = pэ + pк ;
здесь pr - внешнее давление газообразных реагентов ( водорода или кислорода ); pэ - гидростатическое давление электролита; pк =(? cos?)/d -
его капиллярное давление в порах электродов; ? - поверхностное натяжение (H/м); ? - угол смачиваемости; d - диаметр поры.
Наряду с KOH в ТЭ возможно использование кислотного электролита - раствора H2SO4.
Требующееся испарение воды из элементов с жидкостным электролитом, работающих при давлении 5Ч105 Па и более, определяет эксплуатацию ТЭ на среднетемпературном ( 373 - 523 К ) или высокотемпературном ( боле 523 К ) уровне, что обусловливает необходимость наличия в составе ЭХГ ряда технически сложных вспомогательных устройств. Для преодоления таких затруднений применительно к АЭУ разработаны водород - кислородные ТЭ с ионообменными мембранами (ИОМ) в виде квазитвердых веществ (гелей), разделяющих разнополярные электроды в ТЭ. Изготовляют ИОМ из фтороуглеродистого аналога тефлона. На полимерной сетке - матрице закреплены ионы, они могут обмениваться на другие ионы, присутствующие в межэлектронной среде. На практике для ТЭ применяют ИОМ с сульфатными катионами, например, По своим функциям ИОМ подобна электролиту, она способна противостоять воздействию нейтральных молекул и атомов H2 и O2. Схема ТЭ с ИОМ приведена на рис. 1б. Пористые керамические электроды 1 и 2 прижаты к мембране 3. Контактирующие с ИОМ поверхности анода и катода покрыты каталитическими слоями металла. Принцип работы ТЭ с ИОМ состоит в следующем.
На аноде подводимый газообразный водород ионизируется по реакции:
Ионы водорода под влиянием градиента их концентрации и соответствующего электрического поля перемещаются сквозь ИОМ к катоду, на котором протекает реакция:
Электроны 4e- через Rн поступают к катоду. Полученная вода (H2O)n под действием градиента ее концентрации возвращается к аноду. Две молекулы воды (2H2O), образующиеся в элементарном акте реакции, необходимо отводить из зоны реакции, например, дренажным устройством. При работе ТЭ гель в ИОМ набухает и находится, как указывалось, в квазитвердом состоянии.
Кроме ИОМ в ТЭ применяются также капилярные мембраны типа волокнистых материалов, пропитанных щелочным электролитом (например, асбест). Принцип действия ТЭ с капилярными мембранами такой же, как ТЭ с жидкостным электролитом. В отдельных установках возможно использование ЭХГ с ТЭ, работающими на других компонентах топлива, кроме H2 - O2. Итоговая электрохимическая реакция окисления восстановителя Red и восстановителя Ox имеет в общем случае вид
В ТЭ имеет место встречное движение разнополярных ионов внутри электролита и переход электронов от анода к катоду по сопротивлению Rн, замыкающему внешнюю цепь. При этом осуществляется прямое преобразование энергии химических связей Red и Ox в электрическую энергию. Конкретизацию общей формы записи токообразующих реакций рассмотрим примере окисления гидразина N2H4. Реакция окисления гидразина имеет место в ЭХГ малой мощности.
Анодное окисление гидразина:
Катодное восстановление кислорода:
Суммарное стехиометрическое уравнение реакции:
2.4 График зависимости U от I
Рис. 2: Характеристики водородно-кислородного ЭХГ:
а - общая форма характеристики и зависимость полезной мощности от тока;
б - аналоги внешней характеристики - зависимости напряжения от плотности тока для ТЭ различного исполнения (1-с раствором электролита; 2-с капилярной мембраной; 3-с ИОМ при Т=355 К; 4-с ИОМ при Т=313 К).
2.5 Внешняя характеристика U=f(I)
Отклонение от состояния равновесия при работе ТЭ практически приводит к уменьшению напряжения и снижению КПД по сравнению с их термодинамическими значениями вследствие изменения потенциала катода и анода при прохождении тока в цепи ТЭ. Совокупность этих явлений называют поляризацией. При совершении работы выхода (активации) из металла электрода в раствор электролита электрон преодолевает потенциальный барьер, образованный двойным слоем разноименных зарядов. На границе "электрод - электролит" наблюдается различие концентраций ионизированных реагентов. Электролит и электроды имеют собственное внутреннее сопротивление. Упрощенно, совместное влияние перечисленных эффектов можно учесть с помощью падения напряжения на нелинейном внутреннем сопротивлении ТЭ Rвн. При этом уравнение внешней характеристики приближенно записывается в виде
где Eн - ЭДС при нагрузке, учитывающая активационную и концентрационную поляризацию; сопротивление электролита Rэл практически равно Rвн и учитывает "омическую" поляризацию.
Общая форма внешней характеристики ЭХГ показана на рис. 2а. Большая крутизна | dU / dI | при малых и повышенных значениях тока обусловлена соответственно поляризацией активации электродов (участок 1) и приграничной поляризацией концентрации (участок 3). Линейный участок 2 с относительно малой крутизной | dU / dI | отражает влияние в основном "омической" поляризации. На рис. 2б. приведены аналоги внешних характеристик U = U(J) для конкретных ТЭ. Геометрическая плотность тока J (на единицу кажущейся поверхности электрода) может при кратковременных режимах достигать 0.1 - 0.2 А/см2.
Электрическая схема ЭХГ, построенная по матричному принципу, дана на рис. 3а; (Iэ, Uэ - ток и напряжение ТЭ). Упрощенная схема замещения ТЭ представлена на рис. 3б. если при T = const рассматривать ТЭ как линейный элемент с постоянными эквивалентными параметрами
где Rн, Lн - сопротивление и индуктивность нагрузки; Lэ,т - индуктивность электродов и токоотводов, то процесс разряда ТЭ описывается уравнением:
Здесь установившийся ток нагрузки;
эквивалентная постоянная времени.
2.6 Электроэнергетические установки на базе электрохимических генераторов
ЭХГ в целом кроме батареи ТЭ и вспомогательного оборудования включает ряд блоков, снабженных взаимными прямыми и обратными связями для обеспечения функционирования в заданном режиме. Можно классифицировать ЭХГ как техническую систему, состоящую из соответствующих подсистем. Укрупненная схема ЭХГ в качестве главной подсистемы содержит батарею топливных элементов БТЭ, а также подсистемы: хранения горючего ПХГ и окислителя ПХО; обработки горючего ПОГ и окислителя ПОО; подачи горючего ППГ и окислителя ППО. Наряду с ними имеются подсистемы отводов продуктов реакции ПОПР, теплоотвода ПТО и подсистема контроля и автоматики ПКА, которая соединена двусторонними связями с подсистемами подачи и отвода. К подсистеме потребления и регулирования электроэнергии ППРЭ подключена БТЭ.
Применительно к водород - кислородному ЭХГ в ПХГ, ПХО осуществляется криогенное хранение сжиженных компонентов топлива, в ПОГ, ПОО производится нагрев H2 и O2 , которые в газообразном состоянии подводятся к ППГ, ППО. Эти подсистемы производят дозированную подачу реагентов при заданных параметрах (давлении, температуре) в БТЭ, где происходит реакция электрохимического окисления. Удаление паров воды в ЭХГ выполняет ПОПР. Для ЭХГ, применяемых на КЛА, важное значение имеет ПТО, содержащая холодильник - излучатель, к которому тепло доставляется с помощью циркуляционных устройств с жидкостным теплоносителем.
Для КЛА многоразового использования "Спейс Шаттл" фирма "Дженерал Электрик" (США) выполнила ЭХГ с водород - кислородными ТЭ, имеющими позолоченные электроды с платиновыми катализаторами. Электроды разделены ИОМ, во избежание высушивания которых организован отвод тепла от анода, что создает движущий градиент концентрации для возвращения H2O к аноду. Отвод воды - продукта реакции - реализован с помощью автоматически действующей схемы с микропористым сепаратором и волокнистыми фитилями, выступающими из сборки ТЭ.
Две секции БТЭ, имеющие по 38 ТЭ, соединены параллельно и генерируют электрическую мощность 5 кВт. Батарея размещена в цилиндрическом контейнере диаметром 0,33 м и габаритной длиной 0,94 м. Удельная масса БТЭ без заправки равна 11 кг/кВт. Эксперименты показали, что сборка ТЭ способна работать более 5000 ч без деградации ИОМ при температуре до 455 К.
На КЛА многоразового использования "Буран" установлены четыре ЭХГ мощностью по 10 кВт ( суммарная мощность 40 кВт ) серии "Фотон" на водород - кислородном топливе H2 - О2. Напряжение одного генератора, состоящего из 128 топливных элементов, составляет 29,2 В ( схема генератора содержит четыре параллельные ветви, в каждой из которых включено последовательно по 32 элемента). Масса ЭХГ составляет 145 кг, масса его блока автоматики - 15 кг ( удельная масса 14,5 кг/кВт, а с учетом блока автоматики - 16 кг/кВт ). Ресурс ЭХГ равен 2000 ч, его КПД 62%
Для длительной эксплуатации в АЭУ перспективны установки, в которых ЭХГ работает совместно с регенератором компонентов топлива, разлагающим воду на водород и кислород. Электролиз воды требует подведения извне энергии для разрыва валентной химической связи
Н - О - Н. При мощностях менее 1 кВт целесообразно интегральное исполнение ЭХГ и электролизера воды (ЭВ). При более высоких электрических мощностях ЭХГ и электролизер воды в раздельном исполнении имеют лучшие технико-экономические показатели, чем у интегрального устройства. В зависимости от вида подводимой к регенератору Р энергии принципиально возможны различные способы разложения воды. Высоким КПД отличается электролиз при пропускании через Н2О электрического тока: отношение теплоты сгорания полученного топлива к энергозатратам на выделение Н2 и О2 достигает 70 - 80%. В особенности электролиз эффективен для АЭУ на КЛА при использовании Солнца в качестве источника первичной энергии с последующим ее преобразованием в ФЭП.
Разложение воды на Н2 и О2 можно реализовать непосредственно в ТЭ при пропускании тока в обратном направлении по отношению к току генераторного режима, используя принцип обратимости ТЭ, который выполняет роль электролизной ячейки. При таком способе регенерации компонентов топлива ресурс регенеративного ТЭ ограничен объемом резервуаров для хранения Н2 и О2. Известны регенеративные ТЭ, в которых полученные газы Н2 и О2 хранятся в пористых или губчатых устройствах внутри ТЭ. Данный тип ТЭ по принципу действия формально аналогичен химической АБ, причем электрическая емкость регенеративного ТЭ определяется количеством адсорбированных газов. Как и ТЭ, возможно выполнение электролизной ячейки с электролитом, ИОМ или капиллярной мембраной. Прикладываемое к электролизной ячейке при электролизе напряжение на 30 - 80% должно превосходить напряжение, генерируемое ТЭ, поскольку поляризационные эффекты в электролизной ячейке проявляются сильнее, чем в ТЭ.
Регенеративная электроэнергетическая установка (РЭУ) космической долговременной технологической базы включает восемь идентичных модулей данного типа, средняя энергетическая мощность каждого из которых составляет 12,5 кВт. Газовые баллоны рассчитаны на запас реагентов . кг, рабочее давление в баллонах поддерживается в диапазоне Па. За один цикл разрядного режима расходуется 3.03 кг реагентов (условная степень разрядки 33%). Регулятор постоянного тока, компенсирующий падение напряжения на выходе ЭХГ, позволяет вдвое повысить ресурс ТЭ, который может доходить до 10 лет.
АККУМУЛЯТОРЫ
АККУМУЛЯТОРЫ электрические (от лат. accumulator- собиратель, накопитель), хим. источники тока многократного действия. При заряде от внеш. источника электрич. тока в аккумуляторе накапливается энергия, к-рая при разряде вследствие хим. р-ции непосредственно превращ. снова в электрическую и выделяется во внеш. цепь. По принципу работы и осн. элементам конструкции аккумуляторы не отличаются от гальванических элементов, но электродные р-ции, а также суммарная токообразующая р-ция в аккумуляторах обратимы. Поэтому после разряда аккумулятора может быть снова заряжен пропусканием тока в обратном направлении: на положит. электроде при этом образуется окислитель, на отрицательном-восстановитель.
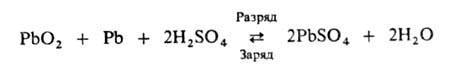
Наиб. распространены свинцовые аккумуляторы, часто наз. также кислотными. Их действие основано на р-ции:
Первый свинцовый аккумулятор был создан Г. Планте в 1859. Сейчас более половины мирового произ-ва Рb расходуется на изготовление свинцовых аккумуляторов с единичной емкостью 2-5000 А * ч и уд. энергией 25-40 Вт * ч/кг. Осн. достоинства таких аккумуляторов: относит. дешевизна, пологие разрядная и зарядная кривые, возможность работать в разл. режимах разряда; недостаток - невысокий ресурс работы (число допустимых циклов заряд-разряд для стартерных аккумуляторов 100-300, для тяговых с панцирными электродами 800-1500). В конце заряда на электродах свинцового аккумулятора наблюдается заметное выделение газов, к-рые часто увлекают за собой туман из капель H2SO4. В связи с этим большое внимание уделяется созданию герметизированных свинцовых акуумуляторов.
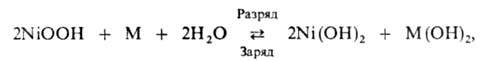
Щелочные никель-кадмиевые (НКА) и никельжелезные (НЖА) аккумуляторы по распространению занимают второе место после свинцовых. Токообразующая реакция:
НЖА используют в осн. для изготовления тяговых аккумуляторных батарей большой емкости (до 1200 А * ч). Они дешевле НКА, но характеризуются повыш. саморазрядом из-за коррозии железа в щелочном р-ре; кроме того, у них более низкие значения отдачи по току и по энергии. В НКА не наблюдается коррозии Cd и связанного с ней газовыделения, что обусловливает большую длительность сохранения заряженного состояния и возможность полной герметизации аккумулятора. Герметичные НКА выпускают емкостью от 0,01 до 160 А * ч. Их широко используют как источники электрич. энергии в приборах бытовой техники, ср-вах связи и т.п.
Серебряно-цинковые аккумуляторы со щелочным электролитом имеют высокую уд. энергию (до 130 Вт*ч/кг) и способны разряжаться большими токами, но из-за высокой стоимости серебра нашли применение только в специальных отраслях, напр. в космической технике. Токообразующая р-ция:
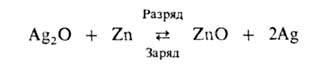
При заряде возможно также образование AgO. Поэтому на зарядных и разрядных кривых наблюдаются ступени, соответствующие р-циям с участием Ag2O и AgO. НРЦ 1,60-1,85 В, ресурс не превышает 100-200 циклов.
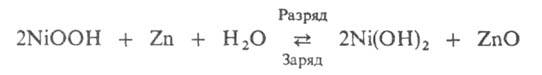
Попытки замены Ag др. материалами привели к созданию никель-цинковых аккумуляторах, в к-рых используют спеченный или прессованный окисноникелевый электрод от НКА и цинковый электрод от серебряно-цинковых аккумуляторов. Токообразующая р-ция:
НРЦ 1,74-1,78 В, уд. энергия ок. 60 Вт*ч/кг, ресурс ок. 300 циклов. Разрабатываемые варианты этих аккумуляторах предназначены в осн. для электромобилей, но широкому использованию их мешает недостаточный пока ресурс работы.
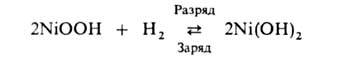
В никель-водородных аккумуляторах протекает след. токообразующая р-ция:
Выделяющийся при заряде Н2 накапливается под давлением. Поэтому блок с электродами помещают в стальной цилиндр, выдерживающий давления до 10 МПа. НРЦ 1,32-1,36 В, уд. энергия 50-60 Вт*ч/кг, ресурс неск. тысяч циклов. Из-за дороговизны произ-ва такие аккумуляторы применяют пока только в космич. технике.
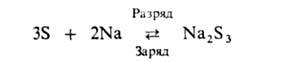
Среди перспективных конструкций аккумуляторов с неводными электролитами Наиб. интерес представляют серно-натриевые с твердым керамич. электролитом из алюминатов натрия, обладающим проводимостью по ионам Na + . Рабочая т-ра такого аккумулятора 300-350°С. Токообразующая р-ция:
НРЦ 2,08 В. Осн. трудность при разработке: создание технологии изготовления тонких, но достаточно стойких деталей из твердого электролита. Разрабатывают также высокотемпературные сульфид-железо-литиевые аккумуляторы; в них вместо твердого электролита применяют расплав солей, окислителями служат FeS или FeS2. По своим характеристикам эти аккумуляторы близки к серно-натриевым.
Если требуется более высокое напряжение, чем у отдельного аккумулятора, применяют аккумуляторные батареи, состоящие из последовательно включенных аккумуляторов, имеющих общий корпус, выводы и маркировку. Батареи широко применяют в транспортных ср-вах для запуска двигателей, освещения и др. Тяговые батареи используют для силовых установок электрокаров, стационарные большой емкости-для электропитания телефонных сетей, в кач-ве аварийных источников электроэнергии на случай перебоев в электросети (напр., в операционных). Малогабаритные герметичные батареи применяют для питания переносных радиоприемников и др. устройств. Большое внимание уделяется разработке батарей для электромобилей. Мировое произ-во одних лишь стартерных батарей из свинцовых аккумуляторов превышает 100 млн. штук в год.
В отличие от гальванич. элементов аккумуляторы требуют ухода при эксплуатации: их необходимо заряжать, периодически доливать электролит и поддерживать постоянной его концентрацию, проводить тренировочные и контрольные зарядно-разрядные циклы и т.п. Разрабатывают т. наз. малообслуживаемые и необслуживаемые аккумуляторы, уход за которыми упрощен.
Свинцово-кислотный аккумулятор — наиболее распространенный на сегодняшний день тип аккумуляторов, изобретен в 1859 году французским физиком Гастоном Планте. Основные области применения: стартерные батареи в автомобильном транспорте, аварийные источники электроэнергии.
Принцип действия
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в сернокислотной среде. Во время разряда происходит восстановление диоксида свинца на катоде и окисление свинца на аноде. При заряде протекают обратные реакции, к которым в конце заряда добавляется реакция электролиза воды, сопровождающаяся выделением кислорода на положительном электроде и водорода — на отрицательном.
Химическая реакция (слева-направо — разряд, справа-налево — заряд):

Элемент свинцово-кислотного аккумулятора состоит из положительных и отрицательных электродов, сепараторов (разделительных решеток) и электролита. Положительные электроды представляют собой свинцовую решётку, а активным веществом является перекись свинца (PbO2 ). Отрицательные электроды также представляют собой свинцовую решётку, а активным веществом является губчатый свинец (Pb). На практике в свинец решёток добавляют сурьму в количестве 1-2 % для повышения прочности. Сейчас в качестве легирующего компонента используются соли кальция, в обеих пластинах, или только в положительных (гибридная технология). Электроды погружены в электролит, состоящий из разбавленной серной кислоты (H2 SO4 ). Наибольшая проводимость этого раствора при комнатной температуре (что означает наименьшее внутреннее сопротивление и наименьшие внутренние потери) достигается при его плотности 1,26 г/см³. Однако на практике, часто в районах с холодным климатом применяются и более высокие концентрации серной кислоты, до 1,29 −1,31 г/см³. (Это делается потому, что при разряде свинцово-кислотного аккумулятора плотность электролита падает, и температура его замерзания, т.о, становится выше, разряженный аккумулятор может не выдержать холода.)
В новых версиях свинцовые пластины (решетки) заменяют вспененным карбоном, покрытым тонкой свинцовой пленкой, а жидкий электролит может быть желирован силикагелем до пастообразного состояния. Используя меньшее количество свинца и распределив его по большой площади, батарею удалось сделать не только компактной и легкой, но и значительно более эффективной — помимо большего КПД, она заряжается значительно быстрее традиционных аккумуляторов. [1]
Физические характеристики
· Теоретическая энергоемкость: около 133 Вт·ч/кг.
· Удельная энергоемкость (Вт·ч/кг): 30-60 Вт·ч/кг.
· Удельная энергоплотность (Вт·ч/дм³): около 1250 Вт·ч/дм³.
· ЭДС заряженного аккумулятора = 2,11 В, рабочее напряжение = 2,1 В (6 секций в итоге дают 12,7 В).
· Напряжение полностью разряженного аккумулятора = 1,75 — 1,8 В (из расчета на 1 секцию). Ниже разряжать их нельзя.
· Рабочая температура: от минус 40 до плюс 40
· КПД: порядка 80-90%
| Напряжение | ~ Заряд |
| 12.70 V | 100 % |
| 12.46 V | 80 % |
| 12.24 V | 55 % |
| 12.00 V | 25 % |
| 11.90 V | 0 % |
Эксплуатационные характеристики
· Номинальная ёмкость, показывает количество электричества, которое может отдать данный аккумулятор. Обычно указывается в ампер-часах, и измеряется при разряде малым током (1/20 номинальной емкости, выраженной в а/ч).
· Стартерный ток (для автомобильных). Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев замеряется при -18°С (0°F) в течение 30 секунд. Различные методики замера отличаются, главным образом, допускаемым конечным напряжением.
· Резервная емкость (для автомобильных). Характеризует время, в течение которого аккумулятор может отдавать ток 25А. Обычно составляет порядка 100 минут.
Эксплуатация
Ареометр может быть использован для проверки удельного веса электролита каждой секции
Такие нехитрые операции вместе с проверкой автомобиля на утечку тока и периодической подзарядкой аккумулятора могут на несколько лет продлить срок эксплуатации батареи.
Свинцово-кислотный аккумулятор при низких температурах
Свинцово-кислотные аккумуляторы необходимо хранить только в заряженном состоянии. При температуре ниже −20 °C заряд аккумуляторов должен проводиться постоянным напряжением 2,275 В/секцию, 1 раз в год, в течение 48 часов. При комнатной температуре — 1 раз в 8 месяцев постоянным напряжением 2,35 В/секцию в течение 6-12 часов. Хранение аккумуляторов при температуре выше 30 °C не рекомендуется.
Слой грязи и накипи на поверхности аккумулятора создает проводник для тока от одного контакта к другому и приводит к саморазряду аккумулятора, после чего начинается преждевременная сульфатизация пластин и поэтому поверхность аккумулятора необходимо поддерживать в чистоте (то есть его надо мыть перед хранением) Хранение свинцово-кислотных аккумуляторов в разряженном состоянии приводит к быстрой потере их работоспособности.
При длительном хранении аккумуляторов и разряде их большими токами (в стартерном режиме), или при уменьшении ёмкости аккумуляторов, нужно проводить контрольно-тренировочные (лечебные) циклы, то есть разряд-заряд токами номинальной величины.[2]
Износ свинцово-кислотных аккумуляторов
При использовании технической серной кислоты и недистиллированной воды ускоряются саморазрядка, сульфатация, разрушение пластин и уменьшение емкости аккумуляторной батареи.
В результате каждой реакции образуется нерастворимое вещество — сернокислый свинец PbSO4, осаждающийся на пластинах, который образует диэлектрический слой между токоотводами и активной массой. Это один из недостатков, влияющий на срок службы свинцово-кислотной аккумуляторной батареи.
Основными процессами износа свинцово-кислотных аккумуляторов являются:
— сульфатация пластин, заключающаяся в образовании крупных кристаллитов сульфата свинца, который препятствует протеканию обратимых токообразующих процессов;
— коррозия электродов, т.е. электрохимические процессы окисления и растворения в электролите, что вызывает осыпание материала токоотводов;
— слабая механическая прочность или плохое сцепление активной массы с токоотводами, что приводит к опаданию активной массы;
— оползание и осыпание активной массы положительных электродов, связанное с разрыхлением, нарушением однородности.
Электри́ческий аккумуля́тор — химический источник тока многоразового действия (в отличие от гальванического элемента, химические реакции, непосредственно превращаемые в электрическую энергию в них, многократно обратимы). Электрические аккумуляторы используются для накопления энергии и автономного питания различных устройств.
Принцип действия
Замена аккумуляторной батареи на электропогрузчике
Принцип действия аккумулятора основан на обратимости химической реакции. Работоспособность аккумулятора может быть восстановлена путём заряда, то есть пропусканием электрического тока в направлении, обратном направлению тока при разряде. Несколько аккумуляторов, объединенных в одну электрическую цепь, составляют аккумуля́торную батаре́ю. Ёмкость аккумуляторов обычно измеряют в ампер⋅часах.
Электрические и эксплуатационные характеристики аккумулятора зависят от материала электродов и состава электролита. Сейчас наиболее распространены следующие аккумуляторы:
| Тип | ЭДС (В) | Область применения |
| свинцово-кислотные (Lead Acid) | 2,1 | автомобили, электропогрузчики, штабелеры, электротягачи, аварийное электроснабжение, источники бесперебойного питания |
| никель-кадмиевые (NiCd) | 1,2 | замена стандартного гальванического элемента, строительные электроинструменты, троллейбусы. |
| никель-металл-гидридные (NiMH) | 1,2 | замена стандартного гальванического элемента, электромобили |
| литий-ионные (Li‑ion) | 3,6 | мобильные устройства, строительные электроинструменты, электромобили |
| литий-полимерные (Li‑pol) | 3,7 | мобильные устройства, электромобили |
| никель-цинковые (NiZn) | 1,6 | замена стандартного гальванического элемента |
По мере исчерпания химической энергии напряжение и ток падают, аккумулятор перестаёт действовать. Зарядить аккумулятор (батарею аккумуляторов) можно от любого источника постоянного тока с бо́льшим напряжением при ограничении тока. Стандартным считается зарядный ток (в амперах) в 1/10 номинальной ёмкости аккумулятора (в ампер⋅часах). Многие типы аккумуляторов имеют различные ограничения, которые необходимо учитывать при зарядке и последующей эксплуатации, например NiMH-аккумуляторы чувствительны к перезаряду, литиевые — к переразряду, напряжению и температуре. NiCd- и NiMH-аккумуляторы имеют так называемый эффект памяти, заключающийся в снижении ёмкости, в случае когда зарядка осуществляется при не полностью разряженном аккумуляторе. Также эти типы аккумуляторов обладают заметным саморазрядом, то есть они постепенно теряют заряд, даже не будучи подключенными к нагрузке. Для борьбы с этим эффектом может применяться капельная подзарядка.
Никель-ка́дмиевый аккумуля́тор (NiCd) — вторичный химический источник тока, в котором анодом является гидрат закиси никеля Ni(OH)2 с графитовым порошком (около 5–8 %), электролитом — гидроксид калия KOH плотностью 1,19-1,21 с добавкой гидроксида лития LiOH (для образования никелатов лития и увеличения ёмкости на 21–25 %), катод — гидрат закиси кадмия Cd(OH)2 или металлический кадмий Cd (в виде порошка). ЭДС никель-кадмиевого аккумулятора около 1,37 В, удельная энергия около 45 — 65 Вт·ч/кг. В зависимости от конструкции, режима работы (длительные или короткие разряды) и чистоты применяемых материалов, срок службы составляет от 100 до 3500 циклов заряд-разряд.
· Теоретическая энергоёмкость: 237 Вт·ч/кг.
· Удельная энергоёмкость: 45–65 Вт·ч/кг.
· Удельная энергоплотность: 50–150 Вт·ч/дм³.
· Удельная мощность: 150..500 Вт/кг.
· Рабочее напряжение = 1,2 В.
· Нормальный ток зарядки = 1/4 ёмкости, время зарядки = 6 часов.
· Саморазряд: 10 % в месяц.
· Рабочая температура: −15…+40 °С.
Аккумулятор, разряжаемый и заряжаемый слабыми токами (например, в пульте дистанционного управления телевизором), быстро теряет ёмкость и пользователь считает его вышедшим из строя. Так же и аккумулятор, длительное время стоявший на подзарядке (например, в системе бесперебойного питания) потеряет емкость, хотя напряжение будет правильным. То есть, использовать никель-кадмиевый аккумулятор в буферном режиме нельзя. Тем не менее, один цикл глубокой разрядки и последующая зарядка полностью восстановят ёмкость аккумулятора.
При систематических недозарядках NiCd аккумуляторы теряют первоначальную ёмкость, но перезарядов они не боятся, а наоборот, повышают свою активность. Поэтому их лучше перезаряжать, чем недозаряжать.
При хранении NiCd аккумуляторы также теряют ёмкость, хотя и сохраняют выходное напряжение. Чтобы избежать неверной разбраковки при снятии аккумулятора с хранения, рекомендуется хранить их в разряженном виде, тогда после первой же зарядки аккумулятор будет полностью готов к использованию.
Области применения
Малогабаритные никель-кадмиевые аккумуляторы используются в различной аппаратуре как замена стандартного гальванического элемента, особенно, если аппаратура потребляет большой ток. Так как внутреннее сопротивление никель-кадмиевого аккумулятора на порядок-два ниже, мощность выдается стабильнее и без перегрева.
Никель-кадмиевые аккумуляторы применяются на электрокарах, трамваях и троллейбусах (для питания цепей управления), речных и морских судах. Широко применяются в авиации в качестве бортовых аккумуляторных батарей самолётов и вертолётов. Используются как источники питания для аккумуляторных шуруповёртов, винтовёртов и дрелей.
Несмотря на развитие других электро-химических систем и ужесточение требований по экологичности, никель-кадмиевые аккумуляторы остаются безальтернативным выбором для высоконадежных решений с большой удельной мощностью, например, фонари для дайвинга.
· Аккумуляторы // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб.: 1890—1907.
· История создания первых аккумуляторов
· Сравнение характеристик NiCd, NiMH, Lead acid, Li-ion, Li-ion polymer и alkaline аккумуляторных батарей(англ.)
· Battery University(англ.) Все о гальванических элементах и аккумуляторах.
Читайте также:

