В чем противоречивость модели атома резерфорда кратко
Обновлено: 05.07.2024
Свидетельство и скидка на обучение каждому участнику
Зарегистрироваться 15–17 марта 2022 г.
Описание презентации по отдельным слайдам:
Тема: “Трудности планетарной модели атома Резерфорда. Модель водородоподобного атома Н. Бора” Урок 11 класс
Модель атома Дж. Дж. Томсона (1903 г) Атом имеет форму шара. По всему объему атома с постоянной плотностью распределен положительный заряд. Внутри (как изюм в кексе) расположены электроны. В целом атом электрически нейтрален. Когда электроны колеблются относительно центра сферы, атом излучает свет.
Планетарная модель атома
Опыты Э. Резерфорда Зная о том, как взаимодействуют одноименно заряженные частицы, а они отталкиваются друг от друга, можно объяснить результаты опыта Резерфорда: - частицы, которые отклонялись, пролетали недалеко от ядра - частицы, которые отражались, попадали точно в ядро - частицы, которые не испытывали отклонений, пролетали далеко от ядра Понимание причин отклонения альфа-частиц позволило Э.Резерфорду выдвинуть собственную планетарную (иначе ядерную) модель строения атома.
Атом по Резерфорду - это положительно заряженное ядро в центре атома и электроны на орбитах вокруг ядра - характер движения электронов определяется действием кулоновских сил со стороны ядра - диаметр ядра в 100000 раз меньше диаметра атома - масса ядра составляет 99,4% от массы всего атома - заряд ядра составляет 99,4% от заряда всего атома - заряд ядра по модулю равен сумме зарядов электронов, поэтому атом в целом нейтрален.
Однако, возникли противоречия между законами классической механики и электродинамики и предложенной Резерфордом моделью атома: 1. Согласно классической механике по модели атома Резерфорда атомы должны быть неустойчивы, т.к.: электроны движутся по орбитам с ускорением, поэтому должны излучать электромагнитные волны. Излучая, должны терять энергию, в результате должны упасть на ядро, тогда атом должен прекратить свое существование. Однако, реальные атомы устойчивы и в невозбужденном состоянии могут существовать неограниченно долго, не излучая электромагнитные волны. 2. По законам классической электродинамики, электрон, приближаясь к ядру, должен двигаться все быстрее, излучая все более короткие электромагнитные волны, поэтому спектр излучения атома должен быть сплошным. Однако, у реальных атомов спектр излучения является линейчатым.
Нильс Бор Изучая противоречия модели атома Резерфорда законам классисической физики Нильс Бор в 1913 г. выдвигает "постулаты", определяющие строение атома и условия испускания и поглощения им электромагнитного излучения. Постулаты Бора показали, что атомы "живут" по законам микромира.
Постулаты Н. Бора I постулат - постулат стационарных состояний: В атоме существуют стационарные квантовые состояния, не изменяющиеся с течением времени без внешнего воздействия на атом. В этих состояниях атом не излучает электромагнитных волн, хотя и движется с ускорением. Каждому стационарному состоянию атома соответствует определенная энергия атома. Стационарным состояниям соответствуют стационарные орбиты, по которым движутся электроны.
Постулаты Н. Бора II постулат - правило частот: При переходе атома из одного стационарного состояния в другое излучается или поглощается 1 фотон. а) Атом излучает 1 фотон(который несет 1 квант энергии), когда электрон переходит из состояния с большей энергией (Е k) в состояние с меньшей энергией (Е n).( Излучение) Энергия излученного фотона: Здесь (Ek - En) - разность энергий стационарных состояний. При Ек > Eп происходит излучение фотона.
Частота излучения: . где k и n - номера стационарных состоянии, или главные квантовые числа. б) Атом поглощает 1 фотон, когда переходит из стационарного состояния с меньшей энергией (E n) в стационарное состояние с большей энергией (E k). При Ек
Модель атома Резерфорда ( она же планетарная модель) заключается в том что электроны вращаются вокруг положительно заряженного ядра. Однако исходя из классической механики , тело движущееся по окружности движется с постоянным ускорением, следовательно должно излучать энергию, что в действительности не происходит. Данное противоречие было преодолено в модели Бора.
Как написать хороший ответ? Как написать хороший ответ?
- Написать правильный и достоверный ответ;
- Отвечать подробно и ясно, чтобы ответ принес наибольшую пользу;
- Писать грамотно, поскольку ответы без грамматических, орфографических и пунктуационных ошибок лучше воспринимаются.
Мореплаватель — имя существительное, употребляется в мужском роде. К нему может быть несколько синонимов.
1. Моряк. Старый моряк смотрел вдаль, думая о предстоящем опасном путешествии;
2. Аргонавт. На аргонавте были старые потертые штаны, а его рубашка пропиталась запахом моря и соли;
3. Мореход. Опытный мореход знал, что на этом месте погибло уже много кораблей, ведь под водой скрывались острые скалы;
4. Морской волк. Старый морской волк был рад, ведь ему предстояло отчалить в долгое плавание.
Первая попытка создания модели атома была предпринята Дж. Томпсоном. Он полагал, что атом – это электронейтральная система формы шара с радиусом 10 - 10 м . На рисунке 6 . 1 . 1 . показано, как одинаково распределяется положительный заряд атома, причем отрицательные электроны располагаются внутри него. Чтобы получить объяснение линейчатых спектров атомов, Томпсон тщетно пытался определить расположение электронов в атоме, для расчета частоты их колебаний в положении равновесия. Спустя время Э. Резерфорд доказал, что заданная Томсоном модель была неверна.
Рисунок 6 . 1 . 1 . Модель Дж. Томпсона.
Электроны в атоме. Опыты Резерфорда и Томпсона
Внутренняя структура атомов была исследована Э. Резарфордом, Э. Марсденом, Х. Гейгером еще в 1909 - 1911 годах. Было применено зондирование атома α -частицами, возникающими во время радиоактивного распада радия и других элементов. Их масса в 7300 раз больше массы электрона, а положительный заряд равняется удвоенному элементарному заряду.
В опытах Резерфорда были использованы α -частицы, имеющие кинетическую энергию 5 М э в .
Альфа-частицы – это ионизированные атомы гелия.
Рисунок 6 . 1 . 2 . Схема опыта Резерфорда по рассеянию α -частиц. K – свинцовый контейнер с радиоактивным веществом, Э – экран, покрытый сернистым цинком, Ф – золотая фольга, M – микроскоп.
Радиоактивный источник, заключенный в свинцовый контейнер, располагается таким образом, что
α -частицы направляются от него к тонкой металлической фольге. Рассеянные частицы попадают на экран со слоем кристаллов сульфида цинка, светящиеся от их ударов. Сцинтилляции (вспышки) можно наблюдать при помощи микроскопа. Угол φ к первоначальному направлению пучка не имеет ограничений для данного опыта.
После испытаний было выявлено, что α -частицы, проходящие через тонкий слой металла, не испытывали отклонений. Наблюдались их отклонения и на углы, превышающие 30 градусов и близкие к 180 .
Модели атомов Томпсона и Резерфорда
Результат Резерфорда противоречил модели Томпсона, так как положительный заряд не был распределен по всему объему атома. Согласно модели Томпсона, заряд не имеет возможности создавать сильное электрическое поле, которое впоследствии отбросит α -частицы. Такое поле однородно заряженного шара максимально на его поверхности и убывает до нуля к центру.
При уменьшении радиуса шара с положительным зарядом атома максимальная сила отталкивания, действующая на α -частицы, по закону Кулона увеличилась бы в n 2 раз.
Если размеры α -частиц достаточно большие, тогда рассеивание может достичь угла в 180 градусов.
Резерфорд пришел к выводу, что пустота атома связана с наличием положительного заряда, сосредоточенного в малом объеме. Данная часть была названа атомным ядром.
Далее возникла ядерная модель атома, показанная на рисунке 6 . 1 . 3 .
Рисунок 6 . 1 . 3 . Рассеяние α -частицы в атоме Томсона ( a ) и в атоме Резерфорда ( b ) .
Резерфорд выяснил, что центр атома имеет положительно заряженное ядро с диаметром 10 - 14 - 10 - 15 м . Оно занимает 10 - 12 полного объема атома, но содержит весь положительный заряд и около 99 , 95 % его массы. Вещество, входящее в состав атома, предполагало наличие плотности p ≈ 10 15 г / с м 3 , а заряд ядра равнялся суммарному заряду электронов. Было установлено, что при взятии за 1 значение заряда электрона, заряд ядра равнялся числу из таблицы Менделеева.
Планетарная модель
Опыты Резерфорда приводили к радикальным выводам и сомнениям ученых. Используя классическое представление о движении микрочастиц, он предлагает планетарную модель атома. Ее смысл заключался в том, что центр атома состоит из положительно заряженного ядра, которое является основной частью массы элементарной частицы. Атом считается нейтральным. При наличии кулоновских сил вокруг ядра по орбиталям вращаются электроны, как показано на рисунке 6 . 1 . 4 . Электроны всегда находятся в состоянии движения.
Рисунок 6 . 1 . 4 . Планетарная модель атома Резерфорда. Показаны круговые орбиты четырех электронов.
Предложенная Резерфордом планетарная модель была толчком в развитии знаний о строении атома. Благодаря ей, опыты по рассеиванию α -частиц смогли объяснить. Но вопрос об его устойчивости остался открытым. Исходя из закона классической электродинамики, заряд, движущийся с ускорением, излучает электромагнитные волны, забирающие и распределяющие энергию. За время 10 - 8 с все электроны потратить всю энергию, вследствие чего упасть на ядро. Так как это не происходит, есть объяснение – внутренние процессы не выполняются согласно классическим законам.

На пути познания сложной структуры атомов вещества наукой пройден непростой путь. Одним из шагов на этом пути явилась планетарная модель атома. Рассмотрим эту модель подробнее.
Электроны и состав атома
Мысль о том, что все вещества в Природе состоят из мельчайших неделимых частиц – атомов, высказывалась еще в античные времена. По мере развития научных представлений, стало ясно, что это не совсем так. Минимальная частица вещества, сохраняющая свойства вещества – это молекула. Молекула же чаще всего состоит из нескольких атомов одного или разных элементов (но иногда молекула состоит из одного атома).
Однако, в самом конце XIXв были открыты электроны – их испускал нагретый электрод в колбе с вакуумом. Стало ясно, что даже атомы простого вещества имеют структуру. Согласно первой атомной теории Дж.Томсона атом представляет собой положительно заряженный шар, внутри которого заключены один или несколько электронов.

Рис. 1. Модель атома Томсона.
Опыты Э. Резерфорда
Для зондирования состава атома Э. Резерфорд использовал поток альфа-частиц, испускаемых радиоактивным препаратом на тонкую металлическую фольгу, а после прохождения фольги частицы попадали на экран, вызывая его свечение. По размеру зоны отклонения можно было судить о том, как воздействовал атом вещества фольги на альфа-частицу.
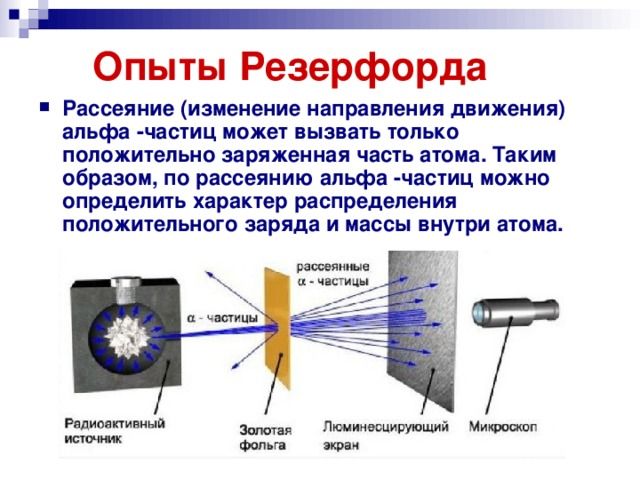
Рис. 2. Опыт Резерфорда по рассеянию альфа-частиц.
Альфа-частица (фактически, представляющая собой ядро атома гелия) имеет гораздо больший вес, чем электрон, таким образом, электроны не могут сколь-нибудь заметно повлиять на ее движение. Отклонение альфа-частицы может происходить только из-за взаимодействия с положительно заряженным атомом. При этом, чем равномернее распределен заряд по атому, тем меньше он будет отклонять альфа-частицу, влияя только на ее скорость (в результате кулоновского взаимодействия).
Опыт дал неожиданный результат. Большинство альфа-частиц, как и следовало ожидать, отклонялись очень слабо. Однако, небольшой их процент отклонялся на большие углы, иногда частицы полностью меняли направление движения. Модель Томсона никак не могла объяснить этого явления.
Планетарная модель атома
Из опыта Резерфорда следовало, что хотя атом имеет размер порядка $10^$ м, весь положительный заряд и вся масса атома сосредоточена в очень малой его части, порядка $10^-10^$ м !
Поэтому была предложена планетарная модель строения атома, согласно которой внутри атома имеется маленькое положительно заряженное ядро, вокруг которого обращаются отрицательно заряженные электроны.
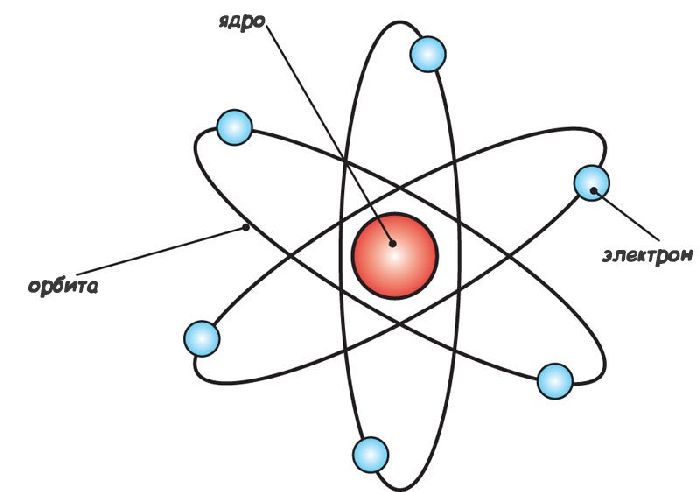
Рис. 3. Планетарная модель атома.
В целом атом получается нейтральным. Электроны не падают на ядро потому, что они вращаются вокруг него по круговым орбитам. Таким образом, атом подобен Солнечной системе, ядро подобно Солнцу, а электроны – планетам.
Проблемы планетарной модели
Планетарная модель атома Резерфорда объяснила опыт по рассеянию альфа-частиц, однако, она противоречила электродинамике Максвелла, согласно которой заряд, движущийся с ускорением, должен излучать электромагнитные волны. Электрон, двигаясь по круговой орбите, имеет постоянное центростремительное ускорение, а значит, должен излучать, теряя энергию, и в конце концов, должен упасть на ядро. Расчеты показывали, что это должно происходить очень быстро. Однако, в реальности атомы устойчивы. Данное затруднение было преодолено только с развитием квантовой физики.
Что мы узнали?
Открытие электрона показало, что атом имеет сложную структуру. В результате опытов Э.Резерфорда была предложена планетарная модель строения атома, где весь положительный заряд и почти вся масса сосредоточена в ядре малых размеров, а электроны вращаются вокруг ядра на некотором расстоянии.
1. Электроны вращаются вокруг ядра, следовательно, обладают центростремительным ускорением.
проблемы:
а) Ускоренно движущиеся электроны излучают электромагнитные волны, поэтому их энергия должна уменьшаться, а вместе с этим должен уменьшаться радиус орбиты. Значит, атом должен быть неустойчивым: примерно за 10 с электрон должен упасть на ядро.
б) Нагретое тело, непрерывно теряя энергию вследствие излучения, должно охладиться до абсолютного нуля.
2. Энергия атома может иметь произвольное значение, значит, и величина поглощаемой (излучаемой) атомом энергии может быть произвольной.
проблемы:
Невозможно объяснить спектральные закономерности.
Несложная инженерная задача. Но физикам плевать на инженера и все его технические науки. То ли все инженеры- дурачки, то ли все физики, третьего не дано.,
Инженерное решение находится примерно так. Раз уж атом не излучает, когда излучают его электроны, значит ядро излучает тоже, и так что сумма излучений равна нулю. А значит в ядре течет периодический э. м. процесс, который и есть источник излучения. Тогда что это за процесс? Чтобы электроны смогли раскачать в ядре процесс достаточной, не ничтожной амплитуды, должен быть резонанс. Ядерные резонансы в принципе найдены.
Однако в ядре развивается только та комбинация колебаний, которая своим излучением гасит излучения электронов. Она отбирает их энергию в себя и за ее счет развивается до полного погашения излучений точно до нуля. Прочие колебания затухают, лишившись энергии.
Это происходит само собой при любом числе электронов и любом воздействии на атом со стороны соседей.
Но все академики мира пишут, что задача не решается, значит я просто дурачок вместе с другими технарями. Кто же мне поверит? Самому-то думать трудно, лучше просто верить авторитетам, они почти всегда правы.
Читайте также:

