Каким образом осуществляется регуляция работы внутренних органов сердца желудка кишечника кратко
Обновлено: 05.07.2024
Гуморальная регуляция секреции пищеварительных соков и моторики желудка и кишечника. Гормональная регуляция пищеварительного тракта.
Центральные, периферические и местные рефлексы осуществляются в тесном взаимодействии с гуморальным механизмом регуляции миоцитов, гландулоцитов и нервных клеток.
В слизистой оболочке желудочно-кишечного тракта и в поджелудочной железе имеются эндокринные клетки, которые вырабатывают гастроинте-стинальные гормоны (регуляторные пептиды, энтерины). Эти гормоны через кровоток и местно (паракринно, диффундируя через межклеточную жидкость) оказывают влияние на миоциты, гландулоциты, интрамураль-ные нейроны и эндокринные клетки. Их выработка запускается рефлекторно (через блуждающий нерв) во время приема пищи и длительное время поддерживается за счет раздражающего влияния продуктов гидролиза пищевых веществ и экстрактивных веществ.
Таблица 11.1. Гормоны желудочно-кишечного тракта, место их образования и вызываемые ими эффекты
| Название гормона | Место выработки гормона | Типы эндокринных клеток | Эффект действия гормонов |
| Соматостатин | Желудок, проксимальный отдел тонкой кишки, поджелудочная железа | D-клетки | Тормозит выделение инсулина и глюкагона, большинства известных желудочно-кишечных гормонов (секретина, ГИПа, мотилина, гастрина); тормозит активность париетальных клеток желудка и ацинарных клеток поджелудочной железы |
| Вазоактивный интестинальный (ВИП) пептид | Во всех отделах желудочно-кишечного тракта | D-клетки | Тормозит действие холецистокинина, секрецию соляной кислоты и пепсина желудком, стимулированную гистамином, расслабляет гладкие мышцы кровеносных сосудов, желчного пузыря |
| Панкреатический полипептид (ПП) | Поджелудочная железа | D2-клетки | Антагонист ХЦК-ПЗ, усиливает пролиферацию слизистой оболочки тонкой кишки, поджелудочной железы и печени; участвует в регуляции обмена углеводов и липидов |
| Гастрин | Антральная часть желудка, поджелудочная железа, проксимальный отдел тонкой кишки | G-клетки | Стимулирует секрецию И выделение пепсина желудочными железами, возбуждает моторику расслабленного желудка и двенадцатиперстной кишки, а также желчного пузыря |
| Гастрон | Антральный отдел желудка | G- клетки | Снижает объем желудочной секреции и выход кислоты в желудочном соке |
| Бульбогастрон | Антральный отдел желудка | G- клетки | Тормозит секрецию и моторику желудка |
| Дуокринин | Антральный отдел желудка | G- клетки | Стимулирует выделение секрета бруннеровых желез двенадцатиперстной кишки |
| Бомбезин (гастринвысвобождающий пептид) | Желудок и проксимальный отдел тонкой кишки | Р-клетки | Стимулирует высвобождение гастрина, усиливает сокращение желчного пузыря и выделение ферментов поджелудочной железой, усиливает выделение энтероглюкагона |
| Секретин | Тонкий кишечник | S-клетки | Стимулирует секрецию бикарбонатов и воды поджелудочной железой, печенью, железами Бруннера, пепсина; тормозит секрецию в желудке |
| Холецистокинин-панкреозимин (ХЦК-ПЗ) | Тонкий кишечник | I-клетки | Возбуждает выход ферментов и в слабой степени стимулирует выход бикарбонатов поджелудочной железой, тормозит секрецию соляной кислоты в желудке, усиливает сокращение желчного пузыря и желчевыделение, усиливает моторику тонкой кишки |
| Энтероглюкагон | Тонкий кишечник | ЕС1-клетки | Тормозит секреторную активность желудка, снижает в желудочном соке содержание К+ и повышает содержание Са2+, тормозит моторику желудка и тонкой кишки |
| Мотилин | Проксимальный отдел тонкой кишки | ЕС2-клетки | Возбуждает секрецию пепсина желудком и секрецию поджелудочной железы, ускоряет эвакуацию содержимого желудка |
| Гастроингибирующий пептид (ГИП) | Тонкий кишечник | К-клетки | Тормозит выделение соляной кислоты и пепсина, высвобождение гастрина, моторику желудка, возбуждает секрецию толстой кишки |
| Нейротензин | Дистальный отдел тонкой кишки | N-клетки | Тормозит секрецию соляной кислоты железами желудка, усиливает высвобождение глюкагона |
| Энкефалины (эндорфины) | Проксимальный отдел тонкой кишки и поджелудочная железа | L-клетки | Тормозит секрецию ферментов поджелудочной железой, усиливает высвобождение гастрина, возбуждает моторику желудка |
| Субстанция Р | Тонкая кишка | ЕС1-клетки | Усиливает моторику кишечника, слюноотделение, тормозит высвобождение инсулина |
| Вилликинин | Двенадцатиперстная кишка | ЕС1-клетки | Стимулирует ритмические сокращения ворсинок тонкой кишки |
| Энтерогастрон | Двенадцатиперстная кишка | ЕС1-клетки | Тормозит секреторную активность и моторику желудка |
| Серотонин | Желудочно-кишечный тракт | ЕС1,ЕС2-клетки | Тормозит выделение соляной кислоты в желудке, стимулирует выделение пепсина, активирует секрецию поджелудочной железы, желчевыделение, кишечную секрецию |
| Гистамин | Желудочно-кишечный тракт | ЕС2-клетки | Стимулирует выделение секрета желудка и поджелудочной железы, расширяет кровеносные капилляры, оказывает активирующее влияние на моторику желудка и кишечника |
| Инсулин | Поджелудочная железа | Бета-клетки | Стимулирует транспорт веществ через клеточные мембраны, способствует утилизации глюкозы и образованию гликогена, тормозит липолиз, активирует липогенез, повышает интенсивность синтеза белка |
| Глюкагон | Поджелудочная железа | Альфа-клетки | Мобилизует углеводы, тормозит секрецию желудка и поджелудочной железы, тормозит моторику желудка и кишечника |
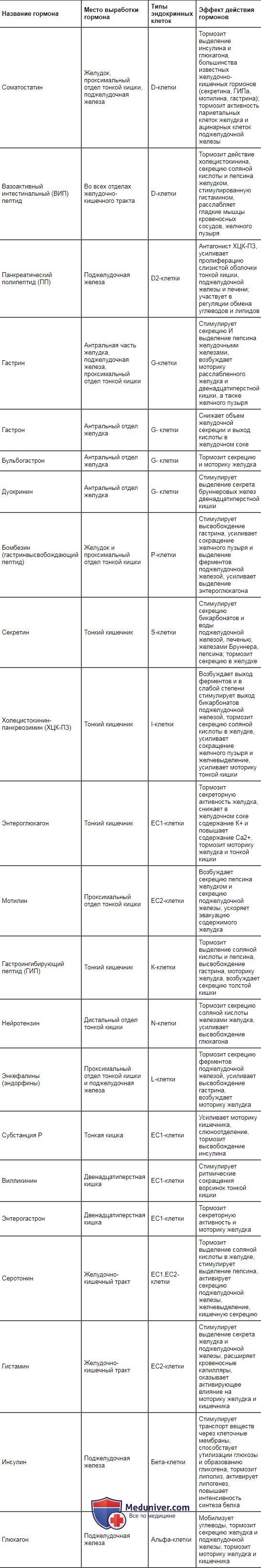
Место выработки основных гастроинтестинальных гормонов, вызываемые ими эффекты и продуцирующие их клетки представлены в табл. 11.1. В настоящее время обнаружено около 30 регуляторных пептидов. Как следует из представленной таблицы, они оказывают стимулирующее, тормозное и модулирующее влияние на секрецию пищеварительных соков, моторику гладкой мускулатуры желудочно-кишечного тракта, всасывание, выделение энтеринов эндокринными элементами слизистой оболочки желудка, кишечника и поджелудочной железы.
Выделение гастроинтестинальных гормонов имеет каскадный характер. Например, под влиянием гастрина обкладочные клетки желез желудка увеличивают выработку соляной кислоты, которая в слизистой оболочке тонкой кишки стимулирует выделение S- и J-клетками секретина и холеци-стокинна — панкреозимина. Секретин усиливает секрецию воды и бикарбонатов поджелудочной железой и печенью, а холецистокинин — панкреозимин — возбуждает выделение ферментов поджелудочной железой и тормозит секрецию соляной кислоты обкладочными клетками, усиливает моторику тонкой кишки и желчного пузыря.
Регуляторные пептиды, поступая в кровоток, быстро разрушаются в печени и почках и тем самым создают условия для осуществления эффектов других гастроинтестинальных гормонов.
Пища вначале попадает в ротовую полость, где в процессе пережевывания она не только измельчается, но и перемешивается со слюной, превращается в пищевой комок. Это перемешивание в ротовой полости осуществляется при помощи языка и мышц щек.

Пищеварительная система человека




Анатомия кишечника
Подвздошная кишка — нижний отдел тонкой кишки, отделяемой от слепой кишки илеоцекальным клапаном. Подвздошная кишка располагается в правой нижней части брюшной полости в области правой подвздошной ямки. Подвздошная кишка со всех сторон покрыта брюшиной. Какой-либо чётко выраженной анатомической структуры, разделяющей подвздошную и тощую кишки нет. Однако имеются различия между этими двумя отделами тонкой кишки: подвздошная имеет больший диаметр, стенка её толще, она богаче снабжена сосудами. Петли тощей кишки лежат главным образом влево от срединной линии, петли подвздошной кишки — главным образом справа от срединной линии.
Толстая кишка - это нижняя часть пищеварительного тракта, а именно нижняя часть кишечника, в которой происходит в основном всасывание воды и формирование из пищевой кашицы (химуса) оформленного кала.
Толстая кишка имеет длину 1,5 м, в свою очередь разделяется на слепую кишку, ободочную кишку и прямую кишку. В толстой кишке в основном усваивается вода, электролиты и клетчатка.
Слепая кишка - является начальным отделом толстой кишки и представляет собой слепой мешкообразный участок длиной от 3 до 8 см. Как правило, она полностью покрывается брюшиной. Свое название она получила вследствие своеобразного строения, напоминающего слепой мешок, в который с левой стороны впадает тонкая кишка. Сзади места соединения тонкой кишки со слепой отходит узкий, полый, слепо оканчивающийся червеобразный отросток - аппендикс, который представляет собой придаток слепой кишки. Он направлен большей частью к малому тазу и несколько изогнут. Однако расположение отростка может быть самым разнообразным.
Болезни органов пищеварения занимают важное место в структуре общей заболеваемости, представляя собой важную экономическую, социальную и медицинскую проблему. Результаты эпидемиологических исследований свидетельствуют об изменении структуры основных заб
Болезни органов пищеварения занимают важное место в структуре общей заболеваемости, представляя собой важную экономическую, социальную и медицинскую проблему. Результаты эпидемиологических исследований свидетельствуют об изменении структуры основных заболеваний верхнего отдела пищеварительного тракта: констатируется снижение частоты язвенной болезни и увеличение числа больных гастроэзофагеальной рефлюксной болезнью (ГЭРБ) в мире. В настоящее время ГЭРБ признана лидирующим по частоте заболеванием в гастроэнтерологии.

Взаимодействие между ЖКТ и ССС представляет несомненный интерес. Близость расположения с сердцем, общность иннервации способны при переполнении желудка, патологии пищевода по типу висцеро-висцеральных рефлексов провоцировать аритмии, имитировать ИБС. Патология верхнего отдела ЖКТ может приводить к функциональным расстройствам сердечно-сосудистой системы, возникающим опосредованно через ВНС. Большинство клинических проявлений ВСД, включая изменения синусового ритма и отчасти эктопические аритмии, зависит от дисбаланса вегетативных влияний. Так, не вызывает сомнения значительная роль нейровегетативных влияний на сердце, способствующих при их дисбалансе возникновению и поддержанию пароксизмальной фибрилляции предсердий (S. H. Hohnloser, A. van de Loo, M. Zabel 1994; P. Coumel 1992; Ю. Р. Шейх-Заде, 1990; Н. П. Потапова, Г. Г. Иванов, Н. А. Буланова, 1997; С. Г. Канорский, В. В. Сибицкий, 1999).
Далеко не последнюю роль в возникновении дисрегуляции ВНС занимают заболевания ЖКТ. Ю. В. Нявяраускус (диссер., 1987 г.) описал повышение тонуса парасимпатической НС, совпадающее с обострениями хронических заболеваний внутренних органов (желчнокаменная болезнь, грыжа пищеводного отверстия диафрагмы (ГПОД), ЯБ). Это дает основание полагать, что первичные заболевания внутренних органов у таких больных являлись главными этиопатогенетическими факторами, способствующими развитию вегетативной дисфункции синусового узла (ВДСУ).
Всего нами обследовано 99 пациентов, из них: первая группа — 35 пациентов с патологией пищевода и кардии (ГЭРБ и/или ГПОД); вторая группа — 31 человек с сочетанием ГЭРБ и/или ГПОД с ЯБ; третья группа — 33 пациента с ЯБ (условная группа сравнения). Средний возраст составил 37,0±10,1 лет.
В нашем исследовании в качестве группы сравнения были выбраны больные ЯБ.
ЯБ считается наиболее ярким примером психосоматических заболеваний в связи с тем, что изменения со стороны вегетативной нервной системы играют значимую роль как в возникновении самой болезни, так и ее клиническом течении. Вегетативные нарушения встречаются у 75–82% больных ЯБ (А. М. Вейн). При этом изменения ВНС выступают в качестве механизма, через который реализуются психосоматические взаимодействия.
Всем больным было проведено полное клиническое и инструментальное обследование в период обострения и через 6–8 нед после стандартной терапии основного заболевания.
Состояние слизистой оболочки пищевода оценивалось по модифицированной классификации M. Savary & G. Miller (1994) с учетом протяженности воспалительных изменений слизистой оболочки пищевода.
При полипозиционном рентгеноскопическом обследовании c контрастированием (cульфат бария) диагностировали грыжу пищеводного отверстия диафрагмы, устанавливали ее размеры и характер согласно классификации В. Х. Василенко и А. Л. Гребенева (1978), а также исключали осложненные формы болезни (стриктуры, язвы, опухоли).
Ультразвуковое исследование сердца (UltraMark-9, Канада) позволяло исключить клапанную патологию, множественные добавочные хорды, гемодинамически значимый пролапс клапанов, рубцовые изменения сердечной ткани, признаки сердечной недостаточности.
Проводили количественный и качественный анализ стандартной ЭКГ, при суточном мониторировании ЭКГ (Brentwood Holter System, Канада) оценивали качественные показатели ЭКГ и характеристики вариабельности сердечного ритма.
Успешность проведенной терапии оценивали по данным суточной рН-метрии и эндоскопии. Достоверных межгрупповых отличий в показателях суточной рН-метрии пищевода у больных основных групп не было выявлено.
Необходимо отметить, что 11 больным проведено одномоментное суточное мониторирование рН и ЭКГ. Цель исследования — проведение дифференциальной диагностики эзофагеальной псевдокоронарной боли от других возможных причин, установить индекс симптома, т. е. совпадение кардиальных симптомов (загрудинных болей, перебоев) с эпизодами ГЭР по данным суточной рН-метрии.
В 81,8% случаев эпизоды загрудинных болей ассоциировались с ГЭР и не сопровождались изменениями на ЭКГ. Положительный симптоматический индекс был отмечен у 63,6% пациентов.
В процессе лечения улучшилась эндоскопическая картина: уменьшилась доля эрозивных поражений пищевода РЭ II стадии с 35,3 до 2,9% и РЭ I стадии с 42,6 до 27,9%.
Исходно нормальная ЭКГ регистрировалась от 16 до 24% обследованных. Нарушения функции автоматизма определялись у 25,7–38,7% обследованных; нарушение проводимости — от 15 до 23% и сочетание этих 2 нарушений — у 13–23%, достоверно не отличаясь в отдельных группах.
Эктопическая активность, выявлявшаяся в среднем в 6% случаев на стандартной ЭКГ, фиксировалась значительно чаще при холтеровском мониторировании (ХМ) ЭКГ. При этом эктопическая активность при сочетании ГЭРБ и ЯБ оказалась выше, чем при изолированной ЯБ (χІ = 5,295; р = 0,021) за счет СВ экстрасистолии (χІ = 4,28; р = 0,039). По данным ХМ, отмечен прирост частоты сердечных сокращений (ЧСС) (минимальной, максимальной, средней; не более чем на 7%) после курса лечения. Значимых межгрупповых отличий не получено. С учетом качественных параметров ЭКГ и ХМ можно сделать вывод, что нарушения внутрижелудочковой проводимости встречались достоверно чаще у пациентов с рефлюкской болезнью и при ее сочетании с ЯБ в сопоставлении с группой сравнения. Кроме того, эктопическая активность, в том числе и суправентрикулярная экстрасистолия, была более характерна для больных ЯБ и РБ. При этом у лиц с эктопической активностью по сравнению без таковой не было достоверных отличий в ЭФИ-показателях (хотя только у больных первой и второй группы были больные с высокой точкой Венкебаха) и вегетативном тонусе, в то время как отмечена разница в некоторых спектральных параметрах. Так, для максимальной ЧСС F = 6,911 (р = 0,011); LF F = 4,102 (р = 0,047); SDNN F = 4,288 (р = 0,042). Можно предположить, что повышенная эктопическая активность у больных ГЭРБ связана с одновременным повышением симпатических и парасимпатических влияний на сердце, что не противоречит литературным данным, так как такие изменения вариабельности сердечного ритма (ВСР) считаются потенциально неблагоприятными. Наиболее аритмогенна ситуация с одновременным повышением симпатического и парасимпатического тонуса ВНС (R. D. Riley, E. L. Pritchett, 1997).
Существуют эпидемиологические работы, посвященные изучению частоты нарушений ритма и проводимости сердца. Так, Н. Г. Гоголашвили провел обследование 673 коренных жителей Республики Саха (82,1% жителей 5 типичных поселков). По данным стандартной ЭКГ, номотопные аритмии наблюдались у 49,9%; гетеротопии — у 6,7% обследованных; нарушения проводимости сердца — 9,5%; блокады сердца — 6,9%. Частота аритмий и нарушений проводимости в якутской популяции была следующей: синусовая аритмия — 33,9%; синусовая брадикардия — 12,8%; синусовая тахикардия —3,2%; АВБ — 3,9%; САБ — 0,2%; блокады правой ножки пучка Гиса (полная и неполная встречались в равной степени); желудочковая экстрасистолия (1-2 градации) — 4,2%; наджелудочковая экстрасистолия — 2,7%; мерцательная аритмия — 0,9%. Все случаи мерцательной аритмии изучались в возрасте 40 лет и старше. У 42,2% обследованных с гетеротопными нарушениями ритма сердца выявить заболевание сердца не удалось. У мужчин в возрасте от 16 до 39 лет сердечно-сосудистые заболевания вообще не выявлялись. ХМ было проведено методом случайной выборки у 174 человек. При ХМ, так же как и в нашем исследовании, наблюдалось увеличение гетеротопной активности: так, желудочковая экстрасистолия отмечена у 37,6% и наджелудочковая у 34,9%. Реже всего выявлялась пароксизмальная тахикардия (1,4% случаев) и мерцательная аритмия (1,4% случаев). Для диагностики ДСУ 46 пациентам была проведена чреспищеводная электрокардиостимуляция. Вегетативная дисфункция наблюдалась у 1,9%; синдром слабости синусового узла у 0,7% обследованных. По данным НИИ терапии СО РАМН, при изучении распространенности ЭКГ-изменений в неорганизованной популяции г. Новосибирска (1563 мужчин и 1550 женщин в возрасте 25–64 лет) нарушения АВ-проводимости регистрировались у 1,9% мужчин и 1,7% женщин; НВЖП — у 4,3% мужчин и у 2,2% женщин; полная блокада левой ножки пучка Гиса — 0,1%; аритмии у 7,2% мужчин и у 3,5% женщин; изменения зубца Т — 4,9% и 6,2% соответственно.
Для оценки функции синусового и атривентрикулярного (АВ) узлов было проведено ЭФИ сердца. Исходные данные превышали нормативные значения: ВВФСУмакс у 25,7%; 30,3% и 45,2% сравниваемых групп и КВВФСУсредн. у 20%, 18,2% и 22,58% соответственно. Дисфункция синусового узла вегетативного генеза была выявлена у 25,7% больных первой группы; 30,3% — второй и 45,2% — группы сравнения. Были определены особенности функционирования АВ-проводящей системы: у 1 больного (2,9%) первой группы и у 2 больных (6,1%) второй группы отмечено возникновение точки Венкебаха на частотах, превышающих 180 имп/мин. Межгрупповые отличия были значимы для показателей ВВФСУсредн., КВВФСУмин и ВВФСУмакс отличались у больных первой группы (р
Что такое вегето-сосудистая дистония (ВСД)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Патриной А.В., невролога со стажем в 17 лет.
Над статьей доктора Патриной А.В. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вегетососудистая дистония (ВСД) — это синдром, представленный в виде разнообразных нарушений вегетативных функций, связанных с расстройством нейрогенной регуляции и возникающих по причине нарушения баланса тонической активности симпатического и парасимпатич еского отдела в егетативной нервной системы [3] . Проявляется функциональными нарушениями, но обусловлены они субклеточными нарушениями [5] .
Краткое содержание статьи — в видео:
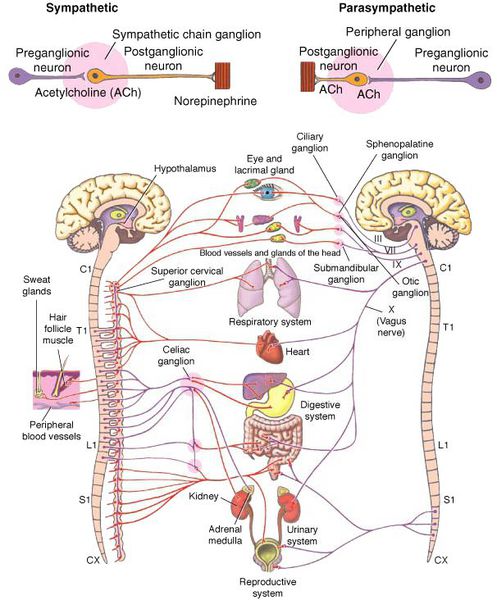
Что такое вегетативная нервная система (ВНС)
Вегетативная (автономная) нервная система (ВСН) является частью нервной системы организма, контролирующей деятельность внутренних органов и обмен веществ во всём организме. Она располагается в коре и стволе головного мозга, области гипоталамуса, спинном мозге, и состоит из периферических отделов. Любая патология этих структур, а также нарушение взаимосвязи с ВСН могут стать причиной возникновения вегетативных расстройств [1] .
Вегетососудистая дистония может возникнуть в разном возрасте, но преимущественно она встречается у молодых [5] .
Особенности проявления заболевания
- У мужчин и женщин. Женщины страдают от ВСД в два раза чаще мужчин, но различий в проявлениях болезни нет [3] .
- У подростков. ВСД распространена у подростков из-за активной гормональной перестройки организма.
- У беременных. ВСД у беременных также возникает в связи с гормональными изменениями. Опасные последствия: при гипотоническом типе ВСД — плацентарная недостаточность, гипоксия плода; при гипертоническом — гестозы, преэклампсия, эклампсия; отслойка плаценты; гипертонус матки, преждевременные роды.
Причины ВСД
ВСД — многопричинное расстройство, которое может выступать в качестве отдельного первичного заболевания, но чаще оно является вторичной патологией, проявляющейся на фоне имеющихся соматических и неврологических заболеваний [15] .
Факторы риска развития вегето-сосудистой дистонии подразделяются на предрасполагающие и вызывающие.
Вызывающие факторы:
- Психогенные[5] — острые и хронические психо-эмоциональные стрессы и другие психические и невротические расстройства [3] , которые являются основными предвестниками (предикторами) заболевания [10] . ВСД — это, в сущности, избыточная вегетативная реакция на стресс [9] . Часто психические расстройства — тревожный синдром депрессия — параллельно с психическими симптомами сопровождаются вегетативными: у одних пациентов преобладают психические, у других на первый план выходят соматические жалобы, что затрудняет диагностику [10] .
- Физические — переутомление, солнечный удар (гиперинсоляция), ионизирующая радиация, воздействие повышенной температуры, вибрация. Часто воздействие физических факторов связано с осуществлением профессиональных обязанностей, тогда они позиционируются как факторы профессиональной вредности [1] , которые могут вызывать или усугубить клиническую картину вегетососудистой дистонии. В таком случае имеются ограничения по допуску к работе с указанными факторами (приказ Минздрава РФ от 2021 года № 29).
- Химические — хронические интоксикации, злоупотребление алкоголем, никотином, спайсами и другими психоактивными веществами [5] . Проявления ВСД также могут быть связаны с побочными действиями некоторых лекарственных препаратов: антидепрессантов с активирующим действием, бронходилататоров, леводопы и препаратов, содержащих эфедрин и кофеин [10] . После их отмены происходит регресс симптомов ВСД.
- Дисгормональные — этапы гормональной перестройки: пубертат, климакс [3] , беременность, дизовариальные расстройства [5] , приём противозачаточных средств с периодами отмены [10] .
- Инфекционные — острые и хронические инфекции верхних дыхательных путей, мочеполовой системы, инфекционные заболевания нервной системы (менингиты, энцефалиты и другое) [5] .
- Иные заболевания головного мозга — болезнь Паркинсона, дисциркуляторная энцефалопатия (ДЭП), последствия черепно-мозговой травмы и другие [3] .
- Иные соматические заболевания — гастрит, панкреатит, гипертоническая болезнь, сахарный диабет, тиреотоксикоз [1] .
Предрасполагающие факторы:
- Наследственно-конституциональные особенности организма — заболевание возникает в детстве или в подростковом возрасте, со временем расстройство компенсируется, но восстановление нарушенных функций нестойкое, поэтому ситуация легко дестабилизируется под воздействием неблагоприятных факторов [10] .
- Особенности личности[5] — усиленная концентрация внимания на соматических (телесных) ощущениях, которые воспринимаются как проявление болезни, что, в свою очередь, запускает патологический механизм психо-вегетативной реакции [6] .
- Неблагоприятные социально-экономические условия — состояние экологии в целом, низкий уровень жизни, экономический кризис в стране, жилищные условия отдельных людей, культура питания (приверженность фастфуду, удешевление производства продуктов питания за счёт использования ненатурального сырья), культура спорта (несмотря на активное строительство спортивных комплексов, всё-таки полноценная интеграция спорта в повседневную жизнь населения не происходит) [5] . Также речь идёт об особенности климата в центральной части России с дефицитом ультрафиолетового излучения в холодное время года, что приводит к обострению многих хронических заболеваний в осенне-весенний период, в том числе и ВСД [1] .
- Патологии перинатального (дородового) периода — внутриутробные инфекции и интоксикации, резусконфликты, внутриутробная гипоксия (кислородное голодание), гестозы матери, фетоплацентарная недостаточность и другие [6] .
Мясищев В.Н., выдающийся отечественный психотерапевт, полагает, что ВСД развивается в результате влияния психо-эмоциональных нарушений на имеющиеся вегетативные аномалии [13] .
Также заболевание может возникать и у здоровых людей как транзиторная (временная) психофизиологическая реакция на какие-либо чрезвычайные, экстремальные ситуации [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы вегето-сосудистой дистонии
ВСД характеризуется проявлением симпатических, парасимпатических или смешанных симптомокомплексов [1] . Преобладание тонуса симпатической части ВСН (симпатикотония) выражается в тахикардии, бледности кожи, повышении артериального давления, ослаблении сокращений стенок кишечника (перистальтике), расширении зрачка, ознобе, ощущении страха и тревоги [2] . Гиперфункция парасимпатического отдела (ваготония) сопровождается замедлением сердцебиения (брадикардией), затруднением дыхания, покраснением кожи лица, потливостью, повышенным слюноотделением, снижением артериального давления, раздражением (дискинезией) кишечника [2] .
Читайте также:

