Какие перспективы в развитии народного хозяйства открывает использование трансгенных животных кратко
Обновлено: 06.07.2024
По применению трансгенных животных можно разделить на пять основных категорий: научные модели, модели для изучения болезней человека, источники для производства фармацевтических препаратов, источники ксенотрансплантантов и источники пищи. Большинство из обсуждаемых ниже областей коммерческого применения трансгенных животных в настоящее время находятся на ранних этапах исследований и разработки, за некоторыми исключениями. Так, с 2004 г. в зоомагазинах некоторых стран (США, Тайвань, Китай, Малайзия) продаются декоративные трансгенные рыбки, окраска которых обусловлена присутствием флуоресцентных белков из кораллов.
Важной вехой в истории применения трансгенных животных стал 2006 г., когда Европейское медицинское агентство (the European Medicines Agency (EMEA)) выдало первое разрешение на коммерческое использование первого рекомбинантного белка из молока трансгенного животного. Им стал рекомбинантный антитромбин III с коммерческим названием ATryn, который предназначен для профилактического лечения пациентов с врожденной антитромбиновой недостаточностью.
Научные модели. Сложность генома млекопитающих, длительные периоды взросления и размножения, трудности изучения большого числа индивидуальных животных с учетом варьирования признаков делают генетический анализ этих систем затруднительным. Трансгенная технология несет в себе большие возможности, в первую очередь, для фундаментальных исследований принципов функционирования геномов и отдельных генов. Например, линии нокаутных мышей, гомозиготных по направленно-инактивированным генам, позволяют изучать детерминируемые данными генами свойства на уровне организма. Регулируемые системы экспрессии трансгенов дают возможность исследовать тонкие механизмы воздействия продуктов того или иного гена на физиологию и эмбриональное развитие животных.
Модельные системы для изучения болезней человека. Используя целых животных, можно моделировать возникновение патологии, исследовать ее развитие и способы лечения. И хотя данные, полученные на трансгенных моделях, не всегда можно экстраполировать на человека в медицинских аспектах, они позволяют выявить ключевые моменты этиологии сложной болезни, ее молекулярные основы и подсказать пути лечения. В настоящее время на мышах смоделированы такие заболевания человека, как СПИД, болезнь Альцгеймера, артрит, мышечная дистрофия, гипертония, образование опухолей, нейродегенеративные нарушения, дисфункция эндокринной системы, сердечно-сосудистые заболевания и многие другие. Получена дрозофила с болезнью Паркинсона.
Источники для производства фармацевтических белков. Существующие методы получения в культурах клеток рекомбинантных человеческих протеинов для медицинских целей имеют ряд существенных недостатков и жестких законодательных ограничений. Одной из особенностей таких медицинских препаратов является их крайне высокая цена, обусловленная в том числе высокой стоимостью клеточного культивирования. Преодолевая эти ограничения, большое количество белков можно получать из молока трансгенных животных, несущих человеческие гены, ответственные за выработку определенного протеина, под контролем промоторов, специфичных для молочных желез. Предполагается, что выход может составить до 35 г белка из одного литра молока при относительно невысокой стоимости производства и очистки.

Таблица 2.3. Терапевтические белки из молока трансгенных животных, готовящиеся к выпуску на фармацевтический рынок
Успешная регистрация препарата ATryn продемонстрировала правильность такого подхода к продукции терапевтических белков и облегчила путь на рынок другим рекомбинантным препаратам из молока трансгенных животных, а также стимулировала научную и коммерческую активность в данной области.
Другим источником продукции рекомбинантных белков является кровь трансгенных животных. Получены трансгенные бычки, продуцирующие биспецифичные антитела человека в своей крови. Эти антитела после очистки из сыворотки были очень стабильны и соответствующим образом стимулировали Т-клеточное уничтожение раковых клеток.
Получение трансгенных цыплят открыло возможность использовать яйца, содержащие немало запасных белков для накопления нужных рекомбинантных белков - активных компонентов лекарственных средств. В этом случае белки можно получать в больших количествах, и их производство будет дешевым, так как сырьем для этого является всего лишь птичий корм. В институте Рослин, где была клонирована Долли, разработаны 2 линии трансгенных кур с перспективой на коммерческое применение.
Одна из линий несет яйца с антителами miR24 в яичном белке, с помощью которых можно будет лечить злокачественную меланому - форму рака кожи, другая производит человеческий интерферон в-1a, который может быть использован для остановки внутриклеточного размножения вирусов. Разрешение на клинические испытания препарата против рака на основе куриных яиц уже получено. В настоящее время продолжаются работы по увеличению выхода рекомбинантных белков, как на стадии производства, так и на стадии очистки.
Чтобы обезопасить рекомбинантные продукты, руководство, разработанное в США и Европейском союзе для получения ГМ-животных, требует контролировать здоровье трансгенных животных, проверять корректность полученных трансгенных конструкций, характеризовать очищенный рекомбинантный белок, а также провести новую трансгенную линию через несколько поколений.
В России также ведутся разработки в области получения трансгенных животных для биопродукции важных белков.
Например, существует государственная программа, нацеленная на создание фармакологического производства человеческого лактоферрина путем секреции в молоко коз. Сильные антибактериальные свойства лактоферрина, содержащегося в грудном молоке, защищают новорожденных детей от инфекций, поэтому получение молока с лактоферрином в больших количествах может стать новой отраслью производства детского питания.
Решением этой проблемы могла бы быть пересадка человеку органов животных. Так, например, органы свиньи подходят человеку по своему строению, размеру и многим биохимическим показателям, но такие пересадки невозможны, так как эти органы будут немедленно отторгнуты иммунной системой пациента.
В настоящее время ряд исследовательских центров работают над выведением генетически модифицированных свиней, органы которых могут быть использованы для трансплантации. Необходимыми условиями для успешной ксенотрансплантации являются:
1) преодоление иммунологических барьеров (гистосовместимость),
2) недопущение переноса патогенов от донорного животного человеку,
3) анатомическая и физиологическая совместимость донорного органа с человеческим.
С помощью соматического ядерного переноса получены животные, у которых супрессирован пока первый иммунологический барьер - реакция отторжения немедленного типа (гиперактивное отторжение). ГМ-свиньи синтезировали человеческие регуляторы комплемента (RCAs) и/или не имели генов 1,3-a-galactosyltransferase (a-gal), кодирующих фермент, ответственный за выработку на поверхности клеток свиньи углеводных антигенов, которые приводят к гиперактивному отторжению.
Первые эксперименты по пересадке свиных трансгенных почек и сердца нечеловекообразным приматам (павианы) с иммунной супрессией показали отсутствие реакции отторжения немедленного типа, но выживаемость пересаженных органов составляла всего 2-6 месяцев. Работы по получению свиней-ксенотрансплантеров с множественными трансгенами, критичными для преодоления других иммунологических барьеров, продолжаются.
Недавние исследования показали, что риск передачи человеку свиных ретровирусов чрезвычайно мал, это открывает путь для доклинических испытаний свиных ксенотрансплантантов. Кроме того, этот факт позволяет использовать свиной эндогенный ретровирус (PERV) в качестве вектора для эффективной доставки экзогенной ДНК в клетки. После селекции такие клетки могут стать родоначальниками трансгенных свиней-ксенотрансплантеров, полученных соматическим ядерным переносом. Также в рамках программы получения свиней для трансплантации несколько компаний занимаются выведением пород свиней с размерами органов, близкими к человеческим.
Следует отметить, что, несмотря на многолетние исследования, пересадка человеку органов свиньи все еще является отдаленным проектом.
Трансгенные животные, служащие источником пищи, еще очень далеки от коммерческого использования, хотя очень много различных вариантов уже создано. Например, в геном свиней удалось встроить несколько ускоряющих рост генов, которые также оказывают влияние на качество мяса, делая его более постным и нежным. Эта работа начата более 10 лет назад, однако в силу определенных негативных морфологических и физиологических изменений, наблюдавшихся у животных, этот вариант не был коммерциализован. Скорее всего, негативные изменения в данных трансгенных свиньях были обусловлены несовершенством использованной генетической конструкции, так что работы в этом направлении продолжаются.
Предложено также большое количество модификаций молока крупного рогатого скота, заключающихся в добавлении новых белков либо в манипуляциях над эндогенными протеинами. Например, были созданы животные, продуцирующие молоко для детского питания, по своему составу максимально приближенное к материнскому молоку человека. Другой пример -недавно ученые из Новой Зеландии получили коров с повышенным содержанием в молоке казеина.
Использование такого молока должно повысить продуктивность сыроваренного производства. Еще несколько групп исследователей работают над снижением содержания в молоке лактозы. Конечной целью является создание молока, пригодного для употребления в пищу людьми с лактозной непереносимостью.
Пока ближе всех на пути к коммерциализации находятся фитазные трансгенные свиньи (экосвиньи, enviropigs), целью создания которых было резкое уменьшение навозного загрязнения окружающей среды. Эта линия несет ген бактериальной фитазы под транскрипционным контролем тканеспецифичного промотора слюнных желез.
Секретируемая рекомбинантная фитаза позволяет свиньям расщеплять растительные фитаты (инозитол гексафосфат, ИГФ - наиболее распространенная нерастворимая форма органического фосфора почвы), что уменьшает выход загрязняющих окружающую среду фекальных токсичных соединений фосфора (до 75 %). Ожидается выход этих свиней на рынок в следующие несколько лет.
С учетом предполагаемого повышения потребности в рыбопродуктах ГМ-рыба может приобрести большое значение как продукт питания. Наиболее вероятно, что первым ГМ-животным на продовольственном рынке станет быстрорастущая семга (Salmo salar), в геном которой встроен ген гормона роста чавычи (Oncorhynchus tschawytscha). Такая семга растет в 3-4 раза быстрее нетрансгенных аналогов, что значительно уменьшает время выращивания. Еще, по крайней мере, 8 искусственно выращиваемых видов рыбы генетически модифицированы с целью ускорения роста. Ген гормона роста в порядке опыта встроили в геномы таких рыб, как белый амур, радужная форель, тиляпия и сом. Во всех случаях трансгены выделяли из геномов рыб других видов.
Трансгенные домашние любимцы. Пока что самым успешным случаем коммерциализации трансгенных животных можно считать декоративных рыбок. Трансгенная аквариумная рисовая рыбка Oryzias latipes, яркая зеленая окраска которой обусловлена встроенным геном зеленого флуоресцентного белка из медуз, продвигается на рынок тайваньской компанией Taikong.
Под торговой маркой GloFish в США продаются (5 дол./шт.) разноцветные рыбки-зебры Danio rerio, окрашенные флуоресцентными белками кораллов. При соответствующем освещении красные, зеленые и желтые рыбки начинают ярко флуоресцировать, хотя природная окраска D. rerio скромного серого цвета. В Европе, Канаде и Австралии трансгенные рыбки запрещены, видимо, вследствие общих предубеждений против трансгенных животных. Дискуссии сторонников и противников трансгенных животных продолжаются.
Трансгенные животные, примеры которых будут приведены ниже, были получены экспериментальным путем. Они содержат во всех своих клетках дополнительную ДНК-трансген, внедренную в клетки животного с хромосомами и там реализующуюся. Трансген наследуется, согласно законам Менделя.

Причины создания
Трансгенные растения и животные различаются степенью сложности своего создания. Животные используются для решения теоретических задач в биомедицине и сельском хозяйстве. Среди причин создания трансгенных организмов можно обозначить следующие:
- животные с геном гормона роста в равных условиях содержания выдают повышенные темпы роста;
- для усиления иммунитета к инфекциям;
- для получения биологически активных веществ;
- для получения человеческого белка от трансгенных животных;
- использование животных как биореакторов для получения медпрепаратов.
Первые такие животные были получены в 1974 году в Кембридже ученым по имени Рудольф Яниш. Он в эмбрион мыши ввел ДНК-вирус обезьяны. В России первые трансгенные животные были выведены в 1982 году.
Получение
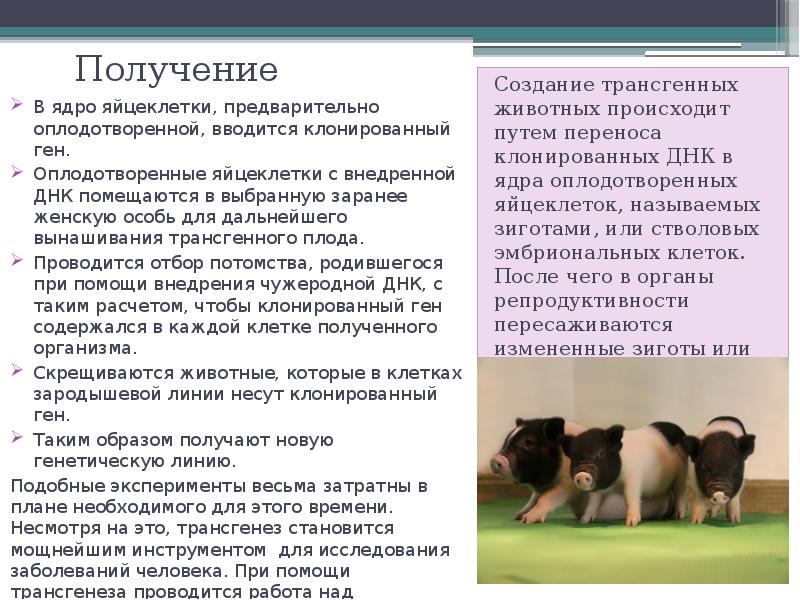
Зачем нужны трансгенные животные? Их создание происходит путем переноса клонированных ДНК в ядра оплодотворенных яйцеклеток, называемых зиготами, или стволовых эмбриональных клеток. После чего в органы репродуктивности пересаживаются измененные зиготы или яйцеклетки.
Если не вдаваться в подробности, то весь процесс заключается в следующем:
- В ядро яйцеклетки, предварительно оплодотворенной, вводится клонированный ген.
- Оплодотворенные яйцеклетки с внедренной ДНК помещаются в выбранную заранее женскую особь для дальнейшего вынашивания трансгенного плода.
- Проводится отбор потомства, родившегося при помощи внедрения чужеродной ДНК, с таким расчетом, чтобы клонированный ген содержался в каждой клетке полученного организма.
- Скрещиваются животные, которые в клетках зародышевой линии несут клонированный ген.
- Таким образом получают новую генетическую линию.
Подобные эксперименты весьма затратны в плане необходимого для этого времени. Несмотря на это, трансгенез становится мощнейшим инструментом для исследования заболеваний человека. При помощи трансгенеза проводится работа над генетической модификацией молочных желез животных для получения из молока белка, идентичного человеческому, а также для изготовления фармацевтических препаратов.
Методы трансгенеза животных
Для чего они нужны? Трансгенные животные – это отдельные особи, геном которых отличается искусственно дополненной генетической информацией. Трансген представляет собой в одном случае самостоятельный участок ДНК с собственными регуляторными последовательностями. В другом - это созданный из различных молекул ДНК-гибридный (рекомбинантный) ген.
Трансген – это введенный искусственно и закрепившийся в ДНК животного чужеродный ген. А трансгенез – это процесс интеграции и переноса в геном животного чужеродной генетической информации.
Существуют определенные методы получения трансгенных животных. Среди них выделяют:
- Микроинъекционный метод.
- Метод использования ретровирусных векторов.
- Пересадка ядер клеток, которые культивируются in vitro.
- Метод липосом – переносчиков ДНК.
- Метод использования половых клеток семенников.
Метод микроинъекции
Впервые для получения трансгенных животных был использован именно метод микроинъекции. Это произошло в 1985 году одновременно в двух исследовательских лабораториях. Одна из них принадлежала США, другая находилась в Германии. В настоящее время этот метод является наиболее часто используемым.
Способ микроинъекции основан на введении раствора генных конструкций в мужской пронуклеус (предшественник ядра) зигот. При оплодотворении в яйцеклетке образуются два ядра, одно из которых мужское (мужской пронуклеус), другое - женское (женский пронуклеус). Мужской и женский пронуклеусы после сближения объединяются в общее ядро с соединением отцовских и материнских хромосом в один генотип эмбриона.
Об успешности микроинъекции можно судить по увеличению объема пронуклеуса в 1,5 раза. Когда процедура завершается, получившиеся эмбрионы несколько часов культивируются, а затем подсаживаются в матку одновременно нескольким самкам.
После рождения потомства производится анализ на интеграцию трансгена путем отбора проб. Число трансгенных малышей от общего числа родившегося при помощи данного метода потомства весьма незначительно. У испытуемых мышей это примерно 15 %, у свиней - от 10 до 15 %, у овец, коз и крупного рогатого скота этот показатель лавируется от 5 до 10 %. Над улучшением данного соотношения ученые работают по сей день.
Метод использования ретровирусных векторов
Перенос ДНК в эмбриональные линии животных при помощи ретровирусных векторов – это довольно результативный метод. Ретровирусы являются ядросодержащими вирусами. Их генетический материал – это одноцепочечная рибонуклеиновая кислота (РНК).

Ретровирусы могут быть экотропными, то есть способными воспроизводиться в клетках одного вида животных или нескольких близкородственных видов. Например, вирус лейкимии мыши может размножаться только в клетках мыши или крысы. Амфотропные же вирусы способны к распространению во многих видах животных.
Ретровирус проникает в клетку при помощи микропиноцитоза – транспорта небольших по размеру молекул. У одних вирусов транскрипция происходит в ядре клетки, у других - в цитоплазме. Если интеграция случается в геноме генеративных клеток, то ретровирусы передаются потомству по наследству. Здесь идет речь об эндогенных ретровирусах.
Впервые вирусная ДНК была обнаружена в клетках взрослой мыши в 1974 году. Инфекция зигот в большинстве случаев приводит к получению трансгенных животных, так как интеграция возможна, если клетка вступает в непрямое деление после репликации ДНК.

Преимущества использования ретровирусных векторов:
- Почти 100 % эмбрионов, обработанных ретровирусом, могут быть инфицированы.
- Становится возможным проведение генной терапией наследственных заболеваний.
- Ретровирусы делают возможной трансформацию отдельных органов (например, молочных желез для повышения удоя).
Недостатки использования ретровирусных векторов:
- Ограниченная емкость.
- Подавление экспрессии трансгенов in vivo.
- Низкий титр (решена при помощи псевдотипирования).
- Возможность клеточных онкогенов.
- Невозможность передачи по наследству трансформации отдельных органов.
Метод пересадки ядер клеток
Особенностью метода является использование трансформированных клеточных линий для получения трансгенных особей при помощи генных конструкций. Для этого берутся стволовые линии, а также соматические клетки, которые культивируются in vitro, то есть в пробирке.
Одним из методов пересадки ядер является метод микроманипуляции, и заключается он в следующем:
- При помощи микропипетки происходит извлечение пронуклеусов после того, как произошло прокалывание зон пеллюцида и зон плазматической мембраны.
- Пипеткой с большим диаметром в тот же прокол вводится ядро с полным набором хромосом от донора.
При помощи такого метода цитоплазма зиготы травмируется намного меньше, как и донорское ядро.
Существует еще один способ трансплантации ядра. Этот метод заключается в использовании для этой цели цитохалазинов, то есть веществ, которые синтезированы при помощи грибов. Структура микроферментов (нитей, состоящих из молекул глобулярного белка актина) разрушается цитохалазином В, после чего ядро может быть расположено уникальным образом.
Ядро при помощи тоненькой нити цитоплазмы остается соединенным с клеткой. Затем эта связь искусственно разрывается при помощи центрифугирования. Образуются цитопласты (клетки без ядра) и кариопласты (ядра, окруженные цитоплазмой). В градиенте плотности цитопласты отделяются от интактных клеток, и могут быть использованы для соединения с кариопластами других клеток, чтобы получилась жизнеспособная клетка.
Метод липосом – переносчиков ДНК
Это самый безвредный метод трансгенеза. Его особенность заключается в использовании липосом для сохранения и переноса в них генов. Липосомы создаются с различными свойствами. Они не иммуногены и не обладают токсичностью.
Однако данный метод не является эффективным, потому что ДНК, транспортированная таким образом в клетку, сразу же захватывается лизосомами и разрушается ими.
Метод использования половых клеток семенников
Сперматозоиды – это природный вектор, который транспортирует ДНК в клетку. Но проводимые в этой области исследования показали неоднозначные результаты метода. В экспериментах М. Lavitrano в 1989 году 30 % опытных мышей, которые были получены при помощи инъекций измененных сперматозоидов в неоплодотворенные яйцеклетки мыши, оказались трансгенными и могли передавать трансген по наследству.
В другом случае множество попыток повторить этот результат в других лабораториях не увенчались успехом, при сходных условиях были получены разные результаты. Из всего этого можно сделать предположение, что удачная трансформация ДНК наблюдается только на определенной стадии клеточного цикла. До сих пор ведутся исследования в области определения механизма встраивания экзогенной ДНК в геном сперматозоида.
Возможность использования после криоконсервации сперматозоидов является положительным моментом данного метода. Отрицательной же стороной считается большое количество микроманипуляций, необходимых при трансгенезе при помощи этого способа.
Но все же сперматозоиды имеют способность поглощать ДНК и накапливать ее в ядре. Для достижения большего эффекта соединения ДНК со сперматозоидом существует несколько методов: липосомный, инъекция в семенники, в семенные канальцы при помощи создания пор в липидной мембране под действием электрического поля.
Выключенные гены
Выключение гена – это подавление экспрессии генов, то есть сайленсинг генов или генный нокаут. При этом процессе экспрессия необходимого гена прекращается, но последовательность нуклеотидов остается неизменной.

Выключение гена может происходить при переносе информации с ДНК на РНК, то есть транскрипции, и после нее. Механизмы выключения генов защищают организм от вирусов и прыгающих генов. Поэтому сайленсинг является частью иммунной системы, которая защищает от чужеродной ДНК. Трансгенные животные с выключенными генами и их создание называются генным таргетингом.
Наследование генов, согласно законам Менделя
Законы Менделя описывают особенности передачи от организма родителя к организму детеныша характеристик, несущих наследственность. Данные принципы находятся в основе классической генетики. В основном во всех научных статьях раскрывается одно из правил Менделя и пара законов.
Правило первого поколения гибридов и их единообразие гласит о том, что данные гибриды всегда наследуют один из признаков родителя.
Закон расщепления признаков является первым законом Менделя. В нем говорится о том, что у ¾ подопытных животных выявились доминантные признаки, а у ¼ - рецессивные.
Закон независимого наследования признаков является вторым законом. Здесь Менделем описывается распределение признаков при скрещивании полигибридном и дигибридном.
Полезные свойства
Создание трансгенных животных с новыми полезными свойствами – это процесс непрекращающийся.
Трансгенные животные, примеры которых приведены ниже, уже существуют в современном мире:
- В Великобритании при помощи трансгенеза были выведены овцы. Молоко этих животных содержит в себе фактор, способствующий свертыванию крови.

- У трансгенных свиней, созданных в России, был изменен обмен веществ посредством введения гена соматотропина, что позволило снизить жирность мяса.
- Американцы работают над созданием коров, в чьем молоке содержится человеческий альбумин, который используется для поддержания нормального давления крови.
Перспективы использования трансгенных животных
В ближайшем будущем предполагается создание таких животных, одни гены которых нокаутированы, а другие введены в состав их генома.
Предполагается, что такое молоко в своем составе будет максимально приближено к составу материнского молока человека. В этом направлении проводится работа с эмбриональными стволовыми клетками.

- Использование трансгенных животных для получения органов, которые пересаживаются человеку.
Не секрет, что человечество нуждается в донорских органах. Сейчас генетики ведут работу над выращиванием таких органов в теле животных. Например, органы свиней вполне могли бы подойти по своему размеру и составу. Но они будут незамедлительно отторгнуты человеческой иммунной системой. Чтобы этого не происходило, создается трансгенная свинья, у которой выключены гены гистосовместимости, а вместо них внедрены гены гистосовместимости человека.

Создание трансгенных животных - трудозатратный процесс. Согласно статистике, на 100 инъецированных зигот овцы, 40 мышиных зигот и 1500 зигот коровы приходится менее 50% особей, экспрессирующих трансгенный белок. При удачной попытке получения трансгенного животного совсем необязательно, что его потомками будет наследован трансген. Поэтому клонирование животного с необходимыми генетическими параметрами – есть оптимальный выход из положения.
Какие перспективы в развитии народного хозяйства открывает внедрение трансгенных животных?
- Виталька Уланский
- Подготовка к ЕГЭ/ОГЭ
- 2019-11-03 14:10:11
- 2
- 1
Трансгенные животные, экспериментально полученные животные, содержащие во всех клеточках собственного организма дополнительную интегрированную с хромосомами и экспрессирующуюся чужеродную ДНК (трансген), которая передается по наследию по законам Менделя. Иногда трансген может реплицироваться и передаваться по наследию как экстрахромосомный автономно реплицирующийся кусок ДНК. Разработка творенья трансгенных животных является одной из более бурно развивающихся биотехнологий в заключительные 10 лет. Трансгенные животные широко используются как для решения великого числа теоретических задач, так и в практических целях для биомедицины и сельского хозяйства. Некоторые научные трудности не могли бы быть решены без творенья трансгенных животных. На модели трансгенных лабораторных животных проводятся широкие исследования по исследованию функции разных генов, регуляции их экспрессии, фенотипическому проявлению генов, инсерционному мутагенезу и др. Трансгенные животные главны для разных биомедицинских исследований. Существует огромное количество трансгенных животных, моделирующих различные заболевания человека (рак, атеросклероз, ожирение и др.). Так, получение трансгенных свиней с модифицированной экспрессией генов, определяющих отторжение органов, позволит использовать этих животных для ксенотрансплантации (пересадки органов свиньи человеку).
Вы можете изучить и скачать доклад-презентацию на тему Зачем нужны трансгенные животные ?. Презентация на заданную тему содержит 9 слайдов. Для просмотра воспользуйтесь проигрывателем, если материал оказался полезным для Вас - поделитесь им с друзьями с помощью социальных кнопок и добавьте наш сайт презентаций в закладки!








В настоящий момент исследования в данной области развиваются по нескольким направлениям: В настоящий момент исследования в данной области развиваются по нескольким направлениям: 1. Создание новых животноводческих пород, дающих продукты с повышенным содержанием некоторых компонентов (например, в Великобритании существует стадо коров, молоко которых идеально подходит для приготовления сыра чеддер). 2. Создание животных, способных продуцировать несвойственные их виду белки (например, сообщалось о разработках направленных на получение свиней, способных продуцировать интерферон человека). 3. Создание трансгенных животных, являющихся донорами при трансплантациях органов человеку.
Причины создания Трансгенные растения и животные различаются степенью сложности своего создания. Животные используются для решения теоретических задач в биомедицине и сельском хозяйстве. Среди причин создания трансгенных организмов можно обозначить следующие: животные с геном гормона роста в равных условиях содержания выдают повышенные темпы роста; для усиления иммунитета к инфекциям; для получения биологически активных веществ; для получения человеческого белка от трансгенных животных; использование животных как биореакторов для получения медпрепаратов. Первые такие животные были получены в 1974 году в Кембридже ученым по имени Рудольф Яниш. Он в эмбрион мыши ввел ДНК-вирус обезьяны. В России первые трансгенные животные были выведены в 1982 году.
Получение В ядро яйцеклетки, предварительно оплодотворенной, вводится клонированный ген. Оплодотворенные яйцеклетки с внедренной ДНК помещаются в выбранную заранее женскую особь для дальнейшего вынашивания трансгенного плода. Проводится отбор потомства, родившегося при помощи внедрения чужеродной ДНК, с таким расчетом, чтобы клонированный ген содержался в каждой клетке полученного организма. Скрещиваются животные, которые в клетках зародышевой линии несут клонированный ген. Таким образом получают новую генетическую линию. Подобные эксперименты весьма затратны в плане необходимого для этого времени. Несмотря на это, трансгенез становится мощнейшим инструментом для исследования заболеваний человека. При помощи трансгенеза проводится работа над генетической модификацией молочных желез животных для получения из молока белка, идентичного человеческому, а также для изготовления фармацевтических препаратов.
Трансгенные животные, примеры которых приведены ниже, уже существуют в современном мире: Трансгенные животные, примеры которых приведены ниже, уже существуют в современном мире: В Великобритании при помощи трансгенеза были выведены овцы. Молоко этих животных содержит в себе фактор, способствующий свертыванию крови. У трансгенных свиней, созданных в России, был изменен обмен веществ посредством введения гена соматотропина, что позволило снизить жирность мяса. Американцы работают над созданием коров, в чьем молоке содержится человеческий альбумин, который используется для поддержания нормального давления крови.
Перспективы использования трансгенных животных В ближайшем будущем предполагается создание таких животных, одни гены которых нокаутированы, а другие введены в состав их генома. 1). Получение модифицированного молока. Предполагается, что такое молоко в своем составе будет максимально приближено к составу материнского молока человека. В этом направлении проводится работа с эмбриональными стволовыми клетками. 2). Использование трансгенных животных для получения органов, которые пересаживаются человеку. Не секрет, что человечество нуждается в донорских органах. Сейчас генетики ведут работу над выращиванием таких органов в теле животных. Например, органы свиней вполне могли бы подойти по своему размеру и составу. Но они будут незамедлительно отторгнуты человеческой иммунной системой. Чтобы этого не происходило, создается трансгенная свинья, у которой выключены гены гистосовместимости, а вместо них внедрены гены гистосовместимости человека.
3). Клонирование трансгенных животных. 3). Клонирование трансгенных животных. Создание трансгенных животных - трудозатратный процесс. Согласно статистике, на 100 инъецированных зигот овцы, 40 мышиных зигот и 1500 зигот коровы приходится менее 50% особей, экспрессирующих трансгенный белок. При удачной попытке получения трансгенного животного совсем необязательно, что его потомками будет наследован трансген. Поэтому клонирование животного с необходимыми генетическими параметрами – есть оптимальный выход из положения.
Читайте также:

