Гиперденсное образование что это такое кратко
Обновлено: 05.07.2024
Вам поставили диагноз: опухоль надпочечника?
Наверняка вы задаётесь вопросом: что же теперь делать?
Предлагаем Вашему вниманию краткий, но очень подробный обзор опухоли надпочечника. Его подготовили высоко квалифицированные специалисты онкологическо-урологического отделения НИИ урологии и интервенционной радиологии имени Н.А. Лопаткина к.м.н. Ирина Огнерубова и Павел Пеньков под руководством заведующего отделением к.м.н. Александра Качмазова.
Данная брошюра содержит информацию о диагностике и лечении опухоли надпочечника. Здесь собраны основные методики лечения данного заболевания, в том числе, последние разработки отечественных и зарубежных ученых-онкологов.
Мы хотим Вам помочь победить рак!
Филиалы и отделения, где лечат рак почки
Введение
Надпочечники (glandulae suprarenales, adrenalеs) – парный орган, железы внутренней секреции, вырабатывающие биологически активные вещества - гормоны. Каждый надпочечник (правый треугольной формы, левый – полулунный) располагается над верхним полюсом почки (Рис.1). Масса и размеры надпочечника индивидуальны. У взрослого масса варьирует от 7 до 20 г (в среднем 11-18г), продольный размер достигает 6 см, поперечный - до 3 см, толщина ≥ 1 см. Надпочечник состоит из паренхимы, заключенной в тонкую фиброзную капсулу от которой в толщу железы отходят отростки. Структурными элементами паренхимы являются: наружный корковый слой, cortex (более толстый, желтовато-коричневого цвета, представлен железистой и соединительной тканью) и внутренний мозговой слой, medulla (буровато-красного цвета, образован хромафинными и симпатическими нервными клетками) (Рис.2). Корковое вещество надпочечников состоит из трех зон и продуцирует гормоны - кортикостероиды: в клубочковой зоне вырабатываются минералкортикоиды (альдостерон), в пучковой зоне- глюкокортикоиды (гидрокортизон, кортикостерон), в сетчатой зоне - половые гормоны (андрогены). Действие кортикостероидов очень разнообразно и заключается в регулировании белкового, жирового, углеводного, водно-солевого обмена веществ. Гормонами мозгового вещества являются катехоламины – адреналин и норадреналин. Они принимают участие в функционировании органов и систем в экстремальных условиях (стресса): усиливают сокращение сердечной мышцы, оказывают сосудосуживающее действие, повышая артериальное давление, изменяют уровень сахара в крови.

Рис.1. Расположение надпочечников.

Рис.2. Строение надпочечника
Адренокортикальный рак надпочечников (рак коры надпочечников)
Адренокортикальный рак (АКР) – редкая злокачественная опухоль исходящая из коркового слоя надпочечников. Частота встречаемости АКР составляет 0,7-2 случая на 1 млн населения в год. Женщины заболевают АКР чаще мужчин (55-60%). Средний возраст заболевших 46 лет (пик заболеваемости 40-60 лет).
Рак коры надпочечников может быть гормонально-активным, избыточно продуцируя гормоны, и гормонально-неактивным, когда секреция гормонов остается в пределах физиологической нормы. Гормонально-активный АКР наблюдается у 50-60% больных.
Факторы риска адренокортикального рака надпочечников
У взрослых в подавляющем большинстве АКР является спорадическим (случайным, не наследственным). В качестве причин описаны различные нарушения 11 и 17 хромосом.
Высокий риск опосредован наличием ряда наследственных синдромов, вследствие хромосомных, генных, митохондриальных мутаций (поломка наследственного аппарата клетки), компонентом которых является АКР:
- Синдром Ли-Фраумени (Li-Fraumeni) - характеризуется возникновением злокачественных опухолей мягких тканей, молочной железы, новообразований головного мозга и АКР.
- Синдром Беквита-Вайдемана (Beckwith-Wiedemann) – клиническими проявлениями являются аномально большой язык, увеличение внутренних органов, дефект передней брюшной стенки (пупочная грыжа), опухоли печени, почек и АКР.
- Карни-комплекс (Carney complex) – редкий синдром, при котором описаны множественные доброкачественные и злокачественные новообразования кожи, сердца, эндокринных органов.
- Синдром Гарднера – множественный полипоз толстой кишки в сочетании с остеомами костей черепа, поражениями кожи.
- Синдром МЭН 1 типа (множественная эндокринная неоплазия) – обусловлен опухолями или гиперплазией (разрастание структурных элементов тканей) щитовидной железы, паращитовидных желез, поджелудочной железы, надпочечников.
Клинические проявления адренокортикального рака надпочечников
Клиническая картина отличается разнообразием и связана с избыточной продукцией гормонов. У женщин в результате выработки повышенного уровня мужских половых гормонов развивается вирильный синдром (лат. virilis - мужской, свойственный мужчине), характеризующийся ростом волос на лице, изменением тембра голоса, прекращением менструаций, у мужчин клинически избыток андрогенов, как правило, может не проявляться.
- альдостерона может вызвать повышение артериального давления, мышечную слабость, судороги, частое мочеиспускание, чувство жажды;
- эстрогенов – у мужчин рост ткани молочных желез, снижение или полное отсутствие полового влечения, импотенцию, у женщин – нерегулярные менструации, маточные кровотечения в менопаузе, ожирение.
Кроме того, в случае метастатического процесса могут появляться жалобы со стороны пораженных органов (легкие, печень, кости).
Неспецифическими клиническими признакам являются: наличие объемного образования в животе, чувство распирания, боль в животе, спине.
Как проявляется синдром Иценко-Кушинга?
Синдром Иценко-Кушинга обусловлен нерегулируемой избыточной секрецией кортизола опухолями коры надпоченика и имеет ряд характерных симпотомов:
Важно помнить, что причиной синдрома Иценко-Кушинга могут служить заболевания не связанные с опухолью надпочечника!
Диагностика при подозрении на опухоль надпочечника
На первом этапе необходимо тщательно изучить жалобы больного, историю заболевания, провести физикальный осмотр (следует обращать внимание на тип оволосения, характер распределения жировой клетчатки, размеры молочных желез, степень развития наружных половых органов и др.).
Далее рекомендовано оценить гормональную активность опухоли с помощью следующих лабораторных методов:
- подавляющий тест с 1 мг дексаметазона (короткая проба с дексаметазоном) и последующим определением концентрации кортизола в сыворотке крови в утренние часы. Тест выполняется в амбулаторных условиях: в 23.00 назначают дексаметазон в дозе 1 мг внутрь, в 8.00 следующего утра осуществляют забор крови и анализируют изменение уровня кортизола. Повышение концентрации кортизола в сыворотке крови свидетельствует об избытке глюкокортикоидов.
- определение экскреции (выделения) свободного кортизола в суточной моче
- определение адренокортикотропного гормона в сыворотке крови в утренние часы
- определение стероидных гормонов сыворотки крови (дегидроэпиандростерон-сульфат, 17-оксипрогестерон, андростендион, тестостерон, 17-β-эстрадиол у мужчин и женщин в менопаузе)
- определение соотношения между уровнем альдостерона и активностью ренина плазмы (у пациентов с повышением артериального давления и / или снижением концентрации калия в сыворотке крови)
- развернутый клинический и биохимический анализы крови
Показания к выполнению лабораторных тестов определяет лечащий врач индивидуально.
Следующим этапом в обследовании является определение локализации опухоли и оценка степени распространенности опухолевого процесса с помощью инструментальных методов визуализации:
- ультразвуковое исследование (УЗИ) органов брюшной полости может быть использовано для первичной диагностики опухолей надпочечника при отсутствии возможности выполнения компьютерной томографии (КТ)
- КТ органов брюшной полости с внутривенным болюсным контрастированием с обязательной оценкой трех фаз: до контрастирования (нативная), фаза контрастирования (артериальная и венозная), отсроченная фаза (вымывания, через 10 мин после введения контраста)
- магнитно-резонансная томография (МРТ) органов брюшной полости с внутривенным контрастированием
- КТ органов грудной клетки
- при подозрении на метастатическое поражение головного мозга, костей – МРТ/КТ головного мозга с внутривенным контрастированием, остеосцинтиграфия (сканирование костей)
- позитронно-эмиссионная томография /компьютерная томография ПЭТ/КТ с введением 18F-фтордезоксиглюкозы (18F-ФДГ) при опухолях небольших размеров (до 4 см)
На этапе диагностики и подготовки к лечению больные должны быть консультированы эндокринологом!
Пути метастазирования злокачественных опухолей надпочечника
Злокачественные опухоли надпочечника метастазируют лимфогенным и гематогенным путем. Выраженной тенденцией к гематогенному метастазированию обладают злокачественные опухоли из коркового слоя надпочечников, поражая легкие, кости, головной мозг, желудочно-кишечный тракт, почки, другие органы эндокринной системы. Злокачественные опухоли из мозгового слоя надпочечников (хромафинной ткани) преимущественно распространяются в легкие, кости, головной мозг и лимфатические узлы.
Лимфогенный путь метастазирования реализуется в лимфатические узлы, которые расположены вокруг аорты (для левого надпочечника), вокруг нижней полой вены (для правого надпочечника), в лимфатические узлы позади аорты на уровне 11 и 12 грудных позвонков (для обоих надпочечников), далее выше диафрагмы в лимфатические узлы средостения на уровне 9 и 10 грудных позвонков.
На момент постановки диагноза распространенный опухолевый процесс выявляют у 30-40% больных.
В каких случаях показано выполнение биопсии опухоли надпочечника?
В диагностике опухолей надпочечников пункционная биопсия не имеет преимуществ, сопряжена с высоким риском осложнений и может быть показана в следующих случаях:
- при подозрении на наличие метастаза в надпочечнике из другой первичной опухоли (другой локализации)
- при подозрении на лимфопролиферативное заболевание с вовлечением надпочечников (характерной чертой является двустороннее поражение надпочечников)
Пункционная биопсия с целью верификации феохромоцитомы не рекомендована.
С какими трудностями можно столкнуться в процессе диагностики опухолей надпочечников?
Выявление опухоли надпочечника ставит перед врачами ряд задач:
- опухоль может быть гормонально-неактивной без клинических и биохимических проявлений нарушения функции соответствующих слоев надпочечника
- опухоль может быть гормонально-активной, что требует точной дифференциальной диагностики с другими состояниями, при которых наблюдается секреция избыточного уровня гормонов
- источником опухоли в надпочечнике могут быть другие органы
- опухоль может быть доброкачественной и злокачественной
Стадирование адренокортикального рака надпочечников
В клинической практике для стадирования АКР используют TNM-классификацию (Международная классификация стадий злокачественных опухолей, где Tumour - первичная опухоль, Node - метастазы в региональные лимфатические узлы, Metastasis - отдалённые метастазы) и классификацию по ENSAT, разработанную европейской рабочей группой по изучению опухолей надпочечника (European Network for the Study of Adrenal Tumors).
Опухоль ограничена надпочечником, размером до 5 см
Опухоль ограничена надпочечником, размером более 5 см
Опухоль любых размеров и распространяется:
- на близлежащие лимфатические узлы, и/или
- на соседние органы (почки, диафрагму, селезенку, поджелудочную железу и/или крупные сосуды (почечная вена, нижняя полая вена).
Опухоль любых размеров и распространяется:
- на отдаленные органы (кости, легкие, головной мозг и т.д.)
- на близлежащие лимфатические узлы, и/или
- на соседние органы (почки, диафрагму, селезенку, поджелудочную железу и/или крупные сосуды (почечная вена, нижняя полая вена).
Правильное стадирование играет ключевую роль в оценке прогноза заболевания и определении тактики лечения (возможность и объем предполагаемого оперативного вмешательства).
Лечение АКР
Основным методом полного излечения АКР в настоящее время является хирургический. Лечение рекомендовано выполнять в специализированном центре, где специалистами накоплен теоретический и практический опыт. Быстрый рост опухоли и склонность к метастазированию обусловливают необходимость проведения оперативного вмешательства безотлагательно, после завершении адекватного объема диагностических процедур. Особенно оправдана такая тактика у категории пациентов с локализованным опухолевым процессом, отсутствием метастазов, когда шансы на полное выздоровление высоки.
Особенности хирургического лечения:
Какие факторы влияют на прогноз заболевания?
Наиболее важными прогностическими факторами являются:
- степень распространенности опухолевого процесса
- возможность полного, радикального удаления опухоли
- предшествующее хирургическое лечение (в случае возврата заболевания или единичных метастазах, возникших после операции, повторное радикальное удаление опухоли является эффективным)
- злокачественный потенциал опухоли. Индекс пролиферативной активности Ki-67 показывает какой процент опухолевых клеток активно делится. Высокие показатели Ki-67 в опухоли надпочечника связаны с худшим прогнозом.
Лекарственное лечение адренокортикального рака надпочечников
При высоком риске прогрессирования заболевания после хирургического лечения рекомендовано проведение адьювантной терапии. С этой целью применяют противоопухолевый препарат (митотан, лизодрен), подавляющий синтез гормонов в корковом слое надпочечников (действует на пучковую зону, частично сетчатую, не затрагивая клубочковую зону). Лечение проводят от 2 до 5 лет под строгим постоянным контролем врача и лабораторным мониторированием концентрации препарата в крови. С целью предупреждения развития острой надпочечниковой недостаточности на фоне приема митотана больные должны получать заместительную гормональную терапию глюкокортикоидами.
При наличии распространенного метастатического процесса после ранее перенесенного хирургического лечения и быстром прогрессировании опухоли, рекомендовано проведение цитотоксической терапии в комбинации с митотаном. В качестве наиболее эффективной описана схема с включением этопозида, доксорубицина и цисплатина.
Лучевая терапия адренокортикального рака надпочечников
Проведение лучевой терапии может быть рекомендовано с целью уменьшения симптоматического проявления метастазов в кости и центральную нервную систему.
Что такое феохромоцитома?
Феохромоцитома – опухоль из хромафинных клеток мозгового слоя надпочечников, продуцирующих катехоламины (адреналин, норадреналин). Частота встречаемости феохромоцитомы составляет 2-8 случаев на 1 млн населения в год. Феохромоцитому обнаруживают у 0,1-1% пациентов с артериальной гипертензией. Одинаково часто заболевают мужчины и женщины в возрасте от 20 до 50 лет. Большинство феохромоцитом спорадические (случайные), лишь у 10% больных отмечают наследственные заболевания.
Клинические проявления связаны с продукцией избыточного уровня катехоламинов, а основным является повышение артериального давления (АД) (систолического и диастолического). Возможны постоянное, стойкое повышение артериального давления, напоминающее по течению гипертоническую болезнь или гипертонические кризы, при этом в межкризовые периоды АД нормализуется. Продолжительность кризов от нескольких минут до нескольких часов. Повышение АД сопровождается головной болью, чувством страха, потливостью, побледнением или покраснением кожных покровов, судорогами, одышкой, нарушением зрения и др. Резкое повышение АД может наблюдаться спонтанно или быть спровоцировано различными событиями (физическое, психическое напряжение).
Важное место в диагностике, наряду с традиционнами инструментальными методами обследования, принадлежит лабораторным тестам. У больных с феохромоцитомой и стойким повышением АД, как правило, повышены уровни катехоламинов в крови и моче. Определение концентрации гормонов позволяет подтвердить или исключить заболевание.
Основной метод лечения феохромоцитомы – хирургический.
Филиалы и отделения, в которых лечат опухоль надпочечников
Все это позволяет выполнить необходимые этапы лечения в рамках одного Центра, что исключительно удобно для пациентов.
Заведующий отделением - к.м.н. ВОРОБЬЁВ Николай Владимирович
Заведующий отделением - к.м.н. КАЧМАЗОВ Александр Александрович
Отделение лучевого и хирургического лечения урологических заболеваний с группой брахитерапии рака предстательной железы МРНЦ имени А.Ф. Цыба
Заведующий отделением - д.м.н., профессор, КОРЯКИН Олег Борисович
Большинство образований почки встречаются в практике, как случайные находки, из которых часть является почечно-клеточная карцинома. Задачей диагностики является дифференцировка доброкачественного и злокачественного образований почки, хотя во многих случаях это не представляется возможным.
В данной статье рассмотрены радиологические находки характерные для доброкачественных и злокачественных образований почки.
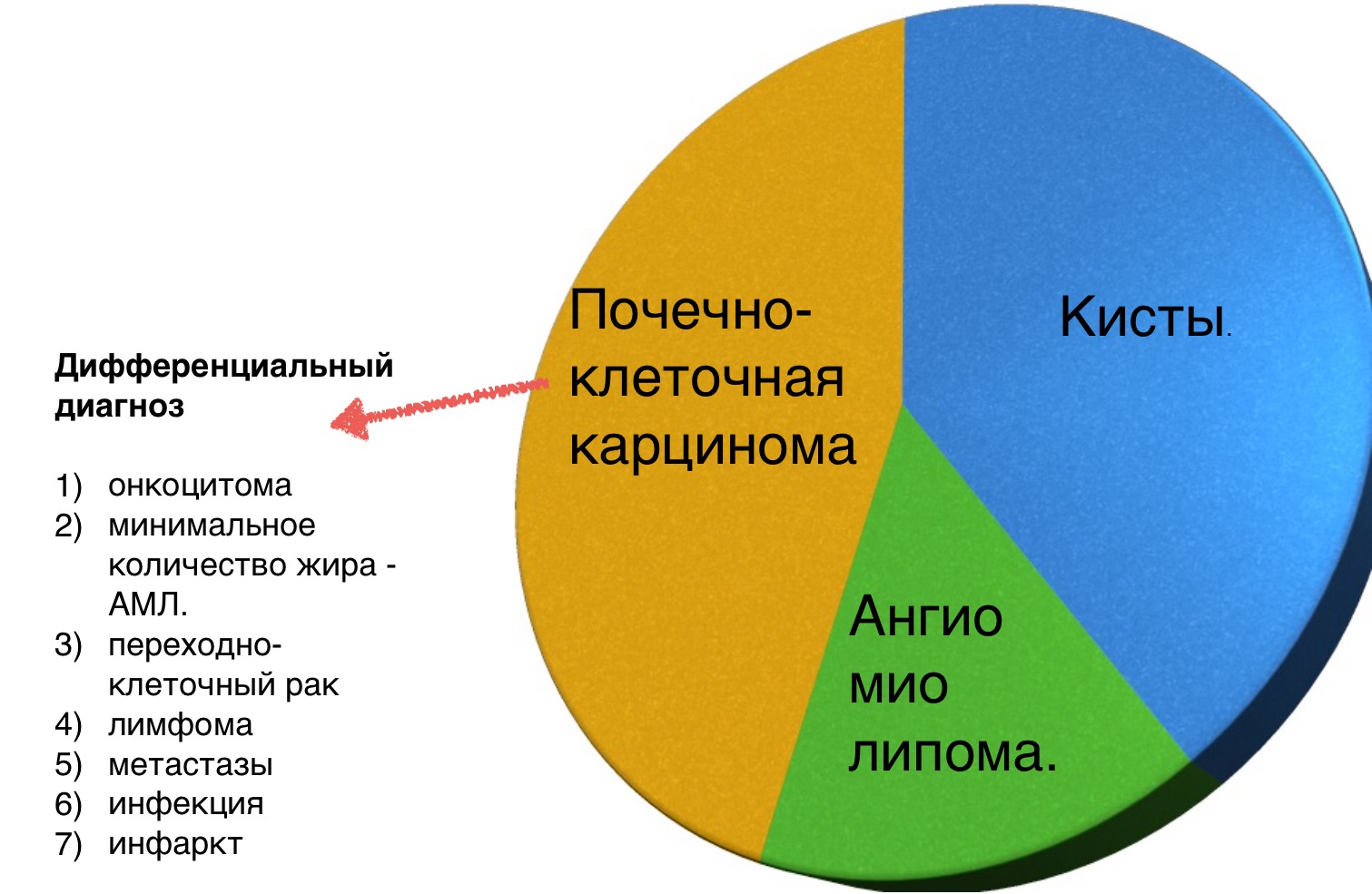
Алгоритм анализа при выявлении образования почки:
- определить кистозное образование или нет?
- если данное образование не кистозное — определите есть ли макроскопические включения жира, что в большей степени соответствует ангиомиолипоме.
- исключить рак почки, маскирующийся под инфаркт или инфекционное поражение, у пациентов с различными клиническими проявлениями.
- исключить лимфому или метастатическое поражение почек. Метастазирование в почки (менее 1%) и поражение почек при лимфоме (0,3%) — это редкость и свидетельствует о тотальном распространении заболевания.
Вы еще много раз столкнетесь с тем, что после выполнения данного алгоритма вы не придете к окончательному диагнозу, а на первом месте дифференциального ряда — почечно-клеточная карцинома.
Затем оцените КТ и МРТ-изображения и ответьте на вопрос, что больше соответствует доброкачественному образования почки, а что злокачественному выделив из этой группы признаки низкодифференцируемой опухоли и высокодифференцируемой почечно-клеточной карциномы.

КТ
Гиперденсное образование на бесконтрасном КТ.
Образование с плотностью выше 70HU на нативном (бесконтрастном) КТ-изображении является геморрагическая киста. Геморрагические кисты также могут быть с плотностью ниже, чем 70HU, но в данном случае должен осуществлен контроль за образованиями на пост-контрастных изображениях. Если на пост-контрастных изображениях отсутствует контрастное усиление, то, следственно, подтверждается кистозное происхождение образование.
Макроскопическое включение жира в образовании почки плотностью 20HU явный признак ангиомиолипомы. Тонкие срезы лучше при исследовании плотности. К сожалению 5% ангиомиолипом макроскопический жир не содержат. КТ-картина данных ангиомиолипом неотличимо схожа с почечно-клеточной карциномой. Как ни странно, но почечно-клеточная карцинома в некоторых случаях также содержит жир. При включениях жира и кальцификатов в образование почки дифференциальный диагноз должен склонятся в сторону почечно-клеточной карциномы.
Сомнительное усиление на 10-20HU псевдо-усиление в кисте, как результат увеличения жесткости излучения. МРТ в данных случаях является отличным методом в дифференциальном диагнозе. Сомнительное усиление также характерно для папиллярной карциномы почки, для которой характерно слабое усиление и которая менее агрессивная опухоль, чем светлоклеточная карцинома.
Гомогенное усиление, а также ослабление (> 40 HU) на нативных снимках в большей степени характерны для ангиомиолипомы с малым содержанием жира, хотя почечно-клеточную карциному нельзя также исключать.
Сильное усиление визуализируется при светло-клеточной карциноме, ангиомиолипомах с малым содержанием жира и онкоцитомах. Светло-клеточная карцинома встречается чаще, чем онкоцитома и ангиомиолипома с малым содержанием жира, поэтому диагноз карциномы ставится чаще в особенности в тех случаях, когда образование гетерогенное и больших размеров.
МРТ при образованиях почки
Гиперинтенсивный сигнал на Т1-взвешенных изображениях, как правило, визуализируется при геморрагических кистах или кистах с белковым содержимым, а также при ангимиолипомах, содержащие макроскопический внеклеточный жир.
Если жир внутри клетки, то на Т1-изображениях не будет гиперинтенсивного сигнала, сигнал будет снижаться на out-phase изображениях, что не характерно для ангимиолипомы, а типичнее для светлоклеточной карциномы почки.
МРТ чувствительнее , чем КТ при определении кистозного образования, а также МРТ показано для дифференциации, если на КТ выявлено псевдо-усиление.
На Т2 гипоинтенсивный сигнал характерен в большей степени для папиллярной карциномы почки и в меньшей степени для ангиолипомы с малым содержанием жира.
На Т2 гиперинтенсивный сигнал характерен для светлоклеточной карциномы, но признак не является специфичным, потому как схожие изменения и при онкоцитомах.
По данным МРТ изображений также трудно, как и по данным КТ изображений сказать однозначно о доброкачественности и злокачественности процесса.

Размер и форма образования.
Ещё один способ в оценке солидных образований почки — это оценка формы образования. Солидные образования разделяют на шарообразные и бобообразные образования .
Шарообразные образования являются наиболее распространёнными образованиями почки. Данные образование чаще обширные деформирующие контур органа. Типичные представители шарообразных образований являются онкоцитома и почечно-клеточная карцинома.
Обратите внимание, что существует много подводных камней в дифференциальной диагностике шарообразных и бобовидных образований.

Бобовидные образования.
Радиологические признаки образований бобовидной формы обычно не специфичны. Данное явление заметно если обратить внимание на схожесть образований, представленных на рисунке. Дифференциальный диагноз обычно строят, исходя из клинических данных и, соответственно, данных визуализации.
Инфильтрирующее почку по центру образование у пожилого пациента соответствует переходно-клеточному раку почки. Инфильтрирующее почку по центру образование у молодого пациента с серповидной перегородкой внутри больше соответствует медуллярной карциноме почки. Мультифокальные и билатеральные или диффузные образования почки в сочетании с лимфоаденопатией, а также с вовлечением в патологический процесс других органов характерны для лимфомы.
Мультифокальные и двусторонние поражения почек характерны для злокачественных образований, в частности для метастазирования. У пациентов с клиникой характерной при инфекции, конечно же, в первую очередь нужно подозревать пиелонефрит. Для инфаркта почки характерно клиновидное поражение почки.

Размер образования.
Размер опухоли является наиболее важным показателем злокачественности опухоли вместе с гистологической оценки дифференцировки образования.
Риск возникновения метастазов зависит от размера опухоли.
Если размер опухоли меньше 3 см риск метастазирования незначительна.
Большинство образований почки в размере обычно меньше, чем 4 см. Многие из данных образований низкодифференцированная почечно-клеточная карцинома, безболезненно протекающие злокачественные или доброкачественные образования.
Образования размером от 1 до 2 см, которые удалили хирургически, в 56% доброкачественные образования. 13% образований размером от 6 до 7 см только являются доброкачественные.
Почечно-клеточный рак. Светлоклеточная карцинома почки.
Почечно-клеточная карцинома является типичным шарообразным образованием. Почечно-клеточная карцинома является случайной находкой выявленная у пациентов, обратившихся с жалобами не связанными с патологии мочевыделительной системы.
Пик заболеваемости 60-70 лет. Почечно-клеточная карцинома связана с наследственными синдромами такими, как синдром Хиппель-Линдау, туберозным склерозом и Бирт-Хогг-Дубе.
Самый распространённый подтип почечно-клеточной карциномы является светло-клеточная карцинома почек, затем папиллярная и хромофобная почечно-клеточная карцинома. Медуллярная и кистозных многокамерная почечно-клеточная карцинома встречается крайне редко.

Светло-клеточная карцинома.
Светло-клеточная карцинома почек составляет 70% случаев рака почек.
Данная опухоль чаще больших размеров и прорастает из почечной коры. Светло-клеточная карцинома является гиперваскулярным образованием с неоднородным содержимым, как следствие некроза, кровоизлияний, кальцинирования или образование внутри кист. В редких случаях почечно-клеточная карцинома содержит внеклеточный жир, соответственно, образование с включением жира и кальцинатов следует рассматривать, как почечно-клеточную карциному.

Характерной особенностью светлоклеточной карциномы явлечётся значительное усиление в кортикомедуллярную фазу.
Хотя трудности бывают, когда образование небольших размеров и локализуется в почечной коре, которая также хорошо контрастируется.
Поэтому нефрографическая фаза при образованиях такой локализации и размеров является для оценки наиболее важной так, как паренхима контрастируется гомогеннее и сильнее, чем опухоль, что хорошо заметно на ниже приведённых изображениях.
На МРТ светло-клеточная карцинома визуализируется, как гипоинтенсивное образование на Т1 и гиперинтенсивное на Т2. Как правило, почечно-клеточная карцинома не имеет экстрацеллюлярного жира, что, соответственно, отличает её от ангиомиолипомы. Хотя в 80% случаях светло-клеточной карциномы есть внутриклеточный жир, что приводит к снижению сигнала на Т1 opposed-phase в сравнении с in-phase изображениями. В данных ситуациях не стоит делать вывод о том, что жир внеклеточный, который характерен в большей степени для ангиомиолипомы. Болезнь Фон-Гиппель-Линдау ассоциирована с развитием светло-клеточной карциномы почек, чаще мультифокальной и билатеральной. Пациенты со светло-клеточной карциномой имеет 5-летнюю выживаемость, что является прогнозом хуже, чем у пациентов с папиллярной и хромофобной карциномой.

Порядка 5% всех светло-клеточных карцином имеют инфильтративный характер роста. Несмотря на то, что это лишь небольшая часть от всех почечно-клеточных карцинома, нельзя забывать про них при построении дифференциального ряда бобовидных образований почки с инфильтративным типом роста. Почечно-клеточные карциномы с инфильтративным типом роста являются агрессивными и гиперваскулярными, которые изменяют внутреннюю архитектуру почек, но не наружные контуры, а изменения лоханки схожи с изменениями при переходно-клеточном раке почки.

Папиллярная почечно-клеточная карцинома
Папиллярная почечно-клеточная карцинома встречается в 10-15% случаях от всех случаев почечно-клеточных карцином. Данные образования чаще гомогенные и гиповаскулярные, поэтому схожи с кистами. В отличии от светло-клеточной карциномы при контрастировании разница плотности образования до и после контрастирования составляет всего 10-20HU. Папиллярные почечно-клеточные карциномы больших размеров могут быть гетерогенными, в следствии геморрагий, некрозов и кальцификатов.
На МРТ данные образования на Т1 дают от изо- до гипотенсивный сигнал и на Т2 гипоинтенсивный. Включения макроскопического жира встречается чаще с кальцификатами.
Образования обычно билатеральные и мультифокальные, что в свою очередь намного чаще встречается в сравнении с другими почечно-клеточными карциномами. 5-летняя выживаемость составляет 80-90%.

Хромофобная почечно-клеточная карцинома
5% от почечно-клеточных карцином типа хромофобная ПКК.
Это твердое, резко ограниченное и иногда с дольчатым строением образование.
Данное образование имеют схожее строение с онкоцитомой так, как в центре визуализируется перегородка или паттерн с радиальным строением, поэтому её невозможно отличить от онкоцитомы при визуализации, хотя и при гистологии тоже сложно.
При контрастировании хромофобная почечно-клеточная карцинома чаще однородная и менее интенсивная, чем светло-клеточная почечная карцинома при контрастировании.
Прогноз хромофобной ПКК схожий с прогнозом папиллярной ПКК и равен 5-летней выживаемости в 80-90% случаях.

Синдром Бёрта — Хога — Дьюба (англ. Birt–Hogg–Dubé syndrome) — редко встречающееся аутосомно-доминантное генетическое заболевание, обусловленное мутацией в гене FLCN и проявляющееся развитием доброкачественных опухолей волосяного фолликула (фиброфолликулом), кистами в лёгких и повышенным риском возникновения рака почки (хромофобная почечной карциномы) и рака толстого кишечника.

Стадирование почечно-клеточной карциномы.
Почечно-клеточная карцинома может распространяться на почечную фасцию и надпочечники, в почечную вену, полую вену.
Для хирурга при планировании операции важно знать, если тромб в нижней полой вене. Это важно в ситуациях, когда тромб поднялся выше диафрагмы, тогда необходимо планирование манипуляций вместе с торакальным хирургом.
Очаговыми образованиями (или очагами) печени называют единичные или множественные участки изменения ее структуры, которые бывают самого разного происхождения – как доброкачественного, так и злокачественного.
Чаще всего очаги выявляются при УЗИ, но иногда являются случайной находкой при компьютерной томографии или МРТ, когда исследование выполнялось по какой-то иной причине. При этом КТ используется для уточнения размеров, количества, расположения и структуры очагов. При этом по результатам КТ врач, как правило, должен ответить на вопросы о характере изменений: имеем ли мы дело с доброкачественным процессом (например, кистой или гемангиомой), либо злокачественным процессом (рак, метастазы, и т.п.). В ряде случаев после выполнения КТ диагноз остается сомнительным. В таких случаях рекомендуется получить второе медицинское мнение по результатам исследования.
Иногда патологическое образование печени выявляется при сцинтиграфии или ПЭТ (очаг гиперфиксации РФП).
Сделать КТ печени в Санкт-Петербурге
ХАРАКТЕРИСТИКИ ПЕЧЕНОЧНЫХ ОЧАГОВ НА КТ
Все объемные образования печени, выявленные при компьютерной томографии, можно разделить в зависимости от следующих параметров:
1) Плотность – характеристика любой ткани организма, которая измеряется на компьютерных томограммах в т.н. единицах Хаунсфилда. В зависимости от рентгеновской плотности очаги бывают гипо-, гипер- и изоденсными по отношению к окружающей нормальной паренхиме. По плотности можно предположить, что находится в структуре очага: кровь, другая жидкость, мягкотканный компонент. Более достоверно выявляются участки обызвествления – кальцинаты.
2) Структура. Кистозные образования подразделяются на одно- и многокамерные; они могут иметь хорошо видимую стенку или не иметь таковой; содержать включения кальция, геморрагическую – гиперденсную – жидкость, гиподенсную жидкость, например, желчь. Внутри можно обнаружить инородное тело или паразита, кистозный или мягкотканный компонент. Также структура может быть однородная или неоднородная, последняя часто объясняется участками некроза. Выявление извести и кальцинатов свидетельствует о длительности процесса.
3) Форма может быть приближенной к шару, вытянутая, неправильная (иррегулярная) и т. д.
4) Контуры. Ровные или неровные, четкие или нечеткие, видимые на всем протяжении или на ограниченном участке.
6) Расположение необходимо указывать в описании КТ-исследования: локализуется ли патологический участок непосредственно в глубине органа, под капсулой, рядом с крупными сосудами, с желчными протоками, с желчным пузырем и т. д. Это может быть навести на мысли о его природе: например, билиарные кисты локализованы чаще всего вблизи желчных протоков, вблизи желчного пузыря.
7) Количество. Солитарный очаг в печени означает одиночный. Число патологических участков (например, метастазов при раке желудка или других органов системы пищеварения) может варьировать. Выявление одного метастаза уже позволяет выставить стадию M1 по системе TNM. Однако следует учитывать, что множественные очаговые образования в печени – это не всегда метастазы, и врач-рентгенолог обязан провести их дифференциальную диагностику, сопоставив многочисленные КТ-признаки.
8) Особенности накопления контраста. Чем меньше накопление контраста в очаге, тем меньше он кровоснабжается. Наоборот, чем быстрее накапливается контраст, тем более развита сосудистая сеть. Чем быстрее снижается плотность после окончания введения контраста, тем интенсивнее кровоток в очаге.
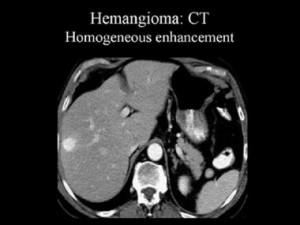
Гемангиома печени или рак? КТ брюшной полости с контрастным усилением: типичное накопление контраста в виде лакун помогает дифференцировать гемангиому от рака и установить правильный диагноз: кавернозная гемангиома.
ГИПОДЕНСНЫЙ ОЧАГ ПЕЧЕНИ
1) Жировые образования имеют плотность от -100 до -10 единиц Хаунсфилда. Это может быть липома, фибролипома, ангиолипома, ангиофибролипома, аденома, липосаркома и некоторые другие опухоли из жировой ткани (а также участок с отрицательной плотностью может быть обусловлен локальным участком жировой инфильтрации, или жирового гепатоза).
2) Гиподенсный очаг плотностью 0…+20 единиц Хаунсфилда чаще всего содержит жидкость. Это может быть простая или паразитарная киста, билома – скопление желчи после операций на желчном пузыре и протоках, а также кистозные метастазы.
3) Гиподенсный очаг плотностью +20…+40 единиц Хаунсфилда бывает обусловлен как жидкостным содержимым, так и мягкотканным. Здесь гораздо больше вариантов, при составлении дифференциального ряда нужно учитывать размеры, форму, характер накопления контрастного вещества.
Капиллярная гемангиома правой доли печени: КТ с контрастным усилением в артериальную фазу выявляет гиперденсный участок.
ГИПЕРДЕНСНЫЙ ОЧАГ В ПЕЧЕНИ
Гиперденсные очаги имеют рентгеновскую плотнтость выше нормальной паренхимы (>70 единиц Хаунсфилда) и могут быть обусловлены кистами, содержащими плотную жидкость (с примесями белка или крови), либо их субстратом является опухоль или кальцинат.
1) Очаг плотностью +200…+400 единиц Хаунсфилда обусловлен наличием кальция в структуре. Это может быть обызвествленная киста, фиброма, фиброаденома (либо другая опухоль), обызвествленная гематома.
2) Локальный участок повышения плотности паренхимы зачастую бывает обусловлен отложениями металлов – солей алюминия, железа и т.д.
3) Опухоли бывают как гиперденсными, так и гиподенсными.
КИСТОЗНЫЕ ИЗМЕНЕНИЯ ПЕЧЕНИ
Кистозный характер при КТ имеют следующие образования:
1) Простая киста печени — что это? Простая киста возникает в результате эмбриогенеза и представляет собой ограниченное капуслой скопление жидкости. На КТ она имеют ровные края, четкие контуры, обычно правильную форму; плотностные характеристики жидкости +5…+20 единиц Хаунсфилда, не содержит каких-либо включений (кровь, кальций и т. д.), в их структуре нет перегородок, стенка ровная, без локальных утолщений. Контраст такие кисты не накапливают. Часто возникает вопрос, может ли киста печени перерасти в рак. Если киста имеет типичные КТ-характеристики, тревоги она вызывать не должна, озлокачествления кисты не бывает. Но важно отличить простую кисту от эхинококковой, от кистозной формы метастаза или кистозного рака.
3) Кистозная форма гепатоцеллюлярного рака: форма неправильная, может выявляться солидный компонент (при кистозной форме он выражен минимально), опухоль единичная, оказывает объемное воздействие на рядом расположенные сосуды и желчные протоки.
4) Паразитарные кисты. Чаще всего эти кисты представлены эхинококком, реже – альвеококком. Бывают множественными или единичными, имеют хорошо видимую стенку, усиливающуюся при контрастировании. Бывают однокамерные и многокамерные паразитарные кисты. Внутри таких кист можно обнаружить паразита.
5) Гемангиома правой доли печени, либо левой доли. Гемангиома печени на КТ выглядит как типичный гиподенсный очаг, при контрастировании в артериальную фазу резко усиливается, в результате чего становятся видимыми сосудистые лакуны, а затем медленно теряет контраст. Атипичные гемангиомы на КТ имеют несколько другие характеристики, и отличить их от злокачественного поражения помогает взгляд опытного рентгенолога, имеющего опыт в диагностике заболеваний брюшной полости.
Вторичные (секундарные) изменения в печени на КТ. Рак кишечника с метастазами. Прогноз неблагоприятный, учитывая размеры и количество метастазов.
СОЛИДНЫЕ ОБРАЗОВАНИЯ ПЕЧЕНИ
1) Объемное образование с включениями жира: липома, липофиброма, ангиолипома, липосаркома и др. Имеют характерную структуру и плотностные характеристики, соответствующие жировой ткани.
2) Фокальная нодулярная гиперплазия (ФНГ) имеет неправильную форму (в виде узла), при нативном исследовании – гиперденсный (незначительно выше нормальной плотности), при контрастировании неравномерно усиливается.
3) Регенераторный узел, локальный участок фиброза либо жировой инфильтрации – признак перерождения печеночной ткани под влиянием различного характера интоксикацией или травм, признак цирроза. Выглядит как локальный гипо- (жировая инфильтрация) или гиперденсный (фиброз) участок.
4) Гепатоцеллюлярный рак (ГЦР). Выглядит как объемное образование неправильной формы, различных размеров (иногда несколько десятков сантиметров в поперечнике), структура его неоднородна – при КТ могут быть выявлены участки некроза, полости (не усиливающиеся при контрастировании). Ткань опухоли за счет хорошего кровоснабжения повышает плотность при контрастировании.
Сделать КТ печени в Санкт-Петербурге
ВТОРОЕ МНЕНИЕ ВРАЧА
Второе консультативное мнение врача, обладающего опытом в анализе КТ-исследований брюшной полости, всегда полезно – заключение по исследованию даст специалист, имеющий высшую врачебную категорию или научное звание, после подробного ознакомления с историей заболевания, с результатами лабораторных тестов и т. д. В результате точность диагностики становится выше, что позволяет определиться с дальнейшим направлением лечения (либо назначить дополнительные инструментальные и иные диагностические исследования).
Чтобы получить Второе мнение по результатам КТ или МРТ, можно обратиться в Национальную телерадиологическую сеть. Сделать это можно удаленно, не выходя из дома. Достаточно иметь результаты исследования на диске. В течение 24 часов с момента отправки снимков вы получите квалифицированный пересмотр КТ или МРТ с подробным описанием в виде заключения с подписью высококвалифицированного диагноста.
Лучевые методы обследования печени
а) Сравнительная анатомия и эмбриогенез:
1. Фиброполикистозные заболевания. Во время эмбрионального развития протоковой пластинки, окружающей воротную вену плода, могут возникать различные аномалии. В зависимости от стадии эмбрионального развития, во время которой они возникают, возможно формирование различных типичных и нетипичных аномалий печени и билиарного тракта, к которым относятся, например, врожденный фиброз печени, поликистоз печени, болезнь Кароли, билиарные гамартомы.
2. Сегментарная анатомия печени. Согласно классификации Куино печень делится на восемь сегментов условными плоскостями, проведенными вертикально через вены печени, и горизонтальной плоскостью, проведенной через правую и левую долевые ветви воротной вены. Понимание сегментарной анатомии становится особенно важным в свете недавних достижений хирургии печени и интервенционных вмешательств.
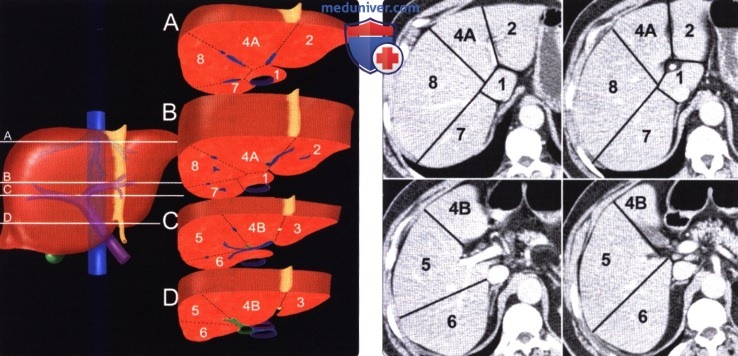
(Слева) На четырех срезах показаны восемь сегментов печени, отделенные друг от друга условными вертикальными плоскостями, проведенными через ветви печеночной вены, и горизонтальной плоскостью, проведенной через воротную вену.
(Справа) Аксиальные томограммы выполнены на уровне срезов, представленных на предыдущем изображении, сегменты печени пронумерованы. Плоскостью, проведенной через серповидную связку печени, медиальный (четвертый) сегмент отделен от латеральных (второй и третий сегменты левой доли). Третий сегмент на томограммах не показан.
Видео анатомия, кровоснабжение и иннервация печени
в) КТ- и МР-протоколы. Томографические исследования, направленные на выявление диффузных или локальных поражений печени, должны быть многофазными и выполняться в различное время в момент введения контрастного вещества и после него.
У пациентов с гемохроматозом (или с наличием в ткани печени патологических очагов с повышенным содержанием железа, например, регенераторных узелков) определяется снижение интенсивности сигнала на МРТ и удлинение времени эха, обычно на томограммах in-phase. Нативная КТ позволяет оценить увеличение плотности печени у пациентов с гемохроматозом, при эффективной терапии из-за устранения избыточного количества ионов железа плотность паренхимы возвращается к нормальным значениям.
3. Поздняя артериальная фаза (35-45 секунд): оптимальна для выявления гиперваскулярных образований в печени, например, гепатоцеллюлярного рака (ГЦР), очаговой гиперплазии, либо гиперваскулярных метастазов (в т.ч. первичных эндокринных опухолей).
4. Портально-венозная (паренхиматозная) фаза (60-70 секунд): характеризуется наиболее оптимальным отображением большинства гиперваскулярных опухолей печени, позволяет визуализировать печеночные вены и воротную вену. Портально-венозную фазу следует включать во все КТ- и МР-протоколы изолированно либо в сочетании с другими фазами.
При проведении исследования редко бывает необходимым выполнение более чем трех фаз для конкретного пациента; следует выбирать оптимальное сочетание фаз для получения наилучшего результата в оценке проявлений заболевания.
Гепатоспецифичные контрастные препараты для МРТ на основе гадолиния используются при динамическом контрастировании и в отсроченной фазе (Т1 ВИ).
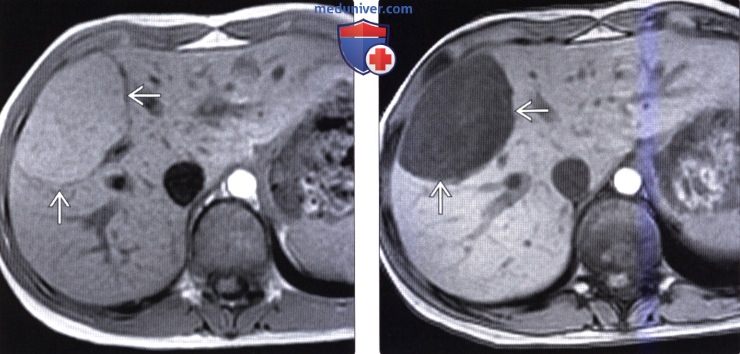
(Слева) На Т1 ВИ МР томограмме (in-phase) у девушки 18 лет, у которой ранее на КТ было случайно обнаружено объемное образование в печени, определяется равномерно гиперинтенсивная опухоль с тонкой капсулой.
(Справа) На Т1 ВИ МР томограмме (opposed-phase) у этой же пациентки определяется потеря сигнала от образования, что означает наличие жировой ткани в нем. Этот факт, наряду с наличием капсулы, молодым возрастом пациентки, отсутствием у нее других заболеваний, позволяет сделать заключение об аденоме печени.
д) Подходы к диагностике заболеваний и образований печени. Практически все очаговые изменения печени, которые возможно обнаружить, являются гиподенсными относительно паренхимы печени, накопившей контраст. Чтобы на заключение рентгенолога могли опираться клиницисты, необходимо вначале охарактеризовать выявленные изменения, а затем составить дифференциально-диагностический ряд.
Рекомендуется следующий подход к анализу патологических изменений со стороны печени: вначале необходимо оценить размеры, форму, плотность, степень васкуляризации и изменения во всех фазах контрастного усиления со стороны печени и любого обнаруженного патологического процесса.
Например, гепатомегалия в сочетании со снижением плотности печени обычно обусловлена стеатозом либо другим инфильтративным процессом. Уменьшение размеров печени на фоне увеличения хвостатой доли, уменьшения правой доли означает цирроз, либо является проявлением синдрома Бадца-Киари.
Окклюзия печеночной вены обычно возникает при синдроме Бадда-Киари, гиперкоагуляции, либо при сдавливании опухолью. Окклюзия воротной вены возникает чаще всего в результате портальной гипертензии, септического тромбофлебита (например, обусловленного дивертикулитом), гиперкоагуляции, сдавливания или опухолевой инвазии воротной вены.
Другие специфические изменения, используемые для характеристики поражений печени, включают в себя наличие или отсутствие кальцинатов, рубцов, кровоизлияний, капсулы и т. д.
При интерпретации результатов лучевых исследований всегда необходимо сопоставлять их с клиническими данными. Пример описания образования печени на КТ: «На КТ в артериальную фазу контрастного усиления определяется объемное образование в четвертом сегменте печени, имеющее округлую форму, равномерно накапливающее контраст, размером около 5 см, с наличием небольшого центрального рубца. Образование имеет плотность, практически не отличающуюся от плотности паренхимы печени в норме до контрастного усиления и в портально-венозную фазу.
е) Дифференциальный диагноз патологии печени:
1. Образования печени с центральным или эксцентрическим рубцом:
Частые:
• Очаговая узелковая гиперплазия
• Кавернозная гемангиома печени
Менее частые:
• Фиброламеллярный рак печени
• Гепатоцеллюлярный рак
• Холангиокарцинома (периферическая)
• Аденома печени
• Метастазы в печени
• Эпителиоидная гемангиоэндотелиома
2. Очаговые поражения печени с кровоизлиянием:
Частые:
• Повреждение печени
• Аденома печени
• Гепатоцеллюлярный рак
• Киста печени
• Врожденная аутосомно-доминантная поликистозная болезнь печени
Менее частые:
• Кровоизлияние в печень, обусловленное нарушением свертываемости крови
• Метастазы в печени
• HELLP-синдром
Частые:
• Очаговый сливной фиброз
• Периферическая холангиокарцинома
• Метастазы в печени и лимфома
• Гепатоцеллюлярный рак
• Метастазы по брюшине (имитируют новообразование в печени)
Менее частые:
• Эпителиоидная гемангиоэндотелиома
• Кавернозная гемангиома печени
• Первичный склерозирующий холангит
• Воспалительная псевдоопухоль печени
4. Объемное образование печени, содержащее жир:
Частые:
• Стеатоз (жировая инфильтрация печени) (может имитировать образование)
• Скопления жира около воротной вены
Менее частые:
• Гепатоцеллюлярный рак
• Аденома печени
• Метастазы в печени
• Гемангиолипома печени
• Опухоли печени после спиртовой абляции (имитируютжировое образование)
• Дефектный участок печени после оперативного вмешательства (имитирует жировое образование)
Редкие, но важные
• Тератома или липосаркома
• Очаговая узелковая гиперплазия
• Ксантоматозные очаги при гистиоцитозе X (Лангерганса)
5. Кистозные образования печени:
Частые:
• Киста печени
• Врожденная аутосомно-доминантная кистозная болезнь печени
• Пиогенный абсцесс печени
• Билиарная гамартома
• Билома/серома
• Стеатоз, жировая инфильтрация (имитирует)
Менее частые:
• Гидатидная киста печени
• Метастазы в печени или лимфома
• Билиарная цистаденокарцинома
• Кандидоз печени
• Болезнь Кароли
• Псевдокиста печени
• Холангиокарцинома (муцин-продуцирующий вариант)
6. Очаговые гиперваскулярные поражения печени:
Частые:
• Кавернозная гемангиома печени
• Очаговая узелковая гиперплазия
• Артерио-портальный шунт
• Преходящие различия плотности печени
• Гепатоцеллюлярный рак
• Метастазы в печени
• Аденома печени
• Артерио-венозная мальформация печени (болезнь Ослера-Вебера-Рендю)
Менее частые:
• Узловая регенеративная гиперплазия
• Фиброламеллярный рак печени
• Изменения, обусловленные обструкцией верхней полой вены
• Периферическая холангиокарцинома
• Пелиоз печени
• Ангиосаркома печени
7. Множественные гиподенсные очаги в печени:
Частые:
• Метастазы в печени и лимфома
• Простые кисты печени
• Кавернозная гемангиома печени
• Пиогенные абсцессы печени
• Врожденная поликистозная болезнь печени
• Гепатоцеллюлярный рак
• Саркоидоз печени
Менее частые:
• Аденома печени
• Амебные абсцессы печени
• Гидатидная кисты в печени
• Кандидоз печени
• Нодулярная регенеративная гиперплазия
Редкие, но важные:
• Ангиомиолипома печени
• Эпителиоидная гемангиоэндотелиома
• Болезнь Кароли
Частые:
• Метастазы в печени
• Пиогенный абсцесс печени
• Гепатоцеллюлярный рак
• Гематома печени
Менее частые:
• Аденома печени
• Гидатидная киста печени
• Амебный абсцесс печени
• Очаговая узелковая гиперплазия
• Нодулярная регенеративная гиперплазия
9. Очаговое гиперденсное объемное образование на КТ без контрастного усиления:
Частые:
• Цирротический регенеративный узел
• Любое образование в печени при жировом гепатозе (кажущийся эффект)
• Сохранный участок паренхимы печени на фоне жирового гепатоза
• Метастазы в печени
• Гематома печени
10. Снижение плотности или отек тканей по ходу воротной вены:
Частые:
• Расширенные желчные протоки (создают ложное впечатление об отеке)
• Системная гиперволемия
• Застойные явления в печени
• Острый гепатит
• Восходящий холангит
• Билиарный некроз или лимфедема после трансплантации печени
• Повреждение печени
Менее частые:
• Лимфаденопатия ворот печени
• Перибилиарные кисты при циррозе
• Тромбоз воротной вены
• Первичный склерозирующий холангит
• Стеатоз (жировая инфильтрация печени)
• Холангиопатия при СПИД
• Гепатоцеллюлярный рак
• Холангиокарцинома
• Метастазы в печени и лимфома
• Холангит, обусловленный химиотерапией
• Рецидивирующий пиогенный холангит
11. Диффузное снижение плотности печени:
Частые:
• Стеатоз (жировой гепатоз)
Менее частые:
• Гепатит
• Токсическое повреждение печени
• Инфаркт печени
• Метастазы в печени и лимфома
• Саркоидоз печени
• Оппортунистические инфекции кишечника
• Гепатоцеллюлярный рак
• Болезнь Вильсона
• Лучевой гепатит
• Синдром Бадда-Киари
• Болезни накопления гликогена
Читайте также:

