Что такое свертывание крови и каков его механизм кратко
Обновлено: 04.07.2024
Многие начинают бояться тромбов после того, как при сдачи крови из вены медсестра сообщает, что она слишком вязкая. Те же, кто обладает слишком жидкой кровью, успешно наполняющей пробирку, надеются, что застрахованны от тромбоза. Но вязкость и свёртываемость – два совершенно разных понятия, и не всегда одно обуславливает другое.
Какая ты вязкая
Ещё одна частая причина повышенной вязкости – повышенный уровень эритроцитов и гемоглобина, характерный для курильщиков. Ведь чем больше дыма и меньше воздуха человек вдыхает, тем большая концентрация переносчиков кислорода необходима. Формируется их компенсаторное повышение. Поэтому визуально кровь курящих нередко кажется более вязкой.
В норме содержание эритроцитов крови составляет 3,7-5,1, тромбоцитов – 180-320.
Вязкость и свёртываемость – в чём разница?
Наиболее важным показателем является свёртываемость крови. К сожалению, получить точную информацию о свёртываемости, даже, несмотря на уровень развития медицины, бывает непросто. С одной стороны давно известны явные заболевания с нарушением свёртываемости, такие как гемофилия. С другой, немало скрытой патологии, которая может долгое время никак себя не выдавать, но проявившись однажды, быстро привести к тяжёлым последствиям.
Лишь в последние десятилетия исследователи научились выявлять эти проблемы с помощью высокотехнологичных генетических анализов. Учитывая, что по статистике врождённая патология свёртывающей системы крови есть у более 1-3% населения Земли, вполне вероятно, что в будущем эти анализы будут проводить в роддоме каждому новорожденному. И совершено точно тем, кому необходимо назначить те или иные лекарства, способные усилить риск появления тромбов.
Предохранение или опасность?
Что покажет анализ?
Какие же анализы необходимо сдать, чтобы проверить свёртываемость крови? Самый распространённый и многим привычный анализ – коагулограмма может дать ответ далеко не на все вопросы, особенно в профилактике тромбозов.
Тем не менее, классическая коагулограмма – первый этап скринингового обследования системы свёртываемости. Если она выявит отклонения от нормы, следующим шагом станут более детальные исследования гемостаза – тромбоэластография или тромбоэластометрия. Отдельная история – определение D-димера, мутации Лейдена и других генетических нарушений свёртывания - тесты, выявляющие склонность к образованию тромбов в будущем. Что и в каких случаях необходимо?
Самая распространённая сегодня стандартная коагулограмма включает в себя пять компонентов: ПТИ ( протромбиновый индекс); МНО ( Международное нормализованное отношение. Отражает отношение времени свёртываемости крови пациента к времени свёртывания крови здорового пациента; АЧТВ (активированное частичное тромбопластиновое время. Оценивает время, за которое образуется сгусток крови после присоединения к плазме специальных реагентов), УРОВЕНЬ ФИБРОГЕНА и ТРОМБОЦИТОВ.
При этом АЧТВ информативен лишь у людей, проходящих лечение гепарином, а МНО важен только для людей, постоянно принимающих разжижающие кровь препараты из группы неодикумаринов (варфарин).
Получается, два показателя из пяти не так важны для скрининга. Общее количество тромбоцитов также не всегда показательно, ведь при большинстве коагулопатий изменяется не их число, а прежде всего функциональная активность.
Поэтому наиболее информативным, позволяющий оценить сразу несколько звеньев свёртывания крови – тромбоэластография. Это своего рода детальное наблюдение за формированием кровяного сгустка, и его последующего растворения (лизиса) с построением графиков каждого из этапов. Тромбоэластометрия – другой вариант этого исследования, считающийся ещё более информативным. К сожалению, приборы для проведения этих исследований дороги и требуют специального обучения персонала, поэтому предложить услуги тромбоэластографии может далеко не каждая лаборатория.
Ещё один важный показатель – D-ДИМЕР (это продукт распада фибрина, небольшого фрагмента белка, присутствующего в крови после разрушения тромба).
Он активно используется для определения риска тромбообразования. Те, у кого D-димер даже незначительно повышен, рискуют столкнуться с появлением тромбов значительно больше остальных. Контролировать D-димер необходимо при заболеваниях вен (тромбофлебиты), после проведенных оперативных вмешательств и при выписке из стационара, если вы были долго прикованы к постели. наблюдать за уровнем D-димера полезно во время беременности и при приеме гормональных контрацептивов (риск образования тромбов при наличии мутации Лейдена на фоне приема противозачаточных таблеток возрастает почти в 9 раз). А теперь и во время COVID-19 и несколько недель после выздоровления.
Мерцающая проблема
Фактор Виллебранда и COVID-19.
Генетические мутации системы свёртывания, выявляемые в ходе анализов:
МУТАЦИЯ V КОАГУЛЯЦИОННОГО ФАКТОРА СВЁРТЫВАЕМОСТИ КРОВИ (ФАКТОР ЛЕЙДЕНА)
ИНГИБИТОР АКТИВАТОРА ПЛАЗМИНОГЕНА 1
МУТАЦИЯ II КОАГУЛЯЦИОННОГО ФАКТОРА (МУТАЦИЯ ПРОТРОМБИНА)
МУТАЦИЯ МЕТИЛЕНТЕТРАГИДРОФОЛАТРЕДУКТАЗЫ (MTHFR C677T)
МУТАЦИЯ VII КОАГУЛЯЦИОННОГО ФАКТОРА СВЁРТЫВАЕМОСТИ КРОВИ (F7 ARG353GLN)
ПОЛИМОРФИЗМ ГЕНА РЕДУКТАЗЫ МЕТИОНИНСИНТАЗЫ (MTRR A66G)
МУТАЦИЯ ФИБРИНОГЕНА, БЕТА (FGB G-455A)
МУТАЦИЯ ПРОМОТОРА ГЕНА КОАГУЛЯЦИОННОГО ФАКТОРА FVII (-312 INS 10BP)
ИНСЕРЦИЯ/ДЕЛЕЦИЯ ALU-ЭЛЕМЕНТА В ГЕНЕ АНГИОТЕНЗИН-ПРЕВРАЩАЮЩЕГО ФЕРМЕНА (ALU INS/DEL)
МУТАЦИЯ ТРОМБОЦИТАРНОГО ГЛИКОПРОТЕИНА 1B, АЛЬФА СУБЪЕДИНИЦЫ
МУТАЦИЯ АДФ-РЕЦЕПТОРА ТРОМБОЦИТОВ (P2RY12 H1/H2)
МУТАЦИЯ A1298С ГЕНА МЕТИЛЕНТЕТРАФОЛАТРЕДУКТАЗЫ
D-димер значительно повышается у большинства больных со среднетяжёлым и тяжёлым течением COVID-19. Поэтому все пациенты получают лечебные дозы антикоагулянтов.
Мутация Лейдена - наиболее частое скрытое нарушение свёртываемости крови, встречается у 2-6% европейцев.
Закрытие мелких повреждений в сосудах. Основная теория свертывания крови
а) Важность тромбоцитарного механизма для закрытия мелких повреждений в сосудах. Механизм формирования тромбоцитарной пробки очень важен для закрытия мельчайших разрывов в мелких кровеносных сосудах, которые появляются много тысяч раз ежедневно. Действительно, множество мелких дырочек в самих эндотелиальных клетках часто закрываются тромбоцитами, которые буквально сливаются с эндотелием, формируя дополнительную мембрану эндотелиальной клетки. У человека с низким содержанием тромбоцитов в крови ежедневно появляются буквально тысячи точечных кровоизлияний под кожей и во всех внутренних тканях, но этого не случается у людей с нормальным содержанием тромбоцитов в крови.
б) Свертывание крови в разорванном сосуде. Третьим механизмом гемостаза является формирование кровяного сгустка. Он начинает развиваться через 15-20 сек при серьезной травме сосудистой стенки, и через 1-2 мин — при незначительной. Запускают процесс свертывания покрывающие место повреждения вещества-активаторы, выделяющиеся из стенки травмированного сосуда, кровяных пластинок и белков крови. Физические явления этого процесса показаны на рисунке ниже, а в таблице перечислены наиболее важные факторы свертывания.
Процесс свертывания в травмированном сосуде
Если отверстие в сосудистой стенке не слишком велико, в течение 3-6 мин после повреждения сосуда все отверстие или разорванный конец сосуда заполняются сгустком крови. Через 20-60 мин происходит ретракция (сжатие) сгустка; это способствует дальнейшему закрытию сосуда. В ретракции сгустка важную роль играют также тромбоциты.
в) Фиброзная организация или растворение кровяного сгустка. После формирования кровяного сгустка возможны два пути его дальнейшего развития: (1) заполнение сгустка фибробластами, которые в дальнейшем формируют соединительную ткань на всем протяжении сгустка; (2) растворение сгустка. При небольшом отверстии в сосудистой стенке сгусток обычно заполняется фибробластами через нескольких часов после его формирования (этому способствует, по крайней мере, частично, фактор роста, секретируемый тромбоцитами). Процесс продолжается в течение примерно 1-2 нед вплоть до полной организации сгустка в фиброзную ткань.
Наоборот, если в ткань вытекло много крови и образовались сгустки там, где в них нет необходимости, внутри самого сгустка обычно активируются особые вещества, функционирующие как ферменты, растворяющие сгусток. Подробнее это изложено далее.
Механизм свертывания (коагуляции) крови
Основная теория. В крови и тканях обнаружены более 50 веществ, вызывающих свертывание крови или влияющих на него. Одни из них способствуют свертыванию и их называют прокоагулянтами, другие — тормозят этот процесс и их называют антикоагулянтами. Останется ли кровь жидкой или произойдет ее коагуляция, зависит от баланса между этими группами веществ. В нормальном кровотоке преобладают антикоагулянты, поэтому кровь, циркулирующая в кровеносных сосудах, не свертывается. Но при разрыве сосуда прокоагулянты из области повреждения ткани активируются и перекрывают действие антикоагулянтов, что способствует образованию сгустка.
Основные этапы коагуляции крови. Все исследователи, занимающиеся проблемой свертывания крови, согласны с тем, что в основе свертывания лежат три основных процесса: (1) в ответ на разрыв сосуда или повреждение самой ткани в крови происходит сложный каскад химических реакций с участием более дюжины факторов свертывания крови. Итогом этого каскада является образование комплекса активированных веществ, в совокупности называемых активатором протромбина; (2) активатор протромбина катализирует превращение протромбина в тромбин; (3) тромбин действует как фермент, превращающий фибриноген в нити фибрина, формируя сгусток, внутрь которого захватываются кровяные пластинки, клетки крови и плазма.
Начнем с обсуждения механизма формирования самого сгустка крови, а именно: с превращения протромбина в тромбин; затем вернемся к начальным стадиям процесса свертывания, в результате которых образуется активатор протромбина.
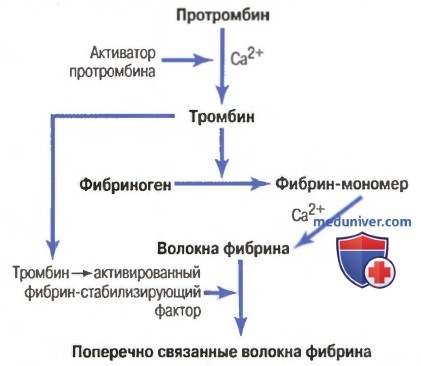
Схема превращения протромбина в тромбин и полимеризации фибрина с формированием волокон фибрина
Видео физиология остановки кровотечения (гемостаза) - профессор, д.м.н. П.Е. Умрюхин
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
1. Purves, William K. Life: The Science of Biology. — 7th. — Sunderland, Mass: Sinauer Associates, 2004.
Человеческое тело состоит из десятков органов, большинство из которых имеет определенную форму и размер. Но есть один, главный, — он не имеет четких границ, но от его состояния зависит работа всех остальных систем организма. Это наша кровь, которая состоит из плазмы и форменных элементов — эритроцитов, тромбоцитов и лейкоцитов 1 . Плазма — жидкая часть крови, которая содержит воду и взвешенные в ней вещества: белки и другие соединения.
Форменные элементы крови
Эритроциты (красные кровяные тельца) — самые многочисленные из форменных элементов 2 . В эритроцитах содержится особый белок — гемоглобин, обеспечивающий главную функцию эритроцитов — транспорт кислорода. Именно гемоглобин придает эритроцитам и крови в целом красную окраску.

Рисунок 1. Форменные элементы крови
Тромбоциты (кровяные пластинки) представляют собой фрагменты гигантских клеток костного мозга. Совместно с белками плазмы они обеспечивают быстрое свертывание крови, вытекающей из поврежденного кровеносного сосуда, что приводит к остановке кровотечения и тем самым защищает организм от кровопотери.
Лейкоциты (белые клетки крови) являются частью иммунной системы организма. Они могут выходить за пределы кровеносных сосудов в ткани. Основные функции лейкоцитов — участие в иммунных реакциях и защита от чужеродных тел или веществ 2 . В обычных условиях лейкоцитов в крови намного меньше, чем других форменных элементов.
Баланс свертывающей и противосвертывающей систем крови
3. Colman R.W. Hemostasis and thrombosis basic principles and clinical practice / Под ред. Г. И. Козинца и В. А. Макарова. — Philadelphia: Lippincott, 1993.
В организме человека, как и в любой живой системе, постоянно поддерживается естественный баланс различных показателей. В случае с кровью это непрерывное удержание равновесия между свертывающими и противосвертывающими факторами, так как одни из главных условий оптимальной жизнедеятельности — это поддержание крови в жидком состоянии и своевременное восстановление поврежденных стенок кровеносных сосудов 3 .
4. Физиология человека. Под ред. Покровского В. М., Коротько Г. Ф. 2-е изд., перераб. и доп. — М.: 2003.
С одной стороны, в кровеносном русле постоянно происходит образование микроскопических сгустков, которые ничем себя не проявляют. С другой стороны, определенные белки с противоположным эффектом непрерывно контролируют образование даже самых мелких фибриновых сетей, которые могли бы в любой момент стать больше, что, следовательно, привело бы к развитию тромбоза 4 .
Факторы, нарушающие это хрупкое равновесие, например, даже незначительные повреждения стенки кровеносного сосуда приводят к ускорению времени свертывания крови и образованию более крупных сгустков крови, видимых невооруженным глазом. Поэтому неудивительно, что и искусственный клапан сердца также может нарушить естественный баланс свертывающей и противосвертывающей систем.
Для измерения свертываемости крови необходим простой анализ на определение времени свертывания крови, позволяющий рассчитать международное нормализованное отношение (МНО) при помощи автоматического анализатора свертывания крови.
Анализ на свертывание крови позволит подобрать наиболее оптимальную дозировку антикоагулянтов.
Одним из проявлений защитной функции крови является ее способность к свертыванию. Свертывание крови (гемокоагуляция) является защитным механизмом Организма, направленным на сохранение крови в сосудистой системе. При нарушении этого механизма даже незначительное повреждение сосуда может привести к значительным кровопотерям.
Первая теория свертывания крови была предложена А. Шмидтом (1863-1864). Ее принципиальные положения лежат в основе современного существенно расширенного представления о механизме свертывания крови.
В гемостатической реакции принимают участие: ткань, окружающая сосуд; стенка сосуда; .плазменные факторы свертывания крови; все клетки крови, но особенно тромбоциты. Важная роль в свертывании крови принадлежит физиологически активным веществам, которые можно разделить на три группы:
• способствующие свертыванию крови;
• препятствующие свертыванию крови;
• способствующие рассасыванию образовавшегося тромба.
Все эти вещества содержатся в плазме и форменных элементах, а также в тканях организма и, особенно, в сосудистой стенке.
По современным представлениям процесс свертывания крови протекает в 5 фаз, из которых 3 являются основными, а 2 - дополнительными. В процессе свертывания крови принимают участие много факторов, из них 13 находятся в плазме крови и называются плазменными факторами. Они обозначаются римскими цифрами (I-XIII). Другие 12 факторов находятся в форменных элементах крови (особенно, тромбоцитах, поэтому их называют тромбоцитарными) и в тканях. Их обозначают арабскими цифрами (1-12). Величина повреждения сосуда и степень участия отдельных факторов определяют два основных механизма гемостаза сосудистотромбоцитарный и коагуляционный.
Сосудисто-тромбоцитарный механизм гемостаза. Этот механизм обеспечивает гомеостаз в наиболее часто травмируемых мелких сосудах (микроциркуляторных) с низким артериальным давлением. Он состоит из ряда последовательных этапов.
1. Кратковременный спазм поврежденных сосудов, возникающий под влиянием сосудосуживающих веществ, высвобождающихся из тромбоцитов (адреналин, норадреналин, серотонин).
2. Адгезия (прилипание) тромбоцитов к раневой поверхности, происходящая в результате изменения в месте повреждения отрицательного электрического заряда внутренней стенки сосуда на положительный. Тромбоциты, несущие на своей поверхности отрицательный заряд, прилипают к травмированному участку. Адгезия тромбоцитов завершается за 3-10 секунд.
3. Обратимая агрегация (скучивание) тромбоцитов у места повреждения. Она начинается почти одновременно с адгезией и обусловлена выделением поврежденной стенкой сосуда, из тромбоцитов и эритроцитов биологически активных веществ (АТФ, АДФ). В результате образуется рыхлая тромбоцитарная пробка, через которую проходит плазма крови.
4. Необратимая агрегация тромбоцитов, при которой тромбоциты теряют свою структурность и сливаются в гомогенную массу, образуя пробку, непроницаемую для плазмы крови. Эта реакция: происходит под действием тромбина, разрушающего мембрану тромбоцитов, что ведет к выходу из них физиологически активных веществ: серотонина, гистамина, ферментов и факторов свертывания крови. Их выделение способствует вторичному спазму сосудов. Освобождение фактора 3 дает начало образованию тромбоцитарной протромбиназы, т. е. включению механизма коагуляционного гемостаза. На агрегатах тромбоцитов образуется небольшое количество нитей фибрина, в сетях которого задерживаются форменные элементы крови.
5. Ретракция тромбоцитарного тромба, т. е. уплотнение и закрепление тромбоцитарной пробки в поврежденном сосуде за счет фибриновых нитей и гемостаз на этом заканчивается. Но в крупных сосудах тромбоцитарный тромб, будучи непрочным, не выдерживает высокого кровяного давления и вымывается. Поэтому в крупных сосудах на основе тромбоцитарного тромба образуется более прочный фибриновый тромб, для формирования которого включается ферментативный коагуляционный механизм.
Коагуляционный механизм гемостаза. Этот механизм имеет место при травме крупных сосудов и протекает через ряд последовательных фаз.
Первая фаза. Самой сложной и продолжительной фазой является формирование протромбиназы. Формируются тканевая и кровяная протромбиназы.
Образование тканевой протромбиназы запускается тканевым тромбопластином (фосфолипиды), представляющего собой фрагменты клеточных мембран и образующегося при повреждении стенок сосуда и окружающих тканей. В формировании тканевой протромбиназы участвуют плазменные факторы IV, V, VII, X. Эта фаза длится 5-10 с.
Кровяная протромбиназа образуется медленнее, чем тканевая Тромбоцитарный и эритроцитарный тромбопластин высвобождаются при разрушении тромбоцитов и эритроцитов. Начальной реакцией является активация XII фактора, которая осуществляется при его контакте с обнажающимися при повреждении сосуда волокнами коллагена. Затем фактор XII с помощью активированного им калликреина и кинина активирует фактор XI, образуя с ним комплекс. На фосфолипидах разрушенных тромбоцитов и эритроцитов завершается образование комплекса фактор XII + фактор XI. В дальнейшем реакции образования кровяной протромбиназы протекают на матрице фосфолипидов. Под влиянием фактора XI активируется фактор IX, который реагирует с фактором IV (ионы кальция) и VIII, образуя кальциевый комплекс. Он адсорбируется на фосфолипидах и затем активирует фактор X. Этот фактор на фосфолипидах же образует комплекс фактор Х + фактор V + фактор IV и завершает образование кровяной протромбиназы. Образование кровяной протромбиназы длится 5-10 минут.
Вторая фаза. Образование протромбиназы знаменует начало второй фазы свертывания крови - образование тромбина из протромбина. Протромбиназа адсорбирует протромбин и на своей поверхности превращает его в тромбин. Этот процесс протекает с участием факторов IV, V, X, а также факторов 1 и 2 тромбоцитов. Вторая фаза длится 2-5 с.
Третья фаза. В третьей фазе происходит образование (превращение) нерастворимого фибрина из фибриногена. Эта фаза протекает в три этапа. На первом этапе под влиянием тромбина происходит отщепление пептидов, что приводит к образованию желеобразного фибрин-мономера. Затем с участием ионов кальция из него образуется растворимый фибрин-полимер. На третьем этапе при участии фактора XIII и фибриназы тканей, тромбоцитов и эритроцитов происходит образование окончательного (нерастворимого) фибрина-полимера. Фибриназа при этом образует прочные пептидные связи между соседними молекулами фибрина-полимера, что в целом увеличивает его прочность и устойчивость к фибринолизу. В этой фибриновой сети задерживаются форменные элементы крови, формируется кровяной сгусток (тромб), который уменьшает или полностью прекращает кровопотерю.
Спустя некоторое время после образования сгустка тромб начинает уплотняться, и из него выдавливается сыворотка. Этот процесс называется ретракцией сгустка. Он протекает при участии сократительного белка тромбоцитов (тромбостенина) и ионов кальция. В результате ретракции тромб плотнее закрывает поврежденный сосуд и сближает края раны.
Одновременно с ретракцией сгустка начинается постепенное ферментативное растворение образовавшегося фибрина - фибринолиз, в результате которого восстанавливается просвет закупоренного сгустком сосуда. Расщепление фибрина происходит под влиянием плазмина (фибринолизина), который находится в плазме крови в виде профермента плазминогена, активирование которого происходит под влиянием активаторов плазминогена плазмы и тканей. Он разрывает пептидные связи фибрина, в результате чего фибрин растворяется.
Ретракцию кровяного сгустка и фибринолиз выделяют как дополнительные фазы свертывания крови.
Нарушение процесса свертывания крови происходит при недостатке или отсутствии какого-либо фактора, участвующего в гомеостазе. Так, например, известно наследственное заболевание гемофилия,которое встречается только у мужчин и характеризуется частыми и длительным кровотечением. Это заболевание обусловлено дефицитом факторов VIII и IX, которые называются антигемофильными.
Свертывание крови может протекать под влиянием факторов, ускоряющих и замедляющих этот процесс.
Факторы, ускоряющие процесс свертывания крови:
• разрушение форменных элементов крови и клеток тканей (увеличивается выход факторов, участвующих в свертывании крови):
• ионы кальция (участвуют во всех основных фазах свертывания крови);
• витамин К (участвует в синтезе протромбина);
• тепло (свертывание крови является ферментативным процессом);
Факторы, замедляющие свертывание крови:
• устранение механических повреждений форменных элементов крови (парафинирование канюль и емкостей для взятия донорской крови);
• цитрат натрия (осаждает ионы кальция);
Противосвертывающие механизмы. В нормальных условиях кровь в сосудах всегда находится в жидком состоянии, хотя условия для образования внутрисосудистых тромбов существуют постоянно. Поддержание жидкого состояния крови обеспечивается по принципу саморегуляции с формированием соответствующий функциональной системы. Главными аппаратами реакций этой функциональной системы являются свертывающая я противосвертывающая системы. В настоящее время принято выделять две Противосвертывающие системы - первую и вторую.
Первая противосвертывающая система (ППС) осуществляет нейтрализацию тромбина в циркулирующей крови при условии его медленного образования и в небольших количествах. Нейтрализация тромбина осуществляется теми антикоагулянтами, которые постоянно находятся в крови и поэтому ППС функционирует постоянно. К таким веществам относятся:
• фибрин, который адсорбирует часть тромбина;
• антитромбины (известно 4 вида антитромбинов), они препятствуют превращению протромбина в тромбин;
• гепарин - блокирует фазу перехода протромбина в тромбин и фибриногена в фибрин, а также тормозит первую фазу свертывания крови;
• продукты лизиса (разрушения фибрина), которые обладают антитромбиновой активностью, тормозят образование протромбиназы;
• клетки ретикуло-эндотелиальной системы поглощают тромбин плазмы крови.
При быстром лавинообразном нарастании количества тромбина в крови ППС не может предотвратить образование внутрисосудистых тромбов. В этом случае в действие вступает вторая противосвертывающая система (ВПС), которая обеспечивает поддержание жидкого состояния крови в сосудах рефлекторно-гуморальным путем по следующей схеме. Резкое повышение концентрации тромбина в циркулирующей крови приводит к раздражению сосудистых хеморецепторов. Импульсы от них поступают в гигантоклеточное ядро ретикулярной формации продолговатого мозга, а затем по эфферентным путям к ретикуло-эндотелиальной системе (печень, легкие и др.). В кровь выделяются в больших количествах гепарин и вещества, которые осуществляют и стимулируют фибринолиз (например, активаторы плазминогена).
Гепарин ингибирует первые три фазы свертывания крови, вступает в связь с веществами, которые принимают участие в свертывании крови. Образующиеся при этом комплексы с тромбином, фибриногеном, адреналином, серотонином, фактором XIII и др. обладают антикоагулянтной активностью и литическим действием на нестабилизированный фибрин.
Следовательно, поддержание крови в жидком состоянии осуществляется благодаря действию ППС и ВПС.
Регуляция свертывания крови. Регуляция свертывания крови осуществляется с помощью нейро-гуморальных механизмов. Возбуждение симпатического отдела вегетативной нервной системы, возникающее при страхе, боли, при стрессовых состояниях, приводит к значительному ускорению свертывания крови, что называется гиперкоагуляцией. Основная роль в этом механизме принадлежит адреналину и норадреналину. Адреналин запускает ряд плазменных и тканевых реакций.
Во-первых, высвобождение из сосудистой стенки тромбопластина, который быстро превращается в тканевую протромбиназу.
Во-вторых, адреналин активирует фактор XII, который является инициатором образования кровяной протромбиназы.
В-третьих, адреналин активирует тканевые липазы, которые расщепляют жиры и тем самым увеличивается содержание жирных кислот в крови, обладающих тромбопластической активностью.
В-четвертых, адреналин усиливает высвобождение фосфолипидов из форменных элементов крови, особенно из эритроцитов.
Раздражение блуждающего нерва или введение ацетилхолина приводит к выделению из стенок сосудов веществ, аналогичных тем, которые выделяются при действии адреналина. Следовательно, в процессе эволюции в системе гемокоагуляции сформировалась лишь одна защитно-приспособительная реакция - гиперкоагулемия, направленная на срочную остановку кровотечения. Идентичность сдвигов гемокоагуляции при раздражении симпатического и парасимпатического отделов вегетативной нервной системы свидетельствует о том, что первичной гипокоагуляции не существует, она всегда вторична и развивается после первичной гиперкоагуляции как результат (следствие) расходования части факторов свертывания крови.
Ускорение гемокоауляции вызывает усиление фибринолиза, что обеспечивает расщепление избытка фибрина. Активация фибринолиза наблюдается при физической работе, эмоциях, болевом раздражении.
На свертывание крови оказывают влияние высшие отделы ЦНС, в том числе и кора больших полушарий головного мозга, что подтверждается возможностью изменения гемокоауляции условно-рефлекторно. Она реализует свои влияния через вегетативную нервную систему и эндокринные железы, .гормоны которых обладают вазоактивным действием. Импульсы из ЦНС поступают к кроветворным органам, к органам, депонирующим кровь и вызывают увеличение выхода крови из печени, селезенки, активацию плазменных факторов. Это приводит к быстрому образованию протромбиназы. Затем включаются гуморальные механизмы,, которые поддерживают и продолжают активацию свертывающей системы и одновременно снижают действия противосвертывающей. Значение условно-рефлекторной гиперкоагуляции состоит, видимо, в подготовке организма к защите от кровопотери.
Система свертывания крови входит в состав более обширной системы - системы регуляции агрегатного состояния крови и коллоидов (PACK), которая поддерживает постоянство внутренней среды организма и ее агрегатное состояние на таком уровне, который необходим для нормальной жизнедеятельности путем обеспечения поддержания жидкого состояния крови, восстановления свойств стенок сосудов, которые изменяются даже при нормальном их функционировании.
Группы крови
Учение о группах крови приобретает особое значение в связи с частой необходимостью возмещения потери крови при ранениях, оперативных вмешательствах, при хронических инфекциях и по другим медицинским показаниям. В основе деления крови на группы лежит реакция агглютинации, которая обусловлена наличием антигенов (агглютиногенов) в эритроцитах и антител (агглютининов) в плазме крови. В системе АВО выделяют два основных агглютиногена А и В (полисахаридно-аминокислотные комплексы мембраны эритроцитов) и два агглютинина - альфа и бета (гамма-глобулины).
При реакции антиген - антитело молекула антитела образует .связь между двумя эритроцитами. Многократно повторяясь, она приводит к склеиванию большого числа эритроцитов.
В зависимости от содержания агглютиногенов и агглютининов в крови конкретного человека в системе АВ0 выделяют 4 основных группы, которые обозначают цифрами и теми агглютиногенами, которые содержатся в эритроцитах этой группы.
• I (0) - агглютиногены в эритроцитах не содержатся, в плазме содержатся агглютинины альфа и бета.
• II (А) - в эритроцитах агглютиноген А, в плазме агглютинин бета.
• III (В) - в эритроцитах агглютиноген В, в плазме агглютинин альфа.
• IV (АВ) - в эритроцитах агглютиногены А и В, агглютининов в плазме нет.
Так как реакция агглютинации происходит при встрече одноименных агглютиногенов и агглютининов (например, А и альфа, В и бета), то считали возможным переливать небольшие количества иногруппной крови. Было разработано правило переливания: в эритроцитах донора (человека, дающего кровь) учитывали наличие агглютиногенов, а в плазме реципиента (человека, получающего кровь) - агглютининов. Донорскую кровь подбирали так, чтобы эритроциты донора не агглютинировались агглютининами крови реципиента. Плазма донора, ввиду переливания небольшого ее объема, во внимание не принималась, т. к. она значительно разбавлялась плазмой реципиента и ее агглютинины теряли свои агглютинирующие свойства. Это правило называется правилом разведения.
Исходя из этого представления, первую группу крови можно переливать во все группы (I, II, III, IV); вторую группу - во вторую и четвертую; третью - в третью и четвертую; четвертую группу можно переливать только в кровь четвертой группы. Поэтому людей с первой группой крови называют универсальными донорами, а людей с четвертой - универсальными реципиентами.
В настоящее время от этого принципа переливания крови отказались практически полностью и для переливания используют только одногруппную кровь. Одной из причин отказа от классических правил переливания крови явилась невозможность переливать донорскую иногруппную кровь в больших количествах, что бывает необходимым при ряде хирургических операций. Другой причиной послужило наличие большого количества подгрупп крови. Оказалось, что агглютиноген А существует более чем в 10 вариантах, различающихся агглютинационными свойствами. Агглютиноген В тоже существует в нескольких вариантах, активность которых убывает в порядке их нумерации.
Кроме того, к настоящему времени стали известны и другие агглютиногены (кроме системы АВ0). Это М, N, S, Р и другие - всего около 400 агглютиногенов. В каждой из этих систем имеется, как правило, несколько агглютиногенов, составляющих разные комбинации, которые определяют группы крови в данной системе. Эти агглютиногены также находятся в эритроцитах независимо от системы АВ0 и друг от друга. Их антигенные свойства выражены слабо и при переливании крови ими можно пренебрегать. Наибольшее значение для клиники имеет система АВ0 и резус-фактора.
Определение группы крови проводится путем смешивания капли крови исследуемого человека со стандартными сыворотками, содержащими иммунные анти-А и анти-В агглютинины.
Резус-фактор. Среди агглютиногенов, не входящих в систему АВО, одним из первых был обнаружен резус-агглютиноген (резус-фактор). Этот агглютиноген содержится у 85% людей. Кровь, в которой содержится резус-фактор, называется резус-положительной, а в которой отсутствует - резус-отрицательной. К настоящему времени выявлено 6 разновидностей резус-агглютиногенов.
Знание о резус-факторе имеет значение при переливании крови, а также в акушерстве и гинекологии. Если резус-положительную кровь перелить резус-отрицательному реципиенту, то в его организме образуются антирезус-агглютинины. При повторном переливании этому человеку резус-положительной крови произойдет агглютинация эритроцитов.
При беременности, если кровь матери резус-отрицательная, а кровь плода резус-положительная, то, проникая в организм матери резус-агглютиногены вызывают у нее образование антител (антирезус-агглютининов), которые, диффундируя в кровь плода, вызывают реакцию агглютинации его эритроцитов с последующим их гемолизом (резус-конфликт). Выраженный резус-конфликт возникает лишь при высокой концентрации антирезус-агглютининов. Поэтому, чаще всего, первый ребенок рождается без осложнений. Опасность резус-конфликта нарастает при повторных беременностях.
Читайте также:

