Что такое энергетический уровень в химии кратко
Обновлено: 02.07.2024
Энергетический уровень — собственные значения энергии квантовых систем, то есть систем, состоящих из микрочастиц (электронов, протонов и других элементарных частиц) и подчиняющихся законам квантовой механики. Каждый уровень характеризуется определённым состоянием системы, или подмножеством таковых в случае вырождения. Понятие применимо к атомам (электронные уровни), молекулам (различные уровни, соответствующие колебаниям и вращениям), атомным ядрам (внутриядерные энергетические уровни) и т.д.
Содержание
Электронные энергетические уровни
В современном понятии об орбитальной модели атома, электроны в атоме способны обладать лишь определёнными величинами энергии, и переходить с одного энергетического уровня на другой лишь скачком. Разница между энергетическими уровнями определяет частоту кванта света, выделяемого или поглощаемого при переходе. Каждой паре значений главного квантового числа n и орбитального квантового числа l соответствует определённый уровень энергии, которой может обладать электрон.
Молекулярные энергетические уровни
Согласно замыслу одного из участников Википедии, на этом месте должен располагаться специальный раздел.
Вы можете помочь проекту, написав этот раздел.
Внутриядерные энергетические уровни
Термин появился благодаря исследованию радиоактивности. Радиационное излучение разделяется на три части: альфа-лучи, бета-лучи и гамма-лучи. Исследования показали, что альфа-излучение состоит из ядер гелия-4 (см. альфа-частица), бета-излучение является потоком быстро движущихся электронов, а гамма-лучи являются электромагнитными. Поскольку энергии переходов между различными электронными уровнями недостаточно для возникновения гамма-лучей, стало понятно, что их источник нужно искать внутри атомного ядра, то есть ядро атома само может обладать различными энергетическими уровнями, при переходах между которыми и происходит излучение гамма-квантов. Гамма-лучи расширили спектр известных электромагнитных волн, и все волны короче 10 −3 нм называются гамма-лучами.
См. также
- Квантовая химия
- Атомная физика
- Квантовая физика
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое "Энергетический уровень" в других словарях:
ЭНЕРГЕТИЧЕСКИЙ УРОВЕНЬ — ЭНЕРГЕТИЧЕСКИЙ УРОВЕНЬ, фиксированное количество энергии, которой обладают ядро атома, ЭЛЕКТРОН, атом или молекула. Например, внутри атома энергия электронов не изменяется беспрерывно. Она выражается в дискретном ряде значений, которые и носят… … Научно-технический энциклопедический словарь
энергетический уровень — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN energy levelstate … Справочник технического переводчика
энергетический уровень — – строго определенная энергия, которой характеризуется данный электрон в атоме, соответствующая его расстоянию от ядра. Чем ближе электрон к ядру, тем меньше энергия, которой он обладает. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
энергетический уровень — energijos lygmuo statusas T sritis chemija apibrėžtis Energijos vertė, kurią gali turėti kvantinė sistema stacionariojoje būsenoje. atitikmenys: angl. energy level rus. уровень энергии; энергетический уровень … Chemijos terminų aiškinamasis žodynas
энергетический уровень — energijos lygmuo statusas T sritis fizika atitikmenys: angl. energy level vok. Energieniveau, n rus. уровень энергии, m; энергетический уровень, m pranc. niveau d’énergie, m; niveau énergétique, m … Fizikos terminų žodynas
энергетический уровень — energijos lygmuo statusas T sritis Standartizacija ir metrologija apibrėžtis Energijos vertė, kurią gali turėti kvantinė nuostoviosios būsenos sistema. atitikmenys: angl. energy level vok. Energieniveau, n rus. энергетический уровень, m pranc.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Энергетический уровень — см. Уровни энергии … Большая советская энциклопедия
энергетический уровень — Возможное значение полной энергии консервативной квантовой системы.. Иначе: Собственное значение гамильтониана, не зависящего от времени … Политехнический терминологический толковый словарь
энергетический уровень механизации (автоматизации) живого труда — энергетический уровень механизации (автоматизации) труда ΩТ Отношение полезных затрат энергии неживой природы в течение неперекрытого машинного времени к сумме полезных затрат энергии неживой природы и людей в течение штучного времени.… … Справочник технического переводчика
энергетический уровень механизации (автоматизации) средств технологического оснащения — энергетический уровень механизации (автоматизации) СТО ΩП Отношение полезных затрат энергии неживой природы в течение полного машинного времени к сумме полезных затрат энергии неживой природы и людей в течение штучного времени. [ГОСТ 23004… … Справочник технического переводчика
Во многих современных учебниках понятия энергетический уровень и электронный слой отождествляются, но это весьма некорректное отождествление. Поясним данный момент.
Энергетические уровни (в англ. energy levels) - это те значения энергии, которые может принимать электрон в атоме.
Если атому водорода сообщить энергию, то его электрон примет значение энергии отличное от значения энергии первого уровня, условно выражаясь, в этом случае электрон первого энергетического уровня атома водорода "перескочит" на второй уровень и т.д., пока от атома не "оторвется" и атом не превратится в ион.
Поэтому употреблять такие фразы как внешний энергетический уровень, или в атоме водорода один энергетический уровень, крайне некорректно. То же касается и атомов других химических элементов.
Для того чтобы объяснить как распределяются электроны в атоме, корректнее применять понятие электронный слой.
Электронный слой (в англ. electron shell) - это совокупность электронов одного энергетического уровня (совокупность электронов, имеющих одинаковое значение n - главного квантового числа).
Или условно выражаясь, электронный слой - это энергетический уровень, на котором есть хотя бы один электрон.
Поэтому можно сказать к примеру, что в атоме водорода один электронный слой (но не один энергетический уровень, энергетических уровней там много), или номер периода равен количеству электронных слоёв в атоме (но не номер периода равен количеству энергетических уровней в атоме).
Также иногда электронный слой отождествляют с электронной оболочкой атома , например, в Википедии. Такое отождествление нецелесообразно, так как приводит к путанице и подмене понятий.
Электронная оболочка атома - это совокупность всех электронов данного атома. То есть, электронная оболочка - это совокупность электронных слоёв атома.
![[[pictureof]]](https://dist-tutor.info/s3/dist-tutor/user/2/ava/thumbnails/ZoUbTSpxT8AyTwl.jpg)
Вам нужны консультации по Химии по Skype?
Если да, подайте заявку. Стоимость договорная.
Чтобы закрыть это окно, нажмите "Нет".
Укажите реальные данные, иначе мы не сможем с вами связаться! Отправляя форму, Вы принимаете Условия использования и даёте Согласие на обработку персональных данных
Основы химии

Данный курс предназначен для тех, кто желает более подробно познакомиться с такой замечательной наукой, как химия и углубить свои знания.
Мы рекомендуем его учителям химии средней школы, репетиторам химии и ученикам профильных классов.
Курс состоит из разделов, каждый из которых посвящён определённой теме. Разделы рекомендуется изучать по порядку. Пока не все темы Вы сможете найти здесь, так как курс только начал пополняться материалами. В разделах особое внимание уделяется спорным теоретическим и методологическим моментам, а также распространённым заблуждениям некоторых авторов.
© Копирование материалов курса разрешено исключительно с указанием ссылки на соответствующий раздел и указанием автора.
Мы приступаем к изучению химии - мира молекул и атомов. В этой статье мы рассмотрим базисные понятия и разберемся с электронными формулами элементов.
Атом (греч. а - отриц. частица + tomos - отдел, греч. atomos - неделимый) - электронейтральная частица вещества микроскопических размеров и массы, состоящая из положительно заряженного ядра (протонов) и отрицательно заряженных электронов (электронные орбитали).
Описываемая модель атома называется "планетарной" и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом

Протон (греч. protos - первый) - положительно заряженная (+1) элементарная частица, вместе с нейтронами образует ядра атомов элементов. Нейтрон (лат. neuter - ни тот, ни другой) - нейтральная (0) элементарная частица, присутствующая в ядрах всех химических элементов, кроме водорода.
Электрон (греч. elektron - янтарь) - стабильная элементарная частица с отрицательным электрическим зарядом (-1), заряд атома - порядковый номер в таблице Менделеева - равен числу электронов (и, соответственно, протонов).
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20) в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.

Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило: порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим электроны занимают различные энергетические уровни.
Состоит из s-подуровня: одной "1s" ячейки, в которой помещаются 2 электрона (заполненный электронами - 1s 2 )
Состоит из s-подуровня: одной "s" ячейки (2s 2 ) и p-подуровня: трех "p" ячеек (2p 6 ), на которых помещается 6 электронов
Состоит из s-подуровня: одной "s" ячейки (3s 2 ), p-подуровня: трех "p" ячеек (3p 6 ) и d-подуровня: пяти "d" ячеек (3d 10 ), в которых помещается 10 электронов
Состоит из s-подуровня: одной "s" ячейки (4s 2 ), p-подуровня: трех "p" ячеек (4p 6 ), d-подуровня: пяти "d" ячеек (4d 10 ) и f-подуровня: семи "f" ячеек (4f 14 ), на которых помещается 14 электронов

Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: "s", "p" и "d", которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или атомным орбиталям, движутся электроны, создавая определенный "рисунок".
S-орбиталь похожа на сферу, p-орбиталь напоминает песочные часы, d-орбиталь - клеверный лист.

Правила заполнения электронных орбиталей и примеры
- Сперва следует заполнить орбитали с наименьшей энергией, и только после переходить к энергетически более высоким
- На орбитали (в одной "ячейке") не может располагаться более двух электронов
- Орбитали заполняются электронами так: сначала в каждую ячейку помещают по одному электрону, после чего орбитали дополняются еще одним электроном с противоположным направлением
- Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Без практики теория мертва, так что приступает к тренировке. Нам нужно составить электронную конфигурацию атомов углерода и серы. Для начала определим их порядковый номер, который подскажет нам число их электронов. У углерода - 6, у серы - 16.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.
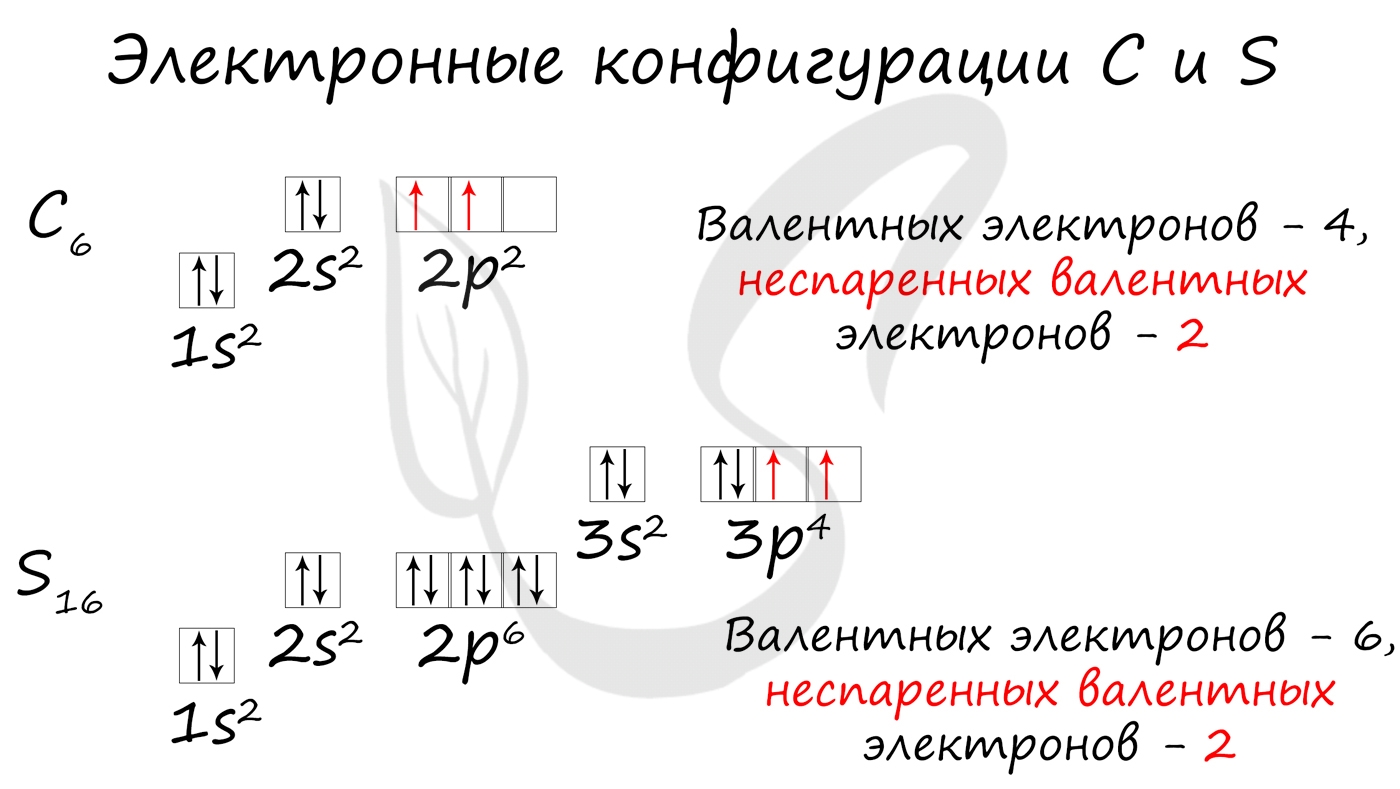
Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил. А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся одним электроном дополнили первую ячейку.
- Углерод - 1s 2 2s 2 2p 2
- Серы - 1s 2 2s 2 2p 6 3s 2 3p 4
Внешний уровень и валентные электроны
- Углерод - 2s 2 2p 2 (4 валентных электрона)
- Сера -3s 2 3p 4 (6 валентных электронов)
Неспаренные валентные электроны способны к образованию химической связи. Их число соответствует количеству связей, которые данный атом может образовать с другими атомами. Таким образом неспаренные валентные электроны тесно связаны с валентностью - способностью атомов образовывать определенное число химических связей.
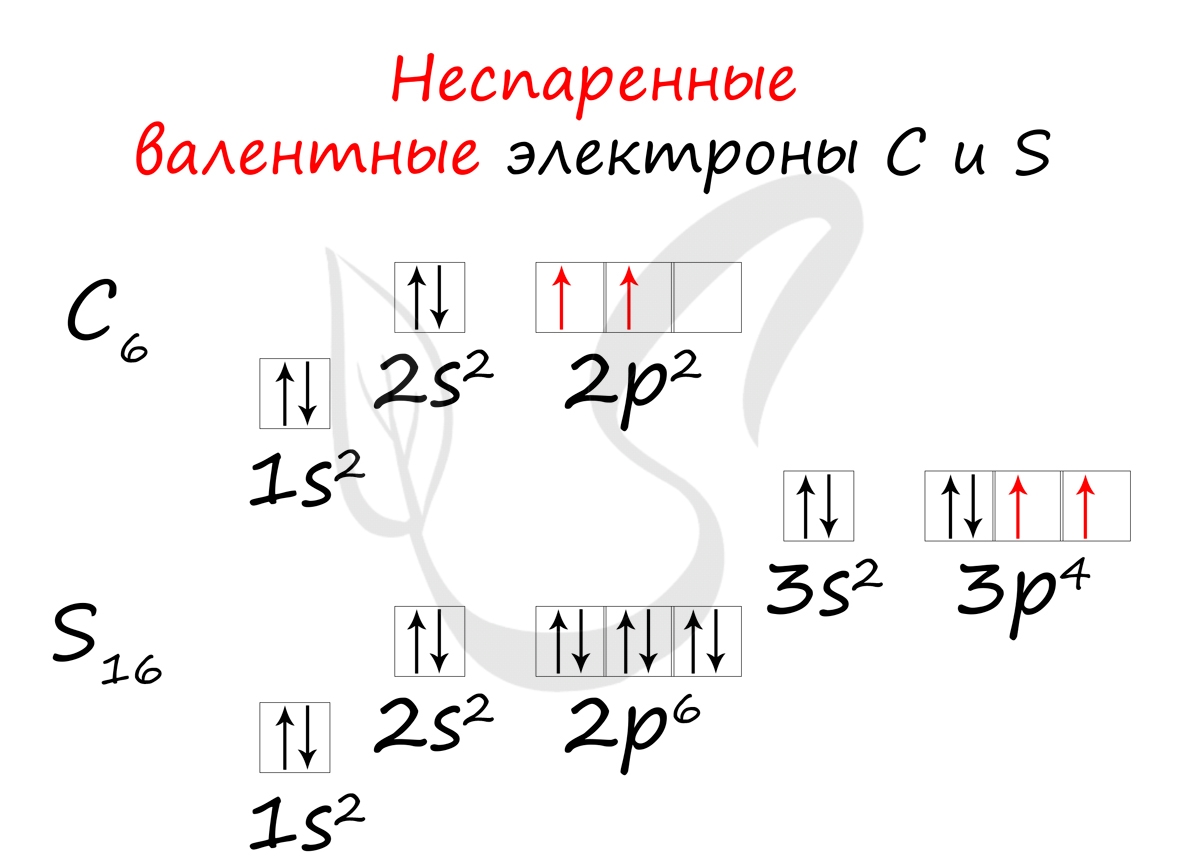
- Углерод - 2s 2 2p 2 (2 неспаренных валентных электрона)
- Сера -3s 2 3p 4 (2 неспаренных валентных электрона)
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных электронов. Ниже будет дано наглядное объяснение этой задаче.
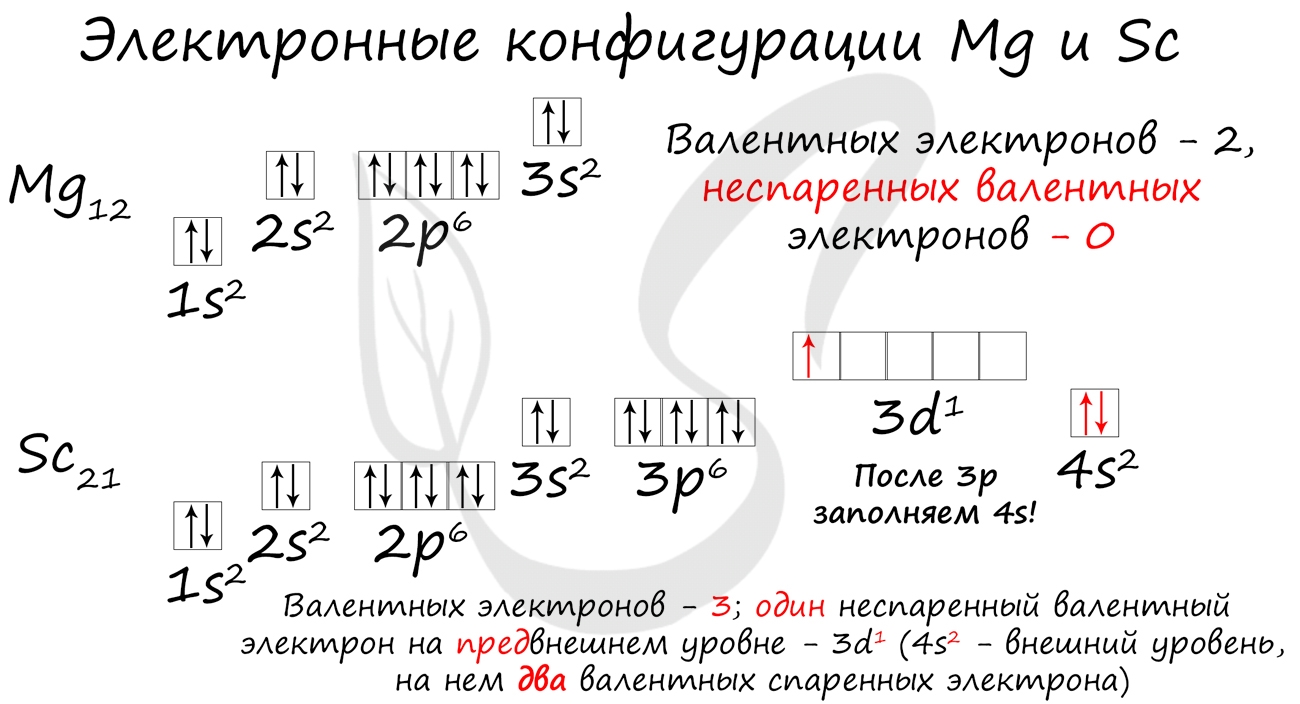
- Магний - 1s 2 2s 2 2p 6 3s 2
- Скандий - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1
Читайте также:
- Проект инклюзивной среды школы
- Какие образы возникают у тебя при прослушивании этюда совпадают ли они с впечатлениями твоих кратко
- Закрытая школа в какой серии появилась юля
- Сенсорное воспитание как основа умственного воспитания дошкольников кратко
- Что такое цивилизация как объяснялось это понятие философами прошлого кратко

