Сообщение на тему применение алканов и алкенов
Обновлено: 02.07.2024
II. Химические свойства алканов
1. Реакции замещения
а) Галогенирование
При действии света - hν или нагревании (стадийно – замещение атомов водорода на галоген носит последовательный цепной характер. Большой вклад в разработку цепных реакций внёс физик, академик, лауреат Нобелевской премии Н. Н. Семёнов )
В реакции образуются вещества галогеналканы RГ или С n H 2n+1 Г
(Г - это галогены F, Cl, Br, I)
CH 4 + Cl 2 hν → CH 3 Cl + HCl (1 стадия)
CH 3 Cl + Cl 2 hν → CH 2 Cl 2 + HCl (2 стадия)
Скорость реакции замещения водорода на атом галогена у галогеналканов выше, чем у соответствующего алкана, это связано с взаимным влиянием атомов в молекуле:
Электронная плотность связи С – Cl смещена к более электроотрицательному хлору, в результате на нём скапливается частичный отрицательный заряд, а на атоме углерода – частичный положительный заряд.
На атом углерода в метильной группе ( - СН3) создаётся дефицит электронной плотности, поэтому он компенсирует свой заряд за счёт соседних атомов водорода, в результате связь С – Н становится менее прочной и атомы водорода легче замещаются на атомы хлора. При увеличении углеводородного радикала наиболее подвижными остаются атомы водорода у атома углерода ближайщего к заместителю:
Со фтором реакция идёт со взрывом.
С хлором и бромом требуется инициатор.
Иодирование происходит обратимо, поэтому требуется окислитель для удаления HI из рекции.
Внимание!
В реакциях замещения алканов легче всего замещаются атомы водорода у третичных атомов углерода, затем у вторичных и, в последнюю очередь, у первичных. Для хлорирования эта закономерность не соблюдается при T>400˚C.
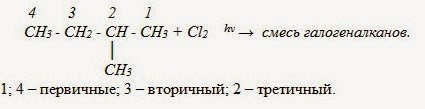
б) Нитрование (реакция М.И. Коновалова , он провёл её впервые в 1888 г)
2. Реакции отщепления (дегидрирование)
б) При нагревании до 1500 С происходит образование ацетилена и водорода:
3. Реакции перегруппировки (изомеризация)
4. Реакции горения (горят светлым не коптящим пламенем)
Помните! Смесь метана с воздухом и кислородом взрывоопасна
5. Реакции разложения
а) Крекинг при температуре 700-1000°С разрываются (-С-С-) связи:
б) Пиролиз при температуре 1000°С разрываются все связи,
продукты – С и Н2:
в) Конверсия метана с образованием синтез – газа (СО + Н2)
III. Получение алканов
1. Получение в лаборатории
1. Гидролиз карбида алюминия (получение метана):
2. Реакция Вюрца (взаимодействие натрия с галогенпроизводными алканов):
(R- это радикал; Г- это галоген)
3. Термическое декарбоксилирование солей карбоновых кислот в присутствии щелочей:
(ацетат натрия+ едкий натр=(метан+карбонат натрия)
этилат натрия этан
4. Каталитическое гидрирование алкенов и алкинов:
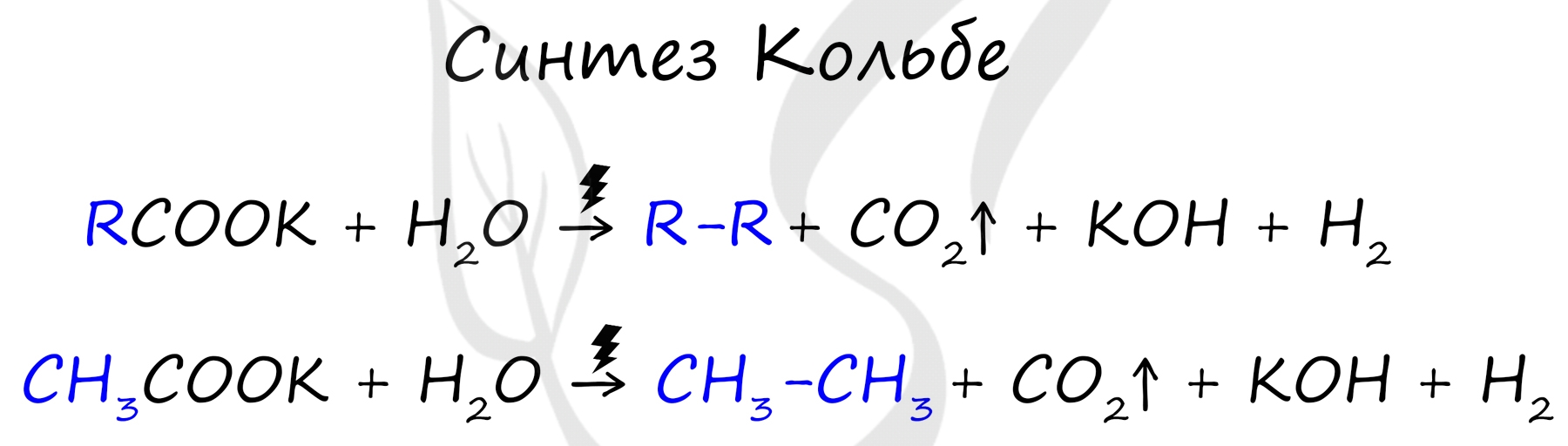
5. Электролиз растворов солей карбоновых кислот - реакция КОЛЬБЕ
Пример. Электролиз водного раствора ацетата натрия
Катод (-): H2O , Na + - Процесс восстановления: 2H 2 O + 2ē → H 2 ↑ + 2OH -
Анод (+): H 2 O, CH3COO - (анионы органических кислот активнее воды) – Процесс окисления:
2H2O + 2CH3COONa эл . ток = H2 + 2NaHCO3 + C2H6
2. Получение в промышленности
1. Из природного и попутного нефтяного газа
Важнейшим источником алканов в природе является природный газ, минеральное углеводородное сырье - нефть и сопутствующие ей нефтяные газы. Природный газ на 95 процентов состоит из метана. Такой же состав имеет болотный газ, образующийся в результате переработки бактериями (гниения) углеводов.
Метан называют ещё и болотным; рудничным газом.
Попутные нефтяные газы состоят в основном из этана, пропана, бутана и частично пентана. Их отделяют от нефти на специальных установках по подготовке нефти. При отсутствии газоконденсатных станций попутные нефтяные газы сжигают в факелах, что является крайне неразумной и разорительной практикой в нефтедобыче. Одновременно с газами нефть очищается от воды, грязи и песка, после чего поступает в трубу для транспортировки. Из нефти при ее разгонке (перегонке, дистилляции) отбирая последовательно все более и более высококипящие фракции получают:
бензины - т. кип. от 40 до 180 С, (содержит углеводороды С5-С10), состоит более, чем из 100 индивидуальных соединений, нормальных и разветвленных алканов, циклоалканов, алкенов и ароматических углеводородов;
легкий газойль (дизельное топливо) 230-305 С (С13-С17);
тяжелый газойль и легкий дистиллят смазочного масла 305-405 С (С18-С25);
смазочные масла 405-515 С (С26-С38).
Остаток после перегонки нефти называется асфальтом или битумом.
2. Синтезом из водяного газа:
3. Синтезом из простых веществ:
IV. Применение
1. Предельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека.
2. Использование в качестве топлива – в котельных установках, бензин, дизельное топливо, авиационное топливо, баллоны с пропан-бутановой смесью для бытовых плит.
3. Вазелин используется в медицине, парфюмерии, косметике, высшие алканы входят в состав смазочных масел, соединения алканов применяются в качестве хладагентов в домашних холодильниках.
4. Смесь изомерных пентанов и гексанов называется петролейным эфиром и применяется в качестве растворителя. Циклогексан также широко применяется в качестве растворителя и для синтеза полимеров.
5. Метан используется для производства шин и краски.
6. Значение алканов в современном мире огромно. В нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Велико значение в медицине, парфюмерии и косметике.
Предельные углеводороды с общей формулой CnH2n+2, основным источником которых служат нефть, газ и каменный уголь, являются сырьевой базой для химической промышленности и основными природным источником энергии.
Применение алканов

Первоначально насыщенные углеводороды использовались как топливо — в результате горения высвобождается энергия:
Области применения алканов связаны с их физико-химическими свойствами:
- Газообразные алканы (метан, пропан и бутан). Горят бледно-голубым или бесцветным пламенем, при этом выделяется большое количество тепла. Применяются для бытовых нужд – как топливо в газовых плитах, зажигалках и газовых баллончиках для туристических горелок. В промышленных объемах — как топливо для газовых электростанций, вырабатывающих тепло и электроэнергию. Метан как часть природного газа — один из лучших природных субстратов, используемых в биотехнологии.
- Жидкие алканы. Являются основной частью горючего для двигателей внутреннего сгорания – от мотоциклетных до ракетных. Изомеры линейных алканов применяют как добавку для повышения качества топлива. Смесь предельных углеводородов с длиной цепочки не более 15 атомов углерода — вазелиновое масло применяют в косметологии и медицине. В промышленности применяют гудрон (остаточный продукт после переработки нефти) для производства строительных кровельных и дорожных битумов и кокса.
- Твердые алканы. Смесь жидких и твердых углеводородов с цепочкой до 25 атомов углерода – вазелин — густая масса, используется в медицине и косметических целях. Смесь алканов С20 -С35 называют парафином и используют для производства свечей, обработки упаковочных материалов и спичек. Парафиновые углеводороды служат основным сырьем для биосинтеза.
Применение в промышленности
Парафины являются основой для производства целого ряда веществ:
- азотной кислоты HNO3;
- насыщенных одноатомных cпиртов СnH2n+1OH;
- сажа (аморфный углерод) — для типографской краски и резины;
- галогензамещенных растворителей и хладонов;
- алкенов;
- альдегидов, которые используются в производстве органических кислот и пластмасс;
- как нефтехимическое сырье для производства ПАВ.
Алканы применяются при производстве синтетических моющих средств.
Исходными веществами для этого служат парафины фракции С41-С44 .
Применение в медицине и фармации

Смесь жидких и твердых парафинов с С Значение алканов
Предельные углеводороды применяются в пищевой и химической промышленности, в энергетике, косметологии и медицине.
Алканы служат растворителями и сырьем для производства лаков, красок, мазей. Их используют в качестве топлива и компонентов для различных битумов.
Химическое производство пластика, ПАВов и синтетических тканей использует в качестве сырья алканы.
С развитием технологий сферы применения насыщенных углеводородов расширяется.

Алканы получают из нефтепродуктов, природного газа, каменного угля. Главное применение алканов – использование в качестве топлива. Из веществ также изготавливают растворители, косметические средства, асфальт.
Описание
Алканы – класс насыщенных или предельных углеводородов. Это значит, что молекулы алканов содержат максимальное количество атомов водорода. Общая формула соединений гомологического ряда алканов – CnH2n+2. Названия веществ составляются из греческого обозначения числительных и суффикса -ан.
Физические и химические свойства алканов зависят от их строения. С возрастанием количества атомов углерода в молекуле происходит переход от газообразных веществ к твёрдым соединениям.
Агрегатное состояние алканов в зависимости от количества атомов углерода:

Рис. 1. Парафиновые свечи.
С увеличением молекулярной массы в гомологическом ряду повышаются температуры плавления и кипения.
Применение
Алканы выделяют из полезных ископаемых – нефти, газа, каменного угля. На разных этапах переработки получают бензин, керосин, мазут. Алканы используются в медицине, косметологии, строительстве.

Рис. 2. Нефть содержит жидкие алканы.
В таблице описаны основные области применения предельных углеводородов.
Область
Что используют
Как используют
Бензин, керосин, мазут
В качестве ракетного, моторного топлива
В качестве бытового газа для приготовления пищи
Петролейный эфир (смесь изопентанов и изогексанов),
Изготовление растворителей, смазочных масел, пропитки
Изготовление вазелинового масла (смесь жидких алканов), вазелина (смесь жидких и твёрдых алканов), свечей, моющих средств, лаков, эмалей, мыла. В качестве пропитки спичек. Использование при производстве органических кислот
Изготовление спиртов, альдегидов, кислот
Вазелин, вазелиновое масло
В качестве пропеллентов для изготовления аэрозолей
Изготовление увлажняющих косметических средств
Гудрон (дёготь) – конечный продукт переработки нефти, содержащий смесь алканов, циклоалканов, аренов, металлов, неметаллов
Для изготовления асфальтовых дорог
В качестве пропитки упаковочной бумаги
Производство жевательных резинок

Рис. 3. Гудрон.
Алканы используются при изготовлении каучука, синтетических тканей, пластмасс, поверхностно-активных веществ. В качестве заправки баллонов для тушения пожаров используются пропан и бутан в сжиженном виде.
Что мы узнали?
Узнали кратко об области применения алканов. Насыщенные углеводороды в газообразном, жидком, твёрдом состоянии используются в химической, пищевой, бумажной, энергетической отраслях, в косметологии и строительстве. Из алканов производят растворители, краски, лаки, мыло, свечи, мази, асфальт. Бензин, керосин, мазут, состоящие из жидких алканов, используют в качестве топлива. Газообразные алканы применяются в быту и для производства аэрозолей. Основные источники алканов – нефть, природный газ, каменный уголь.
Предельными углеводородами (алканами) называются соединения, состоящие из атомов углерода и водорода, соединенных между собой только Q-связями, и не содержащие циклов. В алканах атомы углерода находятся в степени гибридизацииsp3 .
1.2 Методы получения алканов.
Главным природным источником предельных углеводородов является нефть, а для первых членов гомологического ряда — природный газ. Однако выделение индивидуальных соединений из нефти или продуктов ее крекинга- весьма трудоемкая, а часто и невыполнимая задача, поэтому приходится прибегать к синтетическим методам получения.
1. Алканы образуются при действии металлического натрия на моногалогенпроизводные — реакция Вюрца:
НзС-СН2—Вг + Вг-СН2-СH3 СНз-СН2—СН2—СНз + 2NaBr
Если взяты разные галогенпроизводные, то образуется смесь трех различных алканов, так как вероятность встречи в реакционном комплексе молекул одинаковых или разных равна, а реакционная способность их близка:
3C2H5I + 3CH3CH2CH2IС4Н10 + С5Н12 + С6Н14 + 6NaI
2. Алканы могут быть получены при восстановлении алкенов или алкинов водородом в присутствии катализаторов :
3. Самые разнообразные производные алканов могут быть восстановлены при высокой температуре иодистоводородной кислотой:
CHBr +2HI CH2 + HBr + I2
Однако в этих случаях иногда наблюдается частичная изомеризация углеродного скелета — образуются более разветвленные алканы.
4. Алканы могут быть получены при сплавлении солей карбоновых кислот со щелочью. Образующийся при этом алкан содержит на один атом углерода меньше, чем исходная карбоновая кислота:
СНз—С +NaOH CH4+Na2C03
1.3 Представители алканов
Согласно теории строения А. М. Бутлерова, физические свойства веществ зависят от их состава и строения. Рассмотрим на примере предельных углеводородов изменение физических свойств в гомологическом ряду .
Четыре первых члена гомологического ряда, начиная с метана, газообразные вещества. Начиная с пентана и выше, нормальные углеводороды представляют собой жидкости. Метан сгущается в жидкость лишь при —162 °С. У последующих членов ряда температура кипения возрастает, причем при переходе к следующему гомологу она возрастает приблизительно на 25°.
Плотность углеводородов при температуре кипения для нижних членов ряда увеличивается сначала быстро, а затем все медленнее: от 0,416 у метана до величины, несколько большей 0,78 .Температура плавления нормальных углеводородов в гомологическом ряду увеличивается медленно. Начиная с углеводорода С16Н34, высшие гомологи при обычной температуре — вещества твердые.
Температура кипения у всех разветвленных алканов ниже, чем у нормальных алканов, и притом тем ниже, чем более разветвлена углеродная цепь молекулы. Это видно, например, из сравнения температур кипения трех изомерных пентанов. Наоборот, температура плавления оказывается самой высокой у изомеров с максимально разветвленной углеродной цепью. Так, из всех изомерных октанов лишь гекса-метилэтап (СН3)3С—С (СНз)3 является твердым веществом уже при обычной температуре (т. пл. 104° С). Эти закономерности объясняются следующими причинами.
Превращению жидкости в газ препятствуют ван-дер-ваальсовы силы взаимодействия между атомами отдельных молекул. Поэтому чем больше атомов в молекуле, тем выше температура кипения вещества, следовательно, в гомологическом ряду температура кипения должна равномерно расти. Если сравнить силы взаимодействия молекул н -пентана и неопентана, то ясно, что эти силы больше для молекулы с нормальной цепью углеродных атомов, чем для разветвленных, так как в молекуле неопентана центральный атом вообще выключен из взаимодействия.
Главным фактором, влияющим на температуру плавления вещества, является плотность упаковки молекулы в кристаллической решетке. Чем симметричнее молекула, тем плотнее ее упаковка в кристалле и тем выше температура плавления (у н -пентана —132° C, у неопентана —20° С)
2.1 АЛКЕНЫ (этиленовые углеводороды, олефины)
Углеводороды, в молекуле которых помимо простых Q-связей углерод — углерод и углерод — водород имеются углерод-углеродные
-связи, называются непредельными. Так как образование -связи формально эквивалентно потере молекулой двух атомсв годорода, то непредельные углеводороды содержат на 2п атомов иодорода меньше, чем предельные, где n число - связей
Ряд, члены которого отличаются друг от друга на (2Н)n, называется изологическим рядом. Так, в приведенной выше схеме изологами являются гексан, гексены, гексадиены, гексины, гексатриены и бензол.
Углеводороды, содержащие одну - связь (т. е. двойную связь), называваются алкенами (олефинами) или, по первому члену ряда - этилену, этиленовыми углеводородами. Общая формула их гомологического ряда — CnH2n
2.2 Методы получения алкенов
При действии спиртовых растворов едких щелочей на галоген производные: отщепляется галогенводород и образуется двойная связь:
Бромистый пропил Пропилен
Если в α-положении к атому углерода, связанному с галогеном, находится третичный, вторичный и первичный атомы водорода, то преимущественно отщепляется третичный атом водорода, в меньшей степени вторичный и тем более первичный (правило Зайцева):
H3C-C-CI H3C-C + KCL + H2O
H3C CH3 H3C CH3
Это связано с термодинамической устойчивостью образующихся алке-нoв. Чем больше заместителей имеет алкен у винильных атомов углерода, тем выше его устойчивость.
2. Действием на спирты водоотнимающих средств: а) при пропускании спиртов над окисью алюминия при 300—400° С.
Втор -Бутиловый спирт
б) при действии на спирты серной кислоты в мягких условияхреакция идет через промежуточное образование эфиров серной кислоты:
НзС-СН-СНз НзС-СН-СН3 H3C-CH=CH2
При дегидратации спиртов в жестких условиях в кислых средах наблюдается та же закономерность в отщеплении водородных атомов разного типа, как и при отщеплении галогенводорода.
Первой стадией этого процесса является протонирование спирта, после чего отщепляется молекула воды и образуется карбкатион:
СНз-СН2-СН-СНз + H CH3-CH2-CH-CH3 CH3-CH-CH-
Образовавшийся карбкатион стабилизируется выбросом протона из соседнего положения с образованием двойной связи (β-элиминирование). В этом случае тоже образуется наиболее разветвленный алкен (термодинамическиболее устойчивыи). При этом процессе часто наблюдаются перегруппировки карбкатионов связанные с изомеризацией углеродного скелета:
CH3 C-CH – CH3 CH3 C-CH-CH3
CH3 CH3 CH3 CH3
CH3 CH3 CH3 CH3
3. При действии Zn или Mg на дигалогенпроизводные с двумя
атомами галогена у соседних атомов углерода:
H3C – C CH2CIH3C - C - CH2+MgCI2
2.3 Представители алкенов.
Как и алкаиы, низшие гомологи ряда простейших алкенов при обычных условиях — газы, а начиная с С5 — низкокипящие жидкости (см. табл. ).
Все алкены, как и алканы, практически нерастворимы в воде и хорошо растворимы в других органических растворителях, за исключением метилового спирта; все они имеют меньшую плотность, чем вода.
3.1 АЛКИНЫ (ацетиленовые углеводороды)
Алкинами называются углеводороды, содержащие кроме Q-связей две
-связи (тройную связь) у одной пары углеродных атомов. Общая формула гомологического ряда ацетиленовых углеводородов СnН2n-2образование одной-связи формально эквивалентно потере двух атомов водорода.
Различными физическими методами доказано, что ацетилен C2H2 — I простейший представитель гомологического ряда алкинов — имеет линейную молекулу, в которой длина углерод-углеродной тройной связи равна 1,20 А, а длина связей углерод—водород 1,06 A.
3.2Методы получения алкинов.
Наиболее общим способом получения ацетиленовых углеводородов является действие спиртового раствора щелочей на дигалогенпроиз-водные предельных углеводородов с вицинальным (а) или геминаль-ным (б) расположением атомов галогена
a) CH2Br –CH2Br-> СНСН + 2НВг
б) СНз—СН2—СНСl2-> СHз-ССН+2ИСl
CH3-CH2-CCl2-CH3-> СНз-СС-СНз + 2НС1
Так как вицинальные дигалогенпроизводные обычно получают присоединением галогенов к этиленовым углеводородам, то реакцию (а) можно рассматривать как реакцию превращения этиленовых углеводородов в ацетиленовые.
Геминальные дигалогенпроизводные (оба атома галогена у одного атома углерода) являются производными кетонов или альдегидов и, следовательно, с помощью реакций (б) можно осуществить переход от карбонильных соединений к алкинам. При отщеплении галогенводородов действует уже известное правило Зайцева, что водород отщепляется от углеродного атома, содержащего меньшее количество атомов водорода.
Ацетилен можно получать непосредственно при высокотемпературном крекинге (термическом или электротермическом) метана или более , сложных углеводородов:
3.3 Представители алкинов.
Как у алканов и алкенов, низшие члены гомологического ряда алкинов в обычных условиях—газообразные вещества. Данные табл. 22 показывают, что основные физико-химические характеристики углеводородов рассмотренных классов мало отличаются друг от друга (см. таблицу).
HCC- CH2CH3 СНзСCСНз
4. ПРИМЕНЕНИЕ АЛКАНОВ, АЛКИНОВ, АЛКЕНОВ
Алкены вместе с алканами, ацетиленом и ароматическими углеводородами являются одним из главных сырьевых источников промышленности тяжелого (многотоннажного) органического синтеза.
Этилен в громадных количествах используется для переработки в полиэтилен и этиловый спирт, он идет на переработку в этилен-гликоль и употребляется в теплицах для ускорения вызревания плодов.
Пропилен перерабатывается в полипропилен, ацетон, изопропиловый спирт.
Ацетилен играет исключительно важную роль в промышленности. Его мировое производство достигает нескольких миллионов тонн. Громадное количество ацетилена используется для сварки металлов, при его горении
в кислороде температура достигает 2800° С. Это значительно более высокая температура, чем при сгорании водорода в кислороде, не говоря уже о сгорании метана. Причина этого в значительно меньшей теплоемкости СО2 по сравнению с Н2О, которой образуется больше при сгорании алканов, чем алкинов:
2СзН6 + 7O2 -> 4СО2 +6Н2О
2С2 Н2+ 5O2-> 4СО2 + ЗН2О
Неприятный запах ацетилена, получаемого из карбида, обусловлен примесями PH3 и AsH3, чистый ацетилен пахнет, как и все низшие углеводороды (бензин). Ацетилен и его смеси с воздухом крайне взрывчаты; ацетилен хранят и транспортируют в баллонах в виде ацетоновых растворов, пропитывающих пористые материалы.
НЕФТЬ И ЕЕ ПЕРЕРАБОТКА
Состав нефти. Главным природным источником предельных углеводородов является нефть. Состав нефтей различается в зависимости от месторождения, однако все нефти при простой перегонке обычно разделяются на следующие фракции: газовая фракция, бензин, реактивное топливо, керосин, дизельное топливо, парафин, нефтяной гудрон.
Газовая фракция (т. кип. до40◦C) содержит нормальные и разветвленные алканы до С,, в основном пропан и бутаны. Природный газ из газовых месторождений состоит в основном из метана и этана.
Бензин авиационный (т. кип. 40—180 °С) содержит углеводороды С6 — С10 В бензине обнаружено более 100 индивидуальных соединений, в число которых входят нормальные и разветвленные алканы, циклоалканы и алкилбензолы (арены).
Реактивное топливо (т. кип. 150—280°С).
Керосин тракторный (т, кип. 110—300 °С) содержит углеводороды С7—С14.
Дизельное топливо (т. кип. 200—330 °С), в состав которого входят углеводороды C13 — C18, в больших масштабах подвергается крекингу, превращаясь в алканы (и алкены) с меньшей молекулярной массой (см. ниже).
Смазочные масла (т. кип. 340—400°С) содержат углеводороды C18 — C25.
Парафин нефтяной (т. кип. 320—500 °С), в его состав входят углеводороды С26—С38, из которых выделяют вазелин. Остаток после перегонки обычно называют асфальтом или гудроном.
Помимо углеводородов самых различных классов в нефти содержатся кислородные, сернистые и азотсодержащие вещества; иногда их суммарное содержание доходит до нескольких процентов.
Хотя общепризнанно, что нефть является наиболее ценным природным источником химического сырья, до сих пор основное количество нефти и нефтепродуктов сгорает в двигателях внутреннего сгорания (бензин), дизелях и реактивных двигателях (керосин).
Моторное топливо. Октановое число. Бензины различного происхождения по-разному ведут себя в двигателях внутреннего сгорания.
Стремясь к максимальному повышению мощности двигателя при малых габаритах и массе, стараются увеличить степень сжатия горючей смеси в цилиндре. Однако в быстроходных четырехтактных двигателях, работающих с принудительным зажиганием, при этом иногда происходит преждевременное воспламенение смеси — детонация. Это снижает мощность мотора и ускоряет его износ. Это явление связано с составом жидкого топлива, так как углеводороды разного строения при использовании их в качестве моторного топлива ведут себя различно. Наихудшие показатели — у парафинов нормального строения.
За стандарт горючего вещества с большой способностью к детонации принят нормальный гептан. Чем больше разветвлена углеродная цепь парафинового углеводорода, тем лучше протекает сгорание его в цилиндре и тем большей степени сжатия горючей смеси можно достичь. В качестве стандарта моторного топлива принят 2, 2, 4-триметилпентан (который обычно называют изооктаном) с хорошими антидетонационными свойствами. Составляя в различных пропорциях смеси этого октана с я-гептапом, сравнивают их поведение в моторе с поведением испытуемого бензина. Если смесь, содержащая 70% изооктана, ведет себя так же, как исследуемый бензин, то говорят, что последний имеет октановое число 70 (октановое число изооктана принято за 100; октановое число н -гептана принято равным нулю).
Одним из путей повышения детонационной стойкости топлив для двигателей с зажиганием от искры является применение антидетонаторов.
Антидетонаторы — это вещества, которые добавляют к бензинам (не более 0,5%) для улучшения аптидетопацнонных свойств. Достаточно эффективным антидетонатором является тетраэтилсвинец (ТЭС) РЬ (C2H5)4
Однако бензин с ТЭС и продукты его сгорания очень токсичны. В настоящее время найдены новые антидетонаторы на основе марганец-органических соединений типа циклопентадиеиклпснтакарбонилмарганца С5Н5Мn (СО)5: они менее токсичны и обладают лучшими антидетонационными свойствами. Добавление этих антидетонаторов к хорошим сортам бензина позволяет получать топливо с октановым числом до 135.
Для ракетных и дизельных двигателей, наоборот, наиболее ценны топлива с нормальной цепью углеродных атомов, обладающие наиболее низкой температурой воспламенения. Эту характеристику принято
оценивать в цетановых числах. Цетановое число 100 имеет углеводород н-Сц,Нд4, а цетаповое число 0 — 1-метилнафталин.
Синтез углеводородовиз CO+H2.Пропуская над мелко раздробленнымникелем смесь окиси углерода (II) и водорода при 250° С, можно получитьметан:
Если эту реакцию проводить при давлении 100—200 атм и температуре до 400°С, получается смесь, состоящая главным образом из кислородсодержащих продуктов, среди которых преобладают спирты; смесь эта была названа счшполом .
При применении железо-кобальтовых катализаторов и температуре 200° С образуется смесь алканов — синтин.
nСО + (2n + 1) Н2 СnН2n +2 + H2О
Синтин и синтол являются продуктами многотоннажного органического синтеза и широко используются в качестве сырья для многих химических производств.
Клатраты. Синтин и бензиновые фракции нефти состоят из смесей углеводородовнормального строения и с разветвленными цепями. Недавно был найден эффективный метод разделения органических соединений с нормальными цепями и разветвленных, получивший в общем случае название метода клатратного разделения. Для разделения углеводородовбыла использована мочевина. Кристаллы мочевины построены таким образом, что внутри кристаллов имеются узкие шестигранные каналы. Диаметр этих каналов таков, что внутрь их может пройти и задержаться за счет адсорбционных сил только углеводород нормального строения. Поэтому при обработке смеси органических соединений мочевиной (или некоторыми другими соединениями) вещества с нормальной цепью углеродных атомов кристаллизуются вместе с ней в виде комплексов. Этот метод имеет, безусловно, очень большое будущее — когда будет найдено большее число эффективных клатратообразователей.
Мы приступаем к новому разделу - органической химии. Совершенно необязательно (и даже преступно по отношению к собственному времени!) знать наизусть, зубрить свойства органических веществ.
По мере изучения вы поймете, что свойства вещества определяются его строением, и научитесь легко предсказывать ход реакций ;)
- Атомы в молекуле соединены в определенной последовательности, в соответствии с их валентностью. Порядок связи атомов отражает химическое строение.
- Зная свойства веществ, можно установить их химическое строение, и наоборот, зная строение вещества можно сделать вывод о его свойствах.
- Атомы или группы атомов оказывают взаимное влияние друг на друга непосредственно или через другие атомы
- Свойства вещества зависят от количественного и качественного состава, а также от химического строения молекулы

Алканы (парафины) - насыщенные углеводороды, имеющие линейное или разветвленное строение, содержащие только простые связи. Относятся к алифатическим углеводородам, так как не содержат ароматических связей.
Алканы являются насыщенными соединениями - содержат максимально возможное число атомов водорода. Общая формула их гомологического ряда - CnH2n+2.
Номенклатура алканов
Номенклатура (от лат. nomen - имя + calare - созывать) - совокупность названий индивидуальных химических веществ, а также правила составления этих названий. Названия у алканов формируются путем добавления суффикса "ан": метан, этан, пропан, бутан и т.д.
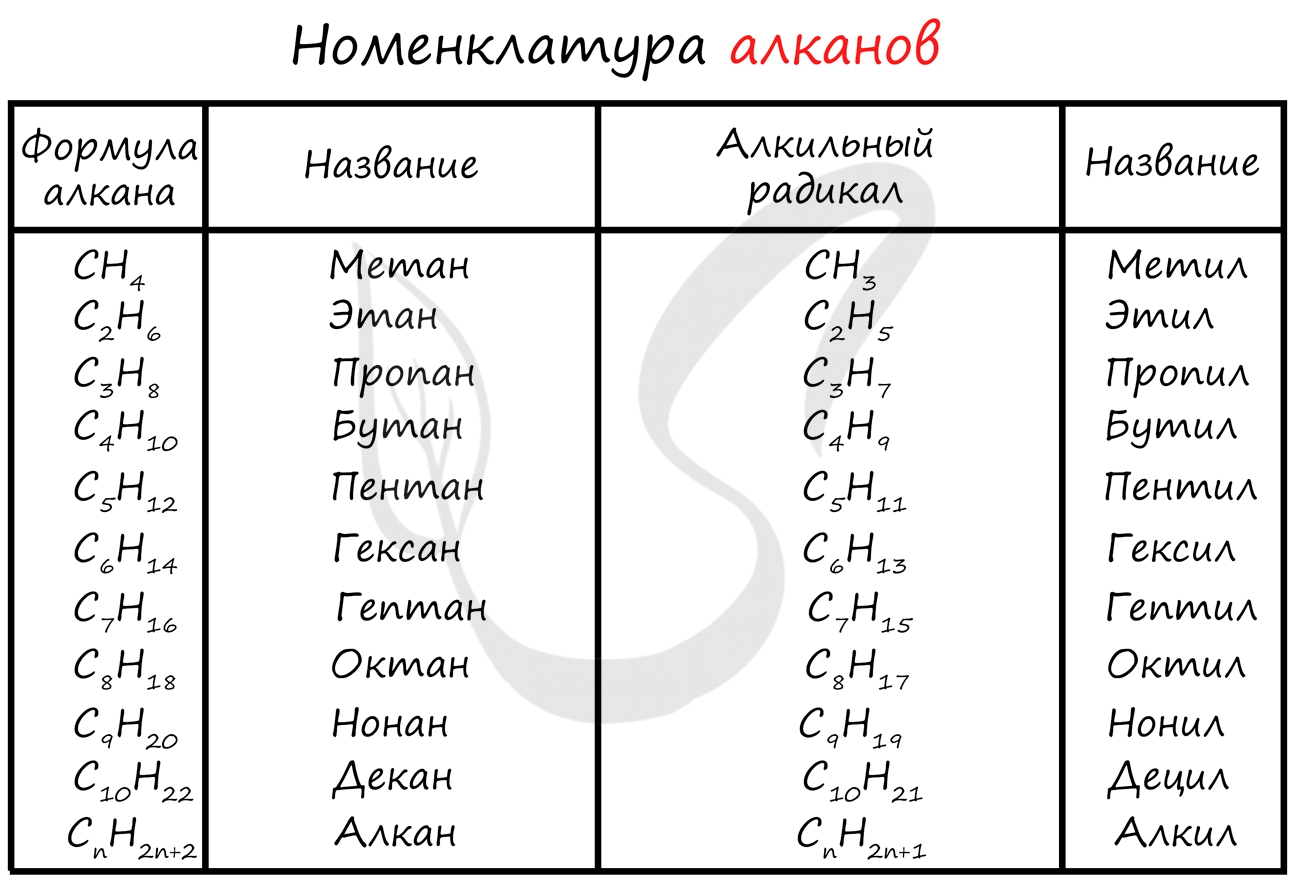
Гомологами называют вещества, сходные по строению и свойствам, отличающиеся на одну или более групп CH2
Перечисленные выше алканы, являются по отношению друг к другу гомологами, то есть составляют один гомологический ряд (греч. homólogos - соответственный).
Названия алканов формируются по нескольким правилам. Если вы знаете их, можете пропустить этот пункт, однако я должен познакомить читателя с ними. Итак, алгоритм составления названий следующий:
- В структурной формуле вещества необходимо выбрать самую длинную (пусть и изогнутую на рисунке!) цепь атомов углерода
- Атомы выбранной цепи нумеруют, начиная с того конца, к которому ближе разветвление (радикал)
- В начале название перечисляют радикалы и другие заместители с указанием номеров атомов углерода, с которыми они связаны. Если в молекуле имеется несколько одинаковых радикалов, то цифрой указывают нахождение каждого из них в главной цепи и перед их названием соответственно ставят частицы ди-, три-, тетра- и т.д.
- Основой названия служит наименование предельного углеводорода с тем же количеством атомов углерода, что и в главной цепи
Внимательно изучите составленные для различных веществ названия ниже.
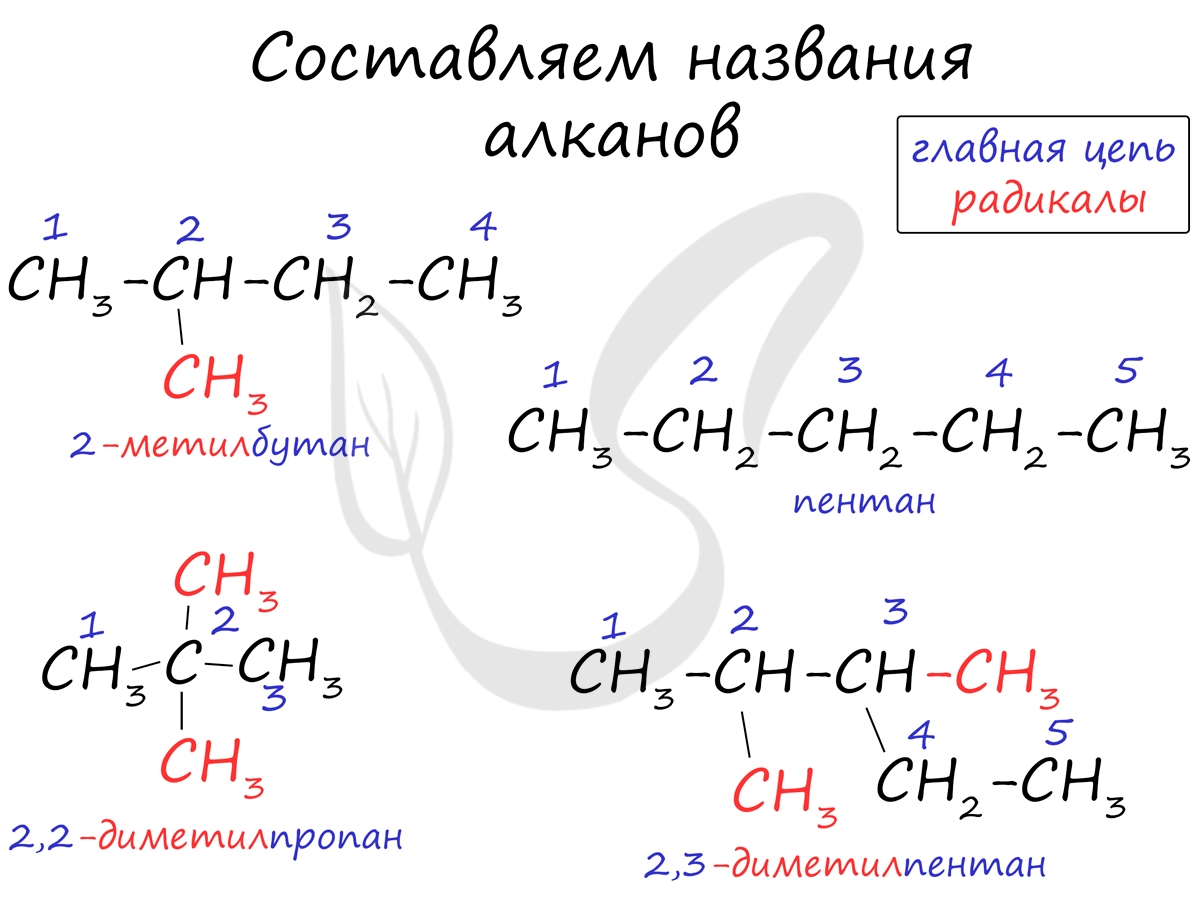
В углеводородной цепочке различают несколько типов атомов углерода, в зависимости от того, с каким числом других атомов углерода соединен данный атом. Различают первичные, вторичные, третичные и четвертичные атомы углерода.

Изомерами (греч. isomeros - составленный из равных частей) называют вещества, имеющие одну молекулярную формулу, но отличающиеся по строению (структурная изомерия) или расположению атомов в пространстве (пространственная изомерия).
Изомерия бывает структурной (межклассовая, углеродного скелета, положения функциональной группы или связи) и пространственной (геометрической, оптической). По мере изучения классов органических веществ вы узнаете о всех этих видах.
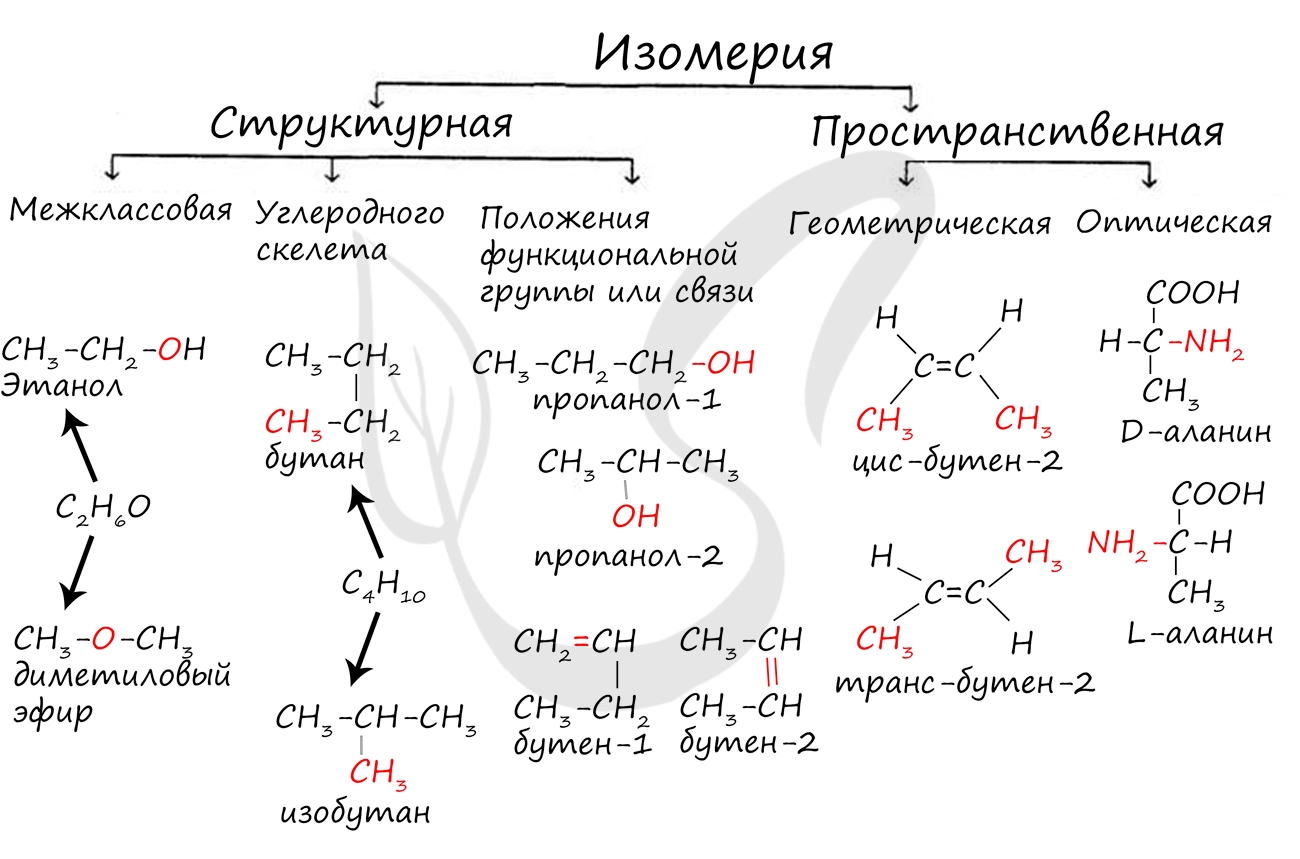
В молекулах алканов отсутствуют функциональные группы, кратные связи. Для алканов возможна изомерия только углеродного скелета. Так у пентана C5H12 существует 3 структурных изомера.

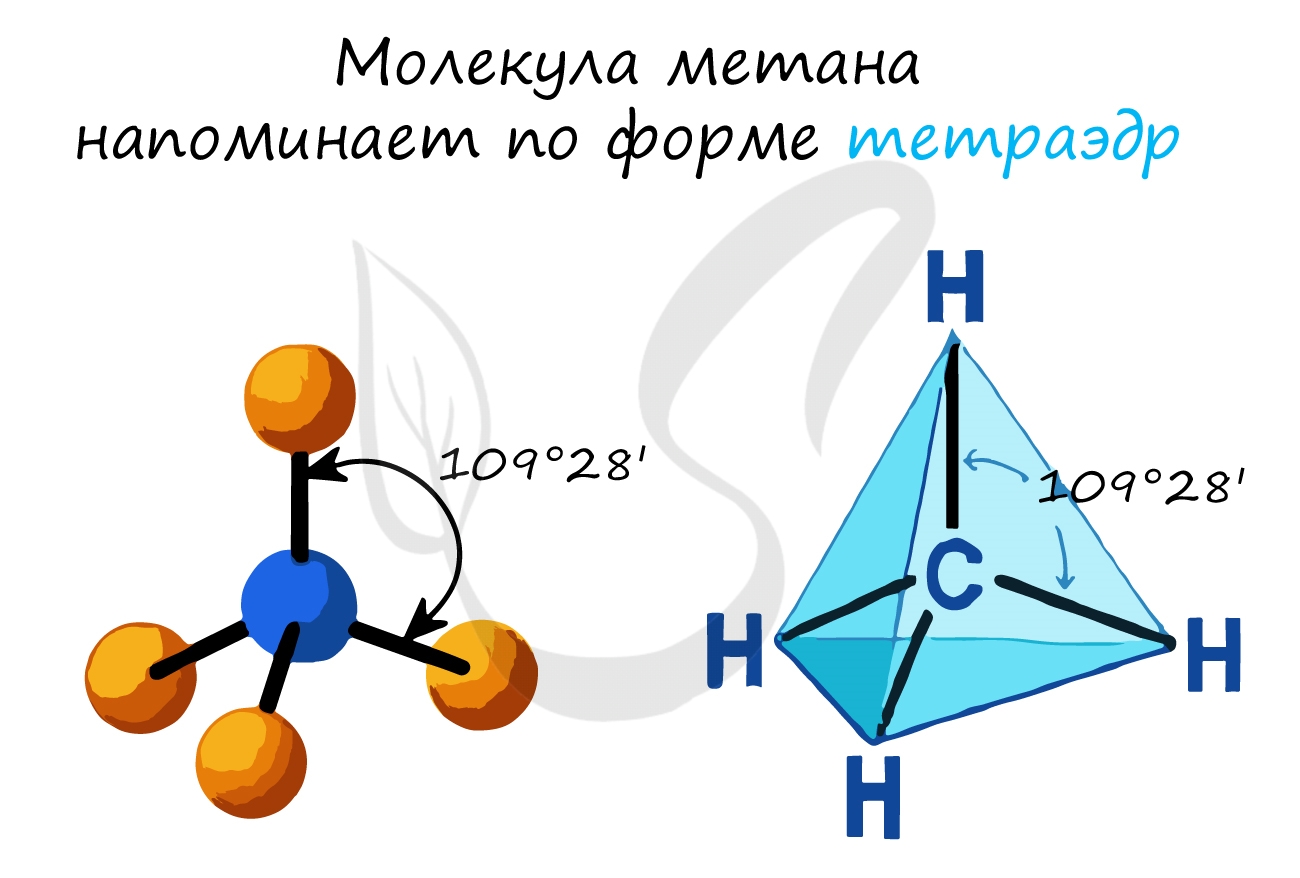
- В молекулах алканов присутствуют одиночные сигма-связи (σ-связи), длина которых составляет 0,154 нм
- Тип гибридизации атомов углерода - sp 3
- Валентный угол (между химическими связями) составляет 109°28'
Природный газ и нефть
Алканы входят в состав природного газа: метан 80-97%, этан 0.5-4%, пропан 0.2-1.5% , бутан 0.1-1%, пентан 0-1%. Состав нефти нельзя выразить одной формулой, он непостоянен и зависит от месторождения.
В состав нефти входят алканы с длинными углеродными цепочками, например: C8H18, C12H26. Путем крекинга из нефти получают алканы.

Получение алканов
В ходе крекинга нефти получается один алкан и один алкен.
Данный синтез заключается в сплавлении соли карбоновой кислоты с щелочью, в результате образуется алкан.

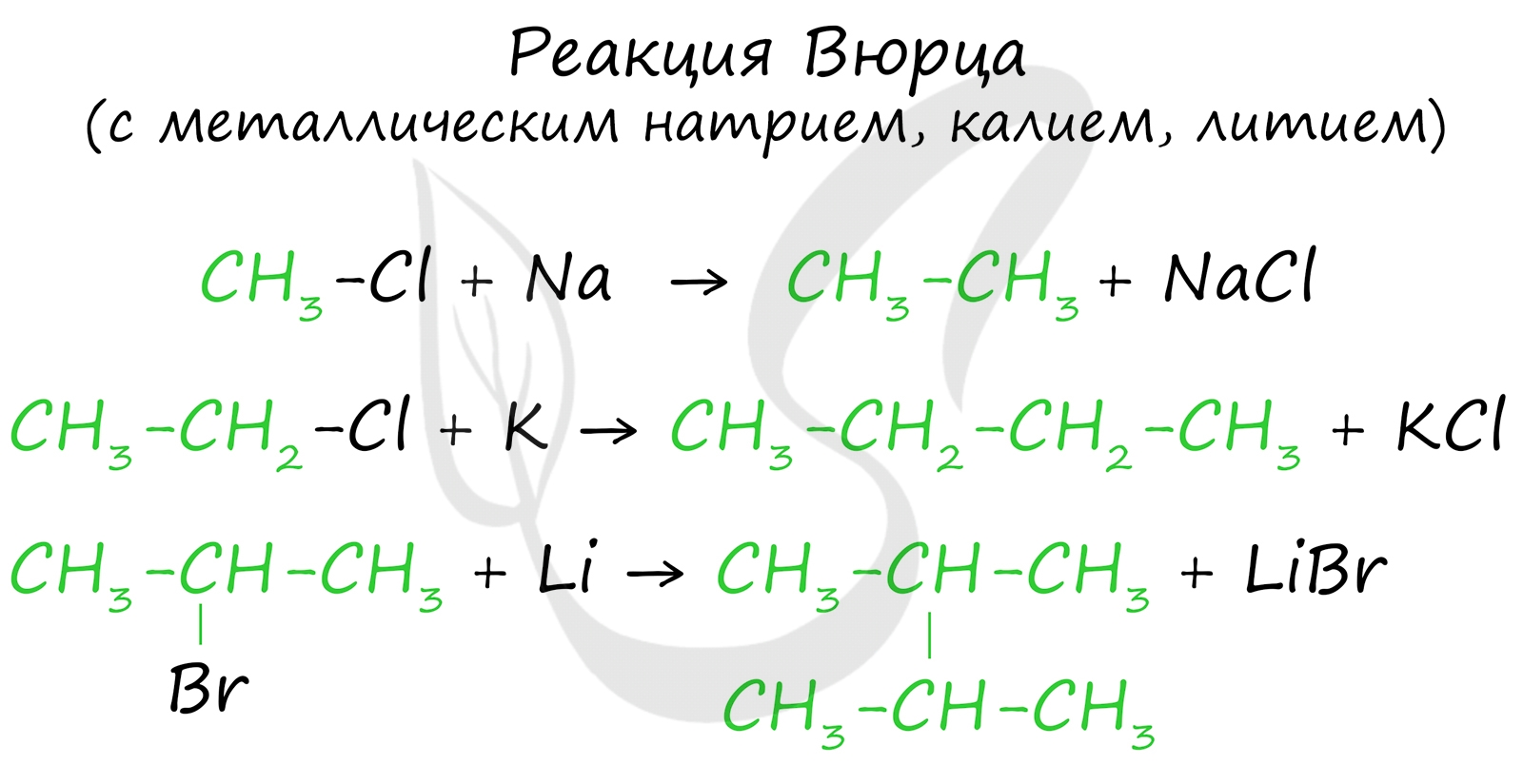
Эта реакция заключается во взаимодействии галогеналкана с металлическим натрием, калием или литием. В результате происходит удвоение углеводородного радикала, рост цепи осуществляется зеркально: в том месте, где находился атом галогена.
В ходе синтеза Гриньяра с помощью реактива Гриньяра (алкилмагнийгалогенида) получают различные органические соединения, в том числе несимметричные (в отличие от реакции Вюрца).
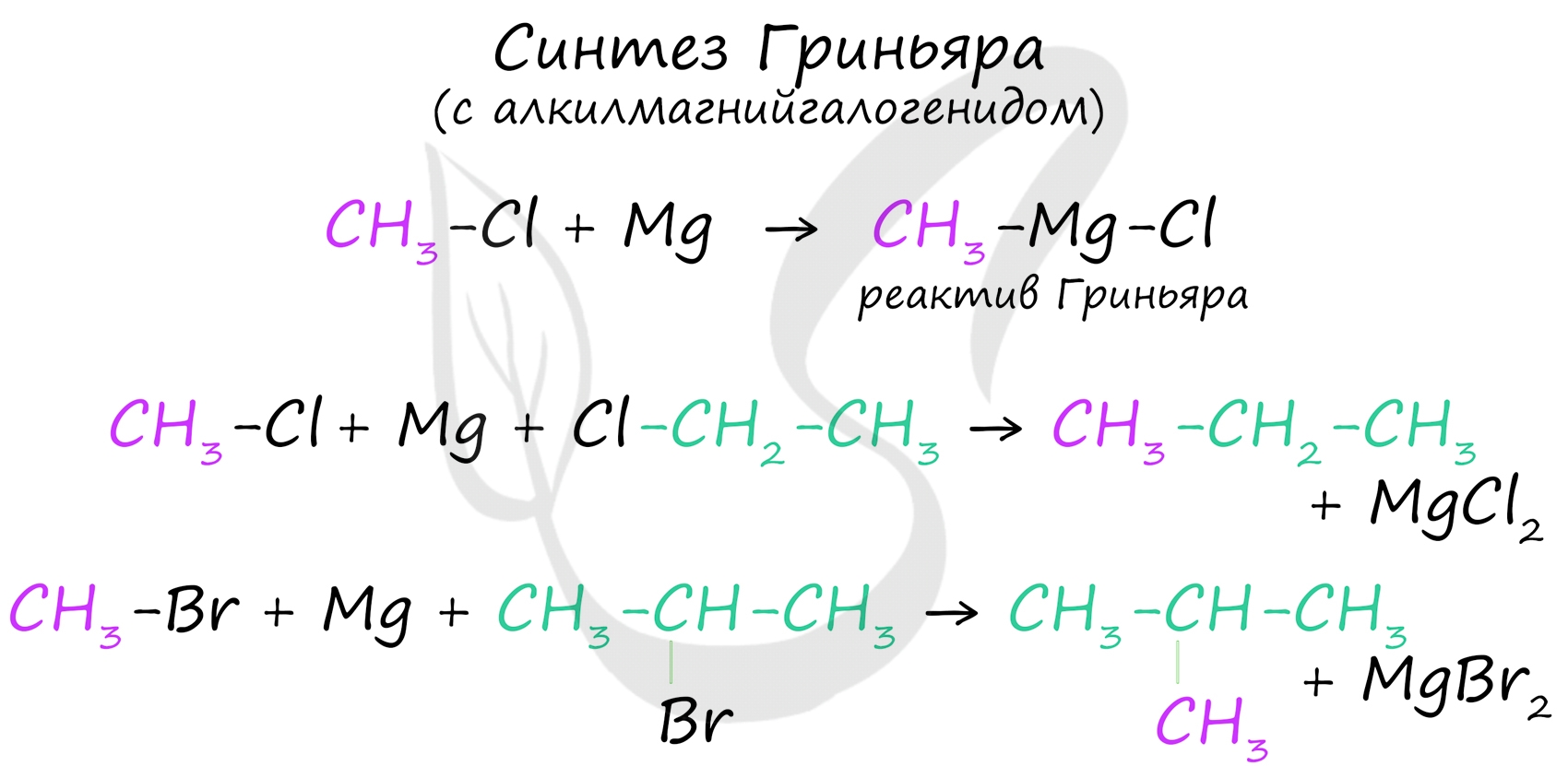
На схеме выше мы сначала получили реактив Гриньяра, а потом использовали его для синтеза. Однако можно записать получение реактива Гриньяра и сам синтез в одну реакцию, как показано на примерах ниже.

В результате электролиза солей карбоновых кислот может происходить образование алканов.
В результате разложения карбида алюминия образуется метан и гидроксид алюминия.
Химические свойства алканов
Атом галогена замещает атом водорода в молекуле алкана. Запомните, что легче всего идет замещение у третичного атома углерода, чуть труднее - у вторичного и значительно труднее - у первичного.

Реакции с хлором на свету происходят по свободнорадикальному механизму. На свету молекула хлора распадается на свободные радикалы, которые и осуществляют атаку на молекулу углеводорода.

Реакция Коновалова заключается в нитровании алифатических (а также ароматических) соединений разбавленной азотной кислотой. Реакция идет при повышенном давлении, по свободнорадикальному механизму.
Для удобства и более глубокого понимания, азотную кислоту - HNO3 - можно представить как HO-NO2.

Все органические вещества, в их числе алканы, сгорают с образованием углекислого газа и воды.
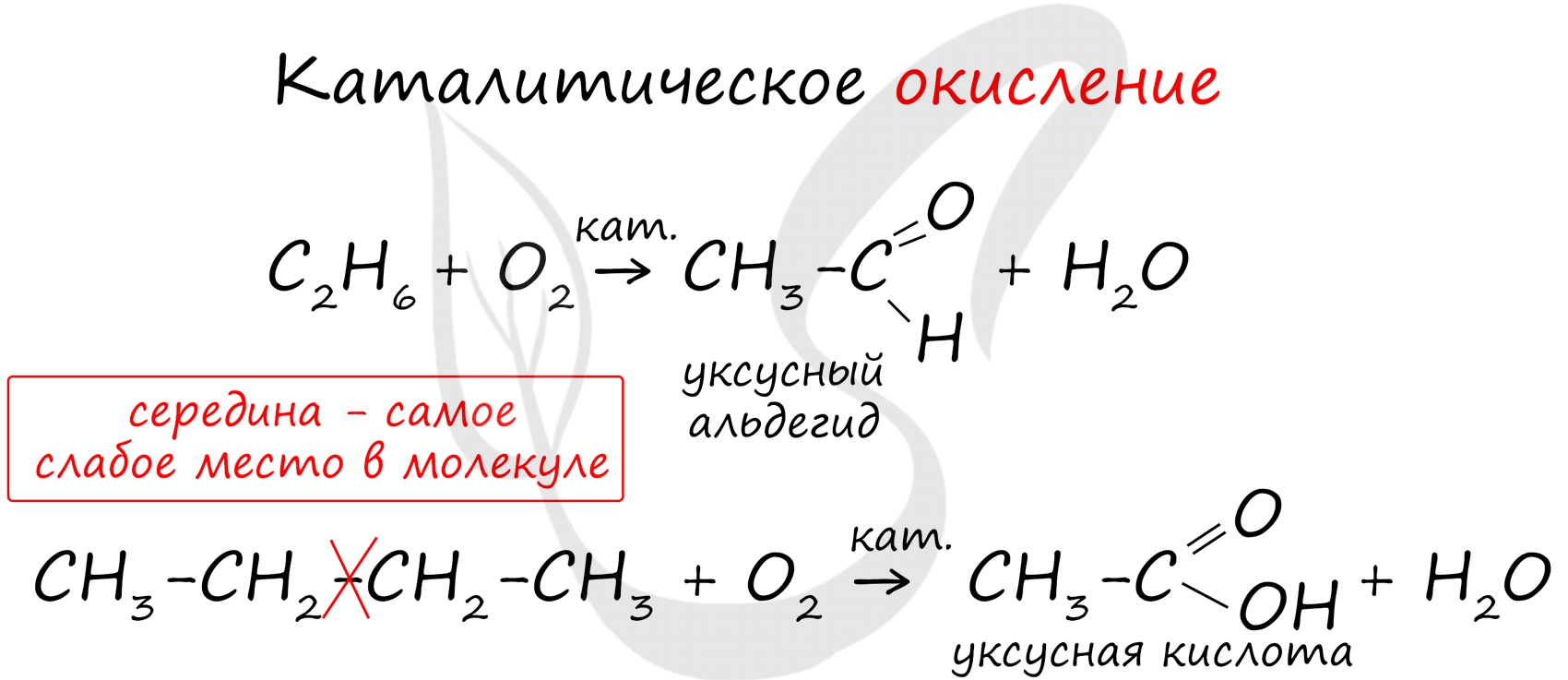
В ходе каталитического, управляемого окисления, возможна остановка на стадии спирта, альдегида, кислоты.
Пиролиз (греч. πῦρ - огонь + λύσις - разложение) - термическое разложение неорганических и органических соединений. Принципиальное отличие пиролиза от горения - в отсутствии кислорода.
В реакциях, по итогам которых образуются изомеры, используется характерный катализатор AlCl3.

Вам уже известно, что в результате крекинга образуется один алкан и один алкен. Это не только способ получения алканов, но и их химическое свойство.
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Читайте также:

