Сообщение на тему акролеин
Обновлено: 03.07.2024
Акролеин (лат. acris — острый, едкий + oleum — масло) (пропеналь) — H2C=CH-CHO, альдегид акриловой кислоты, простейший ненасыщенный альдегид. Бесцветная легколетучая слезоточивая жидкость с резким запахом, сильный лакриматор.
Содержание
Реакционная способность
Акролеин, будучи непредельным альдегидом, проявляет реакционную способность, свойственную как олефинам, так и альдегидам. Так, акролеин образует ацетали:

его альдегидная группа легко окисляется до карбоксильной:
![\mathsf<H_2C\text</p>
<p>CH\textCHO \xrightarrow[] H_2C\textCH\textCOOH>](https://dic.academic.ru/dic.nsf/ruwiki/628065459c120a13610d54fae7f403a1.jpg)
и восстанавливается до гидроксильной:
![\mathsf<H_2C\text</p>
<p>C\textCHO \xrightarrow[] H_2C\textCH\textCH_2OH>](https://dic.academic.ru/dic.nsf/ruwiki/ba9702336da0789f1dd8d26da1694458.jpg)
Карбонильная группа акролеина находится в сопряжении с двойной связью, что обуславливает его высокую реакционную способность по отношению к нуклеофилам, при этом присоединение идёт по β-атому углерода:

Галогены присоединяются к акролеину по двойной связи с образованием дигалогенпроизводного, которое далее отщепляет галогеноводород с образованием α-галогенакролеина:


Благодаря наличию электронакцепторной альдегидной группы, сопряженной с двойной связью, акролеин является диенофилом и реагирует с диенами с образованием продуктов циклоприсоединения (реакция Дильса-Альдера):

Синтез
В лаборатории акролеин получается дегидратацией глицерина в присутствии гидросульфата калия.
В промышленности акролеин получают каталитическим окислением пропилена над оксидными висмут-молибденовыми катализаторами или оксидом меди. Ранее в промышленности был распространён процесс парофазной кротоновой конденсации ацетальдегида с формальдегидом (устаревший метод):

Токсичность
Относится к I классу опасности (чрезвычайно опасные вещества).
Акролеин является одним из продуктов термического разложения глицерина и жиров-глицеридов, чем объясняется раздражающие слизистые оболочки свойства дыма горелых жиров.
Применение
Применяют для синтеза акрилонитрила, глицерина, пиридина, β-пиколина, аминокислот (метионина, белка), этилвиниловых эфиров, глутарового альдегида, полиакролеина. Также используется в производстве лекарственных препаратов. Во время Первой мировой войны использовался в качестве химического оружия.
Ссылки
Примечания
- Найти и оформить в виде сносок ссылки на авторитетные источники, подтверждающие написанное.
- Чрезвычайно опасные вещества
- Альдегиды
- Производные этилена
- Продукция основного органического синтеза
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое "Акролеин" в других словарях:
АКРОЛЕИН — (ново лат., от лат. acer острый, и oleum масло). Летучее, едкое для глаз и носа масло, образующееся при сухой перегонке железа и глицерина и при сильном нагревании многих жиров. Словарь иностранных слов, вошедших в состав русского языка. Чудинов… … Словарь иностранных слов русского языка
АКРОЛЕИН — АКРОЛЕИН, СНа : СН.СН : О, простейший ненасыщенный альдегид. Бесцветная жидкость с резким запахом. Кипит при 52,4°. Пары акролеина сильно раздражают слизистые оболочки носа и горла, разрушают ткани глаза, а при продолжительном действии… … Большая медицинская энциклопедия
АКРОЛЕИН — CH2=CHCHO, бесцветная жидкость с резким запахом, tкип 52,7 .C. Акролеин сырье для получения многих продуктов органического синтеза. Сильный лакриматор … Большой Энциклопедический словарь
акролеин — сущ., кол во синонимов: 2 • альдегид (10) • масло (74) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Акролеин — 1 С2Н,СНО Альдегид олефинового ряда, относящийся к J классу опасности 11 Источник: ГОСТ Р 51206 98: Автотранспортные средства. Содержание вредных веществ в воздухе салона и к … Словарь-справочник терминов нормативно-технической документации
Акролеин — (акрол) акриловый альдегид С3Н4О (СН2=СН СОН), представляет собою простейший непредельный альдегид, отвечающий простейшему непредельному первичному спирту, аллильному, так же как обыкновенный альдегид этильному. Он образуется при окислении… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
акролеин — СН2 = HCHCHO, бесцветная жидкость с резким запахом, tкип 52,7ºC. Акролеин сырьё для получения многих продуктов органического синтеза. Сильный лакриматор. * * * АКРОЛЕИН АКРОЛЕИН, CH2=CHCHO, бесцветная жидкость с резким запахом, tкип 52,7 °C.… … Энциклопедический словарь
акролеин — akrilaldehidas statusas T sritis chemija formulė CH₂=CHCHO atitikmenys: angl. acrylaldehyde; acrolein rus. акриловый альдегид; акролеин ryšiai: sinonimas – akroleinas sinonimas – propenalis … Chemijos terminų aiškinamasis žodynas
Акролеин — CH2 = CH CHO, простейший ненасыщенный альдегид. Бесцветная легколетучая жидкость; tkип 52,5°C. Его пары сильно раздражают слизистые оболочки глаз и дыхательных путей. Ядовит; предельно допустимая концентрация в воздухе 0,7 мг/м3. … Большая советская энциклопедия
Акролеин – это желтая до бесцветная жидкость с резким запахом. Огнеопасное, пары тяжелее воздуха, может стелиться по земле. Является промежуточным продуктом в полимерном производстве, применяется как дубильное вещество.

Аварийная карточка (АХОВ)
АКРОЛЕИН, КЛАСС ТОКСИЧЕСКОЙ ОПАСНОСТИ – 2
ICSC: 0090
Классификация ООН
ОСТРАЯ ОПАСНОСТЬ / СИМПТОМЫ
ПРЕДУПРЕЖДЕНИЕ
ИЗБЕГАТЬ ЛЮБОГО КОНТАКТА!
ТРАНСПОРТИРОВКА/ ХРАНЕНИЕ
ЛИКВИДАЦИЯ
НЕЙТРАЛИЗАЦИЯ
В случае пожара: сохранять бочки и пр. охлажденными, обливая их водой. Тушить большим количеством воды, пеной, спиртоустойчивой пеной, порошком, двуокисью углерода.
Провести эвакуацию из опасной зоны! Проконсультироваться со специалистом! Собрать подтекающую жидкость в закрытые контейнеры. Засыпать оставшуюся жидкость песком или инертным абсорбентом, собрать и удалить его в безопасное место. НЕ допускайте попадания этого химического вещества в окружающую среду.
Нейтрализуют акролеин 30%-ным водным раствором гидроксиламина (например, 300 л. гидроксиламина и 900 л. воды) с нормой расхода: 2 тонны раствора на 1 тонну акролеина.
При пожаре тушить инертными газами, распыленной водой, воздушно – механической и химической пеной. Для распыления воды или растворов применяют поливомоечные и пожарные машины, авторазливочные станции (АЦ, ПМ-130, АРС-14, АРС-15), мотопомпы (МП-800), а также имеющиеся на химически опасных объектах гидранты и спецсистемы.
Место разлива промывают большим количеством воды, изолируют песком, воздушно-механической пеной, обваловывают и не допускают попадания веществ в поверхностные воды. Для утилизации загрязненного грунта на месте разлива срезают поверхностный слой грунта на глубину загрязнения, собирают и вывозят на утилизацию с помощью землеройно-транспортных машин (бульдозеров, скреперов, автогрейдеров, самосвалов). Места срезов засыпают свежим слоем грунта, промывают водой в контрольных целях.
ПЕРВАЯ ПОМОЩЬ
В зараженной зоне: обильное промывание глаз водой, надевание противогаза, обильное промывание пораженных участков кожи водой, срочный выход (вывод) пострадавших из зоны заражения.
После эвакуации из зараженной зоны: покой, тепло, теплое питье, обильное промывание слизистых водой или 2%-ным раствором борной кислоты, при нарушении дыхания ингаляция кислорода, искусственная вентиляция легких. Удалить загрязненную одежду. Полусидячее положение. Прополоскать рот. НЕ вызывать рвоту.
ФИЗИЧЕСКОЕ СОСТОЯНИЕ, ВНЕШНИЙ ВИД:
ЖЕЛТАЯ ДО БЕСЦВЕТНОЙ ЖИДКОСТЬ С РЕЗКИМ ЗАПАХОМ
ФИЗИЧЕСКАЯ ОПАСНОСТЬ:
Пар тяжелее воздуха и может стелиться по земле; возможно возгорание на расстоянии.
ХИМИЧЕСКАЯ ОПАСНОСТЬ:
Вещество может образовать взрывоопасные перекиси. Вещество может полимеризоваться с опасностью пожара и взрыва. При нагревании образуются токсичные пары. Реагирует со щелочами, кислотами, аминами, диоксидом серы, тиомочевиной, солями металлов и окислителями с опасностью пожара и взрыва.
ПУТИ ПОСТУПЛЕНИЯ:
Вещество может всасываться в организм при вдыхании паров и через рот.
РИСК ПРИ ВДЫХАНИИ:
Опасное загрязнение воздуха будет достигаться очень быстро при испарении этого вещества при 20°C.
ВЛИЯНИЕ КРАТКОВРЕМЕННОГО ВОЗДЕЙСТВИЯ:
Разъедающее действие. Слезоточивое действие. Вещество оказывает разъедающее действие на глаза, кожу и дыхательные пути. Вдыхание этого вещества может вызвать отек легких (см. Примечания). Воздействие в большой дозе может вызвать смерть. Эффекты могут быть отсроченными. Показано медицинское наблюдение.
НАЛИЧИЕ АКРОЛЕИНА ОПРЕДЕЛЯЮТ:
ФИЗИЧЕСКИЕ СВОЙСТВА
ПРЕДЕЛЬНО ДОПУСТИМАЯ КОНЦЕНТРАЦИЯ (ПДК)
Температура кипения: 53°C
Температура плавления: -88°C
Относительная плотность (вода = 1): 0.8
Растворимость в воде, г/100 мл при 20°C: 20
Давление паров, кПа при 20°C: 29
Относительная плотность пара (воздух = 1): 1.9
Относительная плотность смеси пар/воздух при 20°C (воздух = 1): 1.2
Температура вспышки: -26°C
Температура самовоспламенения: 234°C
Предельно допустимая концентрация (ПДК) акролеина составляет: в воздухе населенных пунктов 0,03 мг/м3. В воздухе рабочей зоны производственных помещений 0,2 мг/м3.
При малых и средних концентрациях наблюдается раздражение верхних дыхательных путей и глаз, кашель, насморк, першение в горле, головокружение, слабость, рвота. При высоких концентрациях – онемение конечностей, тошнота, потеря сознания. Средняя смертельная концентрация 350 мг/м3 в течение 10 мин, 20 мг/м3 в течение 4 часов.
ПО КНОПКЕ СКАЧАТЬ
АКРОЛЕИН
АКРОЛЕИН (пропеналь, акриловый альдегид) СН2=СНСНО, бесцв. жидкость с удушливым запахом; т. пл. от -86,5 до -88°С, т. кип. 52,7°С; d4 20 0,838, nD 20 1,4013; 0,329 мПа (20°С); 27,6 мН/м (20°С); С 0 p 2,14 кДж/моль;H 0 обр -107 кДж/моль,Н 0 сгор -1630 кДж/моль; давление пара (МПа): 0,145 (5°С), 0,905 (50°С);9,99*10 -30 Кл-м. Раств. во многих орг. р-рителях, воде (21,4% по массе). Образует азеотроп с водой и метанолом с т. кип. соотв. 52,36°С (97,4% акролеина) и 51,5°С (84,5% акролеина), а также тройной азеотроп с т. кип. 51,2°С (85,7% акролеина, 13,4% СН3ОН).
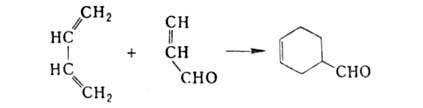
Акролеин вступает во все р-ции, характерные для альдегидов и непредельных соединений. Проявляет св-ва диенофила в диеновом синтезе:
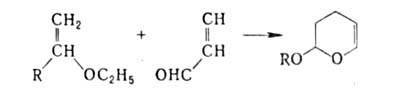
С алкил- и арилвиниловыми эфирами реагирует как диен:
Акролеин легко взаимод. с водой, спиртами и орг. к-тами: СН2=СНСНО + ROH -> ROCH2CH2CHO. Нуклеоф. присоединение протекает поуглеродному атому, напр.:
Взаимод. акролеина с галогеноводородами приводит кгалогенпропионовому альдегиду, с галогенами-кгалогенакролеину.
В отсутствие ингибиторов акролеин способен при комнатной т-ре к взрывной полимеризации с образованием неплавкого и нерастворимого диакрила. Ингибиторы полимеризации -полифенолы. При нагр. до 150 С С акролеин димеризуется с образованием 2-формил-2,3-дигидропирана. Акролеин сополимеризуется с разл. мономерами, напр. с акриламидом, акрилонитрилом, винилацетатом, 2-винилпиридином, винилбутиловым эфиром. Полимеризуется в присут. как радикальных, так и ионных катализаторов с образованием полимеров разл. структуры.
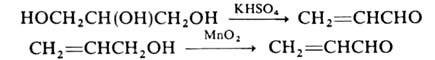
Синтезируют акролеин дегидратацией глицерина или окислением аллилового спирта:
В пром-сти акролеин получают: конденсацией формальдегида с ацетальдегидом при 300-320 °С в газовой фазе в присут. SiO2, пропитанного р-ром Na2SiO3; окислением пропилена кислородом воздуха в присут. водяного пара на висмут-молибденовых кат. (соотношение пропилен : воздух : водяной пар составляет 1:10:2; конверсия пропилена-96%; побочные продукты-акриловая к-та и ацетальдегид).
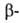
Акролеин применяют для синтеза акрилонитрила, глицерина, пиридина,пиколина, аминокислот (метионина, протеина), этилвиниловых эфиров, глутарового альдегида, полиакролеина. Полиакролеин и его Na-соли-эмульгаторы, структурирующие агенты почв; лактонные производные полиакролеина улучшают св-ва бумаги и текстильных изделий.
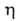
бесцветная жидкость с удушливым запахом; т. пл. от −86,5 до −88 °C, т. кип. 52,7 °C; d4 20 0,838, nD 20 1,4013; 0,329 мПа (20 °C); σ 27,6 мН/м (20 °C); С 0 p 2,14 кДж/моль; ΔH 0 обр −107 кДж/моль, ΔH 0 сгор −1630 кДж/моль; давление пара (МПа): 0,145 (5 °C), 0,905 (50 °C); μ 9,99∙10 −30 Кл∙м. Раств. во многих органических растворителях, воде (21,4% по массе). Образует азеотроп с водой и метанолом с т. кип. соотв. 52,36 °C (97,4% А.) и 51,5 °C (84,5% А.), а также тройной азеотроп с т. кип. 51,2 °C (85,7% А., 13,4% CH3OH).
А. вступает во все реакции, характерные для альдегидов и непредельных соединений. Проявляет свойства диенофила в диеновом синтезе:
С алкил- и арилвиниловыми эфирами реагирует как диен:
А. легко взаимод. с водой, спиртами и орг. кислотами: CH2=CHCHO + ROH → ROCH2CH2CHO. Нуклеоф. присоединение протекает по β-углеродному атому, напр.:
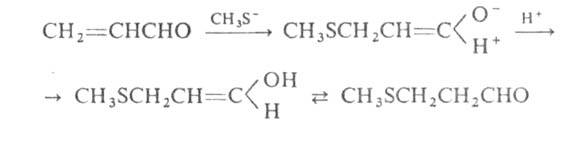
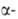
Взаимод. А. с галогеноводородами приводит к β-галогенпропионовому альдегиду, с галогенами-кгалогенакролеину.
В отсутствие ингибиторов А. способен при комнатной температуре к взрывной полимеризации с образованием неплавкого и нерастворимого диакрила. Ингибиторы полимеризации — полифенолы. При нагр. до 150 С С А. димеризуется с образованием 2-формил-2,3-дигидропирана. А. сополимеризуется с разл. мономерами, напр. с акриламидом, акрилонитрилом, винилацетатом, 2-винилпиридином, винилбутиловым эфиром. Полимеризуется в присутствии как радикальных, так и ионных катализаторов с образованием полимеров разл. структуры.
Синтезируют А. дегидратацией глицерина или окислением аллилового спирта:
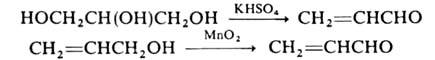
В промышленности А. получают: конденсацией формальдегида с ацетальдегидом при 300–320 °C в газовой фазе в присутствии SiO2, пропитанного раствором Na2SiO3; окислением пропилена кислородом воздуха в присутствии водяного пара на висмут-молибденовых кат. (соотношение пропилен : воздух : водяной пар составляет 1:10:2; конверсия пропилена-96%; побочные продукты-акриловая кислота и ацетальдегид).
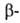
А. применяют для синтеза акрилонитрила, глицерина, пиридина, пиколина, аминокислот (метионина, протеина), этилвиниловых эфиров, глутарового альдегида, полиакролеина. Полиакролеин и его Na-соли-эмульгаторы, структурирующие агенты почв; лактонные производные полиакролеина улучшают свойства бумаги и текстильных изделий.
Сильно раздражает слизистые оболочки глаз и дыхат. путей; обладает токсич. действием; ПДК в воздухе 0,7мг/м 3 . Т. всп. А. 29 °C; КПВ 2,8–31% по объему.
Лит.: Энциклопедия полимеров, т. 1, М., 1972, с. 50–54; Паушкин Я. М., Технология нефтехимического синтеза, ч. 1, М., 1973; Ullmanns. Enzyclopadie. 4 Aufl, Bd 3, Munch.-В., 1974, S. 72.
Читайте также:

