Органические кислоты в природе и на производстве сообщение
Обновлено: 30.06.2024
Органические кислоты – вкусовые вещества, содержащиеся почти во всех пищевых продуктах в свободном состоянии или в виде солей (яблочная, лимонная, винная, уксусная, муравьиная, молочная, щавелевая, бензойная и др.).
Кислоты придают продуктам определенный вкус, улучшают их сохраняемость, способствуют лучшему усвоению и перевариванию пищи.
Органические кислоты обладают определенной энергетической ценностью: 1 г кислоты дает 3 ккал энергии.
Органические кислоты могут быть природной составной частью сырьевых продуктов, они могут образовываться в процессе производства продуктов переработки, принимая участие в формировании его вкуса, кислоты можно добавлять в процессе приготовления пищи для улучшения вкуса, органические кислоты используют при консервировании. Летучие кислоты участвуют в образовании запаха продуктов.
В процессе хранения в некоторых пищевых продуктах наблюдается увеличение кислотности (в муке, жирах), в связи с увеличением количества свободных жирных кислот. Повышение кислотности свидетельствует о том, что продукты недостаточно свежие и доброкачественные.
В стандартах на некоторые виды пищевых продуктов установлены нормы содержания кислот. Кислотность пищевых продуктов определяют титрованием вытяжек или навесок продукта растворами щелочей. Результаты титрования выражают (в зависимости от вида продукта) в градусах или процентах в пересчете на преобладающую кислоту.
Общее количество кислот недостаточно характеризует вкус продуктов. Кислый вкус зависит в большей мере от степени диссоциации кислот. Чем выше концентрация ионов водорода, тем сильнее кислый вкус. Концентрация ионов водорода выражают показателем pH. Ощущение кислого вкуса увеличивается с понижением значения pH.
Органические кислоты оказывают благоприятное влияние на процесс пищеварения – они снижают pH среды, способствуя созданию определенного состава микрофлоры, тормозят процессы гниения в желудочно-кишечном тракте.
При рекомендации продуктов для составления рациона необходимо учитывать способность щавелевой кислоты интенсивно связывать кальций, фитиновой кислоты – кальций, железо, цинк и другие металлы. Лимонная кислота, наоборот, способствует усвоению организмом кальция.
Муравьиная кислота обнаружена в небольших количествах в пчелином меде, яблоках, малине, черешне. Она обладает асептическим действием.
Уксусная кислота содержится в небольших количествах в плодах, пиве, квашеных и соленых овощах и плодах. Слабый раствор уксусной кислоты, называемый уксусом, применяют в качестве приправ, а также как консервант при мариновании. Содержание уксусной кислоты в маринадах нормируется. Повышенное содержание уксусной кислоты в соках, пиве, вине свидетельствует о снижении их качества.
Яблочная кислота распространена в растениях, особенно в плодах, отсутствует в цитрусовых и клюкве. Используется при производстве безалкогольных напитков и кондитерских изделий.
Винная кислота в основном содержится в винограде. Используется в кондитерской промышленности и в производстве безалкогольных напитков.
Молочная кислота накапливается во многих продуктах (квашеные, соленые и моченые плоды и овощи, кисломолочные продукты и др.) при молочнокислом брожении. Обладает бактерицидным действием, применяется для подкисления безалкогольных напитков и кондитерских изделий.
Щавелевая кислота встречается в щавеле, ревене, шпинате и других растениях. В значительных количествах вредна.
Лимонная кислота широко распространена в растениях, особенно в плодах. В цитрусовых содержится только лимонная кислота. Широко применяется в кондитерской промышленности, производстве безалкогольных напитков, ликероводочных изделий, в хлебопечении.
Бензойная кислота встречается в бруснике и клюкве. Обладает антисептическими свойствами, применяется в производстве отдельных видов консервированных продуктов.
Сорбиновая кислота обнаружена в плодах рябины. Применяется в качестве консерванта.

Органические кислоты – это продукты распада веществ, образующиеся в процессе реакций обмена. В состав молекулы входит карбоксильная группа.
Эти соединения выступают промежуточными элементами и основными компонентами метаболического преобразования энергии, основанного на производстве аденозинтрифосфата, цикле Кребса.
Концентрация органических кислот в организме человека отражает уровень функционирования митохондрий, окисления жирных кислот и обмена углеводов. Помимо этого, соединения способствуют восстановлению кислотно-щелочного баланса крови. Дефекты метаболизма митохондрий вызывают отклонения в обменных реакциях, развитие нервно-мышечных патологий и изменение концентрации глюкозы. Более того, они могут повлечь гибель клетки, что связано с процессами старения и появлением бокового амиотрофического склероза, болезнями Паркинсона, Альцгеймера.
Классификация
Органические кислоты человеческий организм получает не только из продуктов питания в процессе переваривания пищи, но и вырабатывает самостоятельно. Такие соединения растворимы в спирте, воде, выполняют обеззараживающую функцию, улучшая самочувствие, восстанавливают здоровье.
Роль органических кислот
Главная функция карбоновых соединений – поддержание кислотно-щелочного равновесия в организме.
Органические вещества увеличивают уровень рh среды, что улучшает поглощение питательных веществ внутренними органами и выведение шлаков. Дело в том, что иммунная система, полезные бактерии в кишечнике, химические реакции, клетки лучше функционируют в щелочной среде.
Закисление организма, наоборот, – это идеальные условия для процветания болезней, в основе которых лежат следующие причины: агрессивное воздействие кислот, нарушающее работу клеток, деминерализация, ферментативная недостаточность. В результате человек испытывает недомогание, постоянную усталость, повышенную эмоциональность; появляются кислая слюна, отрыжка, спазмы, гастрит, трещины на эмали, гипотония, бессонница, неврит. В итоге ткани пытаются за счет внутренних резервов нейтрализовать лишнюю кислоту. Человек теряет мышечную массу, ощущает нехватку жизненных сил.
Органические кислоты участвуют в следующих процессах пищеварения, ощелачивая организм:
- активируют перистальтику кишечника;
- нормализуют ежедневный стул;
- замедляют рост гнилостных бактерий, брожение в толстом кишечнике;
- стимулируют выделение желудочного сока.
Функции некоторых органических соединений:

- Муравьиная кислота. Обладает асептическим действием, замедляет процессы распада, гниения, поэтому используется в качестве антибактериального консервирующего агента при заготовке корма. Может применяться в пчеловодстве для борьбы с паразитами, как отбеливатель при дублении кожи, в протравном крашении шерсти, при консервировании фруктов, сквашивании овощей, производстве соков, безалкогольных напитков. В природе встречается в яблоках, малине, черешне, крапиве, пчелином меде. . В качестве пищевой добавки используется при изготовлении кондитерских изделий, фруктовых вод. В медицине применяется для создания лекарств от запора, в косметологии – для смягчения и обеззараживания продукции. Содержится в рябине, барбарисе, малине, незрелых яблоках, винограде.
- Винная кислота. Применяется в аналитической химии, медицине, пищевой промышленности для обнаружения сахаров, альдегидов, при изготовлении безалкогольных напитков, соков. Выступает антиоксидантом. В наибольшем количестве содержится в винограде.
- Молочная кислота. Обладает бактерицидным действием, используется в пищевой промышленности для подкисления кондитерских изделий и безалкогольных напитков. Образуется при молочнокислом брожении, накапливается в кисломолочных продуктах, квашеных, соленых, моченых плодах и овощах.
- Щавелевая кислота. Стимулирует работу мышц, нервов, улучшает усвоение кальция. Если в процессе обработки становится неорганической, образуемые ее соли (оксалаты) вызывают образование камней, разрушают костную ткань. В результате у человека развиваются артрит, артроз, импотенция. Помимо этого, щавелевая кислота используется в химической промышленности (для производства чернил, пластмасс), металлургии (для очистки котлов от оксидов, ржавчины, накипи), в сельском хозяйстве (в качестве инсектицида), косметологии (для отбеливания кожи). В природе содержится в бобах, орехах, ревене, щавеле, шпинате, свекле, бананах, батате, спарже.
- Лимонная кислота. Активирует цикл Кребса, ускоряет метаболизм, проявляет дезинтоксикационные свойства. Применяется в медицине для улучшения энергетического обмена, в косметологии – с целью регулирования рН, отшелушивания мертвых клеток эпидермиса, разглаживания морщин. Служит консервантом для кремов, пенок, гелей и прочей продукции. В пищевой промышленности (в хлебопечении, для производства шипучих напитков, ликероводочных, кондитерских изделий, желе, кетчупа, майонеза, джема, плавленого сыра, холодного тонизирующего чая, рыбных консервов) используется как регулятор кислотности для защиты от брожения, скисания, порчи, придает продукции характерный кисловатый вкус. Источники соединения: китайский лимонник, незрелые апельсины, лимоны, грейпфруты, свити. . Обладает антисептическими свойствами, поэтому ее применяют как противогрибковое, противомикробное средство при кожных заболеваниях. Соль бензойной кислоты (натриевая) – отхаркивающее средство. Помимо этого, органическое соединение используют для консервации пищевых продуктов, синтеза красителей, создания парфюмерной воды. Для продления срока годности, Е210 входит в состав жевательной резинки, варенья, джема, повидла, конфет, пива, ликера, мороженого, фруктовых пюре, маргарина, молочной продукции. Природные источники: клюква, брусника, черника, йогурт, простокваша, мед, гвоздичное масло.
- Сорбиновая кислота. Является природным консервантом, обладает антимикробным действием, поэтому используется в пищевой промышленности для обеззараживания продуктов. Кроме того, она предотвращает потемнение сгущеного молока, плесневение безалкогольных напитков, хлебопекарных, кондитерских изделий, плодовоягодных соков, полукопченых колбас, зернистой икры. Полезные свойства сорбиновая кислота проявляет исключительно в кислой среде (при рН ниже 6,5). Наибольшее количество органического соединения обнаружено в плодах рябины. Уксусная кислота. Участвует в обмене веществ, используется для приготовления маринада, консервации. Содержится в соленых/квашеных овощах, пиве, вине, соках.
- Урсоловая, олеиновая кислоты расширяют венозные сосуды сердца, препятствуют атрофии скелетных мышц, снижают количество глюкозы в крови. Тартроновая замедляет превращение углеводов в триглицериды, предупреждая атеросклероз и ожирение, уроновая выводит из организма радионуклиды, соли тяжелых металлов, а галловая оказывает противовирусный, противогрибковый эффект.
Органические кислоты – вкусовые компоненты, которые в свободном состоянии или в виде солей входят в состав пищевых продуктов, определяя их вкус. Данные вещества увеличивают срок годности продуктов, улучшают усвояемость и переваривание пищи. Энергетическая ценность органических кислот – три килокалории энергии на грамм. Карбоновые и сульфоновые соединения могут образовываться во время производства продуктов переработки или быть природной частью сырья. Для улучшения вкуса, запаха органические кислоты добавляют в блюда в процессе приготовления (в выпечку, джемы). Помимо этого, они снижают pH среды, тормозят процессы гниения в ЖКТ, активируют перистальтику кишечника, стимулируют сокоотделение в желудке, оказывают противовоспалительное, антимикробное действия.
Суточная норма, источники
Для сохранения кислотно-щелочного баланса в пределах нормы (рН 7,36-7,42) важно ежедневно употреблять продукты, содержащие органические кислоты.
Для большинства овощей (огурцы, болгарский перец, капуста, лук репчатый) количество соединения на 100 грамм съедобной части составляет 0,1-0,3 грамма. Повышенное содержание полезных кислот в ревене (1 грамм), грунтовых томатах (0,8 грамма), щавеле (0,7 грамма), фруктовых соках, квасе, творожной сыворотке, кумысе, кислых сортах вин (до 0,6 грамм). Лидерами по уровню органических веществ выступают ягоды и фрукты:
- лимон – 5,7 грамма на 100 грамм продукта;
- клюква – 3,1 грамма;
- красная смородина – 2,5 грамма;
- черная смородина – 2,3 грамма;
- рябина садовая – 2,2 грамма;
- вишня, гранат, мандарины, грейпфрут, земляника, рябина черноплодная – до 1,9 грамма;
- ананас, персики, виноград, айва, алыча – до 1,0 грамма.
До 0,5 грамм органических кислот содержат молоко, кисломолочные продукты. Их количество зависит от свежести и вида изделия. При длительном хранении происходит закисление такой продукции, в результате она становится непригодной к употреблению в диетическом питании.
Учитывая, что каждый вид органической кислоты обладает особым действием, суточная надобность организма во многих из них варьирует в пределах от 0,3 до 70 грамм. При хронической усталости, пониженной секреции желудочного сока, авитаминозах потребность возрастает. При заболеваниях печени, почек, повышенной кислотности желудочного сока, наоборот, снижается. Показания к дополнительному приему природных органических кислот: низкая выносливость организма, хроническое недомогание, снижение тонуса скелетной мускулатуры, головные боли, фибромиалгия, спазмы в мышцах.
Вывод
Органические кислоты – группа соединений, которая ощелачивает организм, участвует в энергетическом обмене и содержится в растительных продуктах (корнеплодах, зелени, ягодах, фруктах, овощах). Недостаток данных веществ приводит к серьезным заболеваниям. Повышается кислотность, снижается усвоение жизненно необходимых минералов (кальция, натрия, калия, магния). Возникают болезненные ощущения в мышцах, суставах; развиваются остеопороз, болезни мочевого пузыря, сердечно-сосудистой системы, падает иммунитет, нарушается обмен веществ.
При повышенной кислотности (ацидозе) в мышечной ткани накапливается молочная кислота, возрастает риск наступления сахарного диабета, образования злокачественной опухоли. Избыток фруктовых соединений приводит к появлению проблем с суставами, пищеварением, нарушает работу почек.
Органические кислоты нормализуют кислотно-щелочное равновесие организма, сохраняют здоровье и красоту человека, оказывая благотворное влияние на кожу, волосы, ногти, внутренние органы. Поэтому в природном виде они должны ежедневно присутствовать в вашем рационе.
Специальность: терапевт, невролог .
Общий стаж: 5 лет .
Образование: Орловский государственный университет имени И.С. Тургенева .
Кислота — это вещество, в молекуле которого находится атом водорода вместе с остатком. Её можно как синтезировать искусственно, так и выделить с живого организма. Пожалуй, каждый в быту сталкивается хотя бы с одним соединением, входящим в список органических кислот. Встречаются они чаще в растительных продуктах и их широко используют в пищевой промышленности. Именно эти вещества и позволяют создавать комбинированные вкусовые ощущения.

Понятие кислота
В 1877 году химик из Швеции Сванте Аррениус предложил разделять ряд веществ на основания и кислоты. Согласно его теории, если при растворении в воде элемент высвобождает протон водорода Н+, его нужно относить к кислоте, а если гидроксид-иона (ОН-), то к основанию. Это правило позволило объяснить нейтрализацию веществ при взаимодействии друг с другом. Позже учёный дал уточнение, что сталкивание гидроксид-иона с ионом водорода образовывает воду H2O.

В начале двадцатого века британец Томас Лаури и датчанин Йоханнсен Брёнстед расширили определение. Они предложили относить к кислотам любую молекулу (ион), способную отдавать протон. Это позволило описать реакции, проходящие c водой, например, хлорид аммония.
В 1923 году американец Льюис на основании двух определений сформулировал своё правило. Его формулировка и стала использоваться повсеместно. По нему, кислота — это химическое соединение, принимающее электронную пару и образовывающее ковалентную связь. Основание же, напротив — соединение, способное избавляться от электронной пары.
Все кислоты в химии принято разделять на 2 типа:
Кроме этого, соединения могут быть одноосновными, двухосновными или трёхосновными. Все кислоты, за исключением кремниевой, отлично растворяются в воде. При взаимодействии с основаниями образуют соль, воду и кислотный остаток. Протекание реакции при соприкосновении с металлами происходит не всегда. Взаимодействие возможно лишь элементов, которые располагаются левее водорода. При этом кислотное соединение должно быть не только сильным, но и способным отдавать частицы водорода, которые выделяются во время взаимодействия.
Кислотные растворы могут изменять цвет. Так, лакмус становится красным. Соединение при взаимодействии имеет кислый вкус, появляется электрическая проводимость.
Если же в кислотный раствор добавить спирт, образуется сложный эфир. Все приведенные свойства характерны как для органических соединений, так и неорганических.
Особенности органического класса
Органическая химия изучает синтезирование углеводородов и их производство. Производные соединения углерода и водорода в молекулах относятся к карбоксильной группе (- COOH). Название веществ состоит из двух элементов: карбонита и гидроксила. Свойства же группы определяется смещением электронной плотности к карбонильному кислороду и образованной поляризацией связи O-H.

Другое название карбонатных кислот — органические. Их свойства определяются строением. Особенности группы из-за диссоциации с образованием частиц водорода в том, что её свойства совпадают с минеральными кислотами. Некоторые соединения, например, уксусная кислота (СН3СОOН) в своей молекуле имеют углеводородный радикал, поэтому возможны реакции, сопровождающиеся выбиванием водорода галогеном. Этот процесс приводит к повышению степени диссоциации, и кислота становится сильнее.
Из свойств органических соединений можно выделить:
- При реагировании с металлами образуется соль и водород — CH3-CH2-COOH + K → CH3-CH2-COO-K + H2.
- Реакция с галогенами описывается формулой: CH3 — CH2 — C = O (-OH) + Cl2 → CH3 — CH (-Cl) — C = O (-OH) + HCl, то есть протекает с появлением галогеносодержащих кислот.
- Взаимодействие со спиртом приводит к возникновению эфира: CH3 — CH2 — COOH + CH3 — OH → CH3 — COOH — CH3.
- При реагировании с металлами образуется соль и вода: CH3-CH2-COOH + MgO →Mg (CH3-CH2-COO)2 + H2O.
- Соединение с солью приводит к слабой кислотности с образованием иной соли: CH3CH2-COO-Na + H2O + CO2.
Так как карбоновые кислоты распадаются на ионы, степень растворимости и достаточно большая температура кипения определяют межмолекулярные водородные связи. При этом с возрастанием молекулярной массы растворимость соединения уменьшается.
Карбоновые кислоты принято разделять и по природе углеводородного радикала: они бывают алифатическими, ароматическими и алициклическими. Если же в первом типе содержится более шести атомов углерода, соединение называют жирной кислотой. Это происходит из-за того, что в виде сложных эфиров они являются частью природных жиров и масел.
Ароматическая представляет собой бензойную и дикарбоновую кислоту, а алициклическая – циклопропан-карбоновую и циклогексанкарбоновую кислоты. Из структуры соединений выделяют радикалы (ацилы). Подписывают их используя суффикс – ил., например, бутрил, формил.
Таблица соединений
Существует две системы обозначений для карбоновых соединений. Их классификация допускает использование тривиального названия и по ИЮПАК. В то же время применение систематической номенклатуры считается более предпочтительной. Всё дело в том, что тривиальные имена не содержат сведений о составе и строении соединений, а некоторые сложные эфиры и соли вовсе не имеют сокращённых наименований.
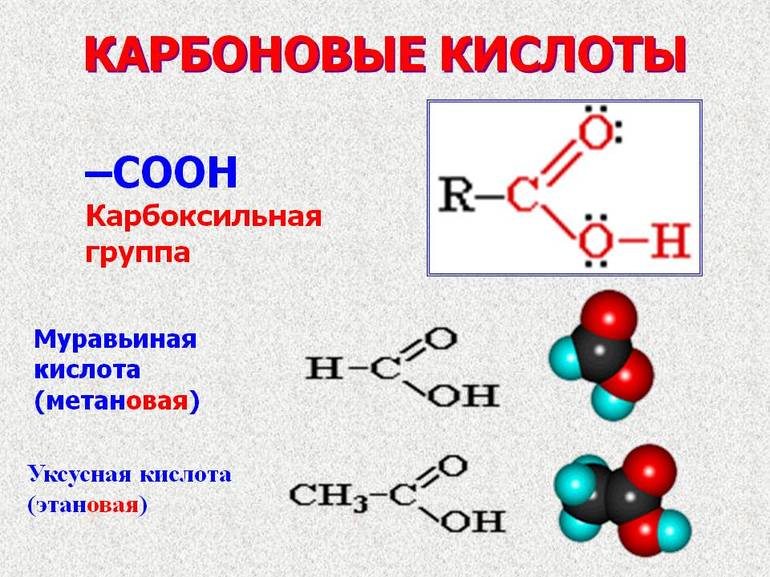
В мире насчитывается более сотни различных видов органических кислот. Они входят в компоненты природных вод и связаны с жизнедеятельностью человека, животных и растений. Общую формулу для всей группы можно изобразить как R—COOH. Из наиболее популярных соединений можно выделить:
Отдельно нужно выделить муравьиную кислоту (HCOOH). Это одноосновное соединение. В природе она вырабатывается у пчёл, муравьёв, содержится в крапиве и хвое. Проявляет восстановительные свойства. Эта кислота очень востребована как антибактериальное средство.
Происхождение и получение
Получение HOOC-соединений связано с окислением спиртов. Протекающую реакцию окисления этилового спирта можно записать как CH3 – CH2 – OH → CH3 – C = O (-OH) + H2O. Окисление же уксусного альдегида выглядит следующим образом: CH3 – C = O (H) → CH3 – C =O (-OH). Образование возможно и гидролизом нитрилов. Побочным продуктом является аммиак: CH3 – C = N + H2O → CH3 – C = O (-OH) + NH3.

Карбоновую кислоту можно создать гидролизом сложного эфира. В результате реакции получается спирт. Что интересно, если в реакции использовать щёлочь, продуктом станет соль. Но если её поместить в минеральную кислоту, получится органическая. Реакция имеет вид: СH3 – C = O (-CH3) + H2O → CH3 – C = O (-OH) – CH3OH. Этот способ применяется для получения высших соединений: пальмитинового ( C 16 H 32 O 2), стеаринового ( c17h35cooh), олеинового ( c17h33cooh). При этом в воде они не растворяются.
Сульфокислоты, описываемые формулой RSO3H с органическим радикалом, по функциям сходны с сульфогруппой -SO3H. Получают их путём сульфирования ароматических углеводов. Например, нуклеофильным обменом иона галогена на сульфогруппу, сульфоокислением алканов, тиолов и органических дисульфидов.
Всего же можно выделить следующие способы:
- окисление;
- гидролиз;
- разложение цианидов;
- использование раствора Гриньяра.
В промышленности предельные монокарбоновые кислоты получают из жиров, восков, масел. Довольно распространённый способ образования соединений - путём окисления алканов и алкенов. Например, муравьиная кислота образовывается из метана 2CH4 + + 3O2 → 2HCOOH + 2H2O, а уксусная из н-бутана 2CH3-CH2-CH2-CH3 + 5O2 → 4CH3COOH + 2H2O. Кроме этого, выполняют окисление алканов, гомологов бензола. Производство возможно и в лабораторных условиях. Так в них выполняют гидролиз сложных эфиров и галогенпроизводных, растворяют ангидриды. Какой способ предпочтителен, зависит от имеющихся реактивов и необходимой концентрации полученного раствора.

Некоторые кислоты можно выделить из живых организмов. Например, муравьиную, уксусную. Если первую выделяют из красных муравьёв, вторая содержится в выделениях животных, образуется в результате брожения или скисания. Бензойная кислота находится в ладане, эфирных маслах, бальзамах. Нельзя не упомянуть и самую известную кислоту - лимонную. Способ её чистого получения был открыт в 1860 году и стал называться биосинтезом.
В свободном состоянии такие многоосновные оксикислоты содержатся довольно-таки часто в плодах, соединения же характерны в первую очередь для остальных элементов растений вроде стебля, листьев и так далее. Если посмотреть на органические кислоты, список их постоянно увеличивается и в целом является не закрытым, то есть регулярно пополняемым. Уже открыты такие кислоты, как:
-янтарная и многие другие органические кислоты.
Зачастую такие вещества можно найти в плодово-ягодных растениях. К плодовым растениям относят абрикосы, айву, алычу, виноград, вишню, груши, цитрусовые и яблоки, к ягодным же растениям причисляют бруснику, вишню, ежевику, клюкву, крыжовник, малину, черную смородину. В них в основе своей находятся винная, лимонная, салициловая, щавелевая и яблочная кислоты. В ягодах также присутствуют органические кислоты, и в том числе немало бензойной кислоты.
На сегодняшний день изучено множество свойств кислот непосредственно в сфере фармакологии и биологического воздействия на организм человека. Так, например:
- во-первых, органические кислоты - достаточно значимые компоненты метаболизма (обмен веществ, а именно белков, жиров и углеводов);
- во-вторых, вызывают секреторную работу слюнных желез; способствуют кислотно-щелочному равновесию;
- в-третьих, принимают значительное участие в увеличении отделения желчи, желудочного и панкреатического соков;
- и наконец, являются антисептиками.
Их кислотность колеблется от четырех целых водородного показателя (pH) до пяти и пяти.
Помимо этого, органические кислоты играют немаловажную роль в пищевой промышленности, выступая как непосредственный выявитель качества или же недоброкачественности продукции. Для последнего используется очень часто метод ионной хроматографии, в котором за раз можно обнаружить не только органические кислоты, но и неорганические ионы. При указанном методе кондуктометрическое детектирование с заглушением фоновой электропроводности показывает результат почти что в десять раз точнее, чем детектирование при низких показателях длины волны ультрафиолетового излучения.
Выявление профиля органических кислот в соках фруктов необходимо не только для установления качества напитка, его допустимости к употреблению, но и способствует определению подделки.
Если рассмотреть уже непосредственно свойства карбоновых кислот, то к ним в первую очередь относятся:
- придание красного цвета лакмусовой бумаге;
- легкая растворимость в воде;
- наличествующий кислый вкус.
Также карбоновые кислоты являются достаточно важным электрическим проводником. По силе распада абсолютно все кислоты относятся к слабой группе электролитов, за исключением, естественно, муравьиной кислоты, которая в свою очередь занимает среднее по интенсивности значение. Высота молекулярной массы карбоновой кислоты влияет на силу распада и имеет обратно-пропорциональную зависимость. С помощью конкретно определенных металлов появляется возможность выделить водород и соль из кислот, что происходит значительно медленнее, чем при взаимодействии с сильными кислотами вроде серной или соляной. Также соли появляются и при воздействии основных оксидов и оснований.
Читайте также:

