Межпредсердное сообщение мкб 10
Обновлено: 05.07.2024
Новорожденные и грудные дети, да и дети раннего возраста в подавляющем большинстве растут и развиваются абсолютно нормально. Родители могут замечать их склонность к частым простудам, иногда заканчивающихся воспалением легких, что должно насторожить. Часто эти дети, в 2/3 случаев девочки, растут бледными, худенькими и несколько отличаются от своих здоровых сверстников. Физических нагрузок они стараются по возможности избегать, что в семье могут объяснить их природной ленью и нежеланием себя утомлять.
Иногда дефект межпредсердной перегородки может сочетаться с неправильным, аномальным впадением одной или двух легочных вен в правое предсердие вместо левого. Клинически это никак себя не проявляет, и является находкой при обследовании ребенка с большим дефектом. Операцию это не усложняет: просто заплата — больше и делается в виде тоннеля в полости правого предсердия, направляющего окисленную в легких кровь в левые отделы сердца.
Сегодня, кроме хирургической операции в некоторых случаях можно безопасно закрыть дефект с помощью рентгенохирургической техники. Вместо ушивания дефекта или вшивания заплаты, его закрывают специальным устройством в виде зонтика — окклюдером, который проводят по катетеру в сложенном виде, и раскрывают, пройдя через дефект.
Сегодня оба способа широко применяются, а результаты – отличные. В любом случае вмешательство носит элективный, не срочный характер. Но нужно делать его в раннем детстве, хотя можно и раньше, если частота простуд и, особенно, пневмоний, становится устрашающей и угрожает бронхиальной астмой, а размеры сердца увеличиваются. Вообще, чем раньше будет сделана операция, тем быстрее ребенок и вы о ней забудете, но это не значит, что при этом пороке надо особенно спешить.
Этиология: факторы, формирующие ВПС (см. Тетрада Фалло).
Патогенез • Величина и направление сброса зависят от размера дефекта и относительной податливости желудочков • У взрослых правый желудочек более податлив, чем левый, вследствие этого сброс происходит из левого предсердия в правое • Небольшой сброс ведёт к умеренной объёмной перегрузке правых отделов сердца, и давление в лёгочной артерии остаётся нормальным • Выраженность лёгочной гипертензии может быть незначительной даже при большом сбросе • Только в редких случаях развивается тяжёлая лёгочная гипертензия, приводящая к правожелудочковой недостаточности и сбросу справа налево • В отличие от ДМЖП, при ДМПП сброс меньше и влияет только на правые отделы сердца.
Варианты ДМПП • Ostium secundum (вторичные дефекты) локализуются в области овальной ямки, часто бывают множественными, сопутствуют многим синдромам: синдрому Холт–Орама (ДМПП типа ostium secundum в сочетании с гипоплазией пальцев), синдрому Лютембаше (сочетание ДМПП со стенозом митрального клапана), сочетанию ДМПП с пролапсом митрального клапана и др. • Ostium primum (первичные дефекты) обычно больших размеров, локализуются в нижней части перегородки, в месте прикрепления митрального и трёхстворчатого клапанов, межпредсердной и межжелудочковой перегородок. Бывают составной частью открытого АВ-канала и нередко сочетаются с аномальным дренажём лёгочных вен, расщеплением передней створки митрального клапана, митральной недостаточностью и синдромом Дауна • Дефекты типа sinus venosus локализуются около устья верхней полой вены и синусового узла, нередко сочетается с синдромом слабости синусового узла, АВ-узловым ритмом и аномальным дренажём лёгочных вен.
Клиническая картина
Жалобы: одышка, сердцебиение, быстрая утомляемость при физической нагрузке, отставание в физическом развитии, частые инфекции, парадоксальные эмболии.
Объективно • Бледность кожных покровов • Борозды Харрисона — смещение участков грудной клетки в результате хронической одышки • Расщепление I тона с выраженным компонентом трёхстворчатого клапана • Выраженное фиксированное расщепление II тона (выраженное — из-за удлинения времени выброса крови из правого желудочка; фиксированное — из-за того, что зависимость венозного возврата от фаз дыхания нивелируется сбросом из левого предсердия) • Щелчок изгнания и мягкий систолический шум относительного стеноза лёгочной артерии во втором межрёберном промежутке слева от грудины • Из-за увеличения кровотока через трёхстворчатый клапан иногда возникает низкочастотный диастолический шум над мечевидным отростком грудины.
Инструментальная диагностика
• ЭКГ. Признаки гипертрофии и перегрузки левых отделов, а при лёгочной гипертензии — и правых. При ostium primum — резкое отклонение ЭОС влево вследствие смещения гипоплазированной ветви левой ножки пучка Хиса вперёд. Различные варианты синдрома слабости синусового узла, АВ-блокады. При дефекте типа sinus venosus — нижнепредсердный ритм или ритм АВ-соединения.
• Яремная флебография: одинаковая амплитуда волн A и V.
• ЭхоКГ. Гипертрофия и дилатация левых отделов, а при лёгочной гипертензии — и правых. Визуализация ДМПП в допплеровском и В-режиме. Дифференцировка от открытого овального окна (анатомическое закрытие последнего происходит не позднее 2 лет жизни) — непостоянство визуализации сброса в режиме цветового допплеровского картирования и наличие створки в полости левого предсердия. Диагностика сопутствующих аномалий (аномального дренажа лёгочных вен, клапанных пороков и др.). Определяют степень сброса и отношение лёгочного минутного кровотока к системному (Qp/Qs). Взрослым проводят чреспищеводную ЭхоКГ. При внутривенном контрастировании правых отделов сердца — эффект отрицательного контрастирования (вытеснение контрастного вещества струёй крови из левого предсердия).
• Радионуклидная ангиокардиография (по методу первого прохождения или равновесная): регистрация патологического сброса и его количественная оценка, диагностика сопутствующего аномального дренажа лёгочных вен и нарушений функций желудочков.
• Зондирование полостей сердца •• Показано при подозрении на лёгочную гипертензию, перед операцией на открытом сердце и при противоречивых клинических данных •• Если катетер удаётся провести из правого предсердия в левое, то само по себе это не может служить признаком дефекта межпредсердной перегородки: иногда катетер удаётся провести и через открытое овальное окно •• Проводят пробы с аминофиллином и ингаляцией кислорода для определения прогноза в отношении обратимости лёгочной гипертензии •• Вычисляют отношение лёгочного минутного кровотока к системному (Qp/Qs) — эталонный показатель величины сброса.
• Правая атриография, ангиопульмонография: поступление контраста из правого предсердия в левое; выявление сопутствующего аномального дренажа лёгочных вен.
Медикаментозная терапия. При неосложнённых ДМПП типа ostium secundum профилактику инфекционного эндокардита обычно не проводят. При ДМПП типа ostium primum, больших дефектах типа sinus venosus и сочетании ДМПП с пороками митрального клапана назначают антибиотики до и в течение 6 мес после неосложнённой хирургической коррекции. При правожелудочковой недостаточности назначают диуретики.
Хирургическое лечение
Показания: отношение Qp/Qs составляет 1,5 и более, дефекты типа ostium primum, крупные дефекты типа ostium secundum, сопутствующие гемодинамически значимые аномалии (аномальный дренаж лёгочных вен, митральный стеноз и пр.).
Противопоказания: тяжёлая сопутствующая патология, угрожающая жизни больного; терминальная стадия недостаточности кровообращения, необратимая лёгочная гипертензия, отношение общего лёгочного сосудистого сопротивления к ОПСС составляет 0,9 и более.
Методы оперативного лечения. Эндоваскулярная коррекция пуговичным или двухзаплатным устройством Сидериса либо устройством Амплатц выполнимо при центральных дефектах размером не более 2 см. При отсутствии опыта эндоваскулярного лечения небольшие дефекты ушивают в условиях искусственного кровообращения. В остальных случаях рекомендуют пластику ДМПП синтетической или аутоперикардиальной заплатой в условиях искусственного кровообращения.
Специфические послеоперационные осложнения • Синдром слабости синусового узла (после коррекции дефектов типа sinus venosus) • АВ-блокада (после коррекции дефектов типа ostium primum) • При митральной недостаточности, существовавшей до операции, возможно усугубление симптомов после коррекции ДМПП • Фибрилляция предсердий, возникшая до операции, как правило, сохраняется и после неё.
Прогноз. В раннем детском возрасте течение доброкачественное. В редких случаях тяжёлые нарушения кровообращения могут приводить к смерти в первые месяцы жизни. Возможно спонтанное закрытие дефекта до 5-летнего возраста. Средняя продолжительность жизни без лечения — 40 лет. 5–15% больных умирают до 30 лет. 10-летняя выживаемость — 90%, 20-летняя — 88%, 30-летняя — 67%; 40-летняя — 44%, 50-летняя — 25%, 60-летняя — 13%, 70-летняя — 7%. Более 75% пациентов с большими дефектами умирают от других причин. При неосложнённых дефектах типа ostium secundum периоперационная летальность — менее 1%, несколько выше она при дефектах типа ostium primum, при последних необходимо также протезирование или пластика митрального клапана.
Сокращения. Qp/Qs — отношение лёгочного минутного объёма кровотока к системному.
Классификация
По эмбриологическому генезу, т.е. в зависимости от характера и степени недоразвития первичной и вторичной межпредсердных перегородок и эндокардиальных валиков, выделяют первичные, вторичные дефекты и полное отсутствие МПП (единственное, общее предсердие, трехкамерное сердце).
2) Вторичные ДМПП возникают вследствие недоразвития вторичной МПП, поэтому обычно полностью окружены ободком септальной ткани и в нижнем отделе всегда отделены краем МПП от перегородки, расположенной между двумя атриовентрикулярными клапанами. Размеры дефекта варьируются в достаточно широких пределах - от 2-5 до 20-30 мм в диаметре. В большинстве случаев дефект находится в центре МПП (65-67%); реже - в верхней (5-7%) и совсем редко - в задней (2,5%) и передней частях перегородки.
Единственное (общее) предсердие формируется в результате недоразвития в эмбриональном периоде или полного отсутствия первичной и вторичной МПП и наличия большого дефекта, равного по площади всей МПП. При этом сохранены два предсердных ушка и дифференциальная структура правой и левой стенок предсердия. Поскольку нарушено развитие первичной МПП и эндокардиальных валиков, порок, как правило, сочетается с дефектом формирования атриовентрикулярных клапанов, поэтому может рассматриваться как одна из форм ОАВК. При данном пороке нередко наблюдается аспления.
Дефекты МПП могут быть также комбинированными (первичный и вторичный ДМПП или в сочетании с дефектом венозного синуса).
Эпидемиология
Распространенность ДМПП колеблется в широком диапазоне - от 5 до 37,1%. Это, вероятно, обусловлено различным возрастным контингентом обследованных и сложностью раннего выявления и диагностики порока у детей младшего возраста. У взрослых ДМПП считается самым распространенным пороком, составляя 20-37%.
ДМПП - это патология, распространенная преимущественно среди лиц женского пола (соотношение женщин и мужчин от 1,5:1 до 3,5:1)
У новорожденных и детей первых месяцев жизни до возникновения выраженного физиологического преобладания левых отделов сердца давление в легочной артерии относительно высокое (30-35 мм рт.ст.), а системное АД низкое, поэтому артериовенозный сброс небольшой и существенных гемодинамических нарушений нет. В первые недели жизни при кратковременной задержке дыхания и повышении сопротивления в МКК (сосание, крик, плач, натуживание, дефекация и др.) даже возможен кратковременный веноартериальный сброс в левое предсердие с возникновением слабого транзиторного цианоза. Это наиболее часто наблюдается при дефектах, расположенных около устьев полых вен.
Характерно для данного состояния расширения ствола легочной артерии на фоне формирования относительного функционального стеноза нормального отверстия легочного клапана, размеры которого не соответствуют уже значительно возросшему ударному объему правого желудочка.
Клинически ДМПП относится к гемодинамически длительно компенсированным и маломанифестным порокам. Выраженность его симптоматики зависит от величины и локализации дефекта, а также в большей степени от длительности существования порока и развития вторичных осложнений.
До 2-5 лет клиническая симптоматика порока очень скудная, поэтому в младшем возрасте порок выявляют редко или расценивают как функциональную кардиопатию (возможное появление в периоде новорожденности транзиторного цианоза при крике и беспокойстве чаще связывают с перинатальной энцефалопатией).
Дети с небольшой величиной дефекта (до 10-15 мм) развиваются нормально, удовлетворительно переносят нагрузки, первые симптомы порока могут появляться у них лишь во втором десятилетии жизни. Несмотря на постоянную бледность, наличие цианоза нехарактерно для детей с ДМПП, так как легочная гипертензия и сердечная недостаточность у них чаще формируются лишь к 20 годам.
АД нормальное, а при больших дефектах снижается максимальное и пульсовое АД. Пульс нормального напряжения и несколько пониженного наполнения.
Деформация грудной клетки в виде умеренного центрального сердечного горба, обусловленная дилатацией и гипертрофией правого желудочка, отмечается лишь в 5-8% случаев - при больших дефектах и быстро прогрессирующей легочной гипертензии в более старшем возрасте. Систолическое дрожание, как правило, не пальпируется. Верхушечный толчок нормальной силы, сердечный толчок выражен в III-IV межреберьях, особенно у худых детей.
Границы сердца увеличены вправо и вверх за счет предсердий, но при больших дефектах и в старшем возрасте отмечается также расширение левой границы сердца, как правило, за счет правого желудочка, оттесняющего левый желудочек кзади. Выраженная кардиомегалия возникает редко.
В поздних стадиях заболевания при значительном расширении ствола легочной артерии (у 10-35% больных) иногда появляется нежный протодиастолический шум относительной недостаточности пульмонального клапана (шум Грехема-Стилла).
Электрокардиография. У большинства больных с ДМПП имеется отклонение ЭОС вправо, в пределах от +90 до +150, и лишь у небольшого числа пациентов (5-10%) выявляется нормограмма. В случаях наличия левограммы при большом ДМПП и признаках перегрузки правых отделов сердца необходимо предположить возможность сочетания ДМПП с расщеплением створки митрального клапана или парциальный блок проведения по передневерхней ветви левой ножки пучка Гиса. Признаки гипертрофии правого желудочка: высокие зубцы R в отведениях aVR, V1-2 и глубокие зубцы S в V5-6 - выражены умеренно и очень редко сопровождаются систолической перегрузкой (глубокие зубцы Т в V1-4 со смещением сегмента ниже изолинии).
Фонокардиография. I тон в 5 ЛСК и 3-4 ЛС, как правило, увеличен по амплитуде, иногда расщеплен до 0,02-0,03 сек. II тон в 2 ЛС раздвоен (более 0,03 сек.) с возрастанием амплитуды пульмонального компонента. В 3-4 ЛС в диастоле может регистрироваться низко- и среднеамплитудный III тон, связанный с быстрым наполнением правого желудочка, и 4-й пресистолический экстратон, обусловленный сильным сокращением правого предсердия. В 2 ЛС и 3-4 ЛС фиксируется среднечастотный среднеамплитудный систолический шум, чаще ромбовидной или веретенообразной формы, на 1 /2- 2 /3 систолы. По мере нарастания легочной гипертензии III тон уменьшается, а II и IV тоны увеличиваются по амплитуде, при этом исчезает раздвоение II тона. Это связано с более ранним и быстрым закрытием пульмонального клапана и приближением пульмонального компонента к аортальному. Шум Грехема-Стилла записывается как высокочастотный низкоамплитудный протодиастолический шум, лучше фиксируемый в 2 ЛС и 3-4 ЛС.
Эхокардиография. В М- и 2D-режимах сканирования при одномерной и двумерной ЭхоКГ выявляются косвенные и прямые признаки ДМПП. Прямыми признаками вторичного ДМПП в 2 D-режиме в проекции 4 камер с верхушки и в парастернальной позиции по короткой и длинной осям сканирования визуализируются перерыв эхосигнала и свободные края дефекта в дистальной от атриовентрикулярных клапанов части. Косвенный признак порока - артериовенозный сброс на уровне предсердий. Он проявляется перегрузкой правых отделов сердца в виде увеличения экскурсий задней стенки правого предсердия и створок трикуспидального клапана, при одновременном уменьшении интенсивности экскурсий створок митрального клапана. Кроме того, отмечается объемная перегрузка и увеличение размеров полости правого желудочка, к косвенным признакам которого относится и парадоксальное движение МЖП.
Рентгенография. Легочный рисунок у большинства больных усилен и обогащен за счет артериального русла. Тени корней легких и ветвей легочной артерии расширены. Размеры сердца и степень обогащения легочного рисунка зависят от величины артериовенозного сброса. При большом сбросе у детей старшего возраста в прямой проекции сердце увеличено в поперечнике за счет правого желудочка, который выходит на левый контур сердца - об этом свидетельствуют также закругление и приподнятость верхушки над диафрагмой. Талия сердца сглажена из-за выбухания легочной артерии. Правый контур сердца увеличен из-за дилатированного правого предсердия и смещения вверх атриовазального угла. В косых и левой боковой проекциях выявляются увеличение правого предсердия, дилатация выходного отдела правого желудочка и выбухание ствола легочной артерии (Ovitt T.W., 1995). У пациентов с малыми дефектами отмечается лишь умеренное усиление легочного рисунка при нормальных размерах сердца.
Катетеризация сердца и ангиокардиография. Совершенствование и широкое внедрение в клиническую практику такого неинвазивного метода, как эхокардиография, сузило показания к использованию катетеризационных методов обследования детей с ВПС.
О наличии ДМПП свидетельствуют возможность прохождения зонда из правого предсердия в левое, более высокое насыщение кислородом крови, взятой из полости правого предсердия, по сравнению с пробами крови, взятой около устьев полых вен. Разница в10% и более считается абсолютным признаком артериовенозного шунта крови.
Ангиокардиография позволяет дифференцировать источник пассажа артериальной крови в правое предсердие между ДМПП и аномальным дренажом легочных вен. Для этого контрастирующее вещество вводится через зонд в легочную артерию и после прохождения через МКК при ДМПП поступает в правое предсердие через левое, а при аномальном дренаже - в основном непосредственно в правое предсердие.
Давление в правом предсердии, правом желудочке и легочной артерии умеренно повышено, однако в детском возрасте оно очень редко превышает 45-50 мм рт.ст. Несмотря на функциональный характер стеноза, систолический градиент между давлением в правом желудочке и легочной артерии достигает 30 мм рт.ст.
Дифференциальную диагностику ДМПП с большим сбросом следует проводить с:
• ВПС, протекающими с обогащением МКК;
• умеренным изолированным СЛА.
При малых вторичных ДМПП необходимо проводить дифференциальную диагностику с функциональной кардиопатией и нейроциркуляторной дистонией.
Естественное течение порока и прогноз определяются размером дефекта и величиной артериовенозного сброса. Дети с вторичными ДМПП и малым сбросом крови развиваются нормально, не предъявляют жалоб, многие годы у них сохраняется физическая работоспособность, а первые симптомы неблагополучия иногда выявляются лишь в третьем десятилетии жизни. Однако в дальнейшем заболевание быстро прогрессирует, и большая часть пациентов умирают в возрасте до 40 лет, а живущие к 50 годам становятся инвалидами. Тем не менее часто описывают случаи, когда больные с вторичным ДМПП доживали до 70-80 лет. У некоторых пациентов с небольшим ДМПП происходит спонтанное закрытие дефекта в течение первых 2-5 лет жизни.
Основной причиной смерти больных после 20-30-летнего возраста становится развитие правожелудочковой сердечной недостаточности, нарушений сердечного ритма и проводимости (пароксизмальная тахикардия, мерцательная аритмия и др.), реже - высокие степени легочной гипертензии.
Младенческая смертность в основном обусловлена первичным ДМПП и (или) наличием ДМПП и АДЛВ, дефектов атриовентрикулярных клапанов, а также сочетанием ДМПП с экстракардиальными врожденными аномалиями. Непосредственными причинами смерти чаще всего являются тяжелые вирусные инфекции, рецидивирующие пневмонии, кишечные инфекции.
ДМПП реже, чем другие ВПС, осложняются инфекционным эндокардитом, хотя ревматизм у таких пациентов возникает относительно часто - в 10% случаев.
Хирургическая коррекция (показания к проведению и результаты). Оптимальный возраст проведения операции - 5-12 лет.
Операция не показана больным в бессимптомной стадии доказанного порока, при которой отсутствуют жалобы и определенная клиническая симптоматика, изменения на ЭКГ, а единственный признак порока - наличие аускультативной и эхокардиографической симптоматики. Другая группа больных (5-я группа), которым не показана операция, - это пациенты в терминальной стадии заболевания, с выраженной легочной гипертензией, у которых произошла смена шунта на веноартериальный, с цианозом и нарушениями в обоих кругах кровообращения.
Больным, у которых уже имеется очерченная клиническая симптоматика, подтвержденная инструментально и рентгенологически, показано оперативное вмешательство. Современная тенденция предусматривает раннюю хирургическую коррекцию ВПС, но часто имеется возможность отложить операцию на более поздний срок, когда риск от ее проведения уменьшается. У детей при условии эффективности консервативного лечения порока операцию можно отложить до 3-5-летнего возраста, однако если консервативное лечение малоэффективно, то операция показана всем больным, независимо от их возраста.
Операция - единственный эффективный метод лечения. Небольшие вторичные ДМПП закрываются ушиванием при больших дефектах, первичных ДМПП, из-за опасности прорезывания швов от натяжения дефект всегда закрывают заплатой из аутоперикарда или синтетической ткани. Операция выполняется на сухом сердце в условиях гипотермии и искусственного кровообращения. Летальность не превышает 2%, а при строгом соблюдении разработанных показаний летальных исходов не бывает. Результаты вмешательства во многом определяются исходным состоянием больного. Летальность тем выше, чем меньше возраст, выше степень легочной гипертензии, выраженнее недостаточность кровообращения и нарушения сердечного ритма и проводимости, тяжелее проявления сопутствующего инфекционного эндокардита.
Наиболее частыми причинами летальных исходов являются острая сердечная недостаточность, эмболия и гипоксические поражения головного мозга.
Открытое овальное отверстие также является вариантом межпредсердной коммуникации и может быть обусловлено как недоразвитием клапана овального отверстия, так и его дефектом. Необходимо отметить, что открытое овальное отверстие не относится к истинным дефектам перегородки, обусловленным недостаточностью ее ткани, поэтому не может быть причислено к ДМПП.
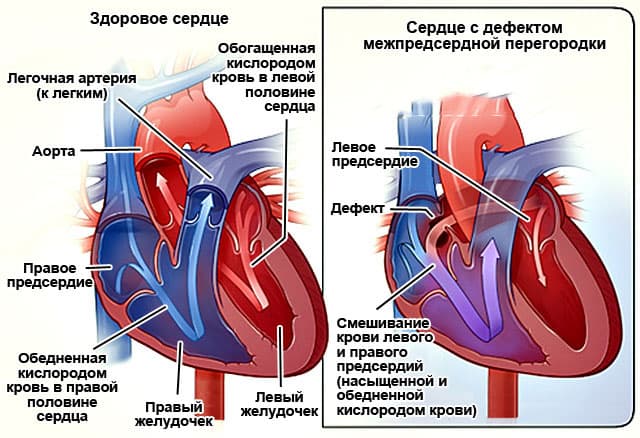
Дефект межпредсердной перегородки – это отверстие в межпредсердной перегородке, через которое кровь поступает из левого в правое предсердие.
Дефекты по своему расположению и формированию подразделяются на первичные, вторичные дефекты межпредсердной перегородки и дефекты венозного синуса.
Дефекты могут иметь различную форму и размеры (вплоть до полного отсутствия перегородки и формирования единого предсердия), могут быть единичными и множественными, могут быть единственным пороком сердца, а могут входить в состав более сложных пороков сердца (открытый AV-канал, аномальный дренаж легочных вен и т.д.).
Причины дефекта межпредсердной перегородки
В основе формирования дефекта межпредсердной перегородки лежит нарушение развития первичной или вторичной перегородки в эмбриональном периоде.
- Первичный дефект располагается в нижней части межпредсердной перегородки рядом с фиброзными кольцами атриовентрикулярных клапанов (митрального и трехстворчатого), по сути его нижним краем является само фиброзное кольцо.
- Вторичный дефект располагается в центральной части межпредсердной перегородки, и все его края представлены самой перегородкой.
- Дефект венозного синуса – это дефект, локализующийся в верхней части межпредсердной перегородки. Данному пороку часто сопутствует аномальный дренаж лёгочных вен (часть лёгочных вен впадает не в левое предсердие, а в верхнюю полую вену).
Гемодинамика
Cмысл порока заключается в сбросе артериальной крови из большого круга кровообращения (левого предсердия) в малый круг кровообращения (правое предсердие), что приводит к перегрузке малого круга кровообращения избыточным объемом крови с поражением, в первую очередь, легких. Крайней формой поражения является формирование легочной гипертензии (высокого давления в сосудах легких). Легочная гипертензия при дефекте межпредсердной перегородки носит злокачественный характер, приводя к тяжелой сердечной недостаточности и гибели пациента.
Симптомы
Первые симптомы заболевания возникают в виде одышки при физической нагрузке, частых простуд, ощущения перебоев в работе сердца. При этом симптоматика разнообразная и зависит от локализации и размера дефекта, сочетания его с другими пороками сердца. Дефекты малого размера не имеют характерной клинической картины. Жалобы пациенты активно не предъявляют, физическая активность их не ограничена - порок обнаруживается случайно. При больших, гемодинамически значимых дефектах у пациентов появляются одышка, повышенная утомляемость, непереносимость физической нагрузки. После физических упражнений возможно возникновение кашля, сопровождающегося иногда кровохарканьем. Для таких пациентов характерны частые пневмонии, бронхиты.
Диагностика
- Осмотр пациента с аускультацией (выслушиванием) сердца выявляет шумы в сердце.
- ЭКГ выявляет гипертрофию миокарда правого желудочка, блокаду правой ножки пучка Гиса, аритмии разной степени тяжести, резкое отклонение электрической оси сердца влево.
- Рентгенография органов грудной клетки выявляет расширение ствола легочной артерии, увеличение сердца, усиление лёгочного рисунка.
- Трансторакальная эхокардиография позволяет не только визуализировать дефект межпредсердной перегородки и уточнить его характер (первичный, вторичный, дефект венозного синуса), но также оценить направление сброса крови через дефект и его гемодинамическую значимость (Qp/Qs).
- Чреспищеводная эхокардиография у взрослых позволяет получить детальную информацию о краях дефекта, что важно для выбора метода оперативного лечения.
- Зондирование камер сердца и атриография используется при недостаточной информации от вышеописанных методов исследования или как часть уже оперативного лечения.
Показания к операции на дефект межпредсердной перегородки
Принятие решения об оперативном лечении зависит от размера дефекта, его гемодинамических характеристик (объем и направление сброса крови через дефект), наличия и величины легочной гипертензии, возраста пациента, наличия сопутствующей патологии и т.д. Решение о целесообразности оперативного лечения принимается совместно лечащим кардиологом, кардиохирургом, врачами других специальностей (при необходимости).
Лечение дефекта межпредсердной перегородки
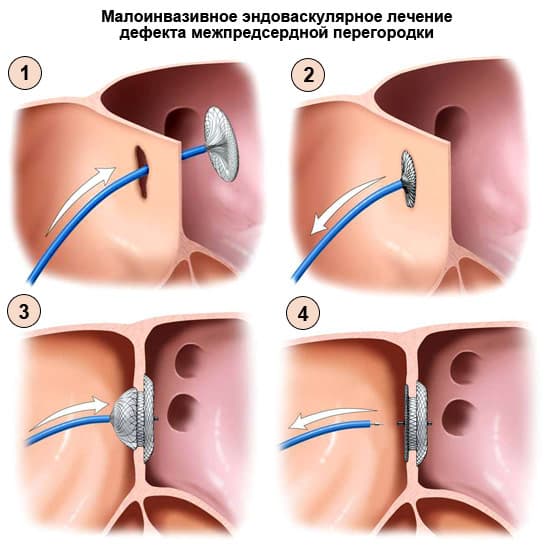
На данный момент существует два вида оперативного лечения:
- 1. Операция на открытом сердце в условиях искусственного кровообращения с ушиванием дефекта или его пластикой заплатой из перикарда.
- 2. Устранение дефекта межпредсердной перегородки с использованием специальных устройств (окклюдеров) в условиях рентгеноперационной через проколы артерий без стернотомии.
- Необходимо понимать, что не каждый дефект может быть устранен оперативным путем, существуют противопоказания к операции (дефекты малого диаметра, тяжелая легочная гипертензия, право-левый сброс через дефект), и не каждый дефект может быть устранен с использованием оккклюдеров (сочетание дефекта с аномальным дренажом легочных вен, первичные дефекты с отсутствующим нижним краем, дефекты большого размера, сочетание дефекта с другой
- патологией сердца являются показанием к открытой операции).
- Более подробно о конкретном случае заболевания, показаниях и противопоказаниях можно узнать в процессе консультации сердечно-сосудистого хирурга (на амбулаторном приеме).
Оформите заявку на сайте, мы свяжемся с вами в ближайшее время и ответим на все интересующие вопросы.
Читайте также: