Возможности реабилитации пациентов при помощи дентальных имплантатов реферат
Обновлено: 05.07.2024
В. И. Шемонаев
к. м. н., доцент, заведующий кафедрой ортопедической стоматологии Волгоградского государственного медицинского университета
Д. В. Ильин
к. м. н., ассистент кафедры ортопедической стоматологии ВолГМУ
О. Г. Полянская
к. м. н., ассистент кафедры ортопедической стоматологии ВолГМУ
Е. В. Власова
студентка стоматологического факультета ВолГМУ
Введение
Полное отсутствие зубов обусловливает нарушения здоровья вплоть до окончательной утраты жизненно важной функции организма — пережевывания пищи. Это сказывается на процессе пищеварения и поступлении в организм необходимых питательных веществ, а также служит причиной развития заболеваний желудочно-кишечного тракта. Вследствие потери зубов нарушается дикция, что сказывается на коммуникационных способностях пациента. Эти нарушения вместе с изменением внешности вследствие утраты зубов и развивающейся атрофии жевательных мышц могут обусловить изменения психоэмоционального состояния, вызывающие расстройства психики.
Отсутствие зубов становится одной из причин развития таких осложнений, как дисфункции височно-нижнечелюстного сустава, и соответствующего болевого синдрома [1].
Протезирование при полном отсутствии зубов представляет собой одну из сложнейших проблем ортопедической стоматологии. Решение этой проблемы возможно только при комплексном изучении причин нарушения функции и анатомии жевательного аппарата, которые приводят к полной утрате зубов.
Учеными были изучены закономерности строения зубочелюстного аппарата, которые легли в основу методов ортопедического лечения при потере всех зубов и учения о протезировании беззубых челюстей.
Протезирование челюстей при полном отсутствии зубов, по мнению В. Ю. Курляндского (1955), состоит из трех взаимозависимых положений:
— фиксация и стабилизация протезов на беззубых челюстях;
— определение необходимой, строго индивидуальной величины и формы протезов для восстановления внешнего вида лица;
— конструирование зубных рядов в протезах для синхронной работы всех органов челюстно-лицевой области, участвующих в обработке пищи, речи, дыхании.
Фиксация съемного протеза во рту обеспечивается механическими (пружины Фошара, утяжеление базисов протезов на нижнюю челюсть), биомеханическими (десневые кламмеры и пелоты), физическими (присоски Рауэ), биофизическими (основан на образовании разряженного пространства по всей поверхности протезного ложа за счет использования анатомических особенностей слизистой оболочки протезного ложа и полного соответствия топографии протезного ложа и базиса протеза) методами.
Улучшения условий протезного ложа можно добиться путем проведения хирургических операций. Ученые пытались увеличить объем атрофированного альвеолярного отростка путем ауто-, гомо-, гетеро- и аллопластики. Г. Б. Брахман подсаживала под надкостницу кусочки трупного хряща или имплантатов из пластмассы АКР-9 или ЭГмасс-12 для формирования альвеолярного отростка в местах наибольшей атрофии тела нижней челюсти.
Были попытки использования магнитных аттачментов, однако они требуют большего пространства, чем замки в виде шарика и муфты, и их фиксирующие силы нельзя регулировать. К тому же магниты не стабилизируют протез против горизонтальных, сдвигающих сил. В результате это приводит к недостаточной фиксации протеза и быстрой стираемости магнитов.
Многочисленные долговременные исследования показали, что лечение при помощи зубных имплантатов может обеспечивать пациентов с полной адентией более устойчивой альтернативой полным зубным протезам, восстанавливая как функцию, так и эстетику, подобно естественному зубному ряду [2]. Внедрение в клиническую практику системы мини-имплантатов существенно расширило показания к применению дентальных имплантатов, дало возможность их использования у пожилых людей, в детской практике, в сложных клинических ситуациях [1, 3, 4].
В конце 90-х годов XX века американским стоматологом В. И. Сендаксом был предложен метод комплексной реабилитации пациентов с полным отсутствием зубов с использованием мини-имплантатов. Суть ее в следующем.
Мини-имплантат представляет собой имплантат небольшого диаметра (диаметр — 1,8 мм, 2,4 мм; длина — 10 мм, 13 мм, 15 мм, 18 мм) из титанового сплава. О-образное резиновое кольцо, входящее в кольцевой аттачмент, устанавливается в базис съемного протеза, обхватывает и удерживает шаровидную головку мини-имплантата (рис. 1, 2).
Рис. 1. Реализация системы мини-имплантатов в съемном протезе на нижнюю челюсть. Рис. 2. Составные элементы системы мини-имплантатов: металлический кольцевидный аттачмент с О-образным резиновым кольцом, который устанавливается в базис протеза.
Это обеспечивает надежную фиксацию и стабилизацию съемного протеза.
Основные сложности при зубной имплантации возникают у пациентов с атрофированными альвеолярными отростками. Плохие условия для имплантационной хирургии и последующего протезирования имеются также при неравномерности атрофических процессов в челюстях, происходящих чаще в вертикальном и переднезаднем направлениях, а также увеличении расстояния между альвеолярными дугами и уменьшении их ширины.
Небольшой диаметр мини-имплантатов позволяет установить их при этих неблагоприятных условиях в кости. Форма сферы внеальвеолярной части мини-имплантатов позволяет добиться надежного соединения посредством О-образного резинового кольца. Это позволяет улучшить устойчивость протеза, его функциональность, а также фонетику пациента.
Минимально инвазивные процедуры и методики становятся быстрорастущим и развивающимся сегментом медицинской индустрии. Исследования и разработка направлены на создание более маленьких инструментов и составляющих систему компонентов. Мини-имплантаты — идеальный пример этих тенденций. Они сильно расширяют спектр пациентов, которым может быть предписана и проведена эта процедура.
К преимуществам системы относятся: минимальное вмешательство в области мягких тканей и кости; упрощенный, щадящий протокол операции, требующий минимального количества инструментов. Не требуется откидывания лоскута — для установки необходимо пройти слизистую дрилем и наметить направляющую в кости. Малый размер и форма позволяют устанавливать эти имплантаты, следуя более простому протоколу. Таким образом, в целом наносится минимальная травма мягким тканям и кости.
Под инфильтрационной анестезией на нижней челюсти в промежутке между ментальными отверстиями, отступая от них 3 мм, устанавливаются 4 имплантата (минимальное количество), по рекомендации-фирмы производителя это можно сделать без дополнительных методов исследования (рис. 3а). На верхней челюсти предварительно проводится рентгеновское обследование и исходя из полученных данных выбирается количество и место для установки имплантатов. Без разреза, через слизистую оболочку, хирургическим сверлом делается отверстие только в компактном слое кости (рис. 3б). После этого достается имплантат из стерильной упаковки и внедряется в костную ткань до появления напряжения (рис. 3в, г).
Рис. 3а. Протокол ведения операции: маркером намечаются места внедрения мини-имплантатов; Рис. 3б. Протокол ведения операции: через слизистую оболочку в намеченных местах сверлом проходится компактный слой кости. Рис. 3 в. С помощью набора ключей внедряются под напряжением мини-имплантаты.
Рис. 3г. С помощью набора ключей внедряются под напряжением мини-имплантаты.
В протезе пациента фрезой делаются углубления в проекции имплантатов. Из стерильной упаковки достается ответная часть, представляющая собой полусферу с силиконовым кольцом внутри (рис. 4а). Методом прямой перебазировки в полости рта эти супраструктуры переходят в протез (рис. 4б). Протез шлифуется, полируется, накладывается в полости рта (рис. 4в, г).
Рис. 4а. Этапы фиксации в полости рта на мини-имплантатах матричной части с резиновым кольцом внутриротовой и клинической перебазировки жестким материалом: установка кольцевидных аттачментов на мини-имплантаты, предварительно изолировав шейки. Рис. 4б. Нанесение материала на базис съемного протеза на нижнюю челюсть (предварительно припасованного и обработанного адгезивом. Рис. 4в. Вид полных съемных протезов в полости рта после клинической перебазировки, шлифовки и полировки.
Рис. 4г. Вид полных съемных протезов в полости рта после клинической перебазировки, шлифовки и полировки.
Результаты и обсуждение
Нами было обследовано и проведено комплексное лечение с установкой мини-имплантатов 32 пациентам в возрасте от 56 до 82 лет с полным отсутствием зубов. Исследование направлено на изучение степени фиксации, стабильности съемных протезов в зависимости от использования различных материалов (как мягких, так и твердых материалов для внутриротовой перебазировки). Для этого применялся метод опроса, анкетирования пациентов, где они оценивали по балльной шкале эффективность жевания, адгезию мягких материалов, удобство ухода и пользования, стабильность протезов.
Также тремя независимыми врачами-стоматологами оценивалось состояние мини-имплантатов в различные сроки: 1, 3, 6 месяцев — в зависимости от использования различных видов материалов. Система мини-имплантатов была установлена на верхнюю челюсть у 6 пациентов, на нижнюю челюсть — у 22, на обе челюсти — у 4. На верхнюю челюсть устанавливали 6, на нижнюю — 4 мини-имплантата (рис. 5), связано это было со строением костной ткани, анатомическими особенностями, наличием лунок удаленных зубов.
Рис. 5. Варианты установки мини-имплантатов на верхнюю и нижнюю челюсти.
Передача жевательной нагрузки через мягкую прокладку полных съемных протезов является временным этапом ортопедического лечения, поэтому разные материалы этой группы имеют свои особенности и специфические свойства: по отношению к базисам протезов, к удержанию втулок замковых креплений, проникновению пищевых красителей, гигиенической обработке, эффективности жевания.
На основании анкет пациентов адгезия к базисным пластмассам съемных протезов была лучше и продолжительнее у следующих материалов: IMTEC (3M) Secure Soft — 7,6 балла, GC Reline Ultra Soft — 7,2 балла: не наблюдалось отхождения краев, материалы плотно прилегали на всем протяжении протезов, хорошо фиксировали втулки, коррекций не требовалось. Результаты других мягких материалов: Sofreliner S Soft — 3,2; GC Reline Extra Soft — 2,7; GC Reline Soft — 5,6.
Лучшую стабильность протезов и эффективность при жевании пациенты отметили при использовании следующих материалов: мягкие — GC Reline Ultra Soft, 7,2 балла, IMTEC (3M) Secure Soft, 6,5; жесткие — IMTEC (3M) Secure, 9,2 балла, REBASE II fast, 9,4; худшие данные: Sofreliner S Soft — 2,3; GC Reline Extra Soft — 2,1; GC Reline Soft — 4,2, — хотя к этим материалам у пациентов с резко выраженной атрофией альвеолярных отростков адаптация происходила лучше и быстрее, по их ощущениям.
Удобство пользования и гигиенического ухода пациенты отмечали с мягким материалом GC Reline Ultra Soft — 8,3 балла — и жесткими: IMTEC (3M) Secure — 8,7; REBASE II fast — 9,5. При использовании других материалов (Sofreliner S Soft — 3,1 балла; GC Reline Extra Soft — 1,7; GC Reline Soft — 3,6) пациенты испытывали трудности при наложении съемных протезов из-за плохой фиксации матричных частей (втулок с О-образными резиновыми кольцами) в самих протезах.
Гигиенический уход был осложнен плохой адгезией к базису протезов: уже через 2-3 недели эти материалы отрывались, отслаивались частично или полностью, изменялись в цвете.
Мы применяли мягкую выстилку съемных протезов в среднем от 1 до 3 месяцев, после чего делали постоянную перебазировку съемных протезов жесткими видами материалов. Независимым врачам-стоматологам предлагали оценить состояние имплантатов по нескольким показателям: устойчивость; перкуссия; пальпация; воспалительные явления десневого края; болезненные ощущения.
При оценке устойчивости мини-имплантатов через 1 неделю отмечали подвижность 2 мини-имплантатов в вестибулооральном и медиодистальном направлениях, где мы применяли материалы средней жесткости GC Reline Soft. После переустановки локально в этой области применяли выстилку самым мягким материалом из нашего обзора Sofreliner S Soft. Несмотря на то что в отношении фиксации и стабилизации протезы были хуже в сравнении с другими материалами, спустя 4 недели подвижности этих мини-имплантатов специалисты не отмечали. В последующем мы успешно применили сначала материал GC Reline Ultra Soft, затем жесткий IMTEC (3M) Secure и REBASE II fast.
Рис. 7. После купирования воспалительных явлений мини-имплантаты стабильны, слизистая в норме.
Заключение
Система мини-имплантатов MDI является доступным, альтернативным, весьма эффективным методом комплексного лечения пациентов с полной адентией, позволяющим качественно повысить уровень их жизни. Простота этой процедуры очевидна, особенно для практикующего врача, который имеет опыт работы с имплантатами. Вся операция по установке мини-имплантатов для стабилизации нижнего протеза может занять менее двух часов и происходить в одно посещение. Если пациент пришел со своим протезом, не требуется даже подключения лаборатории для переработки или изготовления нового протеза.
Исследование динамики структурных изменений в костном аутотрансплантате на границе "кость-имплантат" при пересадке имплантатов из никелида титана. Разработка основных показаний к дентальной имплантации после костнопластических операций на челюстях.
| Рубрика | Медицина |
| Вид | автореферат |
| Язык | русский |
| Дата добавления | 13.01.2018 |
| Размер файла | 434,7 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
На правах рукописи
диссертации на соискание ученой степени
доктора медицинских наук
ОРТОПЕДИЧЕСКАЯ РЕАБИЛИТАЦИЯ БОЛЬНЫХ НА ДЕНТАЛЬНЫХ ИМПЛАНТАТАХ ПРИ КОСТНОЙ ПЛАСТИКЕ ЧЕЛЮСТЕЙ
ЖЕЛЕЗНЫЙ СЕРГЕЙ ПАВЛОВИЧ
доктор медицинских наук, профессор Сысолятин Павел Гаврилович, Заслуженный деятель науки РФ
доктор медицинских наук, профессор Семенюк Владимир Михайлович, Омская государственная медицинская академия Росздрава (г.Омск)
доктор медицинских наук, профессор, Тупикова Людмила Николаевна, Алтайский государственный медицинский университет (г.Барнаул)
Автореферат разослан 2009 г.
Ученый секретарь диссертационного совета Недосеко В.Б.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. В настоящее время костная пластика дефектов челюстей прочно вошла в практику лечебных учреждений страны и широко используется при лечении опухолей, диспластических процессов, врожденных и приобретенных дефектов различной этиологии.
Цель исследования. Повышение эффективности стоматологической ортопедической реабилитации больных после костнопластических операций на челюстях с использованием дентальных имплантатов.
В клинике изучить сроки формирования органотипичного регенерата при различных видах костнопластических операций на челюстях с проведением дентальной имплантации.
Изучить нуждаемость больных в ортопедическом лечении с использованием дентальных имплантатов после костнопластических операций в челюстно-лицевой области
Разработать показания к дентальной имплантации после костнопластических операций на челюстях.
Разработать методику дентальной имплантации при первичной, и отсроченной костной пластике дефектов челюстей, пересадке в сформированный костный регенерат и при синус-лифтинге с костной пластикой
Определить показания к применению различных видов ортопедических конструкций с использованием дентальных имплантатов после костной пластики дефектов челюстей
Определить сроки ортопедической реабилитации с использованием дентальных имплантатов у больных с дефектами зубных рядов после костнопластических операций на челюстях.
Изучить ближайшие и отдаленные результаты ортопедического лечения с использованием дентальных имплантатов у больных с дефектами зубных рядов после костнопластических операций на челюстях.
Изучить характер и частоту осложнений дентальной имплантации у больных с остеопластическим замещением дефектов челюстей.
Разработать методику прогнозирования эффективности ортопедической реабилитации больных на дентальных имплантатах при костной пластике челюстей
Научная новизна. Впервые в эксперименте установлено, что при свободной пересадке костного аутотрансплантата в сочетании с внутрикостными имплантатами в дефект нижней челюсти наблюдается интеграция внутрикостных имплантатов в формирующийся органотипичный костный регенерат.
Впервые установлено, что дентальные имплантаты не влияют на сроки формирования регенерата, в большей степени они зависят от характера и размеров дефекта, вида костнопластической операции.
Выявлено, что нуждаемость в ортопедическом лечении после костнопластических операций при дефектах челюстей составляет 100%, при этом у 65,61% больных показано изготовление съемных протезов и у 34,39% больных - несъемных конструкций.
Впервые показано, что использование дентальных имплантатов после костной пластике челюстей в качестве опоры расширяет возможности к применению несъемного протезирования до 94,47% наблюдений.
Впервые разработаны показания и методики непосредственной дентальной имплантации при ауто- и аутоаллотрансплантации, отсроченной дентальной имплантации в сформированный костный регенерат.
Впервые определены сроки начала протезирования при различных видах костнопластических операций и показания к использованию тех или иных видов конструкций зубных протезов с опорой на дентальные имплантаты у больных с полной или частичной адентией при костной пластике дефектов челюстей.
Впервые изучены результаты протезирования дефектов зубных рядов на дентальных имплантатах после костно-реконструктивных операций и доказана высокая эффективность ортопедического лечения, позволяющего у большинства больных использовать более функциональные несъемные виды зубных протезов. аутотрансплантат никелид титан костнопластический
Впервые изучен характер и частота осложнений при ортопедическом лечении на дентальных имплантатах после костной пластики челюстей и показано, что наиболее часто к отрицательному результату приводит возникновение воспалительного процесса в периимплантатных тканях и отсутствие остеоинтеграции имплантата.
Впервые, на основании анализа субъективных и объективных данных, частоты и характера осложнений разработана методика прогнозирования эффективности ортопедической реабилитации на дентальных имплантатах после костной пластики челюстей.
Практическая значимость работы.
Использование дентальных имплантатов при устранении дефектов челюстей костными трансплантатами расширяет возможности ортопедической реабилитации больных. Дентальные имплантаты целесообразно применять для пересадки в костный регенерат, сформировавшийся на месте костного трансплантата, сочетать свободную пересадку костного аутотрансплантата и васкуляризированной кости вместе с дентальными имплантатами для устранения дефектов нижней челюсти, а также при поднятии дна верхнечелюстной пазухи с костной пластикой.
Дентальная имплантация при костной пластике дефектов челюстей позволяет расширить показания к несъемному протезированию дефектов зубных рядов и обеспечивает более высокие результаты ортопедического лечения.
Положения, выносимые на защиту:
Пересадка свободного костного аутотрансплантата в дефект нижней челюсти в сочетании с внутрикостными имплантатами сопровождается интеграцией имплантатов с формированием органотипичного регенерата. Оптимальная остеоинтеграция обеспечивается при пересадке имплантатов из никелида титана с проницаемой пористостью за счет формирования костных структур в порах.
Разработанные виды дентальной имплантации при свободной первичной и отсроченной костной ауто- и аллотрансплантации, отсроченной дентальной имплантации в сформированный регенерат могут успешно использоваться при ортопедическом лечении больных с дефектами зубных рядов.
Ортопедическое лечение больных проводится после полной интеграции имплантатов в регенерат при восстановлении плотности костной ткани, подтвержденной остеоденситометрией: при свободной костной пластике - через 6-12 месяцев, при пересадке кости на микрососудистых анастомозах, при синус-лифтинге и при дентальной имплантации в сформированный регенерат - через 2-4 месяца.
Использованием дентальных имплантатов при ортопедической стоматологической реабилитации больных после костной пластики челюстей позволяет использовать несъемные конструкции зубных протезов, что улучшает результаты ортопедического лечения дефектов зубных рядов.
Публикации. По теме диссертации опубликовано 48 работ, в том числе издано 2 монографии и 2 учебно-методических пособия для студентов и врачей, 11 работ опубликовано в изданиях, рекомендованных ВАК РФ.
Объем и структура диссертации. Диссертация изложена на 263 страницах, состоит из введения, обзора литературы, 4 глав собственных исследований, выводов, практических рекомендаций и списка литературы. Работа иллюстрирована 76 рисунками, 22 таблицами. Список литературы содержит 331 источник (236- отечественных и 95- иностранных авторов).
Материал и методы исследования.
В экспериментальной части проведены экспериментальные исследования на животных, цель которых заключалась в изучении интеграционных возможностей различных видов внутрикостных имплантатов при костной пластике нижней челюсти. Использовались: макроскопический, рентгенологические (рентгенография и остеоденситометрия), морфологический методы, проводилось изучение шлифов имплантатов с прилегающими структурами и статистическая обработка результатов.
Для проведения эксперимента было использовано 4 вида имплантатов: никелид-титановый с проницаемой пористостью, титановый с винтовой резьбой, титановый с гладкой поверхностью и углеродситаловый с гладкой поверхностью. В эксперименте использовались 16 беспородных собак массой 20-25 кг. Под внутримышечным наркозом подчелюстным доступом скелетизировалось тело нижней челюсти от угла кпереди на 55,0-65,0 мм. С помощью дисковых пил и фрез наносились горизонтальные и вертикальные распилы и иссекался фрагмент кости размером 7,5-10,0 х 40,0-50,0 мм, в результате чего формировался краевой дефект нижней челюсти. В изъятом фрагменте нижней челюсти цилиндрической фрезой создавали 4 вертикальных отверстия диаметром 2,5 мм и длиной 4,0-5,0 мм. В эти отверстия плотно внедряли все 4 вида имплантатов. Фрагмент резецированной кости с помещенными в него имплантатами реплантировали в дефект нижней челюсти и фиксировали к костному ложу проволочными швами. Рану ушивали наглухо кетгутом, шелком.
Животных выводили из опыта в сроки: 1, 3, 6, 9 и 12 месяцев. После изъятия тела нижней челюсти макроскопически определяли спаянность трансплантата с ложем, наличие подвижности, характер поверхности, наличие границы соединения с костным ложем.
После рентгенологического исследования из макропрепарата нижнечелюстной кости иссекали участки кости вместе с имплантатами. Полученные фрагменты размером 10,0Ч20,0 мм фиксировали в 10% растворе нейтрального формалина. Блоки декальцинировали в 10% азотной кислоте, проводили через спирты различной крепости и заливали в целлоидин. Из блоков готовили тотальные срезы, которые окрашивали гематоксилин-эозином и по Ван Гизону и исследовали с помощью светового микроскопа. Микроскопически определялось наличие соединительной и остеогенной ткани, прирост или убыль костной ткани вокруг имплантатов, динамику остеогенных процессов в течение всего периода наблюдения. Морфологические исследования экспериментального материала проводили в лаборатории патоморфологии НИИТО МЗ и СР РФ (руководитель - д.м.н., профессор А.М.Зайдман).
Цель клинических исследований заключалась в изучении возможностей протезирования на имплантатах при костно-реконструктивных хирургических вмешательствах в челюстно-лицевой области. Проводилось клиническое обследование, рентгенологические исследование (прицельная дентальная рентгенография, ортопантомография, спиральная компьютерная томография с 3D моделированием и остеоденситометрия), функциональные пробы по И.С.Рубинову, опрос по анкете Г.Слэйда-К.МакГрата (1997). Проводилась статистическая обработка данных.
На протяжении с 1996 по 2007 годы в клинике были проведены костно-реконструктивные операции в челюстно-лицевой области у 311 больных в возрасте от 16 до 68 лет. В дальнейшем изучение результатов дентальной имплантации и протезирования с опорой на имплантаты проведено у 265 больных. 46 пациентам, у которых, или развились осложнения, или по другим обстоятельствам (отсутствие мотивации, смена места жительства и т.п.), протезирование не проводилось.
Наиболее часто реконструктивные вмешательства проводились по поводу доброкачественных опухолей, опухолевидных образований, кист челюстей, послеоперационных и посттравматических дефектов.
Из доброкачественных опухолей наиболее часто встречались амелобластома, остеобластокластома и фиброзная дисплазия (145 наблюдений), реже другие новообразования и кисты челюстей. При отсроченной костной пластике замещались дефекты, образовавшиеся после огнестрельных ранений, переломов челюстей, секвестрэктомии и удаления опухолей. У больных имели место дефекты нижней челюсти с нарушением ее непрерывности, размеры которых по протяженности составляли от 4 до 16 см.
Реконструкция челюстей костными трансплантатами у 103 больных проводилась при наличии концевых дефектов альвеолярного отростка верхней челюсти, тела и ветви нижней челюсти, у 56 - сегментарных включенных дефектов челюстей и у 106 пациентов проведена остеопластика в ходе операции поднятия дна гаймровой пазухи. Показанием к синус-лифтингу и одномоментной костной пластике служило недостаточное количество костной ткани альвеолярного отростка в области верхнечелюстной пазухи для введения имплантата. Во всех случаях использовали открытый синус-лифтинг.
В качестве пластического материала использовали аутокость и аутоаллокость.
В качестве аутотрансплантата наиболее часто использовали гребень подвздошной кости и ребра больных, реже трансплантаты из подбородочного отдела, ретромолярной области и альвеолярной части челюстей, а также остеоиндуктивный метериал PRP или FRP. У 22 больных аутогребень пересаживался в дефект челюсти на микрососудистых анастомозах.
Аллогенные консервированные трансплантаты в сочетании с аутокостью использовали у 77 пациентов.
Аллотрансплантаты забирали от трупов-доноров из нижнечелюстной кости, гребня подвздошной кости, больших трубчатых костей и ребер. Сроки консервации используемых костных аллотрансплантатов не превышали 3 месяцев.
Аллотрансплантаты получали в лаборатории консервации и пересадки тканей Новосибирского научно-исследовательского института травматологии и ортопедии МЗ и СР. Трансплантаты консервировали замораживанием при -25єС; в слабых (0,25-0,5% растворах) формалина.
Из таблицы 1 видно, что у 265 больных при проведении костной пластики дефектов челюстей было использовано 579 дентальных имплантатов. Наибольшую группу составили больные пятой группы, которым проводилась операция синус-лифтинга с одномоментной костной пластикой (106 пациентов) им проведена пересадка 186 дентальных имплантатов.
Таблица 1 - Характер оперативных вмешательств и вид дентальных имплантатов при реконструктивных вмешательствах в челюстно-лицевой области
Дентальная имплантация является достаточно прогрессивной отраслью стоматологии, в которой продолжают успешно развиваться достойные альтернативы классическим конструкциям дентальных имплантатов, как, например, таковые, изготовленные из высокопрочной керамики (внутрикостные опоры на основе диоксида циркония). Благодаря своим эстетическим характеристикам и биосовместимости цирконий лучше взаимодействует с окружающими мягкими тканями, и более точно имитирует структуру естественного зуба. Циркониевые структуры также способствуют поддержке достаточно высокого уровня пародонтологического здоровья и позволяют снизить риск аккумуляции бактериальных контаминантов в участках, контактирующих с основой керамических имплантатов. Последние представляют собой достойную альтернативу классическим металлическим опорам из титана в ходе реабилитации пациентов с частичной адентией. На сегодняшнее время у стоматологических пациентов уже есть возможность выбора материала, из которого потенциально может быть изготовлена та или иная составляющая протеза.
В данной статье мы опишем протокол работы с керамическими имплантатами, используемыми в качестве опор одиночных коронок и мостовидных протезов, и продемонстрируем характер их взаимодействия с окружающими тканями. Также мы проанализируем сходства естественных зубов и керамических имплантатов.
Клинический случай 1. Установка и шинирование нескольких керамических имплантатов
Пациент обратился за стоматологической помощью с множественными переломами корней, очагами вторичного кариеса, и потребностью в проведении процедур удлинения клинической коронки, эндодонтического лечения, восстановления зубов при помощи культевых конструкций, и конечной реабилитации при помощи несъемных ортопедических реставраций. Пациент понимал весь объем предстоящий работы и был настроен на достижение надлежащего долгосрочного результата. Ему было предложено два варианта материалов, из которых могли быть изготовлены дентальные имплантаты, используемые в качестве опор, и он согласился на применение керамических конструкций.
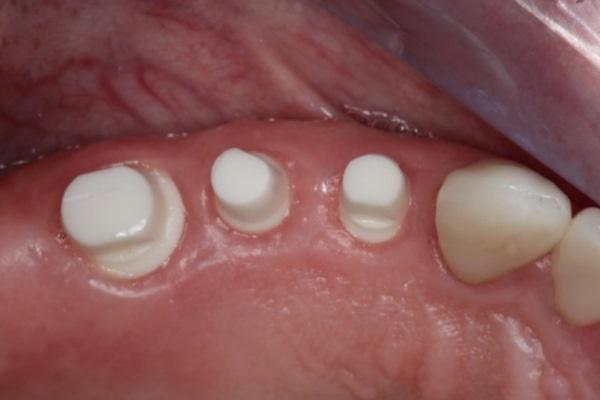
На фото 1-2 изображена ситуация до лечения с последующим удалением трех дистальных зубов и немедленной установкой циркон-оксидных керамических имплантатов, которую выполняли одновременно с мягкотканной аугментаций посредством фибрина, обогащенного тромбоцитами (PRF). Зубы были удалены атравматически без наложения швов. Поскольку керамические имплантаты являются монолитными (имплант соединен с абатментом в единую конструкцию), было принято решение зашинировать все конструкции, дабы минимизировать негативный эффект латеральных сил, действующих во время жевания, глотания и движений языка.
Фото 1. Фото до вмешательства.
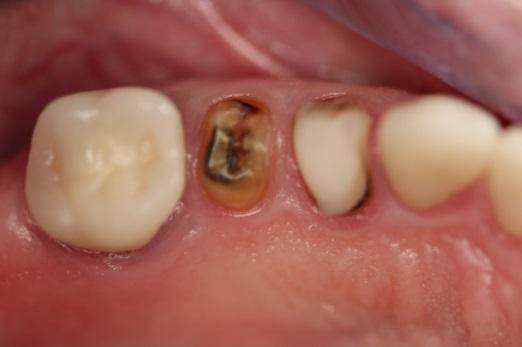
Фото 2. Экстракция зубов и установка керамических имплантатов.
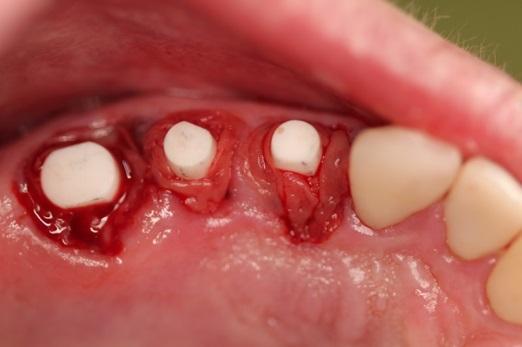
На фото 3-5 продемонстрировано процесс соединения трех внутрикостных опор при помощи фотополимеризующейся пластмассы и текучего композита. Установленная шина находилась вне окклюзионных взаимодействий на период последующих 12 недель. Пациент был проинформирован о потребности пережёвывать пищу на противоположной стороне на период этих 12 недель. После удаления шины окружающие мягкие ткани демонстрировали оптимальный профиль, имплантаты были окружены полностью кератинизированной слизистой, состояние которой полностью соответствовало состоянию здорового пародонта (фото 6-7).
Фото 3. Провизорная шина.
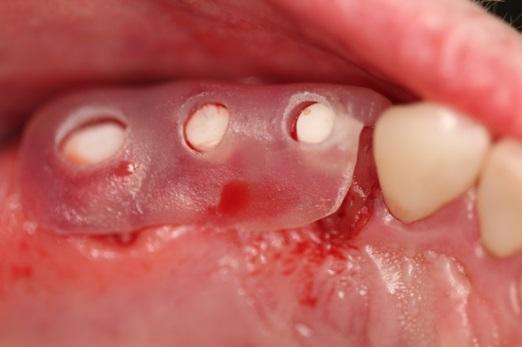
Фото 4. Фиксация шины при помощи текучего композита.
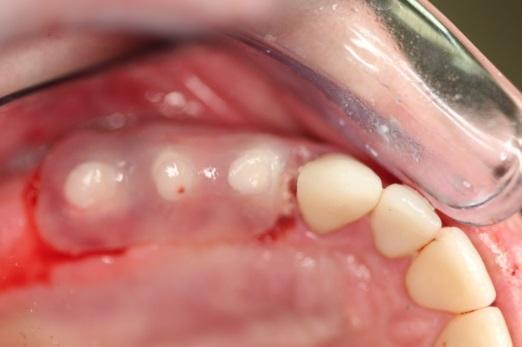
Фото 5. Латеральный вид шины.
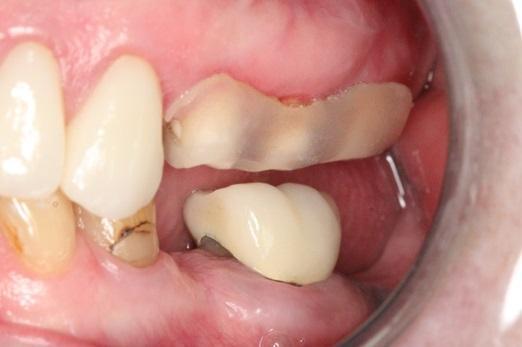
Фото 6. Вид после удаления провизорной шины.
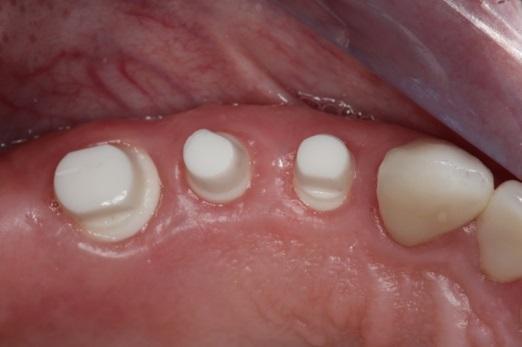
Фото 7. Вид через 12 месяцев после операции.
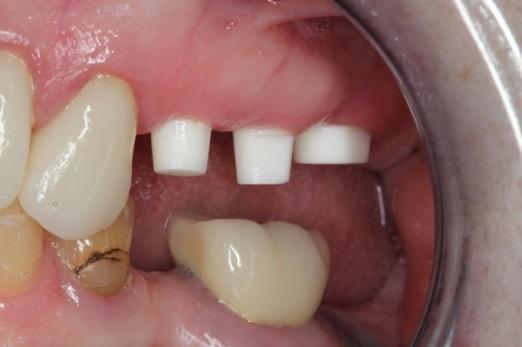
В некоторых случаях отмечается корональная миграция тканей десен относительно уровня установленных имплантатов из-за биосовместимости керамических опор. В подобных случаях для ретракции или коррекции положения слизистой можно использовать нити или же разные типы лазеров для гингивоэктомии. Если же уровень имплантата находиться выше уровня десен, то при помощи специального высокоскоростного бора можно приступить к формированию уступа под будущие коронки.
В принципе, подготовка керамических имплантатов под коронки после 12-16 месячного периода их остеоинтеграции, никак не отличается от подготовки естественных зубов. Врач лишь может выбрать протокол менеджмента окружающих мягких тканей во время получения окончательного оттиска. На рентгенограммах, изображенных на фото 8 и 9, показано достаточный объем окружающих твердых и мягких тканей, который удалось сохранить благодаря атравматическому характеру вмешательства, исключительной биосовместимости керамических опор и использованию биопрепарата PRF после атравматической экстракции.
Фото 8. Рентгенограмма до лечения.
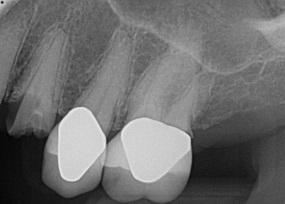
Фото 9. Рентгенограмма через 12 месяцев после установки имплантатов.
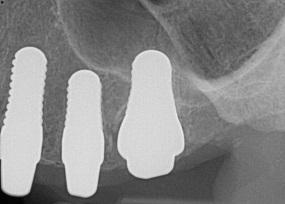
Клинический случай 2. Восстановление зубного ряда с применением керамических дентальных имплантатов
Часто стоматологу приходиться одновременно восстанавливать не только беззубые участки челюстей, но и отдельные зубы с достаточно компрометированным состоянием. После разработки плана лечения и его согласования с пациентом, врач приступает к изготовлению восковых диагностических моделей будущих реставраций, опирающихся как на собственные зубы, так и керамические имплантаты, дабы потом изготовить временные конструкции и уже с ними приступить к последующим этапам реабилитации. Провизорные коронки позволяют сформировать необходимый контур десен, обеспечивают незначительное давление на окружающие твердые и мягкие ткани, и главное – предоставляют возможность пациенту согласовать все необходимые, на его взгляд, коррективы с лечащим врачом до изготовления окончательных вариантов протетических реставраций. Стоматолог также имеет возможность апробировать разные окклюзионые схемы и соотношения, корректируя паттерн взаимодействия зубов-антагонистов на временных коронках.
Фото 10. Ортопантомограмма до установки имплантатов.
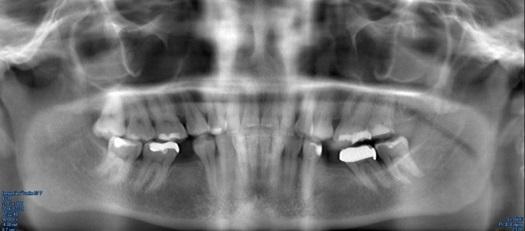
Фото 11. Вид до вмешательства.
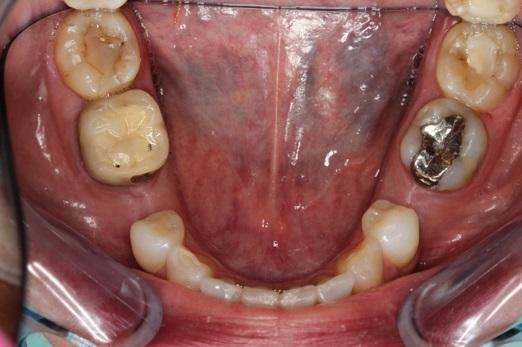
Фото 12. Вид после установки керамических имплантатов.
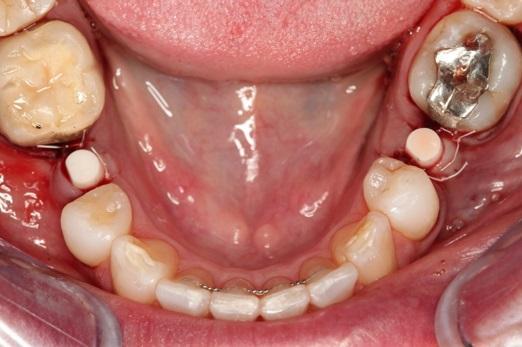
Фото 13. Латеральный вид после установки имплантатов.
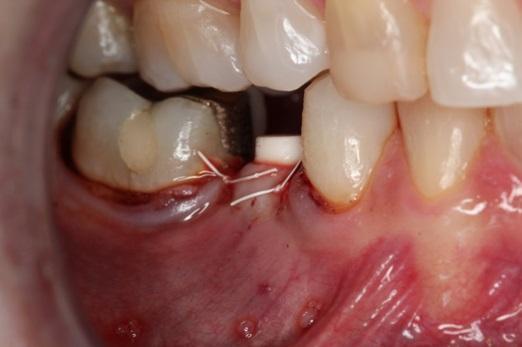
Фото 14. Вид оттисков и моделей.

Фото 15. Вид с провизорными реставрациями через 12 недель после установки имплантатов.
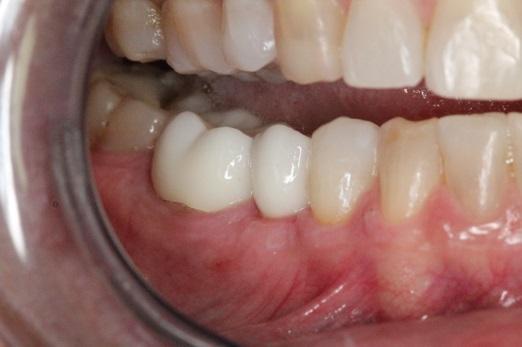
Фото 16. Вид с окончательными реставрациями (15 недель после установки имплантатов).
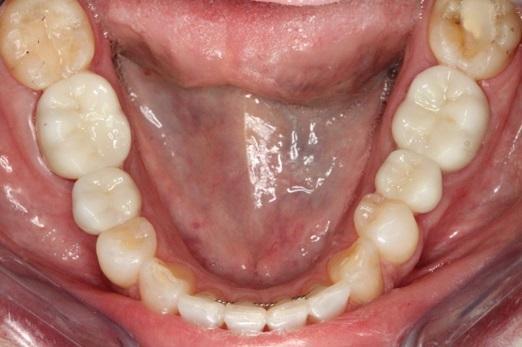
Фото 17. Рентгенограмма через 12 недель после установки имплантата.
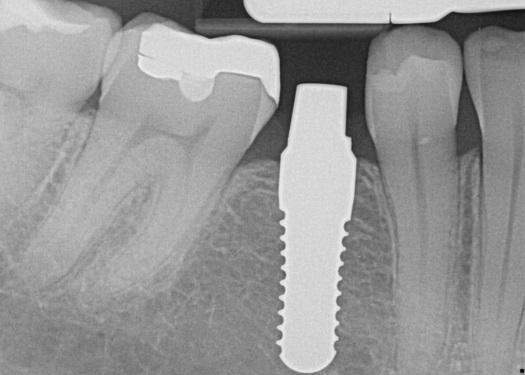
Клинический случай 3. Восстановление переднего участка верхней челюсти конструкцией на керамическом имплантате
Иногда стоматологи сталкиваются с достаточно серьезными проблемами, связанными с восстановлением зубного ряда в передних участках челюстей. В подобных случаях нужно тщательно подойти к этапу планирования, дабы максимально согласовать терапевтические возможности и ожидания пациента. На фото 18 представлен клинический случай пациентки с 3 классом междуокклюзионных соотношений и глубоким прикусом, признаками множественных абфракций и желанием восстановить участок верхнего клыка справа. После обсуждения с пациентом вопроса, касающегося потребности в тотальной реабилитации из-за окклюзионных нарушений, он констатировал имеющийся ограниченный бюджет на лечение. С учетом этого обстоятельства было проведено атравматическое удаление верхнего клыка справа (фото 19) и немедленная установка керамического дентального имплантата (фото 20). Для поддержки мягких тканей были наложены PTFE-швы, а поверх участка вмешательства устанавливали ретейнер по типу Essix. Для имитации профиля удаленного клыка использовали конструкцию композитного винира, которую фиксировали к ретейнеру (фото 21).
Фото 18. Вид до вмешательства.
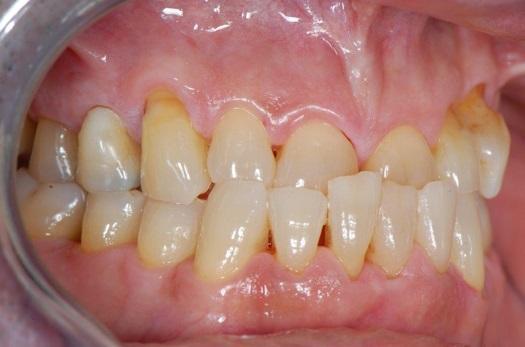
Фото 19. Атравматическая экстракция.
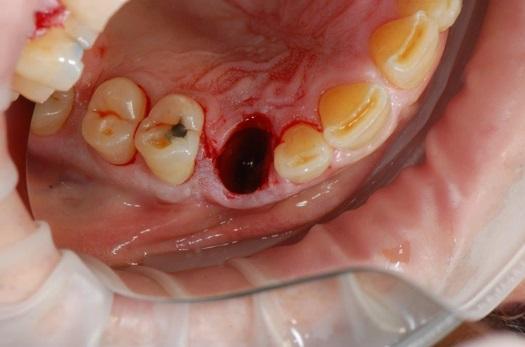
Фото 20. Установка имплантата сразу после экстракции.
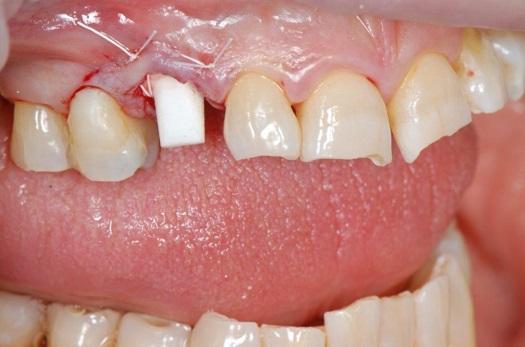
Фото 21. Внешний вид после установки провизорного ретейнера.
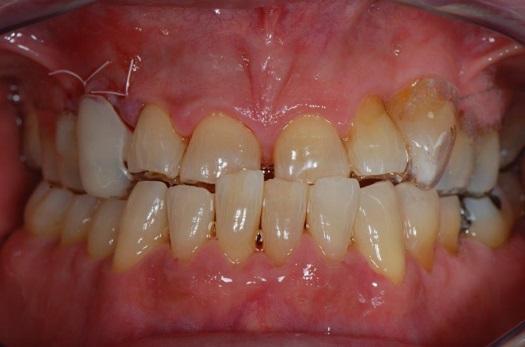
Нужно помнить, что имплантат и ретейнер не должны находиться в контакте, при этом сам ретейнер может пассивно контактировать с зубами-антагонистами. Швы были удалены через 2 недели после установки имплантата, и пациент был проинструктирован о потребности использования ретейнера на протяжении 12 недель, особенно во время приема пищи. Через 12 недель состояние мягких тканей было более чем удовлетворительным; с целью незначительной коррекции использовали метод абразивной обработки десен с последующим нанесением на область вмешательства алюминия хлорида.
На фото 23 изображен результат окклюзионной миграции окружающих мягких тканей над язычной границей керамического имплантата. Такой эффект был достигнут за счет уникальной биосовместимости керамического имплантата и особенностей его дизайна, который не предусматривает наличие интерфейса на границе винта-абатмента, а, следовательно, нивелирует риск бактериальной контаминации в данной области.
Фото 22. Вид через 12 недель после операции.
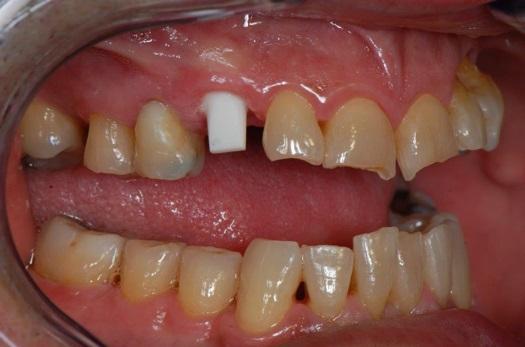
Фото 23. Вид через 12 недель после операции.
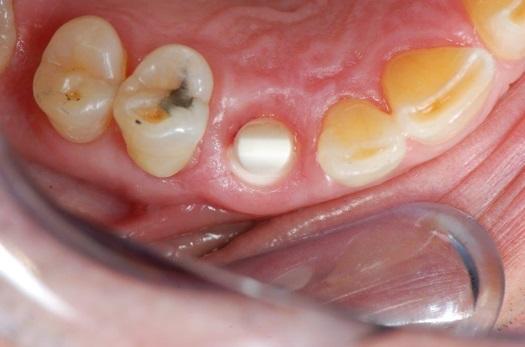
После получения оттиска были изготовлены цельнокерамические коронки. Все манипуляции от получения оттиска до фиксации коронок проводились по классическому протоколу, оригинально разработанному для препарирования собственных зубов. Через 18 месяцев в ходе контрольного визита было подтверждено здоровое состояние мягких тканей, ретенция уровня сосочка и окружающей костной ткани (фото 24-25).
Фото 24. Вид через 18 месяцев после операции.
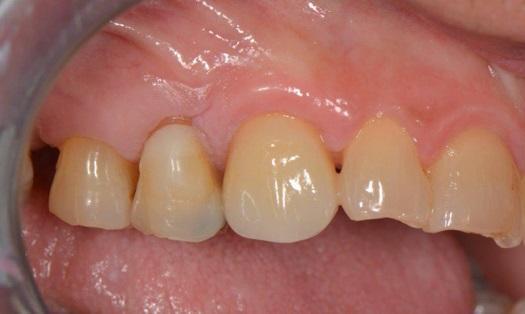
Фото 25. Ортопантомограмма через 18 месяцев после установки керамического имплантата.
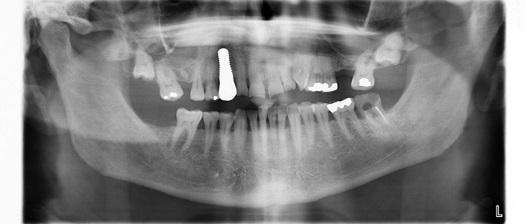
Результаты гистологических исследований
В Университете Миннесоты было проведено гистологическое исследование с участием людей для оценки характера прикрепления мягких и твердых тканей к имплантатам из диоксида циркония. Через три месяца после операции, области костной ткани вокруг опор были трепанированы, изъяты и проанализированы под микроскопом. Гистологические препараты оценивали на предмет наличия прямого контакта костной тканью с керамической поверхностью имплантата. Результаты показали значительную продолжительность контакта кости с керамическим винтом. Кроме того, окружающие мягкие ткани также демонстрировали наличие контакта с поверхностью циркония. Подобную связь удается очень редко зарегистрировать в области двухкомпонентных титановых имплантатов, поскольку интерфейс соединения таковых с абатментом находится как раз на уровне костного гребня, и является крайне чувствительным к возможности бактериальной контаминации и развитию хронического воспаления, периимплантита, и, как следствие, - к дезинтеграции. Высокопрочная керамика по типу диоксида циркония все чаще рассматривается как альтернатива металлокерамическим реставрациям и имплантатам. Цирконий является более эстетическим и биосовместимым, чем титан. Было обнаружено, что диоксид циркония лучше реагирует на мягкие ткани из-за его некондуктивной, некоррозионной поверхности, которая более резистентна к бактериальной аккумуляции.
В ходе одного из проведенных исследований два пациента согласились предоставить установленные им керамические имплантаты для гистологического анализа. Реабилитация обеих пациентов проводилась цельноциркониевыми мостовидными конструкциями через 4 месяца после установки имплантатов. Результаты исследования показали, что протравленная кислотой поверхность цельноциркониевых имплантатов, по-видимому, обеспечивает прикрепление мягких тканей и остеоинтеграцию опор уже через 3 месяца после их установки. При этом в ходе гистологического анализа не удалось идентифицировать признаков воспалительного инфильтрата, который присутствует в периимплантатной костной ткани вокруг интерфейса соединения двухкомпонентных титановых имплантатов.
На фото 26 изображены профили мягких тканей двухкомпонентного титанового имплантата и монолитного керамического имплантата. Кроме лучшего уровня прикрепления мягких тканей, керамический имплантат также характеризуется более эстетическими параметрами. Стоматолог всегда должен учитывать возможность выбора имплантатов из керамики для реабилитации пациентов с проблемным тонким биотипом мягких тканей.
Фото 26. Сравнение десневого профиля в области титанового и керамического имплантатов.
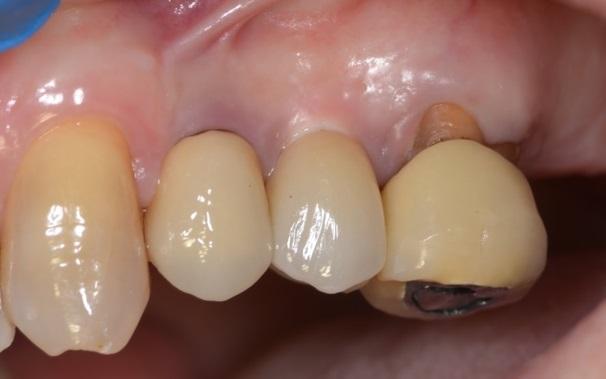
Заключение
Со временем стоматологические пациенты становятся настолько опытными, что понимают возможность выбора материала дентальных имплантатов, которые планируется использовать в ходе их реабилитации. И врач должен понимать, что кроме титановых конструкций, доступны еще и их неметаллические альтернативы. Клинические исследования керамических имплантатов установили, что такие опоры позволяют добиться меньшей потери костной ткани, формирования лучшего профиля окружающих мягких тканей и более оптимального состояния десен. Все это связано не только с биосовместимостью циркониевых имплантатов, но и с фактом отсутствия в их дизайне интерфейса соединения инфра- и супрасоставляющих ввиду монолитной структуры. Край реставраций и их фиксация на керамические имплантаты проходит на уровне слизистой, позволяя деснам сформироваться таким же образом, как и вокруг собственных зубов. Данные гистологического анализа свидетельствуют о том, что параметры остеоинтеграции керамических имплантатов ничем не хуже титановых. Пациенты, предпочитающие неметаллические конструкции, или же пациенты с гиперчувствительностью к составляющим титанового сплава, а также пациенты с высокими эстетическими ожиданиями могут свободно выбирать керамические имплантаты в качестве альтернативы обычным внутрикостным опорам в ходе комплексной реабилитации для восстановления биомеханических и функциональных возможностей зубочелюстного аппарата.
Распространенность таких патологий зубочелюстной системы, как частичное и полное отсутствие зубов, обусловливает высокую потребность в зубном протезировании среди пациентов трудоспособного возраста и составляет до 52% случаев.
Чаще всего среди дефектов зубных рядов встречаются односторонние, двусторонние дистально не ограниченные дефекты, дефекты большой протяженности и полное отсутствие зубов. Ортопедическое лечение таких дефектов с применением традиционных методов протезирования не соответствует возрастающим требованиям пациентов.
Протезирование съемными конструкциями зубных протезов во многих случаях не удовлетворяет пациентов, особенно лиц молодого возраста. По данным целого ряда исследователей, до 26% пациентов не пользуются съемными протезами.
Практически в половине случаев съемные протезы плохо фиксируются (определяется подвижность при жевании). Из всех пациентов, которые обращаются за ортопедической помощью, 86% предпочитают несъемные конструкции зубных протезов.
Последние 25 лет дентальная имплантология занимает важное место в отечественной стоматологии. Развитие данного направления становится возможным благодаря достижениям в области материаловедения и биомеханики, а также в результате изучения закономерностей биологического взаимодействия имплантатов с окружающими тканями.
На данный момент дентальная имплантация характеризуется высокой эффективностью и значительным спектром возможностей, как при замещении дефектов зубных рядов, так и в реабилитации пациентов при полном отсутствии зубов.
Ортопедическая реабилитация стоматологических больных с применением дентальных имплантатов довольно часто бывает ограниченной и сопровождается трудностями.
Прежде всего, это близкое расположение важных анатомических структур, а именно гайморовой пазухи, носовой полости, сосудисто-нервного пучка нижней челюсти.
Длительное отсутствие зубов вызывает вторичные нарушения зубочелюстной системы:
Атрофия альвеолярного отростка
Вторичные окклюзионные деформации
Патологические изменения в височно-нижнечелюстных суставах
Изменения объема верхней челюстной пазухи и другие.
Поэтому проведение дентальной имплантации в боковых отделах верхней челюсти нередко бывает затруднено в результате значительной атрофии альвеолярных отростков челюстей.
Дентальная имплантация как метод ортопедической реабилитации стоматологических больных остается одним из ведущих при замещении дефектов зубных рядов. Она направлена не только на восстановление жевательной функции, но и на получение высокого прогнозируемого результата ортопедической реабилитации.
На современном этапе эксперты в области дентальной имплантологии акцентируют внимание на минимизации продолжительности остеинтеграции за счет новейших систем имплантатов, которые обладают остекондуктивнимы свойствами, и за счет создания благоприятных условий для скорейшей остеинтеграции.
Особенности дентальной имплантации в сложных анатомических условиях
Оптимизация хирургического этапа дентальной имплантации как важной ступени подготовки пациента к протезированию существенно повышает качество и эффективность реабилитации и делает более предсказуемым и прогнозируемым результат.
Мы постараемся рассмотреть аспекты применения дентальной имплантации в сложных анатомо-топографических условиях. Изучение особенностей состояния окружающих тканей в участке имплантации, оптимизация репаративной регенерации костной ткани, взаимодействия различных белков и их соотношения, динамики тканевого ответа на имплантат обосновывают необходимость разработки оптимизированного алгоритма хирургического этапа дентальной имплантации.
Ознакомимся с размещением имплантатов в анатомических опорных структурах.
Наклонные имплантаты
Доктор Krekmanov и коллеги в оригинальном исследовании установили 138 имплантатов на 22 атрофичных альвеолярного отростка верхней челюсти. Сорок из указанных имплантатов устанавливались с наклоном в сторону синуса.
Через 6 месяцев имплантаты были раскрыты с последующим изготовлением несъемных конструкций зубных протезов. По результатам четырехлетнего периода функционирования протезов, 5 ненаклонных и один наклонный имплантат были потеряны, демонстрируя процент успеха 92.5% и 95.7% соответственно.
Эти же авторы в другом исследовании установили 75 имплантатов на 22 атрофичных верхних челюстях. 54 имплантата были наклонены, а 21 имплантат был установлен в участках челюстей с подсадкой остеопластического материала.
Три наклонных имплантата были потеряны, не достигнув остеоинтеграции, один был потерян после воздействия нагрузки. Через 18 месяцев процент успеха составил 94,7%.
Авторы предложили версию, что главные преимущества наклонных имплантатов — уменьшение плеча консоли, обеспечение повышенной кортикализации, замечательная первичная стабильность и длительное функционирование имплантата.
Perales и коллеги проводили ретроспективное исследование на 25 пациентах с установкой 101 имплантата, из которых 59 были установлены в осевой позиции и 42 наклонных.
Все пациенты были реабилитированы по изготовлению несъемных зубных протезов. Через 33 месяца наблюдения процент успеха составил 95,2% для наклонных имплантатов против 91,3% для осевых.
Согласно отчету, в 55,2% осложнения были связаны с механическими факторами.
Авторы сделали вывод, что установка наклонных имплантатов с точки зрения биомеханики имеет больший риск осложнений — они связываются с помощью супраструктуры, которая действует как жесткая шина.
Другая терапевтическая возможность в заднем отделе верхней челюсти — это размещение имплантата в крылонебного отростка, в сочетании с установкой имплантата во фронтальном отделе. Данное образование сформировано задней частью верхнечелюстной кости и фронтальным фрагментом вертикальной кортикальной пластинки небной кости.
Крылонебный отросток имеет прочную кортикальной пластинку, которая обеспечивает хорошую первичную стабилизацию имплантата.
Wolfinger и коллеги привели результаты исследований, в которых были размещены 356 имплантатов в крылонебный отросток верхней челюсти, в сочетании с 1461 имплантатом, установленным во фронтальном отделе на 189 беззубых верхних челюстях.
Процент успеха составил 92,1% после среднего наблюдения 5 лет. Из 356 имплантатов, установленных в крылонебный отросток верхней челюсти, 41 имплантат потерян из-за неудачной остеоинтеграции.
Другие авторы, в том числе Vila Biosca, проводили критическое сравнение результатов установки имплантатов в крылонебный отросток по сравнению с результатами установки имплантатов после операции синуслифтинга.
Nocini и коллеги представили клинический случай, в котором они описывают установку имплантатов в крылонебный отросток верхней челюсти, используя при этом модифицированную остеотомию.
Осуществляя установку имплантатов под углом в 20 градусов, они адаптировали модифицированную остеотомию к анатомии ротовой полости, таким образом сокращая риск повреждения губ или слизистой оболочки щеки и одновременно облегчая работу оператора.
Ограничения, связанные с атрофией альвеолярного отростка, и проблемы со стороны кости, возникающие при синус-лифтинге, подталкивают исследователей к поиску альтернативных способов дентальной имплантации.
Установка имплантатов в скуловую кость — относительно новая техника, которая предусматривает расположение двух имплантатов с обеих сторон, имеющих длину 35-55 мм, которые, проходя через транссинусовую траекторию, прочно фиксируются в скуловой кости.
Эти имплантаты, как правило, комбинируются как минимумом с двумя имплантатами, установленными во фронтальном отделе, и фиксируются пластиночным протезом.
Aparicio и коллеги, основываясь на сериях клинических исследований 29 случаев, описали основные характеристики этой техники показания к ее применению, хирургический протокол и клинические этапы изготовления протеза.
Parel опубликовал ретроспективное исследование, включавшее 65 имплантатов, установленных в скуловой кости у 27 пациентов. Через 6 лет наблюдения ни один из имплантатов ни был потерян, процент успеха достиг 100%.
Stella и Warner описали вариант техники, которая предусматривает установку имплантата, минуя гайморову пазуху, по контуру малярной кости с фиксацией в скуловой кости.
Этот подход исключает создание окна в стенке гайморовой пазухи и облегчает установку имплантата, проводя ее над альвеолярным отростком в области первого моляра, под более вертикальным углом.
Данная техника дентальной имплантации была применена у пациентов с полной первичной адентией в результате генетических изменений или синдромов.
Balshi и Wolfinger описывают случай реабилитации 20-летнего пациента с эктодермальной дисплазией путем установки двух имплантатов в скуловую кость в сочетании с размещением четырех имплантатов во фронтальном отделе верхней челюсти, избегая любых реконструктивных операций.
Наращивание дна гайморовой пазухи
Данная оперативная методика — одна из наиболее широко применяемых в реабилитации пациентов с атрофией альвеолярного отростка боковых отделов верхней челюсти, с точки зрения прогнозируемого конечного результата.
Основной целью этой операции является увеличение толщины альвеолярного отростка в области дна гайморовой пазухи при атрофии альвеолярного отростка верхней челюсти, что делает возможным установку в будущем имплантатов.
Такая хирургическая процедура — это стандартное асептический мероприятие, которое осуществляется либо под местной или общей анестезией.
При дентальной имплантации врачу приходится сталкиваться с трудностями, которые связаны с анатомическими и возрастными особенностями челюстей.
Для врача-имплантолога установка дентального имплантата на верхнечелюстной кости бывает затруднительным из-за атрофии альвеолярного отростка или при пневматическом типе строения верхнечелюстных пазух.
Для увеличения высоты альвеолярного отростка, как в боковом, так и во фронтальном отделах, можно использовать различные методы:
Поднятие дна верхнечелюстной пазухи (синус-лифтинг)
Поднятие дна носовой полости (антропластика или антро-лифтинг)
Костная пластика (использование остеопластических материалов на атрофированной части альвеолярного отростка).
При атрофии альвеолярных отростков челюстей в качестве остеопластического материала для наращивания кости и реконструкции альвеолярных отростков используют как ауто- или аллокость, так и ксеногенные (Остеоматрикс) в виде костных чипсов и др.
Проведение реконструктивно-восстановительных операций для наращивания альвеолярного отростка осуществляется по стандартным правилам костно-пластических операций с разной фиксацией подсаживаемого материала.
В зависимости от типа, размера и локализации костной атрофии альвеолярного отростка Тюлан и Патарая (2001) предлагают следующие классификации клинических форм:
Анатомические разновидности: горизонтальная резорбция (уменьшение толщины альвеолярной стенки, которая превращается в тонкую пластинку, сохранив при этом достаточную высоту), вертикальная (приводит к потере высоты альвеолярного отростка и наблюдается после травматического экстракции) и смешанная резорбция (одновременное уменьшение высоты и толщины альвеолярного гребня).
Топографические формы: одиночная (отмечается дефицит костной ткани в области одного зуба, чаще в области резцов), сегментарная (встречается в дистальных отделах альвеолярного отростка) или полная (наблюдается по всей челюсти).
Особое место занимает планирование операции при отсутствии премоляров и моляров, когда для установки имплантатов высота нижней стенки пазухи менее 10 мм.
На основании накопленного практического опыта отечественных и зарубежных авторов подобные случаи дефицита кости верхней челюсти разделяют на 4 группы.
Первая группа — высота альвеолярного отростка верхнечелюстной кости составляет 10 мм и более. Здесь возможна установка дентальных имплантатов по обычной методике.
Вторая группа — высота альвеолярного отростка верхней челюсти в пределах 6 - 8 мм. В таких случаях возможно применение имплантата длиной 8 мм и получить бикортикальную фиксацию. После установки дентального имплантата обязательным условием является достаточная первичная стабилизация.
Образовавшуюся полость можно заполнять ауто- или аллокостью, ксеногенными остеопластическими материалами или биокерамикой. Высота альвеолярного отростка в 5-7 мм является необходимым условием для первичной костной фиксации дентального имплантата со стороны альвеолярного гребня.
Четвертая группа — высота альвеолярного отростка верхнечелюстной кости составляет менее 4 мм. В подобных случаях установка дентальных имплантатов является проблематичной ввиду того, что не представляется возможным обеспечить даже минимальную первичную костную стабилизацию имплантата.
Рекомендуется на первом этапе проводить классический синус-лифтинг без установки имплантатов, только заполняя полость остеопластическим материалом (Остеоматрикс).
Исходя из ранее сказанного и в зависимости от степени атрофии альвеолярных отростков, можно использовать классификацию, предложенную Misch (1987). В зависимости от степени выраженности атрофии альвеолярных отростков верхнечелюстных костей исследователь разделил обследуемых на 4 группы.
По классификации Cawood (1998) можно выделить 5 классов состояния верхнечелюстных пазух в зависимости от величины резорбции костной ткани альвеолярного отростка.
Операция наращивания толщины альвеолярного отростка за счет поднятия дна гайморовой пазухи верхней челюсти очень подробно описана Boyne и James с применением аутогенного костного материала, содержащего собственно кость и костный мозг.
Увеличение толщины дна гайморовой пазухи в современной стоматологической практике, осуществляется двумя путями. Это классический подход, когда вход в гайморову пазуху достигается через латеральную стенку, как описано Tatum в 1986. Или же использование методики доступа через альвеолярный отросток, разработанной Summers.
При методе закрытого увеличение толщины альвеолярного отростка большое неудобство доставляет возникновение сконцентрированного давления, создаваемого остеотомом или фрагментами разрушенной кости на очень маленькую площадь.
Довольно часто это приводит к перфорации мембраны Шнайдера. По этой причине применение метода ограничено теми клиническими случаями, где требуется поднятие мембраны не более чем на 3-5 мм.
Была предпринята попытка разработать методику не только контролируемого, минимально инвазивного доступа к верхнечелюстной пазухи, но также осторожного отделения большого участка слизистой оболочки, обеспечивая повышение мембраны Шнайдера до 10 миллиметров и более, в случаях значительного дефицита костной ткани.
Рабочая группа профессора Benner разработала и внедрила в стоматологическую практику новую методику и набор хирургических инструментов для поднятия мембраны с помощью воздушного шара — баллонный синус-лифтинг (БСЛ).
Во многих клинических ситуациях боковой отдел верхней челюсти представлен костью III или IV типа. Это пористая кость, содержащая много губчатого вещества, и недостаточная по толщине кортикальная пластинка, усложняющая процесс установки имплантатов.
Это отмечается в клинических ситуациях, где наблюдается катастрофическая атрофия костной ткани альвеолярного отростка. Выбор соответствующей длины имплантата ограничен близким расположением гайморовой пазухи верхней челюсти.
Прогнозировалось, что через время после удаления зубов или корней количество костной ткани должно измениться в сторону уменьшения вследствие атрофии гребня альвеолярного отростка и расширения гайморовой пазухи, что повлияет на качество кости.
Профессором использовалась методика DASK — минимально инвазионная техника открытого синус-лифтинга, без риска повреждения мембраны.
Открытый синус-лифтинг по методике DASK применяли в тех клинических случаях, когда имеется значительная атрофия альвеолярного отростка боковых отделов верхней челюсти и толщина дна гайморовой пазухи составляет порядка 1-3 миллиметров.
Чтобы установить 2-3 имплантата, необходимо обеспечить контакт остеопластического материала минимум с тремя костными стенками пазухи. Ранее с этой целью в латеральной стенке делали окно, чем ослаблялась латеральная стенка гайморовой пазухи.
Техника DASK предусматривает возможность создания одного или двух окон на латеральной стенке гайморовой пазухи, в зависимости от количества устанавливаемых имплантатов.
В последние годы благодаря новейшим разработкам и технологиям в предимплантационной подготовке пациента с целью создания адекватного объема костной ткани, а также благодаря совершенствованию поверхности имплантатов, удалось значительно улучшить хирургический протокол методики дентальной имплантации.
Как результат такого усовершенствования было достигнуто прогнозируемое использование остеопластических материалов при операции синус-лифтинга, что позволяет устанавливать имплантаты в области моляров верхней челюсти.
Оптимизация хирургического этапа дентальной имплантации при подготовке пациентов к протезированию существенно повышает качество и эффективность реабилитации и делает более предсказуемым клинический результат.
Читайте также:

