Токсокароз у собак реферат
Обновлено: 05.07.2024
* Данная работа не является научным трудом, не является выпускной квалификационной работой и представляет собой результат обработки, структурирования и форматирования собранной информации, предназначенной для использования в качестве источника материала при самостоятельной подготовки учебных работ.
Содержание
1. Морфо-экологические особенности паразита
1.1. Систематическое положение
1.2. Морфологические особенности
1.3. Цикл развития
2. Клиническая картина заболевания
3. Численность и распространение паразита на территории России
ВВЕДЕНИЕ
Для человека токсокароз - зоонозная инвазия. Она характеризуется тяжелым, длительным и рецидивирующим течением, полиморфизмом клинических проявлений, обусловленных миграцией личинок токсокар по различным органам и тканям. Заражение человека происходит при проглатывании инвазионных яиц токсокар. Симптоматика его очень разнообразна, поэтому с ним могут встретиться врачи самых разных специальностей - педиатры, терапевты, окулисты, гематологи, гастроэнтерологи, невропатологи и другие.
Еще в 1911 г. F. Fulleborn высказал предположение о возможности паразитирования у человека несвойственных ему видов аскаридат с развитием аллергических реакций. В 1952 г. P. Beaver назвал феномен миграции личинок гельминтов животных у человека "larva migrans" (мигрирующие личинки) и утвердил этот термин как диагностическую единицу. "Larva migrans" - это большая группа зоонозных болезней, характеризующаяся следующими особенностями:
1. человек для их возбудителя - несвойственный хозяин;
2. возбудители в организме человека не достигают половозрелого состояния;
3. симтомокомплекс обусловлен миграцией личинок или взрослых гельминтов в коже или внутренних органах человека.
В зависимости от преобладающих симптомов выделяют кожную, висцеральную и глазную формы larva migrans. Позднее, в 1969 г., P. Beaver предложил в тех случаях, когда известен возбудитель, обозначать заболевание не расплывчатым термином "мигрирующая личинка", а конкретным названием, происходящим от названия возбудителя (дирофиляриоз, гнатостомоз, ангиостронгилез, капиляриоз, спарганоз и др.). Инвазию, вызываемую аскаридатами собак (Toxocara canis), он назвал токсокарозом.
В нашей стране внимание к токсокарозу человека привлекли работы И.Р. Дробинского (1961), Е.С. Лейкиной (1962), М.И. Алексеевой (1982) и др.
Морфо-экологические особенности паразита
Phylum NEMATHELMINTHES Schneider, 1866
Classis NEMATODA Rudolphi, 1808
Ordo ASCARIDIDA Skrjabin & Schulz, 1938
Subordo ASCARIDATA Skrjabin, 1915
Familia ANISAKIDAE Skrjabin & Karokhin, 1945
Genus TOXOCARA Stiles, 1905
T. canis Stiles, 1905
Морфологические особенности
Toxocara canis - червь, самка которого имеет длину 6-8 см, самец - 4-10 см. Одним из важных дифференциальных морфологических признаков токсокар являются вздутия кутикулы на головном конце, образующие боковые крылья размером 2.3 на 0.3 мм.
Яйца токсокар почты круглой формы. Они крупнее оплодотворенных яиц аскарид - соответственно 65-75 и 50-70 мкм. Наружная оболочка яиц толстая, плотная, мелкобугристая, напоминающая поверхность наперстка, цвет ее - от светло-коричневого до темно-коричневого. Внутри незрелого яйца расположен шаровидный темный бластомер, заполняющий почти все яйцо. В зрелом инвазионном яйце содержится живая личинка.
Жизненный цикл
T. canis паразитирует в тонком кишечнике и желудке собак, волков, лисиц, песцов – облигатных хозяев. Средняя продолжительность жизни половозрелых особей составляет 4 мес., максимальная 6 мес. Самка Т. canis откладывает более 200 тыс. яиц в сутки. Яйца выделяются незрелыми и неинвазионными (на стадии развития одного бластомера). Срок созревания яиц зависит от температуры окружающей среды и влажности. Инвазионное яйцо содержит личинку, совершившую две линьки. В почве яйца длительное время сохраняют жизнеспособность и инвазионность. Широкому распространению токсокароза среди животных способствует совершенный механизм передачи возбудителя, при котором сочетаются прямой (заражение яйцами из окружающей среды), внутриутробный (заражение плода личинками через плаценту), трансмаммарный (передача личинок с молоком) пути передачи и заражение через резервуарных (паратенических) хозяев.
В желудке или тонкой кишке собаки из яиц выходят личинки, которые совершают миграцию. Через слизистую оболочку кишечника личинки проникают в венозные сосуды кишечника систему воротной вены и заносятся в печень, откуда – в нижнюю полую вену, затем в правую половину сердца, через легочную артерию в капиллярную сеть легких, где выходят в просвет альвеол и бронхиол. Из бронхиол личинки попадают в бронхи, затем в трахею, глотку, откуда при проглатывании – в желудок и кишечник. Здесь через 4-5 недель после заражения паразит достигает половозрелости. Такой путь миграции реализуется чаще у щенков до 5 недель.
Часть личинок, достигнув легких, пенетрирует в легочную вену, попадает в большой круг кровообращения, через артериальную систему заносится в различные органы и ткани, где инцестируется. Этот путь миграции характерен для заражения старших животных. В соматических тканях этих животных личинки могут сохранять жизнеспособность в течение ряда лет. В период беременности таких животных происходит эксцистирование личинок, которые чрез плаценту проникают в плод (внутриутробное заражение). В результате у новорожденных щенков на 3-4 неделе жизни образуется половозрелые особи гельминтов.
Трансмаммарная передача начинается сразу после родов и достигает максимума на второй неделе лактации.
Человек является факультативным хозяином T. canis, у которого гельминт паразитирует только в стадии личинки. Заражение человека происходит при попадании инвазионных яиц токсокар в ЖКТ. Яйца могут быть занесены в рот загрязненными руками, овощами, ягодами. Не исключается возможность заражения человека при поедании в сыром или недостаточно термически обработанном виде мяса паратенических хозяев – цыплят, голубей, ягнят, свиней. При пероральном заражении человека инвазионные яйца проходят желудок, и в проксимальном отделе тонкой кишки из них вылупляются личинки. Они проникают через слизистую оболочку кишки в кровоток, заносятся в печень, оттуда в правую половину сердца. Попав в легочную артерию, личинки проникают из легочных капилляров в легочную вену, достигают левой половины сердца и затем разносятся по разным тканям и органам. Личинки в процессе миграции, попав в узкие капилляры, застревают в паренхиме органов, где оседают. Они не растут, не изменяются, но длительно сохраняют жизнеспособность. Не исключается при этом возможность их активизации и продолжают миграции при ослаблении защитных сил организма. Постепенно личинки инкапсилируются и погибают.
Клиническая картина заболевания
Спектр клинических проявлений является производной от интенсивности заражающей дозы и частоты реинфекций, распространения личинок в тех или иных органах и тканях, а также степени иммунного ответа хозяина. Токсокароз характеризуется длительным рецидивирующим течением (от нескольких месяцев до нескольких лет), что связано с периодическим возобновлением миграции личинок токсокар. Редкие летальные случаи при токсокарозе связаны с миграцией личинок в миокард и важные в функциональном отношении участки центральной нервной системы.
В последние годы было установлено (Лысенко А.Я., Фельдман Э.В., Рыбак Е.А.), что токсокароз у детей приводит к снижению эффективности вакцинации и ревакцинации против кори, дифтерии и столбняка.
Висцеральный токсокароз
Висцеральным токсокарозом болеют как дети, так и взрослые, хотя у детей это заболевание встречается чаще. Развитие висцерального токсокароза происходит вследствие заражения большим числом личинок и ассоциируется, например, у детей, с привычкой геофагии. Основными симптомами токсокароза являются рецидивирующая лихорадка, легочный синдром, увеличение размеров печени, лимфаденопатия, эозинофилия, гипергаммаглобулинемия.
По литературным данным, у больных токсокарозом детей температура повышается обычно в полдень или вечером, сопровождаясь небольшим ознабливанием.
Синдром поражения легких встречается у 65% больных висцеральным токсокарозом и варьирует в широких пределах. У больных наблюдаются рецидивирующие бронхиты, бронхопневмонии. Беспокоит сухой кашель, частые приступы ночного кашля, в некоторых случаях - тяжелая одышка с астматическим дыханием и цианозом. При аускультации выслушиваются сухие, нередко влажные хрипы. При токсокарозе известны случаи развития тяжелых пневмоний, которые протекали с осложнениями и заканчивались летальными исходами.
Наряду с синдромом поражения легких очень часто (до 80 % по нашим наблюдениям) отмечается увеличение размеров печени. Печень при пальпации уплотнена, гладкая, часто напряженная. Примерно у 20 % больных увеличена селезенка, у 67 % - лимфатические узлы, вплоть до системной лимфаденопатии, особенно часто у детей. Лимфоузлы небольшого размера, безболезненные, не спаяны с окружающими тканями.
Кроме перечисленных проявлений у 46 % больных отмечаются боли в животе, вздутие живота, тошнота, иногда рвота, диарея.
Часто заболевание сопровождается разнообразного типа рецидивирующими высыпаниями на коже (эритематозные, уртикарные). Пальпаторно в местах высыпаний обнаруживаются небольшие уплотнения.
В последнее время некоторые исследователи наряду с висцеральным и глазным выделяют неврологическую форму токсокароза. При миграции личинок токсокар в головной мозг выявляются признаки поражения центральной нервной системы. Заражение токсокарозом вызывает также различные неврологические нарушения, проявляющиеся в изменении поведения: гиперактивность и аффекты в широком спектре поведенческих реакций - обучение, исследование внешней среды, решение комплекса проблем по выходу из сложной ситуации. Проведенное в Нью-Йорке обследование детей 1-15 лет показало, что инвазированные токсокарами дети имели существенные отклонения от здоровых детей во многих нейропсихологических тестах, моторной и познавательной функции.
Глазной токсокароз
Развитие глазного токсокароза связывают с заражением человека минимальным количеством личинок. Пациенты с глазным токсокарозом обычно старше, чем с висцеральным, иммунный ответ на заражение не так ярок, титры специфических противотоксокарных антител у них, как правило невысокие.
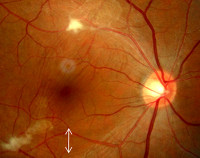
Первые случаи глазного токсокароза были выявлены в начале 50-х гг. нашего столетия. В последующем токсокароз глаза начали диагностировать в разных странах с достаточным постоянством. Клинически у детей заболевание проявляется в виде косоглазия, снижения зрения, лейкокории. Личинки могут быть обнаружены при офтальмологическом исследовании.
Практически всегда токсокарозом поражается только один глаз. При глазном токсокарозе обнаруживают, как правило, не более одной личинки.
Поражение зрительного нерва личинкой токсокары может привести к односторонней слепоте.
Надежных методов диагностики глазного токсокароза не существует. Во многих случаях диагноз выясняется только при гистологическом исследовании. Дополнительными методами диагностики глазного токсокароза являются иммунологические реакции (которые не всегда в случаях глазного токсокароза бывают информативными), ультразвуковое и рентгенографическое исследование. В 1977 г. предложено в сомнительных случаях ретинобластомы проводить серологическое исследование на токсокароз пунктата передней камеры, а в 1979 г. - биоптата стекловидного тела.
Численность и распространение паразита на территории России
А.Я. Лысенко, Т.Н. Константинова, Т.И. Авдюхина провели расчеты оценочного числа лиц, больных висцеральным токсокарозом в РФ. Ожидаемое число больных среди детей в возрасте до 14 лет составляет 184 тыс. человек, в возрастной группе старше 14 лет - 366 тыс. Всего расчетное число больных токсокарозом может быть близким к цифре 550 тыс. человек, что составляет 380 на 100 тыс. населения.
Глазной токсокароз еще более недовыявляется, чем висцеральный. Это следует из сравнения с данными в США, где среди 700-1000 ежегодно регистрируемых Центром по борьбе с болезнями случаев токсокароза (по мнению специалистов Центра, эти сведения далеко не полные) на глазной токсокароз приходится 500-600 случаев, т.е. 67 %.
ПРОФИЛАКТИКА
В течение последних нескольких лет токсокароз введен в систему отчетности, на каждый случай его выявления должно подаваться экстренное извещение в территориальный центр Госсанэпиднадзора.
Профилактика токсокароза является комплексной медико-ветеринарной проблемой. Можно выделить следующие направления в этой работе.
1. Мероприятия, направленные на источник инвазии. Одним из основных мероприятий в этом отношении является обследование собак и их своевременная дегельминтизация. Весьма эффективно преимагинальное лечение щенков в возрасте до 4 недель (до окончания периода миграции паразитов и выделения пропагативных стадий). Особое внимание должно быть обращено на дегельминтизацию собак во время их беременности, а также щенков до 6-месячного возраста, которые бывают инвазированны токсокарами особенно часто. В последующем необходимо регулярно (не реже 1 раза в год) проводить паразитологическое обследование животного и при выявлении токсокароза - лечение. Для лечения токсокароза у собак используют левамизол (эффективность лечения - 99%), мебендазол (эффективность лечения - 99%), пирантел (эффективность лечения - 95%), а также пиперазин (эффективность лечения - 82.5%).
Важным мероприятием в отношении источников инвазии является ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак и содержание этих площадок в хорошем гигиеническом состоянии.
2. Влияние на другие факторы передачи. Это обычные гигиенические мероприятия, мало отличающиеся от таковых в отношении других инфекций и инвазий зоонозной природы: мытье рук после контакта с почвой или животными; тщательная обработка зелени, овощей и других пищевых продуктов, которые могут содержать частицы почвы; защита игровых детских площадок, парков, скверов от посещений животных; использование естественных факторов санации почвы (открытые солнечные лучи).
Одной из актуальных задач санитарно-профилактической службы является изучение роли почвы и других объектов, как факторов передачи возбудителя токсокароза. Для этого должны регулярно проводиться санитарно-паразитологические исследования таких объектов (проб почвы, смывов с объектов окружающей среды) и осуществляться анализ полученных результатов.
3. Влияние на поведение человека. Абсолютное большинство жителей не имеют адекватной информации не только о токсокарозе, но и о риске зоонозных инвазий вообще. В таких условиях трудно надеяться на осознанное гигиеническое поведение людей, способствующее профилактике заражения, поэтому важнейшей задачей является санитарное просвещение населения. Оно может быть эффективным лишь в случае неформального подхода. Например, информация для владельцев собак должна предусматривать все аспекты мер по профилактике заражения животных и их хозяев, в то же время для тех, кто не имеет в доме животных, может быть достаточно информации в отношении факторов передачи и профилактики заражения гельминтозами.
Риск заражения токсокарозом может быть значительно снижен, если отсутствует привычка пикацизма, особенно геофагии. Кроме разъяснения ее эпидемиологического значения, в некоторых странах применяются заменители веществ, употребляемых в таких случаях: в магазинах можно приобрести специальную глину, мел для тех, кто не может преодолеть тягу к пикацизму. Интересно, что в некоторых странах Юго-Восточной Азии распространенная привычка жевать бетель издавна является одним из способов профилактики паразитных болезней, включая и токсокароз, так как содержащиеся в бетеле жирные кислоты оказывают ларвицидное действие на личинки токсокар.
Установлено, что заболевание токсокарозом ведет к развитию иммунитета против повторного заражения, хотя одновременно отмечается иммуносупрессивное воздействие паразита. Привакцинации различными антигенными препаратами из личинок токсокар получен лишь частичный эффект. Предполагается, что с помощью современных иммунологических методов можно получить высокоспецифичные протективные препараты, разработать методы подавления их иммуносупрессивного действия токсокар, в результате чего уже в ближайшем будущем будет получена вакцина против токсокароза.
ЗАКЛЮЧЕНИЕ
Токсокароз - относительно новая проблема практического здравоохранения. Ее решение в огромной степени зависит от целенаправленной совместной работы медицинской и ветеринарной служб, а также от внедрения в практику здравоохранения новейших методов диагностики, лечения и профилактики этой инвазии.
СПИСОК ЛИТЕРАТУРЫ
1. Лысенко А.Я., Константинова Т.Н., Авдюхина Т.И. Токсокароз/ Учебное пособие. – М.: Российская медицинская академия последипломного образования, 1999
2. Уткин Н.А. Простейшие и беспозвоночные Курганской области. Список известных видов. – Курган: Изд-во Курганского государственного университета, 1999. – 363 с.
3. Токсокароз. – Вестник инфектологии и паразитологии 4. Токсокароз. Этиология. Патогенез. Симптомы токсокароза. Висцеральный токсокароз. Диагностика
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
Токсокароз – это хроническое инфекционное заболевание, вызываемое личинками круглого червя токсокары. Для инвазии характерна лихорадка, рецидивирующие высыпания и увеличение размеров печени. Патология сопровождается поражением глазных яблок и внутренних органов: сердца, головного мозга, легких. Диагностика заключается в обнаружении специфических антител к возбудителю. Лечение этиотропное (антигельминтные препараты), также применяются средства симптоматической терапии, в некоторых случаях производятся хирургические вмешательства.
МКБ-10
B83.0 Висцеральная форма заболеваний, вызываемых миграцией личинок гельминтов [висцеральная Larva migrans]
Общие сведения

Причины токсокароза
Возбудитель – круглый червь Toxocara, наиболее часто встречаются инвазии видами Т. сanis (собачий) и T. сati (кошачий). Основной цикл развития паразита не включает в себя человеческий организм, поэтому люди оказываются случайными хозяевами гельминта, который в подобных условиях неспособен достигать половозрелой формы. Источником инфекции является больное животное (чаще собака), больной человек эпидемиологически не опасен. Считается, что доля зараженных токсокарозом среди взрослых собак варьирует от 15 до 50%, щенков – до 80%.
Больные животные выделяют яйца гельминтов с фекалиями, сами паразиты в половозрелой форме находятся у постоянного хозяина в пищеварительном тракте. Наиболее опасными считаются дворы, детские площадки, парки, поскольку контаминация земли яйцами паразита встречается в 10-40% почвенных проб. Инфицирование людей происходит контактным и пищевым путем – при поглаживании, играх со зверями, особенно бродячими, употреблении в пищу немытых ягод, фруктов и овощей. Отмечено, что тараканы могут поглощать яйца токсокар с последующим выделением до 25% потенциально жизнеспособных особей, что играет важную роль в распространении инфекции в быту.
Патогенез
После попадания яиц токсокары в тонкий кишечник человека (преимущественно двенадцатиперстную кишку) высвобождаются личинки, проникающие в системный кровоток через слизистую оболочку. Сначала токсокары заносятся в печень и правую половину сердца, затем в легочную артерию и левый желудочек, откуда выходят в большой круг кровообращения. Распространяясь по организму, личинки оседают в различных органах и тканях, вызывая геморрагические и некротические изменения, образование воспалительных очагов в виде гранулем, в центре которых находится некротизированная ткань и личинка, вокруг – воспалительный инфильтрат.
При попадании в кровеносное русло продуктов жизнедеятельности возникают аллергические реакции. Часть личинок гибнет, оставшиеся гельминты выделяют особую маскирующую субстанцию, которая позволяет им персистировать в организме до 10 лет, периодически мигрируя по кровеносной системе и поражая новые ткани. Характерной особенностью токсокар является формирование гранулем в поджелудочной железе, головном мозге, печени, легких, миокарде и мезентериальных лимфатических узлах. Патогенез поражения глаз до конца не изучен, имеются гипотезы о низкой активности инвазии и малой выраженности иммунного ответа.
Патогенез эпилепсии при токсокарозе окончательно не ясен. Предполагается, что поражение головного мозга может привести к формированию волокнистых рубцов после острого воспаления или хронических гранулем. Другая теория объясняет появление эпилептических припадков при повреждении нейронов усиленным образованием провоспалительных цитокинов из-за повышения проницаемости гематоэнцефалического барьера, вызываемого паразитами, а также аутоантителами к нейрональным элементам, которые нередко обнаруживаются у больных токсокарозом.
Классификация
Классификация токсокароза у человека основывается на глубине инвазии в организм человека. Гельминтоз практически всегда протекает с минимальной либо неспецифической клиникой (субклинически), бессимптомная форма встречается в 13% случаев заболевания, органные поражения более характерны для детей. Выделяют следующие виды токсокароза:
- Глазной.Типичен для детей старше 8 лет, подростков и молодых взрослых. Поражение зрительного аппарата обычно одностороннее, протекает в виде хронического эндофтальмита, увеита, абсцессов стекловидного тела, папиллитов, кератитов и косоглазия. При длительном течении возможна слепота.
- Висцеральный.Протекает остро или хронически с вовлечением дыхательной системы, сердца, кожи, лимфатических узлов, селезенки, печени, суставов и мышц. Часто наблюдается диарея, тошнота и рвота. Описаны поражения головного мозга: рецидивирующие головные боли, менингоэнцефалит, эпилептические припадки.
Симптомы токсокароза
Инкубационный период определить сложно, считается, что он может занимать несколько лет. При остром начале наблюдается лихорадка до 38,5°C и выше, поражения дыхательной системы – от заложенности носа, сухого кашля и першения в горле до тяжелой одышки и астматического статуса. На коже появляется зудящая сыпь в виде волдырей и пятен, при подкожном расположении личинок видны приподнятые над поверхностью прямые или извилистые красновато-коричневые ходы. У детей нередко выявляются увеличенные плотноэластические безболезненные лимфоузлы. Пациенты с токсокарозом часто предъявляют жалобы на боли в животе, тошноту, иногда – рвоту и срывы стула.
Осложнения
Наиболее частые осложнения висцерального токсокароза – бронхиальная астма, хронический бронхит и эпилепсия, глазного – отслойка сетчатки и односторонняя слепота. Подкожное расположение личинок токсокар приводит к присоединению вторичной бактериальной инфекции, образованию инфильтраов, абсцессов и флегмон, поражение легких – к тяжелым пневмониям смешанной этиологии с нарастающей дыхательной недостаточностью. Массивная инвазия гельминтов, полиорганное поражение могут стать причиной летального исхода. У беременных женщин токсокароз часто выявляется невынашивание, задержка внутриутробного развития плода.
Диагностика
Диагноз токсокароза подтверждается врачом-инфекционистом. Для исключения сочетания висцерального и глазного гельминтоза обязательным является осмотр офтальмолога, по показаниям назначаются консультации других специалистов. Диагностические методы, необходимые для верификации токсокарозного поражения, включают следующие методики:
Дифференциальную диагностику проводят с аскаридозом, при котором нередко наблюдаются кишечная непроходимость, острая обструкционная дыхательная недостаточность. Необходимо исключить описторхоз и стронгилоидоз, которые протекают с желтухой, болями в правом подреберье и срывами стула. Глазную форму токсокароза дифференцируют от ретинобластомы, проявляющейся лейкокорией, косоглазием, слезотечением, светобоязнью, вторичной глаукомой. Кожные проявления могут быть следствием укусов насекомых, воздействия аллергенов.
Лечение токсокароза
Показанием для стационарного лечения являются висцеральные формы болезни. Постельный режим назначается только при наличии лихорадки и рекомендуется до 2-4 дней устойчивого отсутствия высоких цифр температуры тела. Специальной диеты нет, однако, учитывая некоторые побочные эффекты применяемых препаратов, рекомендуется воздержаться от приема жирной, жареной пищи, алкоголя, специй, маринадов, сладостей. Важно соблюдение питьевого режима, исключение контакта с возможными пищевыми и бытовыми аллергенами. Недопустимо самовольное прекращение начатого медикаментозного лечения.
- Антигельминтная терапия. Высокоэффективными антигельминтными средствами для разрушения мигрирующих личинок считаются албендазол, мебендазол, диэтилкарбамазин, которые применяются в таблетированных формах. В отношении токсокар, находящихся в гранулемах, данные препараты не обладают выраженным нейтрализующим эффектом.
- Хирургические методы лечения применяются при глазном токсокарозе и включают в себя микрохирургическое удаление гранулем, лазерную коагуляцию для расщепления личинок в средах глаза и коррекции отслойки сетчатки.
- Симптоматическая терапия проводится по показаниям. Включает жаропонижающие (парацетамол, целекоксиб), дезинтоксикационные (хлосоль, глюкозо-солевые растворы), десенсибилизирующие (глюконат, хлорид кальция), антигистаминные (хлорапирамин, дезлоратадин), отхаркивающие (ацетилцистеин, мукалтин), ферментативные (панкреатин) и другие средства.
Прогноз и профилактика
Прогноз при неосложненных формах благоприятный, летальных случаев не описано. Длительность приема лекарственных средств может составлять до 3-4 недель и более, иногда требуются несколько курсов с перерывами в 2-4 месяца. Критериями эффективности считаются исчезновение клиники, снижение уровня антител и эозинофилии крови. Описаны случаи диссеминированного токсокароза среди ВИЧ-инфицированных лиц в стадии СПИДа, а также пациентов, длительно принимающих системные глюкокортикостероиды или проходящих лучевую терапию по поводу онкологических болезней.
Профилактические вакцины на основе ДНК показали положительный эффект в экспериментах на мышах, исследования в настоящее время продолжаются. Рекомендуется осуществлять контроль за популяцией бродячих животных, проводить выгул собак на специально отведенных территориях. Важными мерами неспецифической борьбы с заболеваемостью являются отучение детей от поедания земли, привитие навыков личной гигиены после игр на улице, песочнице, общения с животными; тщательное мытье ягод, зелени, овощей и фруктов перед едой; назначение антигельминтных препаратов беременным собакам, новорожденным щенкам.
2. Токсокароз. Клиника. Диагностика. Лечение. Профилактика. Информационно¬методическое пособие. – 2004.
4. Токсокароз у детей/ Глазунова Л.В., Артамонов Р.Г., Бекташянц Е.Г., Куйбышева Е.В., Шиц О.Л., Кирнус Н.И., Иванова Е.Ю. // Лечебное дело. – 2008.
Тохосага canis Werner, 1782 — довольно крупная нематода белого или светло-желтого цвета (рис.). Тело веретенообразное, покрыто поперечно исчерченной кутикулой, которая образует закругленные широкие шейные кутикулярные крылья, формирующие капюшон на головном конце. Длина половозрелых самцов 5. 10 см, самок — 10. 18 см. Хвостовой конец у самца изогнут, на нем находятся две одинаковые спикулы. Ротовое отверстие обрамлено тремя толстыми губами: дорсальной и двумя латерально-вентральными. По внутреннему краю губ проходят зубчики, собранные в один ряд. Дорсальная губа вооружена двумя большими, симметрично расположенными сосочками, латеро-вентральные несут по одному сосочку. Между пищеводом и кишечником расположен желудочек, являющийся характерным признаком вида данного семейства. Максимальная продолжительность жизни токсокары в кишечнике собаки достигает 6 месяцев [9].
Яйца темно-серого или коричневого цвета, субсферической формы, размеры 0,068?0,075 мм. Оболочка толстая, с хорошо выраженной ячеистостью, покрыта клейкой субстанцией, способствующей прикреплению к окружающим предметам. Внутри незрелого яйца расположен шаровидный темный бластомер, заполняющий почти все пространство. В зрелом инвазионном яйце содержится живая личинка [9]. Размер личинок L2 — 0,34…0,47, L3 — 0,46…0,48 мм.
Биология развития токсокары
Дефинитивные хозяева Тохосага canis — собака, песец, лисица, фенек, шакал, гиена, енотовидная собака, волк.
Токсокары развиваются по аскаридному типу. Основные хозяева выделяют наружу яйца гельминтов, достигающие инвазионности при благоприятных условиях за 8…15 суток. Биология развития Тохосага canis характеризуется рядом особенностей, имеющих большое эпизоотологическое значение. В зависимости от возраста животного различают 10 вариантов развития токсокар.
Взрослые основные хозяева заражаются алиментарным путем, поедая яйца токсокар или резервуарных хозяев. Большую эпизоотологическую роль в заражении плотоядных токсокарами также играет каннибализм, когда инкапсулированные личинки в мышцах одних животных служат источником заражения других особей.
Щенки инвазируются внутриутробно и через молоко в первые 3 недели лактации. У щенков обнаруживают личинок токсокар в легких и печени [9].
Резервуарные хозяева (грызуны, птицы и олигохеты) заражаются при проглатывании инвазионных яиц токсокар, а также при поедании инвазированных личинками животных и их трупов. Личинки в кишечнике выходят из яиц и мигрируют в различные органы и ткани, где инкапсулируются, длительное время сохраняя жизнеспособность. Если резервуарный хозяин не будет съеден окончательным хозяином, то цикл развития прерывается. Также возможны внутриутробное заражение и через молоко [9].
В.А. Васильева [15] отмечает высокий процент заражения щенков до полугода, а также возможную гибель в возрасте до 2 месяцев при высокой интенсивности инвазии.
Эпизоотологические данные
Токсокароз — широко распространенное заболевание. Яйца токсокар устойчивы во внешней среде, значительную роль в распространении играют бродячие собаки, зараженность которых составляет 55%, в то время как домашних - 15,2 % [9].
С.В. Пузенько [35] считает, уровень зараженности животных токсокарозом значительно выше. До 50% - домашние собаки и животные частных подворий, до 90% - безнадзорные.
Яйца токсокар могут находиться на шерсти собак, преимущественно до года, что повышает риск заражения не только контактных животных, но и их владельцев [42].
У служебных собак уровень инвазированности значительно ниже. Так, по данным А.В. Соргиной [39] токсокарозом заражены около 5,9% исследованных животных. Однако уровень инвазированности животных год от года растет [10].
Согласно исследованиям, проведенным в г. Казани, 58,6% паразитарных заболеваний плотоядных приходится на токсокароз [40].
Обобщая данные литературы, Е.И. Анисимова и др. [3] отмечают, что распространение гельминтозов зависит от культуры содержания собак и кошек. Отмечены факты экстенсивного (50% и выше) и интенсивного (60 и долее яиц/кг) обсеменения территории детских площадок. Эти данные согласуются с общемировыми тенденциями, где уровень заражения колеблется от 14,4% до 53%.
З.М. Губейдуллина, А.Х. Султангареева [18] отмечают высокую зараженность в районах, где располагается большее число свалок, располагаются места несанкционированной торговли. Эти факторы, по мнению автора, способствуют скоплению бездомных животных.
Яйца токсокар могут длительно сохраняться во внешней среде, сохраняя активность в состоянии анабиоза, при температуре ниже минус 15ОС. Наиболее интенсивная инвазия наблюдается с мая по сентябрь, когда создаются благоприятные условия для развития яиц. Способствуют распространению инвазии тараканы и мухи — механические переносчики яиц возбудителя [9].
Патогенез токсокароза
Взрослые токсокары вызывают механические повреждения слизистой оболочки кишечника, приводя к развитию очагов воспаления и некроза. При высокой инвазии возможно закупоривание просвета кишечника, желчных ходов и просвета поджелудочной железы. Это может привести к смерти животного.
Массовая миграция личинок в организме взрослых собак (особенно беременных самок) и щенков приводит к поражению сосудов слизистой кишечника и многих органов, в том числе и плаценты. Это способствует переносу патогенной микрофлоры, а продукты обмена веществ гельминта оказывают токсическое действие и способствуют развитию аллергической реакции. [9].
Важную роль в патогенезе токсокароза играет изменение состава микрофлоры кишечника. У экспериментально зараженных собак из содержимого прямой кишки изолировали патогенных стафилококков, кишечную палочку, патогенную для белых мышей [1].
Иммунитет при токсокарозе
Основное значение в формировании иммунного ответа при токсокарозе играют эозинофилы и IgE, тканевые базофилы и макрофаги. Это связано прежде всего с тем, что личинки при миграции проходят через многие органы и ткани. Кутикула личинки защищает паразита от факторов иммунитета [9].
Клинические признаки токсокароза
Классическую картину токсокароза наблюдают при интенсивной инвазии. У щенков нарушается пищеварение, запоры чередуются с поносами, часто гельминтов находят во рвотных массах. Слизистые анемичные, животные отстают в росте и развитии. У собак может проявляться кашель, учащение дыхания, пенистые истечения из носа. Возможен летальный исход [9].
У интенсивно инвазированных животных наблюдают исхудание, анемию, расстройство деятельности пищеварительного тракта. Аппетит обычно ослаблен или извращен (животные поедают свои фекалии). Отмечают поносы, сменяющиеся запорами, колики и рвоту. В рвотных массах нередко можно обнаружить токсокар. Иногда у щенков наблюдают нервные явления в виде эпилептических припадков. Больные токсокарозом щенки отстают в росте и развитии, живот сильно вздут, и они производят впечатление рахитичных[9].
У Toxocara canis самыми опасными являются пренатальная и галактогенная инвазия, которые могут привести к гибели в первые дни жизни. С 2 и 3 недели поражается и кишечник. Миграция личинок через лёгкие способствует развитию пневмонии, которая проявляется хрипами и кашлем и истечениями из носа. При наличии взрослых аскарид в кишечнике может произойти его закупорка, вплоть до разрыва. У поражённых щенков увеличенный, болезненный, так называемый аскаридовый живот, часто происходит рвота, и вследствие этого может произойти дальнейшее осложнение – аспираторная пневмония. Из других симптомов наблюдают исхудание, метаболическую остеопатию, анемию, отсутствие аппетита, тусклую шерсть, судороги, доходящие до эпилептических припадков, признаки гиперчувствительности организма, например, прурит и крапивница. Слабая инвазия (особенно у подросших особей) в большинстве случаев протекает без выраженных клинических признаков. Аскариды вырабатывают токсин аскаридин, который вызывает нервные расстройства и быстро высвобождается из тел мёртвых гельминтов. Разрушение большого количества аскарид в кишечнике может, поэтому вызвать сильные судороги, а может даже привести к смерти поражённого животного. Съедание кала щенков сукой считается одним из этиологических факторов послеродовой эклампсии, вызванной аскаридином. У взрослых особей наличие соматических личинок в большинстве случаев клинически не проявляется.
Клинические симптомы у кошек практически одинаковы с собаками. Может наблюдаться плохой аппетит, тусклая и взъерошенная шерсть. Массовые гепатопульмональные миграции могут вызывать также хронический кашель, который обычно проявляется лишь спорадически. Рвота, сменяющаяся поносом, и вытекающие из этого потери жидкости проявляются дегидратацией кожи, западением глаз и прикрытием глаза третьим веком. Живот бывает увеличен и при его пальпации наблюдается повышенное скопление газов в кишечнике и верёвкообразный тонкий кишечник, а при аускультации – бурную перистальтику [8,19].
С.А. Акимова [25] отмечала у больных собак сдвиг ядра нейтрофилов влево, увеличение эозинофилов и лимфоцитов.
Определенный интерес представляют работы В.И. Колмогорова и др. [24], связанные с изучением повреждения наследственного аппарата при токсокарозе. Достоверно установлено, что интенсивность такого повреждения зависит от интенсивности инвазии. Подобные повреждения связаны не только с описанными выше процессами, но и токсическим действием продуктов из тканей токсокары. В частности, автор указывает на нарушение перекисного окисления липидов.
Патологоанатомические изменения
Токсокары у плотоядных животных вызывают геморрагический энтерит, язвы, атрофию слизистой оболочки, а иногда и разрывы кишечника. При проникновении гельминтов в желчные ходы печени наступает закупорка последних и развивается холангит [7].
Н.С. Бепалова и Н.М. Алтухова [11,12] установили изменения многофункционального состояния тимуса при токсокарозе. Так же автором отмечена низкая активность лимфоцитов. В почках установлено нарушение микроциркуляции, воспалительные процессы и дистрофия.
Диагностика токсокароза
Прижизненный диагноз у плотоядных ставят на основании изучения эпизоотологических данных, симптомов болезни и результатов гельминтоовоскопии по Фюллеборну. Посмертно для обнаружения токсокар проводят полное или частичное вскрытие кишечника и желчных ходов печени. Личинок обнаруживают при гистологических исследованиях.
Для диагностики токсокароза у людей разработаны серологические методы. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует о заражении, но не о болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных образований — гранулем и личинок, и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар [7].
М.Д. Новак и П.А. Солопов [28] отмечают эффективность использования иммуноферментного анализа и непрямой реакции гемагглютинации с антигеном, выделенным из экскреторно-секреторных белковых компонентов Toxacara canis.
О.А. Пановой [32,31] и соавторами разработан способ посмертной диагностики токсокароза. Суть его состоит в измельчении печени или легких, проваривании при температуре 41-42°С и изучении перешедших в раствор личинок под микроскопом. Ими же был разработан метод выделения личинок перевариванием легочной ткани [28].
Лечение и профилактика токсокароза
Для лечения и профилактики токсокароза плотоядных в настоящее время применяют соли пиперазина, нилверм, пирантел, мебендазол, фенбендазол и другие нематоциды [33].
Исследованиями Ю.Ф. Петрова и других авторов [33,30] подтверждена эффективность фенбендазола (30 мг/кг по действующему веществу) с интервалом в 24 часа и азинокса плюс по одной таблетке на 10 кг массы тела однократно. Автором так же отмечено повторное заражение животных спустя два месяца после проведенного лечения.
И.А. Архипов с соавторами [5] провели масштабные исследования Празитела на плотоядных. Испытание препарата в виде суспензии в дозе 3 мг/кг по празиквантелу и 30 мг/кг пирантелу показало 100% эффективность. Однако автор отмечает признаки отравления у животных при трехкратном превышении дозы этого препарата.
Исследования по созданию препаратов для профилактики и лечению токсокароза ведутся и в настоящее время. М.В. Арисов и др. [4] исследовали комплексный препарат на основе фипронила 0,4%, миксодектина 0,1% и пирипроксифена 0,2%.
Д.Ю. Дергачев [20] проводил исследование нового производного бензимидазола и получил терапевтическую эффективность в дозе 7,5 мг/кг.
М.С. Гогоберишвили [17] отмечает высокую эффективность каниверма и дронтала плюс. Эффективность последнего по сравнению с канивермом составило 100% против 96,3%. Однако, анализируя приводимые данные, следует отметить эффективность каниверма, при испытании на 16 щенках, только в одном случае были выявлен яйца токсокар.
Т. Дж. Хопкинс [41] оценивает эффективность препарата Дронтал плюс в отношении T. canis у собак на уровне 94%. В состав этого препарата входят пирантел, празиквантел и фебантел.
З.Г. Мусаев [27] использовал для лечения собак комбинированный препарат на основе аверсектина С (0,5 мг/кг) и празиквантела (5мг/кг) однократно внутримышечно с эффективностью 100%. Необходимо отметить, что все исследования проводились на базе кинологического питомника, а собаки были заражены несколькими видами гельминтов.
А.М. Смирнов с соавторами [38] получили положительный эффект от применения празицид-комплекса, состоящего из ивермектина, празиквантела и левамизола.
В.А. Оробец [30] использовала для лечения собак с гельминтозами новую форму альбендазола в дозе 10 мг/кг.
А.П. Богачева [14] получила положительные результаты при использовании отодектина (0,1% раствор ивермектина) в дозе 200 мкг/кг. Такие же результаты были получены И.А. Прохоровой [48]: при двукратном использовании той же дозы с интервалом в 8 дней эффективность лечения достигала 100%.
Читайте также:

