Термодинамика необратимых процессов реферат
Обновлено: 05.07.2024
Оглавление
Введение…………………………………………………………………………. 3
1. Основные законы термодинамики…………………………………………….4
1.1. Первый закон термодинамики…………………………………………….4
1.2. Второй закон термодинамики……………………………………………..6
1.3. Третий закон термодинамики……………………………………………. 9
2. Применение в теплофизике…………………………………………………..11
Заключение……………………………………………………………………….12
Список литературы………….………………………………………………. 13
Введение
Термодинамика — раздел физики, изучающий наиболее общие свойства макроскопических систем [1] и способы передачи и превращения энергии в таких системах. Данный раздел занимается изучением состояний и процессов, которые определены разнообразными связями с температурой. Термодинамика во многом опирается на обобщение опытных фактов, то есть она является феноменологической наукой. Все термодинамические процессы описываются макроскопическими величинами. Основными из них являются следующие величины: температура, давление, концентрация компонентов. Они вводятся для описания систем, состоящих из большого количества частиц, при этом не применяются к отдельным составляющим вещества.
В данное время термодинамика относится к строгой теории, развивающейся на основе нескольких постулатов, которые имеют определенную связь со свойствами частиц и законами их взаимодействия. Это обусловлено не только процессами самой термодинамики, но и статической физикой. Именно статическая физика занимается выяснением границ применимости термодинамики [3].
Все законы термодинамики имеют общий характер и не зависят от определенных деталей строения вещества на молекулярном уровне, поэтому они применяются довольно-таки широком круге науки и техники, затрагивая самые разные области: энергетика, химия, теплотехника, машиностроение, материаловедение, инженерия и т.д. Для каждой области термодинамика имеет большое значение и находит свое применение в ней [2].
1. Основные законы термодинамики
1.1. Первый закон термодинамики
Закон о сохранении и превращении энергии для термодинамической системы является первым законом термодинамики. По его определению работа может совершаться за счет какого-либо существующего вида энергии, например теплоты. Поэтому работу и количество теплоты, как и энергию измеряют в одних единицах – Джоулях.
Первое начало термодинамики было сформулировано немецким ученым Ю. Л. Манером в 1842 г. и подтверждено экспериментально английским ученым Дж. Джоулем в 1843 г.
Первый закон термодинамики формулируется так: изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
ΔU = A + Q, где ΔU — изменение внутренней энергии, A — работа внешних сил, Q — количество теплоты, переданной системе.
Из (ΔU = A + Q) следует закон сохранения внутренней энергии. Если систему изолировать от внешних воздействий, то A = 0 и Q = 0, а, следовательно, и ΔU = 0.
При любых процессах, происходящих в изолированной системе, ее внутренняя энергия остается постоянной.
Если работу совершает система, а не внешние силы, то уравнение (ΔU = A + Q) записывается в виде:
Q = ΔU + Á, где A' — работа, совершаемая системой (A' = -A).
Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Первый закон определяет собой невозможность существования вечного двигателя, который мог бы совершать работу исключительно за счет своей внутренней энергии, не используя сторонней.
Действительно, если к телу не поступает теплота (Q - 0), то работа A', согласно уравнению первый закон термодинамики, совершается только за счет убыли внутренней энергии А' = -ΔU. После того, как запас энергии окажется исчерпанным, двигатель перестает работать.
Следует помнить, что как работа, так и количество теплоты, являются характеристиками процесса изменения внутренней энергии, поэтому нельзя говорить, что в системе содержится определенное количество теплоты или работы. Система в любом состоянии обладает лишь определенной внутренней энергией.
1.2. Второй закон термодинамики
Второй закон термодинамики указывает на существование энтропии [4] как функции состояния термодинамической системы и вводит понятие абсолютной термодинамической температуры. То есть второе начало определяет начало об энтропии, а также её свойствах и признаках. Важно отметить, что энтропия, находясь в изолированной системе, остается либо неизменной, либо возрастает (в условиях неравновесных процессов). Энтропия достигает своего максимума при установлении термодинамического равновесия. Это определено законом возрастания энтропии. Частым образом в литературных источниках встречаются разнообразные формулировки второго закона термодинамики, являясь следствиями закона возрастания энтропии.
Второй закон тесно связан с понятием энтропии (S). Она порождается буквально всеми процессами и связана с потерей способности системы совершать работу. Рост энтропии является стихийным процессом. Изменения в системе увеличения энтропии происходят в том случае, если объем и энергия системы не являются постоянными. В обратном случае (если объем и энергия непостоянны) энтропия подвержена уменьшению.
Чтобы можно было использовать энергию, необходимо иметь в системе области с высоким и низким уровнем энергии. Полезная работа производится в результате передачи энергии от области с высоким уровнем энергии к области с низким уровнем энергии.
Если в замкнутой системе происходит процесс, то энтропия этой системы не убывает. В виде формулы второй закон термодинамики записывают как:
где S – энтропия; L – путь, по которому система переходит из одного состояния в другое.
В данной формулировке второго начала термодинамики следует обратить внимание на то, что рассматриваемая система должна быть замкнутой. В незамкнутой системе энтропия может вести себя как угодно (и убывать, и возрастать, и оставаться постоянной). Заметим, что энтропия не изменяется в замкнутой системе при обратимых процессах.
Рост энтропии в замкнутой системе при необратимых процессах — это переход термодинамической системы из состояний с меньшей вероятностью в состояния с большей вероятностью. Известная формула Больцмана дает статистическое толкование второго закона термодинамики:
где k – постоянная Больцмана; w – термодинамическая вероятность (она определяет количество способов реализации макросостояния системы). Таким образом, второе начало термодинамики определяется статическим законом, непосредственно связанным с описанием закономерностей теплового движения молекул (при этом движение является хаотическим). Данное движение молекул и составляет систему термодинамики.
Второй закон термодинамики имеет другие формулировки. Из них можно выделить две основных – формулировка Кельвина и формулировка Клаузнуса.
Формулировка Кельвина звучит следующим образом: невозможно создать круговой процесс, результатом которого станет исключительно превращение теплоты, которое получено от нагревателя, в работу. Данная формулировка позволяет сделать вывод о невозможности создания вечного двигателя второго рода. Это означает, что периодически действующая тепловая машина должна иметь нагреватель, рабочее тело и холодильник. При этом КПД идеальной тепловой машины не может быть больше, чем КПД цикла Карно:
где Tn – температура нагревателя; Th — температура холодильника; (T_n > T_h).
Формулировка Клаузиуса имеет следующий вид: невозможно создать круговой процесс, в результате которого будет происходить исключительно передача тепла от тела с меньшей температурой к телу с большей температурой.
Таким образом, второй закон термодинамики обуславливает огромное различие между двумя формами передачи энергии, а именно между работой и теплотой [5]. Данный закон позволяет сделать вывод о том, что переход упорядоченного перемещения тела является необратимым процессом. Притом такое перемещение может переходить в хаотическое движение без каких-либо дополнительных процессов.
1.3. Третий закон термодинамики
Третий закон термодинамики носит и другое название – теорема Нернста. Она основана на физическом принципе, который определяет энтропию при приближении температуры к абсолютному нулю. Закон определен обобщением значительного количества экспериментальных данных по термодинамике гальванических элементов [6]. Теорема сформулирована Вальтером Нернстом в 1906 году. Современная формулировка теоремы принадлежит Максу Планку.
Теорема Нернста утверждает, что всякий термодинамический процесс, протекающий при фиксированной температуре T в сколь угодно близкой к нулю не должен сопровождаться изменением энтропии S, то есть изотерма T=0 совпадает с предельной адиабатой S0.
Данная теорема имеет несколько эквивалентных между собой формулировок:
- энтропия любой системы при температуре, значение которой приближено к абсолютному нулю, является универсальной постоянной и не зависящей от различных переменных параметров;
- при приближении к абсолютному нулю энтропия стремится к конкретному пределу, который не зависит от конечного состояния системы;
- приращение энтропии при приближении к абсолютному нулю не может зависеть от различных значений параметров термодинамики, всегда стремится к конечному определенному пределу;
- при процессах, происходящих при абсолютном нуле, система способна переходить из одного состояния равновесия в другое, при этом энтропия совершенно не изменяется [7].
Данный закон позволяет находить абсолютное значение энтропии. Этого нельзя сделать в рамках первого и второго закона термодинамики, поскольку в них энтропия определяется с точностью до произвольной аддитивной постоянной S0. Это не мешает исследованию и изучению термодинамических процессов, разность энтропий измеряется в различных состояниях.
Третий закон термодинамики имеет определенные следствия:
- абсолютный нуль температур не может достигаться ни в каких конечных процессах, связанных с изменением энтропии. К нулю можно приближаться лишь асимптотически;
- стремление теплоемкости к нулю при постоянном давлении и объеме. К нулю стремятся также коэффициенты теплого расширения и другие аналогичные величины [8].
Справедливость третьего начала термодинамики одно время подвергалась сомнению, но позже было выяснено, что все кажущиеся противоречия (ненулевое значение энтропии у ряда веществ при T=0) связаны с метастабильными состояниями вещества, которые нельзя считать термодинамически равновесными.
2. Применение в теплофизике
Каждый закон термодинамики имеет своё применение в теплофизике. Первый закон имеет практическое применение к различным процессам в физике. К примеру, благодаря ему можно вычислить идеальные параметры газа при самых разнообразных процессах, как тепловых, так и механических.
Применение второго закона имеет достаточно обширную область, поскольку относится ко всем процессам естествознания. Там, где встречается превращение нестройных видов энергии молекул и атомов в более стройную форму механической или электрической энергии, второй закон термодинамики проводит свою линию. Именно на его основах стоит физическая и теоретическая химия, а вместе с этим спектральный анализ и большая часть астрофизики.
Третий закон термодинамики иначе называется постулатом Нернста. В свою очередь его формулировка звучит следующим образом: с помощью конечного числа процессов нельзя достигнуть абсолютного нуля. Это говорит о том, что никаким способом невозможно остановить молекулы и атомы веществ. Этот процесс обусловлен постоянным теплообменом с окружающей средой. Рассмотрев закон, можно сказать, что уменьшение энтропии заключается в движении к абсолютному нулю. Данный вывод можно использовать в различных областях, применяя его во многих ситуациях. К примеру, для перевода парамагнетиков в ферромагнитное состояние при охлаждении.
Таким образом, применение трех законов термодинамики распространено во многих областях науки и жизни человека в целом. Во многом термодинамика упрощает жизнь, позволяет совершать новые открытия.
Заключение
Термодинамика в физике обусловлена существованием трех законов, каждый из которых имеет свою определенную формулировку. Она во многом имеет общую связь с процессами энтропии и её основными свойствами. Термодинамика играет большую роль в различных областях и сферах жизни человека. Её правила и закономерности оставляют след в следующих областях: теплотехника, энергетика, биология, машиностроение и другие. Кроме того термодинамика позволяет совершать новые открытия человечества. Это было бы невозможно без основных законов, открытых великими учеными в прошлом.
Таким образом, изучив и рассмотрев основные аспекты данной темы, можно сказать, что термодинамические процессы в физике являются немаловажными и играют большую роль в науке. Такой раздел физики, как термодинамика, всегда будет актуальным, поскольку он позволяет совершенствовать существующие аспекты науки и формировать новые.
Список литературы
Базаров И. П. Термодинамика. — М.: Высшая школа, 1991. — 376 с.
Воронин Г. Ф. Основы термодинамики. — М.: Изд-во Моск. ун-та, 1987. — 192 с.
Гиббс Дж. Термодинамика. Статистическая механика. Серия: Классики науки. М.: Наука 1982. 584 с.
Квасников И. А. Термодинамика и статистическая физика. Т. 1: Теория равновесных систем: Термодинамика. — Изд. 2, сущ. перераб. и доп.. — М.: Едиториал УРСС, 2002. — 240 с.
Киттель Ч. Статистическая термодинамика. — М.: Наука, 1977. — 336 с.
Кубо Р. Термодинамика. М.: Мир, 1970.
Сивухин Д. В. Общий курс физики. — Т. II. Термодинамика и молекулярная физика. — 5 изд., испр.. — М.: ФИЗМАТЛИТ, 2005. — 544 с.
Ферми Э., Термодинамика. Харьков: Изд-во Харьковского ун-та, 1969. — 140 с.
Нет нужной работы в каталоге?

Сделайте индивидуальный заказ на нашем сервисе. Там эксперты помогают с учебой без посредников Разместите задание – сайт бесплатно отправит его исполнителя, и они предложат цены.
Цены ниже, чем в агентствах и у конкурентов
Вы работаете с экспертами напрямую. Поэтому стоимость работ приятно вас удивит
Бесплатные доработки и консультации
Исполнитель внесет нужные правки в работу по вашему требованию без доплат. Корректировки в максимально короткие сроки
Если работа вас не устроит – мы вернем 100% суммы заказа
Техподдержка 7 дней в неделю
Наши менеджеры всегда на связи и оперативно решат любую проблему
Строгий отбор экспертов

Требуются доработки?
Они включены в стоимость работы ![]()

Работы выполняют эксперты в своём деле. Они ценят свою репутацию, поэтому результат выполненной работы гарантирован
Термодинамика изучает закономерности теплового движения в равновесных системах и при переходе систем в равновесие (классическая или равновесная, термодинамическая), а так же обобщает эти закономерности на неравновесные системы равновесная термодинамическая или термодинамика необратимых процессов.
Термодинамика необратимых процессов является сравнительно молодым и интенсивно развивающимся разделом термодинамической физики. Она возникла в результате обобщения классической термодинамики на область малых отклонений системы от равновесия и в дальнейшем была распространена на построение теории процессов в сильно неравновесных системах.
Прежде чем перейти к изложению основных законов и методов термодинамики и изучения свойств различных систем, раскроем содержание главных термодинамических понятий.
1. Основные понятия
Макроскопическая система - всякий материальный объект, всякое тело, состоящее из большого числа частиц.
Равновесное состояние системы - это такое состояние, когда в системе не только все параметры постоянны во времени, и нет никаких стационарных потоков за счет действия каких-либо внешних источников.
Изолированная или замкнутая система - система, которая не обменивается с окружающими телами ни энергией, ни веществом.
Открытая система - система, которая обменивается с окружающими телами энергией и веществом.
Закрытая система - система, не обменивающаяся с другими телами веществом, но обменивающаяся энергией.
Энергия системы - энергия непрерывно движущихся и взаимодействующих частиц.
Полная энергия системы разделяется на внешнюю и внутреннюю.
Часть энергии, состоящая из энергии движения системы как целого и потенциальной энергии системы в поле внешних сил, называется внешней энергией. Остальная часть энергии системы называется внутренней энергией.
Количество теплоты - энергия, переданная системе без изменения её внешних параметров.
Процесс называется равновесным или квазистатическим, если все параметры системы изменяются физически бесконечно медленно, так что система все время находится в равновесных состояниях.
Время релаксации - промежуток времени, в течении которого система возвращается в состояние равновесия.
Если изменение какого-либо параметра a происходит за время t , меньшее или равное времени релаксации τ ( t ≤τ), так что , то такой процесс называется неравновесным или нестатическим.
Процесс перехода системы из состояния 1 в 2 называется обратимым, если возвращение этой системы в исходное состояние из 2 в 1 можно осуществить без каких бы то ни было изменений в окружающих внешних телах.
Процесс же перехода системы из состояния 1 в 2 называется необратимым, если обратный переход системы из 2 в 1 нельзя осуществить без изменений в окружающих телах.
2. Первое начало термодинамики
Термодинамика - дедуктивная наука. Её основные успехи могут быть охарактеризованы тем, что она позволяет получить множество различных соотношений межу величинами, определяющими состояние тел, опираясь на весьма общие электрические законы - начала-термодинамики.
Обсудим содержание этих основных законов и соответствующим им основных уравнений термодинамики.
Одной из аксиом термодинамики является первое начало термодинамики, утверждающее следующее: внутренняя энергия термодинамической системы является функцией состояния, изменяющейся только при взаимодействии с окружением. Изменение внутренней энергии связано с работой и количеством теплоты уравнением первого начала термодинамики:
Выражение (1) по существу является законом сохранения энергии, описывающим взаимодействие макросистемы с окружением.
Первое начало термодинамики, устанавливая связь между dE , δ А и δ Q , тем самым позволяет свести измерение dE к измерению макроскопических величин, таких как работа или количество теплоты.
С другой стороны, первое начало термодинамики позволяет сделать определенный вывод о той механической работе, которую можно получить в том или ином процессе, что представляет большой практический интерес. Исторически установление первого начала термодинамики (закона сохранения энергии) было связано как раз с неудачами при попытках сконструировать машину, которая совершала бы работу, не затрачивая при этом никакой энергии и не получая теплоты извне. В термодинамике такую неосуществимую машину называют вечным двигателем первого рода .
Для периодически действующей машины dE = 0; поэтому для периодического производства ею работы в силу закона сохранения энергии необходимо или подводить количество теплоты δ Q или использовать работу δ А других источников энергии. Невозможно построить вечный двигатель, который производил бы большую работу, чем количество поглощаемой им извне энергии. Последнее утверждение можно рассматривать как одну из формулировок первого начала термодинамики. В дальнейшем для обозначения элементарного изменения внутренней энергии dE , элементарной работы δ А и количества теплоты δ Q будем использовать только один символ: d .
3. Энтропия и вероятность
Понять энтропию - это знать ее происхождение, знать связь ее с другими понятиями, уметь применять энтропию на практике.
В приборе Гей-Люссака в одном шаре находится газ (при малой его плотности). Другой шар эвакуирован. Открывают кран на трубке, соединяющей оба шара. Результат опыта известен: газ равномерно заполняет оба шара. Температура всего газа та же, что и до расширения. При самопроизвольном изотермическом расширении газа увеличивается его энтропия (процесс адиабатический, и энтропия источников теплоты не изменяется). Самопроизвольное сжатие газа в приборе Гей-Люссака до прежнего объема исключено: энтропия уменьшилась бы.
Газ состоит из молекул (некоторые газы состоят из атомов). В газе малой плотности одна молекула воздействует на другую только в короткие моменты столкновений между молекулами. Большую же часть времени молекула свободно двигается по объему, предоставленному всему газу.
Предположим, что физик может отличить одну молекулу от других. Физика спрашивают, в каком шаре находится выбранная молекула, подчеркнутая красным, как говорил Эйнштейн. (Объемы шаров, чтобы упростить рассуждения, равны) Физик ответит: до наблюдения не знаю. Он сошлется на то, что на выбранную молекулу (как и на все остальные) ничего не воздействует. Выбранная молекула (как и все остальные) никак не предпочитает один шар другому. Объемы шаров равны. Поэтому и физик не может предпочесть один шар другому. На техническом языке, вероятность нахождения выбранной молекулы в любом из шаров равна половине. Сумма вероятностей равна единице (половина плюс половина), равна достоверности. В каком-нибудь из двух шаров выбранная молекула обязательно находится.
Физику дальше ставят как будто совсем неразрешимый вопрос: в каком из шаров находятся все молекулы газа? На вопрос, где находится одна выбранная молекула, физик не мог ответить. Где же ему ответить на второй вопрос?! Ведь при О °С и 1 атм в 1 см 3 газа находится 2,7x10 19 молекул. [Для сопоставления: пять миллиардов лет (возраст Земли) - 1,6х10 17 секунд.] Физик, однако, с полной уверенностью ответит: ни в одном из шаров не содержатся все молекулы газа. Молекулы газа равномерно распределены между обоими шарами. Во всяком случае, отклонение от равномерного распределения при значительном объеме шаров, значит, и при большом числе молекул крайне мало, и этим отклонением можно спокойно пренебречь.
Откуда такая уверенность? Из подсчета вероятностей. Именно потому, что для каждой молекулы вероятность находиться в том или другом шаре равна половине, все молекулы не могут находиться в одном только шаре. Вероятность такого случая тем меньше, чем больше число молекул. При том числе молекул, с каким обычно имеют дело в термодинамике, вероятность скопления всех молекул в одном только шаре чрезвычайно мала. Выдающийся французский математик Э. Борель (1871-1956) писал: "Я пришел к выводу, что не следует бояться применить слово достоверность для обозначения вероятности, которая отличается от единицы на достаточно малую величину". Статистический закон для большого числа молекул пробил себе дорогу через случайности для отдельной молекулы.
Приведенный пример свидетельствует, что существует связь между возрастанием энтропии в опыте Гей-Люссака и вероятностью распределения газа между обоими шарами. Обобщая, можно сказать: при самопроизвольном процессе система переходит из менее вероятного состояния в более вероятное.
4. Энтропия и приведенная теплота
Первое начало термодинамики позволяет определить, возможен ли с энергетической точки зрения тот или иной процесс в замкнутой системе. Но оно ничего не говорит о возможных направлениях процессов (в частности самопроизвольных). Так, например, первый закон не запрещает самопроизвольного перехода теплоты от холодного тела к горячему, либо концентрирования газа в малой части сосуда и снижения давления в остальной части сосуда. Но, как известно, в природе такие процессы не наблюдаются.
Для суждения о возможном направлении процессов в термодинамике вводится еще одна функция состояния - энтропия.
Так как энтропия является функцией состояния макросистемы, то внутренняя энергия может рассматриваться как функция энтропии и, в простейшем случае, одного внешнего параметра, например V .
При равновесных процессах . С другой стороны, первое начало термодинамики утверждает, что
Сравнивая выражения (2) и (3), нетрудно установить тождественность этих соотношений при условии выполнения равенств:
Из равенства (4) видно, что для обратимых процессов
Так как dS является полным дифференциалом, то и величина также есть полный дифференциал, т.е. множитель является для количества теплоты dQ нормирующим. Величина называется приведенной теплотой , ее значение можно определить экспериментально, что имеет большое практическое значение.
Зная элементарное изменение энтропии dS , можно без труда найти и конечное изменение этой величины для любого обратимого процесса. Именно:
Если обратимый процесс характеризуется замкнутым циклом, то очевидно изменение энтропии и контурный интеграл от приведенной теплоты в этом случае равны нулю (рис.1):
Для адиабатного обратимого процесса приведенная теплота равна нулю, а энтропия остается постоянной. Однако если процесс протекает необратимо, то энтропия, как было выяснено ранее, возрастает, т.е. для адиабатного необратимого процесса (9).
Изменение энтропии при необратимых адиабатных процессах наводит на мысль использовать эту величину для характеристики необратимости любых процессов в макросистемах. Причем за меру необратимости удобно принять разность между dS и , которая равна нулю для обратимых процессов и больше нуля для необратимых.
Используя это соображение, можно утверждать, что все процессы в макросистемах протекают таким образом, что
Если процесс круговой, то
причем знак неравенства относится к неравновесным процессам, а равенство характеризует равновесные процессы.
Таким образом, энтропия действительно является такой функцией состояния, применение которой позволяет определить направленность протекания реальных процессов в макросистемах. Второе начало термодинамики выражает это утверждение в форме постулата.
Похожие страницы:
Экология (21)
. химии, биологии, но и в экологии для решения проблем, связанных с изменением состояния окружающей . ). Фундаментальным понятием термодинамики необратимых процессов является стационарное состояние системы. Процесс жизнедеятельности биообъектов сопровождается .
Экология и безопасность жизнедеятельности (1)
. , ванадия, сурьмы, теллура). Американский эколог О. Бартон так охарактеризовал проблему, связанную с запыленностью атмосферы . необратимых процессов компенсируется ее притоком от Солнца. Условие стационарности согласно первому началу термодинамики .
Экология: конспект лекций
Термодинамика и открытые системы
. соответствии со вторым началом термодинамики для необратимых процессов энтропия системы S . , развивающееся. При рассмотрении проблем такого мира надо учитывать . включая биосферу в целом (глобальная экология), биотехнологии (генная инженерия), системы .
Концепции современного естествознания (31)
. курсов физики, химии, биологии и экологии - это продукт междисциплинарного синтеза на . культуры - гуманитарный и естественнонаучный. §§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§§ Изучив процесс становления естественнонаучных картин мира, историю .

ГОСТ
Термодинамика необратимых процессов заключается в неравновесности и предметом ее изучения является закономерность поведения различных систем, которые не находятся в состоянии термодинамического равновесия.
Рисунок 1. Необратимые процессы/ Автор24 — интернет-биржа студенческих работ
Прежде всего, под подобными процессами понимают:
- теплопередачу;
- диффузию;
- электрический ток;
- химические реакции.
Неравновесные процессы протекают в различных системах и характеризуются своей необратимостью в термодинамическом смысле.
Основные задачи необратимых процессов в термодинамике
В термодинамике выделяют ряд задач необратимых процессов. Они способны:
- исследовать балансы физических величин, в том числе массы, энтропии и энергии при превращениях и переходах энергии;
- устанавливать законы эволюции макроскопических систем.
Термодинамика необратимых процессов заключается в введении переменной времени, которая не присутствует в равновесном термодинамическом процессе. Принято различать феноменологическую термодинамику необратимых процессов, а также статистическую теорию неравновесных процессов. При этом сама феноменологическая термодинамика подразделяется на линейную и нелинейную теории.
Первое начало термодинамики для изопроцессов. Автор24 — интернет-биржа студенческих работ">
Рисунок 2. Первое начало термодинамики для изопроцессов. Автор24 — интернет-биржа студенческих работ
Готовые работы на аналогичную тему
В общем смысле при рассмотрении термодинамике необратимых процессов уделяют внимание на познание нескольких типов систем. Среди них оказались:
- однородные;
- прерывные;
- непрерывные.
Так, в однородных системах параметры состояния приобретают интенсивные свойства в любой момент времени, при этом температура, давление и химический потенциал остаются в тех значениях по всему объему рабочего тела.
При прерывных типах необратимых процессов системы могут состоять из нескольких однородных частей, которые разделены границей фаз или иным техническим приспособлением. К примеру, вентилем, что направляет в определенную сторону газы, жидкости и иные рабочие среды. Подобные типы систем принято называть вентильными или гетерогенными. В этих системах свойства меняются резко при переходе из одной фазы взаимодействия в другую.
В непрерывных типах интенсивные свойства начинают действовать внутри системы с определенной точкой координат и времени.
В виде балансовых уравнений записываются соотношения, которые характеризуют процессы переноса массы, энергии, заряда и энтропии. Подобные формулы имеют смысл при написании для непрерывных и прерывных систем. Примечательной особенностью этих систем стало наличие величин двух основных типов. Первые характеризуются и распознаются в виде потоков, вторые – трактуются в форме силы. При этом потоки формулируют скорость переноса определенной физической величины. Это может быть масса, энтропия, энергия. Перенос происходит сквозь воображаемую площадку. Также для этих целей подходит обычная химическая реакция.
Причиной зарождения потока стали термодинамические силы. В непрерывных системах они играют роль особых градиентов. При переносе в прерывных системах имеют характер конечных разностей изучаемых величин.
Виды неравновесных процессов
Рисунок 3. Неравновесные термодинамические системы. Автор24 — интернет-биржа студенческих работ
Существует несколько основных видов неравновесных процессов. Их делят на векторные, скалярные, тензорные. При этом силы и потоки в системах должны иметь признаки и соответствовать векторам, скалярам и тензорам. Для описания подобных процессов необходимо пользоваться скалярным, векторным или тензорным полем второго ранга.
Группа скалярных процессов состоит из химических реакций. В векторных процессах главными составляющими являются теплопроводность, диффузия, направление. Также с ними плотно связывают поля векторов потоков вещества и тепла.
В тензорном неравновесном процессе причиной его возникновения служит течение вязкого типа. Подобные процессы не имеют формального значения, однако связаны с принципом Кюри.
Принцип локального равновесия
Макроскопический объект является элементом объема неравновесной силы всей системы. Такие свойства он приобретает в любой момент времени, при этом должен находиться в состоянии равновесия. Из этого понятия формируется принцип локального равновесия.
Его идея лежит в плоскости введения понятия малых дополнительных систем, которые как бы отдыхают (покоятся) в равновесии быстрее, чем этого достигает вся система в целом. Если рассматривать этот принцип с точки зрения феноменологической теории, то он будет иметь смысл основополагающего понятия для линейной и нелинейной термодинамики. Постулат для необратимых процессов может использовать ряд фундаментальных уравнений равновесной термодинамики. Это необходимо для того, чтобы тщательно можно было исследовать неравновесные процессы во всем многообразии.
Также для изучения неравновесных процессов в термодинамике необратимых процессов активно используют особую систему уравнений, которая связывает потоки и силы в одно выражение. Они также основаны на общем термодинамическом подходе. В этом случае силы и потоки распределяют путем производства энтропии. Оно выражается всегда в стандартной билинейной форме уравнений.
Сегодня линейная феноменологическая термодинамика необратимых процессов стала теорией с законченным смыслом. Она имеет огромное техническое практическое применение во многих областях науки и в промышленном производстве. В них часто используют процессы диффузии, вязкого течения, а также теплопередачи. Все подобные процессы не могут выполняться без предварительных просчетов и согласований на теоретическом уровне. Также они учитываются в процессе проектирования и анализе режимов работы химических реакторов, точной аппаратуры, приборов и иных устройствах, используемых в производственном режиме.
Кроме построения линейной термодинамики необратимых процессов в рамках локальной полевой теории есть также собственный запасной подход, который основан на использовании найденных ранее вариационных принципов. Подобный принцип ввел в обращение Онсангер. Его называют принципом наименьшего рассеяния энергии, и он ориентирован на поиск оптимального альтернативного решения поставленных задач в термодинамике.
Первый закон термодинамики – закон сохранения тепловых процессов, устанавливающий связь между количеством теплоты Q и изменением ∆ U внутренней энергии и работой А , совершенной над внешними телами:
Исходя из закона, энергия не может быть создана или уничтожена: производится процесс передачи от одной системы к другой, принимая другую форму. Еще не было получено процессов, нарушающих первый закон термодинамики. Рисунок 3 . 12 . 1 показывает устройства, противоречащие первому закону.
Рисунок 3 . 12 . 1 . Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный двигатель 1 рода, совершающий работу без потребления энергии извне; 2 – тепловая машина с коэффициентом полезного действия η > 1 .
Обратимый и необратимый процессы
Первый закон термодинамики не устанавливает направления тепловых процессов. Опыты показывают, что большинство тепловых процессов протекают в одном направлении. Их называют необратимыми.
Если имеется тепловой контакт двух тел с разными температурами, тогда направление теплового потока направляется от теплого к холодному. Самопроизвольной передачи тепла от тела с низкой температуры к телу с высокой не наблюдается. Отсюда следует, что теплообмен с конечной разностью температур считается необратимым.
Обратимым процессом называется переход системы из одного равновесного расстояния в другое, которые возможно проводить в обратном направлении в той же последовательности промежуточных равновесных состояний. Она вместе с окружающими телами возвращаются к исходному состоянию.
Если система находится в состоянии равновесия во время процесса, она называется квазистатической.
Когда рабочее тело тепловой машины контактирует с тепловым резервуаром, температура которого неизменна во время всего процесса, то только изотермический квазистатический процесс считается обратимым, так как протекает с бесконечно малой разницей температур рабочего резервуара. Если имеется два резервуара, причем с разными температурами, тогда обратимым путем можно провести процессы на двух изотермических участках.
Так как адиабатический процесс проводится в обоих направлениях (сжатие и расширение), наличие кругового процесса с двумя изотермами и двумя адиабатами (цикл Карно) говорит о том, что это и есть единственный обратимый круговой процесс, где рабочее тело контактируется с двумя тепловыми резервуарами. Остальные при наличии 2 тепловых резервуаров считаются необратимыми.
Превращение механической работы во внутреннюю энергию считаются необратимыми при наличии силы трения, диффузии в газах и жидкостях, а процесс перемешивания по причине начальной разности давлений и так далее. Все реальные процессы считаются необратимыми, даже если значения будут максимально приближены к обратимым. Обратимые рассматриваются как пример реальных процессов.
Первый закон термодинамики не различает их. Правило требует от термодинамического процесса определенного энергетического баланса, но не говорит о том, возможен ли он. Установка направления прохождения процесса определяется вторым законом термодинамики. Его формулировка может звучать как запрет на определенные термодинамические процессы.
Второй закон был трактован У. Кельвином в 1851 .
В циклически действующей тепловой машине невозможно прохождение процесса, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара.
Предположительно, машина с такими процессами могла бы получить название вечного двигателя второго рода.
При земных условиях могла бы быть отбита энергия Мирового океана и полностью превратилась бы в ее работу. Масса воды Мирового океана – 10 21 к г . Для его охлаждения хотя бы на 1 градус потребуется огромное количество энергии ≈ 10 24 Д ж , которое сравнимо с сжиганием 10 17 к г угля. Вырабатываемая энергия на Земле за год в 10 4 раз меньше. Отсюда и вывод о том, что вечный двигатель второго рода мало вероятен, как и двигатель первого, потому как оба они недопустимы, исходя из первого закона термодинамики.
Второй закон термодинамики
Формулировка 2 -го закона термодинамики была дана физиком Р. Клаузиусом.
Невозможно прохождение процесса, единственным результатом которого была бы передача энергии при помощи теплообмена от тела с низкой температуры к телу с более высокой.
Рисунок 3 . 12 . 2 объясняет процессы, которые запрещены вторым законом, но разрешены согласно первому. Они соответствуют трактовкам второго закона термодинамики.
Рисунок 3 . 12 . 2 . Процессы, не противоречащие первому закону термодинамики, но запрещаемые вторым законом: 1 – вечный двигатель второго рода; 2 – самопроизвольный переход тепла от холодного тела к более теплому (идеальная холодильная машина).
Формулировки обоих законов считаются эквивалентными.
Когда тело без помощи внешних сил переходит при теплообмене от холодного к горячему, то возникает мысль о возможности создания вечного двигателя второго рода. Если такая машина получит количество теплоты Q 1 от нагревателя и отдаст холодильнику Q 2 , тогда совершается работа A = Q 1 - Q 2 . Если бы Q 2 самопроизвольно перешло к нагревателю, то конечный результат тепловой машины и идеальной холодильной машины выглядело бы таким образом Q 1 - Q 2 . Причем сам переход происходил бы без изменений холодильника. Отсюда вывод – комбинация тепловой машины и идеальной холодильной машины равноценна двигателю второго рода.
Прослеживается связь между вторым законом термодинамики и необратимостью реальных тепловых процессов. Энергия теплового движения молекул отлична от механической, электрической и так далее. Она способна превратиться в другой вид энергии только частично. Поэтому при наличии энергии теплового движения молекул любой процесс считается необратимым, так как полностью в обратном направлении он не осуществим.
Свойство, относящееся к необратимым процессам, говорит о том, что они проходят в термодинамически неравновесной системе, а результат получается в виде замкнутой системы, приближающейся к состоянию термодинамического равновесия.
Теоремы Карно
Имеются теоремы Карно, которые могут быть доказаны, исходя из второго закона термодинамики.
КПД тепловой машины, работающей при данных значениях температур нагревателя холодильника, не может иметь значение больше, чем КПД действия машины, работающей согласно обратимому циклу Карно с теми же значениями температур нагревателя и холодильника.
КПД действия тепловой машины, работающей по циклу Карно, не зависит от рода рабочего тела, а только от температур нагревателя и холодильника.
Отсюда следует, что КПД действия машины с циклом Карно считается максимальным.
η = 1 - Q 2 Q 1 ≤ η m a x = η К а р н ю = 1 - T 2 T 1 .
Знак равенства данной записи говорит об обратимости процесса. Если машина работает по циклу Карно, тогда:
Q 2 Q 1 = T 2 T 1 или Q 2 T 2 = Q 1 T 1 .
Знаки Q 1 и Q 2 всегда отличаются независимо от направления цикла. Поэтому получаем:
Q 1 T 1 + Q 2 T 2 = 0 .
Рисунок 3 . 12 . 3 говорит о том, что данное соотношение обобщается и представляется в виде последовательности малых изометрических и адиабатических участков.
Рисунок 3 . 12 . 3 . Произвольный обратимый цикл как последовательность малых изотермических и адиабатических участков.
Полный обход замкнутого обратимого цикла имеет вид:
∑ ∆ Q i T i = 0 (обратимый цикл).
Откуда ∆ Q i = ∆ Q 1 i + ∆ Q 2 i – количество теплоты, полученное рабочим телом на двух изотермических участках с температурой T i . Чтобы данный цикл провести наоборот, нужно рабочее тело сконтактировать со многими тепловыми резервуарами с T i .
Энтропия
Отношение Q i T i получило название приведенного тепла. Формула показывает, что полное приведенное тепло на любом обратимом цикле равно нулю. Благодаря ей вводится еще одно понятие – энтропия, обозначаемая S . Ее открыл Р. Клаузиус в 1865 году.
При переходе из одного равновесного состояние в другое изменяется и ее энтропия. Разность энтропий двух состояний равняется приведенному теплу, полученному системой во время обратного перехода состояния.
∆ S = S 2 - S 1 = ∑ ( 1 ) ( 2 ) ∆ Q i о б р T .
Если рассматривается адиабатический процесс ∆ Q i = 0 , тогда энтропия S не изменяется.
Изменение энтропии ∆ S во время перехода в другое состояние фиксируется как формула:
∆ S = ∫ ( 1 ) ( 2 ) d Q о б р T .
Определение энтропии достаточно точное. Разность ∆ S двух состояний системы подразумевает физический смысл. Если имеется необратимый переход, а необходимо найти энтропию, тогда нужно придумать обратимый процесс, который свяжет начальное и конечное состояние. После этого перейти к нахождению приведенного тепла, полученного системой.
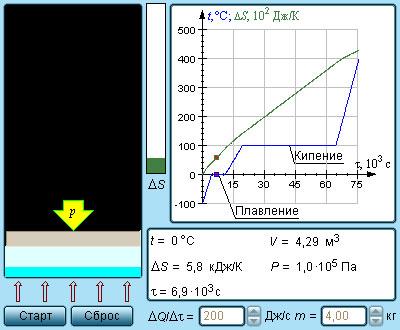
Рисунок 3 . 12 . 4 Модель энтропии и фазовых переходов.
Рисунок 3 . 12 . 5 показывает необратимый процесс расширения шага с отсутствием теплообмена. Равновесными считаются начальное и конечное значение, изображаемые на диаграмме p , V . Точки a и b соответствуют состояниям и располагаются на одной изотерме. Чтобы найти ∆ S , следует перейти к рассмотрению обратимого изотермического перехода из a в b . При изопроцессе газ получает определенное количество теплоты окружающих тел Q > 0 , тогда при необратимом расширении энтропия возрастет до ∆ S > 0 .
Еще одним примером необратимого процесса считается теплообмен при конечной разности температур. Рисунок 3 . 12 . 6 и показывает два тела, заключенные в адиабатическую оболочку, где начальные температуры обозначаются как T 1 и T 2 T 1 . Течение процесса теплообмена способствует выравниванию температур. Очевидно, что теплое тело отдает, а холодное принимает. Холодное тело превосходит по модулю приведенное тепло, отдаваемое горячим. Отсюда вывод – изменение энтропии в замкнутой системе необратимого процесса ∆ S > 0 .
Рисунок 3 . 12 . 6 . Теплообмен при конечной разности температур: a – начальное состояние; b – конечное состояние системы. Изменение энтропии Δ S > 0 .
Все самопроизвольно протекающие процессы в изолированных термодинамических процессах характеризуются ростом энтропии.
Обратимые процессы имеют постоянную энтропию ∆ S ≥ 0 . Соотношение называют законом возрастания энтропии.
При любых процессах, протекающих в термодинамических изолированных системах, энтропия либо не меняется, либо возрастает.
Наличие энтропии говорит о самопроизвольно протекающем процессе, а ее рост – приближение всей системы к термодинамическому равновесию, где S принимает максимальное значение. Возрастание энтропии можно трактовать как формулировку второго закона термодинамики.
В 1878 году Л. Больцман дал вероятностное определение понятию энтропии, так как было предложено рассматривать ее в качестве меры статистического беспорядка замкнутой термодинамической системы. Все самопроизвольно протекающие процессы в таких системах приближают ее к равновесному состоянию, так как сопровождаются ростом энтропии, и направляют в сторону увеличения вероятности состояния.
Если состояние макроскопической системы содержит большое число частиц, то его реализация может предусматривать несколько способов.
Термодинамическая вероятность W системы – это количество способов, которыми реализуется данное состояние макроскопической системы, макросостояний, осуществляющих его.
Из определения имеем, что W ≫ 1 .
При наличии 1 м о л ь газа в емкости существует число N способов размещения молекулы по двум половинам емкости: N = 2 N А , где N А - число Авогадро. Каждое из них – это микросостояние.
Одно из них соответствует случаю с молекулами, собранными в одной половине сосуда. Вероятность такого события приравнивается к нулю. Большое количество состояний соответствует такому, где молекулы распределяются равномерно по всей площади емкости.
Тогда равновесное состояние является наиболее вероятным.
Равновесное состояние считается состоянием наибольшего беспорядка в термодинамической системе с максимальной энтропией.
Исходя из трактовок Больцмана, энтропия S и термодинамическая вероятность W связаны:
S = k · ln W , где k = 1 , 38 · 10 - 23 Д ж / К является постоянная Больцмана. Отсюда следует, что определение энтропии определяется логарифмом числа микросостояний. Именно они способствуют реализации данного макросостояния. Тогда энтропия может быть рассмотрена в качестве меры вероятности состояния термодинамической системы.
Вероятностная трактовка второго закона термодинамики допускает самопроизвольное отклонение системы от состояния термодинамического равновесия. Их называют флуктуациями.
В системах с большим числом частиц отклонения от состояния равновесия имеют достаточно малую вероятность на существование.
Первый закон термодинамики – закон сохранения тепловых процессов, устанавливающий связь между количеством теплоты Q и изменением ∆ U внутренней энергии и работой А , совершенной над внешними телами:
Исходя из закона, энергия не может быть создана или уничтожена: производится процесс передачи от одной системы к другой, принимая другую форму. Еще не было получено процессов, нарушающих первый закон термодинамики. Рисунок 3 . 12 . 1 показывает устройства, противоречащие первому закону.
Рисунок 3 . 12 . 1 . Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный двигатель 1 рода, совершающий работу без потребления энергии извне; 2 – тепловая машина с коэффициентом полезного действия η > 1 .
Обратимый и необратимый процессы
Первый закон термодинамики не устанавливает направления тепловых процессов. Опыты показывают, что большинство тепловых процессов протекают в одном направлении. Их называют необратимыми.
Если имеется тепловой контакт двух тел с разными температурами, тогда направление теплового потока направляется от теплого к холодному. Самопроизвольной передачи тепла от тела с низкой температуры к телу с высокой не наблюдается. Отсюда следует, что теплообмен с конечной разностью температур считается необратимым.
Обратимым процессом называется переход системы из одного равновесного расстояния в другое, которые возможно проводить в обратном направлении в той же последовательности промежуточных равновесных состояний. Она вместе с окружающими телами возвращаются к исходному состоянию.
Если система находится в состоянии равновесия во время процесса, она называется квазистатической.
Когда рабочее тело тепловой машины контактирует с тепловым резервуаром, температура которого неизменна во время всего процесса, то только изотермический квазистатический процесс считается обратимым, так как протекает с бесконечно малой разницей температур рабочего резервуара. Если имеется два резервуара, причем с разными температурами, тогда обратимым путем можно провести процессы на двух изотермических участках.
Так как адиабатический процесс проводится в обоих направлениях (сжатие и расширение), наличие кругового процесса с двумя изотермами и двумя адиабатами (цикл Карно) говорит о том, что это и есть единственный обратимый круговой процесс, где рабочее тело контактируется с двумя тепловыми резервуарами. Остальные при наличии 2 тепловых резервуаров считаются необратимыми.
Превращение механической работы во внутреннюю энергию считаются необратимыми при наличии силы трения, диффузии в газах и жидкостях, а процесс перемешивания по причине начальной разности давлений и так далее. Все реальные процессы считаются необратимыми, даже если значения будут максимально приближены к обратимым. Обратимые рассматриваются как пример реальных процессов.
Первый закон термодинамики не различает их. Правило требует от термодинамического процесса определенного энергетического баланса, но не говорит о том, возможен ли он. Установка направления прохождения процесса определяется вторым законом термодинамики. Его формулировка может звучать как запрет на определенные термодинамические процессы.
Второй закон был трактован У. Кельвином в 1851 .
В циклически действующей тепловой машине невозможно прохождение процесса, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара.
Предположительно, машина с такими процессами могла бы получить название вечного двигателя второго рода.
При земных условиях могла бы быть отбита энергия Мирового океана и полностью превратилась бы в ее работу. Масса воды Мирового океана – 10 21 к г . Для его охлаждения хотя бы на 1 градус потребуется огромное количество энергии ≈ 10 24 Д ж , которое сравнимо с сжиганием 10 17 к г угля. Вырабатываемая энергия на Земле за год в 10 4 раз меньше. Отсюда и вывод о том, что вечный двигатель второго рода мало вероятен, как и двигатель первого, потому как оба они недопустимы, исходя из первого закона термодинамики.
Второй закон термодинамики
Формулировка 2 -го закона термодинамики была дана физиком Р. Клаузиусом.
Невозможно прохождение процесса, единственным результатом которого была бы передача энергии при помощи теплообмена от тела с низкой температуры к телу с более высокой.
Рисунок 3 . 12 . 2 объясняет процессы, которые запрещены вторым законом, но разрешены согласно первому. Они соответствуют трактовкам второго закона термодинамики.
Рисунок 3 . 12 . 2 . Процессы, не противоречащие первому закону термодинамики, но запрещаемые вторым законом: 1 – вечный двигатель второго рода; 2 – самопроизвольный переход тепла от холодного тела к более теплому (идеальная холодильная машина).
Формулировки обоих законов считаются эквивалентными.
Когда тело без помощи внешних сил переходит при теплообмене от холодного к горячему, то возникает мысль о возможности создания вечного двигателя второго рода. Если такая машина получит количество теплоты Q 1 от нагревателя и отдаст холодильнику Q 2 , тогда совершается работа A = Q 1 - Q 2 . Если бы Q 2 самопроизвольно перешло к нагревателю, то конечный результат тепловой машины и идеальной холодильной машины выглядело бы таким образом Q 1 - Q 2 . Причем сам переход происходил бы без изменений холодильника. Отсюда вывод – комбинация тепловой машины и идеальной холодильной машины равноценна двигателю второго рода.
Прослеживается связь между вторым законом термодинамики и необратимостью реальных тепловых процессов. Энергия теплового движения молекул отлична от механической, электрической и так далее. Она способна превратиться в другой вид энергии только частично. Поэтому при наличии энергии теплового движения молекул любой процесс считается необратимым, так как полностью в обратном направлении он не осуществим.
Свойство, относящееся к необратимым процессам, говорит о том, что они проходят в термодинамически неравновесной системе, а результат получается в виде замкнутой системы, приближающейся к состоянию термодинамического равновесия.
Теоремы Карно
Имеются теоремы Карно, которые могут быть доказаны, исходя из второго закона термодинамики.
КПД тепловой машины, работающей при данных значениях температур нагревателя холодильника, не может иметь значение больше, чем КПД действия машины, работающей согласно обратимому циклу Карно с теми же значениями температур нагревателя и холодильника.
КПД действия тепловой машины, работающей по циклу Карно, не зависит от рода рабочего тела, а только от температур нагревателя и холодильника.
Отсюда следует, что КПД действия машины с циклом Карно считается максимальным.
η = 1 - Q 2 Q 1 ≤ η m a x = η К а р н ю = 1 - T 2 T 1 .
Знак равенства данной записи говорит об обратимости процесса. Если машина работает по циклу Карно, тогда:
Q 2 Q 1 = T 2 T 1 или Q 2 T 2 = Q 1 T 1 .
Знаки Q 1 и Q 2 всегда отличаются независимо от направления цикла. Поэтому получаем:
Q 1 T 1 + Q 2 T 2 = 0 .
Рисунок 3 . 12 . 3 говорит о том, что данное соотношение обобщается и представляется в виде последовательности малых изометрических и адиабатических участков.
Рисунок 3 . 12 . 3 . Произвольный обратимый цикл как последовательность малых изотермических и адиабатических участков.
Полный обход замкнутого обратимого цикла имеет вид:
∑ ∆ Q i T i = 0 (обратимый цикл).
Откуда ∆ Q i = ∆ Q 1 i + ∆ Q 2 i – количество теплоты, полученное рабочим телом на двух изотермических участках с температурой T i . Чтобы данный цикл провести наоборот, нужно рабочее тело сконтактировать со многими тепловыми резервуарами с T i .
Энтропия
Отношение Q i T i получило название приведенного тепла. Формула показывает, что полное приведенное тепло на любом обратимом цикле равно нулю. Благодаря ей вводится еще одно понятие – энтропия, обозначаемая S . Ее открыл Р. Клаузиус в 1865 году.
При переходе из одного равновесного состояние в другое изменяется и ее энтропия. Разность энтропий двух состояний равняется приведенному теплу, полученному системой во время обратного перехода состояния.
∆ S = S 2 - S 1 = ∑ ( 1 ) ( 2 ) ∆ Q i о б р T .
Если рассматривается адиабатический процесс ∆ Q i = 0 , тогда энтропия S не изменяется.
Изменение энтропии ∆ S во время перехода в другое состояние фиксируется как формула:
∆ S = ∫ ( 1 ) ( 2 ) d Q о б р T .
Определение энтропии достаточно точное. Разность ∆ S двух состояний системы подразумевает физический смысл. Если имеется необратимый переход, а необходимо найти энтропию, тогда нужно придумать обратимый процесс, который свяжет начальное и конечное состояние. После этого перейти к нахождению приведенного тепла, полученного системой.

Рисунок 3 . 12 . 4 Модель энтропии и фазовых переходов.
Рисунок 3 . 12 . 5 показывает необратимый процесс расширения шага с отсутствием теплообмена. Равновесными считаются начальное и конечное значение, изображаемые на диаграмме p , V . Точки a и b соответствуют состояниям и располагаются на одной изотерме. Чтобы найти ∆ S , следует перейти к рассмотрению обратимого изотермического перехода из a в b . При изопроцессе газ получает определенное количество теплоты окружающих тел Q > 0 , тогда при необратимом расширении энтропия возрастет до ∆ S > 0 .
Еще одним примером необратимого процесса считается теплообмен при конечной разности температур. Рисунок 3 . 12 . 6 и показывает два тела, заключенные в адиабатическую оболочку, где начальные температуры обозначаются как T 1 и T 2 T 1 . Течение процесса теплообмена способствует выравниванию температур. Очевидно, что теплое тело отдает, а холодное принимает. Холодное тело превосходит по модулю приведенное тепло, отдаваемое горячим. Отсюда вывод – изменение энтропии в замкнутой системе необратимого процесса ∆ S > 0 .
Рисунок 3 . 12 . 6 . Теплообмен при конечной разности температур: a – начальное состояние; b – конечное состояние системы. Изменение энтропии Δ S > 0 .
Все самопроизвольно протекающие процессы в изолированных термодинамических процессах характеризуются ростом энтропии.
Обратимые процессы имеют постоянную энтропию ∆ S ≥ 0 . Соотношение называют законом возрастания энтропии.
При любых процессах, протекающих в термодинамических изолированных системах, энтропия либо не меняется, либо возрастает.
Наличие энтропии говорит о самопроизвольно протекающем процессе, а ее рост – приближение всей системы к термодинамическому равновесию, где S принимает максимальное значение. Возрастание энтропии можно трактовать как формулировку второго закона термодинамики.
В 1878 году Л. Больцман дал вероятностное определение понятию энтропии, так как было предложено рассматривать ее в качестве меры статистического беспорядка замкнутой термодинамической системы. Все самопроизвольно протекающие процессы в таких системах приближают ее к равновесному состоянию, так как сопровождаются ростом энтропии, и направляют в сторону увеличения вероятности состояния.
Если состояние макроскопической системы содержит большое число частиц, то его реализация может предусматривать несколько способов.
Термодинамическая вероятность W системы – это количество способов, которыми реализуется данное состояние макроскопической системы, макросостояний, осуществляющих его.
Из определения имеем, что W ≫ 1 .
При наличии 1 м о л ь газа в емкости существует число N способов размещения молекулы по двум половинам емкости: N = 2 N А , где N А - число Авогадро. Каждое из них – это микросостояние.
Одно из них соответствует случаю с молекулами, собранными в одной половине сосуда. Вероятность такого события приравнивается к нулю. Большое количество состояний соответствует такому, где молекулы распределяются равномерно по всей площади емкости.
Тогда равновесное состояние является наиболее вероятным.
Равновесное состояние считается состоянием наибольшего беспорядка в термодинамической системе с максимальной энтропией.
Исходя из трактовок Больцмана, энтропия S и термодинамическая вероятность W связаны:
S = k · ln W , где k = 1 , 38 · 10 - 23 Д ж / К является постоянная Больцмана. Отсюда следует, что определение энтропии определяется логарифмом числа микросостояний. Именно они способствуют реализации данного макросостояния. Тогда энтропия может быть рассмотрена в качестве меры вероятности состояния термодинамической системы.
Вероятностная трактовка второго закона термодинамики допускает самопроизвольное отклонение системы от состояния термодинамического равновесия. Их называют флуктуациями.
В системах с большим числом частиц отклонения от состояния равновесия имеют достаточно малую вероятность на существование.
Читайте также:


