Синтез эйкозаноидов их биологическая роль реферат
Обновлено: 30.06.2024
Эйкозаноиды — окисленные производные полиненасыщенных жирных кислот — эйкозотриеновой (С20:3), арахидоновой (эйкозотетраеновая, С20:4), тимнодоновой (эйкозопентаеновая, С20:5). Пищевыми источниками полиненасыщенных жирных кислот являются растительные масла, рыбий жир и препараты омега-3-жирных кислот.
Депонироваться эйкозаноиды не могут, разрушаются в течение нескольких секунд, поэтому клетка должна синтезировать их постоянно из поступающих в неё соответствующих жирных кислот.
Работа содержит 1 файл
Eikozanoidy.docx
Казахский Национальный Медицинский Университет имени С.Д. Асфендиярова
Кафедра Биологической Химии
Выполнил: Жунисбеков Г.Ш.
Факультет: Общая Медицина
Проверила: Колесникова Л.Г.
Эйкозаноиды — окисленные производные полиненасыщенных жирных кислот — эйкозотриеновой (С20:3), арахидоновой (эйкозотетраеновая, С20:4), тимнодоновой (эйкозопентаеновая, С20:5). Пищевыми источниками полиненасыщенных жирных кислот являются растительные масла, рыбий жир и препараты омега-3-жирных кислот.
Депонироваться эйкозаноиды не могут, разрушаются в течение нескольких секунд, поэтому клетка должна синтезировать их постоянно из поступающих в неё соответствующих жирных кислот.
Выделяют три основные группы эйкозаноидов:
Простагландины (Pg) — синтезируются практически во всех клетках, кроме эритроцитов и лимфоцитов. Выделяют типы простагландинов A, B, C, D, E, F. Их функции сводятся к изменению тонуса гладких мышц бронхов, мочеполовой и сосудистой систем, желудочно-кишечного тракта, при этом направленность изменений различна в зависимости от типа простагландинов и условий. Они также влияют на температуру тела.
Простациклины являются подвидом простагландинов (Pg I), но дополнительно обладают особой функцией — ингибируют агрегацию тромбоцитов и обусловливают вазодилятацию. Особенно активно синтезируются в эндотелии сосудов миокарда, матки, слизистой желудка.
Тромбоксаны (Tx) образуются в тромбоцитах, стимулируют их агрегацию и вызывают сужение мелких сосудов.
Лейкотриены (Lt) активно синтезируются в лейкоцитах, в клетках лёгких, селезёнки, мозга, сердца. Выделяют 6 типов лейкотриенов: A, B, C, D, E, F. В лейкоцитах они стимулируют подвижность, хемотаксис и миграцию клеток в очаг воспаления. Также вызывают сокращение мускулатуры бронхов в дозах в 100—1000 раз меньших, чем гистамин.
В зависимости от исходной жирной кислоты все эйкозаноиды делят на три группы:
Первая группа образуется из эйкозотриеновой кислоты. Хотя в пищевых продуктах этой кислоты нет, она способна образовываться в клетках при удлинении линолевой кислоты (С18:3), которой много в растительных маслах. Для этой группы в соответствии с числом двойных связей простагландинам и тромбоксанам присваивается индекс 1, лейкотриенам — индекс 3: например, PgE1, PgI1, TxA1, LtA3.
Вторая группа синтезируется из арахидоновой кислоты (С20:4), по тому же правилу эйкозаноидам этой группы присваивается индекс 2 или 4: например, PgE2, PgI2, TxA2, LtA4.
Третья группа эйкозаноидов производится из тимнодоновой кислоты (С20:5), по числу двойных связей присваиваются индексы 3 или 5: например, PgE3, PgI3, TxA3, LtA5.
Подразделение эйкозаноидов на группы имеет клиническое значение, так как их активность напрямую зависит от числа двойных связей. Особенно это изучено и ярко проявляется на примере простациклинов и тромбоксанов. В ряду простациклинов от PgI1 до PgI3 возрастает антиагрегационная и вазодилататорная активность, в ряду Tx1 до Tx3 снижается проагрегационаая и вазоконстрикторная активность. В целом вязкость крови и тонус сосудов весьма существенно понижаются, что актуально для больных гипертензией.
Результирующим эффектом использования в пищу полиненасыщенных жирных кислот является образование тромбоксанов и простациклинов с большим числом двойных связей, что сдвигает реологические свойства крови к снижению вязкости, понижению тромбообразования, расширяет сосуды и улучшает кровоснабжение тканей. Наличие лейкотриенов с 5 двойными связями активирует лейкоциты и ускоряет течение воспалительных реакций, предотвращая их хронизацию. Интересно, что PgE1 (то есть всего одна двойная связь) препятствует расщеплению жира в жировой ткани.
1)Биохимия: Учебник для мед.вузов / под ред. Е.С. Северина. — М.: ГЭОТАР-МЕД, 2003.
2)Титов В.Н. Патогенез атеросклероза для XXI века (обзор литературы) // Клинич. лаб. диагностика. — 1998, № 1, с. 3-11.
3)Титов В.Н. Биологическое обоснование применения полиненасыщенных жирных кислот семейства w3 в профилактике атеросклероза // Вопросы питания. — 1999, № 3, с. 34-40.
4)Эндакова Э.А., Новгородцева Т.П., Светашев В.И. Модификация состава жирных кислот крови при сердечнососудистых заболеваниях. – Владивосток: Дальнаука, 2002
Эйкозаноиды – обширная группа физиологически и фармакологически активных соединений. К ним относятся простаноиды (простагландины, простациклины, тромбоксаны) и лейкотриены.
Наиболее активным предшественником эйкозаноидов является входящая в состав фосфолипидов плазматических мембран арахидоновая кислота. Последняя освобождается из фосфолипидного бислоя мембраны при действии фосфолипазы А2. В образовании эйкозаноидов принимают участие также и другие незаменимые жирные кислоты (линолевая и α-лино-леновая), но только после элонгации на два углеродных атома и десату-рации, т.е. после превращения в 20-углеродные тетраеновые кислоты. Поэтому эйкозаноиды можно разделить на 3 группы (в каждую входят простагландины, тромбоксаны и лейкотриены) в зависимости от предшественников: линолеата, арахидоната и линолената.
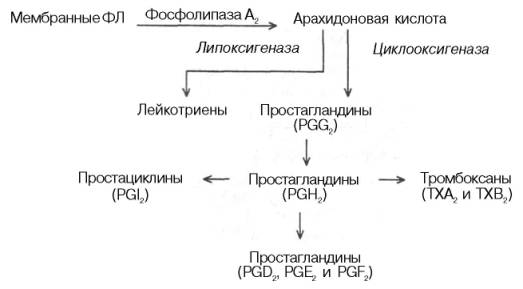
Рис. 11.5. Участие арахидоновой кислоты в образовании эйкозаноидов (по А.Н. Климову и Н.Г. Никульчевой).
Пути метаболизма арахидоната (субстрата) различны, причем синтез простаноидов конкурирует за субстрат с синтезом лейкотриенов. Эти два пути называют соответственно циклооксигеназным и липоксигеназным (рис. 11.5).
Простагландины (ПГ, Pg). По существу ПГ представляют собой 20-углеродные жирные кислоты, содержащие 5-углеродное кольцо и гидро-кси- и/или кетогруппы:
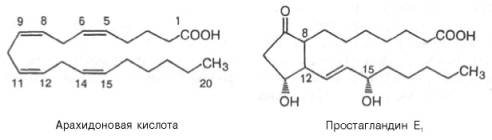
Обнаружено шесть первичных природных ПГ, три из них серии Е (ether-soluble) и три – серии F (phosphate-soluble). ПГ серии Е содержат в положении 9 кетогруппу, а ПГ серии F – гидроксигруппу. Имеется также несколько вторичных ПГ, представляющих собой продукты энзиматическо-го превращения первичных.
ПГ проявляют свое действие в чрезвычайно низких концентрациях (1– 10 нг/мл). Будучи введенными в организм, они вызывают сокращение гладкой мускулатуры, регулируют приток крови к определенному органу, оказывают переменчивое влияние на кровяное давление, контролируют транспорт ионов через мембраны и т.д.
В целом ПГ, не являясь гормонами, модулируют действие последних. Они преимущественно влияют на физиологические функции тех клеток, в которых синтезируются. Характер воздействия ПГ зависит от типа клетки, и этим ПГ отличаются от гормонов с их однозначным эффектом.
ПГ могут использоваться как терапевтическое средство для предотвращения оплодотворения, стимулирования нормальных родов, прерывания беременности, предупреждения развития или обезболивания язвы желудка, лечения воспалительных процессов и регуляции кровяного давления, а также для снятия приступов астмы и др.
Среди продуктов эндопероксидации вторичных ПГ необходимо отметить тромбоксаны и простациклины. Тромбоксаны образуются в тромбоцитах и после выхода в кровяное русло вызывают сужение кровеносных сосудов и агрегацию тромбоцитов.
Простациклины образуются в стенках кровеносных сосудов и являются сильными ингибиторами агрегации тромбоцитов. Таким образом, тромбо-ксаны и простациклины выступают как антагонисты. Поэтому соотношение тромбоксана и простациклина во многом определяет условия тромбообра-зования на поверхности эндотелия сосудов. Приводим формулы двух важнейших представителей этих соединений:
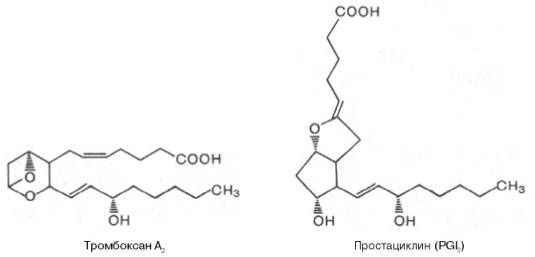
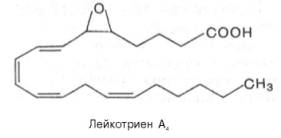
Лейкотриены прежде всего рассматриваются как медиаторы воспалительных реакций; они вызывают сокращение мышечной ткани бронхов в концентрациях, в 100–1000 раз меньших, чем гистамин; способствуют сокращению коронарных сосудов. В целом функция лейкотриенов в норме и при патологии во многом еще неясна.
Источником для синтеза эйкозаноидов служат фосфолипиды мембран клетки. Под влиянием фосфолипазы А2 из фосфолипидов высвобождается свободная арахидоновая кислота (см. схему 1). Дальнейший метаболизм этой кислоты протекает по трем независимым путям:
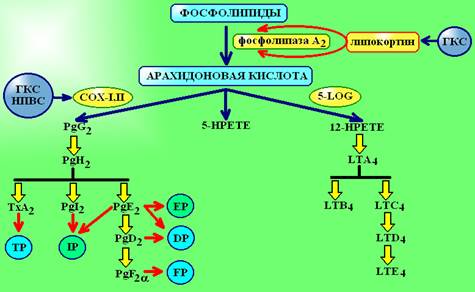
Схема 1. Биосинтез эйкозаноидов. COX-I,II - циклооксигеназы I и II типов, 5-LOG – 5-липоксигеназа, Pg – простагландины, LT – лейкотриены, 5- и 12-HPETE – 5- и 12-гидропероксиэйкозатетраеновые кислоты, ГКС – глюкокортикостероиды, НПВС – нестероидные противовоспалительные средства. На схеме показаны рецепторы для простагландинов ТР, IP, ЕР, DP, FP.
· Циклооксигеназный путь. Под влиянием гемсодержащего фермента циклооксигеназы (ЦОГ) образуются циклические эндоперикиси PgG2 и PgH2, которые являются весьма нестойкими и подвергаются воздействию 3 ферментов: 1) изомеразы, которая преобразует их в PgE2, PgD2 и PgF2a; 2) тромбоксанситетазы, которая преобразует их в ТхА2; 3) простациклинсинтетазы, которая синтезирует из них простациклин (PgI2);
· Р450-монооксигеназный путь. В этом пути арахидоновая кислота окисляется до 19-гидрокси или 20-гидрокси-эйкозатетраеновых кислот (19-НЕТЕ и 20-НЕТЕ), а также эпоксиэйкозатетраеновой кислоты (ОЕТЕ);
· Липоксигеназный путь. Под влиянием фермента 5-липоксигеназы (5-ЛОГ) из арахидоновой кислоты вначале образуется 5-НРЕТЕ, которая подвергается восстановлению до LTA4, а затем либо гидролизу до LTB4, либо конъюгации с глутатионом до LTC4, LTD4, LTE4.
На схемах 2 и 3 более подробно показан ЦОГ- и ЛОГ-зависимый путь метаболизма арахидоновой кислоты в тканях млекопитающих. Основными эйкозаноидами в клетках млекопитающих являются простагландины ряда [2] и лейкотриены ряда [4]. В клетках некоторых других организмов (например, морских рыб) основными эйкозаноидами служат простагландины ряда [3] и лейкотриены ряда [5], которые синтезируются из эйкозапентаеновой и докозагексаеновой кислот. Использование этих эйкозаноидов или их кислот-предшественниц у человека вызывает ряд положительных эффектов, которые однако, не являются предметом нашей дискуссии.
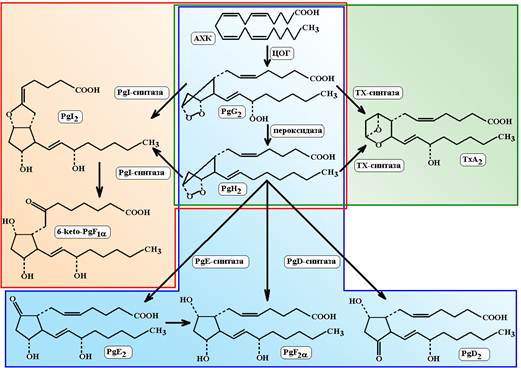
Схема 2. ЦОГ-зависимый путь метаболизма арахидоновой кислоты. Превращение арахидоновой кислоты (АХК) в эндоперикиси PgG2 и PgH2 (циклооксигеназная и пероксидазная реакции) катализируются одним и тем же ферментом – ЦОГ-1,2.
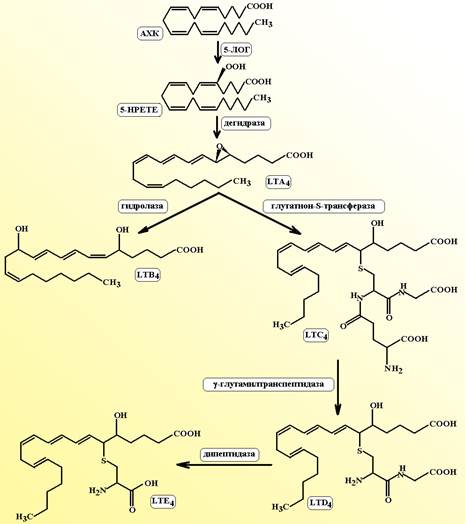
Схема 3. ЛОГ-зависимый путь метаболизма арахидоновой кислоты. Липоксигеназная и дегидразная стадии контролируются ферментом 5-ЛОГ.
В организме человека эйкозаноиды выполняют ряд важных функций, некоторые из них приведены в таблице 3.
Таблица 3. Физиологическая роль эйкозаноидов в организме.
| Мишени | Эйкозаноид | Эффект |
| Дыхательные пути | LTC4, LTD4 | Сокращение бронхов. |
| Сердечно-сосудистая система | PgI2 PgE2 LTC4, LTD4 | Понижение артериального давления Функционирование ductus arteriosus Повышение, а затем снижение АД, коронарного кровотока |
| Кровь | PgI2 TxA2 PgE2 19- и 20-HETE | Снижение свертываемости крови и агрегации тромбоцитов Повышение свертываемости крови и агрегации тромбоцитов Увеличение секреции эритропоэтина Увеличение секреции эритропоэтина |
| Почки | PgI2, PgE2 | · Увеличение кровотока в почках · Увеличение диуреза, натрий- и калийуреза · Устранение эффекта АДГ · Усиление секреции ренина. |
| ЖКТ | PgE2 PgE2, PgF2a | Снижение секреции соляной кислоты и пепсина в желудке · Усиление секреции слизи с желудке · Усиление моторики кишечника и секреции в него воды |
| Эндокринные железы | PgE2 PgF2a LTC4, LTD4, ОЕТЕ | · Усиление секреции АКТГ, СТГ, ЛТГ, ФСГ, ЛГ · Увеличение синтеза стероидов · Усиление секреции инсулина и липолитический эффект · Увеличение синтеза прогестерона желтым телом Снижение синтеза прогестерона желтым телом Усиление секреции гонадолиберина и ЛГ |
| ЦНС | PgE2 | · Регуляция процессов сна; · Термогенез (регуляция температуры тела) · Ноцицепция (восприятие боли) |
| Репродуктивная система | PgE2, PgF2a | · У женщин стимуляция сокращения миометрия · У мужчин эрекция |
Синтез простагландинов, как уже было сказано выше, протекает под влиянием ЦОГ. Выделяют две изоформы этого фермента, которые имеют ряд отличий (см. таблицу 4).
Таблица 4. Изоформы циклооксигеназы.
| Признак | ЦОГ-1 | ЦОГ-2 |
| Ген | 9 хромосома | 1 хромосома |
| Строение | Длинный гидрофобный канал содержит участок связывания арахидоната (Arg120-Tyr385) и каталитический центр (Ser530) | Гидрофобный канал содержит участок связывания арахидоната (Arg120-Tyr385), каталитический центр имеет боковую полость из-за замены крупного Ile523 на Val523 |
| Регуляция | Конститутивная – фермент постоянно присутствует в клетке | Индуцибельная – синтез фермента происходит при развитии воспаления, беременности. В почках и ЦНС выполняет роль конститутивной ЦОГ. |
| Функция | Синтез простагландинов, участвующих в: · физиологических процессах; · восприятии острой боли. | Синтез простагландинов, участвующих в: · процессе воспаления; · восприятии хронической боли; · онкогенезе; · развитии болезни Альцгеймера. |
Таким образом, синтез простагландинов, которые осуществляют нормальные физиологические процессы, происходит под влиянием ЦОГ-1, тогда как воспалительные реакции связаны с образованием простагландинов под влиянием ЦОГ-2.
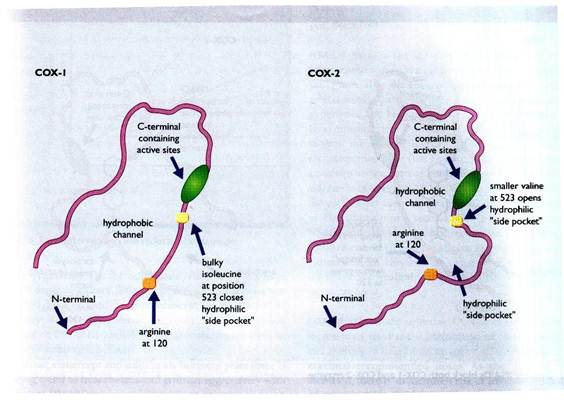
Схема 4. Изоформы ЦОГ. Замена крупного изолейцина на валин приводит к формированию бокового кармана в молекуле ЦОГ-2.
Фармакологические подходы к регуляции процесса воспаления.
Исходя из представленного выше процесса образования эйкозаноидов, можно предложить следующие подходы к регуляции воспалительной реакции:
Эйкозаноиды - это общая группа физиологически и фармакологически активных соединений включающая в себя простаноиды (простагландины, простоциклины, тромбоксаны) и лейкотриены. Оказывают эффекты как "гормоны местного действия". Главный субстрат для синтеза эйкозаноидов у человека - арахидоновая кислота, так как её содержание в организме человека значительно больше остальных полиеновых кислот - предшественников эйкозаноидов.

Число двойных связей в боковых цепях простагландинов зависит от структуры предшественника - полистовой кислоты, из которой образовались простагландины. Две двойные связи полиеновой кислоты используются при образовании кольца в молекуле простагландина, а количество оставшихся двойных связей в радикалах, связанных с кольцом, определяет серию простагландина: 1 - если одна двойная связь, 2 - если две двойные связи и 3 - если в радикалах имеются три двойных связи.
Тромбоксаны. В отличие от простагландинов, тромбоксаны синтезируются только в тромбоцитах, откуда и происходит их название, и стимулируют их агрегацию при образовании тромба.
Тромбоксаны имеют шестичленное кольцо, включающее атом кислорода. Так же, как и другие эйкозаноиды, тромбоксаны могут содержать различное число двойных связей в боковых цепях, образуя ТХ А2, или ТХ A3, отличающиеся по активности. ТХ В2 - продукт катаболизма ТХ А2 и активностью не обладает.
Синтез простагландинов. Фермент, катализирующий первый этап синтеза простагландинов, называется PG Н2 синтазой и имеет 2 каталитических центра. Один из них называют циклооксигеназой, другой - пероксидазой. Этот фермент представляет собой димер гликопротеинов, состоящий из идентичных полипептидных цепей.
В организме имеются 2 типа циклооксигеназ (PG Н2 синтаз). Циклооксигеназа 1 - конститутивный фермент, синтезирующийся с постоянной скоростью. Синтез циклооксигеназы 2 увеличивается при воспалении и индуцируется соответствующими медиаторами - цитокинами. Оба типа циклооксигеназ катализируют включение 4 атомов кислорода в арахидоновую кислоту и формирование пятичленного кольца. В результате образуется нестабильное гидропероксидпроизводное, называемое PG G2.
Дальнейшие превращения PG Н2 специфичны для каждого типа клеток. Например, PG Н2 в клетках ГМК может быть восстановлен под действием PG E синтазы с образованием PG Е2 или под действием PG D синтазы с образованием PG D2.
31. Биохимическая роль вторичных мессенджеров при передаче гормонального сигнала.
Вторичные посредники (вторичные мессенджеры, англ. second messengers) — это малые сигнальные молекулы, компоненты системы передачи сигнала в клетке. Вторичные посредники являются компонентами каскадов передачи сигнала, быстро образуются и далее активируют эффекторные белки, которые опосредуют ответ клетки. К наиболее распространенным вторичным посредникам относятся- сАМР,Са +2 ,Инозитол-трифосфат (ИФЗ),Диацилглицерол (ДАГ),c GMP.
Концентрация вторичных посредников в цитозоле может быть повышена различными путями: активацией ферментов, которые их синтезируют, как, например в случае активации циклаз, образующих циклические формы нуклеотидов (цАМФ, цГМФ), либо путем открывания ионных каналов, позволяющих потоку ионов металлов, например, ионов кальция войти в клетку. Эти малые молекулы могут далее связывать и активировать эффекторные молекулы — протеинкиназы, ионные каналы и разнообразные другие белки.
Гормоны, нейромедиаторы и другие агонисты способны быстро активировать внутриклеточные процессы. Агонисты взаимодействуют с рецепторами на наружной стороне клеточной мембраны , далее сигнал передается в клетку путем активации синтеза вторичных посредников
Механизм действия. цАМФ является аллостерическим эффектором протеинкиназ А (ПК-Α) и ионных каналов. В неактивном состоянии ПК-Α является тетрамером, две каталитические субъединицы (К-субъединицы) которого ингибированы регуляторными субъединицами (Р-субъединицы) (аутоингибирование). При связывании цАМФ Р-субъединицы диссоциируют из комплекса и К-единицы активируются. Фермент может фосфорилировать определенные остатки серина и треонина в более чем 100 различных белках, в том числе во многих ферментах и факторах транскрипции. В результате фосфорилирования изменяется функциональная активность этих белков.
Уровень ионов кальция. Концентрация ионов Са2+ в цитоплазме нестимулированной клетки очень низка (10-100 нМ). Низкий уровень поддерживается кальциевыми АТФ-азами (кальциевыми насосами) и натрий-кальциевыми обменниками. Резкое повышение концентрации ионов Са2+ в цитоплазме (до 500-1000 нМ) происходит в результате открывания кальциевых каналов плазматической мембраны или внутриклеточных кальциевых депо (гладкого и шероховатого эндоплазматического ретикулума). Открывание каналов может быть вызвано деполяризацией мембран или действием сигнальных веществ, нейромедиаторов, вторичных мессенджеров (ИФ3 и цАМФ), а также вещества растительного происхождения рианодина. В цитоплазме и клеточных органеллах имеется множество белков способных связывать Са2+, некоторые из них выполняют роль буфера.
Действие кальция опосредовано специальными Са2+-связывающими белками, к которым принадлежат аннексин, кальмодулин и тропонин. Кальмодулин — сравнительно небольшой белок (17 кДа) — присутствует во всех животных клетках. При связывании четырех ионов Са2+ кальмодулин переходит в активную форму, способную взаимодействовать с многочисленными белками. За счет активации кальмодулина ионы Са2+ оказывают влияние на активность ферментов, ионных насосов и компонентов цитоскелета.
Читайте также:

