Синдром раздраженного кишечника у детей реферат
Обновлено: 04.07.2024
Синдром раздраженного кишечника (СРК) является одной из наиболее распространенных форм функциональных расстройств органов пищеварения как у взрослых, так и у детей и подростков. В обзоре рассмотрены вопросы этиологии и патогенеза СРК, в частности одной из его форм — постинфекционного СРК (ПИ-СРК), ассоциированного с перенесенной острой кишечной инфекцией. В данном обзоре обсуждаются факторы риска, вопросы диагностики и лечения ПИ-СРК. Авторы приводят собственное клиническое наблюдение развития ПИ-СРК у ребенка с описанием тактики диагностического поиска и лечения. Лечение больных с СРК заключается в коррекции диеты и образа жизни, приеме фармакологических средств, применении психотерапевтических методов воздействия. Представленное клиническое наблюдение актуально для клиницистов, поскольку в настоящее время только предпринимаются попытки систематизировать рекомендации по диагностике и лечению ПИ-СРК. Специфические лечебные рекомендации для ПИ-СРК не разработаны, что часто затрудняет постановку диагноза этой формы СРК и приводит к более позднему старту терапии.
Ключевые слова: синдром раздраженного кишечника, функциональные расстройства органов пищеварения, прокинетик, синбиотик, Максилак.
D.V. Pechkurov, A.A. Tyazheva
Samara State Medical University, Samara, Russian Federation
Irritable bowel syndrome (IBS) is one of the most common functional gastrointestinal disorders in adults, children, and adolescents. This paper reviews the etiology and pathogenesis of IBS, particularly one of its subtypes, postinfectious IBS, associated with a prior acute intestinal infection. The authors discuss risk factors, diagnosis, and treatment for postinfectious IBS and describe diagnostic search and therapeutic algorithm in a child. Treatment for IBS involves changes in diet and lifestyle, pharmacotherapy, and psychotherapy.This case report is interesting for clinicians since only attempts are made to systematize guidelines on the diagnosis and treatment for postinfectious IBS. However, specific management strategies for this condition are scarce, making the diagnosis difficult and resulting in treatment delay.
Keywords: irritable bowel syndrome, functional gastrointestinal disorders, prokinetic agent, synbiotic, Maxilac.
Введение
Синдром раздраженного кишечника (СРК) является одной из наиболее распространенных форм функциональных расстройств органов пищеварения (ФРОП) не только у взрослых, но и у детей и подростков. Распространенность СРК варьирует в пределах 10–15% [1, 2]. Считается, что СРК характерен в большей степени для лиц молодого и среднего возраста, среди пациентов преобладают лица, не достигшие 50 лет [2, 3]. Подъем заболеваемости СРК приходится и на подростковый возраст, в котором частота встречаемости достигает 35%. У детей до 6 лет с ФРОП, протекающими с абдоминальными болями, СРК диагностируется в четверти случаев, причем, как правило, в этой возрастной группе он развивается в исходе острых кишечных инфекций (ОКИ) [4, 5].
Все формы СРК оказывают значительное влияние на качество жизни, вызывают тревожность у пациентов, что в свою очередь снижает эффективность лечения. Все это подчеркивает клиническую и социальную значимость данного заболевания [6–8].
СРК: классификация, этиология и патогенез
Причиной боли у больных СРК выступает так называемый феномен висцеральной гиперчувствительности [13]. На возможную триггерную роль когнитивно-поведенческих расстройств в формировании СРК указывают M.J. Spence et al. [14]: высокий уровень тревожности, негативное восприятие болезни, депрессия, ипохондрия увеличивают риск развития СРК после перенесенной кишечной инфекции.
Согласно действующей классификации выделяют варианты СРК по преобладанию клинических признаков:
неспецифический, или смешанный, вариант.
По этиологическим механизмам выделяют следующие варианты СРК:
классический, индуцированный стрессом;
связанный с пищевой непереносимостью, индуцированный пищей;
постинфекционный, ассоциированный с перенесенной ОКИ (ПИ-СРК).
Считается, что от 3% до 33% больных, перенесших инфекционный гастроэнтерит, отмечают впоследствии симптомы ПИ-СРК [15]. Впервые описание ПИ-СРК выполнил G.T. Stewart [16] в 1950 г. по данным наблюдения за пациентами, перенесшими дизентерию. ПИ-СРК развивается у 4–32% пациентов после перенесенного бактериального гастроэнтерита, вызванного бактериями родов Campylobacter, Salmonella, Shigella, Yersinia [17]. В настоящее время доказано, что не только острые бактериальные гастроэнтероколиты являются серьезным фактором риска развития ПИ-СРК, но и вирусные инфекции [13]. Например, ПИ-СРК у детей, перенесших ротавирусную инфекцию, развивается в 24,6% случаев [18]. А.А. Белова и соавт. [19] сообщают, что лямблиоз повышает риск развития ПИ-СРК, оказывая влияние на видовой состав и разнообразие микробиоты кишечника, метаболизм хозяина, иммунный ответ, слизистый барьер и моторику желудочно-кишечного тракта (ЖКТ).
Ряд факторов, таких как молодой возраст, женский пол, продолжительность диареи, тяжесть течения ОКИ, могут увеличить риск развития ПИ-СРК [20–23]. M. Thabane et al. [23] установили, что риск развития ПИ-СРК после ОКИ повышается в 6 раз, при этом к факторам риска относятся молодой возраст, продолжительная лихорадка, наличие тревожности и депрессии. Риск развития ПИ-СРК увеличивается как минимум в 2 раза при длительности диареи более 1 нед. и более чем в 3 раза при длительности диареи свыше 3 нед. Кроме того, на частоту развития СРК оказывает влияние выраженность местного воспалительного процесса, увеличивая риск развития ПИ-СРК при наличии гемоколита [20, 22].
Роль микробиома в патогенезе ПИ-СРК
Доказана и роль микробиома в развитии ПИ-СРК. Нарушение микробиологической экосистемы может приводить к сдвигам в составе желчных кислот, цитокинов и иммунной среды, что способно повлиять на эпителиальную и нервно-мышечную функцию и вызвать еще большее нарушение в составе микробиома. При ПИ-СРК чаще обнаруживается снижение числа бактерий, относящихся к роду Bacteroidetes, в то время как при других вариантах СРК нарушается соотношение Firmicutes/Bacteroidetes [15, 26]. Из бактерий, продуцирующих бутират, у пациентов с ПИ-СРК было обнаружено снижение числа бактерий рода Subdoligranulum, отвечающих за синтез интерлейкина 1β [27]. Это указывает на специфическую активность иммунной системы против симбиотических микробов в период патологических состояний и предполагает сложное и двунаправленное взаимодействие между микробиотой и иммунным ответом, возникающим при ПИ-СРК.
Диагностика и лечение СРК
В настоящее время предпринимаются попытки систематизировать рекомендации по диагностике и лечению ПИ-СРК, при этом специфические лечебные рекомендации для ПИ-СРК не разработаны, что часто затрудняет постановку диагноза этой формы СРК и приводит к более позднему старту терапии. До последнего времени считалось, что диагноз ПИ-СРК может быть поставлен после комплексного обследования (эндоскопические методы исследования, КТ-колонография), позволяющего исключить у пациента органические заболевания ЖКТ [17], однако в последнее время опубликован ряд работ [1, 9, 10, 28], которые продемонстрировали, что дополнительные инструментальные исследования не имеют значимой диагностической ценности у большинства больных СРК без симптомов тревоги.
Лечение ПИ-СРК, как правило, симптоматическое и включает в себя диетические рекомендации, спазмолитики, пробиотики, кишечные антисептики, антидиарейные средства или слабительные в зависимости от преобладающих симптомов. Лечение может включать психотерапию и антидепрессанты [1, 9, 28]. В лечении ПИ-СРК важно не только купирование абдоминального синдрома, но и воздействие на основные звенья патогенеза, поскольку купирование абдоминального синдрома влияет на качество жизни и степень выраженности тревоги у пациента, а патогенетическая терапия – на качество жизни и на объективный статус пациента. Одним из универсальных препаратов является тримебутин (Необутин®). Помимо способности модулировать висцеральную гиперчувствительность и модифицировать субъективное восприятие боли, тримебутин обладает неспецифическим сродством к периферическим δ-, μ- и κ-рецепторам, не проявляя селективности ни к одному из них, благодаря чему может как усиливать, так и угнетать перистальтику ЖКТ в зависимости от предшествовавшей настройки рецепторов [29].
Эффективность пробиотической терапии зависит от соответствия применяемых штаммов определенным требованиям: они должны быть фенотипически и генотипически идентифицируемыми, обладать кислотоустойчивостью и быть безопасными. Представителем подобных синбиотиков является Максилак®. Благодаря применению инновационной технологии производства — MURE (Multi Resistant Encapsulation) бактерии, присутствующие в синбиотике Максилак®, защищены от кислого содержимого желудочного сока, солей желчи и пищеварительных ферментов. Такая защита позволяет им адаптироваться и прижиться в просвете кишечника, сохранив высокую биологическую активность.
Клиническое наблюдение ПИ-СРК
Пациент М., 9 лет, поступил с жалобами на абдоминальные боли, преимущественно по утрам, сопровождающиеся учащенным до 3–4 раз в день неоформленным стулом со слизью. Болевой синдром ослабевал или купировался после дефекаций. Вышеуказанные жалобы наблюдались в течение 7 мес. Из анамнеза известно, что 8 мес. назад ребенок перенес острый инфекционный гастроэнтероколит сальмонеллезной этиологии тяжелой степени, по поводу которого получал антибактериальную терапию (цефтриаксон) и кишечные антисептики (нифуроксазид). Выписан домой с минимальными диспепсическими симптомами, неоформленным стулом. Через 2 нед. появились боли в животе, преимущественно по утрам, купирующиеся после акта дефекации, стул кашицеобразный со слизью. Еще через 7 дней частота стула увеличилась до 3 раз в день. Лечились самостоятельно, применяя препараты панкреатина и спазмолитики, без эффекта. Через 1 мес. обратились к педиатру по месту жительства. При обследовании по результатам клинического анализа крови не было обнаружено анемии и воспалительных изменений; в копрограмме стеаторея 2 типа, большое количество йодофильной флоры, слизи. Мазок на дизентерийную группу, сальмонеллез трехкратно показал отрицательный результат. Были назначены энтеросорбенты, нитрофураны повторным курсом и спазмолитики. На фоне лечения интенсивность болевого синдрома уменьшилась, но боли возникали несколько раз в неделю, преимущественно по утрам, стул полуоформленный, тип 4–5 по Бристольской шкале, 1–2 раза в день. После курса лечения педиатром было рекомендовано ограничение объема потребления продуктов, содержащих пищевые волокна, на этом фоне боли, купирующиеся после дефекации, беспокоили ребенка 1–2 раза в неделю. Через 1 мес. после лечения, на этапе расширения диеты, вновь участились боли в животе, сопровождающиеся отхождением кашицеобразного стула со слизью. В течение месяца лечились самостоятельно, принимая энтеросорбенты, ферментные препараты с непродолжительным положительным эффектом.
Учитывая сохраняющиеся жалобы, ребенка направили на обследование в центральную районную больницу по месту жительства. При обследовании клинические и биохимические анализы крови были в пределах нормы, при УЗИ органов брюшной полости патологических изменений не выявлено. При микробиологическом исследовании кала высевалась условно-патогенная флора. В стационаре были назначены антибактериальные препараты (цефалоспорины 4-го поколения), энтеросорбенты, ферменты, спазмолитики. На фоне лечения динамика положительная, болевой синдром купирован, стул 1–2 раза в день, полуоформленный (тип 4–5 по Бристольской шкале). Через 2 нед. после лечения мать ребенка отметила появление болевого синдрома и учащение стула при употреблении молочных продуктов. Было исключено молоко, но болевой синдром сохранялся. Через некоторое время вновь участился стул до 3 раз в день. При обследовании отмечалось повышение уровня кальпротектина до 180 мкг/л. Ребенок был направлен на консультацию к гастроэнтерологу. При осмотре отмечено, что ребенок мнительный, с выраженным беспокойством по отношению к своему здоровью, проявляет особую тревожность по поводу вынужденных пропусков в школе из-за нарушения здоровья. Мать ребенка плаксива, излишне эмоциональная. При сборе анамнеза установили, что ранее ребенок был пролечен по поводу лямблиоза, после чего отмечались редкие боли в животе, купируемые самостоятельно без лечения. За последние 4 мес. вес ребенка снизился на 2 кг.
Проведен дыхательный водородный тест с лактулозой, выявлена высокая бактериальная контаминация тонкой кишки. При анализе кала на условно-патогенную флору высеяны Escherichia coli (лактозонегативная) 10 9 КОЕ/г, Enterobacter cloacae 1,4×10 8 КОЕ/г, Proteus mirabilis 2×10 7 КОЕ/г. По данным колоноскопии определялся эритематозный проктосигмоидит, терминальный илеит. При морфологическом исследовании биоптата тонкой кишки были выявлены признаки диффузной слабовыраженной лимфоплазмоцитарной инфильтрации собственной пластинки. При проведении биопсии слизистой поперечной ободочной кишки были выявлены отек, диффузная полиморфноклеточная инфильтрация. По данным биопсии материала слизистой нисходящей ободочной кишки: отек, очаговая полиморфноклеточная воспалительная инфильтрация, слизь. При проведении биопсии материала слизистой сигмовидной кишки отмечены умеренно выраженный отек, полиморфноклеточная воспалительная инфильтрация, биопсии материала прямой кишки: очаговая и полиморфноклеточная воспалительная инфильтрация. С учетом основных симптомов ПИ-СРК был назначен курс терапии тримебутином, диоктаэдрическим смектитом, а также мультиштаммовым синбиотиком Максилак ® , психотропными препаратами. Через 1 мес. от начала лечения у пациента отмечено значительное улучшение: стул не чаще 1–2 раз утром после завтрака. При этом сохранялись проявления депрессии, тревожность. Пациенту была дана рекомендация принимать тримебутин по потребности при болях в животе, назначены повторный курс синбиотика и седативные препараты. Через 3 мес. на следующем визите к гастроэнтерологу пациент жалоб не предъявлял, было отмечено восстановление массы тела. Мальчик активно занимался спортом.
Заключение
Лечение СРК должно учитывать патогенетические механизмы развития заболевания у каждого конкретного пациента. Согласованная тактика лечения должна включать мероприятия, направленные на уменьшение симптомов (или их исключение) и улучшение качества жизни пациентов. Пациенты с ПИ-СРК нуждаются в коррекции синдрома избыточного бактериального роста путем деконтаминации тонкой кишки с помощью современных энтеросептиков. Кроме того, хорошие результаты приносит назначение современных прокинетиков, в частности тримебутина (Необутин ® ) в сочетании с пробиотической терапией мультиштаммовыми синбиотиками.
Благодарность
Acknowledgments
The technical edition is supported by JSC "Alium".
Сведения об авторах:
Печкуров Дмитрий Владимирович — д.м.н., профессор, заведующий кафедрой детских болезней ФГБОУ ВО СамГМУ Минздрава России; 443099, Россия, г. Самара, ул. Чапаевская, д. 89; ORCID iD 0000-0002-5869-2893.
Тяжева Алена Александровна — к.м.н., доцент кафедры детских болезней ФГБОУ ВО СамГМУ Минздрава России; 443099, Россия, г. Самара, ул. Чапаевская, д. 89; ORCID iD 0000-0001-8552-1662.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах и методах.
Конфликт интересов отсутствует.
Статья поступила 13.07.2021.
Поступила после рецензирования 05.08.2021.
Принята в печать 30.08.2021.
About the authors:
Dmitry V. Pechkurov — Dr. Sc. (Med.), Professor, Head of the Department of Children’s Diseases, Samara State Medical University; 89, Chapaevskaya str., Samara, 443099, Russian Federation; ORCID iD 0000-0002-5869-2893.
Alena A. Tyazheva — C. Sc. (Med.), associate professor of the Department of Children’s Diseases, Samara State Medical University; 89, Chapaevskaya str., Samara, 443099, Russian Federation; ORCID iD 0000-0001-8552-1662.
There is no conflict of interests.
Received 13.07.2021.
Revised 05.08.2021.
Accepted 30.08.2021.
Название протокола: Синдром раздраженного кишечника у детей
Синдром раздраженного кишечника – это комплекс функциональных нарушений кишечника, наиболее частыми симптомами которого, являются нарушение самого акта дефекации, различные варианты абдоминального болевого синдрома и отсутствие при этом значимых воспалительных или иных органических изменений кишечной трубки.[1–3] (УД – A).
Код (ы) по МКБ-10:
K58 Синдром раздраженного кишечника
K58.0 Синдром раздраженного кишечника с диареей
K58.9 Синдром раздраженного кишечника без диареи
Сокращения, используемые в протоколе:
Дата разработки протокола: 2015 г.
Категория пациентов: дети.
Пользователи протокола: педиатры, гастроэнтерологи детские, врачи общей практики.
Оценка на степень доказательности приводимых рекомендаций.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++или+), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 800 RUB / 4500 KZT / 27 BYN - 1 рабочее место в месяц

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место - 800 RUB / 4500 KZT / 27 BYN в месяц
Мне интересно! Свяжитесь со мной
Классификация
Клиническая классификация[1,2]:
· СРК с преобладанием запора;
· СРК с преобладанием диареи;
· СРК смешанный;
· СРК не классифицируемый.
Клиническая картина
Cимптомы, течение
Диагностические критерии постановки диагноза** 7 (УД – B):
Жалобы:
· рецидивирующую абдоминальную боль или дискомфорт в животе (чувство сдавления, распирания, вздутия), связанные с дефекацией, изменениями частоты и характера стула или другими признаками.
Негастроэнтерологические жалобы:
· характерные для неврологических и вегетативных расстройств – головная боль, боли в поясничной области, чувство кома в горле, сонливость или, наоборот, бессонницу, дизурию, нарушение менструального цикла у девочек.
Клинические симптомы СРК, согласно Римским критериям III (2006):
· частота дефекации менее 3 раз в неделю или более 3 раз в день;
· шероховатый и твёрдый, либо мягкий и водянистый стул;
· натуживание во время дефекации;
· императивные позывы к дефекации (невозможность задержать опорожнение кишки), ощущение неполного опорожнения кишки;
· Выделение слизи во время дефекации;
· Чувство переполнения, вздутия или переливания в животе.
Все перечисленные жалобы могут усиливаться при стрессовых ситуациях (экзамены, контрольные, ссоры и др.).

Физикальное обследование:
· Общий осмотр – выявление признаков системного заболевания, симптомов интоксикации – отсутствие симптомов интоксикации и других патологических сдвигов. Возможны симптомы вегетативных расстройств.
· Осмотр области живота – (осмотр, аускультация, пальпация) – без патологических проявлений, кроме умеренного вздутия; аускультация - без особенностей; пальпация: умеренная болезненность по ходу толстого кишечника.
· Исследование перианальной области – без патологии.
· Пальцевое исследование прямой кишки – без патологии.
Обнаружение каких-либо отклонений от нормы (гепатоспленомегалия, отёки, свищи и т.д.) при физикальном обследовании свидетельствует против диагноза СРК. (Алгоритм диагностики – Приложение 1)
Диагностика
Перечень основных и дополнительных диагностических мероприятий:
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне:[3–9] (УД – A).
· общий анализ крови;
· общий анализ мочи;
· исследование кала (копрограмма) общеклиническое;
· исследование кала на простейшие и гельминты;
· обнаружение скрытой крови в кале (качественное);
· бактериологическое исследование испражнений на патогенную и условно – патогенную микрофлору.
Дополнительные диагностические обследования, проводимые на амбулаторном уровне:
· биохимический анализ крови (общий белок, мочевина, креатинин, билирубин, АЛТ, АСТ, СРБ (количественное));
· УЗИ комплексное органов брюшной полости;
· бактериологическое исследование испражнений на кишечный дисбактериоз.
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
Основные (обязательные) диагностические исследования, проводимые на стационарном уровне (при экстренной госпитализации проводятся диагностические исследования, не проведенные на амбулаторном уровне):
· общий анализ крови;
· общий анализ мочи;
· обзорная рентгенография органов брюшной полости;
· бактериологическое исследование испражнений на патогенную и условно- патогенную микрофлору (выделение чистой культуры);
· исследование кала (копрограмма) общеклиническое;
· обнаружение скрытой крови в кале качественное;
· определение общей альфа-амилазы в сыворотке крови;
· определение общей альфа-амилазы в моче;
· ультразвуковая диагностика комплексная (печень, желчный пузырь, поджелудочная железа, селезенка, почки);
· пальцевое исследование прямой кишки.
· тотальная фиброколоноскопия.
Дополнительные диагностические обследования, проводимые на стационарном уровне (при экстренной госпитализации проводятся диагностические обследования не проведенные на амбулаторном уровне):
· определение антител к тканевой трансглютаминазе IgA (анти - tTG IgA);
· определение тиреотропного гормона (ТТГ) в сыворотке крови ИФА-методом;
· определение свободного трииодтиронина (T3) в сыворотке крови ИФА –методом;
· определение тиреоглобулина в сыворотке крови ИФА-методом;
· определение кальпротектина (маркер воспаления) в кале;
· фиброэзофагогастродуоденоскопия;
· компьютерная томография толстого кишечника (виртуальная колоноскопия).
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводятся.
Инструментальные исследования: без патологических изменений.
Показания для консультации узких специалистов:
· гастроэнтеролога – на амбулаторном уровне для решения вопроса о госпитализации;
· психоневролога – для исключения психических расстройств;
· невролога – для исключения патологического состояния со стороны ЦНС;
· уролог – при наличии внекишечных проявлений у пациентов: дизурия, боли в пояснице для исключения патологии органов мочевыделения.
· хирурга – при наличии выраженного болевого абдоминального синдрома, для исключения аномалии развития толстого кишечника;
· эндокринолог – для исключения гипотиреоза, тиреотоксикоза и сахарного диабета;
· гинеколога – для исключения гинекологических заболеваний;
· инфекциониста – для исключения кишечных инфекции (амёбные, бактериальные, глистные инвазии).
Лабораторная диагностика
Дифференциальный диагноз
Дифференциальный диагноз:
Для детского возраста симптомами, исключающими диагноз СРК (Римские критерии III, 2006), считают:
· немотивированное уменьшение массы тела;
· сохранение симптомов ночью (во время сна);
· постоянную интенсивную боль в животе;
· прогрессирование ухудшения состояния;
· лихорадку;
· ректальные кровотечения;
· безболезненные поносы;
· стеаторею;
· непереносимость лактозы, фруктозы и глютена;
· изменение лабораторных показателей.
Дифференциальный диагноз проводится со следующими заболеваниями и состояниями:
· кишечные инфекции (бактериальные, вирусные, амебные);
· воспалительные заболевания кишечника (язвенный колит, болезнь Крона);
· синдромом мальабсорбции (постгастроэктомический, панкреатический, энтеральный);
· патологические состояния со стороны ЦНС (переутомление, испуг, эмоциональные нагрузки, волнение);
· психопатологические состояния (депрессия, синдром тревоги, панические атаки, синдром соматизации);
· нейроэндокринные опухоли (карциноидный синдром, опухоль, зависимая от вазоинтестинального пептида);
· эндокринные заболевания (тиреотоксикоз);
· функциональные состояния у женщин (предменструальный синдром, беременность);
· проктоанальная патология (диссинергия мышц тазового дна, синдром опущения промежности, одиночная ректальная язва);
· неадекватные реакции на пищевые продукты (кофеин, алкоголь, жиры, молоко, овощи, фрукты, чёрный хлеб и др.), обильный приём пищи, изменение привычек питания;
· побочные реакции на прием лекарственных средств (слабительные, препараты железа, желчных кислот).
Самой распространенной патологией, сопровождающейся проявлениями СРК, является врожденная ферментопатия - лактазная и дисахаридазная недостаточность, простейшим способом диагностики которой, является диета с исключением цельного молока и творога, сорбитола (жевательная резинка), усвоение которых требует достаточного количества лактазы или дисахаридазы.
Органические заболевания кишечника - колоректальный рак, полипоз, дивертикулез, болезнь Крона и неспецифический язвенный колит, микроскопические колиты, мастоцитоз, кишечные инфекции, паразитарные инфекции, синдром мальабсорбции, синдром короткой тонкой кишки, долихосигма, целиакия, туберкулез обязательно входят в круг дифференциально диагностического поиска.
Нейроэндокринные опухоли ЖКТ, в первую очередь гастриномы, карциноидный синдром и VIP-омы, на первых стадиях могут протекать под маской диарейной или болевой формы СРК. Гинекологические болезни (чаще эндометриоз и пластический рубцовый перитонит) могут иметь типичную для СРК клиническую картину. Среди эндокринных заболеваний чаще тиреотоксикоз и сахарный диабет с автономной диабетической энтеропатией протекают по типу диарейной формы СРК.
Лечение
Немедикаментозное лечение:
Режим:
· достаточный ночной сон (7-8 часов);
· ограничение времени просмотра телевизора и работы за компьютером до 30-60 минут в день;
· ежедневные игры и прогулки на свежем воздухе;
· умеренная физическая активность;
· коррекция психоэмоциональной неустойчивости – аутотренинг, психотерапевтические меры.
Диетотерапия: является ключевым моментом в терапии – регулярный прием пищи, потребление достаточного количества жидкости. Снижение потребления продуктов с лактозой, фруктозой, сорбитом.
Диета при СРК, протекающем с запором:
· разнообразные напитки, газированные воды в холодном виде;
· хлеб ржаной и хрустящие хлебцы с отрубями;
· однодневные молочнокислые продукты (кефир, ацидофильное молоко, простокваша, мацони), сметана, творог;
· сливочное и растительное масло;
· мясо и рыба в любом виде;
· супы в холодном виде;
· крупы (гречневая, ячневая, перловая);
· яйца вкрутую;
· сырые овощи и фрукты (морковь, чернослив, квашеная капуста, абрикосы).
То есть, при преобладании запоров – включить продукты, богатые пищевыми волокнами. Исключаются кофе, крепкий чай, какао, шоколад, кисели, слизистые супы, протертые каши, сдобное тесто. Ограничиваются блюда в горячем виде.
При запоре, сопровождающемся болью - овощи дают в отварном и протертом виде, мясо рубленое или отварное. При запоре в сочетании с выраженным метеоризмом в рационе ограничивают капусту, картофель, бобовые, арбуз, виноград, ржаной хлеб и цельное молоко.
Диета при СРК, с преобладанием диареи:
Пищу следует принимать 5-6 раз в день небольшими порциями. При диарейном синдроме – ограничить содержание грубой клетчатки, поваренную соль, сахар и сахаристые вещества.
Рекомендуется:
· крепкий черный чай, отвар из черники, белые сухари, сухое несдобное печенье;
· молочнокислые продукты
· масло сливочное в небольшом количестве;
· яйца и яичные блюда в ограниченном количестве;
· рисовый или овсяный отвар.
Медикаментозное лечение, оказываемое на амбулаторном уровне и стационарном уровне:
C целью регуляции моторно-эвакуаторной функции:
Тримебутин – детям 3-5 лет по 25 мг за 15 мин. до еды 3 раза в день перорально, детям 5-12 лет 50 мг за 15 мин. до еды 3 раза в день перорально, детям с 12 лет: по 100-200 мг 3 раза в сутки за 15 мин. до еды 3 раза в день перорально – длительность приема определяют индивидуально, но не более 2 месяцев.
При склонности к запорам: Лактулоза (дозу препарата подбирают индивидуально) детям в возрасте от 1 до 6 лет – 5-10 мл перорально 1 раз в день утром во время еды; от 7 до 14 лет начальная доза составляет 15 мл, поддерживающая – 10 мл. Длительность приема определяют индивидуально, но не более 1 месяца.
Макрогол – детям старше 8 лет внутрь в дозе 10-20 г (предварительно растворить в 50 мл.воды) один раз в сутки, утром во время еды, перорально. Курс лечения – до 3 месяцев.
С целью купирования диареи: Лоперамид – детям старше 5 лет по 2 мг/сутки в 2-3 приема перорально, до нормализации стула или при отсутствии стула более 12 ч.(УД – В).
С целью купирования болевого синдрома и чувства дискомфорта (в качестве альтернативы при непереносимости других спазмолитических препаратов):
Дротаверин гидрохлорид – детям с 6 лет 80-200 мг в 2-5 приема, максимальная суточная доза 240 мг, длительность 3-5 дней, перорально.
Гиосцина-бутил-бромид – суточная доза 0,3-0,6 мг /кг массы тела в 2-3 приема; максимальная суточная доза – 1,5 мг на кг массы тела, длительность 3-5 дней, перорально.
Папаверин – от 6 мес до 2 лет по 5 мг, 3–4 лет по 5–10 мг, 5–6 лет по 10 мг, 7–9 лет по 10–15 мг, 10–14 лет по 15–20 мг. п/к или в/м 2–4 раза в сутки; в/в медленно – 20 мг с предварительным разведением в 10–20 мл 0,9% раствора NaCl; ректально по 20–40 мг 2–3 раза в день. Длительность 3-5 дней
Для купирования метеоризма: Симетикон по 1-2 ч. ложки эмульсии или 1-2 капсулы 3-5 раз в день, перорально, детям раннего возраста – по 1 ч. ложке 3-5 раз в день. Длительность курса определяется степенью болевых ощущений.
При депрессивных состояниях, сопровождающихся нарушениями сна, ажитацией, тревожностью (по назначению психоневролога): Амитриптилин – детям с 12 лет 10-30 мг или 1-5 мг/кг/сутки, дробно, перорально, после еды до 50 мг в сутки, длительность 4-6 недель;
Тофизепам – перорально по 25-50 мг 1-3 раза в день; максимальная суточная доза – 150 мг. Курс лечения – от 4 до12 недель.
Для подготовки к эндоскопическим или рентгенологическим исследованиям на стационарном уровне: детям старше 15 лет макрогол 4000 из расчета 1 пакетик на 15-20 кг массы тела (Содержимое 1 пакетика необходимо развести 1 литром воды). Один стакан раствора принимают в течение 10 минут, затем 1 литр – за следующие 60 минут. Рассчитанную дозу макрогола можно принять однократно, перорально или в 2 приема (утром и вечером). Если запланированная процедура или операция состоится утром, то раствор выпивают вечером.
Другие виды лечения:
Другие виды лечения, оказываемые на амбулаторном уровне: различные психотерапевтические методы.
Другие виды, оказываемые на стационарном уровне: различные психотерапевтические методы.
Другие виды лечения, оказываемые на этапе скорой медицинской помощи: не проводятся.
Хирургическое вмешательство: нет.
Индикаторы эффективности лечения.
· отсутствие болевого синдрома и диспепсического синдромов, дискомфорта, нормализация моторики кишечника и психоэмоционального статуса;
· ремиссия;
· улучшение самочувствия без существенной положительной динамики объективных данных (частичная ремиссия).
Препараты (действующие вещества), применяющиеся при лечении
| Амитриптилин (Amitriptyline) |
| Гиосцина бутилбромид (Hyoscine butylbromide) |
| Дротаверин (Drotaverinum) |
| Лактулоза (Lactulose) |
| Лоперамид (Loperamide) |
| Макрогол (Macrogol) |
| Натрия хлорид (Sodium chloride) |
| Папаверин (Papaverine) |
| Симетикон (Simethicone) |
| Тофизопам (Tofisopam) |
| Тримебутин (Trimebutine) |
Госпитализация
Показания для госпитализации с указанием типа госпитализации:
Показания для плановой госпитализации:
· длительность заболевания (болевой синдром, диарея или задержка стула) более 3-х месяцев;
· неэффективность амбулаторного лечения;
· необходимость исключения органической патологии кишечника.
Показания для экстренной госпитализации: нет.
Профилактика
Профилактические мероприятия: соблюдение режима питания, исключение неоправданного применения лекарственных препаратов.
Дальнейшее ведение:
Прогноз заболевания благоприятный, но ухудшается у пациентов с тяжелой степенью заболевания. Течение хроническое, рецидивирующее, но не прогрессирующее и не осложненное. Риск развития воспалительных заболеваний кишечника и колоректального рака у больных СРК такой же, как и в общей популяции [7,47,48].
Информация
Источники и литература
Информация
Указание на отсутствие конфликта интересов: нет.
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Примечание: Диагноз СРК является диагнозом исключения, т.е. выставляется только после исключения какой-либо органической патологии.
Синдром раздраженного кишечника у детей - функциональное заболевание желудочно-кишечного тракта, сопровождающееся моторно-эвакуаторными нарушениями. Синдром раздраженного кишечника у детей характеризуется болями в животе, уменьшающимися после дефекации, урчанием, метеоризмом, частыми позывами на дефекацию и ощущением неполного опорожнения кишечника, чередованием поносов и запоров. Диагностика синдрома раздраженного кишечника у детей проводится путем исключения органической патологии с помощью УЗИ брюшной полости, ирригоскопии, ЭГДС, колоноскопии, анализа кала на яйца гельминтов и пр. Лечение включает коррекцию питания, назначение спазмолитиков, ветрогонных, седативных, противодиарейных или слабительных препаратов, энтеросорбентов.

Общие сведения
Синдром раздраженного кишечника у детей (СРК, синдром раздраженной толстой кишки, дискинезия толстой кишки и др.) – комплекс гастроинтестинальных симптомов, развивающихся в отсутствии биохимических или структурных нарушений желудочно-кишечного тракта. Истинная частота синдрома раздраженного кишечника у детей неизвестна, однако эпидемиологические исследования свидетельствуют, что характерные для СРК жалобы предъявляет более половины детей, страдающих рецидивирующим абдоминальным синдромом. Распространенность синдрома раздраженного кишечника во взрослой популяции составляет 15-25%, и справедливо считается, что в большинстве случаев формирование СРК происходит еще в детском возрасте. Эти обстоятельства делают проблему синдрома раздраженного кишечника у детей, заслуживающей пристального внимания со стороны педиатрии и детской гастроэнтерологии.

Причины синдрома раздраженного кишечника у детей
В этиологии синдрома раздраженного кишечника у детей играют роль различные факторы, к числу которых относятся наследственность, психоэмоциональные феномены, характер питания, нарушения моторики, реакции воспаления и др.
О значении наследственной предрасположенности свидетельствует тот факт, что у 33% детей родственники страдают синдромом раздраженного кишечника, а у монозиготных близнецов заболевание встречается чаще, чем у разнояйцовых (гетерозиготных). Замечено, что примерно у трети детей с синдромом раздраженного кишечника возникновение первых симптомов заболевания и обострения тесно связаны с психотравмирующими ситуациями. Еще не менее чем в 30-40% случаев манифестация синдрома раздраженного кишечника у детей наступает после перенесенной острой кишечной инфекции, а хронизации заболевания способствует антигенная агрессия в отношении энтериновой системы. Следствием воспаления, нарушения иннервации и перерастяжения мышц кишечной стенки служит гиперрефлексия - повышенная чувствительность, когда на все раздражители (увеличение объема поступающей пищи, расширение кишки газом и т. д.) возникает болевая реакция.
Нарушение кишечного транзита при синдроме раздраженного кишечника у детей может быть обусловлено ригидностью, спастичностью кишки, дефицитом пищевых волокон в рационе ребенка, дисбактериозом, гиподинамией и пр.
Наблюдения показывают, что синдром раздраженного кишечника чаще встречается у детей с перинатальной энцефалопатией, рано переведенных на искусственное вскармливание; страдавших гипотрофией на 1-ом году жизни; перенесших энтеровирусные и ротавирусные инфекции, лямблиоз, гельминтозы; нарушающих режим питания.
Классификация синдрома раздраженного кишечника у детей
В зависимости от преобладающих клинических проявлений выделяют 4 основных варианта синдрома раздраженного кишечника у детей:
- СРК с преобладаниемзапоров – из общего количества испражнений >25 % кала имеет твердую или шероховатую консистенцию и
- СКР с преобладанием диареи - из общего количества испражнений >25 % кала имеет кашицеобразную или водянистую консистенцию и
- смешанный СРК - из общего количества испражнений >25 % кала имеет водянистую консистенцию и столько же – твердую;
- неклассифицируемый СРК – на основании выделенных критериев не может быть отнесен ни к одному из вышеперечисленных вариантов.
Симптомы синдрома раздраженного кишечника у детей
Синдром раздраженного кишечника у детей, протекающий с явлениями диареи, характеризуется отсутствием жидкого стула в ночные часы и возникновением преимущественно по утрам, после завтрака. Императивные позывы на дефекацию возникают 3-4 раза за короткий промежуток времени. Первая порция испражнений имеет, как правило, оформленный характер; при последующих актах дефекации стул приобретает кашицеобразную или жидкую консистенцию. Диарея нередко сопровождается спастическими болями в правой подвздошной области.
При неклассифицируемой форме синдрома раздраженного кишечника у детей отмечаются различные симптомы без явного преобладания - чередование поносов и запоров, метеоризм, урчание и чувство распирания в животе, болевой абдоминальный синдром. Для постановки диагноза синдрома раздраженного кишечника необходимо, чтобы данные симптомы сохранялись у ребенка не менее 3-х месяцев.
Внекишечные проявления синдрома раздраженного кишечника у детей могут включать дисфагию, изжогу, тошноту. Дети пубертатного возраста предъявляют жалобы на головные боли, сердцебиение, утомляемость, дискомфорт за грудиной, нехватку воздуха, потливость, бессонницу. Часто отмечаются невротические реакции: мнительность, тревожность, раздражительность, импульсивное поведение. У 25-30% детей синдром раздраженного кишечника сочетается с дискинетической диспепсией, нейрогенным мочевым пузырем.
Диагностика синдрома раздраженного кишечника у детей
Диагностировать синдром раздраженного кишечника у ребенка довольно не просто; для этого требуется консолидация усилий детских специалистов различных профилей: педиатра, детского гастроэнтеролога, детского колопроктолога, детского невролога, детского эндокринолога и др. Диагностическая тактика основывается, главным образом, на исключении органических заболеваний ЖКТ. В связи с этим после оценки жалоб больного и физикального обследования устанавливается связь клинической манифестации синдром раздраженного кишечника у детей с ОКИ, стрессовыми ситуациями, сменой питьевой режима и характера питания.
Из методов лабораторной диагностики применяются исследования клинического и биохимического анализа крови; кала на скрытую кровь, лямблии и яйца гельминтов, копрограмму; бакпосев кала на кишечную группу, анализ на дисбактериоз. В порядке скрининга проводится УЗИ органов брюшной полости ребенку и ультрасонография толстого кишечника.
С целью исследования моторно-эвакуаторной функции толстого кишечника выполняется ирригография, выявляющая в дистальных отделах участки спазмированной кишки. Эндоскопия у детей (ректороманоскопия, колоноскопия) может обнаруживать поверхностные катаральные изменения слизистой оболочки толстой кишки. Эндоскопическая биопсия позволяет исключить подозрение на неспецифический язвенный колит и болезнь Крона. При необходимости исследования верхних отделов ЖКТ проводится ЭГДС, рентгенография желудка с барием.
Оценить моторную функцию толстой кишки при синдроме раздраженного кишечника у детей помогают колодинамические исследования – энтероколосцинтиграфия, аноректальная манометрия.
Комплексный и индивидуализированный подход позволяет провести дифференциальную диагностику синдрома раздраженного кишечника у детей с мегаколоном, колитом, паразитозами, лактазной недостаточностью, целиакией и другой структурной и биохимической патологией.
Лечение синдрома раздраженного кишечника у детей
Лечения синдрома раздраженного кишечника у детей проводится дифференцированно, с учетом клинической формы заболевания. Во всех случаях осуществляется коррекция рациона ребенка с учетом возраста и ведущих симптомов (диареи, запора, метеоризма). Диетический режим предполагает дробный прием пищи 5–6 раз в сутки; исключение из питания животных жиров, шоколада, молока, капусты, бобовых, черного хлеба, газированных напитков. Важную роль играет нормализация психологического микроклимата в семье и школе, водные процедуры, достаточная физическая активность, занятия ЛФК, выработка навыков ежедневной дефекации.
При синдроме раздраженного кишечника с запорами детям назначаются слабительные (препараты лактулозы), прокинетики (домперидон), пре- и пробиотики. В случае преобладания диарейного синдрома показаны энтеросорбенты (смекта, полифепан), кишечные антисептики (фуразолидон, интетрикс), ферменты (панкреатин, креон и др.), антидиарейные (имодиум, лоперамид), пре- и пробиотические препараты. В терапии смешанного и неклассифицируемого вариантов синдрома раздраженного кишечника у детей применяются спазмолитики (бускопан), ветрогонные средства (эспумизан), пробиотики (линекс, бифиформ), пребиотики (хилак-форте, дюфалак), ферменты. Психотерапевтическая коррекция проводится по назначению детского психоневролога.
При гипермоторной дисфункции ЖКТ ребенку с синдромом раздраженного кишечника могут назначаться грязевые, озокеритовые или парафиновые аппликации на живот, СМТ-терапия, электрофорез, рефлексотерапия; в случае гипомоторной дискинезии – дарсонвализация и электростимуляция на область живота, массаж передней брюшной стенки.
Прогноз и профилактика синдрома раздраженного кишечника у детей
Внимание к проблеме синдрома раздраженного кишечника у детей позволяет предотвратить его хронизацию. Если причины синдрома раздраженного кишечника у детей не устранены, вполне вероятно, что будет отмечаться прогрессирование заболевание и снижение качества жизни ребенка.
Профилактические мероприятия носят неспецифический характер и включают предупреждение и адекватное лечение ОКИ, создание комфортной психосоциальной обстановки вокруг ребенка, соблюдение режима и принципов рационального питания, достаточной физической активности.
Синдром раздраженного кишечника (СРК) является самым распространенным функциональным заболеванием кишечника у взрослых и представляет значимую социальную проблему, влияя на качество жизни. В основе развития СРК лежит взаимодействие двух основных патогенетических механизмов: психосоциального воздействия и нарушения моторной функции толстой кишки, что проявляется повышением висцеральной чувствительности и изменением двигательной активности кишки.
Сведения об авторах:
Ключевые слова: дети, синдром раздраженной кишки, прокинетики, тримебутин, необутин, пробиотики, максилак.
В основе ФРОП лежат комбинированные физиологические и морфологические отклонения, связанные с висцеральной гиперчувствительностью, нарушениями моторики ЖКТ, защитного слизистого барьера, иммунной функции и состава кишечной микробиоты, а также расстройствами со стороны ЦНС.
В развитии ФРОП у детей в раннем возрасте немаловажную роль играют такие факторы, как морфофункциональная незрелость, недостаточная активность панкреатических и гастроинтестинальных ферментов, нарушение микробиоценоза, недостаточность мукозального иммунитета. В более старшем возрасте висцеральная гиперчувствительность обусловлена совокупностью факторов: социальными взаимоотношениями, стрессом, переутомлением, нарушением режима дня, отдыха.
В основе развития СРК лежит взаимодействие двух основных патогенетических механизмов: психосоциального воздействия и нарушения моторной функции толстой кишки, что проявляется повышением висцеральной чувствительности и нарушением двигательной функции кишки (таблица 1).
Таблица 1. Диагностические критерии СРК для детей (признаки должны присутствовать не менее 2 месяцев) [1].
Должны присутствовать следующие симптомы:
1. Абдоминальная боль не менее 4 дней в месяц, ассоциированная с 1 или более из следующих симптомов:
а. связано с дефекацией;
б. ассоциирована изменением частоты опорожнения;
c. ассоциирована с изменением формы (внешнего вида) стула.
2. При СРК с запором боль не проходит после опорожнения (если боль проходит после опорожнения, то у ребенка функциональный запор, а не СРК).
3. После соответствующей оценки симптомы не могут быть отнесены под другое заболевание.
Боль может быть различной интенсивности, локализуется, как правило, внизу живота, хотя может отмечаться и в других его отделах. Она часто усиливается при погрешностях в диете, психоэмоциональной нагрузке, переживаниях, также при физической нагрузке. Важно отметить, что абдоминальная боль исчезает в ночное время, когда ребенок спит.
Таблица 2. Симптомы тревоги у пациентов с ФРОП.
| Семейный анамнез воспалительного заболевания кишечника, целиакии или язвенная болезнь; |
| Постоянная боль в правом верхнем или правом нижнем квадранте; |
| Дисфагия, одинофагия; |
| Рецидивирующая рвота; |
| Кровотечения из органов желудочно-кишечного тракта; |
| Ночная диарея; |
| Артрит; |
| Периректальные поражения; |
| Немотивированное похудание, потеря веса, недостаточность питания; |
| Задержка полового созревания; |
| Необъяснимая лихорадка; |
У детей, как и у взрослых, СРК можно разделить на разные типы, отражающие преобладающий характер стула (СРК с запор, СРК с диареей, СРК с запором и диарея и неуточненный СРК) и эти типы теперь включены в Рим IV [7].
Таблица 3. Функциональные расстройства органов пищеварения: нарушение взаимодействия ЖКТ и ЦНС по данным Римских критериев IV (коды Рим IV и МКБ-10).
С. Кишечные расстройства
С.1 Синдром раздраженного кишечника (СРК)
СРК с преобладанием запора (СРК-3)
СРК с преобладанием диареи (СРК-Д)
СРК смешанного типа (СРК-См)
Неклассифицируемый СРК (СРК-Н)
Формулировка
Коды Рим IV
МКБ-10
С.2
K59.0 запор
K58.2 Синдром раздраженного кишечника с преобладанием запоров
С.3
K59.1 Функциональная диарея
K58.1 Синдром раздраженного кишечника с преобладанием диареи
Функциональное абдоминальное вздутие/растяжение
С.4
R14 Метеоризм и родственные состояния
K59.9 Функциональное нарушение кишечника неуточненное
K58.8 Другой или неуточненный синдром раздраженного кишечника
Неспецифическое функциональное кишечное расстройство
С.5
K59.2 Неврогенная возбудимость кишечника, не классифицированная в других рубриках
K58.3 Синдром раздраженного кишечника со смешанными проявлениями
С.6
K59.0 Запор
В научных исследованиях показано, что висцеральная гиперчувствительность может быть связана с детским психологическим стрессом (тревога, депрессия, импульсивность, гнев) [8].
У детей с СРК могут наблюдаться повышенный уровень стресса, беспокойства, депрессии и эмоциональных проблем, о которых они сообщают сами [9]. Тяжелые заболевания, требующие медицинского инвазивного вмешательства в раннем возрасте (например, операция) связаны с более высоким риском развития ФРОП у детей, включая СРК [10].
Патофизиология СРК включает воздействие внешних раздражающих факторов (стресс, высокая эмоциональная нагрузка, недостаток сна и т. д.), что возбуждает ЦНС, вегетативный ответ, с воздействием на нейроэндокринную систему кишечника, включая гипоталамо-гипофизарно-надпочечниковую (кортизол) систему. Это нарушает двигательную активность кишечника, усиливает спазм гладкой мускулатуры, нарушает пассаж кишечного содержимого. С другой стороны, изменения двигательной активности кишечника приводят к перевозбуждению внутрикишечных нервных волокон, клеток Кахаля, усиливая спазм гладких мышц, изменяется микробиота, что влияет на среду и синтез КЖК. Таким образом, возникает порочный круг (таблица 4).
Кортикотропин-релизинг-фактор (CRF)
Активация энтеральной нервной системы
Изменение микробиоты
Активирует CRF-1 рецепторы → усиление моторики при стрессе
Провоспалительная активность → увеличение синтеза ИЛ-1 и ИЛ-2
Усиление ответа на эндотоксины
Повышение уровня кортизола и адреналина
Повышение сенситивности кишечных нервов
Нейротрансмиттеров → нарушение перистальтики
Повышенная дегрануляция тучных клеток → нарушение серотонинового сигнального каскада
Дисбаланс синтеза провоспалительных и воспалительных медиаторов
Повышение проницаемости кишечного барьера
Нарушение местного иммунитета
Экспрессия синтеза нейротрансмиттеров
(серотонин, ГАМК, гистамин, ацетилхолин, мелатонин и др.)
Нарушение слизистого барьера
и микробной биопленки
Модуляция кишечной чувствительности
афферентных волокон
Часто СРК развивается после перенесенной острой кишечной инфекции, отмечено повышение содержания провоспалительных цитокинов в слизистой оболочке ЖКТ и развивается постинфекционный СРК [12]. Систематический обзор, опубликованный в 2015 году, показал частоту регистрации постинфекционной функциональной диспепсии и СРК в популяции, включая детей 10,0% (ФД, n = 976; ОГЭ, n = 9737) и 13,1% (СРК, n = 1128; ОГЭ, n = 8624), соответственно. Так же указано длительное сохранение расстройств, установлено, что через 1 год после перенесенного о. гастроэнтерита постинфекционная функциональная диспепсия сохранилась у 13,5 % пациентов (n = 380; ОГЭ n = 2807) и синдром раздраженной кишки у 38,9% детей (n = 86 ; ОГЭ n = 221) [13].
В другом исследовании указана роль паразитарной инфекции (Balantidiumcoli, Strongyloidesstercoralis, Ascarislumbricoides, Necatoramericanus, Ancylostomaduodenale, Taeniasolium, Taeniasaginataи Hymenolepisnana) в развитии постинфекционных ФРОП, в частности в развитии СРК (OР составил: 1,69), функционального запора (Oр: 4,13) [14].
Роли кишечной микробиоты в патофизиологии СРК в настоящее время посвящено большое количество экспериментальных и клинических исследований. Были продемонстрированы изменения в микробиоме кишечника, хотя неясно, являются ли эти изменения причиной или результатом СРК и его симптомов [15].
Установлено, что качественные и количественные изменения микрофлоры оказывают влияние на функцию кишечника, выступая в качестве причины нарушений его двигательной активности, чувствительности и нейроиммунных взаимоотношений, включая нарушение экспрессии рецепторов слизистой оболочки и изменения функции гипоталамо-гипофизарно-надпочечниковой системы. Известно, что кишечная микрофлора утилизирует нерастворимые углеводы и выделяются метаболиты, среди них важное значение имеют короткоцепочечные жирные кислоты (уксусная, пропионовая и масляная кислоты). Именно эти короткоцепочечные жирные кислоты (КЦЖК) в разных отделах толстой кишки оказывают противоположное влияние на моторную ее активность, через стимуляцию определенных рецепторов, вырабатывающих биологически активные вещества. В проксимальных отделах толстой кишки КЦЖК стимулируют рецепторы L-клеток, которые вырабатывают регуляторный полипептид PYY, замедляющий двигательную активность не только толстой, но и тонкой кишки. А в дистальных отделах КЦЖК стимулируют рецепторы Ecl-клеток, вырабатывающих гистамин, который, действуя на 5-HT 4-рецепторы афферентных волокон блуждающего нерва, инициирует рефлекторное ускорение моторики. Среди КЦЖК, важное значение для колоноцитов имеет масляная кислота (бутират), которая является важнейшим энергетическим источником для колоноцитов, синтеза липидов мембран, защитного барьера и проницаемости слизистой оболочки толстой кишки, подавления окислительного стресса, воспаления, колоректального канцерогенеза, восстановления водно-электролитного баланса. Кроме этого, масляная кислота (бутират) оказывает регулирующее влияние на кишечную моторику [16].S.A.Vanhoutvin с соавт. изучали влияние масляной кислоты (бутирата) на висцеральную гиперчувствительность у здоровых добровольцев. Участникам исследования ректально вводили масляную кислоту. Результаты исследования показали, что введение масляной кислоты повышало порог болевой чувствительности и снижало боль и дискомфорт, вызванные раздуванием ректального баллона, что оценивалось по аналоговой шкале. При этом отмечено, что введение бутирата имело дозозависимый эффект, чем выше была доза бутирата, тем больше снижалась висцеральная чувствительность [17].
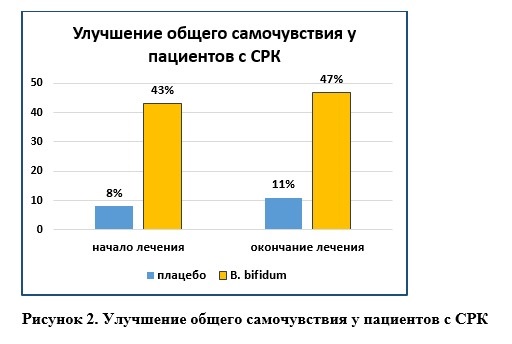
Применение одного из штаммов Bifidobacterium bifidum у пациентов с симптомами СРК приводило к значимому снижению таких симптомов как боль/дискомфорт в животе, метеоризм, нарушение пищеварения у 57% пациентов по сравнению с 21% в группе плацебо [19].

В метаанализе проводилась оценка результатов 24 клинических исследований с участием 2001 пациентов с СРК. Результаты анализа показали достоверное уменьшение симптомов боли и общих симптомов у пациентов при применении мультиштаммовых пробиотиков. Мультиштаммовые пробиотики оценивались в 12 РКИ с участием 1197 пациентов со значительным влиянием на симптом абдоминальной боли (ОР = 0,81; 95% ДИ 0,67–0,98, р 8 КОЕ, а также пребиотический компонент фруктоолигосахарид. Инновационная капсула DRcaps™, в свою очередь, нейтрализует негативное воздействие кислого содержимого желудка, солей желчных кислот и пищеварительных ферментов.
Ведущую роль в структуре абдоминального болевого синдрома наиболее часто играет спастическая висцеральная боль, в основе которой лежит непроизвольное сокращение гладких мышц кишечника, не сопровождающееся их немедленным расслаблением. Селективные миотропные спазмолитики имеют возрастные ограничения у детей. По клинической эффективности тримебутин сопоставим с такими спазмолитиками, как пинаверия бромид и мебеверин в терапии боли в животе при СРК у взрослых [27].
Механизм действия тримебутина заключается в стимуляции периферических опиоидных (энкефалиновых) рецепторов (μ-, k-, δ-) на протяжении всего ЖКТ. Связывание с k-рецепторами приводит к снижению мышечной активности, а связывание с μ- и δ-рецепторами вызывает ее стимуляцию. При этом препарат не оказывает влияние на другие рецепторы. Тримебутин оказывает прямое действие на гладкомышечные клетки через рецепторы миоцитов и ганглиев энтеральной нервной системы, имитируя действие энкефалинов [28]. На российском фармацевтическом рынке присутствует дженерик препарата тримебутина: Необутин® (выпускается в таблетированной форме в дозировках 100 и 200 мг), который разрешен детям с 3-х лет. Препарат оказывает нормализирующее влияние на моторную функцию желудочно-кишечного тракта: в зависимости от исходного состояния ЖКТ он оказывает стимулирующее или расслабляющее воздействие на ЖКТ. Кроме того, тримебутин оказывая влияние на Na + и Ca 2+ -каналов, обеспечивает анестезирующее действие и прямой спазмолитический эффект, таким образом опосредованно нормализует моторику ЖКТ и висцеральную гиперчувствительность.
Проведена сравнительная оценка эффективности терапии препаратами, координирующими моторику кишечника (тримебутин) как монотерапии, так и в комбинации с пробиотиками у детей в возрасте 5-17 лет с симптомами СРК. В первой группе (n=15) проводилась терапия тримебутином в возрастной дозировке курсом 1 месяц, во второй группе (n=15) проводилась комбинированная терапия тримебутин + пробиотики. Авторы определяли уровень фекального кальпротектина (белка, отражающего выраженность воспалительного процесса), как показателя воспаления в кишечнике. Уровень кальпротектина у пациентов с СРК был исходно повышен у 27,3% детей, средний уровень показателя превышал нормальные показатели в 2 раза.
Полученные результаты показали высокую эффективность тримебутина (у 82% детей) при монотерапии, и наилучший результат (до 98%) при комбинации тримебутина с пробиотиком. В группе плацебо купирование абдоминальной боли наблюдалось у 22 % детей. Нормализация стула у 99% детей второй группы и 15% группы плацебо [29].
В другом исследовании оценивали распространенность СРК у детей и эффективность тримебутина в коррекции клинической симптоматики. Были включены 345 детей и подростков от 4-18 лет. Распространенность СРК в соответствии с критериями Рима III у детей и подростков составила 22,6%, причем преобладающим подтипом был СРК с запором. 78 детей и подростков с нормальными лабораторными показателями и установленным диагнозом СРК были рандомизированы на две группы: 39 пациентов получали тримебутин 300 мг в сутки три недели, 39 пациентов не получали медикаментозного лечения. Клиническое улучшение наблюдалось у 94,9% пациентов, принимавших тримебутин против 20,5% в группе, не применявшей медикаментозное лечение (P
Читайте также:

