Реферат по физике насыщенный пар
Обновлено: 30.06.2024
Вещества могут переходить из твердого состояния в жидкое, а из жидкого в газообразное. При том они поглощают энергию. Вы уже познакомились с первым переходом — процессом плавления. Теперь мы будем рассматривать следующий переход вещества из одного состояния в другое — превращение жидкости в газ.
Повседневные наблюдения позволяют сказать, что количество жидкости, находящейся в открытом сосуде, со временем уменьшается. Но жидкость не может просто так исчезнуть. Что же с ней происходит? Она превращается в пар.
Парообразование — это явление превращения жидкости в пар.
Есть два способа превращения жидкости в газ:
В данном уроке мы рассмотрим первый способ — испарение.
Испарение
Испарение — это парообразование, происходящее с поверхности жидкости.
Молекулы жидкости находятся в беспрерывном движении. Движутся они с разными скоростями.
Иногда достаточно “быстрые молекулы” могут оказаться у поверхности жидкости. Тогда они преодолевают притяжение соседних молекул и вылетают из жидкости. Такие молекулы образуют над жидкостью пар.
Другие молекулы при движении соударяются друг с другом и со стенками сосуда. При этом меняются их скорости. Так образуются новые “быстрые” молекулы, способные вылететь из жидкости.
Этот процесс все время продолжается, поэтому жидкость испаряется постепенно.
Скорость испарения и род жидкости
Очевидно, что жидкости испаряются не всегда одинаково. Когда-то быстрее, когда-то медленнее. Скорость испарения зависит от определенных причин.
Наполним два одинаковых открытых сосуда водой и эфиром одинаковой массы (рисунок 1).
Мы заметим, что эфир будет испаряться намного быстрее, чем вода. Мы можем фиксировать эти изменения, взвешивания воду или отмечая ее объем.
Скорость испарения зависит от рода жидкости.
Быстрее будет испаряться та жидкость, в которой молекулы притягиваются друг к другу с меньшей силой. В таких жидкостях большему количеству молекул проще преодолеть сопротивление и вылететь.
Скорость испарения и температура
В жидкостях всегда имеется некоторое число быстро движущихся молекул. Значит,
Испарение происходит при любой температуре.
Наполним два одинаковых сосуда водой одинаковой массы. Но в один сосуд нальем воду комнатной температуры, а в другой — подогретую до высокой температуры (рисунок 2).
Наблюдения покажут, что количество подогретой жидкости в сосуде уменьшилось быстрее, чем жидкости комнатной температуры.
Испарение происходит тем быстрее, чем выше температура жидкости.
При увеличении температуры жидкости, увеличивается ее внутренняя энергия. При этом увеличивается средняя кинетическая энергия молекул и средняя скорость их движения. Значит, чем выше температура жидкости, тем больше в ней быстро движущихся молекул, которыe способны вылететь с поверхности.
Например, после дождя на улице остаются лужи. Дождь может пройти и холодной осенью, и жарким летом. Когда лужи высыхают быстрее? Конечно же летом, когда на улице более высокая температура.
Скорость испарения и площадь поверхности жидкости
Возьмем два сосуда одинакового объема, но разной формы. Один широкий, а второй — узкий (рисунок 3). Заполним их водой одной и той же массы.

Рисунок 3. Зависимость скорости испарения от площади поверхности жидкости
Наблюдения покажут, что вода из широкого сосуда будет испаряться быстрее, чем из узкого.
Скорость испарения жидкости зависит от площади ее поверхности.
Испарение происходит с поверхности жидкости. Значит, чем больше поверхность, тем большее количество молекул одновременно вылетает в воздух.
Зачем мы развешиваем белье после стирки? Чтобы оно быстрее высохло. Ведь в скомканном состоянии его площадь намного меньше, чем в расправленном виде.
Скорость испарения и ветер
Быстро движущиеся молекулы вылетают из жидкости, образуя пар. Одновременно с этим происходит обратный процесс. Некоторые молекулы пара, беспорядочно двигаясь над поверхностью жидкости, снова возвращаются в нее.
Очевидно, что если уменьшить количество возвращающихся в жидкость молекул, скорость испарения увеличится. Количество жидкости будет уменьшаться быстрее. Это возможно при наличии ветра (рисунок 4).
При наличии ветра испарение жидкости происходит быстрее.
Ветер уносит молекулы пара, не давая их части вернуться обратно в жидкость.
Насыщенный пар и динамическое равновесие между паром и жидкостью
Рассмотрим испарение жидкости в закрытом сосуде (рисунок 5).

Рисунок 5. Жидкость и пар в динамическом равновесии
Вначале испарение будет идти точно так же как и в открытом сосуде: количество вылетающих молекул будет больше количества молекул, которые возвращаются обратно в жидкость. Но они не могут улететь в окружающую среду, поэтому плотность пара над поверхностью жидкости будет постепенно увеличиваться.
С увеличением плотности пара будет увеличиваться и число молекул, возвращающихся обратно в жидкость. Постепенно, число молекул, вылетающих из жидкости, станет равным числу молекул, возвращающихся в нее. Число молекул пара над жидкостью станет постоянным — наступит динамическое равновесие между паром и жидкостью.
В таком случае пар называют насыщенным.
Насыщенный пар — это пар, находящийся в динамическим равновесии со своей жидкостью.
При динамическом равновесии масса жидкости в закрытом сосуде несмотря на испарение не изменяется.
Ненасыщенный пар
Если в пространстве, которое окружает рассматриваемую жидкость и содержит ее пары, может происходить дальнейшее испарение, то пар, находящийся в этом пространстве называют ненасыщенным.
Ненасыщенный пар — это пар, не находящийся в состоянии равновесия со своей жидкостью.
Так, в открытом сосуде масса жидкости будет постепенно уменьшаться. Большинство молекул пара будет оставаться в воздухе, не возвращаясь обратно в жидкость.
Испарение твердых тел
Некоторые твёрдые тела тоже могут испаряться. Испарение твердых тел называют возгонкой (или сублимацией).
Например, таким свойством обладает лёд. Это объясняет то, что белье после стирки высыхает и на зимнем морозе. Нафталин испаряется при комнатной температуре, поэтому мы чувствуем его запах.
Запах создается молекулами, оторвавшимися от вещества и достигшими нашего носа. Поэтому говорят, что всякое пахнущее твёрдое вещество возгоняется в значительной степени.
На самом деле испаряются все твердые тела (даже железо). Но плотность насыщенного пара оказывается настолько мала, что обнаружить его очень сложно, иногда практически невозможно.
Молекулярно-кинетическая теория позволяет не только понять, почему вещество может находиться в газообразном, жидком и твёрдом состояниях, но и объяснить процесс перехода вещества из одного состояния в другое.
Вспомните, что представляет собой модель идеального газа.
Можно ли с помощью этой модели объяснить явление конденсации?
Идеальный газ нельзя превратить в жидкость.
В жидкость превращается реальный газ.
Испарение и конденсация.
Молекулы жидкости движутся беспорядочно.
Чем выше температура жидкости, тем больше кинетическая энергия молекул.
Среднее значение кинетической энергии молекул при заданной температуре имеет определённое значение.
Но у каждой молекулы кинетическая энергия в данный момент времени может оказаться как меньше, так и больше средней.
В какой-то момент времени кинетическая энергия отдельных молекул может стать настолько большой, что они окажутся способными вылететь из жидкости, преодолев силы притяжения остальных молекул.
Процесс превращения жидкости в пар называется испарением.
При этом процессе число молекул, покидающих жидкость за определённый промежуток времени, больше числа молекул, возвращающихся в неё.
Плотно закрытый флакон с духами может стоять очень долго, и количество духов в нём не изменится.
Если же флакон оставить открытым, то через достаточно продолжительное время вы увидите, что жидкости в нём нет.
Жидкость, в которой растворены ароматические вещества, испарилась.
Гораздо быстрее испаряется (высыхает) лужа на асфальте, особенно если высока температура воздуха и дует ветер.
Если поток воздуха над сосудом уносит с собой образовавшиеся пары жидкости, то жидкость испаряется быстрее, так как у молекулы пара уменьшается возможность вновь вернуться в жидкость.
Чем выше температура жидкости, тем большее число молекул имеет достаточную для вылета из жидкости кинетическую энергию, тем быстрее идёт испарение.
При испарении жидкость покидают более быстрые молекулы, поэтому средняя кинетическая энергия молекул жидкости уменьшается.
Смочив руку какой-нибудь быстро испаряющейся жидкостью (например, бензином или ацетоном), вы тут же почувствуете сильное охлаждение смоченного места.
Охлаждение этого места усилится, если на руку подуть.
Процесс испарения происходит со свободной поверхности жидкости.
Если лишить жидкость возможности испаряться, то охлаждение её будет происходить гораздо медленнее.
Вспомните, как долго остывает жирный бульон.
Слой жира на его ности мешает выходу быстрых молекул воды.
Жидкость почти не испаряется, и её температура падает медленно (сам жир испаряется крайне медленно, так как чего большие молекулы более прочно сцеплены друг с другом, чем молекулы воды).
Вылетевшая молекула принимает участие в беспорядочном тепловом движении газа.
Беспорядочно двигаясь, она может навсегда удалиться от поверхности жидкости, находящейся в открытом сосуде, но может и вернуться снова в жидкость.
Процесс превращения пара в жидкость называется конденсацией.
При этом процессе число молекул, возвращающихся в жидкость за определённый промежуток времени, больше числа молекул, покидающих её.
Насыщенный пар.
Если сосуд с жидкостью плотно закрыть, то сначала количество жидкости уменьшится, а затем будет оставаться постоянным.
При неизменной температуре система жидкость—пар придёт в состояние теплового равновесия и будет находиться в нём сколь угодно долго.
Одновременно с процессом испарения происходит и конденсация, оба процесса в среднем компенсируют друг друга.
В первый момент, после того как жидкость нальют в сосуд и закроют его, жидкость будет испаряться и плотность пара над ней будет увеличиваться.
Однако одновременно с этим будет расти и число молекул, возвращающихся в жидкость.
Чем больше плотность пара, тем большее число его молекул возвращается в жидкость.
В результате в закрытом сосуде при постоянной температуре установится динамическое (подвижное) равновесие между жидкостью и паром.
Динамическое равновесие — это состояние, при котором число молекул, покидающих поверхность жидкости за некоторый промежуток времени, будет равно в среднем числу молекул пара, возвратившихся за то же время в жидкость.
Для воды при комнатной температуре это число приблизительно равно 10 22 молекул за время, равное 1 с (на 1 см 2 площади поверхности).
Пар, находящийся в динамическом равновесии со своей жидкостью, называют насыщенным паром.
Согласно этому определению в данном объёме при данной температуре не может находиться большее количество пара.
Если воздух из сосуда с жидкостью предварительно откачан, то в сосуде над поверхностью жидкости будет находиться только её насыщенный пар.
Основы термодинамики. Тепловые явления - Физика, учебник для 10 класса - Класс!ная физика
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам
Лекция № 7
Испарение и конденсация. Насыщенный пар и его свойства. Влажность воздуха
Взаимные превращения жидкостей и газов - это процессы перехода вещества из одного состояния в другое.
Испарение – это процесс перехода жидкости в пар (газообразное состояние).
Испарение происходит при любой температуре жидкости.
Пар - это газообразное состояние вещества, в которое переходят жидкости при испарении.
Молекулы жидкости при тепловом движении движутся с разными скоростями. Самые быстрые молекулы способны преодолеть притяжение остальных молекул и выскочить из жидкости.
Эти молекулы образуют пары в воздухе.
Скорость испарения жидкости зависит от:
- температуры (чем выше температура жидкости, тем большей скоростью обладают ее молекулы)
- от площади поверхности испаряющейся жидкости (чем больше площадь поверхности, тем большее число быстрых молекул покидает жидкость)
- от наличия ветра над поверхностью жидкости
Так как при испарении жидкость покидают наиболее быстрые молекулы, обладающие соответственно большей кинетической энергией, средняя кинетическая энергия молекул жидкости уменьшается, значит температура жидкости при испарении понижается.
Насыщенный пар
Рассмотрим процесс образования насыщенного пара:
В сосуд наливаем жидкость и закрываем его. Жидкость в сосуде начинает испаряться, и плотность пара над жидкостью в сосуде увеличивается.
В результате теплового движения часть молекул водяного пара возвращается в жидкость. Чем больше плотность водяных паров в сосуде, тем большее число молекул пара возвращается в жидкость.
Через некоторое время в сосуде устанавливается динамическое равновесие между жидкостью и паром:
число молекул, покинувших жидкость за какой-то отрезок времени, становится равным числу молекул, возвращающихся в жидкость за такой же отрезок времени.
В сосуде образовался насыщенный пар.
Насыщенный пар – это пар, находящийся в динамическом равновесии со своей жидкостью.
Давление насыщенного пара
Давление насыщенного пара это давление пара, при котором жидкость находится в равновесии со своим паром.
где
n - концентрация молекул пара
k - постоянная Больцмана
Т - температура
Давление и концентрация молекул (плотность) насыщенного пара при постоянной температуре не зависят от занимаемого паром объема.
Давление насыщенного пара зависит только от его температуры .
Давление насыщенного пара растет как вследствие повышения температуры жидкости, так и вследствие увеличения концентрации молекул пара.
Ненасыщенный пар
Пар называется ненасыщенным , если его давление меньше давления насыщенного пара при данной температуре.
Давление ненасыщенного пара зависит от его объема:
при уменьшении объема давление увеличивается, а при увеличении объема - уменьшается.
Влажность воздуха
Влажность воздуха – это содержание водяного пара в воздухе.
Атмосферный воздух состоит из смеси газов и водяных паров.
Влажность воздуха характеризуется следующими величинами:
1. Абсолютная влажность воздуха – это масса водяных паров, содержащихся в 1 куб. метре воздуха при данных условиях.
Абсолютная влажность воздуха может оцениваться:
а) через плотность водяного пара в воздухе, тогда единицы измерения – г/м3.
б) в метеорологии - через парциальное давление водяного пара, тогда единицы измерения - мм рт. ст. или Па.
Парциальное давление водяного пара – это давление, которое производил бы водяной пар, если бы остальные газы воздуха отсутствовали.
2. Относительная влажность воздуха - это отношение парциального давления водяного пара, содержащегося в воздухе при данной температуре, к давлению насыщенного водяного пара при той же температуре.
Единицы измерения относительной влажности - %.
Ф = *100%
где
р – парциальное давление водяного пара в воздухе при температуре t
р 0 - давление насыщенного водяного пара при той же температуре
В прогнозе погоды указывается величина относительной влажности воздуха в процентах!
Относительная влажность воздуха показывает как близко содержание водяных паров в воздухе к насыщению.
При относительной влажности 100% - в воздухе насыщенный водяной пар.
Прибор для измерения относительной влажности воздуха называется психрометром .
Все мы гении. Но если вы будете судить рыбу по её способности взбираться на дерево, она проживёт всю жизнь, считая себя дурой.
Альберт Эйнштейн
Вопросы к экзамену
Для всех групп технического профиля
Учу детей тому, как надо учиться
Часто сталкиваюсь с тем, что дети не верят в то, что могут учиться и научиться, считают, что учиться очень трудно.
Урок 18. Лекция 18. Свойства паров
Насыщенные и ненасыщенные пары.
Рассмотрим процессы, происходящие в закрытом сосуде:
- процесс испарения, скорость которого постепенно уменьшается
- конденсации, скорость которого постепенно возрастает
С течением времени в сосуде закрытом крышкой между жидкостью и её паром устанавливается состояние динамического (подвижного) равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, то есть когда скорости процессов испарения и конденсации одинаковы. Такую систему называютдвухфазной.
Пар, находящийся в динамическом равновесии со своей жидкостью, называютнасыщенным.
Ненасыщенный пар – это пар, не достигший динамического равновесия со своей жидкостью. При данной температуре давление ненасыщенного пара всегда меньше давления насыщенного пара. При наличии над поверхностью жидкости ненасыщенного пара процесс парообразования преобладает над процессом конденсации, и потому жидкости в сосуде с течением времени становится все меньше и меньше.
Рассмотрим некоторые свойства насыщенного пара:
1. Концентрация молекул насыщенного пара не зависит от его объёма при постоянной температуре. Если уменьшить объем насыщенного пара, то сначала концентрация его молекул увеличится и из газа в жидкость начнет переходить больше молекул до тех пор, пока опять на установится динамическое равновесие.
2. Давление насыщенного пара при постоянной температуре не зависит от его объёма.
p = n*k*T, т.к. n не зависит от V , то и р не зависит от V.
Независимое от объёма давление пара, при котором жидкость находится в равновесии со своим паром, называется давлением насыщенного пара. Это наибольшее давление, которое может иметь пар при данной температуре.
3. Давление насыщенного пара зависит от температуры. Чем выше будет температура жидкости, тем больше молекул будет испаряться, динамическое равновесие нарушится, но концентрация молекул пара будет расти до тех пор, пока равновесие не установится опять, а значит, больше станет и давление насыщенного пара. С увеличением температуры давление насыщенных паров возрастает.
В атмосферном воздухе всегда присутствуют пары воды, которая испаряется с поверхности морей, рек, океанов и т.п.
Воздух, содержащий водяной пар, называют влажным.
Влажность воздуха оказывает огромное влияние на многие процессы на Земле: на развитие флоры и фауны, на урожай сельхоз. культур, на продуктивность животноводства и т.д. Влажность воздуха имеет большое значение для здоровья людей, т.к. от неё зависит теплообмен организма человека с окружающей средой. При низкой влажности происходит быстрое испарение с поверхности и высыхание слизистой оболочки носа, гортани, что приводит к ухудшению состояния.
Значит, влажность воздуха надо уметь измерять. Для количественной оценки влажности воздуха используют понятия абсолютной и относительной влажности.
Абсолютная влажность – величина, показывающая, какая масса паров воды находится в 1 м³ воздуха. Она равна парциальному давлению пара при данной температуре.
Парциальное давление пара – это давление, которое оказывал бы водяной пар, находящийся в воздух , если бы все остальные газы отсутствовали.
Относительная влажность воздуха – это величина, показывающая, как далек пар от насыщения. Это отношение парциального давления p водяного пара, содержащегося в воздухе при данной температуре, к давлению насыщенного пара p0 при той же температуре, выраженное в процентах:
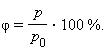
Если воздух не содержит паров воды, то его абсолютная и относительная влажность равны 0.
Если влажный воздух охлаждать, то находящийся в нем пар можно довести до насыщения, и далее он будет конденсироваться.
выпадение росы под утро,

запотевание холодного стекла, если на него подышать,

образование капли воды на холодной водопроводной трубе,

сырость в подвалах домов.

Точка росы – это температура, при которой водяной пар, содержащийся в воздухе, становится насыщенным.
Варианты структурирования теоретического учебного материала по теме "Насыщенные и ненасыщенные пары. Влажность воздуха" в курсе физики, которая в определенных аспектах является проблемной как с содержательной, так и с методической точек зрения.
| Рубрика | Физика и энергетика |
| Вид | статья |
| Язык | русский |
| Дата добавления | 09.11.2018 |
| Размер файла | 336,4 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
К вопросу об особенностях изучения темы "насыщенные и ненасыщенные пары. Влажность воздуха" в курсе физики
Грачева Ирина Николаевна
В статье предлагается вариант структурирования теоретического учебного материала по теме "Насыщенные и ненасыщенные пары. Влажность воздуха" в курсе физики, которая в определенных аспектах является проблемной как с содержательной, так и с методической точек зрения. Проанализировав учебную и методическую литературу школьного курса физики и технических вузов, авторы разработали таблицы, наглядно отображающие весь материал данной темы. Приводится методическое обоснование соответствующего учебного материала.
Столь большая значимость физики как науки формирует необходимость ее изучения не только с научной точки зрения, но и как учебной дисциплины. Основы физической науки являются обязательными для преподавания в общеобразовательном курсе современной школы, поскольку служат передаче накопленного человечеством опыта в познании мира новым поколениям, а также занимают важное место в формировании разносторонней личности учащегося, обеспечивая оптимальное развитие всех его потенциальных способностей.
Несмотря на длительный опыт преподавания физики, в современном образовании существуют традиционные проблемы, вызывающие определенные трудности в процессе обучения. Зачастую это связанно с недостаточным уровнем знаний в смежных дисциплинах. Одной из проблем в этой области является недостаточно высокий уровень базовых математических знаний, необходимый для решения физических задач. Другой не менее важной и гораздо более сложной в разрешении проблемой является непонимание учащимися основных физических принципов и, исходя из этого, сложности с применением неусвоенных теоретических знаний при решении конкретных практических задач как на бумаге, так и в жизни.
Для преодоления этих трудностей необходимо усовершенствовать методику преподавания отдельных разделов физики, реструктурировать их, это позволит повысить уровень знаний, образовательную активность и успеваемость учащихся, а также высвободит время для изучения более сложных и глубоких для понимания и проработки разделов.
Таким образом, в учебно-образовательной литературе образуется своеобразная информационная лакуна. С одной стороны, тема по сути своей (в сравнении с прочими разделами физики) не представляет особой сложности, но, ввиду некоторых особенностей подачи материала, учащиеся сталкиваются с проблемами, что вызывает распространённые ошибки, в основе которых лежит недопонимание теоретических основ темы.
В первой таблице нами были структурированы различия в поведении ненасыщенного и насыщенного пара в различных термодинамических процессах. Для наглядности были использованы графики этих процессов.
Читайте также:

