Реферат на тему глицин
Обновлено: 04.07.2024
Заменимая аминокислота. Белый кристаллический порошок, легко растворим в воде.
Фармакологическое действие
Фармакологическое действие - антистрессовое, ноотропное, нормализующее обменные процессы, противоэпилептическое, седативное.
Фармакология
Легко проникает в большинство биологических жидкостей и тканей организма, в т.ч. в головной мозг. Быстро разрушается в печени глициноксидазой.
Является нейромедиатором тормозного типа действия и регулятором метаболических процессов в головном и спинном мозге. Нормализует процессы возбуждения и торможения в ЦНС , повышает умственную работоспособность, устраняет депрессивные нарушения, повышенную раздражительность. Глицин эффективен в качестве вспомогательного средства при эпилептических приступах. Нормализует сон. Оказывает многокомпонентное противоишемическое действие: активирует тормозную трансмиссию, снижает содержание в ЦНС токсических продуктов (альдегиды, кетоны и др.), образующиеся в каскадных реакциях при острой ишемии и регулирует тонус симпатической нервной системы.
Не проводящий электрический ток 1,5% раствор используется исключительно в урологической практике для трансуретральной инстилляции при проведении трансуретральной резекции предстательной железы и других трансуретральных электрохирургических манипуляций (по данным PDR Generics, 1997).
Применение вещества Глицин
Стрессовые состояния, психоэмоциональное напряжение, повышенная возбудимость, эмоциональная лабильность, неврозы, неврозоподобные состояния, вегетососудистая дистония, последствия нейроинфекций и черепно-мозговой травмы, различных форм энцефалопатий (перинатальные и другие формы), в т.ч. алкогольного генеза, нарушение сна; острый ишемический инсульт. Для повышения умственной работоспособности, в т.ч. подросткам с девиантными формами поведения.
Противопоказания
Побочные действия вещества Глицин
Возможны аллергические реакции.
Взаимодействие
Снижает выраженность токсических эффектов противосудорожных средств, нейролептиков, антидепрессантов.
Способ применения и дозы
Внутрь сублингвально, при психоэмоциональном напряжении, снижении памяти, внимания, умственной работоспособности, детям с задержкой умственного развития, подросткам с девиантными формами поведения — по 0,1 г 2–3 раза в сутки в течение 14–30 дней. Суточная доза — 0,3 г, курсовая — 4,2–9,0 г.
При функциональных и органических поражениях нервной системы, сопровождающихся повышенной возбудимостью, эмоциональной лабильностью и нарушением сна, детям до 3 лет назначают по 0,05 г на прием 2–3 раза в сутки в течение 7–14 дней, в дальнейшем — 0,05 г 1 раз в сутки 7–10 дней. Суточная доза — 0,1–0,15 г, курсовая — 2,0–2,6 г. Детям старше 3 лет и взрослым — по 1 табл. 2–3 раза в сутки, курс лечения 7–14 дней. При необходимости курс лечения повторяют.
При нарушениях сна — по 0,05–0,1 г за 20 мин до сна или непосредственно перед сном. Детям до 3 лет — 0,05 г на прием 2–3 раза в сутки в течение 7–14 дней, в следующие 7–10 дней — по 0,05 г 1 раз в сутки. Суточная доза — 0,1–0,4 г, курсовая — 2,0–2,6 г.
При ишемическом мозговом инсульте — в течение первых 3–6 ч от развития инсульта назначают 1 г (трансбуккально или сублингвально) с 1 ч.ложкой воды, далее в течение 1–5 суток по 1 г/сут, в течение следующих 30 суток по 0,1–0,2 г 3 раза в сутки.
Меры предосторожности
Следует иметь в виду, что во время проведения трансуретральной резекции предстательной железы, как правило сопровождающейся местной аппликацией глицина, он может попадать в системный кровоток и влиять на состояние сердечно-легочной системы и почек, особенно у пациентов с сердечно-сосудистыми заболеваниями.
В работе представлена общая характеристика препарата "Глицин", области его применения, технологии производства, свойства, биологическая роль и многое другое. Также рассмотрены преимущества препарата Глицин форте
Содержание работы
Файлы: 1 файл
МИНИСТЕРСТО ОБРАЗОВАНИЯ И НАУК РОССИЙСКОЙ ФЕДЕРАЦИИ.doc
МИНИСТЕРСТО ОБРАЗОВАНИЯ И НАУК РОССИЙСКОЙ ФЕДЕРАЦИИ
Кемеровский технологический институт пищевой промышленности
Кафедра: органическая химия
Реферат на тему:
Выполнила студентка гр. ПБ-81
Проверил д.т.н, профессор
Эта была первая попытка понять, из каких компонентов состоят белки.
Гликоколл (позже его переименовали в глицин, поскольку он входит не только в коллаген) был первой аминокислотой, найденной в составе белков.
Это открытие Браконно было первым указанием на то, что молекулы белков состоят из более простых молекул, однако ученые еще не могли прийти к такому выводу, для этого не хватало фактов.
Анри Браконно (1780-1855), Франция
Открытие Браконно сыграло особенно важную роль, поскольку оно явилось первым случаем получения аминокислот из гидролизата белка; в дальнейшем из гидролизатов белков были выделены и идентифицированы и остальные аминокислоты, содержащиеся в составе белковых молекул.
Характеристика и биологическая роль глицина
Глицин начали производить уже несколько десятков лет назад. Его продуцируют из соединительной ткани сельскохозяйственных животных.
Глицин, как простая аминокислота для начала производится в организме человека, где он имеется во всех клетках, особенно высоко его содержание в нервных клетках головного мозга. В фармацевтической промышленности организовано полное синтетическое его производство.
Глицин входит в состав многих белков и биологически активных соединений. Из глицина в живых клетках синтезируются порфирины и пуриновые основания.
Химическая формула: NH2-CH2- COOH
Активно участвует в обеспечении кислородом процесса образования новых клеток. Является важным участником выработки гормонов, ответственных за усиление иммунной системы. Эта аминокислота является исходным веществом для синтеза других аминокислот, а также донором аминогруппы при синтезе гемоглобина и других веществ. Глицин очень важен для создания соединительных тканей; в анаболической фазе потребность в этой аминокислоте повышается. Недостаток ее вызывает нарушение структуры соединительной ткани. Повышенное потребление глицина снижает содержание фермента катепсина D и в катаболической ситуации препятствует распаду белков. Он способствует мобилизации гликогена из печени и является исходным сырьем в синтезе креатина, важнейшего энергоносителя, без которого невозможна эффективная работа мышц. Глицин необходим для синтеза иммуноглобулинов и антител, а следовательно, имеет особое значение для работы иммунной системы. Недостаток этой аминокислоты ведет к снижению уровня энергии в организме. Глицин также способствует ускоренному синтезу гипофизом гормона роста. Природные источники глицина: Желатин Говядина Печень Арахис Овес .
Применение глицина
Применяется глицин в основном в медицинской, пищевой и химической промышленности. Физические свойства: Белый кристальный порошок, имеет сладкий вкус, легко растворяется в воде, хуже в метиловом спирте, не разлагается в ацетоне и эфире. Точка плавления 232-236 ℃ .
Назначение глицина медицинской категории:
- Используется, как лекарство для изучения обмена аминокислоты в области медицинских микробов и биохимии.
- Кака синтетическое сырье для производства аминокислот, например: дуомицин, лекарство от болезни Паркинсона, L-доба, витамин В6 и треонин и т.д..
- Как аминокислотная питательная жидкость.
- Как сырье для цефалоспорина, уксусной кислоты и Thiamphenicol и.т.д.
- Как сырье для косметики.
Фармакологический препарат глицина оказывает седативное (успокаивающее), мягкое транквилизирующее и слабое антидепрессивное действие, уменьшает чувство тревоги, страха, психоэмоционального напряжения, усиливает действие противосудорожных препаратов, антидепрессантов, антипсихотиков, уменьшает проявления алкогольной и опиатной абстиненции. Обладает некоторыми ноотропными свойствами, улучшает память и ассоциативные процессы .
Назначение глицина пищевой категории:
- Используется в качестве пищевой добавки Е 640. Вместе с DL-аланином и лимонной кислотой используется на производстве сока и спирта как добавка предохраняющая от кислого вкуса, при солении соленых овощей, изготовлении сладкой пасты, соуса, уксуса и сока; используется для улучшения, сохранения и создания сладкого вкуса и.т.д.
- Используется как консервант для изделий из рыбной муки, пасты арахиса, способен к торможению размножения сенной палочки и кишечной палочки.
- Используется как средство для удаления горького запаха у пищевых продуктов, как стабилизатор для масла, сыра, исскуственного молока, лапши быстрого приготовления, пшеничной муки и т.д.
- В пищевом производстве стабилизирует витамин С .
Назначение глицина промышленной категории
- Используется как добавка для гальванической жидкости;
- Как регулирующее PH средство ;
- Как в корме для домашних птиц и животных.
Разновидности глицина и его свойства
Медицинская категория
Пищевая категория
после прокаливания
Производство глицина
Аминокислоты получают путем химического синтеза, биосинтеза или экстракцией из белковых гидролизатов. К химическому синтезу относят способ получения глицина через аммонолиз и последующее омыление водных растворов гликолонитрила
HOCH2CN H2NCH2CN____→ H2NCH2COOH 1 Однако исходный гликолонитрил не является доступным реагентом, а должен быть специально получен из формальдегида и синильной кислоты или ее солей. Необходимость применения этих сильно-ядовитых веществ в синтетической цепи - один из основных недостатков способа. К другим относятся: проведение стадий аммонолиза и омыления в разбавленных водных растворах и количественные затраты минеральных кислот и щелочей, что обусловливает наличие больших количеств загрязненных сточных вод и невысокий выход глицина в расчете на гликолонитрил, который составляет 69% или 85%.
Известен способ получения глицина щелочным гидролизом гидантоина. Выход глицина составляет 95% , тем не менее ему присущи недостатки описанного способа, поскольку для получения исходного гидантоина необходима синильная кислота (синтез Штрекера), а его гидролиз требует количественных затрат водной щелочи.
В промышленной практике наиболее распространен способ получения глицина аммонолизом монохлоруксусной кислоты (МХУК), доступного многотоннажного реагента, в водном растворе в присутствии гексаметилентетрамина
ClCH2COOH+NH H2NCH2COOH+NH4Cl Так известен способ получения глицина обработкой МХУК или ее аммонийной или натриевой солей аммиаком и NaOH в водной среде, содержащей гексаметилентетрамин и NH4 + -ионы в молярном соотношении с МХУК не менее, чем 1 : 3 (5).
Первые 1/4 - 1/2 количества МХУК обрабатывают аммиаком в молярном соотношении 1 : 2, затем оставшуюся МХУК обрабатывают водным раствором NaOH в молярном соотношении 1 : 2 при 65-70 о С. Общая продолжительность синтеза 3 ч. Выход глицина 93,0% .
Способ имеет высокие расходные показатели: 0,57 т NaOH, 0,30 т гексаметилентетрамина, 2,85 т воды на 1 т неочищенного глицина, а главное - большой объем загрязненных сточных вод, что недоступно в современной экологической ситуации.
Наиболее близким по технической сущности и достигаемому эффекту к предлагаемому является способ синтеза глицина из МХУК и аммиака в присутствии гексаметилентетрамина, проводимый в среде метилового или этилового спирта (6-прототип).
Глицин по этому способу получают одновременным введением метанольного раствора МХУК и газообразного аммиака в реакционный сосуд, заполненный водно-метанольным раствором гексаметилентетрамина при температуре, близкой к температуре кипения реакционной смеси.
Продукт, представляющий из себя, близкую к эквимолекулярной, смесь хлористого аммония и глицина, выпадает в виде кристаллического осадка при охлаждении реакционной смеси.
Согласно способу-прототипу в 1000 л 90% -ного водного метанола растворяют 70 кг гексаметилентетрамина, нагревают смесь до 40-70 о С, и одновременно добавляют к ней раствор 189 кг МХУК в 80 л 90% -ного метанола и 68 кг газообразного аммиака. После охлаждения реакционной смеси удаляют кристаллический глицин в смеси с NH4Cl. Выход глицина в расчете на затраченную МХУК составляет 144 кг или 95% . Чистота глицина после очистки - 99,5% .
Недостатками прототипа являются:
недостаточно высокий выход глицина;
недостаточно высокая производительность процесса - 36 кг/час с 1 м 3 реакционного пространства;
низкие технико-экономические показатели процесса (расходные показатели процесса в расчете на 1 т полученного после синтеза глицина составляют: метанол 100% -ный - 5,7 т, гексаметилентетрамин 0,5 т, вода 0,64 т, МХУК 1,35 т, NH3 - 0,5 т).
Глицин — является одной из заменимых аминокислот, входящих в состав белков и других биологически активных веществ в организме человека.
Глицин был назван так за сладкий вкус (от греческого glykos — сладкий).
Глицин (гликокол, аминоуксусная кислота, аминоэтановая кислота).
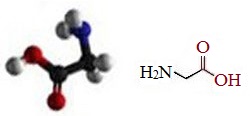
Глицин (Гли, Gly, G) имеет строение NH2-CH2-COOH.
Глицин оптически неактивен, так как в структуре отсутствует асимметрический атом углерода.
Глицин впервые выделен Braconnot в 1820 г. из кислотного гидролизата желатина.
Суточная потребность в глицине составляет 3 грамма.
Физические свойства
Глицин – бесцветные кристаллы сладкого вкуса с температурой плавления 232-236°С (с разл.), хорошо растворяется в воде, нерастворим в спирте и эфире, ацетоне.
Химические свойства
Глицин обладает общими и специфическими свойствами, присущими аминокислотам, обусловленными наличием в их структуре амино- и карбоксильной функциональных групп: образование внутренних солей в водных растворах, образование солей с активными металлами, оксидами, гидроксидами металлов, хлороводородной кислотой, ацилирование, алкилирование, дезаминирование по аминогруппе, образование галагенангидридов, сложных эфиров, декарбоксилирование по карбоксильной группе.
Основным источником глицина в организме служит заменимая аминокислота серин. Реакция превращения серина в глицин легко обратима.
Биологическая роль
Глицин необходим не только для биосинтеза белка и глюкозы (при ее недостатке в клетках), но и гема, нуклеотидов, креатина, глутатиона, сложных липидов и других важных соединений.
Важна роль производного глицина – трипептида глутатиона.
Он является антиоксидантом, препятствует пероксидному
окислению липидов клеточных мембран и предотвращает их повреждение.
Глицин участвует в синтезе компонентов клеточных мембран.
Глицин относится к тормозным нейромедиаторам. Этот эффект глицина сильнее выражен на уровне спинного мозга.
Успокаивающий эффект глицина основан на усилении процессов активного внутреннего торможения, а не на подавлении физиологической активности.
Глицин защищает клетку от стресса. Успокаивающий эффект при этом проявляется в уменьшении раздражительности, агрессивности, конфликтности.
Глицин увеличивает электрическую активность одновременно в лобных и затылочных отделах головного мозга, повышает внимание, увеличивает скорость счетновычислительных и психофизиологических реакций.
Применение глицина по схеме в течение 1,5 – 2 месяцев приводит к снижению и стабилизации артериального давления, исчезновению головной боли, улучшению памяти, нормализации сна.
Применение глицина позволяет предупредить вызванную гентамицином почечную недостаточность, оказывает положительное влияние на структурные изменения в почках, предупреждает развитие окислительного стресса и снижает активность антиоксидантных ферментов.
Глицин уменьшает токсическое действие алкоголя. Это связано и с тем, что образующийся в печени ацетальдегид (токсичный продукт окисления этанола) соединяется с глицином, превращаясь в ацетилглицин – полезное соединение, используемое организмом для синтеза белков, гормонов, ферментов.
Глицин уменьшает случаи возникновения токсикозов при беременности, угрозу выкидышей, несвоевременное отхождение вод, асфиксию плода.
У женщин на фоне приема глицина реже рождались дети с врожденной гипотрофией, не было новорожденных с родовыми травмами и поражениями тканевых структур головного мозга, множественными врожденными пороками развития, отсутствовала смертность новорожденных.
Природные источники
Говядина, желатин, рыба, печень трески, яйцо куриное, творог, арахис.
Области применения
Очень часто глицин применяют для лечения детских заболеваний. Применение глицина дает положительный эффект при лечении вегето-сосудистой дистонии, у детей с психосоматическими и невротическими нарушениями, при острой ишемии головного мозга, при эпилепсии.
Применение глицина у детей повышает концентрацию внимания, снижает уровень личностной тревожности.
Применяется глицин также для профилактики ранней алкоголизации и накотизации подростков.
Глицин применяется при астенических состояниях, для повышения умственной работоспособности (улучшает умственные процессы, способность воспринимать и запоминать информацию), при психоэмоциональном напряжении, повышенной раздражительности, при депрессивных состояниях, для нормализации сна.
Как средство, уменьшающее тягу к алкоголю, при разных функциональных и органических заболеваниях нервной системы (нарушения мозгового кровообращения, инфекционные заболевания нервной системы, последствия перенесенных черепно-мозговых травм).
Применяется препарат под язык, т.к. в области ядра подъязычного нерва плотность глициновых рецепторов наибольшая, а следовательно, чувствительность в этой области к воздействию глицина максимальна.
Физиологической активностью обладает также производное глицина - Бетаин (триметилглицин).
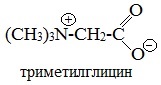
Бетаины распространены в животном и растительном мире. Они содержатся в свекле, представителях семейства губоцветных.
Бетаин гликокола и его соли широко применяется в медицине и сельском хозяйстве.
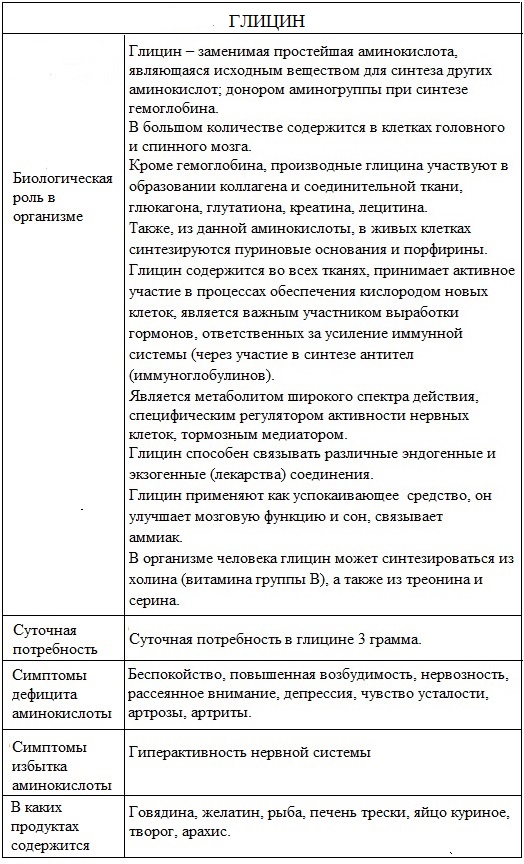
Триметилглицин участвует в процессах обмена живых организмов и наряду с холином используется для профилактики заболеваний печени, почек.

Рубрики: Аминокислоты

Обзор
Молекула глицина на фоне шелка, в состав которого глицин входит в больших количествах
Автор
Редакторы
Эта статья о глицине — самой маленькой аминокислоте в природе, чья роль, тем не менее, огромна. Вы узнаете, в состав каких белков и пептидов входит глицин, как синтезируется в организме и предшественником каких веществ является.
Введение в курс дела
Аминокислоты — это одни из самых важных веществ в живой природе. Будучи довольно небольшими молекулами, они играют огромную роль в живых организмах. Подобно жемчужинам в ожерелье, они слагают большие молекулы — белки, из которых построены все живые существа — от мала до велика. Функция аминокислот не исчерпывается только тем, что они становятся строительным материалом для белков. Аминокислоты могут специализироваться на других задачах. Общая формула аминокислот приведена на рисунке 1.

Рисунок 1. Структура аминокислот. а — Общая формула α-аминоксилот. Компонентами этих соединений являются углеродный скелет, карбоксильная и аминогруппы, а также боковая группа, определяющая индивидуальные свойства разных аминокислот. Важно, что почти во всех природных аминокислотах аминогруппа расположена слева от углеродного скелета (L-изомеры). α-L-аминокислоты — основа природных белков. б — Формула глицина. Боковая группа в этой молекуле представлена протоном. Таким образом, глицин — самая простая аминокислота из всех возможных.
В первой части статьи мы рассмотрим некоторые белки и пептиды, для которых глицин имеет большое значение, а также разберем, откуда глицин в организме вообще берется и в чем, кроме белков, используется. Мы не будем претендовать на абсолютную полноту картины функций глицина, но остановимся на наиболее важных моментах.
Глицин в белках и пептидах
Коллаген — сложно устроенный белок, являющийся одним из основных компонентов соединительной ткани. Он присутствует в сухожилиях, коже, кровеносных сосудах, роговице, костях и хрящах, а также в чешуе рыб и шерсти млекопитающих, выполняя структурную роль и составляя до 30% массы позвоночных животных [2]. Таким образом, это один из самых распространенных животных белков. Существует несколько типов коллагена.
Коллаген обеспечивает прочность соединительных тканей, а потому и сам обладает свойством устойчивости к растяжению, и это качество определяется его структурой (рис. 2) [2].

Рисунок 2. Структура коллагена. Три обвивающие друг друга нити образуют суперспираль, как пряди волос — косу. Суперспирали, располагаясь друг относительно друга строго определенным образом, формируют фибриллу. Такое устройство белка способствует его механической устойчивости: кости ломаться не должны.
[2], рисунок с изменениями
Из этой формулы видно, что глицин составляет треть аминокислот коллагена! Природа не стала бы играть такими цифрами просто забавы ради. Присутствие глицина — одна из предпосылок к формированию прочных фибрилл и волокон коллагена, необходимых для многих тканей. Три нити, формирующие коллагеновую суперспираль, переплетаются настолько плотно, что между ними нет свободного пространства. И только лишь один глицин со своей крохотной боковой группой способен интегрироваться в эту систему, как кусочек мозаики. Замена глицина на какую-то другую аминокислоту, имеющую более объемную боковую группу (например, серин), может привести к серьезным патологиям, например, к синдрому Элерса—Данлоса (это гетерогенная группа наследственных нарушений соединительной ткани) [4], [5].
Глицином богат еще один структурный белок — фиброин — основной компонент паутины и шелка. Почти половина аминокислотных остатков фиброина — глицин! Как и в случае с коллагеном, там он входит в состав повторяющейся последовательности.
Белкам близка еще одна группа биологических веществ — пептиды. Они тоже сложены из аминокислот, только меньше белков по размерам (но граница между белками и пептидами размыта).

Рисунок 3. Pyrrhocoris apterus. Это известный многим клоп-солдатик — яркий (во всех смыслах этого слова) представитель отряда полужесткокрылые, или клопы (Hemiptera). При внедрении бактерий в его гемолимфе обнаруживаются несколько антимикробных пептидов, включая богатый глицином гемиптерицин [8]. Не только он, но и многие другие животные борются с патогенами с помощью глицин-богатых пептидов.
Посмотрим на так называемые антимикробные пептиды. Это, как правило, положительно заряженные (катионные) молекулы, которые участвуют в иммунном ответе, воздействуя на мембраны бактерий или других патогенов [6]. С помощью этих относительно небольших молекул человек и другие животные, включая разнообразных букашек, борются с болезнетворными организмами, которым удалось пробраться во внутреннюю среду. До сих пор не разработано единой классификации антимикробных пептидов, но известно, что те или иные из них характеризуются определенными структурными особенностями. В частности, в них может в большом количестве присутствовать какая-то аминокислота, в том числе и глицин.
К глицин-богатым антимикробным пептидам относят акалолептины из гемолимфы жука-дровосека Acalolepta luxuriosa, акантоскуррин из гемоцитов паука Acanthoscurria gomesiana, аттацины из насекомых отрядов чешуекрылые и двукрылые, гемиптерицин из известного многим клопа-солдатика Pyrrhocoris apterus (рис. 3) и другие (гименоптецин, гловерины, колеоптерицины, риноцерозин, холотрицин-2 и −3). Глицин-богатые домены имеют пептиды гиастатин и крустины [7], [8].
Конечно, глицин присутствует и во многих других белках и пептидах. Это делает его одной из самых распространенных природных аминокислот.
Откуда берется глицин в организме?
Конечно, эта чудесная аминокислота попадает к нам с пищей в составе белков. Тем не менее основной источник глицина — процессы синтеза, проходящие в нашем теле, что позволяет отнести глицин к заменимым аминокислотам.

Рисунок 4. Синтез глицина из 3-фосфоглицерата через серин. Цифрами обозначены ферменты: 1 — фосфоглицератдегидрогеназа; 2 — фосфосеринаминотрансфераза; 3 — фосфосеринфосфатаза; 4 — серин-гидроксиметилтрансфераза.
CO2 + NH4 + + N 5 ,N 10 -метилентетрагидрофолат + NADH + H + = глицин + тетрагидрофолат + NAD +
Voilà! (Извините за мой французский.) Образовавшийся глицин поступает на службу организму.
Глицин — предшественник гема
Почему кровь красная? Потому что в ней есть гемоглобин — красный белок, имеющий в своем составе гем. Это железосодержащая порфириновая система, на которую и садится кислород, от легких с кровью поступающий к разным тканям. Глицин является одним из предшественников гема у животных. Реакция с участием глицина представлена на рисунке 5.

Глицин как участник других жизненно важных реакций


Рисунок 7. Одним из предшественников креатина является глицин
Разнообразие комбинаций азотистых оснований в молекуле ДНК является основой биологического разнообразия на планете.
Кроме этого, глицин участвует в синтезе креатина (рис. 7) — вещества-аккумулятора энергии в мышцах и нервных клетках, то есть в тех местах организма, где требуется поддерживать высокий уровень энергии.
Читайте также:

