Реферат химические реакции вокруг нас
Обновлено: 05.07.2024
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке "Файлы работы" в формате PDF
Поверьте без химии жизни нет ,
Без химии стал бы тусклым весь свет.
Мы с химией ездим , живём и летаем ,
В разных точках Земли обитаем,
Чистим ,стираем , пятна выводим.
Химией лечимся, клеим и шьём
С химией мы бок о бок живём!
Химия - удивительная наука. С одной стороны, эта наука весьма абстрактная: она изучает мельчайшие частицы, которые не увидишь в самый сильный микроскоп, рассматривает громоздкие формулы и сложные законы. С другой стороны, она очень конкретна и имеет дело с бесчисленными полезными и вредными веществами. Вещество – это то, из чего состоит все вокруг нас и внутри нас.
Поэтому представить нынешний мир без химии невозможно. Это и наше жилье, и одежда, которую мы носим, и транспорт, на котором мы ездим, и даже наша еда стала продуктом химической промышленности.
Поэтому химия нужна всем: повару, шоферу, садоводу, строителю.
Чтобы устроить дома настоящую научную лабораторию совершенно не обязательно приобретать дорогостоящее оборудование и реактивы, достаточно будет подручного материала.
Потому что даже такое привычное приготовление пищи - это химические процессы и наша кухня напоминает химическую лабораторию. Только вместо колб и пробирок на кухне используются кастрюли и сковородки, стаканы и тарелки.
А наша ванна царит изобилием химических веществ, без которых трудно уже представить уборку.
Актуальность:
Знания по химии мы не очень часто используем в повседневной жизни, но тем не менее, этот предмет может стать источником знаний о процессах в окружающем мире, так как только при изучении химии мы знакомимся с составом веществ на нашей Земле. Благодаря этому мы узнаем, каким образом эти вещества взаимодействуют и влияют на процессы жизнедеятельности организма, да и в целом на саму жизнь человека, что полезно нам и в каких количествах и, наконец, что вредно и до какой степени.
Гипотеза:
Капуста меняет цвет, так как ее сок содержит растительный пигмент;
При взаимодействии соды и уксуса происходит выделение углекислого газа;
Раствор уксусной кислоты растворит яичную скорлупу.
Цель:
Используя химические эксперименты, показать, что из повседневных веществ можно получить химические процессы, иногда даже не безопасные для человека.
Задачи:
Изучить литературу по теме исследования.
Провести химические эксперименты.
Научно обосновать полученные результаты.
Методы исследования:
В работе мы использовали как общенаучные методы исследования – это анализ, синтез и наблюдения, так и специальные – это химический эксперимент.
Проверим это экспериментально:
Капусту мелко порезали и залили ее кипятком.
Через полчаса, когда вода стала насыщенного темно-синего цвета, отделили капусту от жидкости с помощью дуршлага
Полученный раствор разлили по стаканчикам и стали добавлять в него различные вещества, меняющие среду.
При добавлении соды, раствор становится голубым.
При добавлении уксуса раствор окрашивается в ярко розовый цвет.
При добавлении нашатырного спирта раствор становится зеленым.
Вывод: Сок краснокочанной капусты при смешивании с различными веществами изменяет свой цвет от красного (в сильной кислоте), к розовому, фиолетовому (это его естественный цвет в нейтральной среде), синему, и, наконец, зеленому (в сильной щелочи). Это связано с тем, что сок краснокочанной капусты содержит рH чувствительный растительный пигмент антоцианин.
Эксперимент 2: Безопасное извержение вулкана дома.
Охос-дель-Саладос – самый большой действующий вулкан в мире. Но, чтобы увидеть извержение вулкана, необязательно уезжать из дома. Создадим свой собственный вулкан дома и посмотрим на его извержение.
Создадим вулкан из подручного материала (картон, пластилин).
Готовим лаву вулкана. Засыпаем в вулкан соду и добавляем не большое количество растворенной в воде красную краску.
Аккуратно заливаем внутрь вулкана уксус. И наблюдаем извержение вулкана.
Вывод: При взаимодействии соды и уксуса происходит химическая реакция нейтрализации. В процессе их взаимодействия происходит обильное выделение углекислого газа, который вырывается из раствора, образуя пену.
Эксперимент 3: Яйцо без скорлупы.
Очистить вареное яйцо от скорлупы не составит труда, а вот можно ли снять скорлупу с сырого яйца? Проверим это экспериментально.
Куриное яйцо состоит на 12% из скорлупы, на 56% - из белка и на 32% - из желтка. Скорлупа защищает продукт от попадания вредных микроорганизмов. В состав скорлупы куриного яйца входит кальций, магний и другие органические элементы.
Очистим сырое яйцо от скорлупы с помощью химической реакции:
Положим сырое яйцо в банку.
Полностью зальем его уксусом.
Наблюдаем реакцию выделения газа, маленькие пузырьки окутали все яйцо.
Оставить яйцо в уксусе на 24 часа.
Вылить уксус из банки а яйцо промыть водой. И оценить результат.
Вывод: Кальций придаёт скорлупе прочность. При попадании яйца в уксус, уксус вступает в активную реакцию с кальцием, который в изобилии содержится в скорлупе, и растворяет его. В результате яйцо становится мягким и остается в оболочке из тонкой плёночки, которая была под скорлупой.
Я понял, что в домашних условиях можно устроить научную лабораторию и проводить эксперименты с самыми обычными пищевыми продуктами. Можно увидеть, как они меняют свои свойства под воздействием химических веществ или сохраняют их.
Проделывая опыты, узнал, что:
Из сока краснокочанной капусты можно сделать лакмусовые бумажки. Для этого нужно пропитать фильтровальную бумагу капустным соком и дать ей высохнуть. После этого разрезать на тонкие полоски.
Нужно хорошо чистить зубы, так как эмаль наших зубов похожа на скорлупу яйца по составу, а бактерии, которые остаются на зубах после еды, выделяют вещество, похожее на уксус. И если плохо чистить зубы и не счищать все бактерии, то их ожидает та же участь, что и скорлупу яйца.
Проделав эту работу, я убедился, что такие серьезные науки, как химия и физика, очень близки к нашей обычной, повседневной жизни. И это очень интересно.
Белько Е. Весёлые научные опыты. Увлекательные эксперименты в домашних условиях. – СПб: Питер, 2015. –64с.
Белько Е. Весёлые научные опыты. Увлекательные эксперименты с водой, воздухом и химическими веществами. – СПб: Питер, 2015. – 64 с.
Белько Е. Весёлые научные опыты. 30 увлекательных экспериментов в домашних условиях. – СПб: Питер, 2015.–64с.
химические реакции Мы можем найти их в повседневной жизни в целом. Это ответ, который химик мог бы дать вам без ошибок, чтобы преувеличивать.
И это то, что кто-то стремится в этом вопросе будет пытаться увидеть вещи с молекулярной или атомной точки зрения, будет пытаться увидеть реакции повсюду, и молекулы постоянно превращаются.

Люди, разбирающиеся в химии, не могут не видеть вещи с этой точки зрения, точно так же, как физик мог видеть вещи с ядерной точки зрения или биолог с клеточной точки зрения..
Для обоснования комментария ниже я привожу 30 примеров химии, присутствующей в повседневной жизни..
Химические реакции, которые остаются незамеченными дома, на кухне, в саду, на улице или даже внутри нашего тела. Я надеюсь, что это поможет осветить обычную и рутинную химию в повседневной жизни..
30 химических реакций, которые вы видите каждый день в своей жизни
Химия на кухне
1- сольватационные реакции: когда соль растворяется в воде, ионные связи разрушаются, что приводит к сольватации катионов и анионов.
Технически готовят раствор хлорида натрия в воде..
2- Фазовые изменения: При кипячении воды во время приготовления или приготовления кофе или чая происходит фазовое изменение между жидкой водой и газированной водой.
3- реакции горения: Газовые плиты используют пропан для производства пламени.
4- ХлорХлор, используемый в качестве моющего средства, на самом деле представляет собой хлорит натрия, который является восстановителем. Пятна от одежды называются хромофорами и имеют ненасыщенность. Хлор атакует эту ненасыщенность, удаляя цвет пятен. Технически это не удаляет пятно, но делает его невидимым.
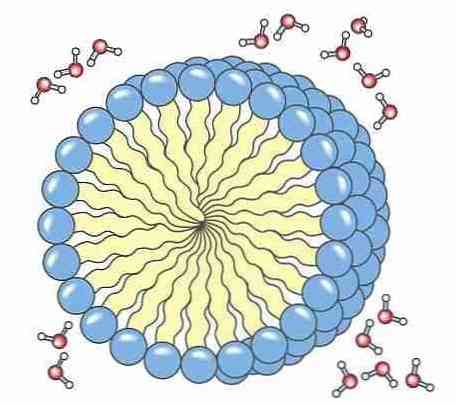
5- мылоМыла и моющие средства имеют полярную часть, обычно карбоновую кислоту, присоединенную к неполярной алифатической цепи, которая дает ей способность образовывать мицеллы. Эти мицеллы обладают способностью окружать грязь, поэтому ее можно удалить с одежды, посуды и нашего тела..
6- Пищевая сода: это слабое основание, которое при взаимодействии с кислотой, такой как уксус или вода (которая является слегка кислой), выделяет углекислый газ.
Это соединение является активным ингредиентом многих антацидов (C., 2015).
7- Среднесрочный: кухня - это химическое изменение, которое меняет пищу, делая ее вкуснее, убивает опасные микроорганизмы и делает их более усвояемыми.
Жар кулинарии может денатурировать белки, стимулировать химические реакции между ингредиентами, карамелизовать сахар и т. Д. (Helmenstine A.M., 10 примеров химических реакций в повседневной жизни, 2017).
9- Плачь о луке: лук содержит аминокислотные молекулы сульфоксидов. При разрезании луковых клеточных стенок происходит разрушение, выделяя эти сульфоксиды вместе с ферментами, которые разлагают его до сульфеновых кислот, сероорганического соединения формулы R-SOH, которое раздражает глаза (Reactions, 2016).
Химия в доме
10- АккумуляторыОни используют электродохимические или окислительно-восстановительные реакции для преобразования химической энергии в электрическую. Спонтанные окислительно-восстановительные реакции происходят в гальванических элементах, тогда как не спонтанные химические реакции происходят в электролитических ячейках (Helmenstine, 2017).
11- ЖК-экраны: ЖК-телевизоры содержат спиральные кристаллические молекулы, которые имеют свойство ориентироваться в соответствии с электрическим сигналом и путем изменения тона или цвета, обеспечиваемого светодиодной лампой. Каждая кристаллическая молекула представляет собой пиксель на телевизоре, и чем больше молекул, тем выше разрешение.
12- Старые книги, которые хорошо пахнут: разложение целлюлозы из бумаги книг, придает листьям желтоватый цвет и запах ванили. Если у вас есть старые книги, которые хорошо пахнут в вашей библиотеке, это происходит из-за молекул лигнина или ванилина в нем.
13- Наркотики и наркотикиНекоторые лекарственные средства представляют собой молекулы, которые частично блокируют гормональную активность, вызываемую определенным раздражителем (например, лекарственные средства для снятия напряжения или противоэпилектические средства), в то время как другие являются ферментативными ингибиторами, такими как, например, анальгетики..

14- ШампуньКак шампуни и мыло, шампуни удаляют жир с кожи головы, образуя мицеллы. Ингредиентом, который заботится об этом, обычно являются сульфаты, такие как додецилсульфат или лауриловый эфир сульфата натрия или аммония.
15- Дезодоранты и антиперспиранты: плохой запах подмышек, ног и дыхания вырабатывается бактериями, которые питаются белками и жирами в поте, который выделяет апокринные железы.
У дезодорантов есть химическое соединение, названное триклозаном, который является сильным антибактериальным и фунгицидным средством. С другой стороны, антиперспиранты содержат соли алюминия, которые проникают в поры и предотвращают потоотделение..
16- Косметика и макияжЭто химические вещества и пигменты, которые прилипают к коже. Обычно это неполярные соединения, такие как воски и масла..
Химия в саду
17- Фотосинтез: это процесс, при котором зеленые растения производят свою еду. Это происходит в присутствии солнечного света и другого сырья, а именно углекислого газа и воды. Пигмент хлорофилла собирает световую энергию солнечного света, которая превращается в глюкозу (Crystal, 2017).
В этом случае железо соединяется с кислородом в присутствии воды, что приводит к образованию оксидов железа (химические реакции в повседневной жизни, 2016 г.).
19- Органическое разложениеРазложение органических продуктов питания или даже живых существ - это реакции окисления, вызываемые бактериями, которые разлагают биохимические макромолекулы в простых молекулах, таких как нитриты, нитраты, СО2 и вода (Helmenstine, Примеры химических изменений, 2017).

20- Удобрения: калий, нитраты, фосфаты и сульфаты используются в почвах для обеспечения растений питательными веществами и могут расти.
21- ПестицидыЭто химические вещества, используемые для окуривания сельскохозяйственных культур или садов. Обычно это нейротоксины, которые поражают бактерии или насекомых, которые потребляют зерновые культуры..
Химия на улице
22- Сжигание бензина: автомобили используют бензин в качестве топлива за счет контролируемых взрывов, которые приводят в движение поршни двигателей.
23- Дым машин: вырабатывает свободные радикалы, которые являются очень реактивными соединениями и атакуют кожу или волосы, делая их сухими и ломкими, не говоря уже о том, что они канцерогенные.
24- кислотный дождь: избыток серы и оксидов азота в атмосфере, производимых заводами и автомобилями, растворяется в воде облаков с образованием серной, серной и азотной кислоты, которая выпадает в осадок в виде кислотных дождей.

25- Конструкции: цемент и другие материалы, используемые при строительстве домов, такие как картины, штукатурка и многие другие, являются продуктами химии. В частности, цемент сделан из молекул гидроксида кальция, также называемых негашеной известью.
Химия в вашем теле
26- Пищеварение: пищеварение основано на химических реакциях между пищевыми продуктами и кислотами и ферментами, которые расщепляют молекулы на питательные вещества, которые организм может усваивать и использовать.
27- Аэробное дыхание: основным процессом, который производит энергию в организме, является аэробный гликолиз. Здесь дыхание помогает расщеплять глюкозу (источник энергии) в воде, углекислый газ и энергию в форме АТФ. С6H12О6 + 6O2 → 6CO2 + 6H2O + Энергия (36 АТП)
29- Мускульное движение: напряжение или расслабление мышц происходит из-за конформационных изменений белков скелетных мышц. Эти изменения происходят благодаря фосфокреатину, который при потере фосфата высвобождает энергию для процесса.

30- Мысль: это сложный биохимический процесс, в котором разность ионного потенциала создает электрические импульсы нейронов (Али, 2013).

Все мы в детстве читали немало сказок о добрых феях и волшебниках, но в жизни нет ни тех, ни других. А вот чудеса – они и в самом деле бывают, хотя совершают их вовсе не джинны, а люди, вооружённые знаниями. Наука вот истинная волшебница. Химия – наука старая и вместе с тем молодая. Старая потому, что ещё в Древнем Египте люди умели осуществлять разные превращения веществ. Ведь уже тогда они научились добывать огонь, лепить и обжигать посуду из глины, окрашивать ткани, печь хлеб… А ведь всё это – химические явления. Химия – наука молодая, потому что, в подлинном смысле наукой, со своими законами, она стала всего два с лишним века назад, правда, за эти два столетия она достигла значительных успехов, чем в предыдущие тысячелетия. С помощью химии человек раскрыл немало природных тайн. Чудесные превращения я предлагаю в своём проекте, расскажу о удивительном и чудесном, о химии.
Актуальность: Химия – удивительная наука, полная разнообразных чудес. Она интересна как сама наша жизнь, ведь всё что происходит с нами можно рассматривать с точки зрения химии. Мы познакомимся с характеристикой веществ, окружающих нас в быту, на кухне, в промышленности. Эти вещества имеют интересную историю и необычные свойства. Мой проект не только существенно расширяет кругозор, но и раскрывает материальные основы окружающего мира, даёт химическую картину природы.
Задачи исследования:
Собрать материал о химических явлениях в природе и в жизни.
Исследовать, как и в каких целях используются продукты химической промышленности.
Составить текст исследовательской работы.
Гипотеза исследования: предполагается, что в условиях высокого уровня развития цивилизации, человек не может обходиться без химии.
Объект исследования: связь человека с химическими продуктами и явлениями.
Предмет исследования: химические опыты.
Этапы работы над проектом:
Реферат на тему:
Химия на кухне и в быту. Питьевая сода.
Оформление выполненных исследований.
Итак, мы начинаем путешествие по безбрежным океанам глубоких познаний в химии, готовы постичь тайну всех земных и неземных превращений, готовы с головой окунуться в бушующее море интересных фактов нашей повседневной жизни!
Глава 1. Знакомство с химией
Из истории химии
Химия существует с глубокой древности, но настоящей наукой она стала совсем недавно – не более 200 лет назад. Теоретические основы химии заложили древнегреческие учёные Анаксагор и Демокрит. Создателям современной системы представлений о строении вещества является русский химик Дмитрий Менделеев. В 1869 году предложил таблицу, где все элементы были упорядочены. Так появилась Периодическая таблица Менделеева.
Менделеев не только записал известные элементы, но и назвал ещё не открытые химические элементы, а также предсказал, как они будут выглядеть и соединяться с другими элементами. Оказывается, что химические элементы живут по строгим правилам.
Известный химик Антуан Лорен Лавуазье сделал в своё время открытие, что вода (Н2О) состоит из двух химических элементов, двух газов: кислорода (О) и водорода (Н).
Он провёл химический опыт с двумя газами и на глазах удивлённых людей получил воду (Н2О)! Оба невидимых газа он поместил в сосуд, нагрел его на сильном огне. Сосуд вскоре помутнел и все увидели на его стенках капельки воды. Свершилось чудо химии!

Н (водород) + О (кислород) Н2О (ВОДА)
1.2. Что такое химия?
Работа началась с посещения школьной библиотеки. Заведующая библиотекой Кузьмина С.А. познакомила меня с новой наукой – химией. Рассказала мне о литературе, новинках по прикладной химии. Здесь я нашла много информации для своего исследования.
Далее я посетила школьный кабинет химии. У учителя химии узнала. Что такое химия? Химия – одна из наук о природе, об изменениях, происходящих в ней. Она изучает из каких веществ состоит тот или иной предмет. Химия – наука удивительная! Как только человек появляется на белый свет, он попадает в мир химических веществ.
Первый вздох и вот уже в лёгких смесь газов, первый глоток материнского молока и самый главный шедевр биохимической эволюции – белок начинает работать в организме малыша.
1.3. Химические явления в природе и в жизни человека
Окружающий нас мир состоит из химических элементов: книги, одежда, мебель, краски. О некоторых химических элементах вы наверно слышали: железо, золото, серебро, йод, водород, кислород, кальций и другие.
На нашей планете больше всего кислорода (О). Одних элементов в природе очень много, других совсем мало. Больше всего на свете водорода (Н) и гелия (Не). Из этих химических элементов почти целиком состоит Солнце, далёкие звёзды, кометы…
Вот почему трава зелёная? Да потому, что в каждой травинке есть химическое соединение – хлорофилл, благодаря которому растения дышат и растут.
Почему соль солёная? Да потому, что в ней есть натрий (Na) и хлор (Cl), который попадая на слюну образуют раствор с особым привкусом.
Химический элемент железо (Fе) есть не только в гвозде или машине, но и в воде, в земле, в деревьях, но и в организме человека. В крови человека есть частички железа (Fе), но они так малы, что увидеть их можно при помощи микроскопа.
А если хочется скорее вырасти – потреблять нужно химический элемент кальций (Са). Его много в молоке и в молочных продуктах. Даже настроение человека, его здоровье, во многом зависят от присутствия некоторых химических элементов в организме. Химический элемент магний (Mg) влияет на работу сердца. Магний (Mg) содержится в абрикосах и персиках.
Химическое явление в природе – это процесс, в результате которого из одних веществ образуются другие. При химических реакциях исходные вещества превращаются в другие вещества, обладающие другими свойствами.
Основные химические реакции:
1. Выделение теплоты.
2. Изменение окраски.
3. Появление запаха.
4. Образование осадка.
5. Выделение газа.
Свойства химических явлений:
1. Горение – химическая реакция, при которой происходит окисление веществ, выделяющих тепло и свет. Процесс горения может происходить только при наличии кислорода (О2), нагревание до температуры воспламенения.
2. Окисление – это взаимодействие веществ с кислородом (О2). Окисление происходит медленно, без выделения света, иногда с выделением тепла.

Глава 2. Химия вокруг на нас
2.1. Химия и вещества
Вокруг нас громадное количество полезных и вредных веществ! Например, в природе есть природные вещества, то есть те, которые были созданы без участия человека. Это – вода, кислород, углекислый газ, камень, древесина и другие.
Есть вещества, созданные человеком. Они называются искусственными веществами. Это – пластмасса, резина, стекло и другие.
Хотя я ещё не изучаю химию в школе, мне уже известен такое распространённое вещество в природе, как вода (H2O). Это вещество удивительным образом может иметь три агрегатных состояния – жидкое, твёрдое, газообразное.
Именно на кухне я проследила все её состояния.
Если вскипятить воду, то она превращается в горячий пар – газ. Если заморозить воду в морозильной камере, то вода превращается в лёд. При этом лёд занимает большой объём, чем вода. Поэтому, чтобы не лопнула бутылка в морозильной камере, мама наливает воду не до конца, оставляя лишнее место в бутылке.
Разобраться с бесчисленными полезными и вредными веществами, узнать их строение, свойства, роль в природе – одна из задач химии. Она нужна всем людям – строителю, фермеру, врачу, домохозяйке, повару и врачу.
2.2 Химия на кухне и в быту. Питьевая сода
Так как я узнала, что химия – это наука о веществе, то разумно было бы предположить, что на кухне много разных веществ.
Интересно, чем же кухня напоминает научную лабораторию?
Раскроем кухонный шкаф. Уксус, пищевая сода, растительное масло, сахар, мука, соль, молоко, крахмал.
Ничего химического, скажите вы, здесь нет. Обычные продукты питания.
Но не тут – было! Это настоящие химические вещества, с помощью которых на нашем столе появляются вкусные, питательные и полезные блюда. У этих веществ даже есть химические названия.
соль – это хлорид натрия;
пищевая сода – гидрокарбонат натрия;
уксус – уксусная кислота;
С П Л О Ш Н А Я Х И М И Я!
Остановлюсь я на пищевой соде. Химическая формула пищевой соды - NaHCO3.
- это белый порошок
- без цвета и запаха, вкус солоновато – мыльный
- хорошо растворима в воде
- при нагревании не горит и не меняет цвет.
Человечеству были известны полезные свойства пищевой соды ещё полторы – две тысячи лет назад. Первые сведения о пищевой соде появились ещё в древней цивилизации Египта. Именно в тех краях были распространены несколько озёр, содержащих природные источники соды. При пересыхании эти озёра отдавали соду в виде белого порошка, а люди её собирали. Использовалась она египтянами в качестве одного из компонентов при изготовлении средств мумификации. Формула пищевой соды тогда ещё известна не была.
В 1791 году французский химик–технолог Николя Леблан придумал способ производства пищевой соды.
Благодаря своим способностям хорошо растворяться в воде, а также вступать во взаимодействие с кислотами, образуя в результате реакции углекислый газ, сода находит применение:
- при выпечке различных изделий
- в медицине для приготовления антибиотиков
- в производстве стекла
- для косметологических целей.
Пищевая сода избавляет от неприятных запахов (например, в холодильнике, шкафчике для обуви или в ведре для мусора). Также сода содержится во всех чистящих средствах (например, Пемолюкс, Пемолюкс сода эффект). При помощи этих средств можно легко очистить эмалированную посуду, изделия из нержавеющей стали, ванны, умывальники, кафельную плитку, канализационные стоки. Хорошо решает вопрос с цветением воды в бассейнах, при помощи соды восстанавливает кислотно–щелочной баланс. Также сода может мгновенно погасить огонь, если возгорание произошло при готовке еды.
2.3. Опыты на кухне
Настало время провести ряд химических опытов на кухне.
Самое главное –
соблюдать правила техники безопасности.
Пищевая сода – это гидрокарбонат натрия NaHCO3.
Уксус – бесцветная жидкость с резко – кислым вкусом и ароматом. Он содержит уксусную кислоту.
При их смешивании происходит химическая реакция – выделяется углекислый газ и вода. Это видно из опыта – смесь пузырится и начинает увеличиваться в объёме. Поэтому получается так называемая лава вулкана.
Самое же главное при использовании соды - тесто сразу же надо выпекать, так как химическая реакция быстро проходит. Гасить соду можно и кисломолочными продуктами (например, кефиром) – если они входят в состав теста, то уксус добавлять необязательно.
Описание опыта см. в приложении
Пищевая сода и сок лимона смешанный с уксусом, вступая в реакцию, выделяют углекислый газ, который и надувает шарик.
Описание опыта см. в приложении
Жидкости разделяются слоями, т.к. имеют разную плотность – масло, как менее плотное будет сверху, краситель – снизу. Шипучая таблетка содержит лимонную кислоту и соду. Вещества таблетки, реагируют с водой и в результате химической реакции, выделяется углекислый газ, который подхватывая частицы красителя, стремится к верху. Далее газ благополучно покидает стакан, а частицы красителя возвращаются обратно вниз. И так далее.
Именно из–за этого постоянного круговорота жидкости получается интересная и очень красивая, эффектная лава.
Описание опыта см. в приложении
4.Опыт с молоком и красками
Молоко – это жидкость, в которой содержатся различные вещества, в том числе и жир. Моющее средство атакует жир в молоке и происходит химическая реакция между жиром и моющим средством Ферри.
Химическая реакция – это процесс смешивания разных веществ, в результате которого образуются новые вещества, при этом они становятся другого цвета, либо выделится газ, либо выделится энергия.
В моём случае выделилась энергия, которая двигает краски.
Описание опыта см. в приложении
Суть опыта в том, что масло всегда будет плавать на поверхности, а вот краска будет тонуть, она же тяжелее масла.
Описание опыта см. в приложении
В молоке содержится вода и другие вещества, такие как белок казеин. Когда я прогладила лист бумаги утюгом, то нагрела молоко, до температуры +100*С. После этого вода испарилась, а белок казеин поджарился и стал коричневый.
Описание опыта см. в приложении
Изучив литературу, проделав опыты, я убедилась в том, что многие процессы, происходящие на нашей кухне и в быту – это химические явления.
Значит, моя гипотеза подтвердилась – химия действительно важный помощник и друг человека, за нею будущее. Кухня – химическая лаборатория.
В процессе данного проекта, с поставленными целями и задачами я успешно справилась. Я узнала, что такое химия и химические вещества, провела химические опыты с различными продуктами. Тем самым доказала, что кухня – это целая химическая лаборатория.
Знакомство с яркими, эффективными химическими опытами имеет важное познавательное значение и оказывает большое эмоциональное воздействие на нас, во многом способствует формированию у нас интереса к химии – очень интересной и важной науки.
И в заключении, хотелось бы сказать: верьте в чудеса, знайте, что весь мир состоит из чудес и всё живое – уже великое чудо. В своём проекте мне удалось познать малую часть того, что может совершать наука, но жизнь непременно ещё много раз будет сталкивать нас с такими волшебными явлениями как химия.
ХИМИЯ УДИВИТЕЛЬНА, в этом я убедилась точно!
СПИСОК ЛИТЕРАТУРЫ
В.А. Крицман , В.В. Станцо Энциклопедический словарь юного химика., испр. М: Педагогика 1990г.
О.Ольгин Давайте похимичим! : Занимательные опыты по химии. М.: Дет. Лит. 2002 – 175 с.: ил.-(Знай и умей).
Вы можете изучить и скачать доклад-презентацию на тему Химия вокруг нас. Презентация на заданную тему содержит 25 слайдов. Для просмотра воспользуйтесь проигрывателем, если материал оказался полезным для Вас - поделитесь им с друзьями с помощью социальных кнопок и добавьте наш сайт презентаций в закладки!

























Введение Повсюду, куда бы ни обратил свой взор, нас окружают предметы и изделия, изготовленные из веществ и материалов, которые получены на химических заводах и фабриках. Кроме того, в повседневной жизни, сам того не подозревая, каждый человек осуществляет химические реакции.
Химия внутри нас Все живые организмы на Земле, в том числе и человек, находятся в тесном контакте с окружающей средой. Пищевые продукты и питьевая вода способствуют поступлению в организм практически всех химических элементов. Они повседневно вводятся в организм и выводятся из него. В народе бытует мнение о том, что в организме человека можно обнаружить практически все элементы периодической системы Д. И. Менделеева. Ученые же утверждают, что в живом организме не только присутствуют все химические элементы, но каждый из них выполняет какую-то биологическую функцию.
Металлы внутри организма: Экспериментально установлено, что в организме человека металлы составляют около 3 % (по массе). Это очень много. Если принять массу человека за 70 кг, то на долю металлов приходится 2,1 кг. По отдельным металлам масса распределяется следующим образом: кальций (1700 г), калий (250 г), натрий (70 г), магнии (42 г), железо (5 г), цинк (3 г).
Что для нас ЯД? Имеется большое число элементов, являющихся ядами для живого организма, например ртуть, таллий, свинец и др. Бывают элементы, которые в относительно больших количествах являются ядом, а в низких концентрациях оказывают полезное влияние на организм. Например: мышьяк является сильным ядом, нарушающим сердечно-сосудистую систему и поражающим печень и почки, но в небольших дозах он прописывается врачами для улучшения аппетита человека; хлорид натрия (поваренная соль) в десятикратном избытке в организме по сравнению с нормальным содержанием является ядом кислород, необходимый человеку для дыхания, в высокой концентрации и, особенно под давлением оказывает ядовитое действие…
Вода в организме человека Человек примерно на 65 % состоит из воды. С возрастом содержание воды в организме человека уменьшается. Эмбрион состоит из воды на 97 %, В теле новорожденного содержится 75 %, У взрослого человека — около 60 %.
Поваренная соль Солевое голодание может привести к гибели организма. Суточная потребность в поваренной соли взрослого человека составляет 10-15 г. В условиях жаркого климата потребность в соли взрастает до 25-30 г. Хлорид натрия нужен организму человека или животного не только для образования соляной кислоты в желудочном соке. Эта соль входит в тканевые жидкости и в состав крови. В последней ее концентрация равна 0,5—0,6 %.
Химия вокруг нас Ежедневно мы используем и сталкиваемся с продуктами химических реакций. Это – спички, стекло, цемент, бетон, пищевые добавки, косметика и др. Познакомимся с ними ближе…
Спички Долгое время люди придумывали легкий способ получения огня. И в 18 веке люди придумали спички. В их состав входит:
Бумага Изначально люди писали на папирусе, после на пергаменте. Так же, как и папирус, пергамент — прочный и долговечный материал. Считают, что и название бумаги (papiera) происходит от слова папирус. Как известно бумагу делают из древесины. Волокна целлюлозы в древесине связаны между собой лигнином. Для удаления лигнина и освобождения от него целлюлозы проводят варку древесины. Распространенным способом варки является сульфитный. Он был разработан в США в 1866 г., а первый завод по данной технологии был построен в Швеции в 1874 г.
Для обеспечения прочности соединения частиц пигментов с бумагой-основой требуются связующие. Часто их роль выполняют вещества, обеспечивающие проклейку бумаги. В качестве минеральных пигментов широко используют каолин — землистую массу, близкую по составу к глинам, но по сравнению с последними характеризующуюся пониженной пластичностью и повышенной белизной. Одним из старейших наполнителей является карбонат кальция (мел), потому такие бумаги и назвали мелованными. Для обеспечения прочности соединения частиц пигментов с бумагой-основой требуются связующие. Часто их роль выполняют вещества, обеспечивающие проклейку бумаги. В качестве минеральных пигментов широко используют каолин — землистую массу, близкую по составу к глинам, но по сравнению с последними характеризующуюся пониженной пластичностью и повышенной белизной. Одним из старейших наполнителей является карбонат кальция (мел), потому такие бумаги и назвали мелованными.
Карандаш Для изготовления рабочей части графитового карандаша готовят смесь графита и глины с добавкой небольшого количества гидрированного подсолнечного масла. В зависимости от соотношения графита и глины получают грифель различной мягкости — чем больше графита, тем более мягкий грифель. Смесь перемешивают в шаровой мельнице в присутствии воды в течение 100 ч. Приготовленную массу пропускают через фильтр-прессы и получают плиты. Их подсушивают, а затем из них выдавливают на шприц-прессе стержень, который режут на части определенной длины. Стержни в специальных приспособлениях высушивают и исправляют возникшую кривизну. Затем их обжигают при температуре 1000—1100°С в шахтных тиглях.
Состав карандашей В состав грифелей цветных карандашей входят каолин, тальк, стеарин (широкому кругу людей он известен как материал для изготовления свечей) и стеарат кальция (кальциевое мыло). Стеарин и стеарат кальция являются пластификаторами. В качестве связывающего материала используют карбоксиметилцеллюлозу. Это клей, используемый для наклейки обоев. Здесь его также предварительно заливают водой для набухания. Кроме того, в грифели вводят соответствующие красители, как правило, это органические вещества. Такую смесь перемешивают (вальцуют на специальных машинах) и получают в виде тонкой фольги. Ее измельчают и полученным порошком набивают пистолет, из которого и шприцуют смесь в виде стержней, которые режут на куски определенной длины и затем сушат. Для окраски поверхности цветных карандашей используют те же пигменты и лаки, которыми обычно окрашивают детские игрушки. Подготовку деревянной оснастки и ее обработку проводят так же, как и для графитовых карандашей.
Стекло История стекла уходит в глубокую древность. Известно, что в Египте и Месопотамии его умели делать уже 6000 лет назад. Вероятно, стекло начали изготавливать все же позже, чем первые керамические изделия, так как для его производства требовались более высокие температуры, чем для обжига глины. Если для простейших керамических изделий было достаточно только глины, то в состав стекла необходимо минимум три компонента.
Производство и состав В стекловарении используют только самые чистые разновидности кварцевого песка, в которых общее количество загрязнений не превышает 2—3 %. Особенно нежелательно присутствие железа, которое даже в ничтожных количествах (десятые доли %) окрашивает стекло в зеленоватый цвет. Если к песку добавить соду Na2CO3, то удается сварить стекло при более низкой температуре.(на 200—300°). Такой расплав будет иметь менее вязкий (пузырьки легче удаляются при варке, а изделия легче формуются). Но! Такое стекло растворимо в воде, а изделия из него подвергаются разрушению под влиянием атмосферных воздействий. Для придания стеклу нерастворимости в воде в него вводят третий компонент — известь, известняк, мел. Все они характеризуются одной и той же химической формулой — СаСО3.
Виды стекол Фотохромные стекла Хрусталь, хрустальное стекло Кварцевое стекло Пеностекло Стеклянная вата и волокно Посуда из стекла
Мыло и моющие средства Мыло было известно человеку до новой эры летоисчисления. Ученые не располагают информацией о начале приготовления мыла в арабских странах и Китае. Самое раннее письменное упоминание о мыле в европейских странах встречается у римского писателя и ученого Плиния Старшего(23—79гг.). Несмотря на то что в конце эпохи средневековья в разных странах существовала довольно развитая мыловаренная промышленность, химическая сущность процессов, конечно, была не ясна. Лишь на рубеже XVIII и XIX вв. была выяснена химическая природа жиров и внесена ясность в реакцию их омыления.
Жиры — сложные эфиры глицерина (глицериды) тяжелых одноосновных карбоновых кислот, преимущественно пальмитиновой СНз(СН2)14СООН, стеариновой СН3(СН2)16COOH и олеиновой СН3(СН2)7СН=СН(СН2)7СООН. Их формулу и реакцию гидролиза можно описать следующим образом: Жиры — сложные эфиры глицерина (глицериды) тяжелых одноосновных карбоновых кислот, преимущественно пальмитиновой СНз(СН2)14СООН, стеариновой СН3(СН2)16COOH и олеиновой СН3(СН2)7СН=СН(СН2)7СООН. Их формулу и реакцию гидролиза можно описать следующим образом: CH2OOCR1 R1COONa CH2OH | | CHOOCR2 + 3NaOH→R2COONa + СНОН | | CH2OOCR3 R3COONa CH2OH жир соли глицерин кислот
Процесс производства мыла состоит из химической и механической стадий. На первой стадии (варка мыла) получают водный раствор солей натрия (реже калия) жирных кислот или их заменителей (нафтеновых, смоляных). На второй стадии проводят механическую обработку этих солей — охлаждение, сушку, смешивание с различными добавками, отделку и упаковку Процесс производства мыла состоит из химической и механической стадий. На первой стадии (варка мыла) получают водный раствор солей натрия (реже калия) жирных кислот или их заменителей (нафтеновых, смоляных). На второй стадии проводят механическую обработку этих солей — охлаждение, сушку, смешивание с различными добавками, отделку и упаковку
Это интересно Кроме использования мыла в качестве моющего средства оно широко применяется при отделке тканей, в производстве косметических средств, для изготовления полировочных составов и водоэмульсионных красок. Имеется и не столь безобидное его применение: Алюминиевое мыло (алюминиевые соли смеси жирных и нафтеновых кислот) применяют в США для получения некоторых видов напалма — самовоспламеняющегося состава, используемого в огнеметах и зажигательных авиабомбах. Само слово напалм происходит от начальных слогов нафтеновой и пальмитиновой кислот. Состав напалма довольно простой — это бензин, загущенный алюминиевым мылом.
Зубная паста Зубные пасты — это многокомпонентные составы. Они подразделяются на гигиенические и лечебно-профилактические. Первые оказывают только очищающее и освежающее действие, а вторые, кроме того, служат для профилактики заболеваний и способствуют лечению зубов и полости рта.
Состав: Основные компоненты зубной пасты следующие: абразивные, связующие, загустители, пенообразующие. Абразивные вещества обеспечивают механическую очистку зуба от налетов и его полировку. В качестве абразивов чаще всего применяют химически осажденный мел СаСО3. Установлено, что компоненты зубной пасты способны влиять на минеральную составляющую зуба и, в частности, на эмаль. Поэтому в качестве абразивов стали применять фосфаты кальция: СаНРО4, Са3(РО4)2, Са2Р2О7, а также малорастворимый полимерный метафосфат натрия (NaРОз). Кроме того, в качестве абразивов в различных сортах паст применяют оксид и гидроксид алюминия, диоксид кремния, силикат циркония, а также некоторые органические полимерные вещества, например метилметакрилат натрия. На практике часто используют не одно абразивное вещество, а их смесь
Список использованной литературы Краткая химическая энциклопедия. – М.: Советская энциклопедия, 1961 – 1967. Т. I—V. Советский энциклопедический словарь. – М:: Сов. энциклопедия, 1983. Бутт Ю.М., Дудеров Г.Н., Матвеев М.А. Общая технология силикатов. – М.: Госстройиздат, 1962 Г.П. Технология спичечного производства. – М.–Л.: Гослесбумиздат, 1961 Козмал Ф. Производство бумаги в теории и на практике. – М.: Лесная промышленность, 1964 Кукушкин Ю.Н. Соединения высшего порядка. – Л.: Химия, 1991 Чалмерс Л. Химические средства в быту и промышленности – Л.: Химия, 1969 Энгельгардт Г., Гранич К., Риттер К. Проклейка бумаги. – М.: Лесная промышленность, 1975
Читайте также:
- Информационные барьеры в области распространения информации реферат
- 13 административно правовой институт государственной регистрации юридических лиц реферат
- Реферат по историографии октябрьской революции
- Мотивация и выбор профессии старшеклассниками реферат
- Опричнина в отечественной историографии реферат

