Реферат аммиак в организме
Обновлено: 20.05.2024
Аммиак — бесцветный газ с резким запахом. Синтезируют из азота и водорода. В природе образуется при разложении азотсодержащих органических соединений.
Львиная доля аммиака идет на изготовление азотной кислоты, красителей, растворителей, азотных удобрений, взрывчатых веществ и даже на получение обычной пищевой соды. При пайке металлов используют нашатырь для очистки паяльника и спаиваемых изделий. Также жидкий аммиак присутствует в холодильных камерах — как хладагент, используется для производства азотных удобрений, взрывчатых веществ и полимеров, азотной кислоты и других продуктов химической промышленности.
В быту жидкий аммиак можно увидеть в виде растворителей и очистителей (25-30%-ые растворы). С их помощью протирают технику, стекла, полы, кафель и избавляются от сложных пятен (лака, краски, жира, масел и др.). 10%-ый аммиачный раствор, или в просторечии нашатырь, присутствует во многих аптечках и помогает при обмороках и алкогольной интоксикации, так как раздражает слизистые оболочки организма. Взаимодействие с подобными средствами также требует повышенной осторожности.
Аммиак является одним из ключевых продуктов химической промышленности, поэтому каждому необходимо знать, вреден ли аммиак и насколько.
Как оказать первую помощь при отравлении аммиаком:
1. При появлении в помещении специфического запаха необходимо защитить дыхательные пути. Но простое закрывание лица марлевой повязкой не поможет — её необходимо прикладывать влажной. При отравлении аммиаком необходимо знать, чем нужно смачивать повязку — для этого подойдёт 2% раствор лимонной или уксусной кислоты.
2. Вывести пострадавшего на улицу подышать свежим воздухом.
3. Вызвать бригаду скорой помощи.
Во избежание подобных случаев следует соблюдать несложные правила техники безопасности, а также регулярно производить производственный лабораторный контроль содержания аммиака в воздухе рабочей зоны лабораториями санэпиднадзора. При работе с такими опасными химическими веществами халатность недопустима, так как при возникновении чрезвычайной ситуации пострадать может не один человек, а многие.
Отравление аммиаком — это патологическое состояние, спровоцированное вдыханием паров данного вещества, а также его приемом внутрь в виде водного или спиртового раствора. При техногенных катастрофах возможно контактное поражение кожи и слизистых оболочек. Основные проявления включают слезотечение, резь в глазах, одышку, осиплость голоса, кашель, удушье, тахикардию, химические ожоги кожи. В тяжелых случаях возникают судороги, коллапс, остановка сердца. Патология диагностируется на основании анамнеза, типичного аромата, исходящего от пострадавшего, данных лабораторного обследования. Специфическое лечение: эуфиллин, преднизолон, ингаляции сальбутамола и кислорода.
МКБ-10

Общие сведения
Аммиак — прозрачный газ с узнаваемым запахом или его водный раствор. Обладает раздражающим действием, способен вызывать отек легких, гипераммониемию, химическое поражение альвеол и интерстициальной ткани. Отравления встречаются редко, их число не превышает 1% от общего количества госпитализаций по поводу экзотоксикоза пульмотоксическими ядами. Распространены среди представителей асоциальных групп населения (алкозависимые люди), поклонников нетрадиционных методов лечения, работников предприятий химической промышленности, деятельность которых связана с синтезом и транспортировкой нашатырного спирта.

Причины
Наиболее тяжелые отравления возникают при производственных катастрофах с выбросом большого объема газа в ограниченном пространстве и при повреждении больших емкостей с водными растворами аммиака. Вещество испаряется, заполняет комнату, делая воздух непригодным для дыхания. Предельно допустимой считается концентрация газа в производственном помещении >20 мг/м 3 , на открытом пространстве >0,2 мг/м 3 . Другие причины поражения:
- Попытка суицида. В редких случаях регистрируются попытки самоубийства с использованием аммиака. Для этого применяют 10% водный раствор — наиболее доступную в быту форму. Преимущественно поражаются слизистые оболочки желудочно-кишечного тракта, ротовая полость, носоглотка. Тяжесть состояния зависит от количества принятого препарата.
- Самолечение. Использование непроверенных средств народной медицины, а также неправильная трактовка существующих рецептов порой приводит к превышению допустимых к употреблению доз нашатырного спирта. Это становится причиной отравлений, которые в абсолютном большинстве случаев протекают в легкой или среднетяжелой форме.
- Нивелирование действия алкоголя. Существует мнение, что прием внутрь нескольких капель нашатырного спирта позволяет добиться отрезвления человека, находящегося под действием этанола. Согласно рецепту, перед питьем вещество растворяют в стакане чистой воды. При приеме концентрированного раствора возникает ожог слизистых оболочек.
- Неправильное местное использование. 10% аммиак применяют локально с целью обезжиривания и антисептической обработки кожи, устранения папиллом. Чрезмерно длительная аппликация или процедура, осуществленная с помощью высококонцентрированного раствора, сопровождается появлением кожных ожогов.
Патогенез
Отравление аммиаком характеризуется наличием удушающего и нейротропного эффектов. Воздействие газа на дыхательные пути провоцирует раздражение слизистых оболочек, венозный стаз и альвеолярный отек. На вскрытии обнаруживается повышенный уровень гидратации тканей, некротизированные участки и зоны субплеврального кровоизлияния. Нейротропное действие проявляется в форме нарушения нервно-мышечной проводимости и деятельности ЦНС. Отмечается атаксия, тремор головы, клонические судорожные припадки.
Смерть наступает от паралича дыхательной мускулатуры, критического снижения функциональных способностей легких, некупирующегося сосудистого коллапса. Употребление концентрированных растворов через рот становится причиной химических ожогов, некроза и перфорации ЖКТ. При отсутствии помощи больной погибает от внутренних кровотечений, инфекционно-токсического шока или повреждения висцеральных органов излившимся желудочным содержимым. Если количество выпитого препарата невелико, возникают только ожоги рта и пищевода, которые редко заканчиваются летально.
Классификация
Отравление аммиаком может классифицироваться в зависимости от причин развития (криминальное, суицидальное, случайное, производственное) или пути поступления яда в организм (ингаляционный, контактный, пищевой). С учетом того, что NH3 обладает высокой летучестью, контактные и пищевые отравления обычно сочетаются с поражением дыхательных путей. Наиболее значимым с клинической точки зрения является деление по степени тяжести:
- Легкая интоксикация. Присутствуют симптомы раздражения слизистых оболочек, гиперсаливация. Одышка выражена слабо. Сознание не нарушено, пострадавший ориентируется в окружающей обстановке, критически относится к собственному состоянию. Данные об изменении сердечного ритма и гемодинамики отсутствуют. Иногда отмечается незначительная тахикардия и гипертония, обусловленная стрессовыми реакциями.
- Поражение средней степени. Наблюдается отек легких с соответствующей клинической и рентгенологической картиной. Пациент возбужден, испуган, мечется, в происходящем ориентируется частично. Поведение неадекватное. Присоединяются нарушения гемодинамики, компенсаторное увеличение ЧСС, которое впоследствии сменяется брадикардией. Выявляются признаки гипоксии. Возможна рефлекторная остановка дыхания.
- Тяжелая интоксикация. Резкое нарушение жизненно важных процессов в организме, развитие метаболических сбоев, ацидоза, массивного пульмонального отека с выраженной дыхательной недостаточностью. Возможно возникновение сосудистого коллапса, коронарной аритмии. Сознание нарушается в значительной степени, формируется сопор или кома.
Симптомы
Ингаляционное поражение проявляется резью в глазах, слезотечением, ухудшением зрения и конъюнктивитом. Отмечаются приступы удушливого кашля, вначале сухого, позже – приобретающего продуктивный характер. При ларингоспазме кашель становится лающим. При осмотре выявляют гиперемию кожи, пациент жалуется на зуд по всему телу. Развитие отека легкого характеризуется появлением одышки, боли в груди, генерализованного цианоза. Выслушиваются хрипы, дыхание проводится не во все отделы. Отмечается компенсаторная тахикардия, на поздних этапах — нарушение сердечного ритма по типу АВ-блокад, фибрилляции предсердий или желудочков.
Нейротропное действие яда проявляется в виде бреда, психомоторного возбуждения, судорожного синдрома. Патогномоничный признак — снижение слухового порога до пределов, когда даже слабые звуки нестерпимы для больного. Во многих случаях именно аудиальный раздражитель становится провоцирующим фактором судорог. Явление сохраняется в течение нескольких часов после удаления пострадавшего из зараженной зоны и начала медицинской помощи. В дальнейшем функции нервной системы могут восстанавливаться не в полной мере.
При контакте с жидкими формами аммиака клиника ингаляционного отравления обычно отсутствует. На участке, контактировавшем с раствором, развивается химический ожог II степени. Наблюдается поражение эпидермиса и верхних слоев кожи, появление пузырей. При принятии средства внутрь аналогичные процессы отмечаются в пищеводе и желудке. Клиника включает боль в поврежденной зоне, рвоту, тошноту, признаки химического ожога слизистой ротовой полости и кожи вокруг рта. Существует риск внутреннего кровотечения, сопровождающегося рвотой цвета кофейной гущи или с примесью алой крови.
Осложнения
Отравление аммиаком с пульмональной симптоматикой в 80% случаев приводит к развитию вторичной пневмонии. Возможна острая дыхательная недостаточность, протекающая в тяжелой форме и требующая искусственной респираторной поддержки. Отсроченные последствия (снижение интеллекта, изменение личности) встречаются в 20-25% случаев, становятся результатом гипоксии и токсического воздействия нитрида водорода на ткани ЦНС. Могут диагностироваться через несколько месяцев или лет после выписки из стационара. Являются необратимыми, на фоне проводимого ноотропного лечения психика восстанавливается в незначительной степени.
Диагностика
Предварительный диагноз устанавливается врачом скорой помощи, прибывшим на место происшествия, подтверждается токсикологом или реаниматологом профильного отделения. Проводится дифференциальная диагностика с отеком легких другого происхождения, а также с поражением боевыми газами и иными ингаляционными химикатами. Ожоги, вызванные приемом аммиака внутрь, следует отличать от отравлений прижигающими жидкостями (уксусная эссенция, бытовые щелочи). Показаны следующие виды обследования:
Лечение
Отравление аммиаком требует немедленных мер по спасению пострадавшего. До приезда медиков следует вынести его из зараженной местности, обеспечить приток свежего воздуха, придать полусидячее положение. Допустимо промыть глаза слабым фосфат-буферным раствором или чистой водой, после чего закапать по 1 капле альбуцида. Прибывшие на место событий сотрудники СМП обрабатывают пораженные участки тела 5% аскорбиновой кислотой. Дальнейшие действия зависят от имеющейся клинической картины.
При ларингоспазме необходима ингаляция дексаметазона или нафтизина через небулайзер. Внутривенно — бронхолитики, в том числе сальбутамол. Отек легких является показанием для дробного введения морфина, строфантина, дроперидола. Психомоторное возбуждение купируется с помощью бензодиазепинов. Тяжелая дыхательная недостаточность требует интубации трахеи с переходом на ИВЛ. При шоке проводят инфузионную терапию кристаллоидными и коллоидными растворами, вводят адреналин, кардиотоники, гидрокарбонат натрия.
В стационаре осуществляется специфическая терапия, направленная на восстановление работы дыхательной системы. Наиболее эффективным средством является преднизолон. Пути введения: внутривенный, ингаляционный через небулайзер. Второе место занимает эуфиллин, который назначают внутримышечно. Также применяется педифен, сальбутамол, комбинированные препараты, аскорбиновая кислота. При необходимости больного помещают в ОРИТ для реанимационного пособия.
Прогноз и профилактика
Отравление аммиаком имеет благоприятный прогноз, если пострадавший находился в зоне заражения не более 3-5 минут. Следует учитывать и концентрацию газа в воздухе. Чем она выше, тем более короткое время требуется для получения токсической дозы. При тяжелой интоксикации, сопровождающейся альвеолярным отеком, смертность составляет 50% при отсутствии терапии, 20% при лечении преднизолоном и эуфиллином, 30-60% при использовании менее эффективных препаратов. Течение патологии ухудшается при наличии сопутствующих болезней легких.
Профилактика заключается в соблюдении техники безопасности во время работы на химическом производстве. При высокой вероятности техногенных катастроф может практиковаться превентивное лечение. В качестве препарата, максимально снижающего риск тяжелого поражения дыхательной системы, применяется преднизолон. Чтобы предотвратить отравление водными растворами, следует держать их в плотно закрытой и промаркированной емкости, в местах, недоступных детям, отдельно от пищевых продуктов.
2. Медико-статистический анализ отравлений аммиаком / Саламе М.Б., Еремина М.В. // Успехи современного естествознания – 2011 год – №8.
3. Острые производственные отравления хлором и аммиаком: клиника, диагностика, лечение. Современные представления /Акимов А.Г., Халимов Ю.Ш., Шилов В.В.// Экология труда – 2012.
Е.В. Голованова
Кафедра поликлинической терапии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России, Москва
Аммиак является одним из важнейших нейротоксических метаболитов в организме человека. В клинической практике наиболее частым проявлением гипераммониемии является печеночная энцефалопатия (ПЭ) при патологии печени, представляющая собой спектр нервно-психических расстройств на фоне острой или хронической печеночно-клеточной недостаточности и/или порто-системном шунтировании крови. Снижение уровня аммиака является патогенетическим подходом к лечению хронических заболеваний печени, позволяющим не только снизить проявления ПЭ, но и уменьшить активацию звездчатых клеток печени, улучшить печеночный кровоток, препятствовать развитию и прогрессированию фиброза печени.
Основным источником образования аммиака в организме человека является азот пищевого белка, образующийся в ходе реакций дезаминирования аминокислот в печени. Дополнительными источниками образования аммиака являются:
- Разложение мочевины и белка уреазаположительной микрофлорой желудочно-кишечного тракта (ЖКТ).
- Образование аммиака в мышечной ткани при физической нагрузке.
- Распад глутамина в тонкой кишке.
- Абсорбция аммиака в почках при гипокалиемии и/или алкалозе.
Выделение мочевины осуществляется преимущественно через почки (около 80%), примерно 20% мочевины повторно поступают в ЖКТ, где вновь разлагается уреазаположительными бактериями до аммиака.
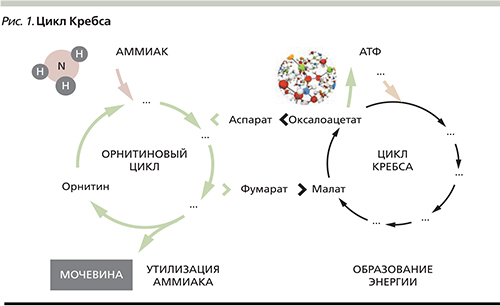
Детоксикация аммиака в организме осуществляется преимущественно в митохондриях перипортальных гепатоцитов за счет связывания в орнитиновом цикле с аминокислотами и образованием нетоксичной мочевины (рис. 1). Частично детоксикация аммиака происходит в мышечной ткани в процессе синтеза глутамина при участии фермента глутаминсинтетазы. Эта реакция с меньшей интенсивностью протекает также в астроцитах головного мозга и перивенозных гепатоцитах печени. Образующийся в результате этих превращений глутамин нетоксичен и выделяется с мочой.
Таким образом, являясь основным источником аммиака, печень в то же время служит главным местом его обезвреживания. Именно поэтому гипераммониемия развивается в организме человека, прежде всего при хронических заболеваниях печени (ХЗП). К причинам этого относятся снижение активности орнитинового цикла и глутаминсинтетазной реакции при печеночно-клеточной недостаточности и порто-системное шунтирование при развитии и прогрессировании портальной гипертензии.
Значительно реже в рутинной клинической практике встречаются генетически детерминированные ферментопатии, которые сопровождаются повышением концентрации аммиака в сыворотке крови. В зависимости от дефицита или дефекта того или иного фермента выделяют несколько видов генетических заболеваний: гипераммониемию типа I (в основе – дефект карбамоилфосфатсинтетазы I), гипераммониемию типа II (в основе – дефект орнитинкарбамоилтрансферазы), цитруллинемию (в основе – дефект аргининосукцинатсинтетазы), аргининосукцинатурию (в основе – дефект аргининосукцинатлиазы), гипераргининемию (в основе – дефицит аргиназы).
Известно, что аммиак является одним из важнейших нейротоксических метаболитов в организме человека. В клинической практике наиболее частым проявлением гипераммониемии является печеночная энцефалопатия (ПЭ) при патологии печени, представляющая собой спектр нервно-психических расстройств на фоне острой или хронической печеночно-клеточной недостаточности и/или портосистемном шунтировании крови. В основе патогенеза ПЭ лежит дисбаланс аминокислот в головном мозге, приводящий к отеку астроглии и нарушениям ее функций, таких как изменения постсинаптических рецепторов и процессов нейротрансмиссии, нарушение проницаемости гематоэнцефалического барьера, снижение энергетического обеспечения нейронов. Степень клинических проявлений напрямую коррелирует с уровнем аммиака в сыворотке крови. В зависимости от выраженности нарушений деятельности головного мозга выделяют четыре степени тяжести печеночной энцефалопатии (от минимальной до комы).
В последние годы в связи с совершенствованием диагностических методик актуально отделение клинически выраженных стадий ПЭ (дезориентация, атаксия, кома) от стадии с минимально выраженными проявлениями (латентная ПЭ). Такую ПЭ можно выявить, используя специальные опросники или метод вызванных потенциалов головного мозга. При этом выявляются когнитивные и психомоторные расстройства, такие как трудности с принятием решений, снижение скорости психомоторных реакций и др. К клиническим симптомам латентной ПЭ относятся повышенная утомляемость, слабость, раздражительность, инверсия сна (сонливость днем и бессонница ночью), нарушения речи, изменения почерка, рассеянность за рулем и при выполнении работы, требующей повышенной концентрации внимания, тремор, снижение мышечных рефлексов.
К сожалению, результатом таких нарушений могут стать серьезные дорожно-транспортные происшествия с тяжелыми последствиями [1, 2]. В связи с этим выявление минимальной ПЭ имеет большое значение для работников многих профессий: водителей автотранспорта, операторов на автоматизированном оборудовании и др.
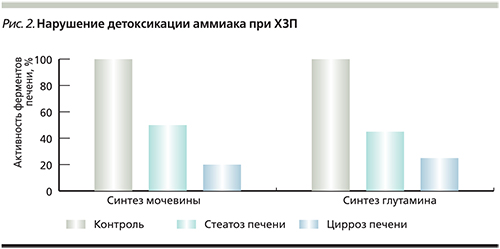
В исследованиях показано, что у больных стеатозом печени при отсутствии клинических признаков воспаления и печеночно-клеточной недостаточности уже имеется выраженное снижение детоксикации аммиака по обоим путям (уменьшается синтез и мочевины, и глутамина) за счет выраженного снижения активности соответствующих ферментов в печени (рис. 2).
В 2016 г. ученые из Великобритании получили новые научные данные, свидетельствующие о том, что гипераммониемия активирует звездчатые клетки печени (ЗКП) и как следствие – может приводить к усиленному коллагенообразованию и прогрессирующему фиброзированию [3].
Известно, что ЗКП являются основными профиброгенными клетками органа. Хроническое повреждение печени под влиянием различных этиологических факторов (алкоголь, вирусная инфекция, лекарства, холестаз и др.) способствует их активации и дифференцировке в миофибробластоподобные клетки, которые приобретают сократительные, провоспалительные и фиброгенетические свойства. При этом ЗКП пролиферируют, из них исчезают капли жира, увеличивается шероховатая эндоплазматическая сеть, в них появляется специфический белок гладких мышц (α-актин), увеличивается количество рецепторов к цитокинам, стимулирующим пролиферацию и фиброгенез.
К факторам, активирующим ЗКП, относятся трансформирующий фактор роста (TGF-β1 – Transforming growth factor beta), тромбоцитарный фактор роста (PDGF – Platelet-derived growth factor), фактор роста фибробластов, интерлейкин-1 (ИЛ-1), эпидермальный фактор роста, фактор некроза опухоли α. Среди всех факторов роста TGF-β1 позиционируется как ключевой медиатор в фиброгенезе у человека. Различные способы, воздействующие на синтез этого фактора или на сигнальные пути, которые реализуются с участием этого фактора, значимо снижают фиброз в экспериментальных моделях [4].
Активированные ЗКП мигрируют и аккумулируются в месте поражения ткани печени, при этом секретируя большое количество внеклеточного матрикса и одновременно регулируя деградацию этих молекул на уровнях транскрипции и посттранскрипции. Повышение содержания информационной коллагеновой РНК является опосредующим фактором, повышающим синтез коллагена активированными ЗКП. В этих клетках посттранскрипционная регуляция коллагена осуществляется путем последовательности 3-го нетранслируемого региона РНК-связующего протеина aСР2, равно как и посредством структуры в 5-м окончании коллагена информационной РНК. Кроме этого ЗКП экспрессируют большое количество нейроэндокринных маркеров (реелин, нестин, нейротрофины, синаптофизин и глиально-фибриллярные кислотные протеины), а также несут рецепторы нейротрансмиттеров, выделяют провоспалительные цитокины, нейрофильный и моноцитарный хемоаттрактаны, которые усиливают воспалительную реакцию в пораженной печени [5].
Фиброз печени является основным, этиологически независимым путем прогрессирования хронических диффузных заболеваний печени вплоть до цирроза. Печеночный фиброз ассоциируется с изменением количества и качественного состава экстрацеллюлярного коллагенового матрикса (ЭКМ). При выраженных стадиях фиброза печень содержит приблизительно в 6 раз больше ЭКМ, чем в норме, а в его составе определяются коллагены (1-го, 3 и 4-го типов), фибронектин, ундулин, эластин, ламинин, гиалуронан и протеогликаны. Снижение скорости резорбции ЭКМ и выведение молекул металлопротеиназ являются в основном следствием перевысвобождения их специфических ингибиторов (TIMPs – tissue inhibitors of metalloproteinases). Результатом превалирования процессов образования внеклеточного матрикса над его разрушением является формирование фиброзного рубца, при этом фиброз на ранних стадиях развития – процесс обратимый, а цирроз с характерными сшивками между коллагеновыми волокнами и узлами регенерации необратим. Прогрессирующее накопление и отложение внеклеточного матрикса в пространстве Диссе приводят к исчезновению фенестров эндотелия, капилляризации и стенозированию синусоидов с постепенным развитием портальной гипертензии [6–8].
In vitro показано, что аммиак дозозависимо снижает клеточную пролиферацию и метаболизм в первичных человеческих ЗКП, но не вызывает гибели клеток.
Длительная обработка клеток аммиаком (до 72 часов) индуцирует развитие и прогрессирование эндоретикулярного стресса в hHSCs, что проявлялось выраженным перинуклеарным накоплением красителя (ER-Tracker™ Red) и появлением цитоплазматических вакуолей по мере роста концентрации аммиака. Использование Image IT™-набора для определения зеленых активных форм кислорода позволило исследователям выявить аммиак-дозозависимое образование активных радикалов кислорода (ROS – Reactive oxygen species) в hHSCs. Таким образом, установлено, что увеличение концентрации аммиака и время его воздействия напрямую влияют на уровни мРНК экспрессии маркеров стресса [3].
Исследование также показало, что при повышенных концентрациях аммиака hHSCs приобретают выраженный профиброгенный и провоспалительный потенциал, что подтверждается результатами исследования in vitro:
- аммиак значительно увеличивает экспрессию белка α-SMA, являющегося активатором ЗКП, а при уровне аммиака 300 мкМ увеличивается синтез виментина – важного промежуточного филамента;
- возрастание концентраций аммиака сопровождается увеличением уровней миозина IIa (играющего ключевую роль в сокращении HSC), миозина IIb (важный фактор активации HSC); экспрессией p38 MAPK, ростом уровней PDGF-Rβ и коллагена I типа;
- повышение уровней аммиака индуцирует сильный и значимый рост мРНК экспрессии металлопротеиназ-2, в то время как мРНК-экспрессия TIMP1 снижается;
- при обработке hHSC аммиаком в концентрации 300 мкМ на протяжении 72 часов мРНК значительно возрастает экспрессия провоспалительного ИЛ-1β;
- аммиак в дозах 50 и 100 мкМ значительно увеличивает в hHSC мРНК- экспрессию ИЛ-6, но не изменяет мРНК-экспрессию ИЛ-8.
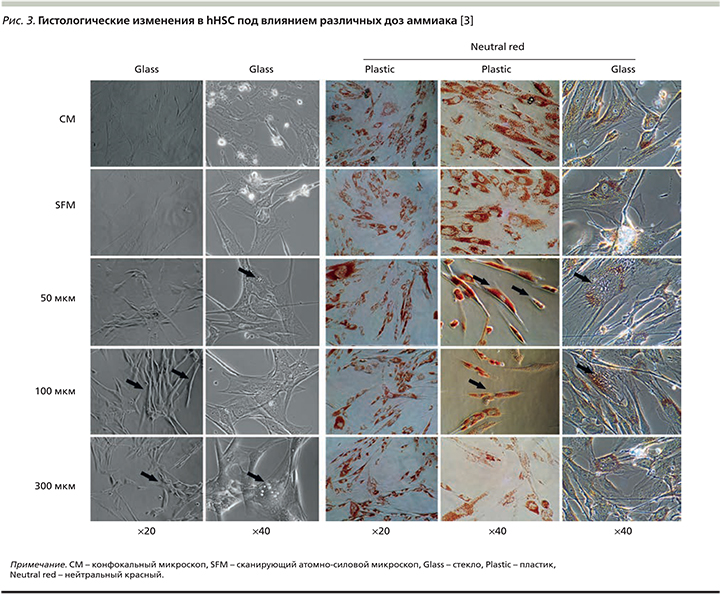
При гистологическом изучении клеток установлено, что аммиак дозозависимо вызывает серьезные морфологические изменения. Так, при световой микроскопии и в тесте жизнеспособности с нейтральным красным (20х, 40х) наблюдали превращение миофибробластоподобных клеток в веретеноподобные фибробласты под действием повышенных концентраций аммиака (рис. 3). Электронная микроскопия показала изменения структуры цитоскелета клеток с образованием цитоплазматических вакуолей при гипераммониемии, однако эти изменения быстро регрессировали после помещения клеток в безаммиачную среду [3].
Вторая часть исследования была проведена на самцах крыс, которые были разделены на три группы: в двух группах проведено перевязывание общего желчного протока (BDL – экспериментальная модель холестаза) с целью формирования экспериментального повреждения печени, при этом крысам одной из групп вводился орнитин (ОР), второй – физиологический раствор. Третья группа животных была контрольной, без повреждения печени.
Анализ результатов опыта показал, что концентрации аммиака были значительно увеличены в плазме крыс с BDL по сравнению с контролем (182±12,8 против 62,51±6,2 мкМ; p
1. Bajaj J.S., Pinkerton S.D., Sanyal A.J., Heuman D.M. Diagnosis and treatment of minimal hepatic encephalopathy to prevent motor vehicle accidents: a cost-effectiveness analysis. Hepatology. 2012;55(4):1164–71.
2. Богомолов П.О., Буеверов А.О., Уварова О.В., Мациевич М.В. Гипераммониемия у пациентов с заболеваниями печени на доцирротической стадии: возможно ли это? Клин. перспективы гастроэнтерол., гепатол. 2013;5:3–8.
3. Джалан Р., Де Чиара Ф., Баласубраманиян В., Андреола Ф., Кхетан В., Малаго М., Пинзани М., Мукерджи Р.П., Ромбоутс К. Аммиак приводит к патологическим изменениям в звездчатых клетках печени, и является целью при лечении портальной гипертензии. Журн. гепатологии. 2016;64:823–33.
4. Gressner A.M., Weiskirchen R., Breitkopf K., Dooley S. Roles of TGF-beta in hepatic fibrosis. Front. Biosci. 2002;7:d793–d807.
5. Lindquist J.N., Parsons C.J., Stefanovic B., Brenner D.A. Regulation of alpha1(I) collagen messenger RNA decay by interactions with alphaCP at the 3?-untranslated region. J. Biol. Chem. 2004;279:23822–29.
6. Benyon R.C., Iredale J.P. Is liver fibrosis reversible? Gut. 2000;46:443–46.
7. Arthur M.J. Fibrogenesis II. Metalloproteinases and their inhibitors in liver fibrosis. Am. J. Physiol. Gastrointest. Liver Physiol. 2000;279:G245–G249.
8. Arthur M.J. Reversibility of liver fibrosis and cirrhosis following treatment for hepatitis C. Gastroenterology. 2002;122:1525–28.
10. Бурков С.Г., Арутюнов А.Г., Годунова С.А., Гурова Н.Ю., Егорова Н.В., Должикова Т.А., Шиковная Ю.Н. Эффективность гранул L-орнитин-L-аспартата в лечении неалкогольной жировой болезни печени. Consilium Medicum. 2010;12(8):43–7.
11. Осипенко М.Ф., Редькина А.В., Бикбулатова Е.А., Моисеенко Е.Е., Скалинская М.А., Казакова Е.А. Оценка L-орнитин-Lаспартата (Гепа-Мерц) в комплексном лечении неалкогольного стеатогепатита. Consilium Medicum. Прил. Гастроэнтерология. 2010;1:35–8.
12. Грюнграйфф К., Ламберт-Бауманн Й. Эффективность гранул L-орнитин-L-аспартата при лечении хронических заболеваний печени. Сучасна гастро-ентерологія. 2008;2:59–67.
13. Ермолов С.Ю., Шабров А.В., Ермолова Т.В. и др. Новые подходы к диагностике и коррекции портопеченочной гемодинамики. Эксперим. и клин. гастроэнтерология. 2007;4:13–6.
14. Ермолова Т.В., Яковлева Д.М. Эффективность применения L-орнитина-L-аспартата у больных стеатогепатитом. Соврем. гастроэнтерология и гепатология. 2012;1:22–6.

Наличие аммиака в окружающей среде не всегда приводит к поражению. Чтобы он вызвал какие-либо неблагоприятные последствия для здоровья, вы должны вступить с ним в контакт. Вы можете подвергнуться воздействию аммиака при вдыхании или проглатывании вещества, а также при попадании его на кожу или в глаза.
После воздействия любого химического вещества неблагоприятное воздействие на здоровье, с которым вы можете столкнуться, зависит от нескольких факторов, включая количество, которому вы подверглись (доза), способ, которым вы подверглись, продолжительность воздействия, форма химического вещества и ваше состояние.
Что происходит при контакте с аммиаком?
Аммиак является агрессивным веществом, и его основное токсическое воздействие ограничивается местами непосредственного контакта с аммиаком (т.е. кожей, глазами, дыхательными путями, полостью рта и желудочно-кишечным трактом). Например, если пролить на пол бутылку концентрированного аммиака, то будет ощущаться сильный запах аммиака, Вы будете кашлять, а глаза слезиться из-за раздражения.
Озабочены загрязнением воздуха рабочей зоны вашего предприятия аммиаком? Мы можем предложить определение концентрации аммиака в воздухе.
Если Вы подвергнетесь воздействию очень высокого уровня аммиака, Вы испытаете более опасные последствия. Например, если Вы попали в густое облако аммиака или если Ваша кожа соприкасается с концентрированным аммиаком, то кожа, глаза, горло или легкие могут сильно обжечься.
Эти ожоги могут быть достаточно серьезными, чтобы вызвать постоянную слепоту, легочную болезнь или смерть. Аналогичным образом, если Вы случайно съели или выпили концентрированный аммиак, у Вас могут появиться ожоги во рту, горле и животе. Нет никаких доказательств того, что аммиак вызывает рак.
Аммиак может также оказывать благоприятное воздействие, например, при его использовании в качестве нюхательной соли. Некоторые соли аммония уже давно используются в ветеринарии и медицине.
Как аммиак может повлиять на детей?
Дети в меньшей степени, чем взрослые, подвержены воздействию концентрированного аммиака, поскольку большинство случаев воздействия концентрированного аммиака происходит в профессиональной среде.
Дети могут подвергаться воздействию аммиака так же, как и взрослые, в результате разливов или утечек из таких источников как резервуары или трубопроводы для аммиака, особенно на фермах, где он используется в качестве удобрения. Дети также могут подвергаться воздействию разбавленных растворов аммиака из бытовых чистящих средств, содержащих аммиак.
Воздействие аммиака на детей может быть таким же, как и на взрослых. Аммиак является раздражающим веществом, а его раствор и газ могут вызвать ожоги кожи, глаз, рта и легких. В случае разлива аммиака дети могут подвергаться воздействию аммиака дольше, чем взрослые, поскольку они могут покинуть эту зону не так быстро.
Нет никаких свидетельств того, что воздействие найденных в окружающей среде уровней аммиака приводит к врожденным дефектам или другим последствиям для развития. Неизвестно, может ли аммиак передаваться от беременной матери развивающемуся плоду через плаценту или от кормящей матери ее потомству через грудное молоко. Одно из исследований на животных показало, что воздействие очень высоких уровней аммиака на матерей во время беременности приводит к тому, что их новорожденные дети становятся меньше, чем обычно, но это происходит при уровне аммиака, который также влияет на матерей.
Читайте также:

