Радиочувствительность органов и тканей реферат
Обновлено: 07.07.2024
В данной статье рассматривается радиочувствительность опухолей, его значение в лучевой терапии, а также процессы и способы радиомодификации. В основе лучевой терапии лежат понятия о действии различных видов ионизирующего излучения, а также возможности целенаправленного изменения эффектов облучения с помощью применения методов радиомодификации. В настоящее время в лучевой терапии методы радиомодификации позволяют, с одной стороны, путем применения радиосенсибилизаторов повысить эффективность облучения злокачественных опухолей, а с другой – увеличить защиту здоровых тканей при применении радиопротекторов. К способам радиомодификации относятся сочетание лучевой терапии с химиопрепаратами, гипертермией, повышение кислорода в опухолевых тканях, в том числе применение электрон-акцепторных соединений, искусственная гипергликемия, - это способы, повышающие радиочувствительность опухолей; гипоксирадиотерапия, применение модификаторов биологических реакций, - это способы, понижающие радиочувствительность нормальных тканей. Знания о радиочувствительности опухолей и нормальных тканей имеет существенное значение в лучевой терапии. Важен правильный выбор лучевой терапии, так как это играет ведущую роль в эффективности лечения опухолей, результатах выживаемости, частоте возникновения осложнений и рецидивов злокачественных новообразований, качества жизни. Благодаря знанию всех способов радиомодификации имеются реальные возможности улучшения результатов лучевой терапии путем управления радиочувствительности злокачественных новообразований с помощью радиомодифициующих агентов, что ведет к расширению радиокурабельности опухолей.

1. Асатурян М.А. и др. Основы и клиническое применение лучевой терапии //Лучевая диагностика и лучевая терапия: учеб. пособие / под ред. Г.Е. Труфанова.- СПб.: ВМедА, 2005. – С. 106-134.
2. Асатурян М.А. и др. Современные принципы лучевой терапии злокачественных опухолей // Сб. учеб. пособий по актуальным вопросам лучевой диагностике и лучевой терапии / под ред. Г.Е. Труфанова. – СПб.: Элби-СПб, 2004. – С. 253-271.
4. Труфанов Г.Е., Асатурян М.А., Жаринов Г.М., Малаховский В.Н. Лучевая терапия: учебник / под ред. Труфанова Г.Е. – М.: ГЭОТАР –Медиа, 2013. – 208 с.: ил.
Введение: Степень восприимчивости к излучению называют радиочувствительностью. Клетки, ткани, органы человека в разной степени чувствительны к облучению. Радиочувствительность тканей и клеток не является величиной постоянной, она меняется в зависимости от состояния организма и от действия внешних факторов, а также от уровня пролиферативной активности органов и тканей. Согласно заключению экспертов ВОЗ, успех лучевой терапии примерно на 50% зависит от радиочувствительности опухоли, на 25% от аппаратного оснащения, на 25% от выбора рационального плана лечения и точности его воспроизведения от сеанса к сеансу облучения[3].
Цель: разделение опухолей по степени восприимчивости к ионизирующему излучению; изучение факторов, от которых зависит радиочувствительность; рассмотрение всех способов радиомодификации.
С целью представления о радиочувствительности различных опухолей и тканей приведем таблицу 12.
Степень восприимчивости к ионизирующему излучению
Неходжкинская лимфома, лимфогранулематоз, лейкемия, семинома, мелкоклеточный рак легкого, опухоли головы и шеи, дисгерминома, опухоль Юинга
Кроветворная, лимфоидная ткань, сперматогенный эпителий, эпителий фолликулов яичников, эпителий ротоглотки, кожа
Опухоли молочной железы, немелкоклеточный рак легкого, аденокарцинома желудочно-кишечного тракта, рак шейки матки, рак предстательной железы
Железистый аппарат желудка, толстой кишки, молочной железы, эпителий слизистой тонкой кишки
Фибросаркома, остеогенная саркома, хондросаркома, рак почки, нейрогенные опухоли
Хрящевая, костная, мышечная, фиброзная ткани
Из данной таблицы следует, что наиболее чувствительны к облучению кроветворная, лимфоидная ткань, сперматогенный эпителий, эпителий фолликулов яичников, эпителий ротоглотки, кожа. Далее по степени радиочувствительности идут железистый аппарат желудка, толстой кишки, молочной железы, эпителий слизистой тонкой кишки хрящевая, костная, мышечная, фиброзная ткани. К радиочувствительным опухолям относят неходжкинская лимфома, лимфогранулематоз, лейкемия, семинома, мелкоклеточный рак легкого, опухоли головы и шеи, дисгерминома, опухоль Юинга. Промежуточной радиочувствительностью обладают опухоли молочной железы, немелкоклеточный рак легкого, аденокарцинома желудочно-кишечного тракта, рак шейки матки, рак предстательной железы. Резистентными являются фибросаркома, остеогенная саркома, хондросаркома, рак почки, нейрогенные опухоли. Несмотря на то, что в данной таблице отмечены железистый аппарат желудка, толстой кишки, эпителий слизистой тонкой кишки, обладающие промежуточной радиочувствительностью, при опухолях с локализацией в этих органах лучевую терапию применяют редко либо вовсе не применяют, так как опухоли данных локализаций подвижны из-за перистальтических движений желудка и кишечника[4]. А при раке печени не применяют лучевую терапию из-за низкой толерантности печени к ионизирующему излучению[5].
Радиочувствительность злокачественной опухоли к ионизирующему излучению определяется большим числом факторов: возрастом, состоянием больного, формой роста, гистологическим типом новообразования, состоянием тканей, окружающих опухоль, соотношением в опухоли клеточных и стромальных элементов, скоростью репопуляции клеток, степенью оксигенации тканей, наличием некротических участков и гипоксических клеток[3].
Рассмотрим некоторые факторы, влияющие на чувствительность опухолей:
- На чувствительность опухоли к излучению влияет степень дифференцировки клеток: чем менее дифференцированы клетки, тем выше радиочувствительность опухоли. Например, мелкоклеточный рак легкого намного чувствительный к облучению, чем плоскоклеточный рак или аденокарцинома этого же органа.
- Степень повреждающего действия зависит от фазы клеточного цикла, в которой находятся пролиферирующие клетки в момент облучения: наибольшей чувствительностью обладают клетки в фазе G2 и M, меньшей – находящиеся в фазах G1 и S.
- Чувствительность к излучению в значительной мере зависит от клеточного состава злокачественной опухоли.
Способы радиомодификации. Достижения в области радиобиологии – изучение прямого и косвенного действия радиации – привели к исследованию процессов радиомодификации.
Прежде чем перейти к способам радиомодификации необходимо знать некоторые понятия о радиомодификации: Радиомодификация – это целенаправленное изменение чувствительности тканей к облучению. Радиомодифицирующие агенты – это физические и химические факторы, с помощью которых эффективность лучевых воздействий может быть повышена путем усиления радиопоражаемости опухоли и ослабления лучевых реакций нормальных тканей. Радиосенсибилизация лучевого воздействия – это процесс, при котором различные способы приводят к увеличению поражения тканей под влиянием облучения. Радиопротекция - действия, направленные на снижение поражающего эффекта ионизирующего излучения. Соответственно радиопротекторы – это вещества, снижающие радиочувствительность.
На основании выше сказанного способы радиомодификации можно разделить на две большие группы. Первая группа это способы, повышающие радиочувствительность опухолей или, другими словами, повышающие радиопоражаемость, вторая группа – способы, понижающие радиочувствиетльность нормальных тканей.
Подробно рассмотрим каждую группу.
Первая группа способов, повышающих радиочувствительность опухолей:
- Чувствительность опухоли ионизирующего излучения можно повысить, сочетая лучевую терапию с приемом некоторых химиопрепаратов. Используя химиопрепараты в качестве синхронизаторов клеточного цикла (5-фторурацил, платидиам, винкристин и др.), можно на некоторое время задерживать опухолевые клетки в фазе S. Затем большинство клеток синхронно вступает в наиболее радиочувствительные фазы G2 и М, и именно в этот период желательно производить облучение опухоли.
В фазе митоза, наиболее чувствительной к излучению, клетку задерживают винкаалколоиды и таксаны. Гидроксимочевина тормозит цикл в фазе G1. Препараты платины при сочетании с лучевым воздействием тормозят процессы восстановления повреждений опухолевых клеток. Митомицин С – влияет на радиорезистентные клетки в состоянии гипоксии. Применение его в сочетании с лучевой терапией при злокачественных новообразованиях головы и шеи значительно повышает выживаемость больных.
- Терморадиотерапия – сочетание ионизирующего излучения с гипертермией. Повышение местной температуры в опухоли до 42-44 °С вызывает гибель многих клеток злокачественного новообразования. Осуществляют с помощью генераторов электромагнитного излучения в СВЧ-, УВЧ-диапазонах. Используют при лечении больных меланомой, рака прямой кишки, молочной железы, опухоли головы и шеи, саркомы костей и мягких тканей.
- Сочетание лучевой терапии с повышением содержания в опухоли кислорода. Содержание кислорода в опухоли удается повысить искусственным путем. Для этого применяют облучение больных с использованием для дыхания чистого кислорода при обычном давлении (оксигенорадиотерапия) либо в барокамере под давлением 3-4 атм. (оксигенобарорадиотерапия). Особенно эффективно при лучевой терапии недифференцированных опухолей головы и шеи.
В качестве модифицирующего агента также используют электрон-акцепторные соединения (ЭАС) – метронидазол, мизонидазол, имитирующие функцию кислорода – его сродство к электрону.
- Сочетание лучевой терапии с искусственной гипергликемией. В связи с активным поглощением и накоплением опухолевой тканью глюкозы крови, введение глюкозы больному приводит к временной гипергликемии. Что, в свою очередь, приводит к снижению рН в опухолевых клетках. Следовательно, будет повышаться радиочувствительность за счет нарушения процессов пострадиационного восстановления в кислой среде. Поэтому гипергликемию обуславливает значительное усиление противоопухолевого действия ионизирующего излучения.
На основании данных о способах радиосенсибилизации рассмотрим частоту использования трех основных методов повышения радиочувствительности (оксигенобарорадиотерапия, терморадиотерапия, химиолучевая терапия) при различных видах опухолей (табл.2)[1,2].
Чувствительность организма или его тканей к действию ионизирующих излучений, ее виды и применение на практике. Радиочувствительность животного и растительного мира. Индивидуальная и возрастная радиочувствительность. Проявление эффектов радиации.
| Рубрика | Медицина |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 03.12.2010 |
| Размер файла | 19,1 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
1. Индивидуальная радиочувствительность
2. Возрастная радиочувствительность
Радиочувствительность -- чувствительность организма (или его тканей) к действию ионизирующих излучений.
Различные виды животного и растительного мира имеют неодинаковую радиочувствительность (видовая радиочувствительность). Так, например, собаки являются более радиочувствительными животными, чем кролики: при равномерном облучении абсолютно смертельной для собак считается доза 350 р, а для кроликов -- 800--1000 р. Абсолютно смертельная доза общего облучения для человека -- 600--700 р. Радиочувствительность изменяется в зависимости от времени года (сезонная радиочувствительность). Например, радиочувствительность собак и кроликов в осенне-зимний период значительно понижена. Радиочувствительность организма неодинакова в различные возрастные периоды (возрастная радиочувствительность), однако литературные данные по этому вопросу противоречивы. Противоречивы сведения и о половой радиочувствительности. На радиочувствительность оказывает влияние исходное физиологическое состояние организма, а также его индивидуальные свойства (индивидуальная радиочувствительность).
Различия в радиочувствительности имеются не только на уровне целого организма, но и на уровне его тканей, органов, клеток и даже молекул. Например, известно, что морфологические изменения в кроветворной ткани выявляются при сравнительно меньших дозах, чем в мышечной или костной. Молодые, быстро размножающиеся клетки более радиочувствительны, чем зрелые.
Накопленные в радиобиологии сведения по вопросу радиочувствительности широко используют в онкологической практике. Различия в тканевой радиочувствительности позволяют осуществлять лучевую терапию больных злокачественными новообразованиями: молодые, быстро размножающиеся опухолевые клетки обладают сравнительно высокой радиочувствительностью и поэтому при облучении повреждаются скорее, чем клетки здоровых тканей, неизбежно попадающих в облучаемое поле. При лучевой терапии больных учитывают различия в возрастной радиочувствительности. Например, реакция детей на облучение проявляется раньше, чем у взрослых. Принимаются во внимание сведения об индивидуальной радиочувствительности. При оценке исходного состояния больных учитывают повышенную радиочувствительность организма в период менструации, особую радиочувствительность тканей, в частности кожи, при воспалительных процессах.
Усилия радиобиологов направлены на изыскание методов, позволяющих повышать радиочувствительность опухоли при одновременном снижении радиочувствительности окружающих здоровых тканей и всего организма в целом.
1. Индивидуальная радиочувствительность
радиочувствительность организм излучения
Индивидуальная радиочувствительность на популяционном уровне колеблется в широких пределах. На уровне целостного организма в качестве критериев РЧ используют ЛД50 - дозу облучения, вызывающую смерть 50% облучённых организмов данного вида за определённое время после облучения. Для индивидуальной радиочувствительности имеют значение особенности генотипа (эффективность репарации системы ДНК), физиологическое состояние организма, пол, возраст.
Особенно радиочувствительны лица, имеющие некоторые наследственные заболевания (атаксия-телеангиэктазия, пигментная ксеродерма). Люди менее радиочувствительны во время сна и более радиочувствительны во время бодрствования, при усталости, беременности, хронических заболеваниях, ожогах.
Исключительно высоко радиочувствительны малодифференцированные ткани эмбриона и плода. Облучение женщин в период беременности может приводить к следующим последствиям у потомства:
1. Эмбриональная, неонатальная и постнатальная гибель плода, нарушение течения беременности.
2. Увеличение вероятности врождённых пороков развития.
3. Увеличение частоты нарушений роста и физического развития.
4. Увеличение частоты нарушений функций центральной нервной системы.
5. Снижение адаптационных возможностей организма. Нарушение функций иммунной и эндокринной систем.
6. Рост онкологических заболеваний.
Эффекты радиации могут проявляться сразу (смерть, пороки развития) или в отдаленные сроки после рождения (отставание в росте и развитии, онкологическая и другая заболеваемость).
2. Возрастная радиочувствительность
Радиочувствительность варьируемая в пределах одного вида в зависимости от возраста называется возрастной радиочувствительностью. Так, наиболее радиочувствительными являются молодые и старые экспериментальные животные, наиболее радиорезистентными -- половозрелые и новорожденные.
Чтобы понять механизмы, определяющие возрастную радиочувствительность организма (без чего невозможно правильно оценить последствия облучения человека), необходимо последовательно рассмотреть клеточные и тканевые аспекты радиочувствительности, так как клетка -- основная биологическая единица, в которой реализуется воздействие поглощенной при облучении энергии, что в последующем приводит к развитию лучевого поражения. Среди многих проявлений жизнедеятельности клетки наиболее чувствительна в отношении ионизирующего излучения ее способность к делению. Под клеточной гибелью (или летальным эффектом) в радиобиологии понимают утрату клеткой способности к пролиферации, а выжившими считают клетки, сохранившие способность к неограниченному размножению.
В зависимости от связи летального эффекта с процессом деления различают две основные формы радиационной гибели клеток: интерфазную (до деления клетки или без него) и репродуктивную (после первого или нескольких последующих циклов деления). Для большинства клеток, в т.ч. и для клеток многих млекопитающих, характерна репродуктивная форма лучевой гибели, основной причиной которой являются структурные повреждения хромосом, возникающие в процессе облучения. Они обнаруживаются с помощью цитогенетических методов исследования на разных стадиях митоза (чаще в анафазе или метафазе) в виде так называемые хромосомных перестроек, или аберраций. Гибель таких аберрантных клеток или их потомков происходит вследствие неравномерного разделения или частичной утраты жизненно необходимого генетического материала из-за неправильного соединения разорванных хромосом или отрыва их фрагментов. Определение доли клеток с хромосомными аберрациями часто используют в качестве надежного количественного показателя радиочувствительности, т.к. с одной стороны, число таких поврежденных клеток четко зависит от дозы ионизирующего излучения, а с другой -- отражая его летальное действие, этот критерий хорошо коррелирует с количеством погибающих клеток, оцениваемым по снижению способности к клонообразованию.
Интерфазная гибель клетки наступает до вступления в митоз, и для большинства клеток такая гибель возможна лишь при очень больших дозах. Однако для некоторых клеток, например малодифференцированных кроветворных элементов и лимфоцитов, интерфазная гибель происходит уже при относительно низких дозах облучения. Клетки, погибающие таким путем, могут быть выявлены через 2--6 ч после облучения с помощью обычных цитологических методов исследования по различным изменениям (чаще по пикнозу ядра и фрагментации хроматина). Подсчет таких клеток также используют в качестве количественного показателя степени лучевого поражения.
Молекулярным субстратом, ответственным за гибель клетки, являются ДНК и ее комплексы с белками и ядерной мембраной. Разработаны молекулярно-биологические методы количественной оценки повреждения ДНК, используемые при изучении механизмов лучевого поражения клеток и восстановления их жизнеспособности. Последнее обусловлено явлением репарации ДНК, осуществляемой специальной системой ферментов. Эффективность репарации ДНК, по современным представлениям, имеет определяющее значение в клеточной радиочувствительности.
Закономерности реакций клеток на облучение сохраняются и при облучении организма, суммарная радиочувствительность которого определяется радиочувствительностью тканей, органов и систем, непосредственно подвергающихся облучению. Однако тканевую, а тем более органную и системную Р. нельзя рассматривать как простую сумму клеточных эффектов. На тканевую радиочувствительность большое влияние оказывают дополнительные факторы: кровоснабжение, объем облучаемых тканей, гомеостатический контроль регулирующих систем. Все это усложняет оценку тканевой радиочувствительности, но не отвергает принципиального и ведущего значения цитокинетических параметров, определяющих тип и меру лучевых реакций на всех уровнях биологической организации. Именно цитокинетическая характеристика, а точнее пролиферативная активность кроветворной системы, эпителия слизистой оболочки кишечника и клеток половых желез (типичных систем клеточного обновления) является причиной их высокой радиочувствительности. Напротив, низкий темп физиологической регенерации или ее отсутствие, свойственные костной, мышечной и нервной системе, а также печени, обусловливает их относительную радиорезистентность.
Таким образом, известно, что дозы излучения, приводящие к заболеванию или смерти различных организмов, различны. Т.е. можно сказать, что каждому биологическому виду свойственна своя мера чувствительности к действию ионизирующей радиации, своя радиочувствительность. Примером крайне низкой радиочувствительности служат бактерии, обнаруженные в канале ядерного реактора. В этих условиях бактерии не только не погибали, но и размножались.
В качестве интегрального критерия радиочувствительности наиболее часто используют величину ЛД50 (летальная доза) - доза, облучение в которой вызывает 50%-ную гибель биообъектов. Величины ЛД50 в природе различаются довольно значительно даже в пределах одного вида. Кроме того, даже в одном организме различные ткани и клетки значительно различаются порадиочувствительности, и наряду с чувствительными (костный мозг, лимфоидная ткань, эпителий слизистой тонкого кишечника) имеются относительно устойчивые ткани (мышечная, нервная, костная). Величина радиочувствительности подчиняется следующему закону: чувствительность клеток к излучению прямо зависит от их способности к размножению в данный момент времени.
1. Проблема радиочувствительности – центральная проблема радиобиологии и радиационной медицины.
2. Молекулярные основы радиочувствительности. Факторы, определяющие радиочувствительность на клеточном уровне.
3. Факторы, определяющие радиочувствительность на тканевом уровне. Правило Бергонье-Трибондо. Факторы, определяющие радиочувствительность на органном, организменном и популяционном уровнях.
4. Индивидуальные и возрастные различия в радиочувствительности. Действие радиации на эмбрион и плод.
5.Модификация радиочувствительности.
7. Радиационные синдромы: костномозговой, желудочно-кишечный, церебральный, зависимость от дозы.
8. Характеристика костномозгового синдрома: патогенез, фазы, причины гибели организма.
9. Характеристика желудочно-кишечного синдрома: патогенез, причины гибели организма.
10. Характеристика церебрального синдрома: патогенез, причины гибели организма.
При общем облучении практически ни одна живая клетка не остается интактной. Любая из них, а следовательно, и любая ткань в целом могут быть поражены ИИ. Однако для достижения равнозначного поражающего эффекта различные ткани необходимо подвергнуть воздействию неодинаковыми дозами. И эти различия могут быть очень значительными. Другими словами, каждому виду клеток и тканей свойственна своя, определенная мера радиопоражаемости (радиочувствительности).
Проблема радиочувствительности занимает центральное место в радиобиологии и радиационной медицине. Познание природы радиочувствительности и механизмов ее регуляции имеет как теоретическое, так и практическое значение, т.к. позволяет разрабатывать методы управления лучевыми реакциями тканей.
2. Радиочувствительность: понятие, виды, биологические механизмы
Радиочувствительность - это чувствительность биологических объектов к действию ИИ. Синонимом данного понятия служит радиопоражаемость.
Альтернативными понятиями являются радиоустойчивость или радиорезистентность.
При сравнении радиочувствительности различных биосистем необходимо использовать адекватные критерии, в качестве которых можно использовать либо непосредственное изменение выживаемости изучаемых объектов в результате облучения в определенных дозах, либо количественные показатели поражения, которые в данном диапазоне доз связаны с выживаемостью. Наиболее часто в качестве меры радиочувствительности используется ЛД 450 0 - доза облучения, вызывающая гибель 50% облученных организмов за различное время после облучения (в зависимости от вида живых организмов).
Различные виды живых организмов существенно различаются по своей радиочувствительности, о чем можно судить, сравнив величины ЛД 450 (табл.1). Степень чувствительности сильно варьирует в пределах одного вида (индивидуальная радиочувствительность), в пределах одного организма клетки и ткани также значительно различаются по своей радиочувствительности.
Следовательно, чтобы правильно оценить последствия облучения организма человека, необходимо оценить радиочувствительность на различных уровнях - клеточном, тканевом, органном, организменном.
На КЛЕТОЧНОМ уровне радиочувствительность зависит от ряда факторов:
1) величина и организация генома (в т.ч. кариопикнотический индекс);
2) состояние системы репарации ДНК;
3) содержание в клетке антиоксидантов;
4) активность ферментов, утилизирующих продукты радиолиза воды (каталаза - разрушает перекись водорода, супероксиддисмутаза - инактивирует супероксидный радикал);
5) интенсивность окислительно-восстановительных процессов.
Диапазоны радиочувствительности различных организмов
На ТКАНЕВОМ уровне работает правило Бергонье-Трибондо: радиочувствительность ткани прямо пропорциональна пролиферативной активности и обратно пропорциональна степени дифференцировки составляющих ее клеток.
Следовательно, наиболее радиочувствительными в организме будут ткани, имеющие резерв активно размножающихся малодифференцированных клеток, а именно: - кроветворная ткань;
- эпителий тонкого кишечника.
Наименее радиочувствительными будут высокоспециализированные малообновляющиеся ткани, например, мышечная, костная, нервная.
Есть исключение из правила Бергонье-Трибондо - лимфоциты. Эти высоко специализированные клетки отличаются высокой радиочувствительностью.
На ОРГАННОМ уровне радиочувствительность зависит от чувствительности отдельных органов и тканей.
1) половые железы
Семенники: в них постоянно идёт размножение сперматогониев, которые обладают высокой радиочувствительностью, напротив, сперматозоиды (зрелые клетки) являются более радиорезистентны. Уже при дозах свыше 0.15 Гр происходит клеточное опустошение семенников. В дозах >3.5 Гр возникает постоянная стерильность. При этом не следует смешивать радиационную стерильность с половой потенцией, на которую облучение не оказывает видимого влияния.
Яичники: в яичниках взрослой женщины содержится популяция незаменяемых овоцитов (их образование заканчивается в ранние сроки после рождения, во взрослом состоянии яичники не способны к активной регенерации). Развитие однократного облучения в дозе 1-2 Гр на оба яичника вызывает временное бесплодие и прекращение менструаций на 1-3 года. Гибель овоцитов при дозах >2.5 Гр может привести к стойкому бесплодию.
2) органы пищеварения
Наибольшей радиочувствительностью обладает тонкий кишечник. Далее по снижению радиочувствительности следуют полость рта, язык, слюнные железы, пищевод, желудок, прямая и ободочная кишки, поджелудочная железа, печень.
3) сердечно-сосудистая система
В сосудах большей радиочувствительностью обладает наружный слой сосудистой стенки (высокое содержание коллагена).
Сердце считается радиорезистентным органом, однако при локальном облучении в дозах 5-10 Гр можно обнаружить изменения миокарда, при дозе 20 Гр отмечается поражение эндокарда.
4) органы дыхания
Лёгкие взрослого человека достаточно радиорезистенты (низкая пролиферативная активность). Однако при локальном облучении в больших дозах может развиться радиационный пневмонит (это часто лимитирует лучевую терапию).
5) органы выделения
Почки достаточно радиорезистентны. Однако облучение почек в дозах >30 Гр за 5 нед может привести к развитию хронического нефрита (это может быть лимитирующим фактором при проведении лучевой терапии опухолей органов брюшной полости).
Возможны 2 типа поражений глаз:
- воспалительные процессы в конъюнктиве и склере ( при дозах 3-8 Гр);
- катаракта (при дозах 3-10 Гр).У человека катаракта появляется при облучении в дозе 6 Гр.
Радиорезистентна. Клеточная гибель наблюдается при дозах свыше 100 Гр. Это высоко специализированная ткань человека.
8) эндокринная система. Основной характеристикой ее является относительная радиорезистентность.
9) кости, сухожилия
В период роста обладают большей радиочувствительностью, во взрослом состоянии радиорезистентны.
На ПОПУЛЯЦИОННОМ уровне радиочувствительность зависит от следующих факторов:
1) особенности генотипа (а значит и фенотипические особенности);
В человеческой популяции 10 - 12% людей отличаются повышенной радиочувствительностью. Связано это с наследственно сниженной способностью к ликвидации разрывов ДНК, а также со сниженной точностью процесса репарации. Повышенная радиочувствительность сопровождает такие наследственные заболевания, как атаксия-телеангиэктазия, пигментная ксеродерма.
2) физиологическое (напр., сон, бодрость, усталость, беременность)
или патофизиологическое состояние организма;
3) пол (более чувствительны мужчины, у мужчин обмен интенсивнее);
4) возраст (наименее чувствительным является зрелый возраст);
Особо следует остановиться на особенностях радиочувствительности во внутриутробном периоде. Радиочувствительность плода тем выше, чем он моложе. В зависимости от времени закладки, формирования и дифференцировки органов и систем любая из них может оказаться крайне радиочувствительной независимо от радиочувствительности во взрослом состоянии.
Эффекты облучения зависят от времени облучения по отношению к зачатию:
1 - преимплантационный период ( до 6-9 сут.) - в морфологическом плане соблюдается принцип "все или ничего", т.е. если доза была высокой, то оплодотворенная яйцеклетка гибнет; если поглощенная доза не вызвала гибель яйцеклетки, то дальше она имплантируется и развивается нормально;
2 - период органогенеза ( до 60 сут.) - эффект зависит от величины поглощенной дозы и ее мощности, от срока от начала беременности.
Возможны следующие эффекты:
- внутриутробная гибель или гибель сразу после рождения;
- задержка развития зародыша, плода, а затем и новорожденного;
- пороки развития. Существуют критические периоды - время максимальной радиочувствительности для возникновения специфического типа аномалий. С увеличением D критический период индукции специфических аномалий удлиняется. Эти эффекты носят детерминированный характер с порогом для человека около 0.1 Гр;
3 - плодный период -
- снижение коэффициента умственного развития (максимальное снижение коэффициента умственного развития происходит при облучении в период с 8 по 15 нед., это детерминированный эффект);
- увеличение опасности заболевания детей раком, особенно в первые 10 лет жизни (радиочувствительность плода по индукции отдаленных последствий облучения в 10-300 раз больше, чем у взрослого организма);
- лучевая болезнь плода, а затем и новорожденного - если облучение произошло после 7 месяца беременности.
На ЭВОЛЮЦИОННОМ уровне радиочувствительность зависит от сложности организации живого организма. Наименее радиочувствительными являются бактерии, для которых показатель ЛД 50 составляет 1000- 3000 Гр (в канале ядерного реактора обнаружены бактерии, названные Micrococcus radiodurens, которые живут при дозах 100 000 Гр в сутки). Наиболее радиочувствительными являются человек (2,5-3 Гр), овцы (1,5-2 Гр), собаки (2,5-3 Гр), обезьяны ( 2,5- 4 Гр).
Радиочувствительность — это ответ опухоли на облучение, который измеряется степенью регрессии, скоростью ее наступления и длительностью. Радиочувствительность зависит от ряда факторов: способности клеток устранять повреждение, гипоксии, периода клеточного цикла и доли растущих клеток. Кроме того, возможность ликвидации опухоли определяется ее начальным объемом.
Прекрасный пример относительно радиорезистентного новообразования — плоскоклеточный рак шейки матки (РШМ). Эта опухоль остается одной из самых излечиваемых, что объясняется возможностью подведения к ней высоких доз излучения и ее происхождением из тканей, которые также относительно радиорезистентны. Ключ к успешному лечению — хорошие условия для расположения радия или цезия в непосредственной близости к опухоли без превышения дозы на окружающие нормальные ткани выше переносимой.
Множество попыток было предпринято, чтобы найти способ определения радиочувствительности опухоли. Однако в настоящее время не существует надежного метода прогнозирования результата лечения данной конкретной опухоли. Не исключено, что опухоли состоят из нескольких популяций клеток с различной чувствительностью к XT и ЛТ. Чувствительные клетки погибают, а резистентные — продолжают расти. Это объясняет, почему вначале ответившие на лечение опухоли в конечном счете не излечиваются.
Для прогнозирования и изучения радиочувствительности опухолевых клеток разработаны модели in vitro. Клеточная радиочувствительность определяется в основном потерей репродуктивной способности, которую показывает кривая выживаемости, характеризующаяся начальным наклоном а и конечным b, причем а отражает невосстановимые повреждения клетки, а b — восстановимые. Отношение а/b — доза, при которой вклад от а эквивалентен вкладу от и, и есть показатель радиочувствительности.
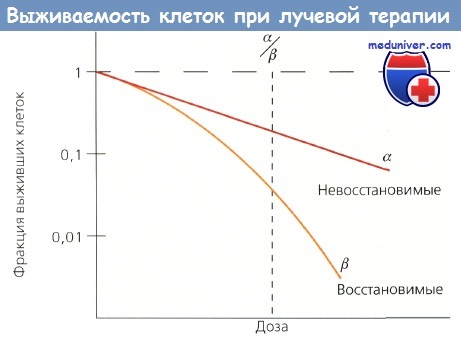
Кривая выживаемости клеток.
Начальный наклон (а) отражает невосстановимые повреждения, а конечный наклон (b) - восстановимые.
Отношение а/b — это точка на кривой, где два значения равны
Большие значения отношения характерны для быстроделящихся клеток, они помогают предсказать ответ опухолей и оценить раннюю эффективность облучения. Низкие значения характеризуют поздно реагирующие ткани.
Размер плеча кривой выживаемости дает важную информацию, т. к. отражает величину репарации сублетальных повреждений. Широкие плечи имеют низкие отношения а/b и хорошую репарацию сублетальных повреждений, которая занимает 2—6 ч. Способность клеток восстанавливать сублетальные повреждения служит основанием для фракционирования дозы ЛТ, при котором используются различия между способностью нормальных и опухолевых тканей к репарации.
Различная способность к репарации также служит основой для ускоренного фракционирования и гиперфракционирования, при которых доза подводится 2 раза в день. Такой подход дает хорошие результаты при быстро растущих опухолях. Лечение 2 раза в сутки оставляет достаточный срок нормальным тканям для репарации, тогда как опухолевые, менее организованные ткани погибают в силу нехватки времени для восстановления.
Некоторые клетки почти не имеют плеча на графике, что говорит об их ограниченной способности к репарации сублетальных повреждений; эти клетки погибают от относительно небольших доз радиации. Например, дисгерминомы излечиваются сравнительно невысокими дозами облучения (20—30 Гр) по сравнению с опухолями шейки матки, к которым необходимо подвести более 70 Гр для получения полного эффекта.
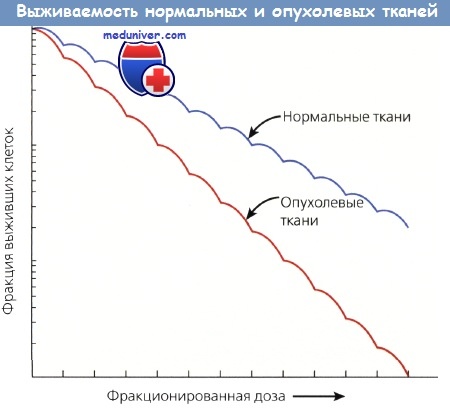
Различная выживаемость нормальных и опухолевых тканей зависит от разной их способности накапливать и репа-рировать сублетальные повреждения, полученные от фракционированных доз.
Нормальные ткани восстанавливаются быстрее и эффективнее
Способность кислорода усиливать излучение, или коэффициент кислородного усиления, вычисляется как отношение дозы излучения, производящей определенный эффект без кислорода, к дозе, дающей тот же эффект, но в присутствии кислорода. Для наблюдения полного кислородного эффекта необходимо наличие по крайней мере 2 % (17 мм рт. ст.) тканевого кислорода.
Способность опухолевых клеток к росту потенциально не ограничена, но практически зависит от поступающих с кровью питательных веществ. Известно, что любая опухоль размером более 200 мкм имеет некроз в центре вследствие ограниченной способности кислорода диффундировать на большие расстояния. Кислород легко проникает на 70 мкм от кровеносного сосуда.
Клетки, располагающиеся дальше этого расстояния, страдают от нехватки кислорода и переходят в фазу покоя. В них может развиться гипоксия и даже аноксия и некроз. Это важно с точки зрения радиобиологии, т. к. покоящиеся клетки проявляют более выраженную способность к восстановлению радиационных повреждений. Клетки в состоянии гипоксии более резистентны к облучению, чем нормально оксигенированные. Таким образом, большие опухоли труднее излечить с помощью ЛТ не только из-за большего числа составляющих их клеток, но и вследствие нахождения в них гипоксических, покоящихся и радиорезистентных клеток.
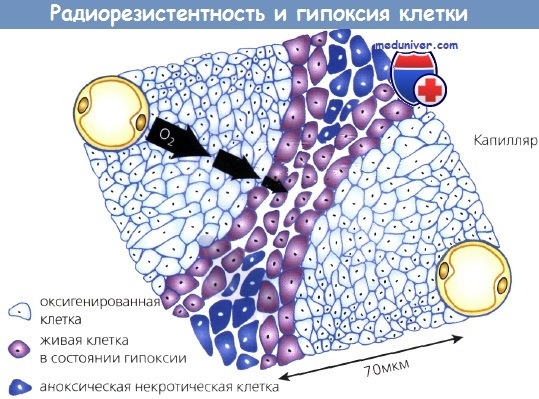
С увеличением расстояния от кровеносных сосудов клетки находятся в состоянии гипоксии и даже аноксии.
Гипоксические клетки более радиорезистентны и поэтому труднее поддаются лечению.
Кислород диффундирует примерно на 70 мкм от капилляров.
Клинический пример: замечено, что экзофитные рыхлые опухоли шейки матки, легко кровоточащие при контакте, лучше и быстрее отвечают на облучение, чем инфильтративные формы. Кровоснабжение и оксигенация этих двух видов новообразований значительно отличаются: рыхлая опухоль лучше васкуляризована и, следовательно, оксигенирована, поэтому ее радиочувствительность выше. К сожалению, к настоящему времени попытки преодолеть такое существенное различие в чувствительности к облучению с помощью гипербарической оксигенации и радиосенсибилизации не дали ожидаемых результатов.
Другим важным фактором, влияющим на радиочувствительность, служит содержание в опухоли митотических, или клоногенных, клеток. Размножающиеся клетки более чувствительны к облучению. Число митозов коррелирует с прогнозом лечения при многих опухолях. Фаза клеточного цикла тоже имеет большое значение. Клетки в поздней G2 и митотической (М) фазах наиболее чувствительны к облучению, а в поздней синтетической фазе (S) — наиболее резистентны. Это учитывается при совместном применении ЛТ и XT. Так, например, паклитаксел задерживает клетки в фазе митоза и, следовательно, выступает в роли чрезвычайно сильного радиосенсибилизатора.
От первоначального объема опухоли в значительной степени зависит возможность излечения: чем меньше объем, тем меньшая доза облучения требуется для уничтожения всехзлокачественных клеток и наоборот, при большем объеме доза, необходимая для исчезновения опухоли, возрастает. Принцип лечения сокращающимися полями заключается в последовательном уменьшении размера полей облучения с тем, чтобы подвести наибольшую дозу на центральную часть опухоли, где предположительно находятся наиболее радиорезистентные клетки в состоянии гипоксии.
В течение длительного времени клиницисты предпринимали попытки установить взаимосвязь между ответом опухоли на облучение и частотой местного рецидивировапия. В целом, чем полнее ответ опухоли к окончанию лечения и чем скорее он наступает, тем дольше период ремиссии, т. к. можно предположить, что отдаленные метастазы не появятся. Хотя эта зависимость не универсальна, при РШМ показана устойчивая корреляция между длительностью ремиссии и степенью резорбции опухоли к концу курса облучения — частичной или полной регрессией.

Grigsby установил взаимосвязь между выживаемостью и ответом опухоли к окончанию лечения, который он определял с помощью ПЭТ, основанной на измерении метаболизма глюкозы.
Другой фактор, ограничивающий излечиваемость с помощью лучевой терапии (ЛТ), — увеличение побочных эффектов со стороны нормальных тканей, связанное с повышением дозы. Появление этих осложнений зависит от суммарной дозы и дозы за фракцию, объема облученных тканей и их радиочувствительности. Цель любой терапии — достижение излечения с минимальным количеством побочных эффектов. Комбинирование ЛТ с хирургическим лечением или XT снижает толерантность нормальных тканей к облучению.
Установлены и хорошо обоснованы размеры полей, суммарные дозы и схемы фракционирования, но они не могут оставаться неизменными. Продолжают исследовать различные методы повышения процента выздоровления и снижения осложнений; для этого используют новые химиотерапевтические радиосенсибилизаторы, а также технические достижения в подведении излучения, такие как ЛТМИ и радиопротекторы, подобные этиолу.
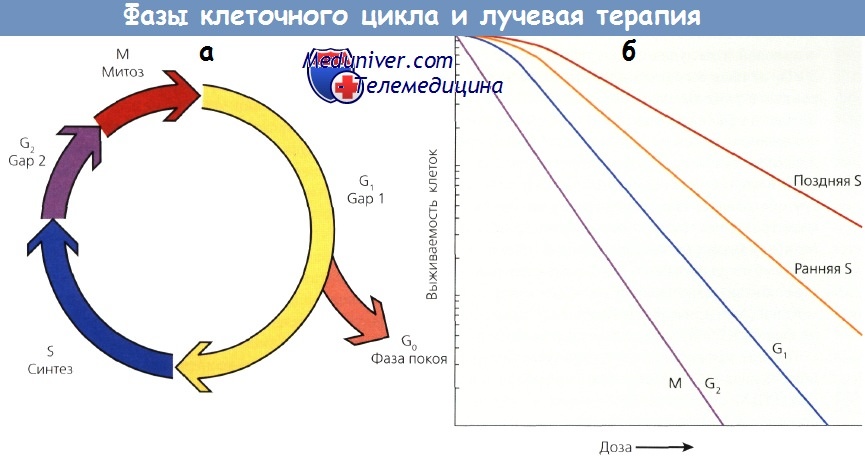
а - клеточный цикл
б - кривая выживаемости клеток в митозе и фазе G2 более крутая и не имеет плеча.
Кривая для клеток в поздней S-фазе более пологая и имеет большое плечо.
Фазы G1 и ранняя S характеризуются промежуточной чувствительностью.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:
- Правовые аспекты нюрнбергского процесса и нравственные итоги второй мировой войны реферат
- Построение отчетов по центрам затрат и центрам прибыли реферат
- Обеспечение безопасности при проведении спортивных мероприятий реферат
- Виды приемов и банкетов реферат
- Аллергены канцерогены и отдаленные последствия их влияния на организм человека реферат

