Первичный склерозирующий холангит реферат
Обновлено: 02.07.2024
Первичный склерозирующий холангит (ПСХ) — редкое аутоиммунное заболевание печени, которое без какого-либо эффективного лечения, модифицирующего заболевание, приводит к высокой заболеваемости, смертности и высокому риску развития гепатобилиарного рака и рака толстой кишки. К сожалению, болезнь встречается все чаще, поражая в т.ч. пациентов без вредных привычек, поэтому при любых неприятных симптомах со стороны ЖКТ нужно обращаться к гастроэнтерологу и проходить обследование.
Пациентам с подозрением на эту патологию назначается широкий спектр анализов и тестов. Это связано с тем, что диагностика и оценка риска прогрессирования заболевания затруднены, поскольку оно часто бывает непредсказуемым, а во многих случаях сопровождается осложнениями — сопутствующим воспалительным заболеванием кишечника (ВЗК). Поэтому очень важно пройти обследование до конца и исключить или подтвердить диагноз.
Диагностика первичного склерозирующего холангита
ПСХ — хроническое аутоиммунное заболевание, характеризующееся прогрессирующим холестазом, воспалением и фиброзом. Поражения при первичном склерозирующем холангите обнаруживаются во внутрипеченочных и внепеченочных желчных протоках. ПСХ связан с высоким риском злокачественного образования множественных стриктур желчных путей, что приводит к осложнениям, циррозу печени и хронической печеночной недостаточности.
Патогенез первичного склерозирующего холангита сложен — на него влияют экологические и генетические факторы, сочетание иммунной дисрегуляции, нарушения кишечной микробиоты и нарушения гомеостаза желчи.
Заболевание диагностируется в клинических исследованиях с холестазом (без объяснения других причин) продолжительностью >6 месяцев и характерными изменениями, выявляемыми на магнитно-резонансной холангиопанкреатографии или после биопсии печени.
Таблица 1. Эпидемиология и клиника ПСХ
До 16,2 на 100000;
60% пациентов — мужчины;
Средний возраст 30-40 лет.
Зуд, боль в правом верхнем углу живота, усталость, лихорадка и озноб, рецидивирующий холангит
Биохимия, серология, методы визуализации, биопсия печени
Вторичный склерозирующий холангит;
Наследственные холестазные заболевания (например, дефицит ABCB4).
Около 80% пациентов с сопутствующим воспалением кишечника.
Выраженность симптомов не коррелирует с тяжестью печеночной дисфункции, биохимическими исследованиями, методами визуализации или риском злокачественного новообразования.
У 50% диагностируется ранняя бессимптомная стадия.
Холестаз (повышены щелочная фосфатаза, гамма-глутамилтранспептидаза, билирубин);
Дисфункция печени при запущенном заболевании паренхимы.
АСТ, АЛТ часто повышены в 2-3 раза;
У 60% больных IgG увеличен в 1,5 раза.
Проверяются подклассы IgG. исключение IgG4.
МРХ — тест первого выбора для выявления стриктур желчных протоков.
Биопсия печени полезна, когда результат МРХ нормален или вызывает сомнения.
У большинства пациентов с первичным склерозирующим холангитом имеются как внутрипеченочные, так и внепеченочные желчные протоки.
Изолированная стриктура большого желчного протока обнаруживается у
Менее 25% пациентов имеют изолированное внутрипеченочное заболевание, называемое ПСХ малого протока, которое может быть диагностировано как хронический холестаз, но показывает нормальный результат МРТ, а биопсия печени характерна для диагноза ПСХ ± сопутствующее воспаление кишечника. Диагностические критерии ПСХ малого протока должны основываться, прежде всего, на характерной гистологии. Прогноз при этой форме заболевания лучше.
У всех пациентов должны быть исключены заболевания, связанные с IgG4. Требуются IgG4 и визуализирующие исследования.
Особенности диагностики и лечения ПСХ
При лечении заболевания гастроэнтеролог делает упор на контроль симптомов — зуд, боль, лечение холангита и отслеживание возможных осложнений. У большинства пациентов заболевание в конечном итоге прогрессирует до фиброза и цирроза печени, поэтому важно своевременно включить таких больных в список трансплантатов печени.
Ортотопическая трансплантация печени обычно выполняется из-за запущенного паренхиматозного заболевания печени или частого рецидивирующего холангита. Средняя 10-летняя выживаемость пациентов составляет 80%. На эту патологию приходится около 10% всех трансплантатов печени в мире. В пересаженной печени ПСХ восстанавливается в 30% случаев в течение первых 5 лет.
Иммунодепрессанты при лечении ПСХ не используются, если совпадение с аутоиммунным гепатитом не подтверждено гистологическим исследованием.
Урсодезоксихолевая кислота — один из двух препаратов, лицензированных для лечения первичного билиарного цирроза (PBC), но лечение этим препаратом первичного склерозирующего холангита остается спорным. В клинических испытаниях не было продемонстрировано статистически значимого улучшения фиброза или симптомов, но было отмечено улучшение результатов биохимического анализа.
Также нет данных, подтверждающих эффективность урсодезоксихолевой кислоты в химиопрофилактике рака.
Лечение холангита
Рецидивирующий холангит — частое осложнение ПСХ. При этом состоянии лихорадка и повышенная частота воспаления крови не всегда выявляются, но внезапное усиление зуда или ухудшение биохимических тестов в ответ на лечение антибиотиками при холангите с ПСХ возникает очень часто.
Холангит можно лечить в амбулаторных условиях короткими интермиттирующими курсами соответствующих антибиотиков, например, ципрофлоксацина. Правда, иногда требуются короткие курсы в нутривенного введения антибиотиков .
Пациенты с рецидивирующим холангитом несколько раз в год получают длительное профилактическое лечение низкими дозами антибиотиков. Но долгосрочные преимущества этого лечения в испытаниях не были продемонстрированы.
Пациентам с рецидивирующими эпизодами тяжелого холангита может выполняться трансплантация печени независимо от степени нарушения функции печени.
Рецидивирующий холангит является естественным течением заболевания, поэтому следует рассмотреть вопрос о вмешательстве в желчевыводящие пути, взвесив преимущества и риски. Эндоскопическая ретроградная холангиопанкреатография может быть полезной при лечении доминантной стриктуры желчных протоков, поставленной на основании холангиографии, когда стриктуры преобладают при стенозе общего желчного протока (BTL)
Во время ЭРХП может быть выполнено временное стентирование пластиковыми стентами или баллонная дилатация.
Лечение сопутствующего воспаления кишечника и риск развития рака толстой кишки
Первичный склерозирующий холангит, сопровождающийся ВК, отличается от классического язвенного колита или болезни Крона. Кишечные симптомы часто слабо выражены или отсутствуют.
Всем пациентам с ПСХ рекомендуется колоноскопия и сегментарная биопсия . Эти исследования очень важны для прогноза, так как риск рака толстой кишки у таких больных очень высок — 20-30% через 20 лет, тогда как при классическом язвенном колите без PSC, он возникает у 5% больных. Колоноскопию следует проводить ежегодно у всех пациентов с ПСХ и воспалением кишечника. Важен хороший контроль активности заживление слизистой.
Ежегодная колоноскопия должна продолжаться даже после трансплантации печени. Важно обратить внимание на обострения.
Риск гепатобилиарного рака

Риск гепатобилиарного рака
Пациенты с ПСХ имеют высокий риск развития гепатобилиарного рака, аденокарциномы желчного пузыря и гепатоцеллюлярной карциномы (ГЦК). Риск развития ГБА составляет 10-15%, треть из которых диагностируется в течение 12 месяцев после постановки диагноза ПСХ.
Рак от ПСХ отличить трудно, можно заподозрить любую доминирующую стриктуру или изменения в биохимических исследованиях и исследованиях с помощью изображений. Пока невозможно предсказать, какие пациенты подвержены наибольшему риску (не коррелирует с тяжестью симптомов или паренхиматозным заболеванием).
Наиболее часто используемый методом для дифференциации рака от доминантной стриктуры — щеточная биопсия, выполняемая во время ЭРХПГ, но диагностический потенциал этого метода относительно невелик, и результирующий отрицательный цитологический анализ не исключает возможности рака этого типа.
В настоящее время разрабатываются новые технологии ,гибридизация in situ, анализ цифровых изображений или прямая визуализация желчных протоков с помощью цифровой холангиоскопии. При этом известно, что раковый маркер Ca19.9 может быть повышен как при первичном склерозирующем холангите, так и при раковом поражении, что приводит к ограниченному диагностическому потенциалу.
Регулярный мониторинг возможного развития гепатобилиарного рака, основанный на доказательствах эффективности Ca19.9, не рекомендуется. В случае подозрения на рак диагностика должна состоять из неинвазивных методов визуализации, Ca19.9 и ERCP (и взятия образцов).
Рак желчного пузыря диагностируется у 2% пациентов с ПСХ (50% аденокарциномы). Больным рекомендуется проводить ежегодно УЗИ брюшной полости, а при обнаружении полипов желчного пузыря — холецистэктомию .
Пациентам, у которых уже развился цирроз печени, УЗИ брюшной полости следует проводить каждые 6 месяцев.
Новые методы лечения, клинические испытания и прогноз
ПСХ — редкое заболевание, которое не требует лечения, модифицирующего болезнь, и не имеет проверенных методов оценки риска. Среднее время от постановки диагноза до трансплантации печени или смерти составляет от 13 до 21 года.
Пациентов с высоким риском прогрессирования заболевания (судя по активному биохимическому холестазу) следует поощрять к участию в клинических испытаниях. Последние доступные методы лечения, проходящие клинические испытания: ванкомицин, моноклональные антитела против лизилоксидазы 2, обетихолевая кислота и другие.
Склерозирующий холангит – редкое хроническое заболевание желчных протоков, вызывающее нарушение оттока желчи, ее застой и повреждение клеток печени с дальнейшим развитием печеночной недостаточности. Патология длительно протекает без клинических проявлений. Основные симптомы: боль в области живота, желтуха, зуд, слабость, похудение. Диагностические мероприятия заключаются в проведении анализа крови и кала, УЗИ органов брюшной полости, МРПХГ, ЭРПХГ, биопсии печени. Лечение направлено на купирование симптомов, замедление патологического процесса и восстановление функций. Наибольший эффект дает трансплантация печени.
Общие сведения
Склерозирующий холангит – это воспалительное заболевание внутрипеченочных и внепеченочных желчных протоков, характеризующееся их склерозированием (рубцеванием) и нарушением оттока желчи. Сопровождается формированием цирроза печени, портальной гипертензии и печеночной недостаточности. Склерозирующий холангит встречается с частотой 1-4:100 000, хотя достаточно трудно судить о распространенности патологии, поскольку она длительно протекает бессимптомно. Кроме того, в большинстве случаев (до 80%) заболеванию сопутствует хроническая патология желудочно-кишечного тракта (язвенный колит, болезнь Крона и т. п.), признаки которой выступают на первый план. Именно это приводит к прогрессированию патологического процесса, нарастанию неблагоприятных симптомов и осложнений. Согласно статистике, заболеваемости склерозирующим холангитом подвержены мужчины в возрасте от 25 до 40 лет и женщины более старшего возраста. Не исключается возникновение болезни у детей, хотя в педиатрии ее регистрируют крайне редко.

Причины склерозирующего холангита
Выделяют первичный и вторичный склерозирующий холангиты. Причины возникновения первичного склерозирующего холангита до сих пор неизвестны. Ученые постоянно выдвигают различные гипотезы, но ни одна из них еще не подтверждена на 100%. Важную роль в развитии патологии играет наследственная предрасположенность в сочетании с нарушением работы иммунитета. Эта теория основана на статистических данных, которые зарегистрировали семейные случаи склерозирующего холангита и аутоиммунных заболеваний. Также выдвигается теория о негативном влиянии токсинов, бактерий и вирусов на желчные протоки.
Заболевание может развиться у любого человека, но есть ряд предрасполагающих факторов, повышающих риск появления патологии: возраст (чаще всего болеют люди старше 30 лет), пол (от заболевания в большей степени страдают мужчины), наличие болезни у родственников.
Вторичный склерозирующий холангит хорошо изучен, причинами его формирования могут быть токсическое повреждение протоков, тромбоз и нарушение работы печеночной артерии, постоперационные осложнения, камни в желчных путях, аномалии развития, цитомегаловирус и криптоспоридиоз при СПИДе, некоторые лекарственные препараты, холангиокарцинома.
Независимо от причин возникновения, патология вызывает нарушение работы желчных протоков и печеночную недостаточность. Воспаление желчных протоков приводит к тому, что они замещаются рубцовой тканью и спадаются, это ведет к нарушению оттока желчи, ее застою и обратному всасыванию в кровяное русло. Таким образом появляется желтуха. Застой желчи и повышение давления в желчных путях из-за нарушения ее оттока провоцируют необратимые изменения в печеночных клетках и их гибель, что проявляется печеночной недостаточностью.
Симптомы склерозирующего холангита
Длительное время склерозирующий холангит протекает бессимптомно, на ранних этапах заболевание можно заподозрить по нарушениям биохимического анализа крови (определяется изменение активности ферментов). При развитии дисфункции печени и рубцевания желчных путей появляются следующие признаки: боль в области живота, зуд, пожелтение слизистых оболочек, кожи и склеры глаз, повышение температуры тела, слабость и утомляемость, похудение.
Хроническое нарушение оттока желчи обусловливает появление стеатореи (увеличение доли жира в каловых массах), недостатка жирорастворимых витаминов (A , D , E и K), остеопороза. Длительный застой желчи ведет к развитию вторичного цирроза печени, который является причиной портальной гипертензии, асцита и кровотечений. Не исключается образование камней в желчных протоках и их стриктур, еще больше усугубляющих ситуацию. Во время внешнего осмотра гастроэнтеролог обнаруживает желтушность кожных покровов и слизистых, увеличение размеров печени и селезенки, чрезмерную пигментацию кожи.
Диагностика
Для подтверждения диагноза склерозирующего холангита гастроэнтеролог проводит сбор анамнеза и жалоб, внешний осмотр и дополнительные методы исследования: анализ крови, кала, ЭРПХГ, МРПХГ, УЗИ органов брюшной полости, биопсию печени.
Анализ крови позволяет выявить повышенную активность печеночных ферментов (АСТ, АЛТ). Во время анализа испражнений определяется изменение характеристик кала: он может быть светлым, дегтеобразным (из-за кровотечений), липким и жирным.
Также проводится эндоскопическая ретроградная панкреатохолангиография: метод основан на введении рентгеноконтрастного вещества в холедох в месте впадения желчного протока в 12-перстную кишку и дальнейшей рентгенографии, на которой видны сегменты сужения протоков. Магнитно-резонансная панкреатохолангиография (МРПХГ) - более щадящее исследование (в отличие от первого способа), но при этом достаточно информативное. Оно позволяет получить четкое изображение печени и желчных протоков и развивающихся отклонений. УЗИ - менее точный метод диагностики, исследование дает возможность определять размеры печени, а также выявлять поврежденные участки печени и изменения в желчных протоках. Биопсия печени помогает полностью оценить степень выраженности патологии (процессы рубцевания).
Лечение склерозирующего холангита
Лечение склерозирующего холангита направлено на замедление прогрессирования патологии, устранение неблагоприятных симптомов и осложнений. Ликвидировать клинические признаки можно путем назначения диеты (ограничение жиров, увеличение концентрации витаминов и кальция); при развитии гиповитаминозов показано внутривенное введение витаминных препаратов. Снизить кожный зуд можно при помощи урсодезоксихолевой кислоты и антигистаминных средств (хлоропирамин, цетиризин и др.).
При развитии бактериального холангита назначаются антибактериальные препараты (ампициллин, клиндамицин, цефотаксим и т. п.). Облегчить состояние пациентов могут желчесвязывающие средства (холестирамин).
Очень часто прибегают к хирургическим манипуляциям, которые помогают замедлить прогрессирование склерозирующего холангита и улучшить состояние пациентов. При обнаружении стриктур желчных протоков проводят баллонную дилатацию с целью расширения желчных путей; если это невозможно, то показано протезирование протоков или иссечение пораженных участков. Камни в желчных путях удаляют при эндоскопических операциях. Но эффективность этих манипуляций оценивается неоднозначно, так как они могут лишь замедлить прогрессирование болезни, а также нередко вызывают осложнения. Максимально возможные результаты дает трансплантация печени (особенно при циррозе и печеночной недостаточности). В 15-20% после пересадки печени возможно повторное развитие склерозирующего холангита.
Прогноз и профилактика
Прогноз склерозирующего холангита неблагоприятный. Длительность жизни пациентов с момента появления первых признаков патологии составляет приблизительно 10-12 лет. Трансплантация печени – единственный метод лечения, позволяющий вернуть пациентов к нормальной жизни. Согласно статистике, выживаемость больных после пересадки, проведенной на 1-ом году после постановки диагноза, составляет 92,2%, на 2-ом году – 90%, на 5-ом - 86,4%, через 10 лет - 69,8 %.
Специфической профилактики патологии нет. Но можно снизить риск ее появления, если своевременно лечить заболевания желчных путей, желчнокаменную болезнь, воспалительные процессы поджелудочной железы, а также проходить периодические медицинские осмотры в отделении терапии или гастроэнтерологии.
Описаны методы лечения первичного склерозирующего холангита (ПСХ). Исследованы распространенность и спектр внепеченочных проявлений ПСХ, наиболее часты из них – хронические воспалительные заболевания кишечника. Установлено, что ПСХ у детей сопровождается
Mehtods of sclerosing cholangitis treatment have been described. Prevalence and the range of out-hepatic preparations of primary sclerosing cholangitis have been researched including the most frequent - bowels' chronic inflammatory diseases. Primary sclerosing cholangitis of children is more frequently followed by system presentations that of adults.
Первичный склерозирующий холангит (ПСХ) — это хроническое прогрессирующее холестатическое заболевание печени неясной этиологии, характеризующееся негнойным деструктивным воспалением, облитерирующим склерозом и сегментарной дилятацией внутри- и внепеченочных желчных протоков, приводящее к развитию вторичного билиарного цирроза, портальной гипертензии и печеночной недостаточности [1]. Распространенность ПСХ в разных странах отличается. Так, в Северной Европе она составляет 10 на 100 тысяч населения, а в Азии ПСХ встречается в 10–100 раз реже. Болезнь развивается чаще у мужчин (женщины болеют в 1,5–2 раза реже) [2]. Чаще всего заболевание начинается в возрасте 30–40 лет, хотя известны случаи развития ПСХ в детском и пожилом возрасте [3].
В патогенезе ПСХ важная роль принадлежит нарушению иммунной толерантности. Доказательством этого являются обнаружение широкого спектра аутоантител в сыворотке крови таких больных: обнаружены антитела к ДНК, к гладкой мускулатуре, к билиарному эпителию, к тиреопероксидазе, антимитохондриальные антитела и некоторые другие (описано более 25 видов аутоантител у больных ПСХ), а также частое сочетание ПСХ с другими аутоиммунными заболеваниями, которые могут быть рассмотрены как системные проявления ПСХ [4]. Хронические воспалительные заболевания кишечника обнаруживают у 80–90% больных ПСХ, чаще это язвенный колит, реже встречается болезнь Крона с поражением толстой кишки [2, 3]. Реже ПСХ сочетается с аутоиммунным гепатитом, аутоиммунным тиреоидитом, сахарным диабетом 1-го типа, псориазом (до 10% случаев). Описаны отдельные наблюдения развития ревматоидного артрита, системной склеродермии, системной красной волчанки, склерита, увеита у больных ПСХ [5]. Частое сочетание ПСХ и воспалительных заболеваний кишечника легло в основу предположения о триггерной роли бактериальных антигенов в возникновении ПСХ, однако доказать это не удалось [2]. У родственников больных ПСХ в 11,5 раз повышен риск развития ПСХ, в 3 раза — язвенного колита и в 1,4 раза — болезни Крона [6]. Было сделано предположение о ключевой роли некоторых генов в развитии ПСХ. Были проведены исследования генов HLA-A, HLA-B, HLA-DR, MST1R, NOD2, ATG16L1, однако какого-либо одного гена, специфичного для ПСХ, не было найдено [2].
Препаратом выбора при консервативном лечении ПСХ является урсодезоксихолевая кислота в дозе 20–30 мг/кг/сут (Урсофальк, Урсосан, Урдокса). Урсодезоксихолевая кислота обладает гепатопротективным действием — она образует нетоксичные мицеллы с токсичными желчными кислотами (хенозедоксихолевой, литохолевой), а также включается в состав мембран гепатоцитов и холангиоцитов, увеличивая их стабильность. Это уменьшает степень повреждения клеток печени токсичными желчными кислотами. Урсодезоксихолевая кислота обладает свойствами иммуномодулятора, угнетая экспрессию HLA-антигенов на мембранах гепатоцитов и холангиоцитов. Кроме того, препарат уменьшает литогенность желчи за счет уменьшения абсорбции холестерина в кишечнике, а также стимулирует холерез, что увеличивает выведение желчных кислот через кишечник [2, 3]. При неэффективности монотерапии урсодезоксихолевой кислотой к терапии добавляют фибраты, которые способствуют уменьшению холестаза [2].
Получены данные о том, что лактулоза (Дюфалак, Нормазе) в дозе 15–45 мл/сут обладает гепатопротективным действием, которое может реализовываться посредством нескольких механизмов: 1) ингибирование продукции аммиака и других ксенобиотиков; 2) утилизация образовавшегося аммиака; 3) нарушение всасывания и быстрое выведение аммиака с калом [7, 8]. Уменьшение образования аммиака в кишечнике под действием лактулозы связано с уменьшением количества кишечной микрофлоры, продуцирующей уреазу. Утилизация аммиака происходит при помощи бактерий, использующих азотсодержащие соединения в качестве субстрата для синтеза собственных белков; лактулоза способствует увеличению количества этих микроорганизмов в кишечнике. Кроме того, лактулоза способна связывать молекулы аммиака и увеличивать скорость транзита содержимого по кишечнику, что способствует быстрому выведению аммиака из организма. Лактулоза обладает свойствами пребиотика: под ее воздействием в кишечнике увеличивается количество бифидобактерий и уменьшается количество патогенных бактерий, что предотвращает избыточный бактериальный рост и снижает риск проникновения антигенов патогенных бактерий из кишечника в кровь [14]. Недавно в России было проведено исследование, согласно результатам которого при лечении больных с холестазом урсодезоксихолевой кислотой в комбинации с лактулозой (Урсолив) наблюдается большее уменьшение выраженности холестаза, чем при лечении только урсодезоксихолевой кислотой [9].
Таким образом, совместное применение урсодезоксихолевой кислоты и лактулозы приводит к синергизму гепатопротективного эффекта обоих веществ.
При сочетании ПСХ с аутоиммунным гепатитом к лечению добавляют глюкокортикостероиды и/или иммуносупрессанты в дозах, стандартных для лечения аутоиммунного гепатита [9]. С целью устранения зуда в качестве препарата первой линии применяют Холестирамин (4 г/сут), однако не все пациенты хорошо его переносят: наиболее частыми причинами отказа от препарата являются его вкус, вздутие живота, запоры или диарея. При непереносимости Холестирамина применяют Рифампицин (300 мг/сут), Сертралин (75–100 мг/сут), Налтрексон (50 мг/сут). При выраженном зуде может потребоваться альбуминовый диализ или плазмаферез. Нестерпимый зуд, не купирующийся консервативными методами, может являться самостоятельным показанием к трансплантации печени. Длительный холестаз является фактором риска развития остеопороза, поэтому таким пациентам в схему лечения необходимо включать кальций (1500 мг/сут) и витамин D (1000 МЕ/сут). Витамин K назначается при наличии геморрагического синдрома, особенно перед инвазивными диагностическими процедурами [3, 10].
К хирургическим методам лечения ПСХ относятся установка стентов, резекция пораженных участков желчных протоков, трансплантация печени. Стентирование, баллонная дилятация и резекция пораженных участков протоков лишь временно уменьшают выраженность холестаза, не останавливая прогрессирование ПСХ. Наиболее эффективным хирургическим методом лечения ПСХ является трансплантация печени, которая улучшает выживаемость больных. Однако у 15–20% больных развивается рецидив ПСХ в трансплантате, что ухудшает прогноз таких пациентов [2, 3, 10].
При естественном течении ПСХ часто развивается холангиокарцинома (до 40% больных), повышен риск развития рака поджелудочной железы и колоректального рака, поэтому необходимы как можно более ранние диагностика и лечение этого заболевания [11, 12].
Цель исследования. Изучение распространенности и спектра внепеченочных проявлений первичного склерозирующего холангита.
Материалы и методы. Объектом исследования были 23 больных первичным склерозирующим холангитом, наблюдавшихся в Клинике нефрологии, внутренних и профессиональных заболеваний им. Е. М. Тареева Первого МГМУ им. И. М. Сеченова в период с 1984 по 2010 гг. В группе было 12 мужчин и 11 женщин, средний возраст данной группы составил 36,4 ± 13,7 года, средний возраст начала заболевания 30,6 ± 15 лет, средняя продолжительность заболевания 5,8 ± 5,2 года.
Материалами исследования служили данные из архивных записей в историях болезни и амбулаторных картах. Критерием включения в исследование являлся подтвержденный диагноз ПСХ (морфологически, посредством магнитно-резонансной холангиографии или ретроградной эндоскопической холангиопанкреатографии). Критерием исключения являлось наличие у больного сочетания ПСХ и аутоиммунного гепатита, так как аутоиммунный гепатит также характеризуется широким спектром системных проявлений. Изучалось наличие следующих системных проявлений ПСХ: хронические воспалительные заболевания кишечника (язвенный колит и болезнь Крона), поражение глаз (склерит, кератит), аутоиммунный тиреоидит, синдром Шегрена, геморрагический васкулит.
Результаты и обсуждение. У 16 больных (69,6%) были выявлены внепеченочные проявления ПСХ. Из данных, представленных в табл. 1, видно, что в обследованной группе были выявлены хронические воспалительные заболевания кишечника (язвенный колит и болезнь Крона), синдром Шегрена, геморрагический васкулит, поражение глаз (склерит, кератит), поражение щитовидной железы (аутоиммунный тиреоидит).
У пациентов с сочетанием ПСХ и болезни Крона (5 больных) в 1 случае была поражена только толстая кишка; в 2 случаях — и тонкая, и толстая кишка; в 2 случаях — только тонкая кишка. Отсутствие поражения толстой кишки у двух больных с болезнью Крона при ПСХ указывает на необходимость длительного динамического наблюдения за этими пациентами, так как в дальнейшем у них возможно присоединение поражения толстой кишки.
У 4 больных (17,4%) отмечено сочетание нескольких системных проявлений ПСХ. У 3 больных выявлено два внепеченочных проявления ПСХ (2 случая — язвенный колит в сочетании с аутоиммунным тиреоидитом, 1 случай — язвенный колит в сочетании с геморрагическим васкулитом). У 1 пациента выявлено три внепеченочных проявления ПСХ — язвенный колит в сочетании с геморрагическим васкулитом и поражением глаз (склерит, кератит).
В связи с повышенным риском развития онкологических заболеваний у больных ПСХ мы изучили распространенность злокачественных заболеваний в изучаемой группе больных. Онкологические заболевания были выявлены у 3 больных (13%): 1 случай (пациент с ПСХ в сочетании с болезнью Крона) — лимфома с поражением тонкой кишки, выявлена одновременно с подтверждением диагноза ПСХ; 1 случай (больная с ПСХ без системных проявлений) — лимфома с поражением печени, лимфатических узлов ворот печени, забрюшинных лимфатических узлов, выявлена одновременно с подтверждением диагноза ПСХ; 1 случай (пациентка с ПСХ в сочетании с язвенным колитом) — аденокарцинома толстой кишки, выявлена через 13 лет после подтверждения диагноза ПСХ. В связи с частым развитием злокачественных опухолей у больных ПСХ необходима постоянная онкологическая настороженность врачей, работающих с этой категорией больных.
Также мы проанализировали распространенность системных проявлений ПСХ в зависимости от пола больных и возраста первых проявлений ПСХ (табл. 2 и 3).
С целью изучения связи частоты обнаружения системных проявлений ПСХ и возраста начала заболевания мы разделили больных ПСХ на две подгруппы — тех, у кого заболевание началось в детском возрасте (6 человек, возраст начала заболевания от 10 до 17 лет), и тех, у кого первые проявления ПСХ возникли во взрослом состоянии (17 человек, возраст начала заболевания от 20 до 66 лет) (табл. 3).
Из табл. 3 следует, что в группе больных, у которых ПСХ начался в детском возрасте, внепеченочные проявления регистрировались чаще, чем в группе пациентов, заболевших во взрослом состоянии. Причина такого различия распространенности системных проявлений ПСХ в различных возрастных группах в настоящее время неясна, необходимы дальнейшие исследования этого вопроса, в том числе обследование больших групп больных ПСХ.
Выводы
- ПСХ часто сопровождается внепеченочными проявлениями, наиболее распространенные из которых — хронические воспалительные заболевания кишечника.
- У одного больного может встречаться сочетание нескольких системных проявлений ПСХ.
- Поражение кишечника при ПСХ чаще развивается у мужчин, поражение щитовидной железы — у женщин.
- ПСХ, развившийся в детском возрасте, сопровождается системными проявлениями чаще, чем ПСХ, начавшийся у взрослых.
Литература
Е. А. Александрова*
Э. З. Бурневич*, кандидат медицинских наук, доцент
Е. А. Арион**
* ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Минздравсоцразвития РФ,
**Клиника нефрологии, внутренних и профессиональных болезней им. Е. М. Тареева, Москва
а) Терминология:
1. Аббревиатура:
• Первичный склерозирующий холангит (ПСХ)
2. Определение:
• Хроническое иммуно-опосредованное заболевание, приводящее к прогрессирующему воспалению, фиброзу и формированию стриктур внутри- и внепеченочных протоков
б) Визуализация:
5. УЗИ признаки первичного склерозирующего холангита:
• Утолщение стенок желчных протоков в области стеноза, перемежающееся расширение протоков, возможно, с наличием желчных конкрементов
• Асимметричное или симметричное утолщение стенки желчного пузыря (в 15% случаев), обусловленное воспалительным процессом при первичном склерозирующем холангите
6. Рекомендации по визуализации:
• Лучший диагностический метод:
о МРХПГ или холангиография (в случаях неоднозначных результатов МРХПГ или для коррекции осложнений)
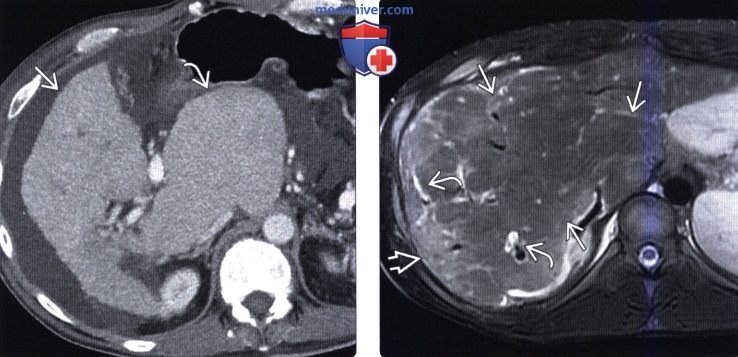
(Слева) На аксиальной КТ с контрастным усилением у пациента с длительно существующим первичным склерозирующим холангитом визуализируется цирротически измененная (с наличием узлов) печень. Обратите внимание на выраженную гипертрофию хвостатой доли и атрофию периферических отделов правой доли печени.
(Справа) На Т2 ВИ FS МР томограмме определяются морфологические изменения, характерные для первичного склерозирующего холангита на поздней стадии. Обратите внимание на увеличение центральных отделов печени и иррегулярное расширение желчных протоков. Зона слегка повышенной интенсивности сигнала на Т2 ВИ в периферических отделах печени обусловлена атрофическими изменениями и фиброзом.
в) Дифференциальная диагностика первичного склерозирующего холангита:
2. Холангиопатия при СПИДе:
• Воспаление желчного пузыря и желчных протоков, вызываемое СПИД-обусловленными оппортунистическими инфекциями
• Множественные стриктуры внутрипеченочных протоков, папиллярный стеноз, утолщение стенки желчного пузыря
• Изменения внутрипеченочных протоков могут быть аналогичны таковым при первичном склерозирующем холангите
3. Аутоиммунный (IgG4-обусловленный) холангит:
• IgG4-обусловленная лимфоплазмоцитарная инфильтрация билиарного дерева, часто сочетающаяся с аутоиммунным панкреатитом
• Лучевые признаки перекрываются с таковыми при первичном склерозирующем холангите, но наблюдаются обычно в старшей возрастной группе; для заболевания характерно более острое начало
4. Холангит, обусловленный химиотерапией:
• Холангит на фоне внутриартериальной химиотерапии
• Заболевание невозможно дифференцировать с первичным склерозирующим холангитом, тем не менее, для него характерно менее выраженное поражение периферических желчных протоков, и более частое поражение центральных
г) Патология. Общая характеристика:
• Этиология:
о Идиопатический воспалительный процесс в желчных протоках малого, среднего и крупного калибра, скорее всего, аутоиммунной природы:
- Поражение желчных протоков обусловлено иммунными клетками (T-клетками, В-клетками, естественными киллерами, макрофагами
- Часто сочетается с наличием аутоантител (антинейтрофильных цитоплазматических антител, антинуклеарных антител, антител ко гладким мышцам)
о В теории, роль пускового фактора при ПСХ могут играть роль бактерии из воспаленной слизистой оболочки толстой кишки
о Генетические факторы, вероятно, также имеют значение в развитии заболевания: риск возникновения заболевания у родных братьев и сестер пациентов, страдающих ПСХ, в сто раз выше
- Первичный склерозирующий холангит ассоциирован с человеческим лейкоцитарным антигеном I и II класса, а также главным комплексом гистосовместимости (хромосома VI)
• Сопутствующие патологические изменения:
о Язвенный колит (до 90%), болезнь Крона (13%)
о Другие аутоиммунные заболевания (тиреоидит, забрюшинный фиброз)
о ↑ риск возникновения холангиокарциномы: риск развития опухоли на протяжении жизни составляет 10-15% и 1,5% в течение года:
- Заподозрить холангиокарциному можно при быстро нарастающем клиническом ухудшении, нарушении функциональных печеночных проб, а также повышении уровня СА 19-9
д) Клинические особенности:
1. Проявления:
• Наиболее частые признаки/симптомы:
о у 40% пациентов на момент возникновения заболевания симптомы могут отсутствовать (часто случайная находка)
о Боль в правом подреберье, зуд, хроническая усталость, гелатоспленомегалия, снижение веса тела, желтуха
о ↑ уровня билирубина, щелочной фосфатазы
2. Демография:
• Возраст:
о Средний возраст дебюта заболевания составляет 30-40 лет
• Пол:
о М:Ж = 2:1
• Эпидемиология:
о Заболеваемость варьирует в зависимости от региона: выше у населения Северной Европы и Северной Америки:
- Распространенность заболевания: до 16,2 на 100000
4. Лечение:
• Могут применяться медикаментозные, эндоскопические и хирургические методы лечения (с малой доказанной эффективностью)
• При наличии доминирующей стриктуры - баллонная дилатация и стентирование:
о Может также потребоваться создание обходного анастомоза на желчных путях или резекция внепеченочного протока со стриктурой и выполнение гепатикоеюностомии Roux-en-Y
• Трансплантация печени позволяет добиться излечения, тем не менее, возможен рецидив ПСХ в аллографте печени
е) Список использованной литературы:
1. Costello JR et al: MR Imaging of Benign and Malignant Biliary Conditions. Magn Reson Imaging Clin N Am. 22(3):467-488, 2014
Читайте также:

