Отходы и их переработка в производстве меди реферат
Обновлено: 05.07.2024
На городских свалках даже среднего города ежегодно скапливаются сотни тысяч тонн бытовых отходов. Разлагаясь, они отравляют воздух, почву, подземные воды и превращаются, таким образом, в серьезную опасность для окружающей среды и человека.
Содержание
Введение
1. Переработка отходов
2. Утилизация
3. Значение переработки отходов
4. Вторичное сырье
5. Технологии переработки отходов
Заключение
Список использованных источников
Повышенный интерес к использованию вторичного сырья в развитых странах мира определяется наряду с экономическими соображениями также и жестким экологическим законодательством в отношении переработки отходов производства и потребления. Все большую роль играют международные соглашения по охране природы, особенно в тех направлениях, которые координируют отношения по обращению с отходами. Например, для стран — членов ЕС требуется обязательность наличия планов создания рынка вторичного сырья, введение нормирования использования наиболее распространенных отходов (макулатуры, стекла, пластиковых упаковок).
1. Переработка отходов
Переработка отходов — деятельность, заключающаяся в обращении с отходами с целью обеспечения повторного (вторичного) использования в народном хозяйстве полученных сырья, энергии, изделий и материалов. Под обращением с отходами понимается деятельность, включающая сбор, размещение, утилизацию, обезвреживание, транспортирование, хранение, захоронение, уничтожение и трансграничные перемещения отходов, а также организационно-технологические мероприятия по техническому регулированию работ с отходами, включая предупреждение, минимизацию, учет и контроль образования и накопления отходов. Целью переработки является превращение отходов во вторичное сырье, энергию или продукцию с определёнными потребительскими свойствами.
Переработка отходов может включать их обработку (англ. processing; treatment) — деятельность, направленную на изменение физического, химического или биологического состояния отходов для обеспечения последующих работ по обращению с отходами. Обработке подвергается множество извлекаемых из отходов материалов, включая стекло, бумагу, алюминий, асфальт, железо, ткани, различные виды пластика и многое другое.
Переработка отходов подвержена влиянию множества факторов. В одних случаях технология использования отходов не требует их обработки, а в других отдельные процессы переработки отходов технически нецелесообразны или экономически невыгодны из-за непомерно больших затрат материальных, транспортных, финансовых и человеческих ресурсов. В условиях рыночной экономики, решения о целесообразности применения тех или иных процессов переработки отходов принимаются с учётом текущей стоимости первичного и вторичного сырья, топлива, техники, труда, капитала и прочих ресурсов. К примеру, рост стоимости горюче-смазочных материалов или падение цен на сырьё могут оказывать существенное влияние на принятие решения о целесообразности обработки отходов, направленной на превращение во вторсырьё или энергию. Если такая обработка в силу совокупности факторов убыточна, степень переработки отходов ограничивается их уничтожением или захоронением и связанными с этим процессами — сбором, хранением и транспортированием к месту уничтожения или захоронения. Уничтожение отходов подразумевает их обработку с целью практически полного прекращения их существования, в то время как при захоронении отходов они транспортируются в назначенное место для хранения в течение неограниченного срока, где исключается опасное воздействие захороненных отходов на незащищенных людей и окружающую природную среду.
2. Утилизация
Переработку отходов следует отличать от утилизации. Под утилизацией отходов понимается следующее:
Нужна помощь в написании реферата?
Мы - биржа профессиональных авторов (преподавателей и доцентов вузов). Наша система гарантирует сдачу работы к сроку без плагиата. Правки вносим бесплатно.
- Использование отходов на различных стадиях жизненного цикла продукции(первичное использование) и обращение с отходами данной продукции, от их сбора до захоронения и/или уничтожения; или
- Обеспечение первичного и/или вторичного использования или переработки отходов, упаковкии отслуживших свой срок или забракованных изделий и материалов.
При проектировании современной продукции рассматривают её утилизируемость — комплекс показателей, обеспечивающих эффективную утилизацию отходов, образующихся при её производстве и эксплуатации и после вывода из обращения.
Также не следует отождествлять переработку отходов с рециклингом. Этот термин в русском техническом языке имеет особый смысл: он используется для обозначения процесса возвращения отходов в процессы техногенеза. Другими словами, рециклинг — это процесс, а переработка отходов — это деятельность, состоящая из отраслей деятельности и множества различных процессов. В этом смысле рециклинг является одним из элементов утилизации отходов, которая в свою очередь является частью переработки отходов. Рециклинг отходов осуществляется повторным использованием отходов по тому же назначению, например стеклянных бутылок после их соответствующей безопасной обработки и маркировки (этикетирования), либо путём возврата отходов после соответствующей обработки в производственный цикл (например жестяных банок — в производство стали; макулатуры — в производство бумаги и картона и т. п.)
3. Значение переработки отходов.
Во-первых, ресурсы многих материалов на Земле ограничены и не могут быть восполнены в сроки, сопоставимые со временем существования человеческой цивилизации.
Во-вторых, попав в окружающую среду, материалы обычно становятся загрязнителями.
В-третьих, отходы и закончившие свой жизненный цикл изделия часто (но не всегда) являются более дешевым источником многих веществ и материалов, чем источники природные.
4. Вторичное сырье
Отличительной чертой вторичных материальных ресурсов является то, что они не могут быть использованы по прямому назначению, однако потенциально пригодны для повторного использования в народном хозяйстве для получения сырья или изделий. Например, открытая потребителем консервная банка не может быть использована повторно по своему первоначальному назначению как контейнер для пищи, однако может быть обработана путём переплавки в сырьё для изготовления металлических изделий, в том числе новых консервных банок. Соответственно, вторичным сырьём называют только такие отходы производства и/или потребления, которые по своей природе являются материальными ресурсами, предназначенными для вторичного использования, непосредственно или после дополнительной обработки, в качестве сырья или изделий.
Нужна помощь в написании реферата?
Мы - биржа профессиональных авторов (преподавателей и доцентов вузов). Наша система гарантирует сдачу работы к сроку без плагиата. Правки вносим бесплатно.
Отходы, которые используются повторно с выделением тепловой и/или электрической энергии, не являются вторичным сырьём; такие отходы называются вторичными энергетическими ресурсами.
Вторичное сырьё
- Макулатура:бумага, картон, газеты, текстиль, упаковка;
- Стекло:стеклотара, стеклобой;
- Металлолом:чёрный, цветной, драгоценный;
- Химикаты:кислоты, щёлочи, органика;
- Нефтепродукты:масла, битум, асфальт;
- Электроника:изделия, платы, аккумуляторы, ртутные лампы, провода;
- Пластмассы:полиэтилентерефталат (ПЭТ), поливинилхлорид (ПВХ), полиэтилен высокого давления (ПВД) и низкого (ПНД), АБС-пластик, полистирол (ПС)
- Резина:шины, резина;
- Биологические: пищевые отходы, жиры,ассенизация;
- Древесина: сучья,стружка, листва
- Строительные:кирпич, бетон;
- Сточные воды.
5. Технологии переработки отходов.
Многие виды отходов могут быть использованы вторично, и для каждого вида отходов есть соответствующая технология переработки. Для разделения отходов по материалу используются различные виды сепарации. Например, для извлечения из мусора чёрных металлов используются магниты.
Металлы
Большинство металлов целесообразно обрабатывать для вторичного использования. Собранный металлолом идёт на переплавку. Особо выгодна переработка цветных металлов (меди, алюминия, олова), технических сплавов (победит) и некоторых чёрных металлов (чугун).
Обработке подлежат изделия электроники — процессоры, микросхемы, радиодетали и проч. Из них извлекаются драгоценные металлы — в частности, золото,платина,медь. Радиодетали вначале сортируют по размерам, затем дробят и погружают в царскую водку, в результате чего все металлы переходят в раствор. Из раствора золото осаждается определенными вытеснителями и восстановителями, другие металлы — сепарацией. Иногда после дробления радиодетали подвергаются отжигу.
Ко вторичным пластмассам относят:
- ПЭТ (ПЭТФ) — Полиэтилентерефталат
- ПВХ — Поливинилхлорид
- ПП — Полипропилен
- ПЭНД — Полиэтилен низкого давления
- ПЭВД — Полиэтилен высокого давления
- ПВ — Полиэтиленовыйвоск
- ПА — Полиамиды
- АВС — Акрилонитрилбутадиенстирол
- ПС — Полистирол
- ПК — Поликарбонаты
- ПБТ — Полибутилентерефталат
Полиэтилентерефталат
Существующие способы переработки отходов полиэтилентерефталата (ПЭТ) можно разделить на две основные группы: механические и физико-химические.
Основным механическим способом переработки отходов ПЭТ является измельчение, которому подвергаются некондиционная лента, литьевые отходы, частично вытянутые или невытянутые волокна. Такая переработка позволяет получить порошкообразные материалы и крошку для последующего литья под давлением. Характерно, что при измельчении физико-химические свойства полимера практически не изменяются.
Нужна помощь в написании реферата?
Мы - биржа профессиональных авторов (преподавателей и доцентов вузов). Наша система гарантирует сдачу работы к сроку без плагиата. Правки вносим бесплатно.
При переработке механическим способом ПЭТ-тары получают флексы, качество которых определяется степенью загрязнения материала органическими частицами и содержанием в нём других полимеров (полипропилена, поливинилхлорида), бумаги от этикеток.
Аккумуляторы и батареи.
На настоящий день все типы батарей, выпускаемые в Европе, могут быть переработаны независимо от того, перезаряжаемы они или нет. Для переработки не имеет значения, заряжена ли батарея, частично разряжена или разряжена целиком. После сбора батарей они подлежат сортировке и далее в зависимости от того, к какому типу они принадлежат, батареи отсылаются на соответствующий завод по переработке. К примеру, щелочные батареи перерабатываются в Великобритании, а никель-кадмиевые — во Франции. Переработкой батарей в Европе занимается около 40 предприятий. Ниже приведены типы батарей и методы их переработки:
Таблица 1. Типы батарей и методы их переработки
| Тип батареи | Процесс переработки |
| Щелочные | Гидро- и пирометаллургический процессы |
| Никель-кадмиевые | Пирометаллургический процесс |
| Никель-металл-гидридные | Процесс восстановления металлов |
| Литий-ионные | Процесс восстановления металлов |
Текстиль и обувь.
Во многих странах Европы на мусоросборных площадках спальных районов, помимо контейнеров для сбора металла, пластика, бумаги и стекла, появились контейнеры для сбора использованной одежды, обуви и тряпи.
Весь текстиль поступает в сортировочный центр. Здесь происходит отбор одежды, которая ещё может быть пригодна для использования, она впоследствии поступает в благотворительные ассоциации для малоимущих, церкви и Красный Крест. Непригодная одежда проходит тщательный отбор: отделяются все металлические и пластмассовые детали (пуговицы, змейки, кнопки и пр.), затем разделяют по типу ткани (хлопок, лён, полиэстер и т. д.). Например, джинсовая ткань поступает на заводы по производству бумаги, где ткань измельчается и отмачивается, после этого процесс производства идентичен целлюлозному. Метод производства бумаги из ткани сохранился неизменным уже многие столетия и был завезён в Европу Марко Поло, когда он впервые посетил Китай.
Заключение
Ученые из Нидерландов представили последние разработки в сфере переработки отходов — улучшенную технологию, которая без предварительной сортировки, в рамках одной системы, разделяет и очищает все отходы, которые туда поступают, до первоначального сырья. Система полностью перерабатывает все виды отходов (медицинские, бытовые, технические) в закрытом цикле, без остатка. Сырье полностью очищается от примесей (вредных веществ, красителей и т. д.), пакуется и может быть использовано вторично. При этом система экологически нейтральна.
В Германии построен и проверен TUV (немецкой Службой технического контроля и надзора) завод, который успешно работает по данной технологии 10 лет в тестовом режиме. На данный момент правительство Нидерландов рассматривает вопрос о строительстве на территории своей страны.
Список использованных источников
1. Катрин де Сильги. История мусора. М., Текст, 2011.
2. ГОСТ 30772-2001. Ресурсосбережение. Обращение с отходами.
Нужна помощь в написании реферата?
Мы - биржа профессиональных авторов (преподавателей и доцентов вузов). Наша система гарантирует сдачу работы к сроку без плагиата. Правки вносим бесплатно.
Принципы пылеулавливания, применяемые для этой цели аппараты и использование газов изложены в первом томе монографии, здесь же приведены лишь некоторые данные, относящиеся к характеристике пылей медеплавильного производства и методов их комплексной переработки.
В современной металлургической практике переработка медных руд и концентратов пирометаллургическим путем обычно сопровождается значительным выходом производственных пылей, количество которых зависит от характера и состава перерабатываемой шихты, характера и температуры металлургических процессов, скорости газовых потоков, конструкции агрегатов, принятых методов работы (например, от способа загрузки шихты) и др.
Пыли медеплавильных заводов содержат заметные количества ценных компонентов и часто в значительной степени обогащены редкими и рассеянными элементами, как правило, сопутствующими рудным минералам в большинстве медных руд.
В связи с указанным, эти пыли могут служить исходным материалом для извлечения редких и других ценных компонентов, поэтому в целях максимальной комплексности использования сырья их необходимо выводить из цикла основного производства для специальной пере работки с извлечением всех ценных составляющих. Состав улавливаемых пылей на некоторых медеплавильных заводах приведен в табл. 36.
Вследствие относительно высокого при температурах металлургических процессов давления паров металлов, сульфидов и окислов значительная часть соединений таких элементов, как свинец, мышьяк, олово, кадмий, индий, германий, таллий, возгоняется и контролируется в металлургических пылях. Пыли обогащены этими металлами по сравнению с исходным сырьем в 8—10 раз, причем самые богатые наиболее тонкие фракции пыли практически не улавливаемы в настоящее время.

Анализ результатов имеющихся исследований распределения редких компонентов при различных стадиях металлургического производства (табл. 37) показывает, что значительная часть их (более 60%) теряется со шлаками, из которых попутное извлечение их возможно только при фьюминговании шлаков Остальная же часть этих элементов концентрируется преимущественно в тонких пылях, несмотря на их небольшой выход (1—3%). Таким образом, по химическому составу различные фракции пыли могут сильно разниться.
Крупные фракции сравнительно мало отличаются от исходной шихты, будучи только слегка обогащены наиболее летучими ее компонентами, в то время как наиболее тонкие фракции, полученные в результате осаждения аэрозолей, будут обогащены преимущественно наиболее летучими компонентами рудного сырья.
В связи с указанным, пыли медеплавильных заводов могут быть разделены на грубозернистые (пыли пылевых камер, циклонов грубой очистки и основных газоходов) и тонкодисперсные (преимущественно пыли высокотемпературных операций — отражательных печей, конвертеров, шахтных печей, уловленные либо в электрофильтрах после грубой газоочистки, либо в удаленных участках газоходной системы).

Грубозернистые и смешанные пыли низкотемпературных операций мало отличаются по составу от исходной шихты, в результате переработки которой они образовались, поэтому в большинстве случаев могут быть возвращены в качестве оборотного продукта в основной процесс. Тонкодисперсные пыли обычно значительно отличаются по составу от исходной шихты, они весьма заметно обогащены летучими, редкими и рассеянными элементами. Эти пыли могут служить сырьем для получения ряда ценных компонентов, поэтому их следует выводить из основного цикла производства для специальной переработки.
При надлежащем использовании металлургических пылей медеплавильных заводов может быть значительно повышена степень комплексности использования сырья и заметно снижены потери ценных компонентов при металлургической переработке. В соответствии с имеющимися литературными данными, унос пыли в трубу при отражательной плавке обычно составляет 1,2—1,8%. В обследовании, выполненном кафедрой тяжелых цветных металлов УПИ, безвозвратные потери пыли в дымовую трубу на СУМЗе были определены равными 3,1% от веса твердой шихты, а при плавке шихты с большим количеством золотосодержащих пиритных огарков (до 20% от шихты) потери достигали 4,5%. Наконец, по данным Унипромеди, потери пыли при плавке сырой шихты на СУМЗе составляли 2,76% от веса твердой шихты, общий же процент пылеобразования при отражательной плавке СУМЗа с учетом оседающей в газоходах пыли составлял 3,5—4,5%.
По данным работ Унипромеди, общий процент пылеобразования при бессемеровании на СУМЗе равен примерно 2,5%, в том числе унос в трубу 1,8%. Общий пылеунос при шахтной плавке, по данным Кировградского и Карабашского заводов, колеблется примерно в пределах 4,2-—4,5% от веса шихты Из этого количества примерно 1,7—1,8% от веса шихты теряется с дымовыми газами.
Опытом установлен следующий унос пыли с отходящими газами из пирометаллургических агрегатов.

Установлено, что неулавливаемые пыли составляют примерно 35% от общего количества образующихся пылей. С неулавливаемыми шалями безвозвратно теряются многие ценные компоненты, в том числе редкие и рассеянные элементы. В целях комплексного использовании сырья и уменьшения потерь ценных компонентов необходимо на медеплавильных заводах организовать рациональное пылеулавливание особенно тонких пылей из газов всех металлургических агрегатов и повысить эффективность существующих пылеулавливающих устройств и внедрить схемы комплексной переработки пылей.
Пыли медеплавильных заводов обычно являются весьма сложным многокомпонентным полупродуктом производства со сравнительно невысоким содержанием ценных компонентов (каждого в отдельности), поэтому непосредственная комплексная переработка их гидрометаллургическим путем в большинстве случаев не дает удовлетворительных результатов, в особенности по извлечению редких элементов. Так, оказались неудачными попытки непосредственно гидрометаллургически перерабатывать пыли Кировградского медеплавильного завода по схеме проф. Сырокомсколо и схеме Гиредмета.
Институтом Унипромедь и Кировградским медеплавильным заводом использован метод переработки пылей с предварительным получением в восстановительных условиях возгонов, обогащенных ценными компонентами и практически свободных от меди, железа, благородных металлов и элементов пустой породы. Такое предварительное обогащение дало возможность сократить в несколько раз количество материала, поступающего в гидрометаллургическую переработку, избавиться от меди и железа, нежелательных для дальнейшей переработки, значительно снизить возможность размазывания денных компонентов по небольшому количеству отходов и полупродуктов и тем самым значительно повысить эффективность всей схемы комплексной переработки пылей.
Переработка возгонов и других металлургических продуктов подобного им состава возможна в следующих направлениях: 1) использование для их переработки специальных селективных осадителей, позволяющих выделять тот или иной элемент независимо от присутствия других; 2) использование ионного обмена растворов со специальными ионитами (смолами); 3) использование ионного обмена между раствором и осадком при дробном (стадиальном) осаждении элементов; 4) использование ионного обмена между раствором и осадком с использованием схемы противотока.
Использование специальных селективных осадителей для осаждения редких металлов в ряде случаев может оказаться эффективным при извлечении этих металлов из растворов. Наиболее перспективными для этого могут явиться органические осадители, образующие с осаждаемым элементом металлоорганические соединения.
Применение ионнообменных смол для извлечения редких элементов является весьма обнадеживающим методом. Этот способ заключается в адсорбции смеси ионов на ионнообменной смоле с последующим избирательным вымыванием отдельных ионов. Он нашел применение для извлечения редкоземельных элементов, а также в аналитической практике. Нет никаких оснований сомневаться в возможности его применения и для извлечения редких и рассеянных элементов из пылей и возгонов. Развитие этого способа осложняется малым ассортиментом смол, выпускаемых нашей промышленностью, и отсутствием достаточных данных о комплексных соединениях редких и рассеянных элементов.
Извлечение редких элементов из растворов в виде сульфидов или гидратов очень затруднено ввиду явления соосаждения, поэтому может быть использовано только в виде дробного осаждения, т. е. при использовании явлений ионного обмена между раствором и осадком. Хорошей мерой борьбы с соосаждением в этом случае может явиться применение принципа противотока (к гетерогенным процессам), который обладает следующими основными положительными качествами большой полнотой осуществления процесса и большой средней движущей силой процесса (определяемой разностью концентраций), что позволяет уменьшить размеры аппаратуры. Используя ионный обмен между раствором и осадком при противоточной схеме, теоретически имеется возможность получить близкое к 100% извлечение почти при 100%-ной чистоте извлекаемого компонента, вернее, приблизиться к этому за счет увеличения ступеней обработки.

Проблема переработки отвальных медных шлаков является одной из актуальных проблем, решение которой может служить дополнительным источником цветных и черных металлов, а также улучшить состояние окружающей среды в районах действия предприятий. Рассмотрены теоретические основы твердофазного восстановления компонентов шлака углеродом с целью создания новой комплексной технологии совместной переработки шлаков медеплавильного производства и отработанного медного электролита.

1. Медиханов Д.Г. Вовлечение в переработку сырья техногенных месторождений БГМК / Сб. научн. работ по проблемам БГМК. – Балхаш: БГМК, 2001. – С. 137–142.
3. Медиханов Д.Г., Алипбергенов М.К., Исабаев С.М., Кузгибекова Х.М. Теория и практика удаления мышьяка при производстве меди. – Караганда, 2003. – 240 с.
4. Харченко Е.М., Жумашев К. Изучение научно-технологических основ совместной переработки отвальных медных шлаков и отработанного медного электролита // Вестник Южно-Уральского государственного университета. – Челябинск: ЮУрГУ, 2011. – № 36 (253). – С. 18–23.
Пирометаллургическое производство цветных металлов характеризуется образованием большого количества отходов производства, основными из которых являются шлаки. Так на медеплавильных заводах при производстве тонны меди выделяется 2–4 т шлаков плавильного, конвертерного и рафинировочного переделов. Комплексное использование техногенных отходов, к которым относятся шлаки, создает предпосылки для экономии природных ресурсов и укрепления минерально-сырьевой базы цветных металлов.
Согласно данным [1] большие объемы медьсодержащих продуктов сосредоточены именно в шлаках: 31 млн тонн отходов Балхашского горнометаллургического комбината (БГМК) содержат 250 тыс. т меди. Практическое отсутствие у БГМК собственных сырьевых источников (Коныратский и Саякский рудники на стадии выработки, Шатыркульский рудник осваивается) почти наполовину компенсируется добычей меди флотационным обезмеживанием отвальных шлаков [2]. Однако, несмотря на вовлечение шлаков в технологический цикл, проблема их утилизации остается нерешенной, и требует разработки дополнительных технологических мероприятий.
Одним из перспективных направлений переработки шлаков представляется их восстановительная обработка с переводом железа в металлическое состояние, которое может рассматриваться в качестве матрицы, цементирующей медь из кислотных растворов, например отработанного медного электролита этого же предприятия. Процесс цементации основан на различии в величинах нормальных потенциалов меди и металла-осадителя. Наиболее распространенным осадителем для меди является железная стружка, железный порошок или железный скрап достаточно дефицитные и дорогие материалы [3].
Попутное извлечение меди и др. компонентов, присутствующих в шлаке, также позволит повысить комплексность использования сырьевых источников и сделать переработку экономически оправданной.
Таким образом, перед нами встала задача металлизации отвального медного шлака. В качестве объекта исследования использован отвальный шлак БГМК состава, %: 34,8 Feобщ; 38,8 SiO2, 6,8 CaO, 0,57 Cu, 1,64 S, 1,1 Pb, 0,8 Zn, 0,4 As.
Так как шлак медеплавильного производства в основном представлен фаялитом Fe2SiO4 (рис. 1), то была поставлена задача изучения протекания реакций:

Рис. 1. РФА отвального шлака Балхашского медеплавильного завода. – Fe2SiO4 (фаялит), – FeSiO3 (ферросилит), – Fe(Са)SiO3(клиноферрит)
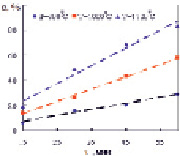
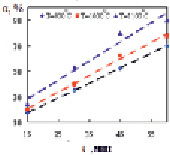
Рис. 2. Изменение степени восстановления от продолжительности восстановления Fe2SiO4 (а) и Fe2SiO4 в смеси с СаО (б)
Восстановление проводили в трубчатой электропечи СУОЛ-044 12-М2 [2] при температурах 900, 1000, 1100 °С с выдержкой при каждой температуре 15, 30, 45, 60 минут. Результаты представлены в виде графиков (рис. 2).
Как следует из графиков повышение температуры и продолжительности обжига ведут к линейному росту степени восстановления. Степень восстановления определена как отношение количества кислорода переведенного в газовую фазу к его количеству в исходных соединениях. Наибольшая степень восстановления Fe2SiO4 достигнута при температуре 1100 °С и выдержке более 60 минут. Добавка в шихту оксида кальция интенсифицирует восстановление. Так при температуре 1000 °С и выдержке 60 мин значение α составляет ~ 57 %, а в тех же условиях с добавкой СаО – 71 %; аналогично при 1100 °С и 60 мин – 80 % и 91 %, соответственно.
Обобщенные уравнения зависимости степени восстановления железа (α) от температуры (Т, °С) и продолжительности (τ, мин) углеродом (3) и с добавлением СаО (4) имеют вид:
α = – 136 + 0,19Т – 690/τ, r 2 = 0,81 (3)
α = – 26,25 + 0,11Т – 1001/τ, r 2 = 0,86 (4)
Магнитная сепарация восстановленных продуктов дала следующие результаты: масса магнитной фракции при сепарации огарка восстановленного при температуре 1000 °С в течение 60 минут составляет ~ 36 %. В тех же условиях, но с добавлением СаО – 49 %, а повышение температуры до 1100 °С (60 мин) сопровождается ростом магнитной фракции до 49 и 55 % соответственно. Селективного извлечения железа в магнитную фракцию не достигнуто, что связано с тонкой вкрапленностью металла. Обобщенные уравнения зависимости выхода магнитной фракции (γ) от параметров восстановления (Т, °С, τ, мин) углеродом (5) и с добавлением СаО (6) имеют вид:
γ = – 69,1 + 0,10Т – 397/τ, r 2 = 0,79 (5)
γ = – 53,34 + 0,05Т – 612/τ, r 2 = 0,90 (6)
Эксперименты по восстановлению отвального шлака Балхашского медеплавильного завода (Feобщ – 34,8 %, фазовый состав представлен на рис. 3) углеродом кокса проведены в неизотермических условиях при нагреве (10 °С/мин) до 900 °С, 1000 и 1100 °С с последующей выдержкой при заданной температуре в течение 30, 45 и 60 минут. Количество выделяющегося газа фиксировали газовым счетчиком. В первые 30–35 минут опыта (540–800 °С), когда объем выделяющегося газа незначителен, происходит лишь частичное восстановление компонентов шлака, оксидов меди и свинца. Выше 800 °С зафиксировано резкое увеличение объема выделяющегося газа, свидетельствующее о восстановлении железа.
Обобщенное уравнение металлизации шлака имеет вид:
α = – 53,76 + 0,15Т – 1191/τ, r 2 = 0,86 (7)
Максимальное значение степени металлизации – 89,9 % достигнуто при 1100 °С и продолжительности обжига 60 мин (рис. 3). Однако при указанной температуре наблюдали частичное спекание шихты, затрудняющее завершение твердофазного восстановления шлака. Поэтому рекомендован восстановительный обжиг при 1050 °С и продолжительности 60 мин, обеспечивающий степень металлизации шлака 85 %.
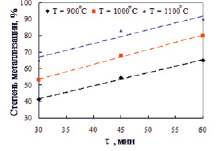
Рис. 3. Изменение степени металлизации железа от продолжительности восстановительного обжига шлака с коксовой мелочью
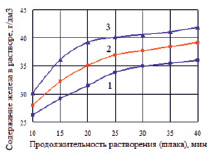
Рис. 4. Изменение содержания железа в водном растворе H2SO4 от продолжительности его перемешивания (Vперем = 100 об/мин) со шлаком имеющим степень металлизации 51 % (1), 68 % (2) и 89 % (3)
Полученный металлизованный продукт, предполагается использовать в качестве нейтрализатора кислых растворов, в частности отработанного медного электролита. С этой целью были изучены условия растворения восстановленного железа шлака в сернокислом растворе (2Н). Как следует из графиков (рис. 4) в первые 20 минут имеет место интенсивный переход железа в раствор для всех трех образцов, затем процесс замедляется в связи с насыщением раствора железом и недостатком кислоты. Повышение степени металлизации шлака способствует насыщению раствора по железу (Fe 2+ ).
При соотношении масс раствор/шлак равном 5, получены растворы, содержащие 36–43 г/дм3 железа (178–213 г/дм3 FeSO4∙7Н2О). Такие растворы могут быть использованы при автоклавном выщелачивании свинцовоцинковых концентратов или для обезвреживания сточных вод ТЭЦ.
Таким образом, результаты проведенных лабораторных испытаний могут стать основой для разработки технологической схемы металлизации шлака с последующим его использованием для цементационного выщелачивания меди из кислотных растворов (отработанного медного электролита). Такой подход позволит заменить дефицитный и дорогой железный скрап, используемый для нейтрализации электролита на доступное сырье – собственные отходы.
3. Существующие технологии переработки медьсодержащих твердых материалов.
Согласно существующей литературе можно сделать следующую классификацию технологий производства купороса (детальное описание технологий приводится ниже)
Рабочий раствор или процесс
Серная кислота разбавленная
Серная кислота концентрированная
Соляная кислота концентрированная
Хлорид меди (II) или раствор поваренной соли
Метод натравочной башни
Растворимый анод, электролит - любая соль щелочного металла
Получение гидроксида с растворением в серной кислоте
Растворимый анод, диафрагма, электролит - любая соль щелочного металла
Прямое получение купороса и щелочи без затраты кислоты
Вертикальный электролизер с потоком кислоты от катода к аноду
Таблица 1 — Возможные технологии переработки медьсодержащих отходов, латунной и бронзовой стружки
3.1 Метод сернокислого выщелачивания. Технологии 1,2.
Для получения чистого медного купороса растворяют медь в крепкой или разбавленной наполовину водой серной кислоте. Раствор разбавляют водой, нагревают, отфильтровывают осадки, фильтрат выпаривают, кристаллизуют и полученные кристаллы очищают повторной кристаллизацией. В настоящее время в большинстве случаев предпочитают растворять медь в слабой серной кислоте при доступе воздуха. Для этого куски металла (обрезки, опилки и т. п.) закладываются в деревянные чаны, опаянные внутри свинцом и расположенные друг над другом, причем на дно чана кладутся более крупные куски. В верхний чан сверху пускают камерную серную кислоту, разбавленную маточным раствором и промывными водами от предшествовавших кристаллизаций до 10° - 30°В. и нагретую паром до 40° - 80°С. Раствор пропускают для насыщения последовательно через нижележащие чаны и затем или прямо выпускают в опаянные свинцом деревянные ящики, где при охлаждении кристаллизуется медный купорос, или предварительно выпаривают его до 40° - 42°В. Кристаллы М. купороса после первой кристаллизации выгребают, дают стечь маточному раствору, обмывают холодной водой, растворяют в возможно малом количестве горячей воды, вновь кристаллизуют, обмывают холодной водой и просушивают, медный купорос получается при этом очень чистый, почти без примеси железа и цинка. Вместо серной кислоты пользуются иногда для растворения меди выделяющуюся при обжигании серного колчедана сернистой кислотой, которую вместе с воздухом прогоняют через башню, наполненную медным ломом и нагретую паром до 100°С. Образующийся медный купорос растворяется притекающим сверху маточным раствором из кристаллизаторов, стекающий раствор прогоняется еще раз через башню для более полного насыщения, кристаллизуется, промывается и перекристаллизовывается, после чего кристаллы содержат от 98 до 99% чистого медного купороса.
Для получения больших и красивых кристаллов медного купороса, какие требуются в торговле, необходимо иметь при кристаллизации по возможности нейтральные и не слишком крепкие растворы и медленное охлаждение в закрытых (особенно зимой) больших кристаллизаторах. Лучшие кристаллы садятся на свинцовых лентах, подвешиваемых в растворе медного купороса. Сушка кристаллов медного купороса должна происходить при невысокой темп. (37° - 40°С) и в затененном помещении. При нечистоте исходных материалов медный купорос может содержать железо и цинк, что при некоторых производствах, напр. при приготовлении красок, нежелательно (железа допускается не более 1 /2%, а цинк, хоть и менее вреден, но все же краски выходят светлее, и невыгодно оплачивать его, как медь). Для удаления железа при приготовлении медного купороса предложено много способов, обыкновенно же выделяют его сильным прокаливанием медного купороса в пламенной печи, причем железо переходит в нерастворимую окись, или же осаждают железо углекислой медью или окисью меди. Под именем двойного, или смешанного, купороса (адмонтский, байрейтский или зальцбургский купорос) идет в торговлю для красилен и для смачивания хлебных зерен голубовато-зеленая изоморфная смесь медного купороса с железным, а иногда еще и с цинковым. Состав такого купороса непостоянен.
3.2 Получение медного купороса при окислении меди хлорной медью. Технология 4.
Этот метод основан на образовании хлористой меди из хлорной и металлической меди:
Cu + CuCl2 = 2CuCl
(хлористую медь получают также хлорированием цементной меди в растворе поваренной соли). Хлористую медь окисляют воздухом с образованием оксихлорида меди:
Оксихлорид растворяют в серной кислоте, в результате чего образуется раствор сульфата меди и регенерируется хлорная медь
Получение оксихлорида меди осуществляют в бетонном баке, куда загружают медь и заливают раствор хлорной меди. После этого продувают массу воздухом, пока вся металлическая медь не перейдет в нерастворимый оксихлорид. После отстаивания и декантации пульпу растворяют при нагревании в серной кислоте. При охлаждении раствора из него кристаллизуется CuSO4 * 5H2O. Маточный раствор возвращают в процесс. Этим способом можно получать также хлорокись меди.
3.3 Производство медного купороса из медного лома методом натравочной башни. Технология 5.
Гранулированную медь загружают в натравочную башню, высотой около 6 м, диаметром 2,5 м. Башня изготовлена из листовой стали, внутри футерована кислотоупорным кирпичом и диабазовыми плитками. На высоте 0,5 - 0,9 м от дна в башне имеется ложное днище, лежащее на колосниковой решетке из стальных балок, опаянных свинцом. На ложном днище находится слой меди, высоту которого поддерживают периодическими загрузками на уровне 0,25 м от крышки башни. Под крышкой помещена турбинка, с помощью которой медь непрерывно орошается смесью серной кислоты с маточным раствором. Количество находящейся в башне меди составляет 22 - 28 т.
В башне происходит одновременно окисление и растворение меди. Эти процессы идут с выделением тепла, достаточным для повышения температуры до необходимого уровня, то есть до 70 - 85 0 С. Для окисления меди в башню под колосниковую решетку вдувают воздух в смеси с паром. Пар подают для нагревания воздуха. Вдувание холодного воздуха вызвало бы охлаждение щелока и выделение из него кристаллов медного купороса, что привело бы к закристаллизовыванию нижнего слоя гранулированной меди. Подачей пара регулируют и температуру в башне. Уходящая из нее паро-воздушная смесь выбрасывается в атмосферу. С 1 м 3 натравочной башни можно получить в сутки более 1,3 т. медного купороса.
Вытекающий из натравочной башни горячий щелок (74 - 76 0 С) представляет собой почти насыщенный раствор медного купороса - он содержит 42-49 % CuSO4 ∙ 5 H2O и 4 - 6 % свободной H2SO4. Этот щелок подают центробежным насосом из хромоникелевой стали во вращающийся кристаллизатор непрерывного действия с воздушным охлаждением раствора. Смесь кристаллов медного купороса с маточным раствором через сборник с мешалкой поступает в центрифугу из нержавеющей стали, где кристаллы, отжатые от маточного раствора, промываются водой. На центрифугирование поступает пульпа с соотношением Т: Ж от 1: 2 до 1: 1,5. Отфугованный продукт, содержащий 4 - 6 % влаги и 0,15 - 0,2 % кислоты, высушивают в барабанной сушилке воздухом при 90-100 0 С. Маточный раствор и промывную воду после смешения с серной кислотой возвращают в производственный цикл.
В маточном растворе происходит постепенное накопление примесей, все больше загрязняющих продукт. Содержащийся в медном купоросе сульфат никеля можно удалить с достаточной полнотой при однократной перекристаллизации. Для удаления FeSO4 необходима многократная перекристаллизация. Получение медного купороса с содержанием 99,9 % CuSO4 ∙ 5 H2O однократной перекристаллизацией из раствора, насыщенного при 70 0 С, возможно при содержании в нем не более 0,3 % NiSO4 и не более 0,15 % FeSO4.
Если в растворе больше 40 г./л FeSO4, то количество железа в продукте больше 0,4 %, то есть выше нормы, допускаемой ГОСТом для продукта III сорта. Из растворов, содержащих больше 100 - 120 г./л FeSO4, выделяются смешанные кристаллы железного и медного купоросов с характерной сине-зеленой окраской.
Содержание железа в кристаллах медного купороса можно уменьшить предварительным окислением Fe 2+ в Fe 3+ . Окислителем может служить воздух (длительный барботаж), азотная кислота, перекись водорода и др. Степень очистки повышается в 2 - 4 раза при добавке к раствору незначительного количества HF (плавиковой кислоты), что приводит к образованию фторидных комплексов Fe 3+ . Установлено также, что при усилении перемешивания в процессе кристаллизации получаются кристаллы с меньшим содержанием железа, но и размеры их уменьшаются. Присутствие ионов никеля также уменьшает размеры кристаллов, а мышьяка - увеличивает.
На производство 1 т. кристаллического медного купороса расходуют: 0,27 - 0,29 т. металлической меди и 0,39 - 0,40 т. серной кислоты (100 %).
На заводе имени Войкова общие затраты тепла на производство медного купороса составляли 0,76 мгкал на 1 т. продукта. Расход тепла распределяется следующим образом. В натравочную башню через инжекторы вводится 47 % тепла, на подогрев воздуха в калориферах сушильного агрегата затрачивается 26 % тепла и 27 % тепла расходуется на подогрев раствора в сборниках, на разогрев мазута в цистернах и т. д. Количество тепла, выводимого с паро-воздушной смесью, больше тепла, вводимого с паром вследствие дополнительного парообразования, обусловленного выделением тепла реакцией. Поэтому вместо паро-воздушной смеси можно вдувать в башню теплый воздух из кристаллизатора с добавкой 20 - 25 % пара от обычного количества, при температуре смеси, исключающей закристаллизовывание нижнего слоя гранул в башне.
Ввод пара в натравочную башню может быть и вовсе исключен при осуществлении процесса с рециркуляцией паро-воздушной смеси. Отходящую из башни паро-воздушную смесь с температурой ~ 80 0 С направляют при помощи вентилятора из нержавеющей стали под ложное дно башни. При осуществлении процесса по такой схеме возможно введение в цикл газообразного кислорода, что значительно интенсифицирует растворение меди.
Отходом производства медного купороса являются илы, скапливающиеся в резервуарах с производственными растворами. Количество илов составляет 1 - 2 % от перерабатываемой меди. Состав их различен; они могут содержать до 8,5 % Ag2O, до 5 % Bi2O3, 0,05 - 0,1 % Au, Pt, Pd. Такие илы могут быть переработаны гидрометаллургическими методами для извлечения из них ценных металлов.
Предложено получать медный купорос из натравочного щелока добавкой к нему серной кислоты (башенной, купоросного масла, олеума или SO3) до содержания свободной H2SO4 60 % и более. При этом быстро осаждается мелкокристаллический белый безводный сульфат меди, примеси же остаются в растворе. CuSO4 отфуговывают и растворяют в чистом маточном растворе медного купороса, из которого кристаллизуется CuSO4 ∙ 5 H2O. Кислый щелок после осаждения безводного CuSO4 возвращается на растворение меди. После накопления в нем значительного количества ценных примесей (никель, цинк, серебро и др.) их можно извлечь. Преимущество этого способа - в простой и быстрой кристаллизации медного купороса без затраты тепла и холода и высокой чистоте продукта.
Можно вообще отказаться от выпуска пятиводного сульфата меди и выпускать безводный продукт, концентрация меди в котором больше (39,8 % вместо 25,5 % в CuSO4 ∙ 5 H2O). Производство и транспорт его будут дешевле, хотя он и потребует более тщательной упаковки из-за гигроскопичности. Впрочем, даже при небрежной упаковке на поверхности белого порошка появится лишь синеватая окраска вследствие гидратации влагой воздуха, но это не ухудшит качества продукта, который предназначен для растворения в воде. Однако, во избежание слеживания, упаковка должна быть герметичной.
Очистка сточных вод, сбрасываемых в водоемы из производств медного купороса и других медных солей, от ионов меди может быть осуществлена на 70 - 90 % с помощью сульфата алюминия. Выделяющаяся при гидролизе сульфата алюминия гидроокись алюминия адсорбирует ионы меди.
3.4 Получение медного купороса электролизом. Технология 7-9.
Суть метода - электрохимическое окисление меди с растворением ее в серной кислоте. При проведении электролиза с растворимым медным анодом в растворе любой соли щелочного металла получающаяся на аноде медная соль, реагируя с образующейся на катоде щелочью, дает гидроксид меди с одновременной регенерацией электролита.
Можно получить электролизом инепосредственно раствор медного купороса, осуществляя процесс в ванне, в которой анод, находящийся на дне ванны, состоит из спрессованных или сплавленных обрезков меди. Через полый катод, помещенный сверху, подается серная кислота. Движение раствора от катода к аноду не допускается нежелательное в данном случае осаждение меди на катоде.
При проведении электролиза с растворимым медным анодом в растворе сульфатат натрия в ванне с диафрагмой можно одновременно получить медный купорос и гидроксид натрия. Купорос при этом легко может быть отделен от сульфатат натрия.
Медь может быть извлечена из разбавленных растворов цементацией и слабой аммиачной водой. При этом образуется осадок Cu(OH)2 * CuSO4 который после отделения от раствора можно растворить в серной кислоте с получением купороса.
3.5 Технология получения медного купороса из электролита цехов электрорафинирования меди (6).
В производстве медного купороса в качестве основного сырья используется раствор цеха электрорафинирования меди и медные гранулы.
Производство медного купороса включает в себе следующие последовательные стадии:
1. Получение насыщенных растворов и нейтрализация серной кислоты;
2. Выпарная вакуум-кристаллизация;
3. Разделение суспензии медного купороса и обработка кристаллов;
4. Затаривание и упаковка.
Первая стадия — получение насыщенных растворов сернокислой меди. Процесс производят путём связывания свободной серной кислоты, присутствующей в передаточном растворе цеха электрорафинирования меди и оборотных растворах купоросной производства, с медью в виде мелких гранул.
На скорость процесса и качество получаемого купороса влияют:
- скорость окисления поверхности меди
- содержание меди в растворе
- температура процесса растворения (растворение проводится при температуре 75-95 0 С)
Растворение меди осуществляется путём загрузки гранул в аппараты нейтрализации колонного типа, подогреваемые паром. Циркуляция осуществляется за счёт подачи в раствор сжатого воздуха. Образующаяся воздушно-жидкостная эмульсия вытесняется вверх по центральной трубе аппарата раствором, подводящимся по боковой трубе.
Скорость циркуляции (объемный расход) поддерживается на уровне от 15 до 30 м 3 /ч путем регулировки подачи воздуха.
Вторая стадия — выпарная вакуум-кристаллизация. Процесс организован в 3 стадии. Первые две производят медный купорос продукционный, а на третьей получают медный купорос некондиционный, который отправляется в начало процесса.
сходный раствор из напорного бака самотёком подают в нижнюю часть вакуум-кристаллизатора. Под давлением напора перегретый маточный раствор, вытекая из сопла струйного насоса, подсасывает суспензию, циркулирующую в аппарате. Поступающий исходный раствор и образовавшаяся смесь поднимаются по центральной циркуляционной трубе вверх и на выходе из неё вскипают. Образовавшиеся кристаллы частично отводятся из вакуум-кристаллизатора. На процесс оказывают влияние температура и растворенные примеси.
В выпарном вакуум-кристаллизаторе поддерживается разряжение не менее 092-098 кПа. Суспензию из аппарата, при достижении концентрации 15-25%, сливают в бак-мешалку и закачивают в механические кристаллизаторы для сбора суспензии.
Третья стадия — разделение суспензии медного купороса и обработка кристаллов. Отделение кристаллов медного купороса от маточного раствора и промывку кристаллов производят на центрифугах, в основе работы которых лежит принцип фильтрации под действием центробежных сил. Для отделения маточного раствора II стадии кристаллизации от нерастворимых примесей дополнительно проводят фильтрацию раствора на рамном фильтр-прессе. Отфильтрованный маточный раствор направляют в бак маточного раствора, а кек после выгрузки фильтр-пресса - на площадку хранения медьсодержащих отходов.
Кристаллы с I и II стадий кристаллизации отправляют на сушку, а с III стадии - растворяют конденсатом в агитаторе при постоянном перемешивании и нагреве паром через рубашку агитатора.
Сушку кристаллов проводят горячим воздухом в барабанной сушилке, откуда купорос поступает на автоматическую линию упаковки и пакетирования или на узел затаривания готового продукта.
Для получения мелкодисперсного купороса от общей массы на двуситовой сортировке отделяют мелкую фракцию кристаллов.
Упаковку производят на автоматизированной линии в полиэтиленовые или бумажные мешки.
Список вариантов технологий, которые предлагаем мы и которые могут быть использованы, но нами не придуманы.
4. Выводы.
На основании имеющихся данных можно сказать:
1. Температура является лимитирующим фактором при растворении меди. В холодных травителях, независимо от их природы, растворение идет с ничтожной скоростью
2. В травителе должно присутствовать 100-120 г/л медного купороса (безводный) для того, чтобы облегчить последующую кристаллизацию
3. Кристаллизация начинается в концентрированном растворе при присутствии там порошковой меди. Присутствие кристаллов купороса, введенных извне кристаллизацию не инициирует
4. Периодический барботаж необходим, т.к. с повышением концентрации купороса растворимость кислорода в нем падает и дополнительно тормозит реакцию. Кроме этого, барботаж делает осадок мелкодисперсным и не дает спекаться
5. Процесс тормозится после первого часа. Это связано с:
- Остывание раствора, если не использовался нагрев
- Расход растворенного воздуха и установление диффузионных ограничений по купоросу
- Повышение концентрации купороса и уменьшение растворимости кислорода вследствие этого
6. Рафинированный и вторичный рафинированный порошок имеют высокую скорость растворения независимо от исходных параметров в рамках первого часа т.к:
- Поверхность меди сильноокисленна. Ионы меди и железа катализируют только ОВ реакцию ионизации меди, а не обменные, которые преобладают в первом часе
- Вторичная меди имеет более высокую скорость, чем первичная. т.к. в процессе ее оксидицзации принимали участие остатки травящего электролита. Т.е создавались условия с избытком окислителя - кислорода и легкостью его доступа вследствие того, что слой электролита имел пленочный характер, а не объемный. Кроме этого, сказывалось каталитическое действие ионов меди и железа.
В итоге выделим основные принципы процесса:
Максимальный нагрев, барботаж, введение оксидизатора, использование травителя с высоким исходным содержанием купороса и введением ионов железа.
Читайте также:

