Металлическая связь реферат по химии
Обновлено: 02.07.2024
Химическая связь - это взаимодействие двух атомов, осуществляемое путем обмена электронами. При образовании химической связи атомы стремятся приобрести устойчивую восьмиэлектронную (или двухэлектронную) внешнюю оболочку, соответствующую строению атома ближайшего инертного газа. Различают следующие виды химической связи: ковалентная (полярная и неполярная; обменная и донорно-акцепторная), ионная, водородная и металлическая
1.Металлическая связь.
. Металлическая связь, химическая связь, обусловленная взаимодействием электронного газа (валентные электроны) в металлах с остовом положительно заряженных ионов кристаллической решетки. Идеальная модель металлической связи отвечает образованию частично заполненных валентными электронами металла зон энергетических уровней, называемых зонами проводимости. При сближении атомов, образующих металл, атомные орбитали валентных электронов переходят в орбитали, делокализованные по кристаллич. решетке аналогично делокализованным p-орбиталям сопряженных соединений. Количественно описать металлическую связь можно только в рамках квантовой механики, качественно образование металлической связи можно понять исходя из представлений о ковалентной связи.
При сближении двух атомов металла, например Li, образуется ковалентная связь, при этом происходит расщепление каждого энергетич. уровня валентного электрона на два. Когда N атомов Li образуют кристаллическую решетку, перекрывание электронных облаков соседних атомов приводит к тому, что каждый энергетич. уровень валентного электрона расщепляется на N уровней, расстояния между которыми из-за большой величины N настолько малы, что их совокупность может считаться практически непрерывной зоной энергетических уровней, имеющей конечную ширину. Поскольку каждый атом участвует в образовании большего числа связей, чем, например, в двухатомной молекуле при том же числе валентных электронов, то минимум энергии системы (или максимум энергии связи) достигается при расстояниях больших, чем в случае двухцентровой связи в молекуле. Межатомные расстояния в металлах заметно больше, чем в соед. с ковалентной связью (металлич. радиус атомов всегда больше ковалентного радиуса), а координационное число (число ближайших соседей) в кристаллических решетках металлов обычно 8 или больше 8. Для наиболее часто встречающихся кристаллических структур координационные числа равны 8 (объемноцентрированная кубическая), 12 (гранецентрированная кубическая и гексагональная плотно-упакованная). Расчеты параметров металлических решеток с использованием ковалентных радиусов дают заниженные результаты. Так, расстояние между атомами Li в молекуле Li2 (ковалентная связь) равно 0,267 нм, в металле Li-0,304 нм. Каждый атом Li в металле имеет 8 ближайших соседей, а на расстоянии, в раз большем,-еще 6. Энергия связи в расчете на один атом Li в результате увеличения числа ближайших соседей увеличивается с 0,96.10-19 Дж для Li2 до 2,9.10-19 Дж для кристаллич. Li.
Во многих металлах металлическая связь между атомами включает вклады ионной или ковалентной составляющей. Особенности металлической связи у каждого металла могут быть связаны, например, с электростатическим отталкиванием ионов друг от друга с учетом распределения электрических зарядов в них, с вкладом в образование связи электронов внутренних незаполненных оболочек переходных металлов, с корреляцией движения электронов в электронном газе и некоторыми другими причинами.
Металлическая связь характерна не только для металлов и их сплавов, но и для интерметаллических соединений, она сохраняется не только в твердых кристаллах, но и в расплавах и в аморфном состоянии.
Обычно в литературе металлическая связь описывается, как осуществленная посредством обобществления внешних электронов атомов и не обладающая свойством направленности. Хотя встречаются попытки (см. ниже ) объяснения направленной металлической связи т.к. элементы кристаллизуются в определенный тип кристаллической решетки.Почему атомы химических элементов объединяются так,а не иначе?Почему происходят аллотропические переходы (изменение типа кристаллической решетки)?Сколько электронов отдает атом в зону проводимости? Что есть металлическая валентность?
Пока невозможно в общем случае вывести из квантовомеханических расчетов кристаллическую структуру металла по электронному строению атома, хотя, например, Ганцхорн и Делингер указали на возможную связь между наличием кубической объемно-центрированной решетки в подгруппах титана, ванадия, хрома и наличием в атомах этих металлов валентных d- орбиталей. Нетрудно заметить, что четыре гибридные орбитали направлены по четырем телесным диагоналям куба и хорошо приспособлены для связи каждого атома с его 8 соседями в кубической объемноцентрированной решетке. При этом оставшиеся орбитали направлены к центрам граней элементарной ячейки и, возможно, могут принимать участие в связи атома с шестью его вторыми соседями /3/ стp. 99.
Первое координационное число (К.Ч.1) “8” плюс второе координационное число (К.Ч.2) “6” равно “14”.
Попытаемся связать внешние электроны атома данного элемента со структурой его кристаллической решетки, учитывая необходимость направленных связей (химия) и наличие обобществленных электронов (физика), ответственных за гальваномагнитные свойства.
Согласно /1/ стр.20, число Z- электрон проводимости от атома в зоне проводимости, получено авторами, предположительно, исходя из валентности металла по кислороду, водороду и обязано быть подвергнуто сомнению, т.к. экспериментальные данные по Холлу и модулю всестороннего сжатия близки к теоретическим только для щелочных металлов. ОЦК решетка, Z=1 не вызывает сомнений. Координационное число равно 8.
На простых примерах покажем, что на одну связь у алмаза при плотности упаковки 34% и координационном числе 4 приходится 34%:4=8,5%.
У кубической примитивной решетки плотность упаковки 52% и координационное число 6 приходится 52%:б=8,66%.
У кубической объемноцентрированной решетки плотность упаковки 68% и координационное число 8 приходится 68%:8=8,5%.
У кубической гранецентрированной решетки плотность упаковки 74% и координационное число 12 приходится 74%:12=6.16%, а если 74%:9=8,22%.
У гексагональной решетки плотность упаковки 74% и координационное число 12 приходится 74%:12=6,16%, а если 74%:9=8,22%.
Очевидно, что эти 8,66-8,22% несут в себе некий физический смысл. Оставшиеся 26% кратны 8,66 и 100% гипотетическая плотность упаковки возможна при наличии 12 связей. Но реальна ли такая возможность?
Внешние электроны последней оболочки или подоболочек атома металла образуют зону проводимости. Число электронов в зоне проводимости влияет на постоянную Холла, коэффициент всестороннего сжатия и т.д.
Построим модель металла-элемента так, чтобы оставшиеся, после заполнения зоны проводимости, внешние электроны последней оболочки или подоболочек атомного остова неким образом влияли на строение кристаллической структуры (например: для ОЦК решетки-8 "валентных" электронов остова, а для ГЕК и ГЦК -12 или 9).
Очевидно, что для подтверждения нашей модели необходимо сравнить экспериментальные и теоретические данные по Холлу, коэффициенту всестороннего сжатия и т.д.
ГРУБОЕ, КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ КОЛИЧЕСТВА ЭЛЕКТРОНОВ В ЗОНЕ ПРОВОДИМОСТИ МЕТАЛЛА - ЭЛЕМЕНТА. ОБЪЯСНЕНИЕ ФАКТОРОВ, ВЛИЯЮЩИХ НА ОБРАЗОВАНИЕ ТИПА РЕШЕТКИ МОНОКРИСТАЛЛА И НА ЗНАК ПОСТОЯННОЙ ХОЛЛА.
(Алгоритм построения модели)
Измерения поля Холла позволяют определить знак носителей заряда в зоне проводимости. Одна из замечательных особенностей эффекта Холла заключается, однако, в том, что в некоторых металлах коэффициент Холла положителен, и поэтому носители в них должны, видимо, иметь заряд, противоположный заряду электрона /1/. При комнатной температуре это относится к следующим металлам:: ванадий, хром, марганец, железо, кобальт, цинк, цирконий, ниобий, молибден, рутений, родий, кадмий, церий, празеодим, неодим, иттербий, гафний, тантал, вольфрам, рений, иридий, таллий, свинец /2/. Решение этой загадки должна дать полная квантовомеханическая теория твердого тела.
Примерно, как для некоторых случаев применения граничных условий Борна-Кармана, рассмотрим сильно упрощенный одномерный случай зоны проводимости. Вариант первый: тонкая замкнутая трубка, полностью заполненная электронами кроме одного. Диаметр электрона примерно равен диаметру трубки. При таком заполнении зоны, при локальном передвижении электрона, наблюдается противоположное движение "места" незаполнившего трубку, электрона, то есть движение неотрицательного заряда. Вариант второй: в трубке один электрон - возможно движение только одного заряда - отрицательно заряженного электрона. Из этих двух крайних вариантов видно, что знак носителей, определяемых по коэффициенту Холла, в какой-то степени, должен зависеть от наполнения зоны проводимости электронами.
На порядок движения электронов также будут накладывать свои условия и структура зоны проводимости, и температура, и примеси, дефекты, а для магнитных материалов и рассеяние на магнитных квазичастицах - магнонах.
Так как рассуждения наши грубые, учитываем в дальнейшем пока только наполнение зоны проводимости электронами. Заполним зону проводимости электронами так, чтобы внешние электроны атомных остовов оказывали влияние на образование типа кристаллизационной решетки. Предположим, что число внешних электронов на последней оболочке атомного остова, после заполнения зоны проводимости, равно числу атомов соседей (координационному числу) /5/. Координационные числа ГЕК, ГЦК (гексагональной и гранецентрированной) плотнейших упаковок 12 и 18, а объемноцентрированной решетки (ОЦК)8и14/3/. Для ГЕК и ГЦК рассмотрим также число 9!
Ключевые слова конспекта: Металлическая химическая связь: ион-атомы и электронный газ. Физические свойства металлов и их применение на основе этих свойств. Чёрные и цветные металлы. Сплавы.
Подавляющее число химических элементов периодической системы Д. И. Менделеева относятся к металлам:
- все s-элементы, кроме водорода и гелия;
- все d-элементы;
- p-элементы IIIА-группы, кроме бора;
- некоторые p-элементы IVA- (олово и свинец) и VA- (сурьма и висмут) групп, а также p-элемент VIIА-группы — полоний.
Анализ положения металлов в периодической системе и учёт особенностей строения их атомов позволяет сделать следующие выводы: атомы этих элементов содержат небольшое число электронов на внешнем слое (1—3), имеют сравнительно большой радиус атома и много свободных орбиталей, которые могут легко перекрываться. Поэтому валентные электроны свободно перемещаются от одних атомов, превращая их в ионы, к другим, связывая их.

В простых веществах-металлах осуществляется бесконечный процесс превращения атомов в ионы и обратно, который можно отразить с помощью схемы:
Эти же процессы происходят и в металлических сплавах.
Металлическая связь определяет и особое кристаллическое строение металлов и сплавов — металлическую кристаллическую решётку, в узлах которой расположены ион–атомы. Обобществлённые подвижные электроны не принадлежат какому–то определённому атому и способны перемещаться по всему объёму металла. В отсутствие в нём электрического поля эти электроны хаотически движутся и сталкиваются, чаще всего с ионами кристаллической решётки. В 1900 г. немецкий физик Пауль Друде предложил называть совокупность этих электронов электронным газом. Этот электронный газ прочно соединяет, как бы склеивает ионный остов металла. При механических нагрузках или нагреве газ не допускает разрыва металлической решётки, связывая положительные ионы. Поэтому при обработке металлов изменение их формы происходит без разрушения кристаллической решётки, так как её слои легко скользят один по другому.
Металлы электропроводны, потому что под действием электрического поля валентные электроны начинают направленное движение — возникает электрический ток. Металлы — это проводники первого рода, в отличие от растворов электролитов, которые относятся к проводникам второго рода.
Мы вряд ли представляем себе жизнь без электричества, которое поступает в каждый дом, в каждую квартиру по сети электрических проводов своеобразной кровеносной системе современной технической цивилизации. Лучше всего проводят электрический ток серебро, медь, золото, алюминий. Серебро и золото — дорогие металлы. Медь также недешёвый металл. Поэтому кабели линий электропередачи (ЛЭП) делают главным образом из алюминия.
Кстати, прочная опора линии электропередачи тоже металлическая. Прочность — одно из основных свойств большинства металлов, позволяющее использовать их в качестве конструкционных материалов. Один из наиболее прочных и в то же время лёгких металлов — титан. Этот металл и сплавы на его основе — незаменимые конструкционные материалы в самолётостроении и космической технике.
Все металлы теплопроводны. Это свойство, как и нетоксичность некоторых металлов, лежит в основе их применения для производства кухонной посуды: кастрюль, сковородок, противней. Батареи центрального отопления должны быстро нагреваться поступающей в них водой и эффективно отдавать теплоту окружающему воздуху, поэтому их тоже изготавливают из металла.
Самыми теплопроводными металлами являются те, которые хорошо проводят электрический ток: серебро, медь, золото, алюминий.
Металлы обладают металлическим блеском. Блестят они потому, что отражают лучи света, а не пропускают их, как стекло, и не поглощают, как сажа. Окраска большинства металлов серебристо–белая, так как они в равной степени отражают все лучи видимой части спектра. Золото и медь частично поглощают коротковолновое излучение, поэтому обладают окраской от жёлтой до красно–коричневой. Самые блестящие металлы — ртуть, палладий, серебро и алюминий, поэтому отражатели прожекторов, автомобильных фар и фонарей покрывают тонким слоем палладия, алюминия или хрома. Почти все измельчённые в порошок металлы, кроме магния и алюминия, теряют блеск и превращаются в серые или чёрные порошки.
Пластичность металлов в сочетании с блеском делают их незаменимым материалом для художников. Самым пластичным по праву считается золото. Из одного грамма этого металла можно вытянуть нить длиной 2 км или раскатать фольгу толщиной 0,00008 мм. Такой тонкий листочек даже в руки взять невозможно: он сразу прилипнет к коже. Это свойство находит своё применение: тонкими золотыми листочками покрывают купола церквей, скульптуры, деревянную резьбу.
Современная техника и промышленность нуждаются в металлических материалах с самыми разнообразными и трудно сочетаемыми свойствами, которых нет у чистых металлов. На помощь технологам приходят сплавы.
Например, из железосодержащих руд выплавляют чугун — сплав железа с углеродом, в котором массовая доля углерода составляет от 2 до 4%. Чугун — хрупкий материал, изделия из которого получают не ковкой, а литьём, как из пластмасс. Из чугуна изготавливают различные массивные конструкции: корпуса станков, турбин, детали двигателей, ограждения. Настоящее произведение искусства — ограды мостов и решётки парков Санкт–Петербурга.
Если из чугуна удалить излишек углерода и довести его содержание до 1—2%, получится сталь. В отличие от чугуна, она пластична, ковка, имеет гладкую блестящую поверхность. Сталь можно прокатать в тонкий лист или железнодорожный рельс, вытянуть в проволоку, согнуть уголком.
Для придания стали специфических свойств в неё добавляют другие металлы — так называемые легирующие добавки. Используя их, выплавляют сотни разных сортов стали. Нержавеющая сталь содержит хром и никель. В жаропрочную сталь добавляют вольфрам. Молибден придаёт стали твёрдость. Алюминий добавляют в сталь, идущую на изготовление кузовов автомобилей.
Сплав меди с оловом, бронза, обладает хорошими литейными свойствами. Из неё отливают не только колокола и художественные изделия, но и подшипники, вентили, клапаны и детали машин.
Сплав меди с цинком называют латунью. Она прочнее меди, устойчива к атмосферной коррозии. Из латуни изготавливают трубки, шестерни, армейские знаки отличия, химическое оборудование.
Нарядные столовые приборы, посуду, недорогие украшения изготавливают из мельхиора — сплава меди с никелем. Несмотря на то, что никеля в этом сплаве всего 20%, мельхиор лишён медного цвета и по внешнему виду напоминает серебро.
Сплав алюминия с медью, магнием и марганцем называют дуралюмин (дюраль) и используют в самолёто-, судо- и машиностроении.
Металлическая химическая связь характерна для металлов и их сплавов в кристаллическом состоянии. Образуется за счет обобществления валентных электронов. Для этого типа строения вещества не характерно образование направленных структурированных связей.
Следует отличать различные типы связи элементов кристаллов - металлическую, ионную и водородную, свойственную кристаллам льда.
Схема образования металлической связи на примерах
Механизм создания металлической связи предусматривает отрыв частично свободных электронов от атома с образованием катионов с положительным зарядом, формирующих “остов” кристаллической решетки и электронного облака. При этом металлический кристалл не приобретает положительного или отрицательного заряда.
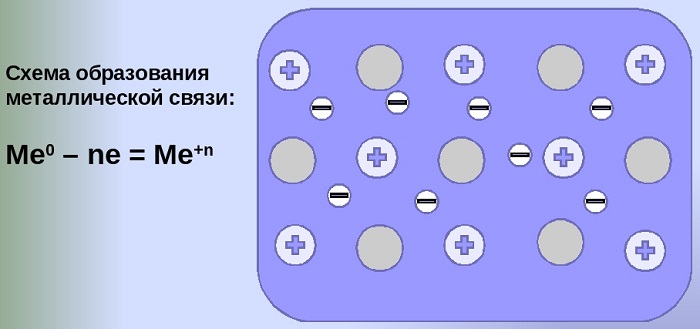
Общий случай формирования связывания металлических атомов в химии, соответствующий данному выше определению:
здесь n - число электронов, участвующих в образовании связи, как правило, от 1 до 3.
В левой части уравнения - атом металла, отдающий электроны, в правой - образовавшийся в результате ион.
Формула показывает, что в кристалле постоянно происходит присоединение и отдача электронов.
Схемы формирования связи на примере атомов различной валентности:
- K - e⁻ ⇆ K;
- Cu - 2e⁻ ⇆ Cu;
- Al - 3e⁻ ⇆ Al.
Отделяющиеся от атома электроны перемещаются на свободные валентные орбитали, которые обобществляются и позволяют всем электронам перемещаться в пределах кристалла. Отделение электронов выгодно атому с точки зрения энергетического баланса, так как позволяет сформировать электронно-стабильную оболочку.
Характерные кристаллические решетки
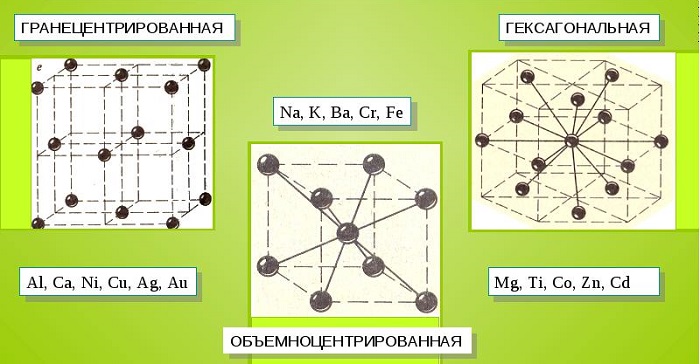
Металлические кристаллы подразделяются на 3 основных типа:
- Объемно-центрированную кубическую решетку, в которой, помимо размещения атомов в четырех вершинах куба, один из них размещается в центре объемной фигуры. Такой тип организации твердого вещества характерен для ряда металлов, включая K, Na и Li, вольфрам, хром, ниобий и др.
- Гранецентрированная кубическая решетка характеризуется расположением атомов в центре граней. Всего в ячейке задействовано 10 атомов, 4 в вершинах и 6 на гранях. Такая решетка встречается у меди, драгметаллов (серебра и золота) и металлов платиновой группы: Pd, Pt.
- Гексагональное строение решетки предполагает размещение атомов в углах и внутри 6-гранной призмы. Ячейка состоит из 15 атомов и свойственна магнию, кальцию, осмию, бериллию и ряду других металлических элементов.
Общими свойствами всех решеток являются высокая симметрия и плотная упаковка составляющих их атомов. Некоторые элементы периодической таблицы формируют уникальную структуру, например, элементарная ячейка In имеет тетрагональное строение.
Для сплавов, являющихся химическими соединениями, также характерно образование кристаллов перечисленных видов, при этом атомы каждого металла занимают определенное место в структуре.
Например, в сплаве никеля и алюминия атомы Al размещаются по углам, а атом Ni - в центре ОЦК ячейки. Свойства сплава и его структура влияют на класс прочности изделия, изготовленного из этого материала.
Физические свойства металлической связи
Физические характеристики металлических кристаллов обусловлены способностью обобществленных электронов свободно перемещаться внутри кристалла.

Характеристики, отличающие подобные вещества:
хорошая электропроводность, благодаря наличию условно свободного электронного облака;
высокая проводимость тепла;
низкая реакционная способность или инертность;
пластичность - большинство металлов можно гнуть и ковать.
Высокий уровень организации вещества обусловливает металлический блеск. Следует иметь в виду, что повышение прочности при пластической деформации и легировании приводит к образованию частично ковалентной связи.
При деформации могут возникать области повышенной прочности и низкими пластическими свойствами, похожие на вещества с ковалентной связью (например, алмаз).
Сходства и отличия металлической химической связи от ионной
Помимо рассматриваемой, металлы могут образовывать другие виды связи, включая простую ионную.
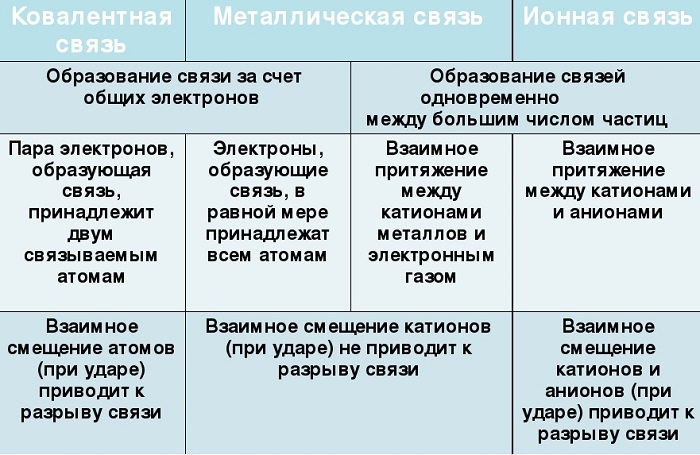
Их общие черты:
участие металлов, при этом металлическая связь формируется исключительно атомами металла, а ионная образуется между металлическим и неметаллическим элементами;
металл высвобождает электроны и становится катионом;
соединения могут существовать в кристаллической форме.
Кристаллы с ионным характером соединения отличают следующие параметры:
- В узлах размещаются как положительно, так и отрицательно заряженные ионы. Каркас металлической решетки формируют исключительно катионы.
- Узлы удерживаются за счет электростатического взаимодействия.
- При низких температурах кристаллические вещества, образованные за счет ионного взаимодействия, проявляют свойства диэлектриков (не проводят ток).
- Переход электронов с атома металла происходит на орбиты атома неметалла.
Характерный пример кристалла с ионной связью - поваренная соль, решетка которой сформирована из ионов Na⁺ и Cl⁻. Такие кристаллические вещества не обладают пластичностью и блеском.
Читайте также:

