Колоректальный рак реферат онкология
Обновлено: 18.05.2024
Для цитирования: Тимофеев Ю.М. Колоректальный рак: современные аспекты диагностики и лечения. РМЖ. 2004;11:653.
Литература
1. Ганичкин А.М. Рак толстой кишки.–Л.:Медицина,1970.–416 с.
2. Кныш В.И. Рак ободочной и прямой кишки.–М.:Медицина,1997.–304
с.
3. МакНелли П.Р. Секреты гастроэнтерологии:англ.– Моск-
ва,СПб.,1999.–1023 с.
4. Мартынюк В.В. Рак толстой кишки (заболеваемость, смертность,
факторы риска, скрининг) Практическая онкология:избранные лек-
ции.–СПб.,2004.–С.151–161.
5. Переводчикова Н.И. Химиотерапия метастатического колоректаль-
ного рака//Практическая онкология: избранные лек-
ции.–СПб.,2004.–С.230–244.
6. Пророков В.В., Малихов А.Г., Кныш В.И. Современные принципы ди-
агностики и скрининга рака прямой кишки //Практическая онколо-
гия:избранные лекции.–СПб.,2004.–С.162–167.
7. Стирнс М.В. Колоректальные новообразования:англ.–М.:Медици-
на,1983.–256с.
8. Тимофеев Ю.М., Зикиряходжаев Д.З. Злокачественные опухоли
анального канала.– Душанбе,1997.–380 с.
9. Федоров В.Д. Рак прямой кишки.–М.:Медицина, 1987.–320с.
10. Царьков П.В.,Воробьев Г.И., Одарюк Т.С. Место и роль расширен-
ной аорто–подвздошно–тазовой лимфаденэктомии в лечении рака
нижнеампулярного отдела прямой кишки.//Практическая онколо-
гия:избранные лекции.–СПб.,2004.–С.168–180.
11. Bertario L. Reducing colorectal cancer mortality by repeated faecal
occult blood test a nested case–control study
//Eur.J.Cancer/–1999.–Vol.35.–P.973–977.
12. Billingham B.P. Extended lymphadenectomy for rectal cancer: cure
vs quality of life // Int.Surg.–1994.–Vol.79,№1.– P.11–22.
13. Schrag D.,Weeks J. Costs and cost–effectiveness of colorectal cancer
prevention and therapy //Semin.Oncol.–1999.– Vol.26.–P.561–568.
14. Takahashi T., Veno M., Azekura K., Ota H. The lymphatic spread of
rectal cancer and effect of dissection:Japanese contribution and experience
//Soreide O., Norstein J. Rectal cancer
surgery.–Berlin,Heidelberg:Springer–Verlag.1997.–P.164–180.
Колоректальный рак (КРР) - это наиболее распространенная опухоль в колорек-тальной хирургии, третий по частоте встречаемости рак и вторая причина в структуре онкологической смертности. В связи с этим, диагноз рака ободочной кишки должен быть исключен практически при любом его симптоме.
Прямые факторы риска: сидячий образ жизни, курение, лучевой колит, состояние после формирования уретеросигмоидных анастомозов; пища с высоким содержанием жира/калорий/протеинов и алкоголь, низкое содержание клетчатки (вновь обсуждаемый вопрос); недостаток витамина D, инсоляции, кальция, фолатов. Популяционные факторы риска:
• Низкий и обычный риск (65-75%): бессимптомный - отсутствие факторов риска, отсутствие КРР у кого-либо из родственников первой степени родства.
• Умеренный риск (20-30%): КРР у одного родственника первой степени родства в возрасте до 55 лет или у двух и более родственников первой степени родства в любом возрасте, наличие крупного полипа (> 1 см) или множественных полипов любого размера, либо наличие в анамнезе резекции по поводу рака ободочной кишки.
• Высокий риск (6-8%): САТК, ННПРТК, ВЗК.
Эволюция от неизмененной кишки до диагностированного рака: 10 лет (в обычной популяции), 3-5 лет (ННПРТК). Теоретически, колоректальный рак (КРР) является полностью предотвратимой опухолью, так как канцерогенез - это медленный процесс, который проходит этап видимых (полипы) предшественников, а ободочная кишка доступна для полной эндоскопии. Руководства по скринингу разработаны, но их осуществление нельзя назвать выполненным, даже приблизительно.
Выбор оптимального лечения зависит от стадии и локализации опухоли, ее осложнений, ситуации (экстренная или плановая операция), наличия сопутствующих заболеваний и других патологических изменений ободочной кишки. Важность разграничения рака ободочной кишки (например сигмовидной ) и рака прямой кишки обусловлена планом лечения, поскольку в последнем случае определенную роль играет (нео-)адъювантная лучевая терапия.
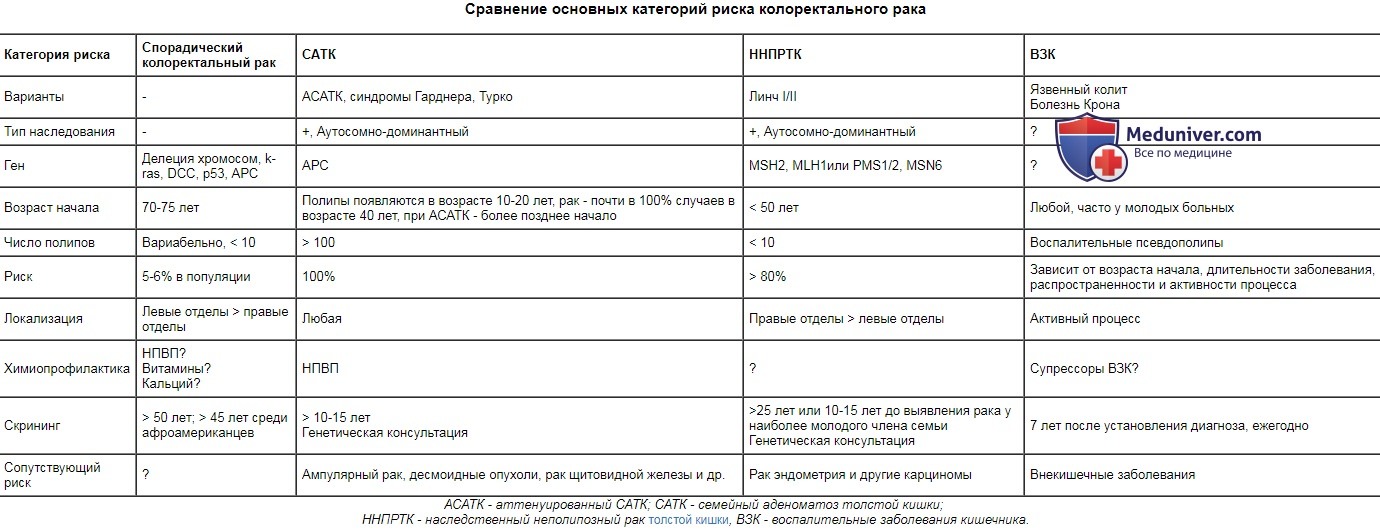
Сравнение основных категорий риска колоректального рака
| Категория риска | Спорадический колоректальный рак | САТК | ННПРТК | ВЗК | |
| Варианты | - | АСАТК, синдромы Гарднера, Турко | Линч I/II | Язвенный колит Болезнь Крона | |
| Тип наследования | - | +, Аутосомно-доминантный | +, Аутосомно-доминантный | ? | |
| Ген | Делеция хромосом, k-ras, DCC, р53, АРС | АРС | MSH2, MLH1или PMS1/2, MSN6 | ? | |
| Возраст начала | 70-75 лет | Полипы появляются в возрасте 10-20 лет, рак - почти в 100% случаев в возрасте 40 лет, при АСАТК - более позднее начало | 100 | 80% | Зависит от возраста начала, длительности заболевания, распространенности и активности процесса |
| Локализация | Левые отделы > правые отделы | Любая | Правые отделы > левые отделы | Активный процесс | |
| Химиопрофилактика | НПВП? Витамины? Кальций? | НПВП | ? | Супрессоры ВЗК? | |
| Скрининг | > 50 лет; > 45 лет среди афроамериканцев | > 10-15 лет Генетическая консультация | >25 лет или 10-15 лет до выявления рака у наиболее молодого члена семьи Генетическая консультация | 7 лет после установления диагноза, ежегодно | |
| Сопутствующий риск | ? | Ампулярный рак, десмоидные опухоли, рак щитовидной железы и др. | Рак эндометрия и другие карциномы | Внекишечные заболевания |
ННПРТК - наследственный неполипозный рак толстой кишки, ВЗК - воспалительные заболевания кишечника.
а) Эпидемиология колоректального рака:
• Ежегодная заболеваемость в США: 145000 новых случаев колоректального рака (КРР), 55000 смертей, обусловленных колоректальным раком (КРР) (9-10% от онкологической смертности по другим причинам).
• Средний риск заболевания в течение жизни: 1:18 американцев (5-6%). Пик заболеваемости - седьмое десятилетие жизни; тем не менее, 5% больных моложе 40 лет, 10% - моложе 50 лет. У 90% пациентов опухоли спорадические, у 10% имеется положительный семейный анамнез, у 1% - САТК. Колоректальный рак (КРР) излечим в 90% случаев при диагностике на ранних стадиях.
• Стадия на момент установления диагноза: I стадия - 25%, II стадия - 30%, III стадия - 35%, IV стадия -25%.

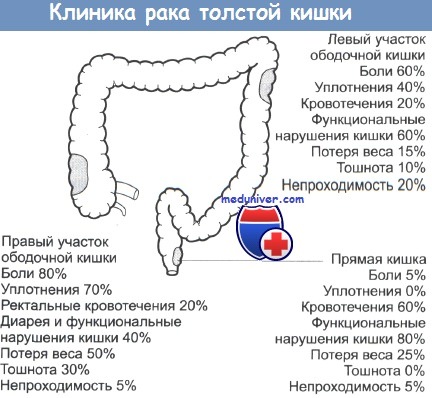
б) Симптомы колоректального рака:
• Наиболее часто бессимптомное течение => обычно симптомы появляются на поздних стадиях заболевания!
• Случайное выявление при колоноскопии.
• Симптомы: примесь крови, необъяснимая анемия, изменение частоты и формы стула, запоры, полная непроходимость, боль в животе, перфорация, инфильтрат в брюшной полости, потеря веса.
• Осложнения: массивное кровотечение, толстокишечная непроходимость, перфорация, печеночная недостаточность.
в) Дифференциальный диагноз колоректального рака:
• Симптомы обструкции и кровотечения могут быть следствием любых причин: ВЗК, в частности болезни Крона, других форм колита (ишемического, инфекционного, включая псевдомембранозный С. difficle-ассоциированный или лучевой колит), дивертикулита, СРК.
• Метастазирование в ободочную кишку опухолей желудка, поджелудочной железы, женских половых органов, почек, долькового инвазивного рака молочной железы; лейкемическая инфильтрация.
• Редкие опухоли: карциноид, лимфома, ГИСТ, меланома.
• Предраковые полипы: в частности ворсинчатые полипы, могут занимать большую площадь и всю окружность кишки.
• Доброкачественные заболевания: эндометриоз, пролапс/инвагинация, доброкачественные опухоли (липома), псевдообструкция (синдром Огилви).
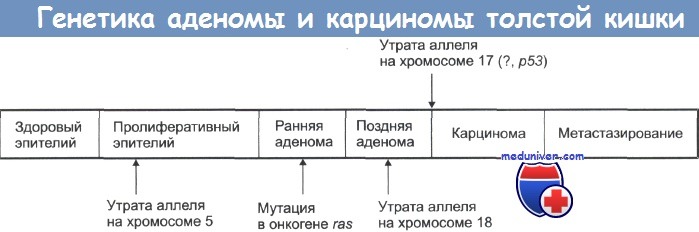
г) Патоморфология
Макроскопическое исследование:
• Полиповидное легкоранимое образование или изъязвленное кратерообразное образование с приподнятыми краями, различного размера и распространенности по окружности кишки. При ВЗК опухоль часто плоская с диффузным внутристеночным ростом.
• Путь метастатической диссеминации: лимфоваскулярный => лимфоузлы, гематогенный => система воротной вены => метастазирование в печень => метастазирование в легкие.
Микроскопическое исследование:
• В подавляющем большинстве случаев (>90%) опухоль представлена аденокарциномой. Редкие подтипы: слизистый или перстневидноклеточный рак, железисто-плоскоклеточный рак.
• Внутрислизистый рак (Тis) — carcinoma in situ = дисплазия высокой степени: рак не прорастает мышечную пластинку слизистой. Инвазивный рак: прорастание в собственную мышечную пластинку слизистой и глубже.
• Такие особенности роста, как лимфоваскулярная инвазия, периневральная инвазия, наличие депозитов опухолевых клеток вне лимфатических узлов - отрицательные прогностические факторы.
• Для адекватного стадирования необходимо исследование минимум 12-15 лимфоузлов в удаленном препарате.
Дополнительные исследования (необязательные):
• Рентгенконтрастные исследования (ирригоскопия с барием или гастрографином): неполная колоноскопия, выраженная обструкция, подозреваемая перфорация (=>водорастворимый контраст).
• Виртуальная колоноскопия: роль не определена, риск перфорации.
• МРТ, ПЭТ, ПЭТ-КТ: диагностическое значение не определено.
• Лабораторные исследования: анемия, функция печени (альбумин, ПТИ, АЧТВ), функция почек.
е) Классификация колоректального рака:
• Основанная на локализации в ободочной кишке.
• Основанная на стадии опухоли: локализованная, местнораспространенная (размер, прорастание в другие структуры), метастазы.
• Основанная на системе TNM.
ж) Лечение без операции рака ободочной кишки:
• Пациенты, неоперабельные в связи с наличием сопутствующих заболеваний.
• Пациенты, иноперабельные/инкурабельные в связи с распространенностью опухоли (например, канцероматоз) => симптоматическое лечение, возможно агентирование.
• Метастазы в печени с поражением > 50% паренхимы => паллиативная химиотерапия.

а - Злокачественный полип нижних отделов толстой кишки. Ректороманоскопия гибким эндоскопом.
б - Колоноскопическая картина геморрагического рака восходящей ободочной кишки.
в - Рак правой половины толстой кишки.
г - Колоноскопическая картина рецидива рака в области анастомоза после удаления опухоли прямой кишки.
з) Операция при колоректальном раке
Показания:
• Любой рак ободочной кишки (за исключением абсолютных противопоказаний).
• Даже при наличии генерализации желательно достижение локального контроля над опухолью, т.к. возможно выполнение условно радикальной симультанной или отсроченной метастазэктомии с лечебными целями.
Хирургический подход при раке ободочной кишки
а) Радикальное лечение:
• Онкологическая резекция с лимфаденэктомией: безопасные границы резекции >5 см, точный объем резекции зависит от локализации опухоли и путей лимфоваскулярного оттока:
- Слепая/восходящая кишка: правосторонняя гемиколэктомия с перевязкой правой ветви средней ободочной артерии.
- Печеночный изгиб/поперечно-ободочная кишка: расширенная правосторонняя гемиколэктомия с перевязкой средней ободочной артерии.
- Селезеночный изгиб:
1) расширенная левосторонняя гемиколэктомия с перевязкой средней ободочной артерии;
2) расширенная правосторонняя гемиколэктомия/субтотальная резекция ободочной кишки.
- Нисходящая кишка:
1) левосторонняя гемиколэктомия с перевязкой левой ветви средней ободочной артерии и нижнебрыжеечной/левой ободочной артерии;
2) субтотальная резекция ободочной кишки.
- Сигмовидная кишка: резекция сигмовидной кишки с перевязкой верхней прямокишечной или нижней брыжеечной артерии.
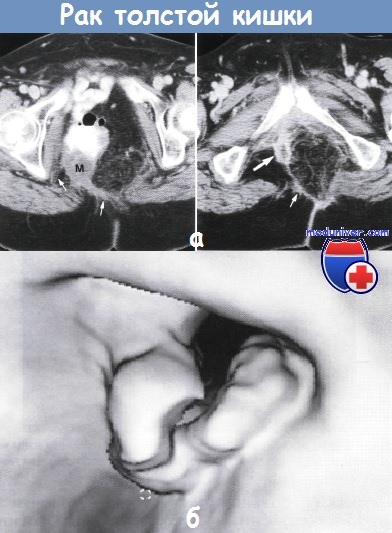
а - Рецидив рака прямой кишки после брюшно-промежностной резекции. Изображение через вертлужную впадину: в расширенной петле тонкой кишки установлено неоднородное образование (М) размером 3 см.
Опухоль инфильтрирует жировую клетчатку (показано стрелками) и правую стенку таза.
Изображение в области седалищно-лонных ветвей — небольшое мягкотканное образование (показано большой стрелкой) и тяжи опухоли (маленькая стрелка), инфильтрирующие тазовую клетчатку. Компьютерная томография
б - Рак толстой кишки.Виртуальная колоноскопия.
• Особые ситуации:
- Синхронные опухоли:
1) две раздельные резекции;
2) субтотальная резекция ободочной кишки.
- Опухоли, прорастающие в другие структуры: резекции eb-bloc.
- Метастазы в печени: симультанные резекции оправданы, если они технически выполнимы и переносимы больным (возможно отсроченные резекции).
- Профилактическая овариоэктомия не показана, но рекомендована при наличии видимых изменений в одном или обоих яичниках.
- Канцероматоз: резекция первичной опухоли, интраперитонеальный катетер как рутинная процедура не имеет смысла.
- Лапароскопический доступ эквивалентен открытому в опытных руках.
• Больной моложе 50 лет/ННПРТК:
1) субтотальная резекция/колэктомия с илеосигмоидным/ректальным анастомозом;
2) сегментарная резекция.
• САТК:
1) проктоколэктомия;
2) колэктомия с илеоректальным анастомозом, если нет рака прямой кишки или число полипов прямой кишки
Экстренное лечение колоректального рака:
• Рак правых отделов: хирургическое лечение, как и в плановой ситуации, первичный тонкотолстокишечный анастомоз.
• Рак левых отделов:
- Резекция с интраоперационным лаважем толстой кишки и первичным анастомозом.
- Установка стента для декомпрессии при обструкции левых отделов => резекция с формированием анастомоза в плановом порядке.
- Более расширенный объем операции, позволяющий сформировать тонкотолстокишечный анастомоз: субтотальная резекция ободочной кишки с первичным илеосигмоидным или илеоректальным анастомозом.
- Двухэтапное лечение:
а) операция Гартмана (=> реконструкция в плановом порядке);
б) формирование первичного анастомоза и проксимальная стома (=> закрытие стомы в плановом порядке);
в) проксимальная стома (=> резекция и ликвидация стомы в плановом порядке).
- Трехэтапное лечение (в основном не применяется): проксимальная стома (трансверзостома) => резекция и формирование анастомоза в плановом порядке (с сохранением отключающей стомы) => закрытие стомы в плановом порядке.
и) Паллиативное лечение:
• Сегментарная резекция.
• Проксимальная стома.
• Формирование обходного анастомоза.
• Стентирование.

л) Наблюдение и дальнейшее лечение:
- Экстренная операция: планирование последующих вмешательств после адекватного восстановления физического состояния и питания.
- Адъювантная химиотерапия: для III стадии и в отобранных случаях - при II стадии.
- Паллиативная химиотерапия: при IV стадии.
- Онкологическое наблюдение: колоноскопия через один год, в дальнейшем - в зависимости от клинических данных. Клиническое обследование и анализы крови (включая РЭА) каждые 3-6 месяцев. КТ органов брюшной полости/малого таза, рентгенография/КТ органов грудной полости - ежегодно.

Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Заболеваемость колоректальным раком стремительно растет с каждым годом. Считается, что основным фактором риска развития рака кишки являются особенности питания, основанные на большом потреблении животных белков и снижением в рационе растительных волокон.
Содержание:
В разных странах приняты специальные государственные программы скрининга колоректального рака, которые позволяют на ранних этапах диагностировать заболевание и эффективно его лечить. Однако многие люди пренебрегают профилактическими обследованиями и не придают достаточного значения первым проявлениям заболевания, что приводит к обращению к врачу на поздних стадиях болезни.

Колоректальный рак представляет собой злокачественную опухоль, развивающуюся в слизистой оболочке толстой или прямой кишки. По мере роста опухоль сужает просвет кишки, что проявляется запорами и кишечной непроходимостью, изъязвление опухолевого узла приводит к появлению сгустков крови в стуле или серьезному кишечному кровотечению.
Причины развития колоректального рака
- Непосредственные причины рака кишки не установлены, однако существует множество факторов риска его формирования:
- Особенности питания. Предполагается, что избыточное потребление легкоусвояемых углеводов и животных белков, недостаток растительной клетчатки и дефицит витаминов А и С в пище способствуют возникновению рака.
- Вредные привычки. Канцерогенные вещества, попадающие в организм человека с табачным дымом, имеют системное воздействие.
- Возраст. Пик заболеваемости приходится на 60-70 лет. В редких случаях заболевают и более молодые люди.
- Наследственная предрасположенность. Если близкие родственники страдали колоректальным раком, то с определенного возраста рекомендуется проходить регулярные профилактические осмотры с проведением колоноскопии. Кроме того, риск развития рака повышается при наличии некоторых врожденных заболеваний: синдром Гарднера, синдром Пейтца-Егерса, синдром Тюрко, семейный аденоматозный полипоз.
- Факторы, обусловленные образом жизни (избыточный вес, сидячая работа, недостаточная двигательная активность) так же могут увеличивать риск заболевания раком.
- Контакт с химическими веществами, такими как асбест и афлотоксин.
- Хронические воспалительные болезни кишечника (болезнь Крона, НЯК), полипоз толстой кишки.
Неконтролируемые деление и рост эпителиальных клеток, измененных под воздействием причинных факторов, ведут к формированию опухоли. Колоректальный рак может расти экзофитно (в просвет кишки), эндофитно (прорастать стенку кишки вглубь), иметь смешанную форму роста. Первичный опухолевый узел может быть одиночным, а может встречаться первично-множественная опухоль (наличие нескольких опухолевых узлов). Раковые клетки распространяются по организму (метастазируют) гематогенно в печень или лимфогенно в легкие, яичники, брюшину.
Симптомы колоректального рака
Рак кишки на начальных стадиях чаще всего протекает бессимптомно. Со временем у пациентов появляются неспецифичные симптомы, наблюдающиеся и при других заболеваниях:
- Ложные позывы на дефекацию (наиболее свойственны раку, локализующемуся в сигмовидной или прямой кишке).
- Чувство неполного опорожнения кишечника или чувство наличия инородного тела в прямой кишке.
- Нарушение эвакуаторной функции толстой кишки (запоры), вплоть до формирования кишечной непроходимости. Запоры могут чередоваться с жидким зловонным стулом. При кишечной непроходимости появляются тошнота, рвота, отрыжка, чувство тяжести и вздутие живота.
- Кишечные кровотечения, в том числе обнаружение прожилок крови в кале.
- Возможно развитие перфорации (сквозного повреждения стенки) толстой кишки.
- Патологические примеси в кале: кровь, слизь, гной.
- Анемия — снижение количества эритроцитов и уровня гемоглобина в крови. Возникает вследствие кровопотери, сопровождается бледностью кожи, одышкой, усталостью.
- Боли в животе. Появляются вследствие развития кишечной непроходимости, воспаления в кишке вокруг опухолевого очага, при распространении рака на соседние органы и структуры. При раке прямой кишки боли могут быть в области крестца и заднепроходном канале.
- Резкое похудание. Наиболее характерно для поздней стадии рака, когда он распространяется по брюшине и метастазирует (дает вторичные опухолевые отсевы) в другие органы.
- Общая слабость и быстрая утомляемость.
- На поздних стадиях может наблюдаться увеличение объема живота.
- При метастазировании присоединяются симптомы недостаточности органов, пораженных метастазами.
Бессимптомное начало и отсутствие специфичных симптомов колоректального рака затрудняют его своевременную диагностику.
Диагностика колоректального рака
При наличии вышеперечисленных жалоб и для постановки диагноза колоректального рака проводятся следующие диагностические мероприятия:
Клинический осмотр. Обращает на себя внимание увеличение объема живота, бледность кожи и видимых слизистых оболочек. Проводится прощупывание живота (в некоторых случаях опухоль удается прощупать через брюшную стенку), печени (при наличии в ней метастазов она увеличивается в размере, становится плотной, бугристой), лимфатических узлов (часто увеличиваются паховые лимфатические узлы). Проводится пальцевое исследование прямой кишки, которое позволяет прощупать опухоль, находящуюся в нижней части толстой или прямой кишке.

Лабораторные анализы
- Общий анализ крови (определяется количество эритроцитов и уровень гемоглобина).
- Биохимический анализ крови (определение уровня общего белка, альбумина, билирубина, АЛТ, АСТ, креатинина, мочевины).
- Определение опухолевых маркеров в крови. В отдельных случаях возможно определение уровня канцерэмбрионального антигена в крови.
- Тест на скрытую кровь (кровь, которую невозможно увидеть) в кале. Данное исследование дает возможность доказать присутствие крови в кале, однако не позволяет определить, откуда она поступает.
Инструментальные методы исследования.
- Ректороманоскопия — визуальный осмотр нижнего отдела толстой кишки и прямой кишки с помощью прибора специального назначения. Позволяет обнаружить опухоль, установить её протяженность и характер роста, а также взять прицельную биопсию для патогистологического исследования и подтверждения диагноза.
- Колонофиброскопия — эндоскопическое исследование толстой кишки. Позволяет визуально исследовать толстую кишку на всем протяжении и взять прицельную биопсию из всех подозрительных участков.
- Виртуальная колоноскопия — исследование толстой кишки без введения эндоскопа, с использованием современнейшего мультиспирального компьютерного томографа и построение трехмерного изображения кишки.
- Ирригоскопия — рентгенологическое исследование толстой кишки с помощью специально предназначенного прибора и использованием контрастного вещества. Данное исследование позволяет оценить рельеф слизистой оболочки толстой кишки, установить наличие опухоли, свищей и изъязвлений.
- Узи органов брюшной полости.
- Рентгенография органов грудной клетки (для выявления отдаленных метастазов).
- Компьютерная томография и магнитно-резонансная томография позволяют уточнить степень распространения опухоли на соседние органы и структуры, а также наличие метастазов колоректального рака в печень, лимфатические узлы и другие органы.
- Остеосцинтиграфия — лучевой метод исследования костей с использованием радиофармацевтического препарата. Применяется при подозрении на существование вторичных опухолевых отсевов в костях.
Стадии колоректального рака
Перед назначением лечения, для большей его эффективности, устанавливают стадию рака, которая выставляется согласно распространенности опухоли, поражению регионарных лимфоузлов, наличия отдаленных метастазов.
Стадия 0 — опухолевый узел небольшой величины, располагающийся в слизистой оболочке толстой кишки.
Стадия 1 — опухоль распространяется в подслизистый слой или в мышечный слой стенки кишки, но не метастазирует.
Стадия 2 подразделяется на подстадии:
Стадия 2А — опухоль прорастает серозную оболочку толстой кишки и врастает в периколическую клетчатку, но не метастазирует.
Стадия 2В — опухоль распространяется на висцеральную брюшину, не метастазирует.
Стадия 2С — опухоль распространяется на соседние органы и структуры, но не метастазирует.
Стадия 3 выставляется, когда обнаруживаются метастазы в регионарных лимфатических узлах при любой распространенности опухоли в стенке кишки. В зависимости от количества пораженных лимфоузлов выделяются подстадии А, В и С.
Стадия 4 выставляется при обнаружении метастазов в других органах. Выделяют подстадии:
4А — обнаружение метастазов в одном органе.
4В — метастазы в более чем одном органе и брюшине.
Лечение колоректального рака
Объем лечебных мероприятий, проводимых пациенту с колоректальным раком, напрямую зависит от размера и локализации рака, стадии опухолевого процесса, общего текущего состояния.
При 0 и первой стадии рака показано только хирургическое лечение (удаляется часть кишки с опухолью и регионарными лимфатическими узлами; если опухоль растёт только в пределах слизистой оболочки, возможно её эндоскопическое удаление).
При второй и третьей стадии рака толстой кишки после проведения хирургического лечения показано назначение нескольких курсов химиотерапии (лечение противоопухолевыми лекарственными препаратами), иногда химиотерапию или лучевую терапию проводят и до оперативного лечения, чтобы уменьшить размеры опухоли. При раке прямой кишки также возможно проведение лучевой терапии (высокоэнергетическое облучение).
При четвертой стадии рака главный метод лечения — химиотерапия. Операции проводятся при необходимости (при кишечной непроходимости, кровотечении из опухоли, перфорации стенки кишки). Химиотерапия может назначаться в комбинации с лучевой терапией.
В комбинации с химиотерапией или в качестве самостоятельного метода лечения при раке кишечника возможно использование препаратов направленного действия, подавляющих непосредственно рост раковых клеток — таргетная терапия (препарат Б — Маб).
Для коррекции симптомов колоректального рака назначается поддерживающая терапия: назначаются обезболивающие средства, диуретики, при кровотечениях иногда возможно проведение эндоскопической остановки кровотечения, для восстановления проходимости кишки при опухолевом сужении в некоторых случаях проводят установку стента (металлического каркаса) или выводят колостому (концевой отрезок кишки выводят наружу, на переднюю брюшную стенку).

Рак толстой кишки (колоректальный рак (КРР)) представляет собой злокачественную опухоль, развивающуюся из эпителиальной ткани.
Эпителиальная ткань присутствует повсеместно в организме и покрывает все внутренние органы. Также слизистая оболочка желудочно-кишечного тракта состоит из эпителиальной ткани.
Данная патология в сфере злокачественных новообразований занимает одно из ведущих мест в индустриально развитых странах (таких как США и Япония) и реже всего встречается в развивающихся странах Африки и Азии. Частота заболеваемости выше среди мужского населения, нежели женского. Несмотря на то, что рак толстой кишки чаще всего поражает пожилых людей, эта патология может быть выявлена и у людей молодого возраста.
В большинстве своем колоректальный рак (КРР) почти в 90% случаев представляет собой аденокарциному, злокачественную опухоль, которая развивается из железистых эпителиальных клеток ободочной и прямой кишки. Помимо этого, но гораздо реже, может встречаться плоскоклеточный, перстневидноклеточный и недифференцированный рак. Приблизительно в 60-65% всех случаев КРР возникает спорадически (то есть у лиц без семейного анамнеза КРР или при наличии ненаследственных генетических мутаций, которые увеличивают риск возникновения КРР) через приобретенные соматические генетические и эпигенетические аберрации. Колоректальный рак имеют наследственную природу, причем исследования близнецов показали наследуемость на уровне 35-40%. Приблизительно 25% КРР имеют семейную историю при отсутствии генетических синдромов. И лишь 5% - это наследственные раковые синдромы, к которым относится наследственный неполипозный колоректальный рак (HNPCC - hereditary nonpolyposis colorectal cancer, также известный как синдром Линча), или семейный аденоматозный полипоз (FAP - familial adenomatous polyposis), вызванный мутациями в редких, но высоко-пенетрантных генах (MLH1 и APC). Обнаруживаемые мутации в общих генетических вариациях с низкой пенетрантностью, ассоциированы лишь с 1% КРР. Следует отметить, что КРР с наследуемым компонентом не является полностью наследственным, а факторы окружающей среды так же участвуют в канцерогенезе.
За последние десятилетия расширилось наше понимание эпидемиологии, этиологии, молекулярной биологии и клинических аспектов КРР. И несмотря на это в мире ежегодно регистрируется около 1,8 миллионов новых случаев КРР. В связи с тем, что довольно часто КРР диагностируется на поздних стадиях заболевания, ежегодно умирает около 900 тысяч больных. Хотя КРР считается болезнью развитых государств, быстрый рост заболеваемости происходит в странах, переживающих экономическое развитие, что сопровождается изменениями в рационе питания и образе жизни. К таковым странам, к сожалению, относится и Россия. В развитых странах скрининг и современные методы лечения снижают заболеваемость и смертность, но несмотря на это данные показатели остаются на достаточно высоком уровне (заболеваемость 30,8 на 100 тысяч населения, смертность – 10,6 на 100 тысяч населения), среднемировые показатели заболеваемости и смертности от КРР 19,7 и 8,9 соответственно. В менее богатых странах существующие программы скрининга (а иногда и его отсутствие) и доступное медицинское лечение в настоящее время недостаточны для сдерживания неуклонного роста этих показателей.
Таким образом для правительства, организации здравоохранения и руководителей, важнейшим моментом является понимание движущих сил заболеваемости КРР и стратегии первичной и вторичной профилактики, необходимых для противостояния росту КРР. Важно также понимать, что рост заболеваемости не обязательно приводит к росту смертности. Несмотря на рост заболеваемости, в некоторых странах (например в Италии и Словении) показатели смертности от КРР снижаются, вероятно за счет качественного скрининга, что ведет к раннему выявлению КРР и улучшению лечения. И наоборот, в некоторых странах, с растущими показателями заболеваемости, но ограниченными медицинскими ресурсами (например в Бразилии и России), показатели смертности растут.
Возраст, пол и расовая предрасположенность.
Поскольку рак является болезнью старения, темпы развития заболевания и смерти возрастают после 50 лет, при этом около 90% случаев заболеваемости и смерти приходится на возраст после 50. Скорректированные по возрасту показатели выше у мужчин, чем у женщин, что дает приблизительно 1,4-кратную и 1,5-кратную разницу по заболеваемости (23,6 против 16,3 случаев на 100 000 человек в год) и смертности (10,8 против 7,2 случаев смерти на 100 000 человек в год), при этом разница становится значимой в возрастной группе после 50 лет. Более высокие показатели заболеваемости КРР у мужчин, вероятно связаны с тем, что мужчины чаще подвержены влиянию факторов окружающей среды, чем генетических факторов в колоректальном канцерогенезе, значимость наследственного фактора у мужчин оценивается в 28%, у женщин – 45%. Исследование миграции населения представляет большой вклад факторов окружающей среды в риск развития КРР у мужчин. Интересно, но факт, среди мужчин, мигрировавших в Швецию в возрасте до 30 лет, через пять десятилетий проживания в Швеции, показатели заболеваемости КРР снизились для мужчин-иммигрантов из стран с более высоким риском, таких как Норвегия, но увеличились для мужчин-иммигрантов из стран с более низким риском, таких как Финляндия. Тем не менее, смещение риска КРР в сторону принимающей страны было менее выраженным у женщин. В дополнение к их потенциально более высокой уязвимости к факторам риска окружающей среды, мужчины имеют более высокую подверженность таким факторам риска, как, например, ожирение, употребление алкоголя, курение и плохой рацион питания, но более низкую склонность в отношении использования скрининговых методов диагностики (анализ кала на скрытую кровь). Кроме того у женщин имеется механизм защитного эффекта эндогенного эстрогена.
Что касается расовой или этнической разрозненности популяций, в 2000-х годах было проведено исследование, которое продемонстрировало самый высокий уровень заболеваемости у чернокожих, и самый низкий – у людей с азиатскими и тихоокеанским происхождением (43,2 против 28,8 случаев на 100 000 человек в год) и смерти (18,6 против 9,9 случаев на 100 000 человек в год). Генетические факторы играют роль в этом расовом неравенстве, например новые нуклеотидные полиморфизмы (SNP), связанные с риском КРР, были идентифицированы в нескольких проведенных исследованиях среди чернокожего населения, хотя нынешнее понимание расовых различий в генетической архитектонике КРР ограничено из-за преобладания европеоидного населения в полногеномных поисках ассоциаций (GWAS). Однако нет данных о расовых различиях в отношении частоты соматических мутаций в известных генах (APC, KRAS,TP53, BRAF) и микросателлитной нестабильности (MSI) – высокого риска КРР, молекулярного подтипа КРР, вызванного мутацией в генах MMR (mismatch repair genes). Кроме того, среди лиц с синдромом Линча кумулятивный риск КРР был сходный между таковым у чернокожего и европейского населения. Более того самые высокие показатели КРР у афроамериканцев резко контрастируют с самыми низкими показателями, наблюдаемыми в Африке по сравнению с другими континентами. В совокупности данные свидетельствуют о том, что несоразмерное воздействие изменяемых факторов риска и медицинской помощи (например, скрининг и лечение) может, вероятнее всего, приводить к расовым различиям в уровне заболеваемости.
Подтипы КРР.
Хотя КРР развивается в одном органе, а именно в толстой кишке, это очень гетерогенное заболевание, состоящее из подтипов с различной этиологией и клиническими исходами. Традиционно подтипы КРР разделяются по локализации опухоли в трех сегментах ободочной и прямой кишки: проксимальной ободочной кишке (слепая кишка, восходящая ободочная кишка, изгиб печени и поперечная ободочная кишка), дистальной ободочной кишке (изгиб селезенки, нисходящая ободочная кишка и сигмовидная кишка) и прямой кишке. Исследования показали, что КРР в разных анатомических отделах имеет разные факторы риска (например, курение было связано с повышенным риском развития рака проксимального отдела толстой кишки и рака прямой кишки, но не с раком дистального отдела толстой кишки). Этиологическая гетерогенность КРР в зависимости от локализации может, частично, варьировать и зависеть от характеристик микробиоты, а также анатомических и физиологических характеристик толстой кишки. От проксимального отдела ободочной кишки до прямой кишки наблюдается прогрессивное увеличение pH, микробной нагрузки и обилия короткоцепочечных жирных кислот (а именно, микробных метаболитов), что может иметь различные последствия для колоректального канцерогенеза.
Генетика вносит вклад в индивидуальный риск, а на частоту КРР в популяции в значительной степени влияют модифицируемые факторы питания и образа жизни, потому что показатели могут сильно меняться в течение коротких периодов времени, низкие показатели заболеваемости КРР мигрантов быстро сравниваются с показателями заболеваемости принимающей страны. Исследователи Всемирного Фонда Рака (WCRF) и Американского Института Рака (AICR) пришли к выводу, что ожирение, низкая физическая активность, плохое питание (высокое содержание красного мяса, низкое содержание растительной клетчатки и цельного зерна, а также кальция в рационе), а также употребление алкоголя увеличивают риск КРР. Около половины заболевших КРР имеют в своем образе жизни модифицируемые факторы риска, кроме которых сюда можно отнести и курение. Совокупность этих факторов, вероятно, является движущей силой увеличения заболеваемости КРР по всему миру.
Ожирение.
Колоректальный рак, а в частности, рак ободочной кишки, является одним из немногих видов рака, для которых нехватка физической активности считается фактором риска. Нет однозначного ответа на сколько должна быть интенсивной и регулярной физическая нагрузка для профилактики КРР. Американское Общество по изучению Рака рекомендует взрослым заниматься как минимум 150 минут (3-5,9 metabolic equivalents of task) в неделю (умеренная интенсивность) или 75 минут интенсивной активности (более 6 MET). Интенсивность упражнений подразумевает определенный уровень затрат энергии посредством физической активности, а не конкретных режимов упражнений, так например увеличение количества упражнений на 5 МЕТ часов в неделю снижает риск развития КРР на 8%. Это может достигаться за счет благотворного влияния физических упражнений на моторику кишечника, иммунную систему, воспаление и метаболические гормоны – это прямое действие, но также может быть и опосредованный эффект за счет потери висцеральной жировой ткани (VAT). Среди взрослых, которые имели избыточный вес или ожирение, 3-4 месяца ежедневных прогулок или бега трусцой приводили к значимому уменьшению VAT, даже при отсутствии общего снижения веса. При этом по данным мета-анализа, значительная потеря висцеральной жировой ткани была связана с аэробными нагрузками, нежели с силовыми упражнениями. В когортном исследовании, где участники были разделены по интенсивности аэробной нагрузки и поднятии тяжестей, наибольшее снижение риска произошло в группе с самой активной нагрузкой около 30 МЕТ-часов в неделю. Независимо от уровня физической активности, длительное сидение или лежание (например просмотр телевизора) около 2-х часов в день увеличивает риск развития КРР на 7% (95% Сl 1,05-1.10).
Алкоголь.
Этанол в алкогольных напитках любого типа является уже доказанным фактором риска развития КРР, из-за входящего в его состав ацетальдегида – канцерогенного вещества. По данным мета-анализа 2018 года, в который было включено 14 когортных исследований из Северной Америки, Европы и Азии, было показано, что даже небольшое регулярное употребление алкоголя (≤1 напитка в день) было связано с незначительным риском развития КРР, но значимо больше чем при случайном употреблении или отсутствием употребления алкоголя (RR 1.04, 95% CI 1.01–1.06). Данная корреляция наблюдается чаще у мужчин из-за более высокого потребления алкоголя. Этанол в просвете кишки метаболизируется с микробной алкогольдегидрогеназой, что приводит к повреждению слизистой и регенеративной клеточной пролиферации. Фермент ADLH2, который синтезируется в печени, приводит к повышению циркулирующего ацетальдегида, который может достигать колоноцитов. Существует подтип данного фермента ADLH2*2, который широко распространен в Восточной Азии, и практически отсутствует в других частях света. В настоящее время убедительных доказательств роли ADLH2*2 в развитии КРР нет. Напротив, по данным одного из мета-анализов при наличии у носителей одного аллеля ADLH2*2 риск развития КРР снижается приблизительно на 20%. Возможно из-за побочных реакций при употреблении алкоголя (покраснение лица, тошнота, головная боль), эта категория лиц не злоупотребляют алкоголем, и вероятно, этот факт влияет на снижение риска заболеть КРР.
Курение.
Сигаретный дым содержит смесь соединений, которые с легкостью могут достигать слизистой кишечника, либо напрямую с пищей, либо систему кровообращения, и вызывать генетические и эпигенетические абберации. Риск заболеть КРР у курильщика повышается в прямой зависимости от стажа курения, и понижается после отказа от курения, приблизительно на 4% на каждые 10 лет. Курение по разному влияет на возникновение рака в различных локализациях толстой кишки, например, по данным когортного исследования 2018 года были сделаны выводы о значительном повышении риска развития рака проксимальных отделов ободочной кишки (RR 1.19, 95% CI 1.05–1.34) и рака прямой кишки (RR 1.27, 95% CI 1.14–1.42). Рак проксимальных отделов ободочной кишки, как правило, характеризуется MSI-high, CIMP-положит. и мутантным типом BRAF. И что интересно, курение повышает риск развития КРР этих типов рака в два раза и никак не влияет на риск развития CIMP-отрицат. и дикого типа BRAF КРР. Мутации в гене BRAF и CIMP-отрицат являются ключевыми молекулярными изменениями, определяющие путь развития зубчатых аденом, а курение связанно именно с риском развития зубчатых полипов, нежели классических аденом. Хочется добавить, что при изучении геномов, имеются изменения в структуре метилирования ДНК курильщиков и тех, кто никогда не курил, и примечательно имеются данные, что при отказе от курения аберрантное метилирование может восстановится до нормы. С другой стороны, имеются данные об отдаленном повреждающем воздействии полициклических ароматических углеводородов на структуру ДНК, и о возможно необратимом влиянии даже после отказа от курения.
Другим нерешенным вопросов остается непропорциональное распределение молекулярных подтипов КРР по анатомическим локализациям толстой кишки, вероятной причиной этого является микробиота, которая также меняется в зависимости от отдела толстой кишки. Было проведено сравнение образцов опухолевой ткани различной локализации, и получен различный бактериальный состав (например в проксимальных отделах большое количество Cl.difficille, в дистальных отделах преимущественно бактероиды). Аналогичная зависимость прослеживается и в образцах ткани у пациентов с полипами. Микробиота толстой кишки влияет на канцерогенез за счет воспаления. В исследовании, в которым сравнивался бактериальный состав образцов слизистой у пациентов с аденомами, аденокарциномами и с контрольной группой, у которых не было диагностировано новообразований в толстой кишке, а также уровень СРБ в плазме, было показано, что в последовательности здоровый-полип-рак увеличивается число микроорганизмов, в частности F. nucleatum и повышается уровень СРБ, и напротив, уменьшается число Eubacterium eligens. В настоящее время проводятся исследования о роли грибов (Malasseziomycetes) и вирусов (Orthobunyavirus) , и уже имеются данные об их возможном влиянии на риск развития КРР, однако пока делать однозначные выводы рано.
Химиопрофилактика КРР.
Скрининг – вторичная профилактика.
Скрининг может снизить заболеваемость и смертность от КРР путем раннего выявления КРР. Существует несколько методов скрининга, один из них, это известный во всем мире –фекальный гемокульт-тест (FOBT – fecal occult blood test, гваяковый тест), может обнаруживать в образце кала небольшое количество крови, которое указывает на наличие предраковых новообразований и рака толстой кишки. Разновидностью FOBT является иммунохимический FOBT (известный как фекальный иммунохимический тест FIT), является более предпочтительным по сравнению с более старшей гваяковой пробой. Он не требует никаких диетических ограничений перед использованием и имеет более высокую чувствительность в выявлении КРР (20 из 34 на 100.000 населения). Недавно появившийся метод скрининга – мультицелевой ДНК-тест кала (FIT-DNA), который выявляет как скрытые кровотечения (за счет иммуноанализа на гемоглобин) и молекулярные абберации (за счет молекулярного анализа на биомаркеры, такие как мутации KRAS. В исследовании у бессимптомных лиц со средним риском КРР, FIT-DNA имел более высокую чувствительность в выявлении распространенных предраковых поражений (42.4% против 23.8%, р
Читайте также:

