Кислородная коррозия внутри трубопроводов реферат
Обновлено: 05.07.2024
Трубопроводы и оборудование в процессе эксплуатации подвергаются процессу коррозии.
Коррозия металла труб происходит как снаружи под воздействием почвенного электролита (в почве всегда находится влага и растворённые в ней соли), так и внутри, вследствие примесей влаги, сероводорода и солей, содержащихся в транспортируемом углеводородном сырье. Коррозия металлических сооружений наносит большой материальный и экономический ущерб. Она приводит к преждевременному износу агрегатов, установок, линейной части трубопроводов, сокращает межремонтные сроки оборудования, вызывает дополнительные потери транспортируемого продукта.
При подземной прокладке стальные трубопроводы подвергаются почвенной коррозии. В грунтах почти всегда содержатся соли, кислоты, щелочи и органические вещества, которые вредно действуют на стенки стальных труб. В некоторых случаях такая коррозия может вызвать очень быстрое появление сквозных свищей в металле трубы и этим вывести трубопровод из строя, такие разрушения происходят особенно часто в трубопроводах, уложенных без достаточной защиты от коррозии.
Успешная защита трубопроводных систем от коррозии может быть осуществлена при своевременном обнаружении коррозионных разрушений, определении их величины и выборе защитных мероприятий. В начальный период эксплуатации состояние трубопровода определяется качеством проектирования и строительства. Влияние этих факторов уменьшается во времени и доминирующее значение приобретают условия работы трубопровода. В процессе работы изменение технического состояния транспортной магистрали происходит под воздействием эксплуатационных факторов, одним из которых является коррозия внутренней и внешней поверхности труб. При электрохимической защите подземных трубопроводов требуется выполнять ряд измерений: разности потенциалов труба-земля; поляризационного потенциала на трубопроводе; величину коррозионной активности грунтов; состояние изоляционного покрытия. Перечисленные измерения позволяют оценить остаточный эксплуатационный ресурс труб с учетом эффекта старения металла.
Периодичность процедур диагностирования и прогнозирования технического состояния нефтепровода зависит от времени эксплуатации трубопровода, поскольку, как правило, первые коррозионные проявления обнаруживаются после шести лет эксплуатации. В связи с этим составляются годовые планы и графики профилактического обследования подземных нефтепроводов, в результате которого выявляются дефекты поверхности трубопровода и его изоляционного покрытия. Обнаруженные крупные дефекты устраняются.
В работе рассмотрены виды коррозии, которой подвергаются трубопроводы при длительной эксплуатации, причины коррозии трубопроводов, а также способы защиты трубопроводов от коррозии.
1. Виды коррозии
Коррозия в зависимости от механизма реакций, протекающих на поверхности металла, подразделяется на химическую и электрохимическую.
Химическая коррозия представляет собой процесс разрушения металла при взаимодействии с сухими газами (газовая коррозия) или жидкими неэлектролитами (коррозия в неэлектролитах) по законам химических реакций и не сопровождается возникновением электрического тока. Продукты коррозии в этом случае образуются непосредственно на всем участке контакта металла с агрессивной средой.
При длительной эксплуатации трубопроводов, защищенных только изоляционным покрытием, возникают сквозные коррозионные повреждения уже через 5—8 лет после укладки трубопроводов в грунт вследствие почвенной коррозии, так как изоляция со временем теряет прочностные свойства и в ее трещинах начинаются интенсивные процессы наружной электрохимической коррозии. Суть процессов электрохимической коррозии заключается в следующем.
Электрохимическая коррозия (коррозионное разрушение) возникает под действием коррозионно-активной среды, разнообразна по характеру, вызывает большинство коррозионных разрушений трубопроводов и оборудования. Электрохимическая коррозия протекает с наличием двух процессов — катодного и анодного.
Электрохимическая коррозия является гетерогенной электрохимической реакцией. Она подразделяется на коррозию в электролитах, почвенную, электрокоррозию, атмосферную, биокоррозию, контактную. Во всех случаях окисление металлов происходит за счет возникновения электрического тока, протекают анодные и катодные процессы на различных участках поверхности и продукты коррозии образуются на анодных участках. При электрохимической коррозии одновременно протекают два процесса - окислительный (аноидный), вызывающий растворение металла на одном участке, и восстановительный (катодный), связанный с выделением катиона из раствора, восстановлением кислорода и других окислителей на другом. В результате возникают микрогальванические элементы, и появляется электрический ток, обусловленный электронной проводимостью металла и ионной проводимостью раствора электролита. Анодные и катодные процессы локализуются на тех участках, где их протекание облегчено. Причины, вызывающие электрохимическую неоднородность поверхности, весьма многочисленны: макро- и микронеоднородности металла; фазовая и структурная неоднородность сплавов; неоднородность и несплошность поверхностных пленок; неоднородность деформаций и напряжений. Кроме того, неоднородны и жидкие фазы, контактирующие с поверхностью.
Существующие виды коррозии металлов представлены на рис. 1.

Рисунок 1 - Виды коррозии: а - пятнами; б - язвенная; в - точечная; г -подповерхностная; д - структурно-избирательная; е -межкристаллитная; ж -коррозионное растрескивание
Согласно теории электрохимической коррозии разрушение металла обусловлено работой множества короткозамкнутых гальванических элементов, образующихся вследствие неоднородности среды и металла. При работе коррозийного элемента уменьшается разность начальных потенциалов, что сопровождается уменьшением коррозийного тока. Этот процесс называется поляризацией. Различают анодную и катодную поляризацию. При анодной поляризации в случае усиленного растворения металла ионы металла медленнее переходят в раствор, чем электроны отводятся в катодную область, и у поверхности электрода накапливаются положительные ионы металла, потенциал анода смещается в сторону положительных значений. Катодная поляризация сопровождается смещением потенциала электрода в отрицательную сторону и вызывается в основном малой скоростью электрохимической реакции соединения деполяризаторов с электронами. Участки, на которых растворяется металл, называются анодными, на них ион-атомы железа переходят в раствор, а на катодных - ток выводит в грунт. Электрохимические процессы на аноде и катоде различны, но взаимосвязаны, и, как правило, самостоятельно не протекают. Такая связанная система называется коррозионным микроэлементом. На анодных участках осуществляется окисление с образованием ионов металла Fe +2 , а на катодных под влиянием кислорода образуется гидроокись (в результате кислородной деполяризации).
В некоторых случаях возможны сложные процессы коррозии при одновременном воздействии двух или более факторов. К ним относятся коррозия под напряжением, щелевая, коррозионная эрозия, коррозионная кавитация. Скорость коррозионных процессов зависит от многих факторов, связанных как со свойствами, составом и строением металлического материала, так и со свойствами среды и внешними воздействиями. Для стальных трубопроводов, уложенных в грунт, скорость разрушения зависит во многом от кор-розионности грунта, в частности, от типа грунта, состава и концентрации веществ, содержания влаги, проникновения воздуха в грунт, структуры грунта, температуры и удельного сопротивления грунта, наличия в грунте бактерий, активизирующих коррозионные процессы. Оценивается коррозионная активность грунта по величине его удельного электросопротивления (чем меньше р, тем больше возможность коррозии). Важной характеристикой грунта является и водородный показатель рН среды (увеличение скорости коррозии при уменьшении рН). На интенсивность коррозии оказывает влияние неоднородность металла, механические напряжения, температуры и т.д. Неоднородность металла приводит к появлению коррозионных микроэлементов (микропар) в местах соприкосновения с грунтом, или в месте изменения физических свойств грунта. Коррозия может произойти и при образовании макропары из-за наличия макровключений - окалины, царапины, вмятины, наклепа, поперечных, продольных сварных швов, макроструктурной неоднородности физико-химических свойств почв, (например, при неоднородном поступлении кислорода к поверхности трубопровода, расположенном под полотном дороги). Существенное влияние на скорость коррозии оказывает жизнедеятельность анаэробных бактерий, особенно в почвах, содержащих большое количество сульфатных солей. В этом случае происходит образование серной кислоты и усиление коррозионных процессов.
Корро́зия (от лат. corrosio — разъедание) — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это разрушение любого материала, будь то металл или керамика, дерево или полимер. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Пример — кислородная коррозия железа в воде: 4Fe + 6Н2О + ЗО2 = 4Fe(OH)3. Гидратированный оксид железа Fe(OН)3 и является тем, что называют ржавчиной.
Файлы: 1 файл
Кислородная коррозия статья.doc
Корро́зия (от лат. corrosio — разъедание) — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это разрушение любого материала, будь то металл или керамика, дерево или полимер. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Пример — кислородная коррозия железа в воде: 4Fe + 6Н2О + ЗО2 = 4Fe(OH)3. Гидратированный оксид железа Fe(OН)3 и является тем, что называют ржавчиной.
Коррозия железа в воде с нейтральной или близкой к нейтральной средой, содержащей растворенный кислород, идет преимущественно с кислородной деполяризацией. В водопроводной воде только лишь около 3% железа коррозирует с водородной деполяризацией, а остальная часть – с кислородной.
Анодными участками являются зерна феррита, катодными – всевозможные включения в структуру металла, окалина и ржавчина на поверхности металла, потенциал которых значительно выше потенциала железа. На аноде происходит растворение металла, например железа, по реакции:
На катоде идет деполяризация электронов молекулами кислорода:
В процессе отвода электронов от катодного участка (процесса деполяризации) создаются предпосылки для развития коррозии, так как деполяризация катодного участка позволяет поддерживать разность потенциалов между катодом и анодом, уменьшается и может упасть до нулевых значений, при которых процесс коррозии прекращается.
На анодном участке накапливаются продукты коррозии – ионы Fe2+ , на катодном участке – ионы OH-. Там, где встречаются продукты катодной и анодной реакций, образуется гидрат закиси коррозирующего металла:
Образование осадка Fe(OH)2 при работе макропар обычно происходит в толще раствора, но в случае работы микропар можно ожидать образования гидроксида металла на корродирующей поверхности.
На поверхности металла в условиях эксплуатации при работе и останове оборудования в период контакта кислорода с водной средой возникает множество анодных и катодных участков, создающих условия для протекания коррозионных процессов. Скорость коррозии железа в воде, не содержащей растворенный кислород, практически ничтожна.
Железо с кислородом образует оксилы FeO, Fe3O4 и Fe2O3. Вюстит ниже 560-5700С распадается на – Fe и Fe3O4. В структуре вюстита есть вакансии ионов Fe2+, концентрация которых возрастает с ростом PO2, образовние вакансий связано с наличием в решетке FeO ионов Fe3+, магнетит Fe3O4 имеет структуру шпинели. Гематит Fe2O3.
В присутствии достаточного количества кислорода коррозия железа протекает с кислородной деполяризацией с образованием окиси трехвалентного железа, а при ограниченном доступе кислорода образуется смесь, содержащая окиси двух- и трехвалентного железа. Скорость коррозии пропорциональна концентрации растворенного в соответствующей среде кислорода. Один литр насыщенной воздухом воды может вызвать коррозию 1 см2 поверхности железа на глубину 0,022мм в случае образования окиси трехвалентного железа и на большую глубину при образовании смеси, состоящей из окиси двух- и трехвалентного железа.
Коррозия в присутствии кислорода – основной вид разрушения оборудования водоподготовки и теплосети. Она наблюдается и при их эксплуатации, и при простаивании.
Между концентрацией кислорода в непассивирующей воной среде при содержании его до 4мг/дм3 проявляется его пассивирующее действие. Наступление пассивного состояния металла характеризуется резким уменьшением скорости коррозии и значительным смещением потенциала металла в положительную сторону – для железа 0,2-0,3 до 0,5-2,5 В.
Установлено, что коррозионный процесс в чистом конденсате при 20-600С практически не сопровождается выделением водорода. Значительное выделение его наблюдается только при 800С, однако повышение рН до 9,0 резко уменьшает скорость процесса при этой сравнительно высокой температуре. При концентрации О2 около 90мг/дм3 водородная деполяризация существенна только при 400С и выше.
Кислород выполняет двойственную роль в процессах коррозии металлов. С одной стороны, он служит мощным деполяризатором катодных участков коррозионных элементов и тем самым ускоряет протекание коррозии при условии, если катодный процесс является контролирующим фактором. С другой стороны, кислород, окисляя металл, повышает стабильность защитных пленок и, следовательно, может снижать скорость коррозии. Чем выше концентрация кислорода в растворе, тем больше возможность образования прочных защитных пленок на поверхности стали и увеличения стационарного потенциала. Вследствие этого участки металла, получающие больше кислорода, выполняют роль катода по отношению к участкам поверхности металла, которые омываются водой с малой концентрацией кислорода, и возникает так называемая макропара неравномерной аэрации, вызывающая дополнительное разрушение металла. В данном случае разрушению подвергается часть поверхности, которая получает меньше кислорода и, следовательно, выполняет роль анода.
На поверхности стали появляются язвы, которые характерны для кислородной коррозии в условиях работы теплоэнергетического оборудования. Здесь роль анодов выполняют язвы, где и сосредоточивается коррозионное разрушение. В результате в отдельных точках поверхности происходит быстрое проникновение коррозии в глубь металла, даже при умеренных его весовых потерях.
В кислых средах пленки из окислов железа нестойкие, а поэтому их защитная роль с понижением значения рН уменьшается. В щелочных же растворах, даже при небольшой концентрации кислорода, коррозионный процесс может прекратиться полностью.
При низких концентрациях весь молекулярный кислород восстанавливается на металлической поверхности и действует как простой деполяризатор. При увеличении содержания кислорода в воде закрытой системы в присутствии депассиваторов скорость коррозии стали увеличивается пропорционально его концентрации.
В некоторых случаях растворенный кислород благоприятствует замедлению коррозионного процесса. Усиленный доступ кислорода уменьшает скорость коррозии железа в фосфате натрия вследствие образования фосфатного покрытия, а также в 0,1н. растворе хлорида натрия при относительно высоких скоростях движения раствора в результате пассивирования.
Растворы нитритов, нитратов, солей железа и меди, перекиси водорода и других окислителей действуют как деполяризаторы и стимулируют коррозию.
Способность сплава пассивироваться под действием кислорода или других окислителей зависит от его состава. С увеличением содержания хрома в сплаве железо-хром потенциал, при котором металл переходит в пассивное состояние, смещается в отрицательную сторону, что приводит к расширению пассивной области. С ростом концентрации хрома скорость растворения сплава в пассивной области уменьшается.
Кислород, растворенный в электролите, может оказывать существенное влияние на скорость коррозии аустенитной нержавеющей стали. Следует, однако, отметить, что кинетика анодного процесса стали 1Х18Н9Т в нейтральной, кислой и щелочной средах, а также в растворах хлоридов не зависит от наличия или отсутствия кислорода в электролите. Так, исследование кинетики анодного процесса стали 1Х18Н9Т показало, что в растворах 1,0н. сульфата натрия, 0,15н.соляной кислоты, 1,0н. гидроокиси натрия анодная поляризационная кривая не изменяется при деаэрации среды и уменьшении концентрации кислорода ниже 0,02мг/дм3. Уменьшение концентрации кислорода с 10 до 0,02мг/дм3 не изменяет скорости растворения металла ни в пассивном, ни в активном состоянии, ни в области перепассивации. Аналогичные результаты получены при температуре 3000С. Способность стали пассивироваться в деаэрированных средах позволяет полагать, что наличие кислорода, растворенного в электролите, необязательно для наступления пассивации.
При повышении рН до 9,6 скорость коррозии при отсутствии кислорода практически равна нулю. Растворение железа в воде, при рН
Кислородная коррозия является самым распространенным видом разрушения металла котла, ей подвергаются, все элементы котла, изготовленные из углеродистых и низколегированных сталей, которые контактируют с водой практически с любым содержанием в ней кислорода. В случае литания котла недеаэрированной водой или неудовлетворительной работы деаэратора при эксплуатации котлов коррозия приобретает опасный характер лишь при содержании кислорода в питательной воде, превышающем 20 мкг/кг. Коррозия может сопровождаться образованием локальных язв с диаметром до 5 и редко —до 10 мм, как. правило, закрытых рыхлым слоем ржавчины.
Кислородная язвенная коррозия развивается в глубь металла. Значительные. язвы коррозии встречаются под влажным шламом (в торцах барабанов и в коллекторах).
При эксплуатации котлов кислородная коррозия наблюдается в основном на входных участках экономайзеров, и при содержании кислорода более 0,3 мг/кг она появляется на остальной части экономайзера, в барабане котла и даже в опускных трубах.
На внутренней поверхности барабана образуются бугорки — ржавчина коричневого цвета, под которой обычно имеется слой оксидов железа черного цвета. При очистке этих мест - стальной щеткой обнаруживается язвина, которая, если не принять меры, может увеличиваться вплоть до образования свищей. Наибольшее количество язвин обнаруживают в паровом пространстве барабана, в местах переменного уровня воды, под коробками сепарационных устройств, на головках заклепок и др.
Кислородная коррозия барабанов может происходить в период ремонта котла и при нахождении, его в резерве. В последнем случае коррозию называют стояночной. Стояночная коррозия может образоваться как в котлах, наполненных водой, так и в котлах без воды. В первом случае она возможна, если в воде имеется растворенный кислород, а во втором — если стенки барабана влажные и к ним имеется доступ кислорода.
При температуре воды 40—75 °С, как правило, йоража-> ется одновременно воздушное и водяное пространство барабана, а при 40 °С и ниже коррозия поражает водяное пространство. Во всех случаях коррозия особенно интенсивно образуется на границе раздела вода — воздух, т. е. на ватерлинии и петли недренируемого перегревателя. Если возникают затруднения в установлении происхождения кислородной коррозии, необходимо вырезать участки труб из петель перегревателя, которые при простаивании заполнены водой и часто имеют солевые отложения.
При выявлении коррозионных язв в вырезанных участках труб можно полагать, что подобные поражения в других местах котла вызваны протеканием стояночной коррозии. Значит, коррозия петель перегревателя является индикатором стояночной коррозии всего котла. Если обнаружены язвы на входных участках экоиомайзерных труб, то это говорит о том, что коррозия вызвана поступлением в котел кислорода во время работы, а не при его простаивании;'поражение в петлях перегревателя в данном случае отсутствуют.
На практике часто выявляются коррозионные поражения металла смешанного характера в виде язв стояночной и рабочей коррозии, которые взаимно усиливают протекание коррозии. Интенсивной коррозии подвергаются элементы котлов после гидравлического испытания на заводах - изготовителях и монтажных площадках. Оставшаяся вода часто является причиной серьезных язвенных поражений металла до включения в работу котла.
Длительное хранение блоков на монтажной площадке без их консервации может привести к опасной коррозии до монтажа котла.
Влияние кислорода на скорость коррозии металла проявляется в двух противоположных направлениях. Во-первых, кислород увеличивает скорость коррозионного процесса, так как является мощным деполяризатором катодных участков, во-вторых — оказывает пассивирующее действие на - поверхность металла. Побочными процессами при воздействии кислорода на металл являются образование пар неравномерной аэрации и резкое снижение концентрации ионов F2+ из-за окисления их до Fe34*. Оба эти& процесса способствуют развитию коррозии.
Кислородная коррозия металла паровых котлов может быть предотвращена термической деаэрацией и термической деаэрацией с последующей обработкой воды сульфитом натрия для устранения остаточного кислорода (суль - фитирование воды). Выбор наиболее приемлемого способа для предупреждения кислородной коррозии производится с учетом параметров и мощности котлов, а также специфики их эксплуатации.
Для предупреждения аварий из-за коррозионных повреждений питательных трубопроводов и пароводяного тракта с давлением до 3,9 МПа паропроизводительностью 2 т/ч и более Правилами по котлам [1] нормируется содержание кислорода в питательной воде в зависимости от применяемых в котельных агрегатах экономайзеров, которое не должно превышать: 100 мкг/кг для котлов без экономайзеров и с чугунными экономайзерами, 30 мкг/кг для котлов со стальными экономайзерами.
На тепловых электростанциях содержание кислорода в питательной воде (до точки ввода обескислороживающих химических реагентов) в соответствии с правилами технической эксплуатации электрических станций и сетей Минэнерго СССР не должно превышать 20 мкг/кг для котлов с давлением 10 МПа и выше.
Выполнение приведенных нормативов обеспечивается обработкой воды в деаэраторах. Содержание кислорода в воде при ее кипении равно нулю. При температуре воды ниже температуры кипения содержание растворенного в ней кислорода тем выше, чем больше недогрев.
При обслуживании деаэраторной установки необходимо следить за давлением и температурой в баках-акумулято- рах. Нормальным считается уровень воды в деаэраторных баках, достигающий 3/4 высоты верхнего водоуказательного стекла.
І Водоуказательные стекла должны быть всегда чистыми, не реже 1 раза в смену их следует продувать. Задвижки на линиях перелива деаэраторов необходимо держать открытыми, работоспособность их проверять не реже одного раза в 10 дней,
Недопустимы перегрузки, переполнение деаэраторов и работа на перелив, а также вибрация деаэраторов, появ^- ление гидравлических ударов в колонках и баках. Не реже двух раз в смену следует производить отбор проб питательной воды из баков для определения содержания в ней кислорода. Периодически определяют также содержание С02 в деаэрированной воде.
Наличие свободного диоксида углерода в питательной воде паровых котлов недопустимо.
Один раз в смену следует проверять исправность клапанов регуляторов уровня и перелива предохранительных клапанов на деаэраторах, коллекторе греющего пара, а также на трубопроводах сбросов из растопочных сепараторов котла в деаэраторы.
Трубопроводный транспорт - самый распространенный способ доставки жидких и газообразных сред в мире. Небольшие внутренние трубопроводы есть в каждом современном доме, в населенных пунктах построены сети надземных и подземных распределительных трубопроводов, все регионы нашей страны соединены системой магистрального трубопроводного транспорта. Трубопроводы транспортируют воду, нефть и нефтепродукты, газ и т.д. В нашей стране был построен даже уникальный трубопровод транспорта аммиака. Большинство отечественных эксплуатируемых трубопроводов - металлические, главная причина их разрушений - коррозия, а видов коррозии - множество. В данном обзоре мы кратко рассмотрим основные виды коррозии трубопроводов в зависимости от их назначения, а также немного поговорим о последствиях коррозионных аварий.

Итак, мы начинаем. В данном обзоре, разделенном на несколько частей, мы отдельно и подробно рассмотрим возможные механизмы коррозии следующих видов трубопроводов, классифицированных по их функциональному назначению:
- магистральные трубопроводы;
- промысловые трубопроводы месторождений нефти и газа;
- трубопроводы систем отопления, горячего и холодного водоснабжения;
- трубопроводы промышленных сточных вод.
Начнем, пожалуй, с наиболее простых с коррозионной точки зрения объектов - магистральных трубопроводов транспорта нефти, газа, аммиака, нефтепродуктов и т.д.
Коррозия магистральных трубопроводов
Итак, ГОСТ выделяет 3 вида участков магистральных трубопроводов, подверженных особым коррозионным опасностям: участки высокой коррозионной опасности, участки повышенной коррозионной опасности и коррозионно-опасные участки. Среди критериев ГОСТ, касающихся механизмов коррозии и позволяющих отнести некоторые участки трубопроводов к особо опасным участкам, можно выделить следующие критерии участков повышенной коррозионной опасности:
- блуждающие токи от источников постоянного тока;
- микробиологическая коррозия;
- коррозионное растрескивание под напряжением.
Дополнительно, ГОСТ относит к участкам повышенной коррозионной опасности участки прокладки магистральных трубопроводов, на которых может резко возрасти опасность обычной почвенной коррозии:
- участки трубопроводов в засоленных почвах любого района страны (солончаковых, солонцах, солодях, сорах и др.);
- участки трубопроводов на участках промышленных и бытовых стоков, свалок мусора и шлака;
- участки трубопроводов с температурой транспортируемого продукта выше 303 К (30 °С).
Обобщая вышесказанное, а также многолетний опыт эксплуатации и диагностики, можно резюмировать, что на магистральных трубопроводах подземной прокладки в основном реализуются следующие виды коррозионного разрушения:
- почвенная электрохимическая коррозия;
- коррозия блуждающими токами от источников постоянного тока;
- коррозия блуждающими токами от источников переменного тока (на участках пересечений и реже сближений с ВЛ 110 кВ и выше);
- коррозионное растрескивание под напряжением (свойственно преимущественно магистральным газопроводам);
- микробиологическая коррозия (на участках, где почва вокруг трубопровода заражена микроорганизмами).
Почвенная электрохимическая коррозия
Коррозия подземных трубопроводов протекает по электрохимическому механизму, базирующемуся на возникновении разности потенциалов между различными участками трубопровода, и, как следствие, возникновении тока коррозии. В результате протекания тока коррозии участки металла на анодных зонах растворяются и переходят в грунт, где впоследствии взаимодействуют с почвенным электролитом, образуя ржавчину.
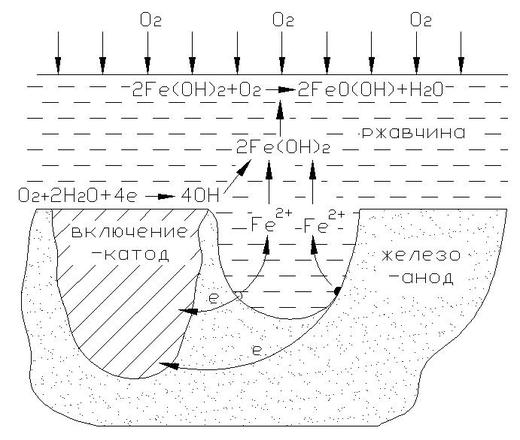
Механизм электрохимической коррозии
Одной из наиболее важных особенностей трубопроводов, с точки зрения коррозии, является их большая протяженность. При своей большой протяженности подземные линии проходят через почвы различного состава и строения, различной влажности и аэрации. Все это создает возможность возникновения значительных разностей потенциалов между отдельными частями подземной линии. Так как трубопроводы имеют высокую проводимость, то на них легко образуются коррозионные гальванопары, имеющие иногда протяженность в десятки и даже сотни метров.
Так как при этом часто создаются большие плотности тока на анодных участках, это сильно увеличивает скорость коррозии. Существенным для развития коррозии оказывается и то, что подземные линии укладываются на такой глубине, где всегда сохраняется некоторая влажность, обеспечивающая течение коррозионных процессов. На глубине заложения трубопроводов температура редко снижается ниже 0 0 С и это также способствует коррозии. Благоприятствует развитию коррозии на подземных трубопроводах и наличие на поверхности труб прокатной окалины, которая далеко не всегда удаляется при очистке.
Было установлено наличие прямой зависимости между площадью, подвергающейся коррозии, и глубиной коррозионного разрушения. Это объясняется тем, что на большей поверхности металла существует большая возможность создания более тяжелых коррозионных условий. В частности, этим объясняется, что другие стальные подземные сооружения, помимо трубопроводов, при прочих равных условиях разрушаются электрохимической коррозией медленнее.
Коррозионная агрессивность самих почв определяется их структурой, гранулометрическим составом, удельным электрическим сопротивлением, влажностью, воздухопроницаемостью, рН и др. Обычно коррозионную агрессивность грунта по отношению к углеродистым сталям оценивают по удельному электрическому сопротивлению грунта, средней плотности катодного тока при смещении электродного потенциала на 100 мВ отрицательнее коррозионного потенциала стали, градиенту естественных потенциалов свободной коррозии на участке трубопровода.
Коррозия блуждающими токами от источников постоянного тока
Блуждающие токи - это токи антропогенного происхождения, протекающие в земле и в подземных металлических конструкциях. Такие токи возникают за счет утечек в землю токов эксплуатируемых устройств и сооружений, работающих на постоянном токе, в частности железных дорог на постоянном токе, электросварочных аппаратов, систем катодной защиты сторонних объектов и т.д., и т.п. Как известно, электрический ток всегда стремится двигаться по пути наименьшего сопротивления, поэтому при наличии в зоне распространения блуждающих токов в земле подземных протяженных металлических трубопроводов, электропроводность которых в разы больше электропроводности почвы, блуждающий ток будет протекать именно по ним. В наиболее удачном месте (с точки зрения того же самого принципа наименьшего сопротивления) блуждающий ток стечет с трубопровода обратно в землю и вернется к своему источнику. При этом участок трубопровода, из которого блуждающий ток выходит в землю, является анодом, а та часть трубопровода, где блуждающий ток попадает в него, является катодом. На анодных участках блуждающие токи повышенной плотности вызывают значительные коррозионные повреждения трубопроводов, скорость коррозии на них практически неограниченна и может достигать гигантских значений 10-20 мм/год.
Коррозия блуждающими токами от источников переменного тока
Данный вид коррозии встречается в местах сближения и параллельного следования ВЛ напряжением 110 кВ и выше и магистральных трубопроводов. Это явление уже подробно освещено на нашем сайте в специальном обзоре и в настоящей статье дополнительно рассматриваться не будет.
Коррозионное растрескивание под напряжением (КРН) или стресс-коррозия
Коррозионное растрескивание под напряжением в магистральных трубопроводах (в основном газопроводах) развивается в результате одновременного воздействия на металл коррозионной среды и растягивающих напряжений. Благодаря проведенным исследованиям, в настоящее время сформировалась водородно-коррозионная теория развития КРН в трубопроводах.
Формирование и развитие микротрещин в металле происходит в результате наводораживания трубной стали в местах дислокаций и вакансий кристаллической решетки и роста в них внутреннего давления до значений, превышающих эквивалент энергии связи атомов решетки. Само наводораживание происходит вследствие протекающих процессов диффузии протонов (H+), образующихся в результате гидролиза воды при повышенных потенциалах катодной защиты, диссоциации ряда неорганических соединений, таких как гидрокарбонаты, гидросульфиды и сульфиды, нитраты, аммонаты, фосфаты и т.д., жизнедеятельности сульфатвосстанавливающих организмов.
После раскрытия трещин на поверхности трубы в местах повреждения изоляционного покрытия трубопровода происходит ускорение трещинообразования за счет коррозионного влияния электролита грунта, проникающего в трещины.
Конечный этап деструкции (включая долом трещин) контролируется условиями механической нагрузки на трубопровод, напряженно-деформированным состоянием трубной стали, а также ее прочностными характеристиками.
Микробиологической коррозией (или биокоррозией) называют коррозию металла, которая возникает в результате жизнедеятельности микроорганизмов. В почвах и природных поверхностных водах содержится огромное количество микроорганизмов - бактерии, грибки, водоросли, простейшие и т.д. В настоящее время установлено, коррозию металла инициируют в большинстве случаев именно бактерии из-за высокой скорости их размножения и активности в химических преобразованиях окружающей среды. Для протекания процесса микробиологической коррозии вызывающие её бактерии должны находиться во влажной или водной среде, также им нужен азот, минеральные соли и ряд других элементов. Необходимо наличие вполне определённых внешних условий, при которых они начинают активно размножаться вблизи трубопровода, таких как:
- температура;
- давление;
- освещённость;
- концентрация водородных ионов;
- концентрация кислорода.
Микроорганизмы могут вызывать коррозию путём продуцирования веществ, вызывающих коррозию (например, кислот), создавая на поверхности металла условия, которые обуславливают появление на поверхности металла разности потенциалов и образования дополнительных анодных и катодных зон, с дальнейшим протеканием коррозионного процесса по электрохимическому механизму.
В случае магистральных трубопроводов наиболее часто встречается микробиологическая коррозия, инициируемая сульфатвосстанавливающими бактериями. Под действием этих бактерий на трубах образуются отдельные каверны. Продукты коррозии имеют чёрный цвет и запах сероводорода. Они содержат около 40% двухвалентного железа и 5% серы в виде сульфидов. Сульфатвосстанавливающие бактерии присутствуют практически во всех грунтах, но заметный коррозионный процесс происходит только тогда, когда присутствует их относительно большое число.
Итак, в настоящей статье мы кратко изложили виды и механизмы коррозии магистральных трубопроводов. Продолжение начатой темы, посвященное водопроводным системам, читайте здесь .
Читайте также:

