Фенол и его производные реферат
Обновлено: 04.07.2024
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам
Выберите документ из архива для просмотра:
Выбранный для просмотра документ фенолы2.doc
Муниципальное бюджетное общеобразовательное учреждение средняя общеобразовательная школа с. Хмелинец Задонского муниципального района Липецкой области
Фенолы: свойства, применение, вред
ученица 11 класса
Братищева Анна
Учитель химии
Воронина Г.Д.
Тема работы: свойства, применение и вред класса фенолов.
Актуальность: с развитием науки химия все прочно и прочно укрепляется в нашей жизни. Особое место в ней занимает такой класс веществ как фенолы. Их значение невозможно переоценить, потому как сфера их влияния очень широка. Поэтому необходимо знать, с какими веществами мы сталкиваемся каждый день, какова опасность отравления ими и как обезопасить себя от негативного влияния этих веществ.
Объект: класс фенолов
Предмет: характерные свойства и применение
Цель: доказать значимость фенолов в быту и промышленности
Задачи: 1) дать определение классу фенолов;
2) рассмотреть номенклатуру и изомерию;
3) изучить классификацию фенолов;
4) проанализировать строение молекулы;
5) выявить физические свойства;
6) выделить химические свойства;
7) описать основные методы синтеза фенола;
8) установить сферы применения данного класса веществ;
9) определить вред фенолов для здоровья человека и экологии;
10) описать симптомы отравления и оказание первой помощи.
Гипотеза: благодаря особенностям строения молекулы и химическим свойствам фенолы незаменимы в науке, производстве, медицине и повседневной жизни.
1. Класс фенолы.
Фенолы – это производные ароматических углеводородов, молекулы которых содержат одну или несколько гидроксильных групп, непосредственно соединенных с бензольным кольцом.
Первый представитель гомологического ряда фенолов - окси-бензол C6H5OH называют обычно просто бензолом или карболовой кислотой.
2. Изомерия и номенклатура фенолов
Возможны 2 типа изомерии:
изомерия положения заместителей в бензольном кольце

изомерия боковой цепи (строения алкильного радикала и числа радикалов)
Для фенолов широко используют тривиальные названия, сложившиеся исторически. В названиях замещенных моноядерных фенолов используются также приставки орто-, мета- и пара -, употребляемые в номенклатуре ароматических соединений. Для более сложных соединений нумеруют атомы, входящие в состав ароматических циклов и с помощью цифровых индексов указывают положение заместителей.
3. Классификация
Различают одно-, двух-, трехатомные фенолы в зависимости от количества ОН-групп в молекуле:


В соответствии с количеством конденсированных ароматических циклов в молекуле различают сами фенолы (одно ароматическое ядро – производные бензола), нафтолы (2 конденсированных ядра – производные нафталина), антранолы (3 конденсированных ядра – производные антрацена) и фенантролы:

4. Строение молекулы

Фенильная группа C6H5 – и гидроксил –ОН взаимно влияют друг на друга.

Неподеленная электронная пара атома кислорода притягивается 6-ти электронным облаком бензольного кольца, из – за чего связь О–Н еще сильнее поляризуется. Фенол - более сильная кислота, чем вода и спирты.
В бензольном кольце нарушается симметричность электронного облака, электронная плотность повышается в положении 2, 4, 6. Это делает более реакционноспособными связи С-Н в положениях 2, 4, 6. и – связи бензольного кольца.
5. Физические свойства
Большинство одноатомных фенолов при нормальных условиях представляют собой бесцветные кристаллические вещества с невысокой температурой плавления и характерным запахом. Фенолы малорастворимы в воде, хорошо растворяются в органических растворителях, токсичны, при хранении на воздухе постепенно темнеют в результате окисления.
Фенол C6H5OH (карболовая кислота) — бесцветное кристаллическое вещество на воздухе окисляется и становится розовым, при обычной температуре ограниченно растворим в воде, выше 66 °C смешивается с водой в любых соотношениях. Фенол — токсичное вещество, вызывает ожоги кожи, является антисептиком.
6. Химические свойства
I. Свойства гидроксильной группы
Кислотные свойства – выражены ярче, чем у предельных спиртов (окраску индикаторов не меняют):
· С активными металлами-
2C6H5-OH + 2Na → 2C6H5-ONa + H2
C6H5-OH + NaOH (водн. р-р) ↔ C6H5-ONa + H2O
! Феноляты – соли слабой карболовой кислоты, разлагаются угольной кислотой –
C6H5-ONa + H2O + СO2 → C6H5-OH + NaHCO3
По кислотным свойствам фенол превосходит этанол в 106 раз. При этом во столько же раз уступает уксусной кислоте. В отличие от карбоновых кислот, фенол не может вытеснить угольную кислоту из её солей
C6H5-OH + NaHCO3 = реакция не идёт – прекрасно растворяясь в водных растворах щелочей, он фактически не растворяется в водном растворе гидрокарбоната натрия.
Кислотные свойства фенола усиливаются под влиянием связанных с бензольным кольцом электроноакцепторных групп (NO2-, Br-)
2,4,6-тринитрофенол или пикриновая кислота сильнее угольной
II. Свойства бензольного кольца
1). Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях поведения гидроксигруппы (см. выше), но и в большей реакционной способности бензольного ядра. Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно, в орто- и пара-положениях (+М-эффект ОН-группы):
Поэтому фенол значительно активнее бензола вступает в реакции электрофильного замещения в ароматическом кольце.
Нитрование. Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов:

При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота):

Галогенирование. Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол):

Конденсация с альдегидами. Например:

2). Гидрирование фенола
C6H5-OH + 3H2 Ni, 170ºC → C6H11 – OH циклогексиловый спирт (циклогексанол)
III. Качественная реакция - обнаружение фенола
6C6H5-OH + FeCl3 → [Fe(C6H5-OH)3](C6H5O)3 + 3HCl
светло- фиолетовый раствор
7. Синтез фенола
1. Получение из галогенбензолов. При нагревании хлорбензола и гидроксида натрия под давлением получают фенолят натрия, при дальнейшей обработке которого кислотой образуется фенол:
С6Н5―Сl + 2NaOH → C6H5―ONa + NaCl + Н2О.
2. При каталитическом окислении изопропилбензола (кумола) кислородом воздуха образуются фенол и ацетон:

Это — основной промышленный способ получения фенола.
3. Получение из ароматических сульфокислот. Реакция проводится при сплавлении сульфокислот с щелочами. Первоначально образующиеся феноксиды обрабатывают сильными кислотами для получения свободных фенолов. Метод обычно применяют для получения многоатомных фенолов:

8. Сферы применения
Разбавленные водные растворы фенола (карболка (5%)) применяют для дезинфекции помещений, белья. Являясь антисептиком, широко применялся в европейской и американской медицине в период 2 мировой войны, но из-за высокой токсичности в настоящее время использование сильно ограничено.
Раствор фенола используют в качестве дезинфицирующего средства (карболовая кислота). Двухатомные фенолы – пирокатехин, резорцин (рис. 3), а также гидрохинон (пара-дигидроксибензол) применяют как антисептики (антибактериальные обеззараживающие вещества), вводят в состав дубителей для кожи и меха, как стабилизаторы смазочных масел и резины, а также для обработки фотоматериалов и как реагенты в аналитической химии.
В виде отдельных соединений фенолы используются ограниченно, зато их различные производные применяют широко. Фенолы служат исходными соединениями для получения разнообразных полимерных продуктов – феноло-альдегидных смол (рис. 7), полиамидов, полиэпоксидов.
На основе фенолов получают многочисленные лекарственные препараты, например, аспирин, салол, фенолфталеин, кроме того, красители, парфюмерные продукты, пластификаторы для полимеров и средства защиты растений.
Широко используется в молекулярной биологии и генной инженерии для очистки ДНК. В смеси с хлороформом ранее использовался для выделения ДНК из клетки.
В настоящее время можно выделить несколько основных направлений использования фенола. Один из них – производство лекарственных средств.
Большинство этих лекарств — производные получаемой из фенола салициловой кислоты: o-HOC6H4COOH. Самое распространенное жаропонижающее — аспирин не что иное, как ацетилсалициловая кислота. Эфир салициловой кислоты и самого фенола тоже хорошо известен под названием салол.
При лечении туберкулеза применяют парааминосалициловую кислоту (сокращенно ПАСК) . Ну и, наконец, при конденсации фенола с фталевым ангидридом получается фенолфталеин, он же пурген.
9. Вред фенолов
Опасность фенола для здоровья человека заключается в том, что он оказывает негативное воздействие на нервную систему. Фенольные пары и пыль, а также раствор фенола, раздражают глаза, слизистые оболочки дыхательных путей, а также кожные покровы. Если фенол попадает в организм, то его всасывание происходит в считанные секунды даже в случае его прохождения через те участки кожи, которые не повреждены.
Буквально через несколько минут после попадания в организм, фенол оказывает паралитическое воздействие на головной мозг человека, а именно – на ткани головного мозга. Первые симптомы отравления фенолом – недолго длящееся возбуждение, после чего наступает паралич дыхательного центра организма. Следует отметить, что попадая в организм даже в минимальном количестве, фенол может вызвать кашель, сильную головную боль, тошноту и общую слабость. Что касается тяжелых случаев отравления этим веществом, то его характерными признаками являются потеря сознания, затруднение дыхания, омертвение роговицы глаза и также сокращением частоты пульса, судорогами и холодным потом.
Сегодня фенол является одним из наиболее опасных для здоровья человека веществ, и, к сожалению, достаточно широко распространенным. Для того, чтобы избежать негативного воздействия фенола на организм и отравления этим материалом, следует свести возможность контакта с ним к минимуму.
При приобретении строительных и отделочных материалов рекомендуется внимательно ознакомиться с их составом – как правило, вероятность наличия фенола особенно высока у материалов, изготовленных на основе полимеров. Рекомендуется выбирать только качественные строительные материалы, избегая подозрительно дешевой продукции. Практически всегда низкая цена свидетельствует о низком качестве продукции, и, как следствие, о том, что в ее составе содержатся вредные вещества. Кроме того, следует обращать внимание и на марку производителя: известные фабрики всегда имеют экологические сертификаты и изготавливают свою продукцию в соответствии с самыми современными требованиями к ее безопасности для здоровья человека. Таким образом, приобретая отделочные или строительные материалы от известных производителей, можно быть уверенным в том, что приобретается экологически чистый и безопасный материал, в составе которого нет вредных веществ, в том числе, и фенола.
10. Симптомы отравления фенолом и первая помощь
При остром отравлении, сопровождающем попадание фенола на кожу или вдыхание его паров, наблюдается сильное жжение в местах, подвергшихся его непосредственному воздействию. Проявляются ожоги слизистых тканей; возникает сильная боль в области рта, в глотке, животе; тошнота, рвота, понос; резкая бледность, слабость, отек легких; возможны острые аллергические проявления; артериальное давление понижено; развивается сердечно-легочная недостаточность, возможны судороги; моча бурая, быстро темнеет на воздухе.
Первая помощь – снять одежду (желательно сразу под душем), промыть пораженное место большим количеством воды. Прикрыть места ожогов фенолом чистой белой тканью. Если брызги фенола попали в глаза, необходимо обильно промывать их водой не менее 15 минут. Промыть желудок водой, внутрь дать активированный уголь. Спирт и вазелиновое масло противопоказаны. Во время стационарного лечения больному даются обволакивающие средства и анальгетики, подается О2 с обеспечением адекватной вентиляции легких, производится коррекция водноэлектролитного баланса.
Хроническое отравление фенолом приводит к анорексии – прогрессирующей потере веса; вызывает диарею, головокружение, трудности при глотании, обильное отделение слюны. При хроническом отравлении фенолами отмечено темное окрашивание мочи. Ученые, исследовавшие последствия фенольных отравлений указывают, что в результате длительного пребывания под воздействием фенола человек может чувствовать боли в мышцах, слабость. Печень у таких людей увеличена. Хроническое отравление фенолом вызывает поражения центральной нервной системы, нервные расстройства, сопровождаемые головными болями и потерей сознания, а также поражения почек, печени, органов дыхания и сердечно-сосудистой системы.
В нашей стране ПДК фенола в жилой зоне составляет 0,03 мг/м3 (СанПин 2.1.2.1002-00), а в воздухе рабочей зоны – 0,3 мг/ м3.
Запах фенола – сильный и сладковатый – начинает ощущаться, если концентрация фенола в воздухе превышает 0.04 ppm (0.000004%)
Помните, если вас настораживает неприятный запах недавно приобретенной вещи, если вам кажется, что ваше здоровье после покупки мебели или недавнего ремонта пошатнулось, будет лучше вызвать специалиста-эколога, который проведет все нужные исследования и даст необходимые рекомендации, чем пребывать в тревоге и сомнениях, опасаясь за свое здоровье и здоровье своих близких.
Фенолами называют соединения общей формулы Ar-OH. Они отличаются от спиртов тем, что в них гидроксильная группа непосредственно присоединена к ароматическому кольцу. В зависимости от количества гидроксильных групп фенолы различаются по атомности: одноатомные, двухатомные, трехатомные и т.д., для бензола до шестиатомных. Для метилфенолов принято специальное название - крезолы.




Фенол 4-Метилфенол (п-крезол) a-Нафтол b-Нафтол
Производные фенолов широко распространены в природе. Тимол является антисептиком и используется в парфюмерии. Эвгенол содержится в различных эфирных маслах, в том числе в гвоздичном масле.


Ароматическое ядро, непосредственно связанное с гидроксильной группой оказывает сильное влияние на ее поведение. Это влияние так велико, что фенолы и спирты представляют собой разные классы органических соединений. Они отличаются, прежде всего, по кислотности. Значения рКа большинства спиртов составляет около 18, в то время как фенолов - менее 11. Сравним, например, циклогексанол и фенол:

рКа = 18 рКа = 9.9
Фенолы являются более сильными кислотами, чем вода, в то время как спирты более слабыми, чем вода. В отличие от спиртов фенолы со щелочью дают соли – феноксиды (феноляты), не разрушающиеся водой, но разлагающиеся более сильной угольной кислотой.


Приведенные реакции используются для разделения фенолов, спиртов и карбоновых кислот. Фенолы, содержащие электроноакцепторные группы в ядре, имеют большую кислотность, чем сам фенол. Большая кислотность фенолов по сравнению со спиртами может быть объяснена тем, что электронная плотность в них с атома кислорода смещена на бензольное кольцо.
1. Реакции нуклеофильного замещения ароматических соединений
Нитрогруппа обладает сильно выраженным электроноакцепторным характером и оказывает значительное влияние на атомы и группы, находящиеся по отношению к ней в о- и п-положениях. Так, при нагревании нитробензола с порошкообразным КОН получается смесь о- и п-нитрофенолов:

(7)

(8)
Реакция проходит по механизму нуклеофильного замещения:

(М 2)

Замещаемый водород должен покидать молекулу с парой электронов, т.е. уходить в виде гидрид-аниона. Гидрид-анион окисляется избытком нитробензола:

(9)
Хорошим нуклеофильным реагентом является гидроксиламин. При его использовании применять специальные меры для удаления гидроксид-аниона не требуется. Из тринитробензола в водноспиртовом растворе по этой реакции получается 2,4,6-тринитроанилин или пикрамид:

(10)
а из a-нитронафталина _ 4-нитро-1-аминонафталин:

(11)
К реакциям нуклеофильного замещения атома водорода в ароматическом кольце относится синтез салициловой кислоты из бензойной под действием пероксида водорода.

(12)
Бензойная кислота Салициловая кислота
Из реакций нуклеофильного замещения электроноакцепторных групп в аренах, не содержащих активирующих групп, наибольшее значение имеют реакции замещения сульфогруппы. Сплавлением щелочных солей сульфокислот с твердыми щелочами и цианидами натрия и калия получают, соответственно, фенолы и арилцианиды.

(13)

(14)
2. Способы получения фенолов
Фенол - один из важнейших продуктов промышленной органической химии; он используется в качестве сырья в синтезе ряда важнейших продуктов, начиная с аспирина и кончая важнейшими пластиками. Мировое производство фенола превышает 3 миллиона тонн в год. Некоторое количество фенола и крезолов выделяют из легкого масла каменноугольной смолы. Используется несколько промышленных методов получения фенола.
2.1 Кумольный метод (Сергеева)
Большую часть фенола в настоящее время производят из изопропилбензола – кумола. Окислением кумола воздухом получают гидроперекись кумола, разлагающуюся под действием водных растворов минеральных кислот на фенол и ацетон. Кумол синтезируют из бензола и пропилена.

(15)

(16)

(17)



(М 3)


(М 4)



Аналогично ведет себя гидроперекись втор-бутила.
2.2 Гидролиз арилгалогенидов
Хлор в хлорбензоле малоподвижен и поэтому гидролиз ведут 8%-ным раствором NaOH в автоклаве при 250оС в присутствии солей меди:

(18)

(19)
По методу Рашига хлорбензол получают окислением бензола в присутствии хлороводорода:

(20)
Гидролиз хлорбензола осуществляют перегретым паром в присутствии медного катализатора. Образующийся при этом хлороводород возвращают на первую стадию процесса:

(21)
Гидролиз в присутствии щелочи проходит при более низкой температуре, но при этом теряется ценная соляная кислота, сохраняющаяся в методе Рашига.
2.3 Сплавление арилсульфонатов со щелочью
При сплавлении со щелочью арилсульфонаты претерпевают реакцию замещения:

(13)
Бензолсульфокислота Бензолсульфонат натрия
Превращение фенолята натрия в фенол осуществляется с помощью диоксида серы, который образуется на второй стадии:

(20)
Фенол получают в виде водного раствора, из которого его выделяют дистилляцией. Этот метод синтеза фенола является самым старым (1890 г.). Метод используется для получения и других фенолов, например:

(21)
Фенолы – органические соединения. Они в небольших количествах есть в природе. Основную массу фенола и производных на его основе получают синтетическим путём.
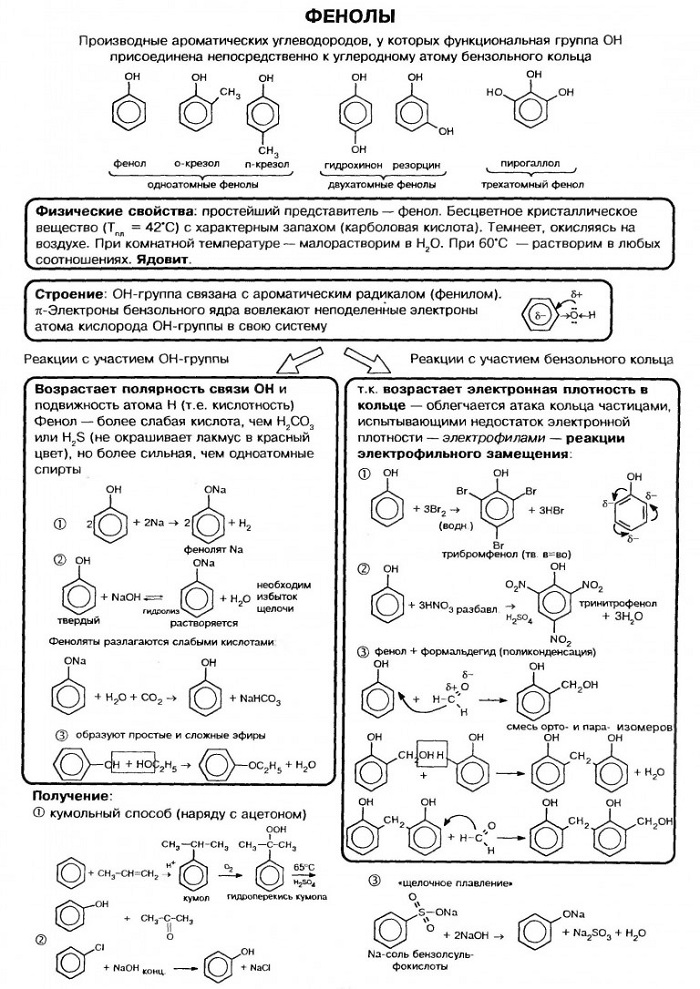
Что такое фенол
К фенолам относят производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с фенил радикалом. Они могут иметь одну или несколько гидроксогрупп.

Самым простым представителем этой группы соединений считают фенол. Он и дал название классу веществ. Это же соединение называют гидроксибензолом.
Общая и структурная формулы
Состав веществ можно выразить общей формулой С6Н6-n(ОН)n.
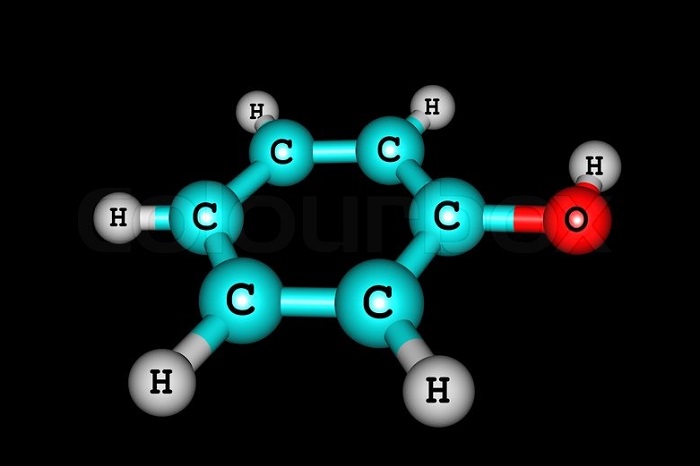
Простейший представитель класса имеет 1 гидроксогруппу. Его молекулярная формула С6Н5ОН. Структурная формула — ОН.
Если в молекуле фенола 1 атом водорода заместить на метильный радикал, получим метилфенол. Если к нему прибавить ещё одно бензольное ядро, получим нафтол.
Химические свойства фенола
Так как гидроксибензол содержит в своём составе 2 группы атомов, выделяют две группы химических свойств.
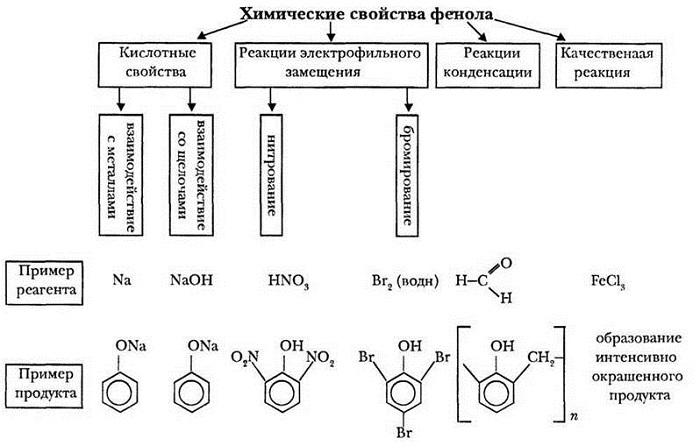
Свойства, идущие за счет фенил радикала:
Свойства, протекающие за счёт гидроксильной группы (кислотные свойства):
взаимодействие с активными металлами;
взаимодействие со щелочами.
Не следует понимать, что фенол, имея в своем составе черты строения бензола и спиртов, просто повторяет их свойства. На самом деле все сложнее. Чтобы понять особенность его химических взаимодействий, необходимо знать строение вещества. В молекуле фенола наблюдается взаимное влияние атомов.
На атоме кислорода гидроксильной группы есть 2 неподелённые электронные пары. Они взаимодействуют с π – электронной системой фенил радикала.
Результат взаимодействия следующий:
Нарушается равномерное распределение электронной плотности в фенил радикале. Она возрастает на атомах 2,4,6, то есть в орто– и параположениях. Именно в этих положениях водород будет легко замещаться на другие атомы.
Атом водорода гидроксогруппы, из-за влияния фенил радикала, приобретает положительный заряд и становится более подвижным.
Результатом влияния служат своеобразные свойства фенола. Он реагирует с активными металлами и щелочами. Спирты – только с металлами. В то же время и бензол, и гидроксибензол реагируют с бромной водой. Но у фенола, в отличие от бензола, идет замещение сразу по 3 атомам.
Физические свойства
С6Н5ОН – это белое кристаллическое вещество. В результате окисления кристаллы могут приобретать розовый цвет. Температура плавления 40,9 0 С. Молярная масса 94 г/моль.

Отличается характерным резким запахом. Вещество ядовито. Проникая в организм человека, вызывает тяжёлое отравление.
С чем реагирует фенол
Гидроксибензол вступает в реакцию с активными металлами. С натрием даёт фенолят натрия. Уравнение выглядит следующим образом:
2 С6Н5ОН + 2Na = 2С6Н5ОNa + H2
В реакциях со щелочами также образует феноляты. Реагируя с гидроксидом калия, образует фенолят калия:
С6Н5ОН + KOН = С6Н5ОK +H2O
Взаимодействуя со спиртами, образует эфиры. Например, в реакции с бутанолом, получают простой эфир:
С6Н5 ОН + НО–С4Н9 = С6Н5–О–С4Н9 +Н2О
Из свойств, протекающих за счёт фенил радикала, можно отметить реакцию нитрования. Взаимодействие с HNO3 даёт 2,4,6 тринитрофенол (пикриновую кислоту):
С6Н5ОН + 3HNO3 = C6H2(NO2)3OH +3H2O
Реагируя с формальдегидом, фенол образует фенолформальдегидную смолу. Это реакция поликонденсации – получение высокомолекулярного вещества из низкомолекулярных веществ с отщеплением побочного продукта. В данном случае – это вода.
Качественные реакции на фенол
К качественным реакциям относят взаимодействие с бромной водой. В результате получают осадок белого цвета:
С6Н5ОН + 3Br2 = C6H2Br3ОН + 3HBr
Ещё одной качественной реакцией является взаимодействие с хлоридом железа(III). Получается фиолетовое окрашивание. Качественные реакции позволяют разделить и определить органические вещества.
Реакция присоединения
К реакциям присоединения относят гидрирование ароматического ядра. Гидрирование – это реакции присоединения водорода. Превращение протекает легко, в присутствии катализатора. В результате разрушается π – электронная система, образуется циклогексанол и циклогексанон:
2С6Н5ОН + 5Н2 = С6Н11ОН + С6Н10О
Окисление
Фенол не устойчив к окислению. Продукты реакции могут быть разными. Это зависит от самого окислителя и от условий, в которых протекает реакция. При окислении перекисью водорода получается двухатомный фенол:
С6Н5ОН + Н2О2 = С6Н4(ОН)2
К реакции окисления относят и реакцию горения. Образуется углекислый газ и вода.
Получение фенола
Фенол в небольшом количестве содержится в каменноугольной смоле. Но потребности в веществе настолько велики, что этого источника недостаточно.
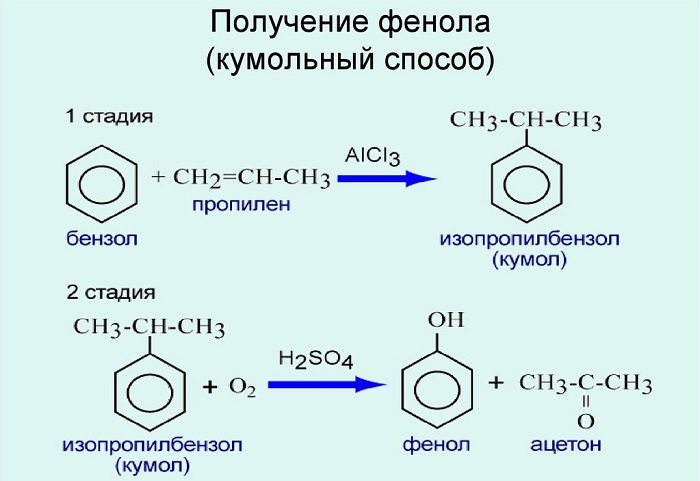
Разработаны разные способы получения:
По схеме С6Н6 ----- С6Н5Cl ----- С6Н5ОН. Минусом метода являются жёсткие условия замещения хлора на гидроксогруппу. Реакции приходится проводить при высокой температуре и давлении.
Используют для получения бензол и пропилен, в результате чего получают кумол. Затем кумол окисляют, в результате получают ценные продукты – фенол, ацетон.
Применение
Вещество применяют для производства разнообразной продукции:
фенолформальдегидных смол и пластмасс;
раствор фенола в воде обладает антисептическими свойствами;
искусственных волокон и другой продукции.
Заключение
Фенол и фенольные соединения – очень важная группа веществ. Не следует забывать, что многие из них являются ядами. Все отходы промышленности, содержащие вещество, тщательно очищаются. Их подвергают каталитическому окислению, обработке озоном и другим способам очистки.

В фенолах одна из неподеленных электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца, это является главной причиной отличия свойств фенола от спиртов.

Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода.
Отличия:
- фенол не реагирует с галогеноводородами: ОН- группа очень прочно связана с бензольным кольцом, её нельзя заместить;
- фенол не вступает в реакцию этерификации, эфиры фенола получают косвенным путем;
- фенол не вступает в реакции дегидратации.
- фенол обладает более сильными кислотными свойствами и вступает в реакцию со щелочами.
1. Кислотные свойства фенолов
| Фенолы являются более сильными кислотами, чем спирты и вода, т. к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается. |
1.1. Взаимодействие с раствором щелочей
В отличие от спиртов, фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты.
| Например, фенол реагирует с гидроксидом натрия с образованием фенолята натрия |

Так как фенол – более слабая кислота, чем соляная и даже угольная, его можно получить из фенолята, вытесняя соляной или угольной кислотой:
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Фенолы взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются феноляты. При взаимодействии с металлами фенолы ведут себя, как кислоты.
| Например, фенол взаимодействует с натрием с образованием фенолята натрия и водорода . |

2. Реакции фенола по бензольному кольцу
| Наличие ОН-группы в бензольном кольце (ориентант первого рода) приводит к тому, что фенол гораздо легче бензола вступает в реакции замещения в ароматическом кольце. |
2.1. Галогенирование
| Фенол легко при комнатной температуре (без всякого катализатора) взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол). |

2.2. Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов.
| Например, при нитровании фенола избытком концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота): |

3. Поликонденсация фенола с формальдегидом
С формальдегидом фенол образует фенолоформальдегидные смолы.

4. Взаимодействие с хлоридом железа (III)
При взаимодействии фенола с хлоридом железа (III) образуются комплексные соединения железа, которые окрашивают раствор в сине-фиолетовый цвет. Это качественная реакция на фенол.
5. Гидрирование (восстановление) фенола
Присоединение водорода к ароматическому кольцу.
Продукт реакции – циклогексанол, вторичный циклический спирт.

1. Взаимодействие хлорбензола с щелочами
При взаимодействии обработке хлорбензола избытком щелочи при высокой температуре и давлении образуется водный раствор фенолята натрия.

При пропускании углекислого газа (или другой более сильной кислоты) через раствор фенолята образуется фенол.

2. Кумольный способ
Фенол в промышленности получают из каталитическим окислением кумола.
Первый этап процесса – получение кумола алкилированием бензола пропеном в присутствии фосфорной кислоты:

Второй этап – окисление кумола кислородом. Процесс протекает через образование гидропероксида изопропилбензола:

Суммарное уравнение реакции:
3. Замещение сульфогруппы в бензол-сульфокислоте
Бензол-сульфокислота реагирует с гидроксидом натрия с образованием фенолята натрия:
Читайте также:

