Фармакотерапия бронхиальной астмы реферат
Обновлено: 04.07.2024
А.В. Емельянов, Г.Р. Сергеева, Е.В. Лешенкова, М.С. Партави
Кафедра пульмонологии Северо-Западного государственного медицинского университета им. И.И. Мечникова, Санкт-Петербург, Россия
В статье обсуждаются современные представления о лечении бронхиальной астмы, одного из самых распространенных
и социально значимых заболеваний в мире. Рассматриваются вопросы лечения заболевания на различных ступенях терапии и длительного ведения пациентов. Приводятся основные группы лекарственных препаратов, рекомендованных в настоящее время для ведения больных бронхиальной астмой при ее стабильном течении. Рассматриваются ближайшие перспективы совершенствования фармакотерапии этого заболевания.
Бронхиальная астма (БА) – одно из самых частых респираторных заболеваний, которым в мире страдают около 360 млн людей. Она существенно снижает качество жизни пациентов, имеет высокую стоимость лечения, ежегодно становясь причиной смерти 400 тыс. больных в мире [1]. Ведение пациентов с БА регламентируется глобальной инициативой по БА (GINA – Global Initiative for Asthma) и Национальными российскими клиническими рекомендациями [2, 3].
В связи с появлением новых знаний об особенностях развития и течения БА в последнее время появляются новые группы препаратов, пересматриваются устоявшиеся схемы ведения пациентов, разрабатываются критерии оценки объема и режима необходимой терапии. В настоящей статье обсуждается терапия БА стабильного течения и перспективы ее развития.
Тяжесть и контроль БА
Выбор лечения в настоящее время определяется степенью тяжести БА, достижением ее контроля и фенотипом заболевания.
Тяжесть астмы ранее определялась на основании выраженности клинической картины и показателей функции легких до начала терапии. Как недостаток этого определения – оно не учитывало особенностей течения заболевания у пациентов, получавших лечение.
В настоящее время в международных и национальных рекомендациях тяжесть течения БА оценивается с учетом объема проводимой терапии, необходимого для достижения контроля (табл. 1).
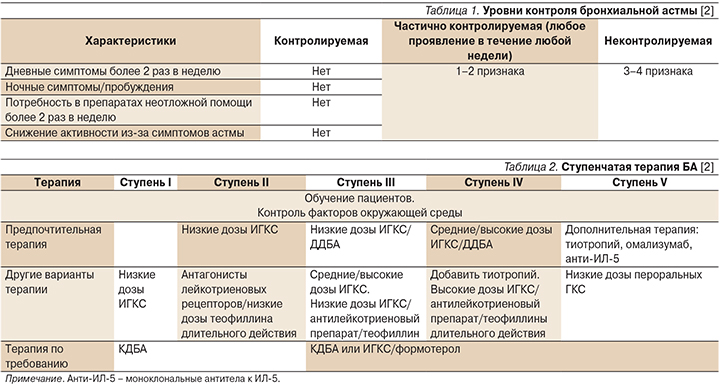
Сегодня выделяют три степени тяжести течения БА у больных, получающих лечение [2].
- Легкая астма: контроль достигается при использовании низких доз ингаляционных глюкокортикостероидов (ИГКС), антилейкотриеновых препаратов или β2-адреномиметиков короткого действия (КДБА).
- Астма средней тяжести: достижение контроля возможно при использовании низких доз ИГКС и β2-адреномиметиков длительного действия (ДДБА).
- Тяжелая астма для лечения требует 4–5 ступеней GINA (высокие дозы ИГКС совместно с ДДБА или антилейкотриеновыми препаратами/теофиллином) в предыдущий год или применения системных ГКС≥50% времени предыдущего года для достижения и сохранения контроля или которая остается неконтролируемой, несмотря на эту терапию [4].
Основные цели ведения пациентов с БА – это достижение и поддержание хорошего контроля симптомов болезни в течение длительного времени, профилактика обострений, улучшение функционального состояния легких.
Оценка контроля осуществляется путем оценки двух составляющих – контроля симптомов и определения риска будущих обострений, который зависит от многих факторов, в т.ч. дисциплины пациента, правильной техники приема ингаляционных препаратов, сопутствующих заболеваний, степени тяжести бронхиальной обструкции.
Показано, что достижение контроля возможно при адекватной терапии большинства пациентов. Для оценки контроля астмы в реальной клинической практике рекомендуется использовать специальные вопросники: АСТ (Asthma Control Test) и ACQ-5 (Asthma Control Questionnaire), позволяющих быстро и точно оценивать состояние больных врачами первичного звена и специалистами.
К факторам риска обострений или плохого контроля относятся высокая потребность в использовании бронхолитиков короткого действия, неправильное или недостаточное использование ИГКС, низкие показатели функции легких (объем форсированного выдоха за 1-ю секунду – ОФВ1
1. Global, regional, and national deaths, prevalence, disability-adjusted life years, and years lived with disability for chronic obstructive pulmonary disease and asthma, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015. Lancet Respir. Med. 2017;5:691–706.
4. Chung K., Wenzel S., Brozek J., et al. International ERS/ATS guidelines on definition, evaluation and treatment of severe asthma. Eur. Respir. J. 2014;43:343–73.
5. Федосеев Г.Б., Трофимов В.И., Петрова М.А. Многоликая бронхиальная астма, диагностика, лечение и профилактика. СПб., 2011. 344 с.
6. Принципы выбора терапии для больных легкой бронхиальной астмой. Согласованные рекомендации РААКИ и РРО. Практическая пульмонология. 2017;1:82–90.
7. Irwin R.S., Richardson N.D. Side effects with inhaled corticosteroids. Chest. 2006;130(
8. Lacasse Y., Archibald H., Ernst P., Boulet L.P. Pattern and determinants of compliance with inhaled steroids in adults with asthma. Can. Respir. J. 2005;12(4):211–17.
9. Papi A., Canonica G.W., Maestrelli P., et al. BEST Study Group. Rescue use of beclomethasone and albuterol in a single inhaler for mild asthma. N. Engl. J. Med. 2007;356(20):2040–52.
12. Bousquet J., van Cauwenberge P., Khaltaev N., et al. Allergic rhinitis and its impact on asthma (ARIA)//ARIA. At a glance pocket reference, 1st edition. 2007. 6 p.
13. Согласованные рекомендации по применению антихолинергического препарата длительного действия тиотропия в терапии бронхиальной астмы. Пульмонология 2015;25(2):143–50.
14. McCracken J., Tripple J., Calhoun W. Biologic therapy in the management of asthma. Curr. Opin. Allergy Clin. Immumol. 2016;16(4):375–82.
15. Pelaia C., Vatrella A., Bruni A., et al. Benralizumab in the treatment of severe asthma: design, development and potential place in therapy. Drug design, development and therapy 2018;12:619–28.
17. Тяжелая бронхиальная астма. Клинические рекомендации Ассоциации русскоговорящих специалистов в области респираторной медицины. М., 2018. [Severe bronchial asthma. Clinical recommendations of the Association of Russian-speaking specialists in the field of respiratory medicine. M., 2018.
18. Bousquet J., Brusselle G, Buhl R., et al. Care pathways for the selection of a biologic in severe asthma. Eur. Respir. J. 2017;50:1701782.
19. Castro M., Corren J., Pavord I.D., et al. Dupilumab Efficacy and Safety in Moderate-to-Severe Uncontrolled Asthma. N. Engl. J. Med. 2018;378:2486–96.
20. Rabe K.F., Nair P., Brusselle G., et al. Efficacy and Safety of Dupilumab in Glucocorticoid-Dependent Severe Asthma. N. Engl. J. Med. 2018;378:2475–85.
21. Corren J., Parnes J.R. Wang L., et al. Tezepelumab in Adults with Uncontrolled Asthma. N. Engl. J. Med. 2017;377:936–46.
22. Gibson P.G., Yang I.A., Upham J.W., et al. Effect of azithromycin on asthma exacerbations and quality of life in adults with persistent uncontrolled asthma (AMAZES): a randomised, double-blind, placebo-controlled trial. Lancet. 2017;12390(10095):659–68.
23. Torrego A., Solà I., Munoz A.M., et al. Bronchial thermoplasty for moderate or severe persistent asthma in adults. Cochrane Database Syst. Rev. 2014;(3):CD009910.
24. Wang L., Yin J., Fadel R., et al. House dust mite sublingual immunotherapy is safe and appears to be effective in moderate, persistent asthma. Allergy. 2014;9:1181–89.
25. Virchow C., Backer V., Kuna P., et al. Efficacy of house dust mite allergen sublingual immunotherapy tablets in adults patients with allergic asthma. A randomized clinical trial. JAMA. 2016;315(16):1715–25.
Читайте также:

