Эректильная дисфункция реферат по урологии
Обновлено: 02.07.2024
Изучение эректильной дисфункции у пациентов, перенесших трансуретральные эндоскопические оперативные вмешательства на предстательной железе по поводу ее доброкачественной гиперплазии. Диагностика и результаты предоперационного обследования пациентов.
| Рубрика | Медицина |
| Вид | статья |
| Язык | русский |
| Дата добавления | 07.05.2014 |
| Размер файла | 28,3 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Новейшие достижения научно-технического прогресса в значительной степени изменили традиционный подход к лечению многих урологических заболеваний, в том числе приводящих к инфравезикальной обструкции, среди которых самым распространенным является доброкачественная гиперплазия предстательной железы (ДГПЖ).
Несмотря на то, что трансуретральные эндоскопические вмешательства давно уже стали традиционными для большинства урологических клиник и их доля по сравнению с открытыми оперативными вмешательствами на нижних мочевых путях значительно больше, постоянное внедрение в клиническую практику новой аппаратуры и инструментария обусловливает необходимость изучения возможных побочных эффектов их применения.
Одним из таких последствий является эректильная дисфункция. Доказано, что у пациентов, перенесших трансуретральную резекцию (ТУР) простаты по поводу ее гиперплазии, в 4-40% случаев развиваются расстройства эрекции той или иной степени выраженности (Bruskenitz, Larsen, Madsen, 1986; Hargreve et al., 1987). В работах М.Л. Гориловского (1997), L. Edwards et al. (1985), P. Soonawalla et al. (1992), A. Le Duc et al. (1993), Internet, National Library of Medicine, USA (1997) дан исчерпывающий анализ осложнений после ТУР. При этом частота возникновения нарушений эректильной функции в послеоперационном периоде отмечена у 3,3-34,8% пациентов.
S. Madersbacher и М. Marberger (1999) в своем исследовании, включающем анализ результатов обследования 3032 пациентов, страдающих ДГПЖ, которым впоследствии была проведена ТУР по стандартной методике и электровапоризация простаты, отмечают возникновение эректильной дисфункции в 19% случаев у больных, которым проведена ТУР и у 21% в группе пациентов после вапоризации. В подобном исследовании M.Y. Hammadeh et al. (2000), включающем две группы пациентов, перенесших ТУР и электровапоризацию (по 52 человека в каждой), в послеоперационном периоде отмечено появление эректильной дисфункции в 11% и 17% случаев соответственно.
В связи с повышением требований к качеству жизни и признанием удовлетворительной сексуальной активности одним из наиболее важных критериев его оценки, проблема лечения эректильных расстройств в настоящее время практически не имеет возрастных ограничений. Поскольку многие мужчины пожилого возраста, составляющие большинство среди больных, подвергающихся трансуретральным эндоскопическим вмешательствам, вкладывают в понятие улучшения качества жизни не только улучшение качества мочеиспускания, но и качества сексуальной жизни, столь высокий процент послеоперационной эректильной дисфункции требует пристального внимания врачей и исследователей к этой проблеме.
Трансуретральная резекция простаты по сравнению с чреспузырной аденомэктомией и особенно с радикальной простатэктомией сопровождается значительно меньшей травматизацией простаты, семенных пузырьков, семенного бугорка, уретры, но зачастую приводит к усугублению копулятивной дисфункции, которая имела место до оперативного вмешательства вследствие возрастных изменений в организме пациента (Geppi-Attee S., Sultana S., Hodgson G. еt al.,2000) .
Madorsky et al. (1997) впервые высказали гипотезу о роли термического повреждения структур кавернозных нервов при выполнении ТУР простаты в проекции 5 и 7 часов условного циферблата.
Повреждения нервных волокон тазового сплетения - основная причина эректильной дисфункции после хирургических вмешательств на органах малого таза. Поэтому тазовое сплетение и его эфферентные волокна, иннервирующие пещеристые тела (пещеристые нервы), в последнее время стали предметом всесторонних исследований. Walsh и Donker (1982) проследили топографию иннервации пещеристых тел на мертворожденных и плодах. Выявлено прохождение важных ветвей тазового сплетения между прямой кишкой и уретрой: они проникают через урогенитальную диафрагму вблизи уретры или через ее мышечную стенку. Авторы пришли к выводу, что после операций на предстательной железе (радикальная позадилонная простатэктомия, чреспузырная аденомэктомия, трансуретральная резекция простаты) эректильная дисфункция может возникать в результате повреждения этих ветвей в двух пунктах: при разделении латеральной ножки или во время апикального рассечения при механическом и термическом воздействии на стенку уретры. Частой причиной развития эректильной недостаточности после трансуретральных вмешательств также является поражение пещеристых нервов и сосудов полового члена, расположенных в парапростатической зоне при перфорации хирургической капсулы простаты (Walsh et аl., 1983; Вigg еt аl., 1990 Вгеndlег еt аl., 1990).
Несмотря на достигнутый в последние годы прогресс в диагностике и лечении эректильной дисфункции, вопросы, касающиеся особенностей этиопатогенеза, характера течения, прогностических критериев, лечения и профилактики данного состояния после эндоскопических оперативных вмешательств, окончательно не изучены. Все вышеперечисленное определяет научную и практическую актуальность решения этой проблемы.
Данное исследование проведено в период с 1997 по 2004 год на базе Научно-исследовательского института урологии МЗ РФ и Городской клинической урологической больницы № 47 города Москвы.
В качестве исследуемого контингента определены больные с диагностированной ДГПЖ, которым проведена трансуретральная резекция или электровапоризация простаты.
Характеристика групп больных
Из всех больных (412 человек) с доброкачественной гиперплазией простаты, которым планировалось выполнение трансуретральной резекции, 68,9% пациентов не были заинтересованы в сохранении адекватной эректильной функции в послеоперационном периоде. Более половины больных, имея потенциальную половую партнершу (жену), тем не менее смирились с возникшей дизритмией половой жизни (вплоть до ее полного отсутствия) на фоне прогрессирующего усиления симптоматики нарушений мочеиспускания. При этом во многих случаях отмечено скептическое отношение пациентов к доводам врача о том, что после нормализации мочеиспускания половая жизнь вполне возможна. Одинокий образ жизни, трудности обретения нового партнера, психологическая травма после потери супруги - это лишь основные причины отказа или воздержания большей части пожилого мужского населения от сексуальной активности.
Основная группа исследуемых пациентов, для которых сохранение, а также возможное улучшение эректильной функции представлялось актуальной задачей, состояла из 128 мужчин в возрасте от 48 до 80 лет (средний возраст 65,2 года). Более половины всех пациентов состояли в первом или повторном браке. Давность заболевания у этих больных составляла от года до пяти лет, а у вдовцов или разведенных в основном - пять лет и более. У 67,2% пациентов исследуемой группы выявлены интеркуррентные патологические изменения, представленные прежде всего сердечно-сосудистыми и дегенеративно-деструктивными заболеваниями. При этом 60,2% получали сопутствующую терапию, в том числе и препаратами, которые сами по себе ухудшают качество эрекции (гипотензивные средства, b- блокаторы, диуретики, блокаторы Н2-рецепторов и др.).
Оценка эректильной функции проводилась до и после операции посредством физикального обследования, заполнения пациентами оценочных шкал (Международного индекса эректильной функции, шкалы количественной оценки мужской копулятивной функции (О.Б. Лоран, А.С. Сегал, 1998), госпитальной шкалы тревоги и депрессии), RigiScan-мониторинга, фармакодопплерографии, электромиографии, исследования гормонального статуса, а также кавернозографии по показаниям.
Результаты предоперационного обследования
У всех 128 пациентов исследуемой группы до операции были выявлены клинические проявления доброкачественной гиперплазии предстательной железы. В 53,1% случаях больные предъявляли жалобы на симптомы, характерные для климактерического периода. Обращает на себя внимание тот факт, что практически все клинические проявления андропаузы (повышенная нервозность, ослабление памяти и внимания, быстрая утомляемость и др.) отрицательно сказываются не только на эректильной, но и на половой функции в целом. Отмечена тенденция к снижению количества предъявляемых "климактерических" жалоб у пациентов старше 60-65 лет при прогрессировании сопутствующих заболеваний.
Подавляющее большинство пациентов, заинтересованных в сохранении, а возможно и улучшении своей эректильной функции (90,6%), жили половой жизнью; у 81% была постоянная половая партнерша. У 75% отмечались той или иной степени выраженности жалобы сексуальной сферы, из которых недостаточность эрекции выявлена в 58,3% случаев, снижение либидо - 78,1%, затрудненная или ускоренная эякуляция - 47,9%, снижение выраженности оргазма - 86,5%. Многие пациенты предъявляли несколько жалоб. Несмотря на такую выраженность симптоматики, только 12,5% из них до операции эпизодически использовали средства, улучшающие качество эрекции (ингибиторы фосфодиэстеразы 5 типа, биологически активные пищевые добавки, а также методы нетрадиционной или народной медицины).
Несмотря на широкое освещение в средствах массовой информации вопросов профилактики и лечения ДГПЖ, при беседе с врачом 64,9% пациентов были уверены, что операция приведет к тотальной потере эректильной функции, а 39,9% высказывали неуверенность в результативности лечения с точки зрения улучшения качества самостоятельного мочеиспускания.
При исследовании половой активности пациентов в зависимости от степени возрастной разницы между супругами выявлено, что в основном (62%) наблюдаются спорадические проявления сексуальной активности (при частоте эксцессов менее 1 раза в неделю), 26,6% пациентов вели регулярную половую жизнь (1-2 раза в неделю) и только 7,4% отмечали повышенную сексуальную активность (более 2 раз в неделю). При этом выявлена общая тенденция повышения уровня сексуальной активности у всех пациентов при увеличении разницы между их возрастом и возрастом их жен.
Половой темперамент среднего уровня выявлен у 46,1% больных, сильный - у 18%, слабый - у 35,9%. При этом с возрастом отмечено снижение половой активности, прежде всего у пациентов со слабым половым темпераментом.
Гипотестостеронемия на дооперационном этапе выявлена у 42,2% больных, при этом отмечена тенденция большего снижения уровня тестостерона для старших возрастных групп. У 91,2% пациентов выявлена зависимость проявлений климактерического синдрома от уровня тестостерона плазмы крови. Однако частота встречаемости жалоб на снижение качества эрекций у пациентов с гипотестостеронемией достоверно не отличалась от таковой в общей группе. Между тем снижение либидо и сексуальной возбудимости были основными жалобами именно в группе с низким уровнем тестостерона.
До оперативного вмешательства гиперэстрогенемия наблюдалась в 12,5% случаев, при этом повышенный уровень эстрадиола плазмы крови в среднем умеренно повышался в старших возрастных группах.
Гиперпролактинемия выявлена в 8 наблюдениях (6,25%). Достоверной корреляции между возрастом и этими клиническими случаями не определено.
По данным трансректального ультразвукового исследования наблюдалась тенденция к увеличению объема предстательной железы с возрастом пациентов за счет роста объема узлов гиперплазии. Данные ультразвукового исследования коррелировали с данными урофлоуметрии, при этом признаки инфравезикальной обструкции были выявлены в 100% случаев.
Проведение RigiScan-мониторирования ночных пенильных тумесценций позволило выявить нарушения у 75,8% больных. Частота наблюдаемых нарушений ночных пенильных тумесценций увеличивалась в старших возрастных группах. В большинстве случаев отмечалась частично недостаточная эрекция (53,6%), недостаточная ригидность определена в 29,9% случаев, ее отсутствие - в 16,5%. Учитывая наличие нарушений сна у многих пациентов на дооперационном этапе, а также стойкую активацию симпатической нервной системы вследствие депрессивного настроения, результаты RigiScan-теста могут быть ложноотрицательными, поэтому для их объективизации необходимо проведение комплексной всесторонней оценки данных физикального, лабораторного и инструментальных методов обследования. При сравнении данных проведенной фармакодопплерографии с данными RigiScan-мониторирования васкулогенные нарушения коррелировали с нарушениями ночных пенильных тумесценций в 76,3% случаев (р
По данным ВОЗ, после 21 года расстройства эрекции выявляются у каждого 10-го мужчины, а после 60 лет — каждый третий мужчина вообще не способен выполнить половой акт. По расчетам J. B. MkKinlay (2000), около 150 млн мужчин в мире страдают от ЭД; предполагается, что в течение ближайших 25 лет эта цифра может удвоиться.
В опубликованном в 2003 г. обзоре A. Nicolosi привел результаты стандартизированного анкетного опроса около 600 мужчин в возрасте от 40 до 70 лет в четырех странах мира, согласно которым частота ЭД составила в Бразилии — 15%, в Италии — 17%, в Малайзии — 22% и в Японии — 34%. Эпидемиологических данных о распространенности ЭД в России нет, однако высокий травматизм среди мужского населения, значительная распространенность алкоголизма, курение низкокачественных сортов табака и бесконтрольный прием медикаментов позволяют предполагать большую распространенность ЭД по сравнению с индустриально развитыми странами мира (Г. С. Кротовский, А. М. Зудин, 2003).
Согласно результатам анкетирования, 10 тыс. мужчин в возрасте от 17 до 70 лет, проводившегося с 12 апреля по 21 мая 2002 г. (P. Costa et al., 2003), только 22,2% опрошенных мужчин с ЭД обращаются за помощью к врачу, и только 36,9% из них получают лечение. Большинство опрошенных не считают ЭД болезнью, связывая ее появление со стрессом и усталостью. По данным других исследований, только треть мужчин консультируется с врачом (K. S. Fugl-Meyer, 1998 O. Kontula et al., 1995), и 75—88% мужчин с ЭД не получают по этому поводу никакого лечения (F. Giuliano et al., 2002, E. J. Meuleman et al., 2001, K. K. Chew et al., 2000).
Таким образом, несмотря на высокую распространенность ЭД, обращаемость пациентов за медицинской помощью все еще остается достаточно низкой. Отсюда неэффективное (а порой и небезопасное) самолечение и дальнейшее прогрессирование болезни. Широкая информированность не только специалистов, непосредственно занимающихся ЭД, но и врачей других специальностей, а именно терапевтов, эндокринологов, может сыграть немаловажную роль в первичной диагностике ЭД. Кроме того, способы лечения ЭД не могут рассматриваться в отрыве от общесоматического состояния пациента, т. е. как изолированная урологическая проблема, поэтому привлечение врачей других специальностей может помочь более квалифицированному оказанию медицинской помощи этим пациентам.
Таким образом, ЭД — это широко распространенное состояние, причем в подавляющем большинстве случаев мужчины не обращаются за медицинской помощью и не получают адекватного лечения. С другой стороны, врач общей практики, к которому прежде всего попадает пациент со всеми своими проблемами, нередко имеет весьма расплывчатые представления о проблеме ЭД и возможных способах коррекции.
Эрекция: физиология и патофизиология
Эрекция представляет собой увеличение полового члена в объеме с резким повышением его упругости, обусловленное растяжением и наполнением пещеристых тел при половом возбуждении. Феномен эрекции состоит из сложной цепи нейрососудистых изменений в кавернозной ткани, конечным звеном в которой является релаксация гладкомышечных элементов артерий, артериол и синусоидов.
В конце прошлого столетия появились новые данные о физиологии эрекции, причинах возникновения ЭД и, соответственно, новые возможности ее коррекции. По современным представлениям, при сексуальной стимуляции происходит активация парасимпатической нервной системы. Высвобождение нейротрансмиттеров, в частности оксида азота, из эндотелия сосудов кавернозных тел приводит к накоплению циклического гуанозинмонофосфата (цГМФ) в кавернозной ткани и расслаблению гладкомышечных клеток стенок приносящих артерий и кавернозных тел. Заполнение артериальной кровью лакун обуславливает сдавление венул и блокирование оттока крови из полового члена (вено-окклюзивный механизм). Основные компоненты эрекции представлены на рисунке 1.
Соответственно, развитие ЭД может быть связано с недостаточной вазодилатацией вследствие дефицита цГМФ, плохой восприимчивостью сосудов к цГМФ, недостатком компрессии пенильных вен вследствие разрастания соединительной ткани; кроме того, может иметь место комбинация вышеперечисленных причин (Д. Ю. Пушкарь соавт., 2002).
Таким образом, эрекция может рассматриваться как сложное нейрососудистое явление, в происхождении которого играют определенную роль сексуальная стимуляция, высвобождение оксида азота и накопление цГМФ в кавернозной ткани, расслабление и сокращение гладкомышечных клеток под влиянием ФДЭ5.
Причины эректильной дисфункции
Почти во всех популяционных исследованиях, посвященных ЭД, выявлена связь ее возникновения с артериальной гипертензией (АГ), сахарным диабетом (СД) и атеросклерозом. Так, по данным Е. Ricci соавт. (2003), ЭД в шесть раз чаще возникает при СД и в три раза — при АГ. Более того, по мнению некоторых авторов, выявление ЭД может свидетельствовать о наличии у пациента одного из этих заболеваний в скрытой доклинической форме (M. R. Nusbaum et al., 2002). По данным M. K. Waiczak соавт. (2002), из 154 мужчин, обратившихся за помощью в связи с ЭД, у 44% была диагностирована АГ и у 23% — СД.
При атеросклерозе стенки кровеносных сосудов утрачивают эластичность, сужается их просвет, возникает несоответствие между потребностью органа в кислороде и возможностью его доставки. При этом существенное значение придается факторам риска, таким, как курение, дислипидемия, СД (R. A. Kloner, M. Speakman, 2002). Так, Е. Ricci соавт. (2003) считают, что 2/3 пациентов с ЭД курят, а частота выявления у них гиперхолестеринемии в два раза выше, чем у пациентов без эректильных нарушений. Атеросклеротические изменения в пенильном кровотоке приблизительно в 40% случаев обуславливают развитие ЭД у мужчин в возрасте старше 50 лет. Нередко различные проявления атеросклероза, например ИБС и ЭД, развиваются параллельно, поскольку факторы риска эндотелиальной дисфункции коронарных и пенильных кровеносных сосудов одинаковы. Поэтому не случайно сердечно-сосудистые заболевания достоверно чаще встречаются у пациентов с АГ и ЭД, чем у больных с АГ без нарушений сексуальной функции (M. Burchardt et al., 2001). По данным H. Solomon и соавт. (2003), среди 174 мужчин, обследованных по поводу ЭД, дислипидемия была выявлена у 37%, неконтролируемая АГ — у 17%, стенокардия напряжения — у 6%. Предполагается, что ЭД может служить маркером сердечно-сосудистых заболеваний, а по степени ее тяжести можно судить о прогрессировании ИБС (A. Greenstein et al., 1997, M. Kirby et al., 2001, H. Solomon, J. W. Man, G. Jackson, 2003). При значительном снижении пенильного кровотока, по данным ультразвуковой допплерографии, некоторые авторы даже рекомендуют выполнять нагрузочные ЭКГ-пробы перед началом лечения ЭД (Y. Kawanishi et al., 2001).
В целом ряде исследований показано, что на фоне артериальной гипертонии ЭД встречается чаще, чем в общей популяции. Так, по данным A. J. Cuellar De Leon et al. (2002), полученным в результате анкетирования 512 пациентов в возрасте от 30 до 86 лет (средний возраст 63,4 года), ЭД встречается у 46,5% пациентов с артериальной гипертензией. В исследовании M. Burchardt соавт. (2000), среди 476 пациентов в возрасте от 34 до 75 лет (в среднем — 62,2 года) 84,8% были сексуально активны и 68,3% имели ЭД различной выраженности (7,7% — умеренную, 15,4% — выраженную и 45,2% — тяжелую), что существенно превышает популяционный уровень. По данным A. Roth соавт. (2003), частота ЭД среди больных АГ составляет 46%.
Еще в 1982 г. Jachuck соавт. отметили связь нарушений половой функции с ухудшением качества жизни у больных АГ, получавших лечение гипотензивными препаратами, в основном диуретиками, β-адреноблокаторами или метилдопой (последний препарат, разумеется, обычно уже не используется в лечении АГ в связи с высокой частотой побочных эффектов). Примерно у 78% больных, у которых существенно ухудшилось качество жизни (по оценке их жен), наблюдалось снижение или отсутствие сексуального интереса. Исследования, в совокупности проводившиеся более 30 лет, показали, что от 2,4% до 58% мужчин с АГ испытывают один или более симптомов нарушения половой функции той или иной степени тяжести на протяжении лечения антигипертензивными препаратами.
Особенно часто возникновение ЭД связывают с приемом тиазидных диуретиков и β-адреноблокаторов (R. Fogari, A. Zoppi, 2002, H. Mickley, 2002, D. Ralph, T. McNicholas, 2000). Так, по данным S. Wassertheil-Smoller et al. (1991), полученным в ходе многоцентрового, рандомизированного, плацебо-контролируемого исследования TAIM, связанные с эрекцией проблемы выявлялись у 11% пациентов, получавших в течение шести месяцев β-адреноблокатор (атенолол), и у 28% пациентов, получавших тиазидный диуретик (хлорталидон). D. T. Ko соавт. (2002) провели метаанализ и оценили безопасность применения β-адреноблокаторов при АГ и ИБС. В метаанализ были включены результаты 15 исследований (более 35 тыс. пациентов). Показано, что применение препаратов этой группы связано с небольшим, но статистически значимым риском возникновения сексуальной дисфункции (один дополнительный случай на каждые 199 пациентов, получавших лечение β-адреноблокаторами в течение года). β-адреноблокаторы первых поколений чаще вызывают ЭД, чем современные препараты, и их влияние на возникновение ЭД не зависит от степени липофильности.
Среди пациентов, получавших тадалафил в дозе 20 мг в сутки, нормальная эректильная функция (сумма баллов 26 и более при анкетировании с использованием IIEF) была достигнута у 59% мужчин по сравнению с 11% в контрольной группе. На фоне лечения тадалафилом в дозе 20 мг в сутки, абсолютная доля успешно завершенных попыток полового акта составила 75%, по сравнению с 32% — в группе плацебо (SEP). В конце лечения 81% мужчин, получавших тадалафил в дозе 20 мг в сутки, и только 35% мужчин из группы плацебо сообщили об улучшении эрекции (опросник GAQ). Эффективность препарата была одинаковой у молодых пациентов и у лиц старше 65 лет и не зависела от этиологии ЭД. При оценке влияния тадалафила на успешность завершения полового акта в зависимости от времени после приема 20 мг препарата (по данным анкетирования с использованием опросника SEP) оказалось, что в общей сложности от 73 до 80% попыток полового акта, совершенных в интервале между 30 мин и 36 ч, были успешными.
Учитывая высокую распространенность ЭД среди больных сахарным диабетом, эффективность и безопасность применения тадалафила в дозе 10 и 20 мг была оценена в ходе 12-недельного, рандомизированного, плацебо-контролируемого исследования, включавшего 216 пациентов с сахарным диабетом I или II типа и ЭД (I. Saenz de Tejada et al., 2002). По данным анкетирования с использованием опросника IIEF, прирост средней суммы баллов, отражающих эректильную функцию, на фоне терапии тадалафилом в дозах 10 и 20 мг составил через 12 недель 6,4 и 7,3 соответственно, по сравнению 0,1 в группе плацебо. Процент пациентов, сообщивших об успехе в достижении и удержании эрекции (SEP) и отметивших улучшение эрекции (GAQ), также был достоверно выше на фоне терапии тадалафилом, чем в группе плацебо.
Среди нежелательных явлений, возникавших на фоне приема тaдалафила, наиболее часто отмечались головная боль и диспепсия, реже — боли в спине, заложенность носа, миалгия и приливы крови к лицу; клинически значимых расстройств зрения не наблюдалось. Побочные явления, как правило, были не тяжелыми и уменьшались при продолжении лечения; частота отмены в связи с нежелательными явлениями составила 1,6% на фоне терапии тадалафилом в дозе 10 мг в сутки, 3,1% на фоне терапии препаратом в дозе 20 мг в сутки и 1,3% в группе плацебо. В исследовании W. J. Hellstrom et al. (2002) ежедневный прием тадалафила в дозе 10 или 20 мг в сутки в течение шести месяцев не оказал отрицательного влияния на сперматогенез человека. Открытое двухлетнее исследование, включавшее 1173 пациента (средний возраст 57 лет), также выявило хорошую переносимость тадалафила (F. Montorsi et al., 2001).
Основные опасения, связанные с применением ингибиторов ФДЭ5, обусловлены их потенциальным сосудорасширяющим действием, поэтому в ряде исследований III фазы прицельно изучались сердечно-сосудистые эффекты тадалафила у здоровых добровольцев и у больных стенокардией напряжения и артериальной гипертензией. У здоровых лиц прием тадалафила в дозе 10 и 20 мг не вызывал статистически недостоверное снижение артериального давления в положении стоя; в целом влияние препарата на показатели гемодинамики не отличалось от влияния плацебо. Тадалафил не удлиняет интервал QT, не вызывает нарушения атриовентрикулярной проводимости и сердечного ритма. Частота побочных сердечно-сосудистых эффектов тадалафила сопоставима с соответствующими показателями в группе плацебо (см. таблицу 5); его применение безопасно у пациентов, получающих гипотензивную терапию. У более чем 1200 пациентов частота развития инфаркта миокарда на фоне терапии тадалафилом составила 0,39 на 100 человеко-лет — против 1,1, у лиц, получавших плацебо, и была сопоставима с соответствующим показателем в стандартизованной по возрасту популяции мужчин (0,6) (J. T. Emmick et al., 2002).
Показана безопасность сочетания тадалафила с амлодипином в дозе 5 мг/сут, метопрололом в дозе 25—200 мг/сут, эналаприлом в дозе 10—20 мг/сут, индапамидом в дозе 2,5 мг/сут, лозартаном в дозе 25—50 мг/сут. Однако тадалафил, как и силденафил, нельзя назначать в сочетании с нитратами, поскольку у определенной группы пациентов комбинированный прием этих лекарственных средств приводит к развитию выраженной артериальной гипотензии (R. A. Kloner, M. I. Mitchell et al., 2002). При развитии приступа стенокардии на фоне терапии ингибиторами ФДЭ5 прием нитроглицерина категорически противопоказан, использование любых форм нитратов возможно через 48 ч после последнего применения тадалафила. С осторожностью препараты этой группы применяют при наличии анатомических деформаций полового члена и заболеваниях, способствующих возникновению приапизма (например, серповидно-клеточной анемии, лейкоза). Таким образом, медикаментозная терапия ингибиторами ФДЭ5 — простой, эффективный и достаточно безопасный способ лечения ЭД.
В заключение хотелось бы подчеркнуть, что ЭД развивается, как правило, на фоне хронических заболеваний, поэтому роль врачей общей практики трудно переоценить в выявлении и терапии этого состояния. Появление новых эффективных, безопасных и простых в применении лекарственных средств для лечения ЭД, позволяет успешно решить эту проблему в условиях общетерапевтической практики.
А. Л. Верткин, доктор медицинских наук, профессор
Д. Ю. Пушкарь, доктор медицинских наук, профессор
А. В. Тополянский, кандидат медицинских наук, доцент
А. С. Сегал, доктор медицинских наук, профессор
МГМСУ, Москва
Что такое нарушение эрекции (эректильная дисфункция)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скатова Бориса Валерьевича, андролога со стажем в 28 лет.
Над статьей доктора Скатова Бориса Валерьевича работали литературный редактор Елена Бережная , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Эректильная дисфункция — продолжительная (не менее 6 месяцев) неспособность мужчины достигать напряжения полового члена, достаточного для полноценного сексуального акта.
Человек — единственный биологический вид на нашей планете, который может поддерживать эрекцию достаточно длительное время. Нарушение этой способности является важной медицинской и социальной проблемой, ведёт к потере самоуважения, семейным конфликтам.
Внутренние причины эректильной дисфункции
- Нарушения сердечно-сосудистой системы. Разнообразные заболевания сердца и сосудов ведут к нарушению в интимной сфере (до 65% случаев) — ишемическая болезнь, нарушение сердечного ритма, гипертензия, состояния после инфарктов миокарда. Сужение сосудов (атеросклероз) в значительной степени присуще также сосудам фаллоса. Недаром некоторые учёные считают дисфункцию потенции предвестником сердечной патологии и рекомендуют начинать обследование сердца как можно раньше, если появились проблемы в интимной сфере. Имеет также значение повышенный холестерин и курение, приводящее к поражению стенки сосудов. Кроме того, препараты для лечения гипертонии и сердца могут сами по себе также вызывать значительные нарушения эрекции. [2]
- Травматический фактор — один из основных в развитии стойких нарушений потенции. Это переломы костей таза, разрывы уретры, травма головы, непосредственное повреждение кавернозных тел, состояния после операций на предстательной железе по поводу аденомы и рака. [3]
- Нарушения нервной проводимости. Чтобы осознать глубину проблемы, рекомендую просто взглянуть на схему нервной регуляции эрекции доктора П.Г. Шварца.
Работа организма в норме:
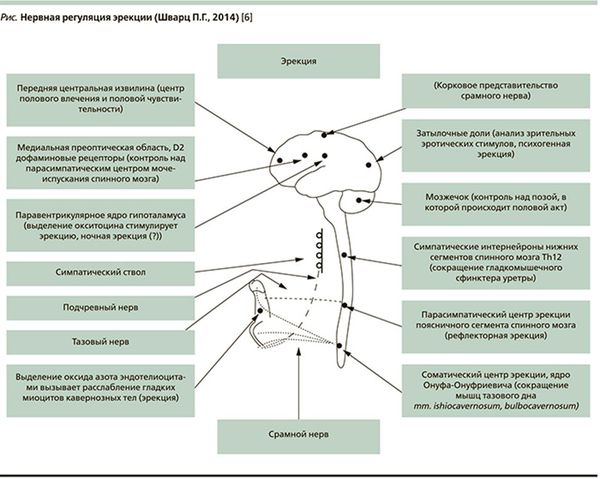
Согласно этой схеме, существует 14 структур регуляции эрекции. Нарушение на любом уровне может повлечь за собой разнообразные нарушения в интимной сфере мужчины. Данные структуры могут нарушаться в результате инсультов, травм, грыж межпозвоночных дисков, опухолей различных локализаций, рассеянного склероза, других неврологических заболеваний. [4]
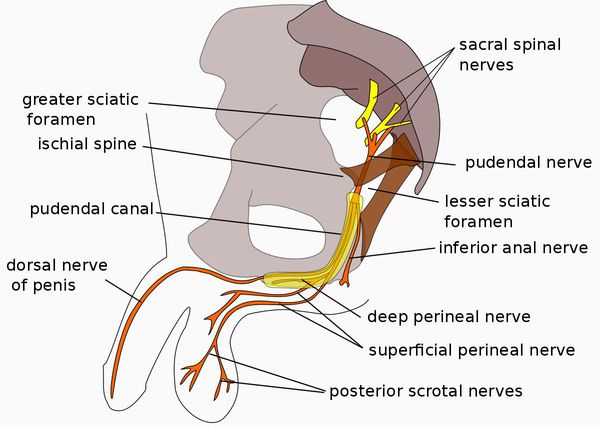
Кроме того, выделяют группу причин, связанных с нарушением работы органов внутренней секреции (эндокринные причины): сахарный диабет, приводящий к поражению периферических сосудов и нервов, нарушение работы щитовидной железы, ожирение. Имеет значение и снижение уровня тестостерона, в том числе возрастное, вследствие утомления, дисбаланс гормонального фона. [5]
Причиной эректильной дисфункции могут явиться воспалительные заболевания мочеполовых органов (простатит, везикулит, уретрит).
Внешние причины эректильной дисфункции
Повышенный радиационный фон, работа в условиях высокочастотного излучения и экологические факторы не могут быть причиной эректильной дисфункции. Однако нарушение эрекции может возникнуть из-за психотравмирующего воздействия в результате этих факторов.
Психогенная этиология
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы нарушения эрекции
Патогенез нарушения эрекции
В патогенезе эректильной дисфункции ведущую роль отводят патологии эндотелиальной ткани, что приводит, в конечном счёте, к нарушению кровоснабжения пещеристых тел фаллоса. Огромную роль играет атрофия сосудов, приводящая к склерозированию, замене здоровых клеток кавернозных тел на грубую соединительную ткань. Следовательно, выраженность эректильной дисфункции зависит от совокупности различных причин и степени их воздействия на кавернозные тела. [7]
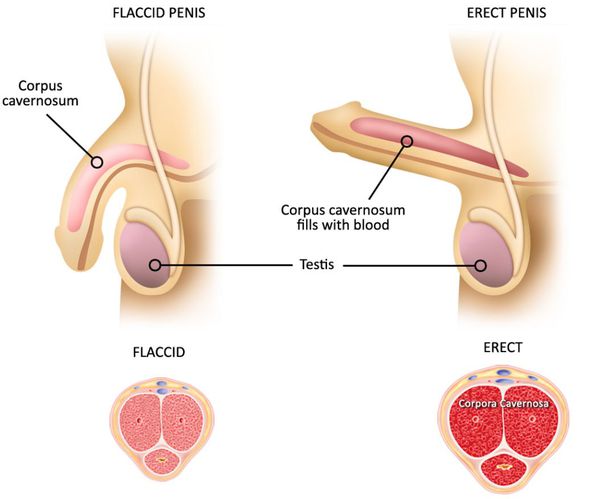
Классификация и стадии развития нарушения эрекции
Классификация эректильной дисфункции (2017 г.): [7]
I. Психозависимая:
1. Распространённая форма:
- общее нарушение восприимчивости;
- изначальное отсутствие либидо;
- снижение сексуальности возрастное;
- общее нарушение либидо;
- хроническое нарушение;
2. Ситуативная:
а) По отношению к половому партнёру:
- нарушение либидо к определённому партнёру;
- отсутствие либидо к предпочтениям объекта;
- подавление либидо в связи с конфликтными отношениями с партнёром;
б) Сомнение в своих возможностях:
- Дисфункциональные нарушения (быстрая эякуляция);
- Ожидание неудачи (сомнение в наступлении эрекции, способности поддержать эрекцию);
в) Стресс хронический:
- Патологическое настроение (потеря супруга, родственника, увольнение с работы).
II. Эректильная дисфункция, связанная с органическими поражениями:
- сосудистая;
- нейрогенная;
- анатомическая;
- гормональная;
- лекарственная.
III. Полиэтиологическая эректильная дисфункция.
Осложнения нарушения эрекции
- полная неспособность достичь хоть какого-то напряжения полового члена (импотенция);
- хронический стресс;
- снижение самооценки;
- нарушение социальной адаптации;
- семейные проблемы; ;
- серьезные нарушения психики, вплоть до суицида.
Диагностика нарушения эрекции
Пациентам с эректильной дисфункцией следует проводить определение гормонального фона (тестостерон свободный и связанный, пролактин, эстрадиол, гонадотропин), определять уровень сахара в крови, гликозированный гемоглобин, липидограмму крови. Результаты этих анализов помогут выявить определённый вид патогенеза дисфункции. [9]
Фармакологический тест: исследуется реакция тканей полового члена на введение в кавернозные тела папаверина, простагландинов и других медикаментозных средств.
Исследование неврологических рефлексов корешков спинного мозга также имеет определённое диагностическое значение.
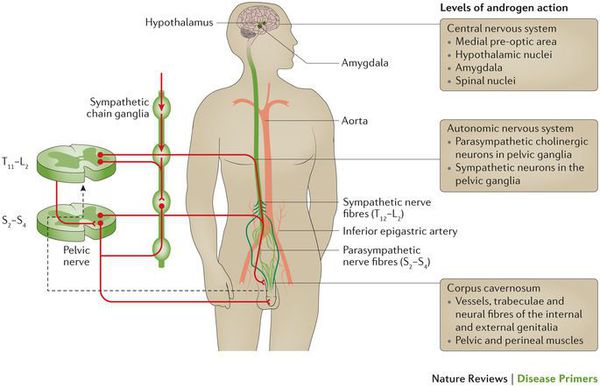
Ультразвуковое исследование:
- ТРУЗИ (трансректальное ультразвуковое исследование простаты) через прямую кишку позволяет точно определить размер и структуру предстательной железы, диагностировать простатит, доброкачественные и злокачественные опухоли простаты. Все эти факторы прямо или косвенно влияют на эрекцию.
- Допплерография сосудов фаллоса может оценить кровоток, степень сужения основных артерий и вен при эрекции. Является значимым прогностическим фактором при эректильной дисфункции. [10]
- УЗИ щитовидной железы выявляет нарушение структуры и размера этой важной железы, имеющей большое влияние на общий баланс гормонального фона.
Оценка состояния пещеристых тел:
- ядерно-магнитно-резонансная томография пениса помогает определить снижение кровотока в фиброзно-склеротических зонах пениса;
- биопсия ткани пещеристых тел, её гистохимическое исследование выявляет процентное соотношение изменённых элементов кавернозной ткани.
Лечение нарушения эрекции
К какому врачу обратиться
При нарушении эрекции нужно обращаться к врачу урологу-андрологу. Самостоятельное лечение недопустимо, так как это может значительно ухудшить состояние.
Оральные ингибиторы фосфодиэстеразы 5-го типа для лечения эректильной дисфункции
Настоящую революцию в терапии нарушений потенции произвели ингибиторы фосфодиэстеразы-5, имеющие влияние на оксид азота. Это вещество препятствует снижению тонуса вен полового члена и, следовательно, улучшает эрекцию. Название чудодейственного препарата "Виагра" было заготовлено давно и несколько лет ждало своего часа. Это ёмкое и приятное название переводится как "сила огромного водопада Ниагары". Час настал в 1993 году, когда американская компания "Пфайзер" случайно открыла выдающийся побочный эффект у нового лекарства для снижения артериального давления — цитрата силденафила. Препарат очень быстро был внедрён в широкую клиническую практику и завоевал первое место среди множества фармакологических средств для терапии эректильной дисфункции. Далее последовали новые поколения ингибиторов ФДЭ-5. У этих препаратов нарастал клинический эффект и сводились к минимуму побочные эффекты. Прежде всего, это "Левитра" (варденафил) и "Сиалис" (тадалафил). Препараты позволяют улучшить эрекцию при многих формах эректильной дисфункции, даже при низких цифрах тестостерона в крови мужчин. [11]
Другие препараты для лечения эректильной дисфункции
Теперь немного о поднятии уровня тестостерона в организме. Изыскания в этой области ведутся уже много десятилетий, однако настоящего прорыва всё же не произошло. Никак не хочет тестостерон накапливаться в мужском организме, вдобавок препараты дорогостоящие, имеют много побочных эффектов. Из них можно выделить "Небидо" — лекарство для внутримышечного введения и "Андрогель", который нужно втирать ежедневно в кожу. Активное использование препаратов тестостерона и анаболических стероидов осложняется широким использованием препаратов этой группы в бодибилдинге, прочих силовых видах спорта, что делает невозможным полный контроль за их применением и распространением. [12]
Психотерапия
При большинстве форм эректильной дисфункции большое значение имеет психосексуальная терапия, а также коррекция образа жизни, устранение или уменьшение неблагоприятных факторов жизни. Для получения консультации следует обратиться к врачу-психотерапевту.
Механические устройства для лечения эректильной дисфункции
Определённую роль в терапии эректильной дисфункции игрaет вакуумно-констрикторная терапия (ЛОД-терапия). Oсновной механизм этого вида терапии заключается в создании с помощью специальных устройств отрицательного давления (вакуума) на кавернозные тела пениса. Вакуумные приборы обеспечивают адекватную эрекцию в 60% случаев. [14]
Хирургическое лечение эректильной дисфункции
Хирургическое лечение при эректильной дисфункции применяют, когда консервативные средства исчерпаны:
- создание соустья (анастомоза) между надчревной артерией и боковой артерией фаллоса, выполняют при сужении этой артерии;
- операции на венах полового члена делают при нарушении веноокклюзивного аппарата;
- фаллопротезирование (имплантация протезов) является финальным этапом лечения эректильной дисфункции, когда другие методы неэффективны. Эта методика позволяет добиться результатов (полноценной эрекции) в 70-80% случаев. [15]
Ударно-волновая терапия (УВТ), магнитно-лазерная терапия (МЛТ), озонотерапия и массаж простаты не имеют доказанной клинической эффективности при лечении эректильной дисфункции и причины их использования исключительно коммерческие.
Диета и физическая активность
Сбалансированное питание и физическая активность играют важную роль в профилактике развития и при лечении эректильной дисфункции.
Физические упражнения направлены на улучшение кровообращения в органах малого таза у мужчины (особенно у лиц с сидячим образом жизни), улучшения кровотока к половому члену и яичкам, где происходит выработка тестостерона, необходимого для полноценной эрекции.
Упражнения самые простые: ходьба – не менее 6 тысяч шагов в сутки, приседания (не менее – 50 раз в сутки). Неплохой эффект показал урологический комплекс дыхательной гимнастики Стрельниковой. Также используются некоторые упражнения из практики йоги: джану ширшасана, пасчимотанасана, уттанасана, баддха конасана, дханурасана.

Массаж
Для лечения и профилактики достаточно эффективен массаж тазовой и лобковой областей. Массаж отлично активизирует сосудистый тонус мужских половых органов.
Лечение народными средствами
Интересны в плане мягкой стимуляции и накопления собственного тестостерона разнообразные растительные препараты. Это алтайский "Красный корень", африканские "Вука-Вука" и "Йохимбе", тайская "Бутеа суперба" и другие природные средства. Однако коэффициент эффективности этих средств неясен, а клинические испытания не проведены в должном объёме. [13]
Прогноз. Профилактика
Прогноз эффективности терапии эректильной дисфункции зависит от этиологического фактора, запущенности процесса (степени фиброза кавернозных тел), возраста больного. Современные методики лечения позволяют, в основном, восстановить потенцию. Если даже терапия оказывается неэффективной, эрекцию можно обеспечить хирургическим путём.
Профилактика:
- Исключение губительных привычек— употребления никотина, алкогольных напитков, наркотиков, мастурбации и других.
- Огромную роль играет физическая активность. Требуется постоянное занятие физической культурой, так как эректильная дисфункция развивается в результате малоактивного образа жизни. Это приводит к застойным явлениям в простате и других мужских органах. Очень эффективными считают обычные приседания. Их рекомендуют выполнять по 60–90 в день. Это помогает нормализовать кровообращение в сосудах малого таза. Очень действенный способ профилактики — попеременное напряжение и расслабление мышц промежности. Отличные результаты в борьбе с недостаточной эрекцией даёт ходьба, бег.
- Сбалансированное питание играет ведущую роль в профилактике развития эректильной дисфункции. Так, морепродукты богаты важнейшими микроэлементами, такими как калий, цинк, магний, кальций, и омега-кислотами, что крайне необходимо для полноценной эрекции. Особенно ими богаты устрицы, крабы, красная икра, скумбрия, камбаловидные рыбы, морские ракообразные. Мёд и орехи содержат значительное количество цинка, повышают иммунитет, предупреждают развитие простатита, увеличивают мужскую силу. Петрушка, спаржа обладают значительными запасами токоферола — сильнейшего антиоксиданта, обладающего регуляторной функцией в отношении потенции. Для мужской силы уникальны такие специи, как кардамон, имбирь, красный перец. Они богаты витаминами Е, С, В2, В6, которые способствуют улучшению притока крови к мужским органам, благоприятствуют полноценной эрекции.
- Своевременная диагностика и терапия воспалительных заболеваний мочеполовой сферы.
Все эти превентивные меры помогут отодвинуть нарушения эрекции, вплоть до самого почтенного возраста.
Изучение эректильной дисфункции у пациентов, перенесших трансуретральные эндоскопические оперативные вмешательства на предстательной железе по поводу ее доброкачественной гиперплазии. Диагностика и результаты предоперационного обследования пациентов.
| Рубрика | Медицина |
| Вид | статья |
| Язык | русский |
| Дата добавления | 07.05.2014 |
| Размер файла | 28,3 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Новейшие достижения научно-технического прогресса в значительной степени изменили традиционный подход к лечению многих урологических заболеваний, в том числе приводящих к инфравезикальной обструкции, среди которых самым распространенным является доброкачественная гиперплазия предстательной железы (ДГПЖ).
Несмотря на то, что трансуретральные эндоскопические вмешательства давно уже стали традиционными для большинства урологических клиник и их доля по сравнению с открытыми оперативными вмешательствами на нижних мочевых путях значительно больше, постоянное внедрение в клиническую практику новой аппаратуры и инструментария обусловливает необходимость изучения возможных побочных эффектов их применения.
Одним из таких последствий является эректильная дисфункция. Доказано, что у пациентов, перенесших трансуретральную резекцию (ТУР) простаты по поводу ее гиперплазии, в 4-40% случаев развиваются расстройства эрекции той или иной степени выраженности (Bruskenitz, Larsen, Madsen, 1986; Hargreve et al., 1987). В работах М.Л. Гориловского (1997), L. Edwards et al. (1985), P. Soonawalla et al. (1992), A. Le Duc et al. (1993), Internet, National Library of Medicine, USA (1997) дан исчерпывающий анализ осложнений после ТУР. При этом частота возникновения нарушений эректильной функции в послеоперационном периоде отмечена у 3,3-34,8% пациентов.
S. Madersbacher и М. Marberger (1999) в своем исследовании, включающем анализ результатов обследования 3032 пациентов, страдающих ДГПЖ, которым впоследствии была проведена ТУР по стандартной методике и электровапоризация простаты, отмечают возникновение эректильной дисфункции в 19% случаев у больных, которым проведена ТУР и у 21% в группе пациентов после вапоризации. В подобном исследовании M.Y. Hammadeh et al. (2000), включающем две группы пациентов, перенесших ТУР и электровапоризацию (по 52 человека в каждой), в послеоперационном периоде отмечено появление эректильной дисфункции в 11% и 17% случаев соответственно.
В связи с повышением требований к качеству жизни и признанием удовлетворительной сексуальной активности одним из наиболее важных критериев его оценки, проблема лечения эректильных расстройств в настоящее время практически не имеет возрастных ограничений. Поскольку многие мужчины пожилого возраста, составляющие большинство среди больных, подвергающихся трансуретральным эндоскопическим вмешательствам, вкладывают в понятие улучшения качества жизни не только улучшение качества мочеиспускания, но и качества сексуальной жизни, столь высокий процент послеоперационной эректильной дисфункции требует пристального внимания врачей и исследователей к этой проблеме.
Трансуретральная резекция простаты по сравнению с чреспузырной аденомэктомией и особенно с радикальной простатэктомией сопровождается значительно меньшей травматизацией простаты, семенных пузырьков, семенного бугорка, уретры, но зачастую приводит к усугублению копулятивной дисфункции, которая имела место до оперативного вмешательства вследствие возрастных изменений в организме пациента (Geppi-Attee S., Sultana S., Hodgson G. еt al.,2000) .
Madorsky et al. (1997) впервые высказали гипотезу о роли термического повреждения структур кавернозных нервов при выполнении ТУР простаты в проекции 5 и 7 часов условного циферблата.
Повреждения нервных волокон тазового сплетения - основная причина эректильной дисфункции после хирургических вмешательств на органах малого таза. Поэтому тазовое сплетение и его эфферентные волокна, иннервирующие пещеристые тела (пещеристые нервы), в последнее время стали предметом всесторонних исследований. Walsh и Donker (1982) проследили топографию иннервации пещеристых тел на мертворожденных и плодах. Выявлено прохождение важных ветвей тазового сплетения между прямой кишкой и уретрой: они проникают через урогенитальную диафрагму вблизи уретры или через ее мышечную стенку. Авторы пришли к выводу, что после операций на предстательной железе (радикальная позадилонная простатэктомия, чреспузырная аденомэктомия, трансуретральная резекция простаты) эректильная дисфункция может возникать в результате повреждения этих ветвей в двух пунктах: при разделении латеральной ножки или во время апикального рассечения при механическом и термическом воздействии на стенку уретры. Частой причиной развития эректильной недостаточности после трансуретральных вмешательств также является поражение пещеристых нервов и сосудов полового члена, расположенных в парапростатической зоне при перфорации хирургической капсулы простаты (Walsh et аl., 1983; Вigg еt аl., 1990 Вгеndlег еt аl., 1990).
Несмотря на достигнутый в последние годы прогресс в диагностике и лечении эректильной дисфункции, вопросы, касающиеся особенностей этиопатогенеза, характера течения, прогностических критериев, лечения и профилактики данного состояния после эндоскопических оперативных вмешательств, окончательно не изучены. Все вышеперечисленное определяет научную и практическую актуальность решения этой проблемы.
Данное исследование проведено в период с 1997 по 2004 год на базе Научно-исследовательского института урологии МЗ РФ и Городской клинической урологической больницы № 47 города Москвы.
В качестве исследуемого контингента определены больные с диагностированной ДГПЖ, которым проведена трансуретральная резекция или электровапоризация простаты.
Характеристика групп больных
Из всех больных (412 человек) с доброкачественной гиперплазией простаты, которым планировалось выполнение трансуретральной резекции, 68,9% пациентов не были заинтересованы в сохранении адекватной эректильной функции в послеоперационном периоде. Более половины больных, имея потенциальную половую партнершу (жену), тем не менее смирились с возникшей дизритмией половой жизни (вплоть до ее полного отсутствия) на фоне прогрессирующего усиления симптоматики нарушений мочеиспускания. При этом во многих случаях отмечено скептическое отношение пациентов к доводам врача о том, что после нормализации мочеиспускания половая жизнь вполне возможна. Одинокий образ жизни, трудности обретения нового партнера, психологическая травма после потери супруги - это лишь основные причины отказа или воздержания большей части пожилого мужского населения от сексуальной активности.
Основная группа исследуемых пациентов, для которых сохранение, а также возможное улучшение эректильной функции представлялось актуальной задачей, состояла из 128 мужчин в возрасте от 48 до 80 лет (средний возраст 65,2 года). Более половины всех пациентов состояли в первом или повторном браке. Давность заболевания у этих больных составляла от года до пяти лет, а у вдовцов или разведенных в основном - пять лет и более. У 67,2% пациентов исследуемой группы выявлены интеркуррентные патологические изменения, представленные прежде всего сердечно-сосудистыми и дегенеративно-деструктивными заболеваниями. При этом 60,2% получали сопутствующую терапию, в том числе и препаратами, которые сами по себе ухудшают качество эрекции (гипотензивные средства, b- блокаторы, диуретики, блокаторы Н2-рецепторов и др.).
Оценка эректильной функции проводилась до и после операции посредством физикального обследования, заполнения пациентами оценочных шкал (Международного индекса эректильной функции, шкалы количественной оценки мужской копулятивной функции (О.Б. Лоран, А.С. Сегал, 1998), госпитальной шкалы тревоги и депрессии), RigiScan-мониторинга, фармакодопплерографии, электромиографии, исследования гормонального статуса, а также кавернозографии по показаниям.
Результаты предоперационного обследования
У всех 128 пациентов исследуемой группы до операции были выявлены клинические проявления доброкачественной гиперплазии предстательной железы. В 53,1% случаях больные предъявляли жалобы на симптомы, характерные для климактерического периода. Обращает на себя внимание тот факт, что практически все клинические проявления андропаузы (повышенная нервозность, ослабление памяти и внимания, быстрая утомляемость и др.) отрицательно сказываются не только на эректильной, но и на половой функции в целом. Отмечена тенденция к снижению количества предъявляемых "климактерических" жалоб у пациентов старше 60-65 лет при прогрессировании сопутствующих заболеваний.
Подавляющее большинство пациентов, заинтересованных в сохранении, а возможно и улучшении своей эректильной функции (90,6%), жили половой жизнью; у 81% была постоянная половая партнерша. У 75% отмечались той или иной степени выраженности жалобы сексуальной сферы, из которых недостаточность эрекции выявлена в 58,3% случаев, снижение либидо - 78,1%, затрудненная или ускоренная эякуляция - 47,9%, снижение выраженности оргазма - 86,5%. Многие пациенты предъявляли несколько жалоб. Несмотря на такую выраженность симптоматики, только 12,5% из них до операции эпизодически использовали средства, улучшающие качество эрекции (ингибиторы фосфодиэстеразы 5 типа, биологически активные пищевые добавки, а также методы нетрадиционной или народной медицины).
Несмотря на широкое освещение в средствах массовой информации вопросов профилактики и лечения ДГПЖ, при беседе с врачом 64,9% пациентов были уверены, что операция приведет к тотальной потере эректильной функции, а 39,9% высказывали неуверенность в результативности лечения с точки зрения улучшения качества самостоятельного мочеиспускания.
При исследовании половой активности пациентов в зависимости от степени возрастной разницы между супругами выявлено, что в основном (62%) наблюдаются спорадические проявления сексуальной активности (при частоте эксцессов менее 1 раза в неделю), 26,6% пациентов вели регулярную половую жизнь (1-2 раза в неделю) и только 7,4% отмечали повышенную сексуальную активность (более 2 раз в неделю). При этом выявлена общая тенденция повышения уровня сексуальной активности у всех пациентов при увеличении разницы между их возрастом и возрастом их жен.
Половой темперамент среднего уровня выявлен у 46,1% больных, сильный - у 18%, слабый - у 35,9%. При этом с возрастом отмечено снижение половой активности, прежде всего у пациентов со слабым половым темпераментом.
Гипотестостеронемия на дооперационном этапе выявлена у 42,2% больных, при этом отмечена тенденция большего снижения уровня тестостерона для старших возрастных групп. У 91,2% пациентов выявлена зависимость проявлений климактерического синдрома от уровня тестостерона плазмы крови. Однако частота встречаемости жалоб на снижение качества эрекций у пациентов с гипотестостеронемией достоверно не отличалась от таковой в общей группе. Между тем снижение либидо и сексуальной возбудимости были основными жалобами именно в группе с низким уровнем тестостерона.
До оперативного вмешательства гиперэстрогенемия наблюдалась в 12,5% случаев, при этом повышенный уровень эстрадиола плазмы крови в среднем умеренно повышался в старших возрастных группах.
Гиперпролактинемия выявлена в 8 наблюдениях (6,25%). Достоверной корреляции между возрастом и этими клиническими случаями не определено.
По данным трансректального ультразвукового исследования наблюдалась тенденция к увеличению объема предстательной железы с возрастом пациентов за счет роста объема узлов гиперплазии. Данные ультразвукового исследования коррелировали с данными урофлоуметрии, при этом признаки инфравезикальной обструкции были выявлены в 100% случаев.
Проведение RigiScan-мониторирования ночных пенильных тумесценций позволило выявить нарушения у 75,8% больных. Частота наблюдаемых нарушений ночных пенильных тумесценций увеличивалась в старших возрастных группах. В большинстве случаев отмечалась частично недостаточная эрекция (53,6%), недостаточная ригидность определена в 29,9% случаев, ее отсутствие - в 16,5%. Учитывая наличие нарушений сна у многих пациентов на дооперационном этапе, а также стойкую активацию симпатической нервной системы вследствие депрессивного настроения, результаты RigiScan-теста могут быть ложноотрицательными, поэтому для их объективизации необходимо проведение комплексной всесторонней оценки данных физикального, лабораторного и инструментальных методов обследования. При сравнении данных проведенной фармакодопплерографии с данными RigiScan-мониторирования васкулогенные нарушения коррелировали с нарушениями ночных пенильных тумесценций в 76,3% случаев (р
Читайте также:

