Энергетический эффект гликолиза реферат
Обновлено: 02.07.2024
Гликолиз - процесс окисления глюкозы, при котором из одной молекулы глюкозы образуются две молекулы пировиноградной кислоты, не является мембранозависимым процессом. Он происходит в цитоплазме. Однако ферменты гликолиза связаны со структурами цитоскелета. Суть гликолиза состоит в том, что молекула глюкозы (C6H12O6) без участия кислорода распадается на две молекулы пировиноградной кислоты (СН3СОСООН). При этом окисление идет за счет отщепления от молекулы глюкозы четырех атомов водорода, связывающихся со сложным органическим веществом НАД с получением двух молекул НАД•Н. Выделяющаяся при этом энергия запасается (40% от общего количества) в виде макроэргических связей двух молекул АТФ. 60% энергии выделяется в виде тепла. При последующем окислении НАД•Н получается еще 6 молекул АТФ. Таким образом, полный энергетический выход гликолиза в анаэробных условиях составляет 8 молекул АТФ.
Аэробный процесс гликолиза (10 реакций), уравнение (с образованием пирувата):
Анаэробный процесс гликолиза (11 реакций), уравнение (с образованием лактата):
Схема процесса гликолиза и его реакции

На схеме в рамках обозначены исходные субстраты и конечные продукты гликолиза, цифрами в скобках - число молекул.
ATP (АТФ) - это аденозинтрифосфорная кислота, универсальный источник энергии
ADP (АДФ) - это аденозиндифосфат, нуклеотид, участвует в энергетическом обмене
NAD (НАД) - никотинамидадениндинуклеотидфосфата
NADH (НАД•Н) - востановленная форма NAD
Таблица процесс гликолиза его реакции
Для распада и частичного окисления молекулы глюкозы требуется протекание 11 сложных последовательных реакций.
Ферменты, Активаторы, ингибиторы
Подготовительная стадия гликолиза
Стадия активации глюкозы проходит в 5 реакций, в ходе которых 1 молекула гексозы (глюкозы) расщепляется на 2 молекулы триоз-глицеральдегидфосфата
1. Необратимая реакция фосфорилирования глюкозы
Процесс гликолиза начинается с фосфорилирования глюкозы за счет АТФ - первая реакция. Это первая пусковая реакция гликолиза. Ее результатом является глюкозо-6-фосфат, имеющий отрицательный заряд. В гликолизе может участвовать не только глюкоза, но и другие гексозы (фруктоза), но в результате фосфорилирования и активации все равно образуется глюкозо-6-фосфат.

Ингибиторы: глюкозо-6-Ф, фосфоенолпируват.
2. Обратимая реакция изомеризации глюкозо-6-фосфата
Во второй реакции происходит изомеризация (внутримолекулярные перестройки) глюкозо-6-фосфата во фруктозо-6-фосфат.

3. Необратимая реакция фосфорилирования фруктозо-6-фосфата (ключевая стадия гликолиза)
В третьей реакции происходит фосфорилирование (присоединение остатка ортофосфорной кислоты) фруктозо-6-фосфата с образованием фруктозо-1,6-дифосфата. При этом затрачивается еще одна молекула АТФ (уже вторая) - это вторая пусковая реакция гликолиза. Она идет в присутствии Mg2 + и является необратимой, так как сопровождается масштабным уменьшением свободной энергии.

Ингибиторы: АТФ, цитрат, НАДН.
4. Обратимая реакция дихотомического расщепления фруктозо-1,6-дифосфата
В четвертой реакции гликолиза происходит расщепление фруктозо-1,6-дифосфата на две молекулы глицеральдегид-3-фосфата.

5. Обратимая реакция изомеризации дигидроксиацетона-3-фосфат в глицеральдегид-3-фосфат
В пятой реакции происходит изомеризация полученных триозофосфатов. На этом заканчивается первая стадия гликолиза.

Стадия генерации АТФ
Проходит в 6 реакций (или 5), в ходе которых энергия окислительных реакций трансформируется в химическую энергию АТФ (субстратное фосфорилирование).
6. Окисление глицеральдегид-3-фосфата до 1,3-дифосфоглицерата (реакция гликолитической оксиредукции)
В шестой реакции происходит окисление альдегидной группы до карбоксильной. Выделившийся Н+ акцептируется NAD, который восстанавливается до NADH. Освобождающаяся энергия затрачивается для образования высокоэнергетической связи 1,3-бифосфоглицерата (1,3-бифосфоглицериновая кислота).

7. Субстратное фосфорилирование АДФ (7)
В седьмой реакции фосфорильная группа 1,3-бифосфоглицерата переносится на ADP, в результате чего образуется АТР (напоминаем, что следует иметь в виду две параллельные цепи реакций, с участием двух молекул триоз, образовавшихся из одной молекулы гексозы, следовательно, синтезируется не одна, а две молекулы АТР).

8. Реакция изомеризации 3-фосфоглицерата в 2-фосфоглицерат
В восьмой реакции гликолиза происходит перенос фосфатной группы с третьего атома углерода на второй. В результате образуется 2-фосфоглицерат (2-фосфоглицериновая кислота).

9. Реакция енолизации
Девятая реакция сопровождается внутримолекулярными окислительно-восстановительными процессами, в результате которых образуется фосфоенолпируват (фосфоенолпировиноградная кислота) с высокоэнергетической связью во втором атоме углерода и отщепляется молекула воды

10. Реакция субстратного фосфорилирования
В ходе десятой реакции фосфорильная группа переносится на ADP. При этом синтезируется АТР и пируват (пировиноградная кислота). Эта реакция также необратима, поскольку высокоэкзергонична.

11. Реакция обратимого восстановления пировиноградной кислоты до молочной кислоты (в анаэробных условиях)
Если после гликолиза следует аэробное расщепление, пируват мигрирует в матрикс митохондрий, где, взаимодействуя с коэнзимом-А, участвует в образовании ацетил-СоА. В анаэробных условиях пируват при участии NADH восстанавливается до лактата (молочной кислоты), который при этом является конечным продуктом гликолиза. Затем в аэробных условиях лактат может обратно превратиться в пируват и окислиться в митохондриях.

_______________
Источник информации:
1. Биология для поступающих в вузы / Г.Л. Билич, В.А. Крыжановский. — 2008.
Гликолиз (от греч. glycys – сладкий и lysis – растворение, распад) – это последовательность ферментативных реакций, приводящих к превращению глюкозы в пируват с одновременным образованием АТФ.
При аэробных условиях пируват проникает в митохондрии, где полностью окисляется до СО2 и Н2О. Если содержание кислорода недостаточно, как это может иметь место в активно сокращающейся мышце, пируват превращается в лактат.
Итак, гликолиз – не только главный путь утилизации глюкозы в клетках, но и уникальный путь, поскольку он может использовать кислород, если
последний доступен (аэробные условия), но может протекать и в отсутствие кислорода (анаэробные условия).
Анаэробный гликолиз – сложный ферментативный процесс распада глюкозы, протекающий в тканях человека и животных без потребления кислорода. Конечным продуктом гликолиза является молочная кислота. В процессе гликолиза образуется АТФ. Суммарное уравнение гликолиза можно представить следующим образом:

В анаэробных условиях гликолиз – единственный процесс в животном организме, поставляющий энергию. Именно благодаря гликолизу организм человека и животных определенный период может осуществлять ряд физиологических функций в условиях недостаточности кислорода. В тех случаях, когда гликолиз протекает в присутствии кислорода, говорят об аэробном гликолизе .
Последовательность реакций анаэробного гликолиза, так же как и их промежуточные продукты, хорошо изучена. Процесс гликолиза катализируется одиннадцатью ферментами, большинство из которых выделено в гомогенном, клисталлическом или высокоочищенном виде и свойства которых достаточно известны. Заметим, что гликолиз протекает в гиало-плазме (цитозоле) клетки.
Первой ферментативной реакцией гликолиза является фосфорилирование, т.е. перенос остатка ортофосфата на глюкозу за счет АТФ. Реакция катализируется ферментом гексокиназой:
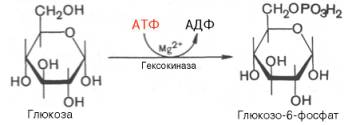
Образование глюкозо-6-фосфата в гексокиназной реакции сопровождается освобождением значительного количества свободной энергии системы и может считаться практически необратимым процессом.
Наиболее важным свойством гексокиназы является ее ингибирование глюкозо-6-фосфатом, т.е. последний служит одновременно и продуктом реакции, и аллостерическим ингибитором.
Фермент гексокиназа способен катализировать фосфорилирование не только D-глюкозы, но и других гексоз, в частности D-фруктозы, D-маннозы и т.д. В печени, кроме гексокиназы, существует фермент глюкокиназа, который катализирует фосфорилирование только D-глюкозы. В мышечной ткани этот фермент отсутствует (подробнее см. главу 16).
Второй реакцией гликолиза является превращение глюкозо-6-фос-фата под действием фермента глюкозо-6-фосфатизомеразы во фруктозо-6-фосфат:
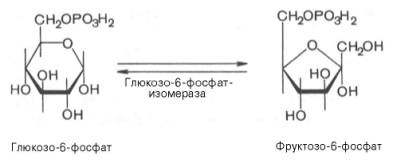
Эта реакция протекает легко в обоих направлениях, и для нее не требуется каких-либо кофакторов.
Третья реакция катализируется ферментом фосфофруктокиназой; образовавшийся фруктозо-6-фосфат вновь фосфорилируется за счет второй молекулы АТФ:
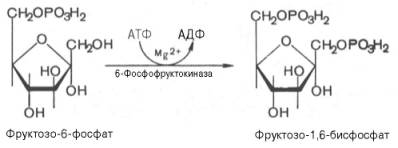
Данная реакция аналогично гексокиназной практически необратима, протекает в присутствии ионов магния и является наиболее медленно текущей реакцией гликолиза. Фактически эта реакция определяет скорость гликолиза в целом.
Фосфофруктокиназа относится к числу аллостерических ферментов. Она ингибируется АТФ и стимулируется АМФ . При значительных величинах отношения АТФ/АМФ активность фосфофруктокиназы угнетается и гликолиз замедляется. Напротив, при снижении этого коэффициента интенсивность гликолиза повышается. Так, в неработающей мышце активность фосфофруктокиназы низкая, а концентрация АТФ относительно высокая. Во время работы мышцы происходит интенсивное потребление АТФ и активность фосфофруктокиназы повышается, что приводит к усилению процесса гликолиза.
Четвертую реакцию гликолиза катализирует фермент альдолаза. Под влиянием этого фермента фруктозо-1,6-бисфосфат расщепляется на две фосфотриозы:
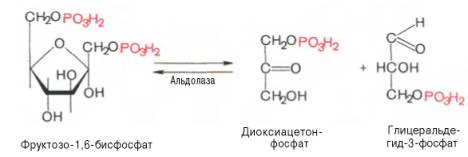
Эта реакция обратима. В зависимости от температуры равновесие устанавливается на различном уровне. При повышении температуры реакция сдвигается в сторону большего образования триозофосфатов (дигидро-ксиацетонфосфата и глицеральдегид-3-фосфата).
Пятая реакция – это реакция изомеризации триозофосфатов. Катализируется ферментом триозофосфатизомеразой:

Равновесие данной изомеразной реакции сдвинуто в сторону дигид-роксиацетонфосфата: 95% дигидроксиацетонфосфата и около 5% глице-ральдегид-3-фосфата. В последующие реакции гликолиза может непосредственно включаться только один из двух образующихся триозофосфатов, а именно глицеральдегид-3-фосфат. Вследствие этого по мере потребления в ходе дальнейших превращений альдегидной формы фосфотриозы ди-гидроксиацетонфосфат превращается в глицеральдегид-3-фосфат.
Образованием глицеральдегид-3-фосфата как бы завершается первая стадия гликолиза. Вторая стадия – наиболее сложная и важная. Она включает окислительно-восстановительную реакцию (реакция гликолитической оксидоредукции), сопряженную с субстратным фосфорилированием, в процессе которого образуется АТФ.
В результате шестой реакции глицеральдегид-3-фосфат в присутствии фермента глицеральдегидфосфатдегидрогеназы, кофермента НАД и неорганического фосфата подвергается своеобразному окислению с образованием 1,3-бисфосфоглицериновой кислоты и восстановленной формы НАД (НАДН). Эта реакция блокируется йод- или бромацетатом, протекает в несколько этапов:
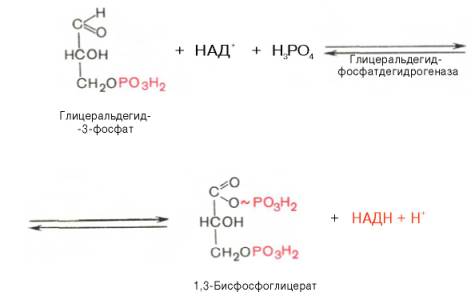
Седьмая реакция катализируется фосфоглицераткиназой, при этом происходит передача богатого энергией фосфатного остатка (фосфатной группы в положении 1) на АДФ с образованием АТФ и 3-фосфогли-цериновой кислоты (3-фосфоглицерат):
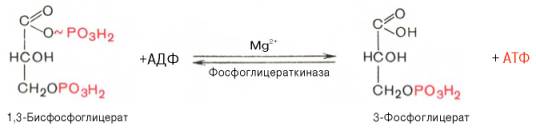
Таким образом, благодаря действию двух ферментов (глицеральде-гидфосфатдегидрогеназы и фосфоглицераткиназы) энергия, высвобождающаяся при окислении альдегидной группы глицеральдегид-3-фосфата до карбоксильной группы, запасается в форме энергии АТФ. В отличие от окислительного фосфорилирования образование АТФ из высокоэнергетических соединений называется субстратным фосфорилированием.
Восьмая реакция сопровождается внутримолекулярным переносом оставшейся фосфатной группы, и 3-фосфоглицериновая кислота превращается в 2-фосфоглицериновую кислоту (2-фосфоглицерат).
Реакция легкообратима, протекает в присутствии ионов Mg 2+ . Кофактором фермента является также 2,3-бисфосфоглицериновая кислота аналогично тому, как в фосфоглюкомутазной реакции роль кофактора выполняет глюкозо-1,6-бисфосфат:

Девятая реакция катализируется ферментом енолазой, при этом 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится высокоэргической:
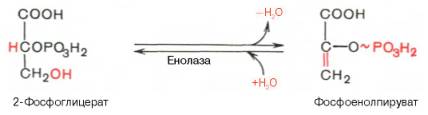
Енолаза активируется двухвалентными катионами Mg 2+ или Мn 2+ и ингибируется фторидом.
Десятая реакция характеризуется разрывом высокоэргической связи и переносом фосфатного остатка от фосфоенолпирувата на АДФ (субстратное фосфорилирование). Катализируется ферментом пируваткиназой:
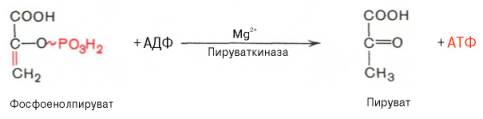
Для действия пируваткиназы необходимы ионы Mg 2+ , а также одновалентные катионы щелочных металлов (К + или др.). Внутри клетки реакция является практически необратимой.
В результате одиннадцатой реакции происходит восстановление пировиноградной кислоты и образуется молочная кислота. Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАДН, образовавшегося в шестой реакции:

Последовательность протекающих при гликолизе реакций представлена на рис. 10.3.
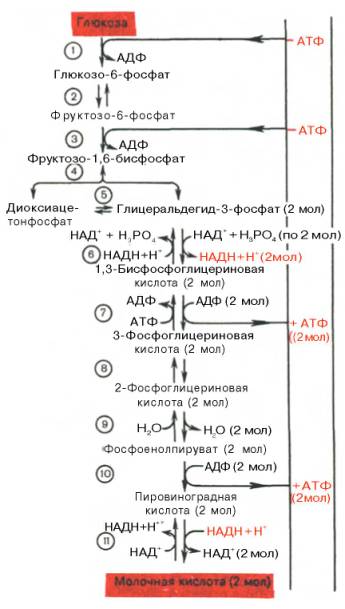
Рис. 10.3. Последовательность реакций гликолиза.
1 - гексокиназа; 2 - фосфоглюкоизоме-раза; 3 - фосфофруктокиназа; 4 - альдо-лаза; 5 - триозофосфатизомераза; 6 - гли-церальдегидфосфатдегидрогеназа; 7 -фосфоглицераткиназа; 8 - фосфоглицеромутаза; 9 - енолаза; 10 - пируватки-наза; 11 - лактатдегидрогеназа.
Реакция восстановления пирувата завершает внутренний окислительно-восстановительный цикл гликолиза. НАД + при этом играет роль промежуточного переносчика водорода от глицеральдегид-3-фосфата (6-я реакция) на пировиноградную кислоту (11-я реакция), при этом сам он регенерируется и вновь может участвовать в циклическом процессе, получившем название гликолитический оксидоредукции.
Биологическое значение процесса гликолиза заключается прежде всего в образовании богатых энергией фосфорных соединений. На первых стадиях гликолиза затрачиваются 2 молекулы АТФ (гексокиназная и фосфофрук-токиназная реакции). На последующих образуются 4 молекулы АТФ (фосфоглицераткиназная и пируваткиназная реакции). Таким образом, энергетическая эффективность гликолиза в анаэробных условиях составляет 2 молекулы АТФ на одну молекулу глюкозы.
Как отмечалось, основной реакцией, лимитирующей скорость гликолиза, является фосфофруктокиназная. Вторая реакция, лимитирующая скорость и регулирующая гликолиз – гексокиназная реакция. Кроме того, контроль гликолиза осуществляется также ЛДГ и ее изоферментами.
В тканях с аэробным метаболизмом (ткани сердца, почек и др.) преобладают изоферменты ЛДГ1 и ЛДГ2 (см. главу 4). Эти изоферменты инги-бируются даже небольшими концентрациями пирувата, что препятствует образованию молочной кислоты и способствует более полному окислению пирувата (точнее, ацетил-КоА) в цикле трикарбоновых кислот.
В тканях человека, в значительной степени использующих энергию гликолиза (например, скелетные мышцы), главными изоферментами являются ЛДГ5 и ЛДГ4. Активность ЛДГ5 максимальна при тех концентрациях пирувата, которые ингибируют ЛДГ1. Преобладание изоферментов ЛДГ4 и ЛДГ5 обусловливает интенсивный анаэробный гликолиз с быстрым превращением пирувата в молочную кислоту.
Как отмечалось, процесс анаэробного распада гликогена получил название гликогенолиза. Вовлечение D-глюкозных единиц гликогена в процесс гликолиза происходит при участии 2 ферментов – фосфорилазы а и фосфо-глюкомутазы. Образовавшийся в результате фосфоглюкомутазной реакции глюкозо-6-фосфат может включаться в процесс гликолиза. После образования глюкозо-6-фосфата дальнейшие пути гликолиза и гликогенолиза полностью совпадают:
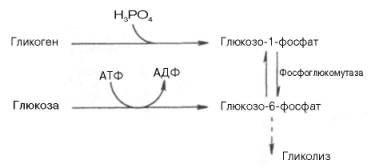
В процессе гликогенолиза в виде макроэргических соединений накапливаются не две, а три молекулы АТФ (АТФ не тратится на образование глюкозо-6-фосфата). Кажется, что энергетическая эффективность глико-генолиза выглядит несколько более высокой по сравнению с процессом гликолиза, но эта эффективность реализуется только при наличии активной фосфорилазы а. Следует иметь в виду, что в процессе активации фосфо-рилазы b расходуется АТФ (см. рис. 10.2).
Название работы: Аэробный гликолиз и его биологическая роль
Предметная область: Биология и генетика
Описание: До стадии образования 3-фосфоглицераль-дегида реакции его совпадают с реакциями анаэробного гликолиза. В дальнейшем, в процессе превращения двух молекул 3-фосфоглицеральдегида в две молекулы 1,3-бисфосфоглицериновой кислоты из двух молекул НАД генерируются две молекулы.
Дата добавления: 2015-09-06
Размер файла: 186.7 KB
Работу скачали: 11 чел.
Аэробный гликолиз и его биологическая роль. Аэробный гликолиз основной источник АТФ в клетках.






До стадии образования 3-фосфоглицераль-дегида реакции его совпадают с реакциями анаэробного гликолиза. В дальнейшем, в процессе превращения двух молекул 3-фосфоглицеральдегида в две молекулы 1,3-бисфосфоглицериновой кислоты из двух молекул НАД генерируются две молекулы НАД-Н2. При окислении последних в дыхательной цепи митохондрий выраба-тывается 6 молекул АТФ (2Х3). Реакции окисления двух молекул1,3-бисфосфоглиц-ериновой кислоты до двух молекул пировиноградной кислоты также совпадают с соответствующими реакциями анаэроб-ного гликолиза. В дальнейшем все идет по-другому: 2 молекулы пировиноградной кислоты превращаются в 2 молекулы ацетил-КоА:

При этом происходит восстановление двух молекул НАД. При окислении двух молекул НАД-Н2 в дыхательной цепи митохондрий вырабатывается 6 молекул АТФ. Реакцию катализирует пируватдегидрогеназный комплекс, отщепляющий от молекул пирувата углекислый газ (окислительное декарбоксилирование) и присоединяющий к месту отщепления S -КоА. В состав его входят 5 коферментов: НАД, ФАД, ТиаминДФ, HS -КоА и липоевая кислота. Образующиеся 2 молекула ацетил-КоА в дальнейшем окисляются в цикле Кребса. При этом генерируются 2 молекулы ГТФ, восстанавливаются 6 (2Х3)молекул НАД и 2 молекулы ФАД. При дальнейшем окислении НАД-Н2 и ФАД-Н2 в дыхательной цепи митохондрий генерируются 22 молекулы АТФ. Физиологическая роль аэробного гликолиза. 1. Этот процесс является основным источником АТФ в клетках. При окислении одной молекулы глюкозы затрачивается 2 молекулы АТФ (в гексокиназной и фосфофруктокиназной реакциях), но генерируется 40 его молекул в реакциях 3-фосфоглицеральдегиддегид-рогеназной 6 АТФ, фосфоглицерат-киназной 2 АТФ, пируваткиназной 2 АТФ, пируватдегидрогеназной 6 АТФ, изоцитратдегидрогеназной 6 АТФ, α-кетоглутаратдегидрогеназной 6 АТФ,
сукцинилтиокиназной 2 АТФ, малатдегидрогеназной 6 АТФ. Итого - 40 молекул АТФ. С учетом двух затраченных молекул АТФ энергетический эффект окисления одной молекулы глюкозы в реакция аэробного окисления глюкозы составляет 38 молекул АТФ. Конечными продуктами этого процесса являются углекислый газ и вода. 2. В реакциях аэробного гликолиза образуются метаболиты, необходимые для биосинтеза других веществ. Пировиноградная, щавелевоуксусная и α-кетоглутаровая кислоты участвуют в реакциях переаминирования аминокислот. 3-фосфоглицеральдегид используется для биосинтеза глицерола, а ацетил-КоА жирных кислот, холестерола и т.д. Из пировиноградной кислоты синтезируется щавелевоуксусная кислота, необходимая для функционирования цикла Кребса.
Углеводы – это многоатомные спирты содержащие оксогруппу.
По количеству мономеров все углеводы делят на: моно-, ди-, олиго- и полисахариды.
Моносахариды по положению оксогруппы делятся альдозы и кетозы.
По количеству атомов углерода моносахариды делятся на триозы, тетрозы, пентозы, гексозы и т.д.
Углеводы. Функции углеводов
Моносахариды – углеводы, которые не гидролизуются до более простых углеводов.
- выполняют энергетическую функцию (образование АТФ).
- выполняют пластическую функцию (участвуют в образовании ди-, олиго-, полисахаридов, аминокислот, липидов, нуклеотидов).
- выполняют детоксикационную функцию (производные глюкозы, глюкурониды, участвуют в обезвреживании токсичных метаболитов и ксенобиотиков).
являются фрагментами гликолипидов (цереброзиды).
Дисахариды – углеводы, которые гидролизуются на 2 моносахарида. У человека образуется только 1 дисахарид – лактоза. Лактоза синтезируется при лактации в молочных железах и содержится в молоке. Она:
- является источником глюкозы и галактозы для новорожденных;
- участвует в формировании нормальной микрофлоры у новорожденных.
Олигосахариды – углеводы, которые гидролизуются на 3 – 10 моносахаридов.
Олигосахариды являются фрагментами гликопротеинов (ферменты, белки-транспортёры, белки-рецепторы, гормоны), гликолипидов (глобозиды, ганглиозиды). Они образуют на поверхности клетки гликокаликс.
Полисахариды – углеводы, которые гидролизуются на 10 и более моносахаридов. Гомополисахариды выполняют запасающую функцию (гликоген – форма хранения глюкозы). Гетерополисахариды (ГАГ) являются структурным компонентом межклеточного вещества (хондроитинсульфаты, гиалуроновая кислота), участвуют в пролиферации и дифференцировке клеток, препятствуют свертыванию крови (гепарин).
Углеводы пищи, нормы и принципы нормирования их суточной пищевой потребности.
Углеводы. Биологическая роль.
В пище человека в основном содержатся полисахариды — крахмал, целлюлоза растений, в меньшем количестве – гликоген животных. Источником сахарозы служат растения, особенно сахарная свёкла, сахарный тростник. Лактоза поступает с молоком млекопитающих (в коровьем молоке до 5% лактозы, в женском молоке — до 8%). Фрукты, мёд, соки содержат небольшое количество глюкозы и фруктозы. Мальтоза есть в солоде, пиве.
Углеводы пищи являются для организма человека в основном источником моносахаридов, преимущественно глюкозы. Некоторые полисахариды: целлюлоза, пектиновые вещества, декстраны, у человека практически не перевариваются, в ЖКТ они выполняют функцию сорбента (выводят холестерин, желчные кислоты, токсины и д.р.), необходимы для стимуляции перистальтики кишечника и формирования нормальной микрофлоры.
Углеводы — обязательный компонент пищи, они составляют 75% массы пищевого рациона и дают более 50% необходимых калорий. У взрослого человека суточная потребность в углеводах 400г/сут, в целлюлозе и пектине до 10-15 г/сут. Рекомендуется употреблять в пищу больше сложных полисахаридов и меньше моносахаров.
Углеводы. Переваривание углеводов
Переваривание это процесс гидролиза веществ до их ассимилируемых форм. Переваривание бывает:
- 1). Внутриклеточное (в лизосомах);
- 2). Внеклеточное (в ЖКТ):
а). полостное (дистантное);
б). пристеночное (контактное).
Переваривание углеводов в ротовой полости (полостное)
В ротовой полости пища измельчается при пережёвывании и смачивается слюной. Слюна состоит на 99% из воды и обычно имеет рН 6,8. В слюне присутствует эндогликозидаза α-амилаза (α-1,4-гликозидаза), расщепляющая в крахмале внутренние α-1,4-гликозидные связи с образованием крупных фрагментов — декстринов и небольшого количества мальтозы и изомальтозы. Необходим ион Cl-.
Переваривание углеводов в желудке (полостное)
Действие амилазы слюны прекращается в кислой среде (рН глюкоза > фруктоза > другие моносахариды.
Моносахариды выходят из энтероцитов в направлении кровеносного капилляра с помощью облегченной диффузии через белки-переносчики.
Углеводы. Нарушение переваривания и всасывания углеводов
Недостаточное переваривание и всасывание переваренных продуктов называют мальабсорбцией. В основе мальабсорбции углеводов могут быть причины двух типов:
- 1). Наследственные и приобретенные дефекты ферментов, участвующих в переваривании. Известны наследственные дефекты лактазы, α-амилазы, сахаразно-изомальтазного комплекса. Без лечения эти патологии сопровождаются хроническим дисбактериозом и нарушениями физического развития ребёнка.
Приобретённые нарушения переваривания могут наблюдаться при кишечных заболеваниях, например гастритах, колитах, энтеритах, после операций на ЖКТ.
Дефицит лактазы у взрослых людей может быть связан со снижением экспрессии гена лактазы, что проявляться непереносимостью молока – наблюдается рвота, диарея, спазмы и боли в животе, метеоризм. Частота этой патологии составляет в Европе 7—12%, в Китае — 80%, в Африке — до 97%. - 2). Нарушение всасывания моносахаридов в кишечнике.
Нарушения всасывания могут быть следствием дефекта какого-либо компонента, участвующего в системе транспорта моносахаридов через мембрану. Описаны патологии, связанные с дефектом натрийзависимого белка переносчика глюкозы.
Синдром мальабсорбции сопровождается осмотической диареей, усилением перистальтики, спазмами, болями, а также метеоризмом. Диарею вызывают нерасщеплённые дисахариды или невсосавшиеся моносахариды в дистальных отделах кишечника, а также органические кислоты, образованные микроорганизмами при неполном расщеплении углеводов.
Транспорт глюкозы из крови в клетки
Глюкоза поступает из кровотока в клетки путём облегчённой диффузии с помощью белков-переносчиков – ГЛЮТов. Глюкозные транспортёры ГЛЮТы имеют доменную организацию и обнаружены во всех тканях.
Выделяют 5 типов ГЛЮТов:
- ГЛЮТ-1 – преимущественно в мозге, плаценте, почках, толстом кишечнике;
- ГЛЮТ-2 – преимущественно в печени, почках, β-клетках поджелудочной железы, энтероцитах, есть в эритроцитах. Имеет высокую Км;
- ГЛЮТ-3 – во многих тканях, включая мозг, плаценту, почки. Обладает большим, чем ГЛЮТ-1, сродством к глюкозе;
- ГЛЮТ-4 – инсулинзависимый, в мышцах (скелетной, сердечной), жировой ткани;
- ГЛЮТ-5 – много в клетках тонкого кишечника, является переносчиком фруктозы.
ГЛЮТы, в зависимости от типа, могут находиться преимущественно как в плазматической мембране, так и в цитозольных везикулах. Трансмембранный перенос глюкозы происходит только тогда, когда ГЛЮТы находятся в плазматической мембране. Встраивание ГЛЮТов в мембрану из цитозольных везикул происходит под действием инсулина. При снижении концентрации инсулина в крови эти ГЛЮТы снова перемещаются в цитоплазму. Ткани, в которых ГЛЮТы без инсулина почти полностью находятся в цитоплазме клеток (ГЛЮТ-4, и в меньшей мере ГЛЮТ-1), оказываются инсулинзависимыми (мышцы, жировая ткань), а ткани, в которых ГЛЮТы преимущественно находятся в плазматической мембране (ГЛЮТ-3) – инсулиннезависимыми.
Известны различные нарушения в работе ГЛЮТов. Наследственный дефект этих белков может лежать в основе инсулинонезависимого сахарного диабета.
Углеводы. Метаболизм моносахаридов в клетке
После всасывания в кишечнике глюкоза и другие моносахариды поступают в воротную вену и далее в печень. Моносахариды в печени превращаются в глюкозу или продукты её метаболизма. Часть глюкозы в печени депонируется в виде гликогена, часть идет на синтез новых веществ, а часть через кровоток, направляется в другие органы и ткани. При этом печень поддерживает концентрацию глюкозы в крови на уровне 3,3-5,5 ммоль/л.
Фосфорилирование и дефосфорилирование моносахаридов
В клетках глюкоза и другие моносахариды с использованием АТФ фосфорилируются до фосфорных эфиров: глюкоза + АТФ → глюкоза-6ф + АДФ. Для гексоз эту необратимую реакцию катализирует фермент гексокиназа, которая имеет изоформы: в мышцах – гексокиназа II, в печени, почках и β-клетках поджелудочной железы – гексокиназа IV (глюкокиназа), в клетках опухолевых тканей – гексокиназа III. Фосфорилирование моносахаридов приводит к образованию реакционно-способных соединений (реакция активации), которые не способны покинуть клетку т.к. нет соответствующих белков-переносчиков. Фосфорилирование уменьшает количество свободной глюкозы в цитоплазме, что облегчает ее диффузию из крови в клетки.
Гексокиназа II фосфорилирует D-глюкозу, и с меньшей скоростью, другие гексозы. Обладая высоким сродством к глюкозе (Кm 107Да (50000 остатков глюкозы), в котором остатки глюкозы соединены в линейных участках α-1,4-гликозидной связью. В точках ветвления, примерно через каждые 10 остатков глюкозы, мономеры соединены α-1,6-гликозидными связями. Гликоген, водонерастворим, хранится в цитозоле клетки в форме гранул диаметром 10-40 нм. Гликоген депонируется главным образом в печени (до 5%) и скелетных мышцах (до 1%). В организме может содержаться от 0 до 450 г гликогена.
Разветвлённая структура гликогена способствует работе ферментов, отщепляющих или присоединяющих мономеры.
Углеводы. Синтез гликогена (гликогеногенез)
Гликоген синтезируется с затратой энергии в период пищеварения (через 1—2 ч после приёма углеводной пищи).


При удлинении линейного участка примерно до 11 глюкозных остатков, фермент ветвления переносит её концевой блок, содержащий 6—7 остатков, на внутренний остаток глюкозы этой или другой цепи с образованием α-1,6-гликозидной связи. Новая точка ветвления образуется на расстоянии не менее 4 остатков от любой уже существующей точки ветвления.
Углеводы. Распад гликогена (гликогенолиз)
Распад гликогена происходит путем последовательного отщепления глюкозо-1-ф в ответ на повышение потребности организма в глюкозе. Реакцию катализирует гликогенфосфорилаза:

Гликогенфосфорилаза состоит из 2 идентичных субъединиц (94500 Да). Неактивная форма обозначается b, активная – a. Активируется киназой фосфорилазы b путем фосфорилирования каждой субъединицы по серину в 14 положении.
Гликогенфосфорилаза расщепляет фосфоролизом α-1,4-гликозидные связи, до тех пор, пока до точки ветвления не остается 4 остатка глюкозы.

Инактивация гликогенфосфорилазы происходит при дефосфорилировании с участием специфической фосфатазы фосфорилазы (фосфопротеинфосфотазы ФПФ).
Удаление ветвления осуществляет деветвящий фермент. Он обладает трансферазной и гликозидазной активностями. Трасферазная часть (олигосахаридтрансфераза) переносит три оставшихся до точки ветвления глюкозных остатка на нередуцирующий конец соседней цепи, удлиняя её для фосфорилазы.

Гликозидазная часть (α-1,6-глюкозидаза) гидролизует α-1,6-гликозидную связь, отщепляя глюкозу.
Глюкозо-1-ф изомеризуется в глюкозо-6-ф фосфоглюкомутазой.
Регуляция метаболизма гликогена в печени

Регуляция метаболизма гликогена в мышцах

Метаболизм гликогена контролируется гормонами (в печени – инсулином, глюкагоном, адреналином; в мышцах – инсулином и адреналином), которые регулируют фосфорилирование /дефосфорилирование 2 ключевых ферментов гликогенсинтазы и гликогенфосфорилазы.
При недостаточном уровне глюкозы в крови выделяется гормон глюкагон, в крайних случаях – адреналин. Они стимулируют фосфорилирование гликогенсинтазы (она инактивируется) и гликогенфосфорилазы (она активируется). При повышении уровня глюкозы в крови выделяется инсулин, он стимулирует дефосфорилирование гликогенсинтазы (она активируется) и гликогенфосфорилазы (она инактивируется). Кроме того, инсулин индуцирует синтез глюкокиназы, тем самым, ускоряя фосфорилирование глюкозы в клетке. Всё это приводит к тому, что инсулин стимулирует синтез гликогена, а адреналин и глюкагон – его распад.
В печени существует и аллостерическая регуляция гликогенфосфорилазы: ее ингибирует АТФ и глюкозо-6ф, а активирует АМФ.
Углеводы. Нарушения обмена гликогена
Гликогеновые болезни — группа наследственных нарушений, в основе которых лежит снижение или отсутствие активности ферментов, катализирующих реакции синтеза или распада гликогена, либо нарушение регуляции этих ферментов.
Гликогенозы — заболевания, обусловленные дефектом ферментов, участвующих в распаде гликогена. Они проявляются или необычной структурой гликогена, или его избыточным накоплением в печени, сердечной или скелетных мышцах, почках, лёгких и других органах.
В настоящее время гликогенозы делят на 2 группы: печёночные и мышечные.
Печёночные формы гликогенозов ведут к нарушению использования гликогена для поддержания уровня глюкозы в крови. Поэтому общий симптом для этих форм — гипогликемии в постабсорбтивный период.
- 1). В гепатоцитах: ↑глюкозо-6-ф → ↑ПВК, ↑лактат (ацидоз), ↑рибозо-5-ф. ↑рибозо-5-ф→ ↑пуринов→ ↑ мочевая кислота
- 2). В крови: ↓глюкоза →↓инсулин/глюкагон→:
а) ↑липолиз жировой ткани → ↑ЖК в крови.
б). ↓ЛПЛ жировой ткани → ↑ТАГ в крови.
Лечение – диета по глюкозе, частое кормление.
Болезнь Кори (тип III) распространена, 1/4 всех печёночных гликогенозов. Накапливается разветвленный гликоген, так как дефектен деветвящий фермент. Гликогенолиз возможен, но в незначительном объёме. Лактоацидоз и гиперурикемия не отмечаются. Болезнь отличается более лёгким течением чем болезнь Гирке.
Мышечные формы гликогенозов характеризуются нарушением в энергоснабжении скелетных мышц. Эти болезни проявляются при физических нагрузках и сопровождаются болями и судорогами в мышцах, слабостью и быстрой утомляемостью.
Болезнь МакАрдла (тип V) — аутосомно-рецессивная патология, отсутствует в скелетных мышцах активность гликогенфосфорилазы. Накопление в мышцах гликогена аномальной структуры.
Агликогенозы
Агликогеноз (гликогеноз 0 по классификации) — заболевание, возникающее в результате дефекта гликогенсинтазы. В печени и других тканях больных наблюдают очень низкое содержание гликогена. Это проявляется резко выраженной гипогликемией в постабсорбтивном периоде. Характерный симптом — судороги, проявляющиеся особенно по утрам. Болезнь совместима с жизнью, но больные дети нуждаются в частом кормлении.
Углеводы. Катаболизм глюкозы. Гликолиз
Основные пути катаболизма глюкозы
Катаболизм глюкозы в клетке может проходить как в аэробных, так и в анаэробных условиях, его основная функция – это синтез АТФ.
Аэробное окисление глюкозы
В аэробных условиях глюкоза окисляется до СО2 и Н2О. Суммарное уравнение:
С6Н12О6 + 6О2 → 6СО2+ 6Н2О + 2880 кДж/моль.
Этот процесс включает несколько стадий:
- 1. Аэробный гликолиз. В нем происходит окисления 1 глюкозы до 2 ПВК, с образованием 2 АТФ (сначала 2 АТФ затрачиваются, затем 4 образуются) и 2 НАДН2;
- 2. Превращение 2 ПВК в 2 ацетил-КоА с выделением 2 СО2 и образованием 2 НАДН2;
- 3. ЦТК. В нем происходит окисление 2 ацетил-КоА с выделением 4 СО2, образованием 2 ГТФ (дают 2 АТФ), 6 НАДН2 и 2 ФАДН2;
- 4. Цепь окислительного фосфорилирования. В ней происходит окисления 10 (8) НАДН2, 2 (4) ФАДН2 с участием 6 О2, при этом выделяется 6 Н2О и синтезируется 34 (32) АТФ.
В результате аэробного окисления глюкозы образуется 38 (36) АТФ, из них: 4 АТФ в реакциях субстратного фосфорилирования, 34 (32) АТФ в реакциях окислительного фосфорилирования. КПД аэробного окисления составит 65%.
Анаэробное окисление глюкозы
Катаболизм глюкозы без О2 идет в анаэробном гликолизе и ПФШ (ПФП).
- В ходе анаэробного гликолиза происходит окисления 1 глюкозы до 2 молекул молочной кислоты с образованием 2 АТФ (сначала 2 АТФ затрачиваются, затем 4 образуются). В анаэробных условиях гликолиз является единственным источником энергии. Суммарное уравнение: С6Н12О6 + 2Н3РО4 + 2АДФ → 2С3Н6О3 + 2АТФ + 2Н2О.
- В ходе ПФП из глюкозы образуются пентозы и НАДФН2. В ходе ПФШ из глюкозы образуются только НАДФН2.
Углеводы. ГЛИКОЛИЗ
Гликолиз – главный путь катаболизма глюкозы (а также фруктозы и галактозы). Все его реакции протекают в цитозоле.
Аэробный гликолиз – это процесс окисления глюкозы до ПВК, протекающий в присутствии О2.
Анаэробный гликолиз – это процесс окисления глюкозы до лактата, протекающий в отсутствии О2.
Анаэробный гликолиз отличается от аэробного только наличием последней 11 реакции, первые 10 реакций у них общие.
Этапы гликолиза
В любом гликолизе можно выделить 2 этапа:
- 1 этап подготовительный, в нем затрачивается 2 АТФ. Глюкоза фосфорилируется и расщепляется на 2 фосфотриозы;
- 2 этап, сопряжён с синтезом АТФ. На этом этапе фосфотриозы превращаются в ПВК. Энергия этого этапа используется для синтеза 4 АТФ и восстановления 2НАДН2, которые в аэробных условиях идут на синтез 6 АТФ, а в анаэробных условиях восстанавливают ПВК до лактата.
Энергетический баланс гликолиза
Таким образом, энергетический баланс аэробного гликолиза:
8АТФ = -2АТФ + 4АТФ + 6АТФ (из 2НАДН2)
Энергетический баланс анаэробного гликолиза:
2АТФ = -2АТФ + 4АТФ
Общие реакции аэробного и анаэробного гликолиза
1. Гексокиназа (гексокиназа II, АТФ: гексозо-6-фосфотрансфераза) в мышцах фосфорилирует в основном глюкозу, меньше – фруктозу и галактозу. Кm
Глюкоза играет главную роль в метаболизме, так как именно она является основным источником энергии. Глюкоза может превращаться практически во все моносахариды, однако возможно и обратное превращение. Основные пути метаболизма глюкозы:
катаболизм глюкозы – гликолиз;
синтез глюкозы – глюконеогенез;
депонирование и распад гликогена;
синтез пентоз – пентозофосфатные пути.
Гликолиз – это серия реакций, в результате которых глюкоза распадается на 2 молекулы пирувата (аэробный гликолиз) или две молекулы лактата (анаэробный гликолиз).
Все реакции гликолиза (10-11 реакций) протекают в цитозоле и характерны для всех органов и тканей.
Главным путем распада глюкозы, ведущим к освобождению энергии, является дихотомический путь. В реакциях этого пути получить из глюкозы энергию можно двумя путями:
1) Путем анаэробного распада глюкозы до молочной кислоты. Этот процесс называется гликолизом. Многоступенчатые реакции можно выразить суммарным уравнением: глюкоза → 2лактат + 134 кДж. Часть этой энергии расходуется на образование 2 молекул АТФ, остальная рассеивается в виде тепла.
2) Путем аэробного распада глюкозы до конечных продуктов – СО2 и Н2О. Глюкоза + 6О2 → 6СО2 + 6Н2О + 2850 кДж. При этом 60% образующейся энергии запасается в виде АТФ. Аэробный путь экономически выгоднее, при равных количествах используемой глюкозы, этот путь дает почти в 20 раз больше АТФ. Аэробный распад глюкозы осуществляется почти всеми тканями нашего организма, исключение – эритроциты, их жизнедеятельность поддерживается путем гликолиза.
Цепь реакций гликолиза можно расчленить на два звена. В первом звене осуществляется распад глюкозы на 2 молекулы по 3 углеродных атома каждая (подготовительная стадия). В этом отрезке цепи еще нет поставки энергии, имеется отрицательный энергетический баланс в результате расходования энергии АТФ на реакции фосфорилирования. Во втором звене гликолиза (гликолитическая оксидоредукция) осуществляется окисление 3-х углеродных молекул в пируват, который будет восстанавливаться в лактат.
Реакции гликолиза.
1-я реакция – образование глюкозо-6-фосфата.
2-я реакция – изомеризация глюкозо-6-фосфата с образованием фруктозо-6-фосфата. Эта реакция обратима и катализируется изомеразой.
3-я реакция – фосфорилирование фруктозо-6-фосфата с образованием фруктозо-1,6-бисфосфата. В этой реакции происходит значительное падение свободной энергии, поэтому она необратима.
Фосфофруктокиназа – Аллостерический фермент, имеет сложную четвертичную структуру. Его аллостерическими активаторами являются АМФ, АДФ, фруктозо-6-фосфат. Угнетают фермент повышенные концентрации АТФ и цитрат. АТФ вначале используется как субстрат этой реакции, а затем, связываясь с аллостерическим центром фермента, прекращает реакцию. В последние годы было установлено, что важным аллостерическим регулятором фосфофруктокиназы является фруктозо-1,6-дифосфат.
4-я реакция – распад фруктозо-1,6-дифосфата на 2 триозы:
Определение активности альдолазы используют в энзимной диагностике при заболеваниях, связанных с повреждением или гибелью клеток, так, при остром гепатите активность этого фермента может увеличиваться в 5-20 раз, при инфаркте миокарда – в 3-10 раз. Образующийся 3-ФГА расходуется в дальнейших реакциях гликолиза, поэтому равновесие реакции смещается в сторону распада фруктозо-1,6-дифосфата. Превращение фосфодиоксиацетона в 3-ФГА осуществляет фермент триозофосфатизомераза.
5-я реакция –образование 1,3-дифосфоглицерата. В этой реакции при окислении 3-ФГА водород альдегидной группы будет переноситься на НАД + . Энергии выделяется достаточно и образующийся 1,3-дифосфоглицерат заключает в себя макроэргическую вязь. Реакция катализируется дегидрогеназой 3-ФГА по суммарному уравнению:
3-ФГА + НАД + + Фн 1,3-дифосфоглицерат + НАДН + Н + .
Фермент состоит из 4-х одинаковых субъединиц, коферментом его является НАД + . Реакция обратима. С этого момента количество последующих продуктов нужно удвоить, так как в предыдущей реакции образовалось 2 молекулы триозы.
6-я реакция – образование АТФ в результате субстратного фосфорилирования:
1,3-дифосфоглицерат + АДФ АТФ + 3-фосфоглицерат.
Эта реакция сопровождается выделением значительного количества свободной энергии, поэтому равновесие ее сдвинуто вправо. При избытке 3-фосфоглицерата реакция может быть обратимой. В данной реакции происходит фосфорилирование АДФ за счет энергии макроэргического субстрата – 1,3-дифосфоглицериновой кислоты.
7-я реакция – изомеризация 3-фосфоглицерата в 2-фосфоглицерат.
9-я реакция – образование АТФ в результате субстратного фосфорилирования:
пируваткиназа Мg 2+
фосфоенолпируват + АДФ пируват + АТФ.
Это вторая реакция субстратного фосфорилирования в гликолизе; здесь фосфоенолпируват используется для образования АТФ. Реакция необратима, так как протекает в большим падением свободной энергии.
10-я реакция – образование лактата. Эта реакция катализируется ЛДГ и обратима.
Итак, гликолиз завершается образованием лактата. В мышцах молочная кислота не используется – она поступает с током крови в печень, где вновь превращается в пируват. Полезный энергетический выход гликолиза – 2 молекулы АТФ.
В дрожжевых клетках и микроорганизмах, подобных им, анаэробный распад углеводов протекает сходно с гликолизом за исключением конечных стадий. Первые стадии до образования пирувата идут одинаково. При спиртовом брожении пируват подвергается декарбоксилированию ферментом пируватдекарбоксилазой, имеющей кофермент ТПФ и требующей ионов Мд 2+ . При этом образуется уксусный альдегид, который восстанавливается в этанол алкогольдегидрогеназой с использованием НАДН2, образовавшегося при окислении 3- ФГА в 1,3 биФГК.
Глюкоза может окисляться по дихотомическому пути и в аэробных условиях. Цепь реакций аэробного распада можно расчленить на несколько основных звеньев:
а) дихотомический распад глюкозы до стадии пирувата, полностью совпадающий с реакциями гликолиза;
б) окислительное декарбоксилирование пирувата, с образованием ацетил-КоА;
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.


Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Читайте также:

