Батарейки их настоящее и будущее реферат
Обновлено: 04.07.2024
В современной жизни химические источники тока окружают нас повсюду: это батарейки в фонариках, аккумуляторы в мобильных телефонах, водородные топливные элементы, которые уже используются в некоторых автомобилях. Бурное развитие электрохимических технологий может привести к тому, что уже в ближайшее время вместо машин на бензиновых двигателях нас будут окружать только электромобили, телефоны перестанут быстро разряжаться, а в каждом доме будет свой собственный электрогенератор на топливных элементах. Повышению эффективности электрохимических накопителей и генераторов электроэнергии посвящена одна из совместных программ Уральского федерального университета с Институтом высокотемпературной электрохимии УрО РАН, в партнерстве с которыми мы публикуем эту статью.
На сегодняшний день существует множество разных типов батареек, среди которых все сложнее ориентироваться. Далеко не каждому очевидно, чем аккумулятор отличается от суперконденсатора и почему водородный топливный элемент можно использовать, не опасаясь нанести вред окружающей среде. В этой статье мы расскажем о том, как для получения электроэнергии используются химические реакции, в чем разница между основными типами современных химических источников тока и какие перспективы открываются перед электрохимической энергетикой.
Химия как источник электричества
Сначала разберемся, почему химическую энергию вообще можно использовать для получения электричества. Все дело в том, что при окислительно-восстановительных реакциях происходит перенос электронов между двумя разными ионами. Если две половины химической реакции разнести в пространстве, чтобы окисление и восстановление проходили отдельно друг от друга, то можно сделать так, чтобы электрон, который отрывается от одного иона, не сразу попадал на второй, а сначала прошел по заранее заданному для него пути. Такую реакцию можно использовать как источник электрического тока.
Помимо материалов анода и катода, важной составляющей химического источника тока является электролит, внутри которого движутся ионы и на границе которого с электродами протекают все электрохимические реакции. При этом электролит не обязательно должен быть жидким — это может быть и полимерный, и керамический материал.
Основным недостатком гальванического элемента является ограниченное время его работы. Как только реакция пройдет до конца (то есть будет полностью израсходован весь постепенно растворяющийся анод), такой элемент просто перестанет работать.
Возможность перезарядки
Первым шагом к расширению возможностей химических источников тока стало создание аккумулятора — источника тока, который можно перезаряжать и поэтому использовать многократно. Для этого ученые просто предложили использовать обратимые химические реакции. Полностью разрядив аккумулятор в первый раз, с помощью внешнего источника тока прошедшую в нем реакцию можно запустить в обратном направлении. Это восстановит исходное состояние, так что после перезарядки батарею можно будет использовать заново.
На сегодня создано много различных типов аккумуляторов, которые отличаются типом происходящей в них химической реакции. Наиболее распространенными типами аккумуляторов являются свинцово-кислотные (или просто свинцовые) аккумуляторы, в основе которых лежит реакция окисления-восстановления свинца. Такие устройства обладают довольно длительным сроком службы, а их энергоемкость составляет до 60 ватт-часов на килограмм. Еще более популярными в последнее время являются литий-ионные аккумуляторы, основанные на реакции окисления-восстановления лития. Энергоемкость современных литий-ионных аккумуляторов сейчас превышает 250 ватт-часов на килограмм.
Основными проблемами литий-ионных аккумуляторов являются их небольшая эффективность при отрицательных температурах, быстрое старение и повышенная взрывоопасность. А из-за того, что металлический литий очень активно реагирует с водой с образованием газообразного водорода и при горении аккумулятора выделяется кислород, самовозгорание литий-ионного аккумулятора очень тяжело поддается традиционным способам пожаротушения. Для того чтобы повысить безопасность такого аккумулятора и ускорить время его зарядки, ученые предлагают модифицировать материал катода, воспрепятствовав образованию дендритных литиевых структур, а в электролит добавить вещества, которые блокируют образование взрывоопасных структур, и компоненты, подавляющие возгорание на ранних стадиях.
Твердый электролит
В качестве другого менее очевидного способа повышения эффективности и безопасности батарей, химики предложили не ограничиваться в химических источниках тока жидкими электролитами, а создать полностью твердотельный источник тока. В таких устройствах вообще нет жидких компонентов, а есть слоистая структура из твердого анода, твердого катода и твердого же электролита между ними. Электролит при этом одновременно выполняет и функцию мембраны. Носителями заряда в твердом электролите могут быть различные ионы — в зависимости от его состава и тех реакций, которые проходят на аноде и катоде. Но всегда ими являются достаточно маленькие ионы, которые могут относительно свободно перемещаться по кристаллу, например протоны H+, ионы лития Li+ или ионы кислорода O2-.
Водородные топливные элементы
Возможность перезарядки и специальные меры безопасности делают аккумуляторы значительно более перспективными источниками тока, чем обычные батарейки, но все равно каждый аккумулятор содержит внутри себя ограниченное количество реагентов, а значит, и ограниченный запас энергии, и каждый раз аккумулятор необходимо заново заряжать для возобновления его работоспособности.
Наиболее подходящее вещество такого типа — газообразный водород. Его окисление кислородом воздуха с образованием воды (по реакции 2H2 + O2 → 2H2O) является простой окислительно-восстановительной реакцией, а транспорт электронов между ионами тоже можно использовать в качестве источника тока. Протекающая при этом реакция является своего рода обратной реакцией к реакции электролиза воды (при котором под действием электрического тока вода разлагается на кислород и водород), и впервые такая схема была предложена еще в середине XIX века.
Но несмотря на то, что схема выглядит довольно простой, создать основанное на этом принципе эффективно работающее устройство — совсем не тривиальная задача. Для этого надо развести в пространстве потоки кислорода и водорода, обеспечить транспорт нужных ионов через электролит и снизить возможные потери энергии на всех этапах работы.
Схема работающего водородного топливного элемента очень похожа на схему химического источника тока, но содержит в себе дополнительные каналы для подачи топлива и окислителя и отвода продуктов реакции и избытка поданных газов. Электродами в таком элементе являются пористые проводящие катализаторы. К аноду подается газообразное топливо (водород), а к катоду — окислитель (кислород из воздуха), и на границе каждого из электродов с электролитом проходит своя полуреакция (окисление водорода и восстановление кислорода соответственно). При этом, в зависимости от типа топливного элемента и типа электролита, само образование воды может протекать или в анодном, или в катодном пространстве.
Если электролит является протонпроводящей полимерной или керамической мембраной, раствором кислоты или щелочи, то носителем заряда в электролите являются ионы водорода. В таком случае на аноде молекулярный водород окисляется до ионов водорода, которые проходят через электролит и там реагируют с кислородом. Если же носителем заряда является ион кислорода O2–, как в случае твердооксидного электролита, то на катоде происходит восстановление кислорода до иона, этот ион проходит через электролит и окисляет на аноде водород с образованием воды и свободных электронов.
Кроме реакции окисления водорода для топливных элементов предложено использовать и другие типы реакций. Например, вместо водорода восстановительным топливом может быть метанол, который кислородом окисляется до углекислого газа и воды.
Эффективность топливных элементов
Несмотря на все преимущества водородных топливных элементов (такие как экологичность, практически неограниченный КПД, компактность размеров и высокая энергоемкость), они обладают и рядом недостатков. К ним относятся, в первую очередь, постепенное старение компонентов и сложности при хранении водорода. Именно над тем, как устранить эти недостатки, и работают сегодня ученые.
Повысить эффективность топливных элементов в настоящее время предлагается за счет изменения состава электролита, свойств электрода-катализатора, и геометрии системы (которая обеспечивает подачу топливных газов в нужную точку и снижает побочные эффекты). Для решения проблемы хранения газообразного водорода используют материалы, содержащие платину, для насыщения которых предлагают использовать , например, графеновые мембраны.
В результате удается добиться повышения стабильности работы топливного элемента и времени жизни его отдельных компонентов. Сейчас коэффициент преобразования химической энергии в электрическую в таких элементах достигает 80 процентов, а при определенных условиях может быть и еще выше.
Огромные перспективы водородной энергетики связывают с возможностью объединения топливных элементов в целые батареи, превращая их в электрогенераторы с большой мощностью. Уже сейчас электрогенераторы, работающие на водородных топливных элементах, имеют мощность до нескольких сотен киловатт и используются как источники питания транспортных средств.
Альтернативные электрохимические накопители
Несмотря на то, что сейчас плотность энергии суперконденсаторов пока в несколько раз меньше плотности энергии аккумуляторов, их используют в бытовой электронике и для двигателей различных транспортных средств, в том числе и в самых современных разработках .
Таким образом, на сегодня существует большое количество электрохимических устройств, каждое из которых перспективно для своих конкретных приложений. Для повышения эффективности работы этих устройств ученым необходимо решить ряд задач как фундаментального, так и технологического характера. Большинством этих задач в рамках одного из прорывных проектов занимаются в Уральском федеральном университете, поэтому о ближайших планах и перспективах по разработке современных топливных элементов мы попросили рассказать директора Института высокотемпературной электрохимии УрО РАН, профессора кафедры технологии электрохимических производств химико-технологического института Уральского федерального университета Максима Ананьева.
N + 1: Ожидается ли в ближайшем будущем какая-то альтернатива наиболее популярным сейчас литий-ионным аккумуляторам?
Максим Ананьев: Современные усилия разработчиков аккумуляторов направлены на замену типа носителя заряда в электролите с лития на натрий, калий, алюминий. В результате замены лития можно будет снизить стоимость аккумулятора, правда при этом пропорционально возрастут массо-габаритные характеристики. Иными словами, при одинаковых электрических характеристиках натрий-ионный аккумулятор будет больше и тяжелее по сравнению с литий-ионным.
Кроме того, одним из перспективных развивающихся направлений совершенствования аккумуляторов является создание гибридных химических источников энергии, основанных на совмещении металл-ионных аккумуляторов с воздушным электродом, как в топливных элементах. В целом, направление создания гибридных систем, как уже было показано на примере суперконденсаторов, по-видимому, в ближайшей перспективе позволит увидеть на рынке химические источники энергии, обладающие высокими потребительскими характеристиками.
Группа ученых стратегической академической единицы (САЕ) Школа естественных наук и математики УрФУ, в которую входит Максим Ананьев, занимается проектированием и разработкой новых материалов и технологий, среди которых — топливные элементы, электролитические ячейки, металлграфеновые аккумуляторы, электрохимические системы аккумулирования электроэнергии и суперконденсаторы.
Исследования и научная работа ведутся в постоянном взаимодействии с Институтом высокотемпературной электрохимии УрО РАН и при поддержке партнеров.
Какие топливные элементы разрабатываются сейчас и имеют наибольший потенциал?
Одними из наиболее перспективных типов топливных элементов являются протонно-керамические элементы. Они обладают преимуществами перед полимерными топливными элементами с протонно-обменной мембраной и твердооксидными элементами, так как могут работать при прямой подаче углеводородного топлива. Это существенно упрощает конструкцию энергоустановки на основе протонно-керамических топливных элементов и систему управления, а следовательно, увеличивает надежность работы. Правда, такой тип топливных элементов на данный момент является исторически менее проработанным, но современные научные исследования позволяют надеяться на высокий потенциал данной технологии в будущем.
Какими проблемами, связанными с топливными элементами, занимаются сейчас в Уральском федеральном университете?
Сейчас ученые УрФУ совместно с Институтом высокотемпературной электрохимии (ИВТЭ) Уральского отделения Российской академии наук работают над созданием высокоэффективных электрохимических устройств и автономных генераторов электроэнергии для применений в распределенной энергетике . Создание энергоустановок для распределенной энергетики изначально подразумевает разработку гибридных систем на основе генератора электроэнергии и накопителя, в качестве которых выступают аккумуляторы. При этом топливный элемент работает постоянно, обеспечивая нагрузку в пиковые часы, а в холостом режиме заряжает аккумулятор, который может сам выступать резервом как в случае высокого энергопотребления, так и в случае внештатных ситуаций.
В рамках совместной лаборатории УрФУ и ИВТЭ ведутся разработки электрохимических устройств на основе протонпроводящей керамической мембраны. Это позволит в ближайшем будущем снизить рабочие температуры для твердо-оксидных топливных элементов с 900 до 500 градусов Цельсия и отказаться от предварительного риформинга углеводородного топлива, создав, таким образом, экономически эффективные электрохимические генераторы, способные работать в условиях развитой в России инфраструктуры газоснабжения.
Примерно в 1800 году итальянский физик Алессандро Вольта изобрёл батарейку, которой мы и по сей день продолжаем пользоваться. Кстати, кто не знает что такое батарейка, так это источник питания, который вырабатывает электричество под действием химического процесса. То есть батарейка это гальванический элемент, работающий на химической реакции. Так можно объяснить и детям.
Как работает батарейка
Катоды выполняют функцию восстановителя, т.е. принимают электроны от прибывшего анода. Электролит это среда, в которой перемещаются ионы, которые образуются в процессе химической реакции. В процессе работы батарейки постепенно образовываются новые вещества, а электроды постепенно разрушаются — батарейка садится.
Вот и вся работа батарейки, кстати, все процессы, проходящие в гальваническом элементе, необратимы, то есть заряжать батарейки нельзя. Кратко говоря о работе батарейки: анод — нагрузка — катод — электролит.
Электролит изначально изготовляли в жидком виде, но это неудобно, так как при переворачивании батарейки она просто не работала. Из-за этого электролит стали загущать, превращать его в сухой вид.
Как устроена батарейка
Внутри металлического корпуса щелочной ячейки находятся три основных химических вещества: цинк, диоксид марганца и гидроксид калия.

Щелочная батарейка. /Роджер Кларк
Когда элемент подключен к цепи — например, к лампочке, — цинк внутри реагирует с диоксидом марганца и теряет электроны.
Электроны собираются с помощью металлического стержня внутри ячейки, что позволяет им течь из нижней части ячейки (отрицательный), через провода к лампе (чтобы она загорелась), а затем обратно в верхнюю часть ячейки. (положительный).
Эта реакция производит около 1,5 вольт электроэнергии. Поскольку не так много устройств могут работать при напряжении 1,5 В, очень часто два или четыре элемента используются вместе для увеличения мощности. Таким образом, четыре ячейки, соединенные вместе (конец в конец), дадут шесть вольт.

Но помните, что большинство элементов и батарей можно утилизировать, поэтому убедитесь, что вы тщательно от них избавились.
Обратная реакция
Все типы батареек и элементов имеют сходный тип химической реакции, происходящей для выработки электроэнергии.
Но в некоторых типах элементов или батарей химические вещества различны, и реакция может быть обратной. Таким образом, элементы могут быть перезаряжены — так же, как литий-ионные аккумуляторы в автомобилях или смартфонах.

Раньше было гораздо дешевле производить неперезаряжаемые элементы, такие как щелочные элементы, поэтому они использовались очень широко.
Но теперь, когда люди осознали, насколько вредно для окружающей среды просто выбрасывать неперезаряжаемые элементы, а поскольку перезаряжаемые элементы становятся дешевле, мы, вероятно, будем использовать неперезаряжаемые элементы все меньше и меньше в будущем.
Типы батареек
- Солевые (угольно-цинковые, марганцево-цинковые) батарейки.
Что это такое солевые батарейки
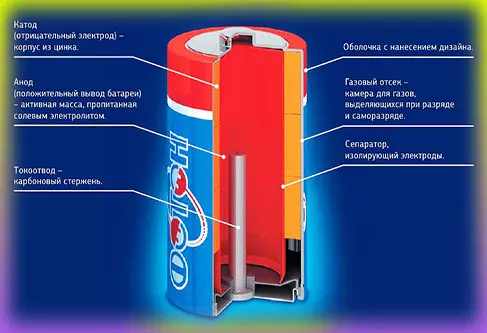
Солевая батарейка изготавливается из пассивного угля и двуокиси марганца, электролит из хлорида аммония и катод из цинка. В перерывах работы элементы питания могут восстанавливаться, т.е. выравнивать локальные неоднородности в композите электролита, вызванных разрядом. Такой процесс немного продлевает срок службы батарейки.
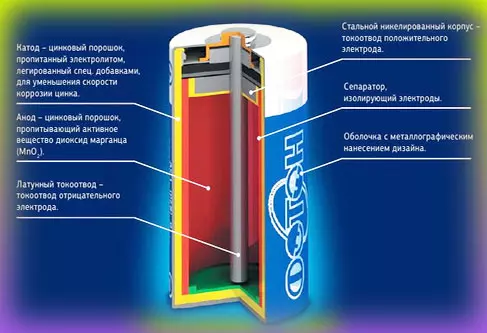
Алкалиновые (щелочные) батарейки что это такое
В отличие от солевых батарей у алкалиновой батарейки химический элемент электролита — щелочной. Щёлочные батарейки (алкалин) имеют продолжительный срок хранения, а в процессе эксплуатации напряжение на электродах меняется гораздо меньше, чем у элементов с солевым раствором.
Литиевые батарейки — что это такое?
Самые современные. В отличие от щелочных и солевых батареек, в состав катода входит литий (Li – наивысший отрицательный потенциал), в состав анода — различные материалы. Электролит — органический электролит. В связи с такими элементами литиевые батарейки получили большой срок хранения, большую плотность энергии и различную рабочую температуру.
Особенностью данной работы является то, что эта проблема встречается повсеместно и связана с нашей жизнью. Моя работа призвана улучшить экологию и призвана научить людей заботиться о сохранении окружающей среды.
Батарейки: вред и польза
Одинцев Андрей Владимирович
Россия, Тюменская область, город Тюмень, МАОУ СОШ № 92, 5 класс
План исследований
Своей работой хочу обратить внимание на то, что с батарейками мы сталкиваемся ежедневно: очень удобно и комфортно использовать их в фотоаппаратах, электронных часах, в пульте дистанционного управления телевизором, в игрушках, в машинках, в фонариках. Куда же их все выбрасывают после использования? Этот вопрос меня заинтересовал еще и тем, что обычные отходы мы выносим в мусорный бак, мусор оттуда вывозится на полигон и что же с ними с батарейками происходит? Они остаются лежать и тем самым разлагаются в земле. Но ведь внутри каждой из них есть вредные элементы, что происходит с ними? Они разлагаются, попадая в грунтовые воды и в атмосферу. Так с каждым годом всё больше и больше в нашей жизни прибавляется экологических проблем!
В связи с тем, что проблема утилизации батареек с каждым годом становится все острее, я решил в своей работе исследовать, знают ли окружающие меня люди о том, как обезопасить себя и свою землю от разлагающихся батареек.
Актуальность данной работы обусловлена негативным влиянием химических веществ, содержащихся в батарейке, на окружающую среду и здоровье человека. Также он заключается в том, что в процессе проведения исследования повышается экологическая культура людей.
изучить историю создания батарейки, классификацию, состав
определить влияние использованных батареек на окружающую среду, здоровье человека;
выяснить способы утилизации использованных батареек;
информировать людей о вреде использованных батареек;
Провести опыт по созданию батарейки, понять, что невозможно получать столько же пользы от батарейки (из лимона), сколько от обычных батареек, произведенных на заводе.
Изучить влияние батареек на окружающую среду и здоровье людей.
Выяснить влияние на экологию при неправильной утилизации батареек.
Изучить осведомленность людей о влиянии использованных батареек на здоровье человека.
Повысить уровень экологической культуры людей.
Объект исследования: батарейки
Предмет исследования: влияние неправильной утилизации батареек, применяемых в быту.
Методы исследования: изучение литературы , сбор и анализ информации из доступных интернет ресурсов, анкетирование, проведение опроса и обобщение данных, анализ результатов исследования, выводы.
Батарейки: вред и польза
Одинцев Андрей Владимирович

В батарейке присутствуют два электрода - катод и анод – они изготавливаются из двух разных металлов. Пространство между ними заполнено третьим материалом, называемым электролитом. В электролите протекает реакция, в ходе которой выделяется энергия в виде электрического тока. Характерные особенности батарейки зависят от материалов для электрода и электролита.
Батарейка нашего времени и её строение
Батарейки различаются как внешне, так и внутренне. Существуют такие разновидности батареек как:
Опыт по созданию своей батарейки
Я провёл опыт по созданию одной из таких батареек. В моём случае – я сделал батарейку из лимона. Для этого я взял лимон, оцинкованный гвоздь, монетку покрытую медью, два провода и диод зелёного цвета. Я вставил монетку и гвоздь в лимон. Сок лимона является природным электролитом, это значит, что в таком соке содержатся кислота и растворенные в ней соли. Следовательно лимон можно реально применить в качестве составной части химического источника тока, корпус ячейки которого уже готов благодаря самой природе.
Итак, что же происходит, когда мы втыкаем в такой плод с одной его стороны оцинкованный гвоздь, а с другой — монетку, покрытую медью, и замыкаем цепь? Гвоздь станет отрицательным электродом – анодом. Медь служит здесь катодом — положительным электродом. Медь является сильным окислителем, она притягивает к себе такое же количество электронов, сколько отдает цинк. То есть на катоде протекает химическая реакция восстановления. Так в цепи инициируется протекание электрического тока.

В итоге мы получаем то, что диод засветился, но на очень короткий промежуток времени, так как один лимон не способен выделять столько энергии. Простейшая схема по сбору батарейки сработала!
Влияние батареек на человека и окружающую cреду
Итак, знали ли вы, что батарейки могут нанести огромный ущерб природе, а также навредить человеку? Ответ – могут. И вот почему: изучив дополнительную литературу и ресурсы интернета, я узнал, что батарейки таят в себе колоссальную угрозу. Экологи подсчитали, что одна пальчиковая батарейка способна загрязнить около 20 квадратных метров земли и около 400 литров воды.
Но, всё же, как этот маленький цилиндрик может навредить нам – людям? Вред батареек заключается в следующем: элементы питания включают в себя опасные вещества, магний, ртуть, олово, свинец, никель, цинк, кадмий, которые способны аккумулироваться в организме вызывая болезни. Отработанные источники питания при сжигании выделяю специфические газы диоксины, отравляющие людей.
Но вместе с тем, батарейки приносят и колоссальную пользу. Например: батарейки нужны нам в электроприборах постоянно. Много пользы они приносят для комфортной жизни! Мы используем их в пультах от телевизора, настенных часах, фотоаппаратах и во многих других электронных приборах.
Что такое переработка батареек и зачем она нужна
Итак, я уже рассказал какую опасность несут батарейки для природы. Я думаю, что не многие задумываются над этой проблемой, потому что никому в голову не придёт, что батарейка - это источник большой опасности как для человека, так и для окружающей среды. Актуальность данной работы обусловлена влиянием химических веществ, содержащихся в батарейке, на окружающую среду и здоровье человека. Данная работа привлекает внимание к проблеме утилизации использованных батареек.
В России существует два завода по переработке использованных батареек – один в городе Челябинске, второй в городе Новосибирске. На заводе в г. Новосибирске сотрудники отбирают щелочные и солевые батарейки от ртутных, серебряных и литиевых, которые там не перерабатываются. Затем с батареек срезается металлическая оболочка. Металлическая часть отделяется от остальных элементов при помощи магнита. Остальные составляющие батарейки: порошок, состоящий из диоксида марганца и графита, бумага и пластик также разделяются на составляющие. Порошок потом используют при создании тротуарной плитки для придания ей темного цвета. При этом он обеззараживается и не наносит вреда окружающей среде и здоровью человека.
Опрос
Мне стало интересно, кто то из моих одноклассников не просто выбрасывает батарейки, а относит их в специальные пункты сбора использованных батареек и я провёл среди своих знакомых опрос – сколько батареек в год они выбрасывают и куда.
Результаты опроса представлены в таблице:
Таким образом, получается, что каждая семья выбрасывает в год примерно 10 батареек. И только два человека относят в пункты сбора использованных батареек. Я, конечно, порекомендовал относить батарейки в специальные пункты сбора, чтобы помочь сберечь окружающую среду.
Таким образом, если 8 человек начнут сдавать батарейки в пункты сбора, то можно спасти 1600 квадратных метров земли и 32000 литров воды. Поэтому всё, что мы можем сделать, защищая окружающую среду, - это проследить, чтобы использованные элементы питания не попадали в баки с обычным бытовым мусором, а оттуда на свалку.
Батарейки: вред и польза
Одинцев Андрей Владимирович
Россия, Тюменская область, город Тюмень, МАОУ СОШ № 92, 5 класс
Заключение
Таким образом, человечество не может отказаться от использования батареек, так как они нужны нам в электроприборах постоянно. Много пользы они приносят для комфортной жизни! Также изучив теоретический материал о влиянии отработанных батареек на окружающую среду, я сделал следующие выводы: выбрасываемые батарейки в мусорные баки, опасны для человека и окружающей среды. Отработанные батарейки необходимо сдавать в пункты приёма для утилизации на специальных заводах. Только специализированная обработка сделает использованные батарейки полезными и безопасными для дальнейшего применения уже в других областях (путем использования их составных частей, которые безопасны для человека и окружающей среды).

В повседневной суете люди часто забывают об этой простой истине. Но настал момент, когда всему обществу необходимо включиться в процесс сокращения уровня образования бытовых отходов. Необходимо осознать, что каждый гражданин является производителем отходов и оказывает негативное воздействие на состояние окружающей среды.
Мы должны заботиться о чистоте нашей планеты, чтобы будущие поколения жили в благоприятных условиях.
Актуальность проекта: Вопросы сбора, переработки использованных батареек чрезвычайно актуальны в настоящее время. Утилизация этих отходов является одной из самых сложных проблем переработки вторичного сырья. Практически во всех батарейках содержатся токсичные вещества в виде различных металлов и химикатов, которые при разрушении корпусов батареек попадают в природную среду. Наша жизнь во многом зависит от состояния окружающей среды.
И сегодня это понимает каждый житель планеты Земля. С каждым годом мы все сильнее ощущаем существующие экологические проблемы. Мы стараемся выбрать качественные, экологически чистые продукты в магазине, гуляем в местах, где чистый воздух, строим дома в экологически чистых районах. И при этом, многие из нас не задумываются, что состояние окружающей среды напрямую связано с нашим поведением в быту, в природе.
Одной из проблем современности в области экологии является проблема утилизации бытовых приборов, которые сегодня стали таким привычным предметом нашего ежедневного пользования.
Гипотеза: Я предположила, что большинство использованных батареек попадая на мусорные свалки, наносят большой вред окружающей среде. Они являются источником вредных химических, биологических и биохимических препаратов. В бытовом пользовании вреда человеку не наносят, но, попадая в окружающую среду, могут при нарушении герметичности корпуса нанести вред природе.
Цель работы: изучить объѐмы потребления в быту батареек и рассмотреть экологические аспекты вредного воздействия неправильно утилизированных батареек, внести посильный вклад в защиту окружающей среды.
Узнать о вреде элементов питания.
Провести опрос учащихся по выявлению знаний о вреде батареек на здоровье человека.
Выяснить, как обстоят дела с утилизацией элементов питания в стране, и в Волгограде, в частности.
Провести в школе Акцию по сбору элементов питания для последующей утилизации.
Разработать рекомендации для одноклассников.
Методы исследования:
1. Изучить теоретические данные о строении, разнообразии, составе батареек, выяснить какой вред могут нанести химические элементы, входящие в состав батареек, окружающей среде.
2. Обратиться к Интернету, с целью найти пункты приема элементов питания в Волгограде.
3. Провести социальный опрос, оформить результаты
4. Изготовить буклеты и провести разъяснительную работу среди учащихся школы.
Ожидаемый результат:
- Информированность всех участников проекта о вредном воздействии неправильной утилизации батареек на окружающую среду и здоровье населения - Понимать, что состояние окружающей среды зависит от каждого из нас - Приобретение навыка – не выбрасывать батарейки вместе с остальным мусором. Необходимо использовать специальные ёмкости или сдавать элементы питания в специальные пункты сбора. Если пунктов сбора рядом с домом нет - собирать батарейки в пластиковые бутылки.
Основная часть
1. Батарейка
1.1 История создания батарейки
Первую батарейку изобрёл итальянский ученый граф Алессандро Вольта в 1799 году. Он предложил назвать химический элемент, который создает электрический ток, в честь другого итальянского ученого Луиджи Гальвани – гальванический элемент.
1.2 Разновидности батареек
Мы живем в 21 веке, с батарейками мы сталкиваемся ежедневно - в пульте дистанционного управления телевизором, в электронных часах, в детских игрушках и карманных фонариках. Постепенно одноразовые источники питания вытесняются перезаряжаемыми аккумуляторами, но списывать со счетов их пока рано.
Батарейка - это элемент питания, автономный источник электричества для разнообразных устройств.
В электронном справочнике в Интернете мы нашли информацию, что в зависимости от того, какое химическое вещество используется, батарейки подразделяются на группы.
1. Солевые батарейки
2. Щелочные батарейки
3. Литиевые батарейки
1.3. Анализ состава батарейки
Когда вещества, находящиеся внутри батарейки истончаются, батарейка разряжается и становится непригодной. Мы выбрасываем ее.
После выбрасывания у батарейки металлическое покрытие разрушается, и тяжелые металлы: цинк, свинец, кадмий, никель, ртуть попадают в почву и грунтовые воды, нанося вред здоровью человека в настоящем и накапливая опасность для будущего поколения Земли.
Цинк – попадая в организм, приводит к расстройству пищеварения, раздражению слизистых оболочек.
Никель – поступление в организм в природных условиях происходит с продуктами питания и питьевой водой. Кроме того, никель поступает в организм с атмосферным воздухом, через кожу. Приводит к возникновению заболеваний носоглотки, легких, появлению экзем и аллергическим реакциям.
Свинец накапливается в основном в почках. Вызывает также заболевания мозга, вызывает нервные расстройства.
Кадмий вредит лёгким. Накапливается в печени, почках, костных тканях.
Ртуть поражает нервную систему. При воздействии ртути возможны острые и хронические отравления. При вдыхании ртутные пары поглощаются и накапливаются в мозге и почках. Вызывает нервные расстройства, ухудшение зрения, слуха, нарушения двигательного аппарата, заболевания дыхательной системы. Независимо от путей поступления в организм ртуть накапливается в почках.
Вывод: Накопление отходов на свалках приводит к тому, что тяжелые металлы попадают в грунтовые воды. Из грунтовых вод эти металлы могут попасть в реки и озера или в артезианские воды, используемые для питьевого водоснабжения.
Один из самых опасных металлов, ртуть, может попасть в организм человека как непосредственно из воды, так и при употреблении в пищу продуктов, приготовленных из отравленных растений или животных, поскольку этот металл имеет свойство накапливаться в тканях живых организмов.
Анализируя всю собранную информацию приходишь к пониманию того, что губительный эффект загрязнения окружающей среды отходами, содержащими тяжелые металлы может стать очевидным для человека через несколько лет, поскольку тяжелые металлы начинают свое воздействие лишь достигая определенной концентрации. Необратимые процессы в организме начинаются незаметно.
Читайте также:

