Атомно кристаллическая структура металлов реферат
Обновлено: 05.07.2024
Металлическое состояние возникает в комплексе атомов, когда при их сближении внешние электроны теряют связь с отдельными атомами, становятся общими, т. е. коллективизируются и свободно перемещаются между положительно заряженными и периодически расположенными ионами. В твердом металле полиморфные превращения происходят в результате зарождения и роста кристаллов аналогично кристаллизации из жидкого… Читать ещё >
Атомно-кристаллическое строение металлов ( реферат , курсовая , диплом , контрольная )
Министерство образования и науки Украины Донбасский государственный технический университет Кафедра ОМД
ЛЕКЦИЯ
по дисциплине Металловедение
на тему
Ст.преп. Горецкий Ю.В.
1. Строение металлов в твердом состоянии
Все металлы и металлические сплавы — тела кристаллические, атомы (ионы) расположены в металле закономерно в отличие от аморфных тел, в которых атомы расположены хаотично.
Металлическое состояние возникает в комплексе атомов, когда при их сближении внешние электроны теряют связь с отдельными атомами, становятся общими, т. е. коллективизируются и свободно перемещаются между положительно заряженными и периодически расположенными ионами.
Устойчивость металла определяется электрическим притяжением между положительно заряженными ионами и обобщенными электронами (такое взаимодействие получило название металлической связи).
Сила связи в металлах определяется силами отталкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстоянии друг от друга, чтобы энергия взаимодействия была минимальной (рис. 1)
Рисунок 1. Энергетические условия взаимодействия атомов в кристаллической решетке вещества Величина, а соответствует расстояние между атомами в кристаллической решетке, а а0 соответствует равновесному расстоянию между атомами. В связи с этим в металле атомы располагаются закономерно, образуя правильную кристаллическую решетку, что соответствует минимальной энергии взаимодействия атомов.
Металлические состояния характеризуются высокой энергией связи между атомами. Мерой ее служит теплота сублимации (сумма энергии необходимой для перехода твердого металла к парообразному состоянию, для металла — от 20 до 200 ккал/(г· атом)).
2. Атомно-кристаллическое строение металлов
Под атомно-кристаллической структурой понимают взаимное расположение атомов, существующее в кристалле. Атомы в кристалле расположены в определенном порядке, который периодически повторяется в трех измерениях.
Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узле которой располагаются атомы (ионы), образующие металл.
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, получил название элементарной кристаллической ячейки (решетки).
Для характеристики элементарной ячейки задают шесть величин: три ребра ячейки a, b, c и три угла между ними б, в, г. Эти величины называют параметрами кристаллической решетки.
Кристаллические решетки бывают простыми (атомы только в вершинах решетки) и сложными.
Металлы образуют одну из следующих высокосимметричных сложных решеток с плотной упаковкой атомов: кубическую объемноцентрированную (ОЦК), кубическую гранецентрированную (ГЦК) и гексагональную (ГПУ) (рис. 2).
ОЦК: Rb, K, Na, Li, Tiв, Tlв, Zrв, Ta, W, V, Feб, Cr, Nb, Ba, и др.
ГЦК: Cu, Al, Pt, Pb, Ni, Ag, Au, Pd, Rh, Ir, Feг, Coб, Caб, Ce, Srб, Th, Sc и др.
Рисунок 2. Кристаллические решетки металлов и схемы упаковки атомов Расстояние между ближайшими параллельными атомными плоскостями, образующими элементарную ячейку, называют периодом решетки, измеряется в нанометрах (1нм = 10 -9 см = Е= 10 -8 см).
Периоды решетки металлов находятся в пределах 0,2 — 0,7 нм.
Для ОЦК: a, b, c; a = b = c.
Для ГЦК: a, b, c; a = b = c.
Для ГПУ: а, с; с/а = 1,633 (к Zn не относится)
Число атомов в каждой элементарной ячейке (плотность упаковки — равняется числу атомов, приходящихся на одну элементарную ячейку):
ОЦК: ПУ (плотноупакованная) = ;
Координационное число — под ним понимают число атомов, находящихся на равном и наименьшем расстоянии от данного атома. Чем выше координационное число, тем больше плотность упаковки атомов:
ОЦК: расстояние (min) между атомами, на этом расстоянии от рассматриваемого атома находится 8 соседей — К8 .
ГЦК:, К12 ["https://referat.bookap.info", 9].
ГПУ: Г12 (с/а = 1,633).
Коэффициент заполнения ячейки (плотность укладки) — определяется как отношение объема, занятого атомами к объему ячейки:
Для характеристики величины атома служит атомный радиус, под которым понимается половина расстояния между ближайшими соседними атомами. Атомный радиус возрастает при уменьшении координационного числа.
3. Полиморфные (аллотропические) превращения
Атомы металла — исходя из геометрических соображений, могут образовать любую кристаллическую решетку.
Однако устойчивым, а, следовательно, реально существующим типом является решетка, обладающая наиболее низким запасом свободной энергии.
Многие металлы в зависимости от температуры могут существовать в разных кристаллических формах (т.н. полиморфных (аллотропических) модификациях). В результате полиморфного превращения атомы кристаллического тела, имеющего решетку одного типа, перестраиваются таким образом, что образуется кристаллическая решетка другого типа.
Полиморфную модификацию, устойчивую при более низкой температуре, для большинства металлов принято обозначать буквой б, при более высокой температуре в, затем г и т. д.
Полиморфное превращение протекает при постоянной температуре (например, при нагреве идет поглощение теплоты).
Известные полиморфные превращения: Feб — Feв; Coб — Coв; Tiб — Tiв; Mnб — Mnв — Mnг — Mnд; Snб — Snв, а также для Ca, Li, N, Cs, Sr, Te, Zr, V и др.
Металл с данной кристаллической решеткой должен обладать меньшим запасом свободной энергии.
Рисунок 3. Полиморфизм железа и его связь со свободной энергией системы Полиморфизм железа. Из рис. 3, видно, что в интервале температур 911 — 1392 °C устойчивым является г-железо (К 12) (имеет min свободную энергию), а при температурах ниже 911 °C и выше 1392 °C устойчиво б-железо (К 8).
В твердом металле полиморфные превращения происходят в результате зарождения и роста кристаллов аналогично кристаллизации из жидкого состояния. Зародыши новой модификации наиболее часто возникают на границах зерна исходных кристаллов.
В результате полиморфного превращения образуется новые кристаллические зерна, имеющие другой размер и форму, поэтому превращение также называют перекристаллизацией.
Полиморфное превращение сопровождается скачкообразным изменением всех свойств металлов и сплавов: удельного объема, теплоемкости, теплопроводности, электропроводности, магнитных свойств, механических и химических свойств и т. д.
Высокотемпературная модификация имеет высокую пластичность.
В таблице № 1 показан интервал температур существования различных аллотропических форм некоторых, имеющих практическое значение металлов, у которых обнаружена температурная аллотропия.
4. Анизотропия свойств металлов
Из атомно-кристаллического строения металлов видно, что плотность расположения атомов по различным плоскостям в кристаллических решетках неодинакова (рис. 4).
Вследствие неодинаковой плотности атомов в различных плоскостях и направлениях решетки многие свойства (химические, физические, механические) каждого кристалла зависят от направления решетки. Подобная неодинаковость свойств монокристалла в разных кристаллографических направлениях называется анизотропией.
Рисунок 4. Расположение атомов в различных плоскостях и направлениях в кубической решетке (ОЦК) Кристалл — тело анизотропное в отличие от аморфных тел (стекло, пластмассы и т. д. ), свойства которых не зависят от направления.
Технические металлы являются поликристаллами, т. е. состоят из большого числа анизотропных кристаллов. В большинстве случаев, как уже указывалось выше, кристаллы статистически неупорядоченно ориентированы один по отношению к другому, поэтому во всех направлениях свойства более или менее одинаковы, т. е. поликристаллическое тело является изотропным (вернее — квазиизотропным (ложная изотропия)). Такая мнимая изотропность не будет наблюдаться, если кристаллы имеют одинаковую преимущественную ориентировку в каких-то направлениях. Эта ориентированность, или текстура, создается в известной степени, но не полностью в результате значительной холодной деформации; в этом случае поликристаллический металл приобретает анизотропию свойств.
Состояния металла как вещества. Пространственная кристаллическая решетка. Строение реальных кристаллов. Краткая характеристика свинца. Состав и группа стали. Диаграмма состояния железо-цементит. Фазы и структурные составляющие железоуглеродистых сплавов.
| Рубрика | Производство и технологии |
| Вид | контрольная работа |
| Язык | русский |
| Дата добавления | 09.12.2014 |
| Размер файла | 18,8 K |
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Задание
1. Атомно-кристаллическое строение металлов. Строение реальных кристаллов.
2. Краткая характеристика свинца
3. Задача: Для изготовления резцов выбрана сталь Р6М5. Укажите состав и определите группу стали по назначению. Назначьте и обоснуйте режим термической обработки, объяснив влияние легирования на превращение, происходящее при термической обработке данной стали. Опишите микроструктуру и главные свойства резцов после термической обработки.
4. Диаграмма состояния железо-цементит. Фазы и структурные составляющие железоуглеродистых сплавов.
1. Атомно-кристаллическое строение металлов
Каждый металл (вещество) может находится в четырех состояниях: газообразном, жидком, твердом и в виде плазмы. В газообразном состоянии расстояние между атомами (частицами) велико, силы взаимодействия малы и атомы хаотично перемещаются в пространстве, отталкиваясь друг от друга. Атомы газообразного вещества обладают большой кинетической энергией. В жидком металле атомы сохраняют лишь ближний порядок, то есть в небольшом объеме упорядоченно и закономерно расположено небольшое количество атомов. Ближний порядок неустойчив, он может возникать и исчезать под действием тепловых колебаний.
В металлах, находящихся в твердом состоянии, порядок расположения атомов строго определен и закономерен, силы взаимодействия уравновешены, тело сохраняет свою форму. Металлы имеют кристаллическое строение с правильным закономерным расположением атомов в пространстве.
Воображаемые линии, проведенные через центры атомов, расположенных в одной плоскости, образуют решетку, в узлах которой располагаются атомы.
Такая конфигурация называется кристаллографической плоскостью. Многократное повторение кристаллографических плоскостей в пространстве позволяет получить пространственную кристаллическую решетку.
Пространственная кристаллическая решетка сложна в изображении, поэтому представление об атомном строении кристаллов дается в виде элементарных кристаллических ячеек. Под элементарной кристаллической ячейкой понимают минимальный объем, дающий представление об атомной структуре металла в целом, его повторение в пространстве образует кристаллическую решетку. Элементарные кристаллические ячейки характеризуются следующими основными параметрами: периодом решетки, координационным числом, атомным радиусом, базисом (атомной плоскостью).
Периодом решетки называется расстояние между центрами двух соседних частиц (атомов, ионов) в элементарной ячейке решетки.
Периоды решетки измеряют в нанометрах (НМ) или пикометрах (ПМ).
Координационное число.
Координационное число показывает количество атомов, находящихся на самом близком расстоянии от любого выбранного атома в решетке. Под атомным радиусом понимают половину межатомного расстояния между центрами ближайших атомов в кристаллической решетке элемента при равновесных условиях. Базисом решетки называется количество атомов, приходящихся на одну элементарную ячейку решетки.
Простейшим типом кристаллического строения является кубическая решетка, в которой атомы расположены в углах куба (например, период решетки равен 6, координационное число К=6, базис решетки равен 1, каждый из атомов, расположенных в углах куба, принадлежит одной из восьми элементарных ячеек, то есть на одну ячейку приходится 1/8 атома).
В простой кубической решетке атомы уложены (упакованы) недостаточно плотно. Стремление атомов занять места, наиболее близкие друг к другу, приводит к образованию новых типов решеток.
Строение реальных кристаллов.
Реальное строение металлов значительно отличается от идеального. При идеальном строении кристаллов (металлов) все атомы теоретически должны находится строго в узлах кристаллической решетки. Теоретическая прочность такого металла чрезвычайно высока. Так, теоретическая прочность при сдвиге (под действием касательных напряжений) Тсдв = G/ (2ri), где G - модуль сдвига (модуль Юнга).
В соответствии с этой формулой теоретический предел прочности железа должен составлять примерно 13000 Мпа, при такой прочности проволока диаметром 1 мм выдержала бы груз массой более тонны (для железа G=80 Мпа).
В действительности же, прочность железа примерно в 100 раз меньше - 150 Мпа. Такое несоответствие объясняется различием идеального и реального строения металлов. Во-первых технические металлы состоят из большого количества кристаллов (зерен), то есть являются поликристаллическими веществами. При этом кристаллы (зерна) в реальном металле не имеют правильной формы и идеально упорядоченного расположения атомов. Во - вторых, даже в самих поликристаллах имеются различные несовершенства (дефекты).
Различают точечные, линейные и поверхностные несовершенства кристаллического строения.
Точечные дефекты малы во всех трех измерениях. К ним относят вакансии и междоузельные (дислоцированные) атомы. Образование точечных дефектов связано с диффузионным перемещением атомов под действием тепловых колебаний. С повышением температуры металла число вакансий растет. Точечные дефекты оказывают влияния на некоторые физические свойства металлов (электропроводность, магнитные свойства и т.д.) и фазовые превращения в металлах и сплавах.
Линейные дефекты имеют малые размеры в двух измерениях и большую протяженность в третьем измерении. Эти несовершенства называются дислокациями. Дислокации образуются в процессе кристаллизации и главным образом при деформации металла.
2. Краткая характеристика свинца
Свинец - элемент 14 группы, шестого периода периодической системы химических элементов Д.И. Менделеева, с атомным номером 82. Обозначается символом Pb (лат. Plumbum). Простое вещество свинец (CAS - номер: 7439-92-1) - ковкий, сравнительно легкоплавкий металл серого цвета.
Свинец известен с глубокой древности. Изделия из этого металла (монеты, медальоны) использовались в Древнем Риме. Указание на свинец, как на определенный металл имеется в Ветхом Завете. Выплавка свинца была первым из известных человеку металлургических процессов. До 1990 г. большое количество свинца использовалось (вместе с сурьмой и оловом) для отливки типографских шрифтов, а также в виде тетраэтисвинца - для повышения октанового числа моторного топлива.
В природе самородный свинец встречается редко, круг пород, в которых он установлен, достаточно широк: от осадочных пород ультраосновных пород. Всегда содержится в рудах урана и тория, имея часто радиогенную природу. В кларковых концентрациях свинец входит практически во все породы.
Самые крупные производители свинца - это США, Китай, Корея и страны ЕС.
Свинец имеет довольно низкую теплопроводность. Она составляет 35,1 Вт/ (м-к) при температуре 0 0 С. Металл мягкий, легко режется ножом. При разрезании открывается блестящая поверхность, которая на воздухе со временем тускнеет.
Чистый свинец - серебристо-белый, но на воздухе быстро покрывается синевато-серым налетом. Это мягкий, плотный, легкоплавкий металл, он пластичен выше 300 0 С, что используют для изготовления оболочек кабелей, выдавливания проволок и трубок, а также в запорных устройствах водопроводных сетей. Свинец иногда формуют, но из-за низкой прочности на разрыв он плохо поддается ковке. На воздухе образует пленку, защищающую его от окисления. В воде, насыщенной кислородом растворяется. Непригоден для трубопроводов с питьевой водой. Все растворимые соединения свинца в воде ядовиты.
Свинец применяют для радиационной защиты в рентгеновских установках и в ядерных реакторах.
металл железоуглеродистый сплав свинец
Сплав олова со свинцом, содержащий 10-15% Pb используется для домашней утвари, а припой (67% Pb) применяют в электротехнике. Сплавы свинца с сурьмой обычно применяются для оболочек кабелей и пластин электрических аккумуляторов. Соединения свинца используются в производстве красителей, красок, стеклянных изделий и как добавки к бензину.
3. Задача
Для изготовления резцов выбрана сталь Р6М5. Укажите состав и определите группу стали по назначению. Назначьте и обоснуйте режим термической обработки, объяснив влияние легирования на превращение, происходящее при термической обработке данной стали. Опишите микроструктуру и главные свойства резцов после термической обработки.
Р6М5 - быстрорежущая инструментальная сталь. Быстрорежущие стали применяют для режущих инструментов, работающих в условиях значительного нагружения и нагрева рабочих кромок.
Инструмент из быстрорежущих сталей обладает высокой стабильностью свойств. В марках стали буквы и означают Р - быстрорежущая, цифра, следующая за буквой - среднюю массовую долю вольфрама (%), М - молибден, цифра, следующая за буквой, означает массовую долю молибдена.
В обозначениях марок стали не указывают массовую долю хрома - при любой массовой доле.
Все металлы и металлические сплавы – тела кристаллические, атомы (ионы) расположены в металле закономерно в отличие от аморфных тел, в которых атомы расположены хаотично.
Металлическое состояние возникает в комплексе атомов, когда при их сближении внешние электроны теряют связь с отдельными атомами, становятся общими, т.е. коллективизируются и свободно перемещаются между положительно заряженными и периодически расположенными ионами.
Устойчивость металла определяется электрическим притяжением между положительно заряженными ионами и обобщенными электронами (такое взаимодействие получило название металлической связи).
Сила связи в металлах определяется силами отталкивания и силами притяжения между ионами и электронами. Атомы (ионы) располагаются на таком расстоянии друг от друга, чтобы энергия взаимодействия была минимальной (рис. 1)

Рисунок 1. Энергетические условия взаимодействия атомов в кристаллической решетке вещества
Величина а соответствует расстояние между атомами в кристаллической решетке, а а 0 соответствует равновесному расстоянию между атомами. В связи с этим в металле атомы располагаются закономерно, образуя правильную кристаллическую решетку, что соответствует минимальной энергии взаимодействия атомов.
Металлические состояния характеризуются высокой энергией связи между атомами. Мерой ее служит теплота сублимации (сумма энергии необходимой для перехода твердого металла к парообразному состоянию, для металла – от 20 до 200 ккал/(г·атом)).
2. Атомно-кристаллическое строение металлов
Под атомно-кристаллической структурой понимают взаимное расположение атомов, существующее в кристалле. Атомы в кристалле расположены в определенном порядке, который периодически повторяется в трех измерениях.
Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узле которой располагаются атомы (ионы), образующие металл.
География атомной энергетики РФ
. мощностью 210 Мвт. Себестоимость 1 квт-ч электроэнергии (важнейший экономический показатель работы всякой электростанции) на этой АЭС систематически снижалась: она составляла 1,24 коп. в . и уменьшения его запасов, обусловленного необходимостью удовлетворять потребности растущих мощностей атомных станций, возникнет экономическая необходимость оптимального использования урана таким образом, чтобы .
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, получил название элементарной кристаллической ячейки (решетки).
Для характеристики элементарной ячейки задают шесть величин: три ребра ячейки a, b, c и три угла между ними α, β, γ. Эти величины называют параметрами кристаллической решетки.
Кристаллические решетки бывают простыми (атомы только в вершинах решетки) и сложными.
Металлы образуют одну из следующих высокосимметричных сложных решеток с плотной упаковкой атомов: кубическую объемноцентрированную (ОЦК), кубическую гранецентрированную (ГЦК) и гексагональную (ГПУ) (рис. 2).

ОЦК: Rb, K, Na, Li, Ti β , Tlβ , Zrβ , Ta, W, V, Feα , Cr, Nb, Ba, и др.
ГЦК: Cu, Al, Pt, Pb, Ni, Ag, Au, Pd, Rh, Ir, Fe γ , Coα , Caα , Ce, Srα , Th, Sc и др.
Рисунок 2. Кристаллические решетки металлов и схемы упаковки атомов
Расстояние между ближайшими параллельными атомными плоскостями, образующими элементарную ячейку, называют периодом решетки, измеряется в нанометрах (1нм = 10 -9 см = Å= 10 -8 см).
Периоды решетки металлов находятся в пределах 0,2 – 0,7 нм.
ДляОЦК: a, b, c; a = b = c.
ДляГЦК: a, b, c; a = b = c.
Для ГПУ: а, с; с/а = 1,633 (к Zn не относится)
Число атомов в каждой элементарной ячейке (плотность упаковки – равняется числу атомов, приходящихся на одну элементарную ячейку):
ОЦК: ПУ (плотноупакованная) = ;
ГЦК: ПУ = ;
ГПУ: ПУ = .
Координационное число – под ним понимают число атомов, находящихся на равном и наименьшем расстоянии от данного атома. Чем выше координационное число, тем больше плотность упаковки атомов:
ОЦК: расстояние (min) между атомами , на этом расстоянии от рассматриваемого атома находится 8 соседей – К8 .
ГЦК: , К12.
ГПУ: Г12 (с/а = 1,633).
Коэффициент заполнения ячейки (плотность укладки) – определяется как отношение объема, занятого атомами к объему ячейки:
Для характеристики величины атома служит атомный радиус, под которым понимается половина расстояния между ближайшими соседними атомами. Атомный радиус возрастает при уменьшении координационного числа.
3. Полиморфные (аллотропические) превращения
Атомы металла – исходя из геометрических соображений, могут образовать любую кристаллическую решетку.
Материаловедение и технология металлов
. направлениями в развитии металловедения является разработка способов производства чистых и сверхчистых металлов, свойства которых сильно отличаются от свойств металлов технической чистоты, с . от любого атома в решетке. ? базис решетки количество атомов, приходящихся на одну элементарную ячейку решетки. ? плотность упаковки атомов в кристаллической решетке - объем, занятый атомами, которые условно .
Однако устойчивым, а, следовательно, реально существующим типом является решетка, обладающая наиболее низким запасом свободной энергии.
Многие металлы в зависимости от температуры могут существовать в разных кристаллических формах (т.н. полиморфных (аллотропических) модификациях).
В превращения металлов">результате полиморфного превращения атомы кристаллического тела, имеющего решетку одного типа, перестраиваются таким образом, что образуется кристаллическая решетка другого типа.
Полиморфную модификацию, устойчивую при более низкой температуре, для большинства металлов принято обозначать буквой α, при более высокой температуре β, затем γ и т.д.
Полиморфное превращение протекает при постоянной температуре (например, при нагреве идет поглощение теплоты).
Известные полиморфные превращения: Fe α ↔ Feβ ; Coα ↔ Coβ ; Tiα ↔ Tiβ ; Mnα ↔ Mnβ ↔ Mnγ ↔ Mnδ ; Snα ↔ Snβ , а также для Ca, Li, N, Cs, Sr, Te, Zr, V и др.
Металл с данной кристаллической решеткой должен обладать меньшим запасом свободной энергии.

Рисунок 3. Полиморфизм железа и его связь со свободной энергией системы
Полиморфизм железа. Из рис. 3, видно, что в интервале температур 911 – 1392°С устойчивым является γ-железо (К 12) (имеет min свободную энергию), а при температурах ниже 911°С и выше 1392°С устойчиво α-железо (К 8).
В твердом металле полиморфные превращения происходят в результате зарождения и роста кристаллов аналогично кристаллизации из жидкого состояния. Зародыши новой модификации наиболее часто возникают на границах зерна исходных кристаллов.
В результате полиморфного превращения образуется новые кристаллические зерна, имеющие другой размер и форму, поэтому превращение также называют перекристаллизацией.
Полиморфное превращение сопровождается скачкообразным изменением всех свойств металлов и сплавов: удельного объема, теплоемкости, теплопроводности, электропроводности, магнитных свойств, механических и химических свойств и т.д.
Высокотемпературная модификация имеет высокую пластичность.
В таблице № 1 показан интервал температур существования различных аллотропических форм некоторых, имеющих практическое значение металлов, у которых обнаружена температурная аллотропия.

4. Анизотропия свойств металлов
Из атомно-кристаллического строения металлов видно, что плотность расположения атомов по различным плоскостям в кристаллических решетках неодинакова (рис. 4).
Вследствие неодинаковой плотности атомов в различных плоскостях и направлениях решетки многие свойства (химические, физические, механические) каждого кристалла зависят от направления решетки. Подобная неодинаковость свойств монокристалла в разных кристаллографических направлениях называется анизотропией.
Кристаллизация металлов
. превращения определяют структуру металла, а, следовательно, и его свойства. Рассмотрим подробней понятие кристаллизации, ее виды и кристаллическое 1.1. Понятие кристаллизации[1,2,4]. Переход металла из жидкого состояния в твердое (кристаллическое) называется кристаллизацией. Кристаллизация . упаковки атомов. В этих направлениях образуются длинные ветви будущего кристалла — так называемые оси .

Рисунок 4. Расположение атомов в различных плоскостях и направлениях в кубической решетке (ОЦК)
Кристалл – тело анизотропное в отличие от аморфных тел (стекло, пластмассы и т.д.), свойства которых не зависят от направления.
Технические металлы являются поликристаллами, т.е. состоят из большого числа анизотропных кристаллов. В большинстве случаев, как уже указывалось выше, кристаллы статистически неупорядоченно ориентированы один по отношению к другому, поэтому во всех направлениях свойства более или менее одинаковы, т.е. поликристаллическое тело является изотропным (вернее – квазиизотропным (ложная изотропия)).
Такая мнимая изотропность не будет наблюдаться, если кристаллы имеют одинаковую преимущественную ориентировку в каких-то направлениях. Эта ориентированность, или текстура, создается в известной степени, но не полностью в результате значительной холодной деформации; в этом случае поликристаллический металл приобретает анизотропию свойств.
Литература
1. Лахтин Ю.М., Леонтьева В.П. Материаловедение. М., 1972, 1980.
2. Гуляев А.П. Металловедение. М., 1986.
3. Новиков И.И. Дефекты кристаллического строения металлов. М., 1983.
4. Антикайн П.А. Металловедение. М., 1972.
Металлы и сплавы
Общая и неорганическая химия
Теория о Высшем Разуме
Давно ли люди гибнут за металл и как именно закалялась сталь
Программа для поступающих в вузы (ответы)
Развитие, становление и основные аспекты фармации
Кристаллы в природе
Кристаллы и их свойства
Сорбционные свойства мха по отношению к микроорганизмам и тяжелым металлам
Химия и технология платиновых металлов
Механизмы имплантации в металлы и сплавы ионов азота с энергией 1-10 кэВ
Биокерамика на основе фосфатов кальция
Методы химического анализа
Концепции современного естествознания
Методы защиты от коррозии металлов и сплавов
Примеры похожих учебных работ
Материаловедение и технология металлов
. материалах для исследования космоса, развития электроники, атомной энергетики. Основными направлениями в развитии металловедения является разработка способов производства чистых и сверхчистых металлов, свойства которых сильно отличаются .
Кристаллические и аморфные тела
. Глава 1. Кристаллические и аморфные тела. По своим физическим свойствам и молекулярной структуре твердые тела разделяются на два класса – аморфные и кристаллические тела. Характерной особенностью аморфных тел является их изотропность, т.е. .
Цветные металлы и сплавы, применяемые в строительстве
. добавляются к некоторым железным сплавам, для повышения стойкости производимой из них продукции. Цветные металлы, в свою очередь, делятся на легкие и тяжелые. При этом производство тяжелых .
Классификация и структура полимеров. Конструкционная прочность металлов и сплавов
. прочностью конструкционных материалов". Таким образом, становится ясным, почему актуальны проблемы физики прочности металлов и сплавов. Российская наука о прочности . структуру, полученную . связей . и тем, что макромолекулы имеют цепное строение и .
Сверхпроводимость металлов в квантовой физике
. и найти для электронов проводимости иной статистический закон. Сверхпроводимость металлов в квантовой физике В сфере . следующем: в металле между электронами появляется особый вид напряжение, помимо интенсивности работы кулоновского отталкивания. .
Под атомно-кристаллической структурой понимают взаимное расположение атомов, существующее в кристалле. Кристалл состоит из атомов (ионов), расположенных в определенном порядке, который периодически повторяется в трех измерениях.
В кристаллах существует не только ближний, но и дальний порядок размещения атомов, т. е. упорядоченное расположение частиц в кристалле сохраняется на больших участках кристаллов.
Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узлах которой располагаются атомы (ионы), образующие металл (твердое кристаллическое тело).
Наименьший объем кристалла, дающий представление об атомной структуре металла во всем объеме, получил название элементарной кристаллической ячейки.
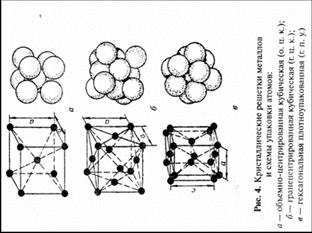
Подавляющее число технически важных металлов образуют одну из следующих решеток: кубическую объемно-центрированную, кубическую гранецентрированную и гексагональную (рис. 4).
В кубической объемно-центрированной решетке атомы расположены в узлах ячейки и один атом — в центре объема куба (рис. 4, а). Кубическую объемно-центрированную решетку имеют металлы: ое-железо, хром, ниобий, вольфрам, ванадий и др.
В кубической гранецентрированной решетке атомы расположены в углах куба и в центре каждой грани (рис. 4, б). Этот тип решетки имеют металлы: железо, никель, медь, золото и др.
В гексагональной решетке (рис. 4, в) атомы расположены в углах и центре шестигранных оснований призмы и три атома в средней плоскости призмы. Эту упаковку атомов имеют металлы: магний, цинк и др.
Некоторые металлы имеют тетрагональную решетку.
Размеры кристаллической решетки характеризуются величинами периодов, под которыми понимают расстояние между ближайшими параллельными атомными плоскостями, образующими элементарную ячейку (рис. 4). Период решетки измеряется в ангстремах (А) (1А=1—8 см).
Период решетки металлов находится в пределах от 1 до 7 А.
Читайте также:

