Аллотропия металлов реферат по химии
Обновлено: 02.07.2024
Основной причиной полиморфных или аллотропических превращений является стремление любого вещества обладать минимальным запасом свободной энергии. Если у металла при достижении какой-то определенной температуры изменение типа кристаллической решетки обеспечивает уменьшение запаса свободной энергии, то такой металл претерпевает полиморфное превращение. Полиморфные превращения металлов имеют важное… Читать ещё >
Аллотропия (полиморфизм) металлов ( реферат , курсовая , диплом , контрольная )
Способность металлов образовывать различные кристаллические структуры одинакового состава называется аллотропией или полиморфизмом.
Например, некоторые металлы (железо, титан, олово и др.) способны при достижении определенных температур изменять свое кристаллическое строение, перестраивая тин элементарной ячейки. Так, ОЦК-жслсзо при нагреве до 911 °C перестраивает кристаллическую решетку и становится ГЦК-железом. Это строение сохраняется до 1392 °C, после чего при повышении температуры решетка снова перестраивается и приобретает ОЦК-строение, сохраняя его вплоть до температуры плавления 1539 °C.
Основной причиной полиморфных или аллотропических превращений является стремление любого вещества обладать минимальным запасом свободной энергии. Если у металла при достижении какой-то определенной температуры изменение типа кристаллической решетки обеспечивает уменьшение запаса свободной энергии, то такой металл претерпевает полиморфное превращение.
Обычно полиморфные формы металла обозначаются буквами греческого алфавита, при этом низкотемпературные модификации обозначают буквой а, а последующие в порядке роста температур — Р> У" б и т. д.
Полиморфные превращения металлов имеют важное практическое значение. Благодаря им изменяются такие свойства металла, как плотность, способность растворять в своей решетке другие элементы и др. Поэтому полиморфные превращения можно использовать для целенаправленного изменения свойств металлов путем термической обработки.
Введение
Аллотропией, или полиморфизмом, называют способность металла в твердом состоянии иметь различные кристаллические формы. Процесс перехода из одной кристаллической формы в другую называют аллотропическим превращением. При нагреве чистого металла такое превращение сопровождается поглощением тепла и происходит при постоянной температуре, что связано с необходимостью затраты определеннойэнергии на перестройку кристаллической решетки. Аллотропические превращения имеют многие металлы: железо, олово, титан и др. Например, железо в интервале температур 911 -1392°С имеет гранецентрированную кубическую решетку (ГЦК) г-Fe (рис. 7). В интервалах до 911°С и от 1392 до 1539°С железо имеет объемно-центрированную кубическую решетку (ОЦК) - б-Fe. Аллотропические формы металла обозначаются буквамиа, в, г и т. д. Существующая при самой низкой температуре аллотропическая форма металла обозначается через букву б, которая в виде индекса добавляется к символу химического элемента металла и т. д.
При аллотропических превращениях происходит изменение свойств металлов - изменение объема металлов (особенно характерно для олова) и растворимости углерода (характерно для железа).Методы изучения строения металлов
Изучение строения металлов и сплавов производится методами макро- и микроанализа, рентгеновского, а также дефектоскопии (рентгеновской, магнитной, ультразвуковой).
Методом макроанализа изучается макроструктура, т. е. структура, видимая невооруженным глазом или с помощью лупы, при этом выявляются крупные дефекты: трещины, усадочные раковины, газовые пузыри и т. д., а также неравномерность распределенияпримесей в металле. Макроструктуру определяют по изломам металла, по макрошлифам. Макрошлиф - это образец металла или сплава, одна из сторон которого отшлифована, тщательно обезжирена, протравлена и рассматривается с помощью лупы с увеличением в 5 -10х.
Микроанализ выявляет структуру металла или сплава по микрошлифам, приготовленным так же, как и для макроанализа, но дополнительно отполированнымдо зеркального блеска. Шлифы рассматривают в отраженном свете под оптическим микроскопом при увеличении до 3000х. Из-за различной ориентировки зерен металла они травятся не в одинаковой степени и под микроскопом свет также отражается неодинаково. Границы зерен благодаря примесям травятся сильнее, чем основной металл, и выявляются более рельефно. В сплаве структурные составляющие травятся такжеразлично. В электронном микроскопе рассматривают реплику - слепок с особо тонкой структуры блоков, фрагментов, дислокации при увеличениях до 100000х. Этот важнейший анализ определяет размеры и форму зерен, структурные составляющие, неметаллические включения и их характер (трещины, пористость и т. д.), качество термической, обработки. Зная микроструктуру, можно объяснить причины изменения свойств металла.
Спомощью рентгеновского анализа изучают атомную структуру металлов, типы и параметры кристаллических решеток, а также дефекты, лежащие в глубине. Этот анализ, основанный на дифракции (отражении) рентгеновских лучей рядами атомов кристаллической решетки, позволяет обнаружить дефекты (пористость, трещины, газовые пузыри, шлаковые включения и т. д.), не разрушая металла. В местах дефектов рентгеновскиелучи поглощаются меньше, чем в сплошном металле, и поэтому на фотопленке такие лучи образуют темные пятна, соответствующие форме дефекта.
Для исследования структуры металла и дефектов изделий широко применяют гамма-лучи, которые проникают в изделие на большую глубину, чем рентгеновские.
Магнитным методом исследуют дефекты в магнитных металлах (сталь, никель и др.) на глубине до 2 мм (трещины различногопроисхождения, неметаллические включения и т. д.). Для этого испытуемое изделие намагничивают, покрывают его поверхность порошком железа, осматривают поверхность и размагничивают изделие. Вокруг дефекта образуется неоднородное поле, вследствие чего магнитный порошок повторяет очертания дефекта. Другой метод - магнитный индукционный - часто используют.
Чтобы читать весь документ, зарегистрируйся.
Связанные рефераты
Аллотропия металлов
Аллотропия
Аллотропия
. План 1 Аллотропия 1.1 История 1.2 Примеры 2 Углерод 2.1 Углерод как атом 2.2 Углерод в.
Понятие аллотропии
Металлы
. КУРС ЛЕКЦИЙ по дисциплине “ЦВЕТНЫЕ МЕТАЛЛЫ И СПЛАВЫ” Для.
Химия изучает свойства и строение простых веществ. В большинстве своем они остаются неизменными в любых ситуациях. Однако есть ряд элементов, способных менять свои свойства в различных своих состояниях. Такое явление называется аллотропией. Знание о поведении элементов, подверженных аллотропии, расширяет понимание устройства мира и поведения в нем веществ и элементов.
Определение
Аллотропия - это возможность элемента трансформироваться в другой. В некоторых случаях даже в два или три. Если переводить название термина с греческого языка, то аллотропия - это "другое свойство". То есть буквальный перевод раскрывает сущность явления.
Виды аллотропии

Аллотропия, свойственная некоторым веществам, условно делится на два вида - по составу и по строению. В первом случае различно число атомов в молекуле. Во втором - строение кристаллической решетки.
В химии аллотропия - это изменение вещества независимо от того, жидкое оно, твердое или газообразное. Единственное отступление от терминологии появляется в работе с твердыми веществами, их строение сложнее, для их трансформации используется слово "полиморфизм", в переводе с греческого означающее "многообразный".
Каким веществам свойственна аллотропия
Не все вещества способны преобразоваться из сложных в простые даже под действием температур или других воздействий. Это может происходить только с теми из них, у которых есть способность к образованию гомоцепных структур или хорошо окисляющихся. Именно поэтому аллотропия веществ свойственна неметаллам. Хотя справедливости ради следует сказать, что есть металлы, способные преобразовываться в простые элементы, но это, скорее, полуметаллы.
Примеры аллотропии
Для понимания процесса существует ряд примеров преобразования вещества, причем оно бывает обратимым и необратимым. То есть вещество может после воздействия на него температуры или давления вернуться к первоначальному состоянию. Но бывает так, что оно остается в видоизмененном состоянии. Например, ромбическая сера - при нагревании ее до температуры 95,5 градуса по Цельсию она преобразуется в моноклинную форму. При снижении температуры до 95,5 градуса наступает обратное преобразование - из моноклинной формы в ромбическую.
Другой пример аллотропии - это изменение белого фосфора в черный. В данном случае для проведения преобразования требуется температура в 200 градусов по Цельсию и давление в 1,25 г Па. При воздействии тех же температур и давления на преобразованный черный фосфор он не сможет вернуться к первоначальному состоянию.
Как уже упоминалось, явление аллотропии свойственно и некоторым металлам. Но из-за сложности их структуры переходы из одного в другое состояние могут чередоваться. Например, в нормальных условиях белое олово является пластичным металлом, но при нагревании его при температуре 173 градуса по Цельсию оно перестраивает свою кристаллическую решетку до очень хрупкого состояния, а при снижении температуры до 13 градусов кристаллическая решетка принимает вид кубической алмазоподобной и делает вещество порошкообразным.
Модификации неметаллов

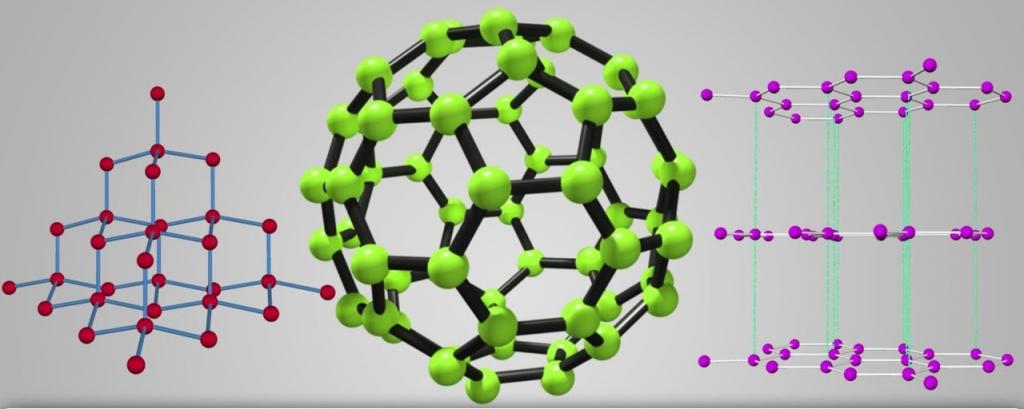
Самыми яркими и многообразными физическими свойствами аллотропии обладает углерод. Он способен перерождаться в самое большое количество аллотропных форм, причем с различными не только свойствами, но и строением кристаллической решетки. Взять, например, графит и алмаз. Формы одного вещества, но с разными строениями кристаллических решеток – графит чуть плотнее порошка, а алмаз - самое крепкое вещество на земле. И это уже не говоря об углеродных нанотрубках, лонсдейлите, фуллерене, карбине и других формах углерода.
Аллотропия характерна для серы. В нормальных условиях структура вещества моноклинная, а под воздействием температур может преобразоваться в пластическую и следом за этим в ромбовидную.
Фосфор способен изменяться в 11 форм. Причем 3 из них - белый, черный, красный - даже встречаются в природе, остальные можно получить искусственным путем. Отличается одна форма вещества от другой количеством атомов в молекуле. Различными цветами в химии представлен селен. Он также бывает серный, черный и красный.
Очень известная аллотропия - это кислород. Он видоизменяется до озона под действием температуры или электрического тока. Известный пример природного воздействия – молния. Во время разряда электрического поля кислород превращается в озон.
Модификации полуметаллов

Бор - это полуметалл, встречающийся в природе в аморфной и кристаллической форме. Но у него есть еще 10 известных науке форм.
Аморфным и кристаллическим бывает кремний. Сурьма в четырех формах по своей структуре представляется металлом, и в трех она аморфная, аллотропная.
Как и в случае с фосфором или селеном, мышьяк бывает серый или черный, в зависимости от формы – полимер или неметаллическая структура.
Модификации металлов

Самым широким спектром форм среди металлов обладает железо. В первом виде феррита, с характерной объемно-центрированной кубической кристаллической решеткой, железо способно существовать в температурных пределах от 0 до 769 градусов по Цельсию. Имеет свойства ферромагнетиков.
Второй тип феррита существует при температурах в диапазоне 769-917 градусов по Цельсию. Отличается объемно-центрированной кубической кристаллической решеткой. Магнетические свойства проявляет как парамагнетик.
Третий тип железа называется аустенит, характерен гранецентрированной кубической кристаллической решеткой. Способен существовать только при температурах от 917 до 1394 градусов по Цельсию. Магнитных свойств не имеет.
Четвертый тип железа возникает при температурах свыше 1397 градусов по Цельсию. Магнитных свойств не имеет, характерен объемно-центрированной кубической кристаллической решеткой.
Другой металл, имеющий несколько типов преобразования, - это олово. В аллотропной форме может существовать в виде порошка с кристаллической решеткой, подобной алмазной. Это так называемое серое олово. Есть и более привычная форма металла – белое олово. Оно встречается в виде пластичного метала серебряного цвета. Третья форма характерна тугоплавкостью, так как обладает ромбической кристаллической решеткой, называется она гамма-оловом.
Заключение

Все металлы, полуметаллы и неметаллы различных аллотропных типов с характерным строением кристаллических решеток, массой, количеством и зарядом протонов и нейтронов могут встречаться в природе в чистом, натуральном виде или получаются только в лаборатории. В обычных условиях они не сохраняют своей стабильности. Все это говорит о многообразии химических элементов и перспективах открытий новых доселе неизвестных науке форм и типов веществ. Такие исследования ведут к развитию всех отраслей жизнедеятельности человека.
- Для учеников 1-11 классов и дошкольников
- Бесплатные сертификаты учителям и участникам

Описание презентации по отдельным слайдам:


Аллотропия- явление существования в виде 2-х или нескольких простых веществ, различных по строению и свойствам Причины аллотропии: 1. Разные типы кристаллических решеток (белый фосфор Р4 – молекулярная, красный фосфор Р – атомная). 2. Разная структура кристаллической решетки (алмаз – тетраэдрическая, графит – слоистая). 3. Разный состав молекул аллотропных модификаций (О2 и О3 )

Аллотропия свойственна не менее чем двенадцати металлам, Ряд из которых имеют важнейшее техническое значение (Sn, Ti, Zr. Сг, Mn, Fe, Co, Ni, V, Np, Pu). Величина является степенью переохлаждения. Это переохлаждение зависит от природы металла, степени его загрязненности различными включениями и скорости охлаждения. У некоторых металлов оно может быть значительным, например для сурьмы достигает 41 °С (кристаллизация начинается при 631 °С-41 °С = 590 °С). При переохлаждении процесс кристаллизации начинается бурно, в результате чего температура металла скачкообразно повышается.

Олово Олово существует в трех аллотропных модификациях. Серое олово (α-Sn) мелкокристаллический порошок, полупроводник, имеющий алмазоподобную кристаллическую решётку, существует при температуре ниже 13,2 °С. Белое олово (β-Sn) — пластичный серебристый металл, устойчивый в интервале температур 13,2—161 °С. Высокотемпературное гамма-олово (γ-Sn), имеющее ромбическую структуру, отличается высокой плотностью и хрупкостью, устойчиво между 161 и 232 °С (температура плавления чистого олова).

Железо Для железа известны четыре кристаллические модификации: до 769 °C (точка Кюри) существует α-Fe (феррит) с объёмноцентрированной кубической решёткой и свойствами ферромагнетика; в температурном интервале 769—917 °C существует β-Fe, который отличается от α-Fe только параметрами объёмноцентрированной кубической решётки и магнитными свойствами парамагнетика; в температурном интервале 917—1394 °C существует γ-Fe (аустенит) с гранецентрированной кубической решёткой; выше 1394 °C устойчиво δ-Fe с объёмоцентрированной кубической решёткой

Лантаноиды Церий, самарий, тербий, диспрозий и иттербий имеют по три аллотропических модификации; празеодим, неодим, гадолиний и тербий — по две.

Актиниды Для всех актиноидов, кроме актиния, характерен полиморфизм. Кристаллические структуры протактиния, урана, нептуния и плутония по своей сложности не имеют аналогов среди лантаноидов и более похожи на структуры 3d-переходных металлов. Плутоний имеет семь полиморфных модификаций (в том числе, при обычном давлении — 6), а уран, прометий, нептуний, америций, берклий и калифорний — три. Лёгкие актиниды в точке плавления имеют объёмно-центрированную решётку, а начиная с плутония — гранецентрированную.
Читайте также:

