Влияние катионов и анионов на вязкость цитоплазмы кратко
Обновлено: 04.07.2024
Цитоплазма, представляющая собой основную массу протопласта (за вычетом ядра, митохондрии и пластид), имеет сложное строение, детали ко-торого до сих пор еще не выяснены. Она состоит из большого количества высокомолекулярных веществ — биополимеров. Часть последних формирует особые структурные образования — мембраны, придающие цитоплазме значительную структурность. Цитоплазма проявляет свойства сравнительно вязкой жидкости, но одновременно и некоторые свойства твердого тела (эластичность).
Прикрепленные файлы: 1 файл
10 50 нет 210.docx
10. Избирательная проницаемость цитоплазмы, ее причины. Строение цитоплазмы и тонопласта.
Цитоплазма, представляющая собой основную массу протопласта (за вычетом ядра, митохондрии и пластид), имеет сложное строение, детали которого до сих пор еще не выяснены. Она состоит из большого количества высокомолекулярных веществ — биополимеров. Часть последних формирует особые структурные образования — мембраны, придающие цитоплазме значительную структурность. Цитоплазма проявляет свойства сравнительно вязкой жидкости, но одновременно и некоторые свойства твердого тела (эластичность). Подобное сочетание свойств возможно благодаря тому, что молекулы биополимеров способны образовывать временные ассоциации различных размеров. Разрушение этих ассоциаций способствует проявлению жидкостных свойств, их восстановлению — проявлению свойств твердого тела.
Структурную основу всей цитоплазмы, так называемый цитоскелет, составляют особые белки, способные преобразовывать химическую энергию в механическую работу. Это — сократительные белки, подобные тем белкам, из которых построены мышцы животных. Благодаря пустой сети мембран внутри цитоплазмы образуется множество так называемых отделов. Тем самым создаются условия для пространственного разграничения различных биохимических процессов. Эти процессы могут протекать одновременно в разных частях цитоплазмы одной и той же клетки, не мешая друг другу.
Схема строения геля
Молекулы биополимеров — белков и липидов — в мембранах расположены в строго определенной последовательности. Благодаря такому строению мембрана обладает способностью избирательно пропускать молекулы одних веществ и не пропускать молекулы других веществ, т. е. она обладает избирательной проницаемостью, и играет важную роль в жизнедеятельности.
Цитоплазма имеет две пограничные мембраны. Одна из этих мембран, называемая плазмалеммой, отграничиваетцитоплазму от вакуоли. Тонопласт — наиболее устойчивая часть цитоплазмы; при гибели содержимого клетки он отмирает последним.
Значительную роль в процессах структурообразования в цитоплазме играют ионы, а также молекулы низкомолекулярных соединений, обладающие полярными группами.
Рис.1. Схематическое изображение различных форм плазмолиза: 1 — выпуклая; 2 — вогнутая; 3, 4 — судорожная.
Вещество, поступившее в цитоплазму, либо связывается самой цитоплазмой, либо поступает из нее в клеточный сок. Растворы солей или сахаров высокой концентрации обычно не проникают в цитоплазму, а оттягивают из нее воду. При этом цитоплазма отходит от стенок клетки. Это явление получило название плазмолиза. При отхождении цитоплазмы от стенок клетки она образует вогнутуюповерхность (вогнутый плазмолиз), которая затем через 15—30 мин переходит в выпуклую форму (выпуклый плазмолиз).
Своеобразную форму плазмолиза можно вызвать действием раствора роданистого калия (KCNS) на клетку чешуи лука. Анионы CNS проникают в клетку и вызывают набухание мезоплазмы, внутрь вакуоли они не проникают. Мезоплазма при этом становится хорошо заметной в виде колпачков на полюсах плазмолизированного протопласта. Отсюда данный тип плазмолиза получил название колпачкового плазмолиза.
Колпачковый плазмолиз обнаруживает первый тип проницаемости цитоплазмы, когда проникшее вещество связывается самой цитоплазмой и не поступает в вакуоль.
Другой тип проницаемости цитоплазмы связан с проникновением вещества в вакуоль. Далеко не все растворы вызывают долго длящийся плазмолиз. Если плазмолизировать протопласт клетки раствором мочевины или глицерина, то сначала наблюдается плазмолиз. Затем плазмолиз сравнительно быстро заканчивается. Мочевина и глицерин быстро проникают внутрь вакуоли, увеличивают концентрацию клеточного сока, который начинает поглощать воду из окружающего раствора. При этом цитоплазма вновь подходит к стенкам клетки. Это явление получило название деплазмолиза, и такой плазмолиз называется временным.
Проникновение вещества в вакуоли клетки можно наблюдать на примере действия красителя метиленового синего (водный раствор 1:5000) на какое-нибудь водное растение, например элодею. Краситель скопляется внутри вакуолей, и очень часто в них даже образуется осадок из красителя, связанного с дубильными веществами вакуолей.
Проницаемость цитоплазмы связана с активной жизнедеятельностью (дыханием) растения. Поступление веществ (солей или, вернее, их катионов и анионов) в цитоплазму идет за счет обмена их на ионы, выходящие из клетки. Это происходит таким образом, что образованные в процессе дыхания Н+ и НСОз (ионы угольной кислоты) выделяются в окружающий раствор, а на их место в цитоплазму поступают ионы калия и натрия вместо ионов водорода, а на место иона НСОз— соответственные анионы.
Не всегда вещества проникают в цитоплазму за счет ее активной жизнедеятельности. Дело в том, что поверхностные слои цитоплазмы богаты липидами, которые не образуют сплошной пленки на поверхности цитоплазмы, а чередуются с молекулами белков или вкраплены в белковый остов поверхностных слоев, т. е. на поверхности цитоплазмы образуется своеобразная мозаика из участков белков и липидов. Растворимые в липидах вещества (спирт, эфир, хлороформ и др.) очень легко проникают в цитоплазму.
Вода и соли, нерастворимые в липидах, проникают в цитоплазму через белковые слои.
Проницаемость цитоплазмы не остается постоянной в течение жизни растения, а меняется с возрастом, а также увеличивается при повышении температуры и интенсивности освещения.
Движение цитоплазмы играет большую роль в жизнедеятельности растительного организма, способствуя перемещению веществ из одной клетки в другую.
Вязкость — одно из важнейших свойств цитоплазмы. Она очень сильно колеблется в зависимости от вида растения, а также от фаз его развития. У некоторых растений вязкость цитоплазмы немного превышает вязкость воды, а у других достигает вязкости глицерина, превосходящего в этом отношении воду в 87 раз. Вязкость цитоплазмы тесно связана с обменом веществ: чем выше вязкость, тем обычно менее интенсивен обмен. У созревших семян цитоплазма переходит в студенистое состояние — гель. Высокая вязкость цитоплазмы способствует увеличению устойчивости растений к повышенной температуре.
50. Влияние факторов среды на поглотительную деятельность корневой системы.
Поглощение растениями питательных веществ в большой степени зависит от свойств почвы — реакции и концентрации почвенного раствора, температуры, аэрации, влажности, содержания в почве доступных форм питательных веществ, продолжительности и интенсивности освещения и других условий внешней среды. Поступление питательных веществ в растение заметно снижается при плохой аэрации почвы, низкой температуре, избытке или резком недостатке влаги в почве. Особенно сильное влияние на поступление питательных веществ оказывают реакция почвенного раствора, концентрация и соотношение солей в нем. При избыточной концентрации солей в почвенном растворе (например, в засоленных почвах) поглощение растениями воды и питательных веществ резко замедляется.
Корни растений имеют очень высокую усвояющую способность и могут поглощать питательные вещества из сильно разбавленных растворов.
Важное значение для нормального развития корней имеет также соотношение солей в растворе, его физиологическая уравновешенность. Физиологически уравновешенным называется раствор, в котором отдельные питательные вещества находятся в таких соотношениях, при которых происходит наиболее эффективное использование их растением. Раствор, представленный какой-либо одной солью, физиологически неуравновешен.
Одностороннее преобладание (высокая концентрация) в растворе одной соли, особенно избыток какого-либо одновалентного катиона, оказывает вредное действие на растение. Развитие корней происходит лучше в многосолевом растворе. В нем проявляется антагонизм ионов, каждый ион взаимно препятствует избыточному поступлению другого иона в клетки корня. Например, Са 2+ в высоких концентрациях тормозит избыточное поступление K + , Na + или Mg 2+ и наоборот. Такие же антагонистические отношения существуют и для ионов K + и Na + , K + и NH4 + , K + и Mg 2+ , NO3 - и H2PO4, Cl - и H2PO4 - и др.
Физиологическая уравновешенность легче всего восстанавливается при введении в раствор солей кальция. При наличии кальция в растворе создаются нормальные условия для развития корневой системы, поэтому в искусственных питательных смесях Са 2+ должен преобладать над другими ионами.
Особенно сильно ухудшается развитие корней и поступление в них питательных веществ при высокой концентрации ионов водорода, т.е. при повышенной кислотности раствора. Высокая концентрация в растворе ионов водорода оказывает отрицательное влияние на физико-химическое состояние цитоплазмы клеток корня. Наружные клетки корня ослизняются, нарушается их нормальная проницаемость, ухудшается рост корней и поглощение ими питательных веществ. Отрицательное действие кислой реакции сильнее проявляется при отсутствии или недостатке других катионов, особенно кальция, в растворе Кальций тормозит поступление ионов H + , поэтому при повышенном количестве кальция растения способны переносить более кислую реакцию, чем без кальция.
Реакция раствора оказывает влияние на интенсивность поступления отдельных ионов в растение и обмен веществ. При кислой реакции повышается поступление анионов (вместе с ионами Н + ), но затрудняется поступление катионов, нарушается питание растений кальцием и магнием и тормозится синтез белка, подавляется образование сахаров в растении. При щелочной реакции усиливается поступление катионов и затрудняется поступление анионов.
Основной запас питательных веществ находится в почве в форме различных труднорастворимых соединений, для усвоения которых необходимо активное воздействие корней на твердую фазу почвы и тесный контакт между корнями и частицами почвы. В процессе жизнедеятельности растений корни выделяют в окружающую среду углекислоту и некоторые органические кислоты, а также ферменты и другие органические вещества. Под влиянием этих выделений, концентрация которых бывает особенно высокой в зоне непосредственного контакта корней с частицами почвы, происходит растворение содержащихся в ней минеральных соединений фосфора, калия и кальция, вытеснение в раствор катионов из поглощенного почвой состояния, высвобождение фосфора из его органических соединений.
Питательные вещества наиболее активно усваиваются растениями из той части почвы, которая находится в непосредственном контакте с корнями. Поэтому все мероприятия, способствующие лучшему развитию корней (хорошая обработка почвы, известкование кислых почв и т.д.), обеспечивают и лучшее использование растениями питательных веществ из почвы.
Питание растений осуществляется при тесном взаимодействии с окружающей средой, в том числе с огромным количеством разнообразных микроорганизмов, населяющих почву. Количество микроорганизмов особенно велико в ризосфере, т.е. в той части почвы, которая непосредственно соприкасается с поверхностью корней. Используя в качестве источника пищи и энергетического материала корневые выделения, микроорганизмы активно развиваются на корнях и вблизи них и способствуют мобилизации питательных веществ почвы.
Ризосферные и почвенные микроорганизмы играют важную роль в превращении питательных веществ и вносимых в почву удобрений. Микроорганизмы разлагают находящиеся в почве органические вещества и вносимые органические удобрения, в результате чего содержащиеся в них элементы питания переходят в усвояемую для растений минеральную форму. Некоторые микроорганизмы способны разлагать труднорастворимые минеральные соединения фосфора и калия и переводить их в доступную для растений форму. Ряд бактерий, усваивая молекулярный азот воздуха, обогащает почву азотом. С жизнедеятельностью микроорганизмов связано также образование в почве гумуса.
При определенных условиях в результате деятельности микроорганизмов питание и рост растений могут ухудшаться. Микроорганизмы, как и растения, потребляют для питания и построения своих тел азот и зольные элементы, т.е. являются конкурентами растений в использовании минеральных веществ. Не все микроорганизмы полезны для растений. Некоторые из них выделяют ядовитые для растений вещества или являются возбудителями различных заболеваний. В почве имеются также микробы, восстанавливающие нитраты до молекулярного азота (денитрификаторы), в результате их деятельности происходят потери азота из почвы в газообразной форме.
В связи с этим одна из важных задач земледелия — создание соответствующими приемами агротехники благоприятных условий для развития полезных микроорганизмов и ухудшение условий для развития вредных.
90. Каротиноиды, их физиологическая роль.
Наряду с зелеными пигментами в хлоропластах и хроматофорах содержатся пигменты, относящиеся к группе каротиноидов. Каротиноиды — это желтые и оранжевые пигменты алифатического строения, производные изопрена. Каротиноиды содержатся во всех высших растениях и у многих микроорганизмов. Это самые распространенные пигменты с разнообразными функциями. Каротинойды, содержащие кислород, получили название ксантофиллы. Основными представителями каротиноидов у высших растений являются два пигмента — каротин (оранжевый) и ксантофилл (желтый). Каротин состоит из 8 изопреновых остатков. При разрыве углеродной цепочки пополам и образовании на конце спиртовой группы каротин превращается в 2 молекулы витамина А. Обращает на себя внимание сходство в структуре фитоласпирта, входящего в состав хлорофилла, и углеродной цепочки, соединяющей пионовые кольца каротина. Предполагается, что фитол возникает как продукт гидрирования этой части молекулы каротиноидов. Поглощение света каротиноидами, их окраска, а также способность к окислительно-восстановительным реакциям обусловлены наличием конъюгированных двойных связей, b каротин имеет два максимума поглощения, соответствующие длинам волн 482 и 452 нм. В отличие от хлорофиллов каротиноиды не поглощают красные лучи, а также не обладают способностью к флуоресценции. Подобно хлорофиллу каротиноиды в хлоропластах и хроматофорах находятся в виде нерастворимых в воде комплексов с белками.
Цель: определить время наступления фаз плазмолиза.
Теоретические сведения
Плазмолиз – отставание цитоплазмы от стенок клетки, помещенной в раствор с большей концентрацией, чем концентрация клеточного сока (гипертонический раствор). В ходе плазмолиза очертания поверхности меняются: сначала она сокращается, а после полной потери тургора протопласт отстает от клеточной стенки по углам (уголковый плазмолиз), затем во многих местах (вогнутый плазмолиз) и, наконец, протопласт округляется (выпуклый плазмолиз).
Временем плазмолиза называется период, который проходит с момента погружения ткани растения в раствор плазмолитика до наступления выпуклого плазмолиза. Этот показатель может характеризовать вязкость цитоплазмы: чем больше время плазмолиза, тем выше вязкость цитоплазмы.
Катионы и анионы солей оказывают специфическое и многообразное действие на цитоплазму. Одним из заметных внешних проявлений этого действия являются изменения в степени набухания и вязкости цитоплазмы, для наблюдения за которыми используют время плазмолиза.
Ход работы:Срез эпидермиса с выпуклой поверхности чешуи цветного лука помещают в каплю раствора испытуемой соли, накрывают покровным стеклом и сейчас же приступают к рассматриванию под микроскопом. Следят за сменой форм плазмолиза. Определяют время плазмолиза в каждой соли. Результаты опыта записывают по форме:
| Вариант | Соль | Концентрация раствора | Время погружения ткани в раствор | Время наступления выпуклого плазмолиза | Время плазмолиза (мин.) |
| Ca(NO3)2 | 0.7 | ||||
| KNO3 | 1.0 | ||||
| KCNS | 1.0 |
На основании полученных результатов делают выводы о влиянии катионов и анионов на вязкость цитоплазмы.
Оборудование:луковица синего лука; растворы на дистиллированной воде: 1 М KNO3, 0,7 М Ca(NO3)2 ,1 М KCNS , скальпель, лезвие бритвы, препаровальная игла, микроскоп, Предметные и покровные стекла; карандаш по стеклу; фильтровальная бумага.
Литература:1, с.19
Контрольные вопросы:
1 Известно, что через клеточные мембраны проникают как вода, так и многие растворенные вещества. Почему тем не менее можно говорить о полупроницаемости мембран, хоть и не идеальной?
2 Какая мембрана обладает более низкой проницаемостью для растворенных веществ – плазмолемма или тонопласт?
Тема 2 Определение осмотического давления клеточного сока плазмолитическим методом
Цель:определить изотоническую концентрацию и вычислить осмотическое давление клеточного сока по уравнению Вант-Гоффа
Теоретические сведения
Клеточный сок – водный раствор различных органических и неорганических веществ. Потенциальное осмотическое давление зависит от числа частиц, находящихся в этом растворе, т.е. от концентрации и степени диссоциации растворенных молекул. Потенциальное осмотическое давление выражает максимальную способность всасывать воду. Величина этого показателя указывает на возможность произрастания растения на почвах различной водоудерживающей силы. Повышение осмотического давления клеточного сока при засухе является критерием обезвоживания растений и необходимости полива.
Данный метод основан на подборе такой концентрации наружного раствора, которая вызывает начальный (уголковый) плазмолиз в клетках исследуемой ткани. В этом случае, осмотическое давление раствора примерно равно осмотическому давлению клеточного сока. Такой раствор называется изотоническим.
Ход работы:В бюксы готовят по 10мл. 0,7М; 0,6М; 0,5М; 0,4М; 0,3М; 0,2М, растворов сахарозы путем разбавления 1M раствора дистиллированной водой. Растворы тщательно перемешивают. Бюксы закрывают крышками, чтобы предотвратить испарение, и ставят в ряд убывающей концентрации растворов.
Лезвием безопасной бритвы делают тонкие срезы с выпуклой поверхности чешуи лука размером примерно 25 мм 2 из среднего хорошо окрашенного участка.
В каждый бюкс, начиная с высокой концентрации, с интервалом в 3 мин. опускают по 2-3 среза. Через 30 мин. после погружения срезов в первый бюкс исследуют их под микроскопом. Затем, через каждые 3 мин. наблюдают под микроскопом срезы из последующих бюксов. Этим достигается равная продолжительность пребывания срезов в растворах плазмолитиков. Рассматривать срезы под микроскопом следует в капле раствора из того бюкса, откуда был взят срез.
Определяют степень плазмолиза клетки в каждом растворе и находят изотоническую концентрацию как среднее арифметическое между концентрацией, при которой плазмолиз только начинается, и при которой уже вызывает плазмолиз.
Результаты опыта записывают по форме таблицы
| Концентрация растворов сахарозы, М | На 10 мл раствора | Продолжительность пребывания срезов в растворе | Степень плазмолиза | Изотоническая концентрация, М | Потенциальное осмотическое давление, кПа |
| IМ сахарозы | воды, мл | время погружения | время наблюдения | ||
| 0,7 | |||||
| 0,6 | |||||
| 0,5 | |||||
| 0,4 | |||||
| 0,3 | |||||
| 0,2 |
Величину потенциального осмотического давления (в кПа) рассчитывают по формуле:
П = R*T*c*i*101,3;
где R – газовая постоянная, равная 0,0821л атм./град моль;
Т – абсолютная температура (273 о С + комнатная);
с – изотоническая концентрация в молях;
i – изотонический коэффициент Вант-Гоффа;
101,3 – множитель для перевода атмосфер в килопаскали.
Коэффициент Вант-Гоффа характеризует ионизацию растворов и для неэлектролитов (сахароза) равен 1.
Оборудование: луковица синего лука; 1 М раствор сахарозы, скальпель, лезвие бритвы, препаровальная игла, микроскоп, предметные и покровные стекла; карандаш по стеклу; фильтровальная бумага, пробирки (бюксы).
Литература: 1, с. 16-18.
Контрольные вопросы:
1 Что такое плазмолиз и каковы его причины?
2 Как происходит деплазмолиз?
3 Способны ли плазмолизироваться мертвые клетки?
Цель: определить время наступления фаз плазмолиза.
Теоретические сведения
Плазмолиз – отставание цитоплазмы от стенок клетки, помещенной в раствор с большей концентрацией, чем концентрация клеточного сока (гипертонический раствор). В ходе плазмолиза очертания поверхности меняются: сначала она сокращается, а после полной потери тургора протопласт отстает от клеточной стенки по углам (уголковый плазмолиз), затем во многих местах (вогнутый плазмолиз) и, наконец, протопласт округляется (выпуклый плазмолиз).
Временем плазмолиза называется период, который проходит с момента погружения ткани растения в раствор плазмолитика до наступления выпуклого плазмолиза. Этот показатель может характеризовать вязкость цитоплазмы: чем больше время плазмолиза, тем выше вязкость цитоплазмы.
Катионы и анионы солей оказывают специфическое и многообразное действие на цитоплазму. Одним из заметных внешних проявлений этого действия являются изменения в степени набухания и вязкости цитоплазмы, для наблюдения за которыми используют время плазмолиза.
Ход работы:Срез эпидермиса с выпуклой поверхности чешуи цветного лука помещают в каплю раствора испытуемой соли, накрывают покровным стеклом и сейчас же приступают к рассматриванию под микроскопом. Следят за сменой форм плазмолиза. Определяют время плазмолиза в каждой соли. Результаты опыта записывают по форме:
| Вариант | Соль | Концентрация раствора | Время погружения ткани в раствор | Время наступления выпуклого плазмолиза | Время плазмолиза (мин.) |
| Ca(NO3)2 | 0.7 | ||||
| KNO3 | 1.0 | ||||
| KCNS | 1.0 |
На основании полученных результатов делают выводы о влиянии катионов и анионов на вязкость цитоплазмы.
Оборудование:луковица синего лука; растворы на дистиллированной воде: 1 М KNO3, 0,7 М Ca(NO3)2 ,1 М KCNS , скальпель, лезвие бритвы, препаровальная игла, микроскоп, Предметные и покровные стекла; карандаш по стеклу; фильтровальная бумага.
Литература:1, с.19
Контрольные вопросы:
1 Известно, что через клеточные мембраны проникают как вода, так и многие растворенные вещества. Почему тем не менее можно говорить о полупроницаемости мембран, хоть и не идеальной?
2 Какая мембрана обладает более низкой проницаемостью для растворенных веществ – плазмолемма или тонопласт?
Тема 2 Определение осмотического давления клеточного сока плазмолитическим методом
Цель:определить изотоническую концентрацию и вычислить осмотическое давление клеточного сока по уравнению Вант-Гоффа
Теоретические сведения
Клеточный сок – водный раствор различных органических и неорганических веществ. Потенциальное осмотическое давление зависит от числа частиц, находящихся в этом растворе, т.е. от концентрации и степени диссоциации растворенных молекул. Потенциальное осмотическое давление выражает максимальную способность всасывать воду. Величина этого показателя указывает на возможность произрастания растения на почвах различной водоудерживающей силы. Повышение осмотического давления клеточного сока при засухе является критерием обезвоживания растений и необходимости полива.
Данный метод основан на подборе такой концентрации наружного раствора, которая вызывает начальный (уголковый) плазмолиз в клетках исследуемой ткани. В этом случае, осмотическое давление раствора примерно равно осмотическому давлению клеточного сока. Такой раствор называется изотоническим.
Ход работы:В бюксы готовят по 10мл. 0,7М; 0,6М; 0,5М; 0,4М; 0,3М; 0,2М, растворов сахарозы путем разбавления 1M раствора дистиллированной водой. Растворы тщательно перемешивают. Бюксы закрывают крышками, чтобы предотвратить испарение, и ставят в ряд убывающей концентрации растворов.
Лезвием безопасной бритвы делают тонкие срезы с выпуклой поверхности чешуи лука размером примерно 25 мм 2 из среднего хорошо окрашенного участка.
В каждый бюкс, начиная с высокой концентрации, с интервалом в 3 мин. опускают по 2-3 среза. Через 30 мин. после погружения срезов в первый бюкс исследуют их под микроскопом. Затем, через каждые 3 мин. наблюдают под микроскопом срезы из последующих бюксов. Этим достигается равная продолжительность пребывания срезов в растворах плазмолитиков. Рассматривать срезы под микроскопом следует в капле раствора из того бюкса, откуда был взят срез.
Определяют степень плазмолиза клетки в каждом растворе и находят изотоническую концентрацию как среднее арифметическое между концентрацией, при которой плазмолиз только начинается, и при которой уже вызывает плазмолиз.
Результаты опыта записывают по форме таблицы
| Концентрация растворов сахарозы, М | На 10 мл раствора | Продолжительность пребывания срезов в растворе | Степень плазмолиза | Изотоническая концентрация, М | Потенциальное осмотическое давление, кПа |
| IМ сахарозы | воды, мл | время погружения | время наблюдения | ||
| 0,7 | |||||
| 0,6 | |||||
| 0,5 | |||||
| 0,4 | |||||
| 0,3 | |||||
| 0,2 |
Величину потенциального осмотического давления (в кПа) рассчитывают по формуле:
П = R*T*c*i*101,3;
где R – газовая постоянная, равная 0,0821л атм./град моль;
Т – абсолютная температура (273 о С + комнатная);
с – изотоническая концентрация в молях;
i – изотонический коэффициент Вант-Гоффа;
101,3 – множитель для перевода атмосфер в килопаскали.
Коэффициент Вант-Гоффа характеризует ионизацию растворов и для неэлектролитов (сахароза) равен 1.
Оборудование: луковица синего лука; 1 М раствор сахарозы, скальпель, лезвие бритвы, препаровальная игла, микроскоп, предметные и покровные стекла; карандаш по стеклу; фильтровальная бумага, пробирки (бюксы).
Литература: 1, с. 16-18.
Контрольные вопросы:
1 Что такое плазмолиз и каковы его причины?
2 Как происходит деплазмолиз?
3 Способны ли плазмолизироваться мертвые клетки?

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.


Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.
Нашёл интересный опыт. Имея микроскоп мне кажется можно по форме плазмолиза определить есть перебор по калию или кальцию.
Цель:
Определить влияние ионов калия и кальция на форму плазмолиза.
Описание самого опыта:
Взять два чистых предметных стекла, капнуть на одно из них 1M KNO3? на другое – 1M Ca(NO3)2, в каждую каплю поместить лист элодеи
накрыть покровным стеклом. Через пять-десять минут рассмотреть препараты под микроскопом, сначала на малом, потом на большом увеличении. Найти участки с плазмолизированными клетками, зарисовать клетки в состоянии плазмолиза.
Результат :
В растворе нитрата калия возникает главным образом выпуклый плазмолиз (см. рисунок 13Г), в растворе нитрата кальция – судорожный плазмолиз (см. рисунок 13Д).
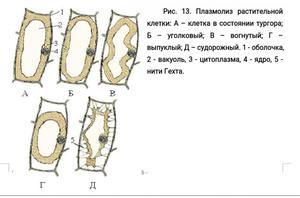
Ион калия (очень медленно по сравнению с водой проходящий через мембрану за счет наличия калиевых каналов) уменьшает вязкость цитоплазмы, способствуя ее отделению от клеточной стенки, вследствие чего возникает выпуклый плазмолиз. Ион кальция, напротив, повышает вязкость цитоплазмы, увеличивая силы ее сцепления с клеточной стенкой, что вызывает преимущественно судорожный плазмолиз.
Оба описанных вида плазмолиза обычно предваряются вогнутым плазмолизом.
Изменено 30.7.16 автор Ananas72
Когда стали понятны такие моменты как плазмолиз и деплазмолиз рассмотрим тот момент когда аквариумисту предложено ни чего не предпринимать, а просто пересилить себя и немножко подождать.
Опытным путем можно при помощи микроскопа отслеживать проницаемость клеточных мембран для различных веществ. Мы рассмотрим на примере мочевины.
Капаем на стекло каплю 1М мочевины и помещаем туда листок элодеи накрываем покровным стеклом. Через небольшой промежуток времени мы получим плазмолиз.
Далее в растворе мочевины по прошествии некого промежутка времени происходит деплазмолиз, так как плазмалемма обладает проницаемостью для мочевины (хотя меньшей, чем для воды, поэтому плазмолиз изначально возникает), и постепенно мочевина проходит в клетку. За ней внутрь клетки следует вода, обеспечивающая тургорное давление – возникает деплазмолиз.
Вывод:
Если что-то не так пошло в аквариуме не так, аквариумисту нужно просто связать руки))), а не вносить ещё и ещё удобрения чтоб стало лучше.

Привет,
пожалуйста, проведите ликбез!
Фотка от 4.10, прозерпинаки уже нет. r.i.p.
Аква 125 литров, воды 100 литров, грунт кварц, посадка средняя, газ-баллон по таймеру днем, свет средний лл, удо аквабаланс макро npk и микро - 2-3 мл., 2-3 раза в неделю, вода для подмен осмос:водопровод (3:1, kh-4, gh-9, ph-7).
Три недели назад стал добавлять при подменах аква-бустер в минимальной дозе, увеличивая kh до 5. Вносил дополнительно калий по 5мл.
Проблема: остановка роста, прекратилось пузыряние, закрутило листы у прозерпинаки, при этом размеры листьев не изменились, впоследствии отмирание точек роста и не только у прозерпинаки; трипартита желтеет, отпадают целые листочки; амания бонсай - отмирание точек роста.
Сделал три подмены 80 литров в течение недели, без бустера (в подменной воде калий - 2), замерил после подмен в акве калий - 25.
Откуда . И что делать. И как жить дальше? Последний вопрос риторический
Изменено 17.10.17 автор Sagall
Изменено 17.10.17 автор Sagall
Привет. А зачем аквариум бустер? Вроде вода и так нормик. Надо поделать подмены по 50% раза три без внесения удо и посмотреть что будет с калием.
Пытался кальций компенсировать, периодически альтернатеру крутило, а прозерпинаку постоянно.
Значит калий в такой воде в концентрации 20-25 это уже предел, получается? Надо снижать и стараться держать около 10-15?
И микро уменьшить чуток, поскольку усваивается лучше?
Изменено 18.10.17 автор Sagall
1653 802
18 час.
Тоже нашёл этот опыт на элодеи. Там ещё было показано, избирательность транспорта через проницаемую мембранну, где ионы натрия и калия, повышают проницаемость, а кальци и магния, в противоположность-понижают. Интересно, а другие соли так же могут вызвать плазмолиз в клетке и как он выглядит на растениях, радикулит или отмирание точек роста и ещё как?
Плазмолиз происходит от повышение концентрации солей в растворе. Значимое изменения в нашем случае могут вызвать только макроэлементы.
1653 802
18 час.
Понимаю, что нет возможности давать лекции заблудшим, но можно ли Ваше мнение услышать кратко, по следующему утверждению.
В воде с параметрами kh-5, gh-10, ph-7.5 (тесты капельные нилпа), недостаток кальция для растений маловероятен, поскольку показатели тестов свидетельствуют о достаточной концентрации в воде и кальция и магния?
Ищите проблему в микро.
Ясно, спасибо за ответ.
Кстати, использую макро NPK (Premium), а микро (основная серия), видимо они несовместимы.
Сравним составы Микро премиум Kh>4: ! Микро (основная серия)
Fe(фумарат, глюконат, глицинат) – 3200 мг ! Fe - 2000 мг
Mn(глицинат) – 800 мг ! Mn - 300 мг
Zn(глицинат) – 8 мг ! Zn - 100 мг
В – 140 мг ! B - 90 мг
Cu(глицинат) – 4 мг ! Cu - 25 мг
Mo – 10 мг ! Mo - 20 мг
Аминокислоты – 6600 мг ! Карбоновые кислоты, витамины
__________________________________________________________________
Бор?/Марганец?/Железо?
Признаки голодания:
- Недостаток железа приводит к тому, что не образуется хлорофилл. листья желтеют, особенно молодые, в которых вообще не образуется хлорофилл.
Все эти признаки являются приблизительными, к тому же одновременно может отсутствовать несколько элементов в достаточном количестве.
- Бор (усиливается при недостатке магния) почернение и гибель точек роста, хлороз от основания и краев. Искривление и гибель. Мертвые кончики отростков, боковые отростки тоже отмирают. Хрупкость стеблей. Признаки подобные недостатку кальция.
- При недостатке марганца наблюдается хлороз между жилками листа - на верхних листьях между жилками появляются желтовато-зеленые или желтовато-коричневые пятна, жилки остаются зелеными, что придает листу пестрый вид. В дальнейшем участки хлорозных тканей отмирают, при этом появляются пятна различной формы и окраски. Признаки недостатка появляются прежде всего на молодых листьях и в первую очередь у основания листьев, а не на кончиках, как при недостатке калия.
Признаки избытка:
- Симптомы избытка железа такие же, как и при дефиците: между жилками развивается хлороз, позже листья желтеют и бледнеют (данные для наземных растений).
- Избыток марганца проявляется в виде межжилкового хлороза молодых листьев, которые бледнеют и желтеют. Появляются темно-бурые или почти белые некротические пятна. На пораженных листьях могут появиться мелкие красно-бурые точки. В отличие от недостатка марганца, при его избытке листья искривляются и сморщиваются.
- Бор. Листья желтеют и деформируются, могут заворачиваться вниз и принимать куполообразную форму. Анализ содержания бора в растении показывает, что он накапливается в значительно большем количестве в старых тканях растений, поэтому вначале поражаются старые листья. Верхушка растений сначала имеет нормальный вид, затем скручивается вместе с поврежденными листьями. Признаки поражения верхушки и молодых листьев в запущенных случаях токсического действия бора может быть ошибочно принята за недостаток этого элемента.
Блин, вместе с избытком калия еще и избыток бора. Потому что у меня действительно листья прозерпинаки вначале начинали деформироваться и заворачиваться вниз, принимали куполообразную форму, а потом нижние листья стали опадать, после все верхушки почернели, а если учесть мягкость воды, то сомнения отпадают.
Откровенно говоря, производитель (Аквабаланс) мог бы без ущерба бизнесу, но с пользой для маркетинга и аквариумистов, дать немного больше информации о своих продуктах, хотя бы достаточных для примерного понимания способов их применения, примерного понимания их состава, взаимодействия друг с другом.

Анионы – хлорид анион, гидрокарбонат анион, гидрофосфат анион, дигидрофосфат анион, карбонат анион, фосфат анион и нитрат анион.
Рассмотрим значение ионов.
Ионы, располагаясь по разные стороны клеточных мембран, образуют так называемый трансмембранный потенциал . Многие ионы неравномерно распределены между клеткой и окружающей средой. Так, концентрация ионов калия (К + ) в клетке в 20–30 раз выше, чем в окружающей среде; а концентрация ионов натрия (Na + ) в десять раз ниже в клетке, чем в окружающей среде.

- Катионы влияют на вязкость и текучесть цитоплазмы.
Ионы калия(К ) уменьшают вязкость и увеличивают текучесть,
ионы кальция (Са 2+ ) обладают противоположным действием на цитоплазму клетки.
рН среды и роль ионов в его поддержании
Значение pH в клетке примерно равняется 7.
Изменение pH в ту или иную сторону губительно действует на клетку, поскольку сразу же изменяются биохимические процессы, проходящие в клетке.
Постоянство pH клетки поддерживается благодаря буферным свойствам её содержимого.
Буферным называют раствор, который поддерживает постоянное значение pH среды . Обычно буферная система состоит из сильного и слабого электролита: соли и слабого основания или слабой кислоты, которые её образуют
Действие буферного раствора заключается в том, что он противостоит изменениям pH среды. Изменение pH среды может возникнуть вследствие концентрирования раствора или разбавления его водой, кислотой или щелочью.

рН среды и роль ионов в его поддержании
рН среды и роль ионов в его поддержании
Некоторые органические соединения, в частности белки, также обладают буферными свойствами.
Катионы магния, кальция, железа, цинка, кобальта, марганца входят в состав ферментов и витаминов
Катионы металлов входят в состав гормонов.
Цинк входит в состав инсулина. Инсулин – это гормон поджелудочной железы, который регулирует уровень глюкозы в крови.
Магний входит в состав хлорофилла.
Железо входит в состав гемоглобина.
При недостатке этих катионов нарушается процессы жизнедеятельности клетки
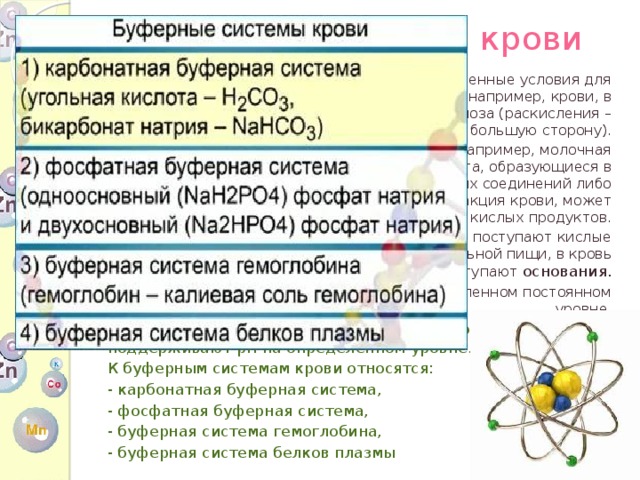
Буферная система крови
В организме человека всегда имеются определенные условия для сдвига нормальной реакции среды ткани, например, крови, в сторону ацидоза (закисления) или алкалоза (раскисления – смещения рН в большую сторону).
В кровь поступают различные продукты, например, молочная кислота, фосфорная кислота, сернистая кислота, образующиеся в результате окисления фосфорорганических соединений либо серосодержащих белков. При этом реакция крови, может сдвигаться в сторону кислых продуктов.
При употреблении мясных продуктов, в кровь поступают кислые соединения. При употреблении растительной пищи, в кровь поступают основания.
Тем не менее, pH крови остается на определенном постоянном уровне.
В крови имеются буферные системы , которые поддерживают pH на определенном уровне.
К буферным системам крови относятся:
- карбонатная буферная система,
- фосфатная буферная система,
- буферная система гемоглобина,
- буферная система белков плазмы

Спасибо за внимание

-75%
Читайте также:

