Теория соматических мутаций старения кратко
Обновлено: 04.07.2024
Скорость мутации
Ну, во-первых, отметим, что частота возникновения мутаций не высока невероятно низка и индивидуальна для разных видов. В целом, при оценке скорости мутаций (я буду выкидывать первые цифры указывая лишь порядок), указывают на 10 -6 – 10 -10 мутации на основание, такой большой разброс как раз и объясняется видовой специфичностью. С другой стороны, самих нуклеотидов в ДНК грубо от 10 4 (вирусы) до 10 9 (хордовые), ещё учтём количество клеток – например в человеке порядка 10 14 клеток, так что не питайте иллюзий мутации есть у всех, хоть их и не так много, как некоторые думают.
А вот дальше начинается магия, о которой так любил рассуждать Мастер Угвэй из известного мультика про панду: случайности не случайны. Ради экономии места и времени давайте сразу отбросим не интересующую нас часть мутаций – генеративных (не то что бы они как то существенно (качественно) отличались, но там творится дополнительная магия, а влияют эти мутации лишь на потомство), нас интересуют соматические мутации – те которые могут влиять на нас сразу.
Что-то я отвлёкся, вернёмся к нашим мутациям. Есть участки ДНК защищённые сильнее обычного, а наоборот? Конечно, есть!
Дело в том, что я хотел снова впечатлить вас порядками и разбросами цифр, но сам я этих цифр не могу вспомнить как не старался. Конечно, я полез в интернет, но получасовое гугление результата не принесло.
Я надеюсь, из описания очевидно, что консервативными становятся те гены, которые критически важны для организма, их защита в общем-то логична и напрашивается сама собой.
Процесс гипермутирования был открыт и лучше всего изучен на примере работы иммунной системы позвоночных. Не буду отходить от классики и расскажу вам всё на том же примере. Помните в первой части я писал, что биосистемы используют хаос себе во благо, а не борются с ним (или как-то так ), так вот это один из ярчайших примеров.
Обычно эволюционный подбор антигена занимает 5-10 дней (а вы сколько болеете гриппом?). Частота мутаций при иммунном ответе составляет 10 -3 – 10 -4 (вернитесь к цифрам выше посмотрите на разницу в порядках), но это цифра на основание в расчёте на всю ДНК. Если же рассматривать конкретный ген (а ещё лучше конкретные локусы) то мутация происходит со 100% вероятностью (ну ладно пусть будет 95% что бы точно вас не обмануть) на деление клетки.
Подобьём промежуточный итог.
- Очевидно, что биологические системы способны в той или иной степени управлять собственным мутагенезом.
- В геноме мутации распределены не равномерно.
- Биосистемы могут запускать и управлять эволюционным процессом.
Экспрессия гена
Вся беда в том, что большинство людей представляют себе синтез белка как-то так: n_Кодон ДНК > n_Кодон РНК > n_аминокислот = белок. Или так:
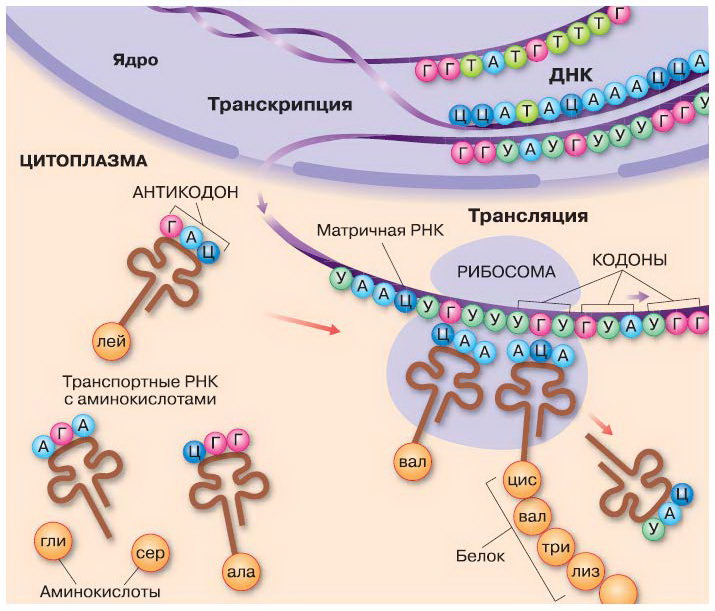

Если испортился старт (промоутер) или регулятор перед стартом, то ген вероятно потеряет активность и белок синтезироваться не будет.
Возможна такая мутация регуляторных участков (например, мотивов), при которых ускорится или замедлится синтез.
Но возможно, что наша мутация случилась именно в кодируемой части гена.
И так мы получили мРНК (иРНК), пора бы получить белок. Но это позже – мы всё-таки не получили мРНК, введём ещё парочку действующих лиц. После транскрипции мы получили пре-мРНК, дальше она должна созреть (в годы моего обучения это прям так и назвалось, сейчас более модное и устоявшееся название – процессинг РНК (или ещё страшнее посттранскрипционные модификации РНК)), сюда входят:
- кэпирование защищающее РНК от необоснованной деградации, также обеспечивает транспорт (через мембраны ядра например), и участвует в следующих трёх словах;
- сплайсинг (выбрасывание лишних кодонов);
- редактирование, да белок может не совсем соответствовать кодонам ДНК, кодирующим его (не всегда есть);
- метилирование (не всегда есть).
Здесь будет уместным заметить, что процесс сплайсинга у одной и той же РНК может приводить к различным результатам, то есть на ДНК вы имеете одну последовательность которая кодирует сразу несколько белков. Другой интересной особенностью сплайсинга является то, что созревшая РНК может состоять из частей разных пре-РНК. Ну вы понимаете к чему я клоню?
Слава богу мы добрались до нашего мутантного белка. Почти добрались, ведь мы снова получили незрелый продукт. Белок должен ещё созреть или как теперь модно: должна пройти посттрансляционная модификация белка (понапридумывают новых словей изверги проклятые).
Не будем обсуждать кем и как этот процесс регулируется я думаю вы догадались.
Я даже не буду описывать этапы и виды созревания (если верить википедии на данный момент известно более 200 видов), нам здесь важнее понять, что же происходит с нашей полипептидной цепью. Самое интересное для нас то, что часть пептидов может быть выброшено (цепь стала ещё короче), часть заменена, к белку могут присоединяются различные химически активные группы. Кроме того, важный процесс, сворачивание белка (фолдинг) в правильную форму.
Почему-то мы не встречаем людей с заменой соседней аминокислоты, или там условно 10. Или мы не видим, что бы вместо глутаминовой кислоты или валина встречалась какая-то ещё аминокислота (замена происходит в первом нуклеотиде кодона – там есть из чего выбрать). Зато именно эта мутация встречается у вполне заметного количества населения. В конечном продукте (гемоглобине) мы имеем 146 аминокислот, а мутаций (и вместе с ней болезней) всего 9 видов. Где все прочие мутации? Вам не странно? Мне было бы странно если бы я считал, что мутации полностью случайны и накапливаясь убивают нас.
Но я снова отвлекаюсь, давайте уже добьём эту часть, нам осталось чуток.
Разбавь мутацию
Ещё одним своеобразным способом защиты от мутаций является многочисленное копирование генов. Важные для функционирования клетки гены могут повторятся сотни раз в разных местах, например тРНК у человека имеет около 500 копий, рРНК (рибосомная) около 300 копий, притом распределённых между пятью(!) разными хромосомами. То есть вы можете потерять хромосому целиком (бывает и такое), а рРНК всё равно сможет экспрессироваться. В классическом же случае мутации одной из копий гена, даже в случае синтеза неправильной РНК (белка) его разбавят правильные РНК (или белки) синтезирующиеся тут же в массе. Таким образом мутация нивелируется.
Аллели
На определённом этапе биосистемам показалось, что мутации слишком не предсказуемы, а потому опасны, с другой стороны, мутации обеспечивают пластичность фенотипическую и генофонда популяций, а потому потенциально очень полезны. Выход, как всегда, нашла эволюция, она взяла, да и удвоила наш генотип, а сверхсложная регуляция, описанная сверху, доделала дело организовав рецессивные и доминантные признаки.
Диплоидность (полиплоидность) выполняет (в том числе) элегантнейшую функцию по накоплению и плавному выводу мутаций в свет. Диплоидность означает наличие всех генов в двойном экземпляре, это приводит к интересным результатам. Практически любая мутация переводит ген в рецессивное состояние (вот теми самыми механизмами что описаны выше), то есть в такое состояние, когда мутантный ген не экспрессирует или экспрессирует с очень низкой скоростью. В то же время вторая копия гена (правильная) является доминантной и продолжает производить правильный белок. Это последний этап ограничения мутаций (который пришёл мне в голову), если не считать системы отчистки цитоплазмы и иммунитета.
Заключение
И так мы разобрали полный путь появления мутаций, и мне хочется надеяться, что в достаточно доходчивой форме. Конечно, всё написанное выше не означает, что мутации не происходят или все они в той или иной форме нейтральны. Естественно, часть мутаций пробиваются в наш фенотип и встраиваются в метаболические пути. Но утверждение, что достаточно редкие, разнонаправленные мутации у разных людей могут вызывать одинаковую реакцию организма (вспомните про маркеры старения) и так точно убивают нас на одном сроке, абсурдны с логической точки зрения. Кроме того, не стоит забывать, что по мимо геронтологов в нашем мире существуют и врачи, погуглите генетические заболевания, и вы увидите, что конкретные мутации вызывают конкретную реакцию фенотипа, мутации не усредняются, выдавая общий результат, они индивидуальны по характеру воздействия на организм.
Конечно, можно отмахнуться от моей стены текста и сказать, что в нашем организме появляются те мутации, которые мы не способны отследить и именно они и старят нас. Только вот бритва Оккама заставляет принять более простой путь, взять и признать, что старение – это часть процесса, который мы именуем онтогенезом или жизнью, и все его части (развитие зародыша, достижение половозрелости, старость) зашиты в нашей программе.
С практической точки зрения для нас важно то, что в теории мы можем бороться со старостью генетическими методами. Но методы эти должны быть на несколько порядков лучше того, что мы имеем сейчас. Человечеству надо разобраться в полных метаболических картах, нужно точно понимать, что и как влияет на экспрессию, нужно точно знать не просто что вот этот ген экспрессируется при таких-то условиях, а надо понимать какие и как белки и РНК в этом учувствуют, какой белок или РНК синтезируют и как именно и с помощью чего он созревает, и для чего он нужен. Этот путь мы только начинаем, а потому с этой стороны ждать эликсира бессмертия пока не стоит.
Я не хочу давать пустых предсказаний, но вы же всё равно захотите узнать моё мнение. Как кажется мне, при очень удачном развитии событий, которые включают в себя дальнейшее развитие нейронных сетей и машинного обучения или даже создание более полноценного ИИ, а также наращивание темпов исследований в генетике и молекулярной биологии, не раньше чем через лет 10 мы достигнем технологий, позволяющих приступить к созданию не стареющих людей (что потребует ещё какого-то времени). При плохом стечении обстоятельств, например, мы близки к потолку эффективности машинного обучения, будет как с термоядерным синтезом – через 15-20 лет в течении ближайшего столетия.
Достижение бессмертия через редактирование генома может столкнуться с этикой, и, надо сказать, повод для этого есть. Чтобы стереть программу старения, нам придётся существенно переписать ДНК, а значит надо решить, что в ДНК считать лишним, а что допустимым отклонением. Кто скажет, где провести грань? Что бы не быть многословным, просто представьте себе государство, где абсолютно законно (граждане сами за всё проголосуют ради здоровья и долголетия) каждый ребёнок оболванен по определённому шаблону. Например у него убрана агрессия, привито трудолюбие, вроде неплохо, но где черта? Например повышенная законопослушность (= послушность) это хорошо или уже плохо?
P.S. В этой статье я старался описывать молекулярную работу в общих чертах, характерных для всех видов, но для экономии места и облегчения понимания, а так же в виду необъятности разнообразия биосистем, многие примеры приведены и описывают работу генетического аппарата именно млекопитающих, или конкретно человека и не могут быть отнесены к другим группам животных.
P.P.S. Честно говоря, я думал, что в этой статье получится охватить ещё несколько аспектов с другой стороны вопроса не касающийся генетики напрямую, но оказывается в словах знания занимают гораздо больше места чем в моей голове. И снова остались не закрытые вопросы, и снова много того, о чём я даже не упомянул и естественно есть прочие (не генетические) пути продлить жизнь, и другие теории старения.
Но в своё оправдание могу сказать, что мы закрыли одну из обширнейших тем, хоть и бегло, хоть и без подробностей. Надеюсь было интересно.
2. Лобачев А.Н. Биогенез митохондрий при дифференциации и старении клеток. ВИНИТИ 19.09.85, №6756-В85 Деп., 1985, с. 28.
4. Руководство по геронтологии и гериатрии: Клиническая гериатрия / Под редакцией В.Н. Ярыгина, А.С. Мелентьева. М.: ГЭОТАР-МЕД, 2003. 523 с.
Сегодня существует несколько альтернативных теорий, которые отчасти противоречат друг другу, а отчасти – дополняют. Современная биология уделяет проблеме старения очень большое внимание, и с каждым годом появляются новые факты, позволяющие глубже понять механизмы этого процесса.
Молекулярно-генетические теории. Гипотеза, согласно которой причиной старения являются изменения генетического аппарата клетки, является одной из наиболее признанных в современной геронтологии. Молекулярно-генетические теории подразделяются на две большие группы. Одни ученые рассматривают возрастные изменения генома как наследственно запрограммированные. Другие считают, что старение – результат накопления случайных мутаций. Отсюда следует, что процесс старения может являться или закономерным результатом роста и развития организма, или следствием накопления случайных ошибок в системе хранения и передачи генетической информации.
Теория свободных радикалов. Практически одновременно выдвинутая Д. Харманом (1956) и Н.М. Эмануэлем (1958), свободнорадикальная теория объясняет не только механизм старения, но и широкий круг связанных с ним патологических процессов (сердечно-сосудистых заболеваний, ослабления иммунитета, нарушений функции мозга, катаракты, рака и некоторых других). Согласно этой теории, причиной нарушения функционирования клеток являются необходимые для многих биохимических процессов свободные радикалы – активные формы кислорода, синтезируемые главным образом в митохондриях – энергетических фабриках клеток. Если очень агрессивный, химически активный свободный радикал случайно покидает то место, где он нужен, он может повредить и ДНК, и РНК, и белки, и липиды. Природа предусмотрела механизм защиты от избытка свободных радикалов: кроме супероксиддисмутазы и некоторых других синтезируемых в митохондриях и клетках ферментов, антиоксидантным действием обладают многие вещества, поступающие в организм с пищей – в том числе витамины А, С и Е. Регулярное потребление овощей и фруктов и даже несколько чашек чая или кофе в день обеспечат вам достаточную дозу полифенолов, также являющихся хорошими антиоксидантами. К сожалению, избыток антиоксидантов – например, при передозировке биологически активных добавок – не только не полезен, но может даже усилить окислительные процессы в клетках.
Теория апоптоза. Академик В.П. Скулачев называет свою теорию теорией клеточного апоптоза. Апоптоз – процесс запрограммированной гибели клетки. Как деревья избавляются от частей, чтобы сохранить целое, так и каждая отдельная клетка, пройдя свой жизненный цикл, должна отмереть и ее место должна занять новая. Если клетка заразится вирусом, или в ней произойдет мутация, ведущая к озлокачествлению, или просто истечет срок ее существования, то, чтобы не подвергать опасности весь организм, она должна умереть. В отличие от некроза – насильственной гибели клеток из-за травмы, ожога, отравления, недостатка кислорода в результате закупоривания кровеносных сосудов и т.д., при апоптозе клетка аккуратно саморазбирается на части, и соседние клетки используют ее фрагменты в качестве строительного материала. Самоликвидации подвергаются и митохондрии – изучив этот процесс, Скулачев назвал его митоптозом. Митоптоз происходит, если в митохондриях образуется слишком много свободных радикалов. Когда количество погибших митохондрий слишком велико, продукты их распада отравляют клетку и приводят к ее апоптозу. Старение, с точки зрения Скулачева, – результат того, что в организме гибнет больше клеток, чем рождается, а отмирающие функциональные клетки заменяются соединительной тканью. Суть его работы – поиск методов противодействия разрушению клеточных структур свободными радикалами. По мнению ученого, старость – это болезнь, которую можно и нужно лечить, программу старения организма можно вывести из строя и тем самым выключить механизм, сокращающий нашу жизнь. По мнению Скулачева, главная из активных форм кислорода, приводящих к гибели митохондрий и клеток – перекись водорода. В настоящее время под его руководством проходит испытания препарат SKQ, предназначенный для предотвращения признаков старения.
Теория соматических мутаций. Многие работы показали увеличение с возрастом числа соматических мутаций и других форм повреждения ДНК, предлагая репарацию (ремонт) ДНК в качестве важного фактора поддержки долголетия клеток. Повреждения ДНК типичны для клеток, и вызываются такими факторами как жёсткая радиация и активные формы кислорода, и потому целостность ДНК может поддерживаться только за счёт механизмов репарации. Действительно, существует зависимость между долголетием и репарацией ДНК, как это было продемонстрировано на примере фермента поли-АДФ-рибоза-полимеразы-1 (PARP-1), важного игрока в клеточном ответе на вызванное стрессом повреждение ДНК. Более высокие уровни PARP-1 ассоциируются с большей продолжительностью жизни.
Теория бактериальной интоксикации организма. Оригинальную гипотезу выдвинул выдающийся русский биолог И.И. Мечников (1845-1916), который считал старение результатом интоксикации организма продуктами обмена бактерий, обитающих в кишечном тракте, и продуктами азотистого обмена веществ самого организма (мочевая кислота). Образуются ядовитые вещества, в том числе - скатол, индол, фенол (карболовая кислота), крезол, кадаверин (трупный яд), тирамин и другие токсины.
Теломерная теория Оловникова. Во многих клетках человека утрата способности их к делению связана с утратой теломер на концах хромосом, после определённого количества делений. Это происходит из-за отсутствия фермента теломеразы, который обычно экспрессуется только у зародышевых и стволовых клеток. Недавно было обнаружено, что окислительный стресс также может иметь влияние на утрату теломер, значительно ускоряя этот процесс в определённых тканях.
В настоящее время нет основной теории старения, они все занимают важное место в науке.
Мысль о том, что старение может быть заложено с момента рождения, была высказана немецким ученым-дарвинистом Августом Вейсманом (Friedrich Leopold August Weismann, 1834-1914). В своей знаменитой лекции, прочитанной в 1891 году, Вейcман выдвинул предположение, что смерть от старости возникла в ходе эволюции: .
Подходы к классификации теорий старения
Теории, объясняющие старение организмов можно классифицировать различными способами.
Например, существует разделение на три группы: генетические теории, в которых генно-контролируемые запрограммированные , такие как теломеры регулируют рост, зрелость и старость, нейроэндокринные теории и теории накопления повреждений. Вообще говоря, это разделение довольно условное, потому как все эти механизмы важны и взаимосвязаны.
Также выделяют 2 большие группы: стохастические (вероятностные) теории и теории программированного старения.
Можно классифицировать теории по уровню организации живой материи.
По мнению В.Н. Анисимова, руководителя Российского Геронтологического Общества, наиболее яркими теориями остаются выдвинутая в 1956 г. Д. Харманом свободнорадикальная теория (Harman, 1956, 1998), теория клеточного (репликативного) старения Л. Хейфлика (Hayflick, Moorhead, 1961; Hayflick, 1998), теломерная теория А.М.Оловникова (Оловников, 1971; Olovnikov, 1996), элевационная теория старения В.М. Дильмана (Дильман, 1987; Dilman, 1971, 1994) и теория расходуемой сомы Т. Кирквуда (Kirkwood, 1997, 2002). выдвинутая в 1956 г. Д. Харманом свободнорадикальная теория, теория клеточного (репликативного) старения Л. Хейфлика и теломерная теория А. М. Оловникова, элевационная теория старения В. М. Дильмана.
Классификация теорий стохастического старения
- Теория cоматических мутаций - Соматические мутации нарушают генетическую информацию и уменьшают функцию клеток
- Катастрофа ошибок - Ошибки процессов транскрипции и/или трансляции уменьшают эффективность клеток
- Повреждения ДНК, репарация ДНК - Повреждения ДНК постоянно репарируются различными механизмами. Эффективность репарации положительно корелирует с продолжительностью жизни и уменьшается с возрастом
- Повреждения белков - Конформационные нарушения белков и ферментов (перекрестные сшивки) повреждают функцию клетки
- Перекрестные сшивки - Химические перекрестные сшивки важных макромолекул (например, коллагена) приводят к нарушениям функции клеток и тканей
- Износ - Накопление повреждений в повседневной жизни уменьшает эффективность организма
Классификация теорий программированного старения
- Генетические теории - Старение вызывается запрограммированными изменениями экспрессии генов, или экспрессией специфических белков
- Гены смерти - Существуют гены клеточной гибели
- Избирательная гибель - Гибель клетки обусловлена наличием специфических мембранных рецепторов
- Укорочение теломер - Укорочение теломер с возрастом in vitro и in vivo приводит к нестабильности хромосом и гибели клеток
- Нарушения дифференцировки - Ошибки в механимзах активации-репрессии генов, приводящие к синтезу избыточных, несущественных или ненужных белков
- Накопление - Накопление отходов метаболизма снижает жизнеспособность клеток
- Нейроэндокринные теории - Недостаточность нервной и эндокринной систем в поддержании гомеостаза. Потеря гомеостаза приводит к старению и смерти
- Иммунологическая теория - Определенные аллели могут увеличивать или сокращать продолжительность жизни.
- Метаболические теории - Долголетие обратно пропорционально скорости метаболизма
- Свободно-радикальная теория - Долголетие обратно пропорционально степени повреждения свободными радикалами и прямо пропорционально эффективности антиокислительных систем
- Часы старения - Старение и смерть являются результатом предопределенного биологического плана
- Эволюционные теории - Естественный отбор устраняет индивидуумов после того, как они произведут потомство
Классификация важнейших теорий старения по уровню интеграции
(Yin, Chen, 2005)
Организменный уровень интеграции
Теория изнашивания - Sacher, 1966
Теория катастрофы ошибок - Orgel, 1963
Теория стрессового повреждения - Stlye, 1970
Теория аутоинтоксикации - Metchnikoff, 1904
Эволюционная теория (теория программированного старения) - Williams, 1957
Теория сохранения информации (теория программированного старения)
Органный уровень
Эндокринная теория - Korenchevsky, 1961
Иммунологическая теория - Walford, 1969
Торможение головного мозга
Клеточный уровень
Теория клеточных мембран - Zg-Nagy, 1978
Теория соматических мутаций - Szillard, 1959
Митохондриальная теория - Miquel et al., 1980
Митохондриально-лизосомальная теория - Brunk, Terman, 2002
Теория пролиферативного лимита клетки (теория программированного старения) - Hayflick, Moorhead, 1961
Молекулярный уровень
Теория накопление повреждений ДНК - Vilenchik, 1970
Теория следовых элементов - Eichhorn, 1979
Свободно-радикальная теория - Harman, 1956
Теория поперченных сшивок - Bjorksten, 1968
Теория окислительного стресса - Sohal, Allen, 1990; Yu, Yang, 1996
Теория неэнзиматической гликозиляции - Cerami, 1985
Теория карбонильной интоксикации - Yin, Brunk, 1995
Теория катастрофы загрязнения - Terman, 2001
Теория генных мутаций
Теория укорочения теломер (теория программированного старения) - Оловников, 1971
Прочие подходы
Cтарение как энтропия - Sacher, 1967; Bortz, 1986
Математические теории и различные унифицированные теории - Sohal, Alle, 1990;
Zg-Nagy, 1991; Kowald, Kirkwood, 1994
Свободнорадикальная теория старения Дэнхема Хармана
Свободнорадикальная теория старения была представлена в 1956 Денхамом Харманом, который предположил, что старение является результатом случайного вредоносного повреждения тканей свободными радикалами. В ходе жизнедеятельности каждой клетки через неё проходит огромное количество кислорода. Он используется для клеточного дыхания, дающего клетке энергию. Но небольшая доля кислорода при этом уходит в паразитные соединения, обладающие огромной реакционной способностью. Их называют АФК - активные формы кислорода (хотя в их составе бывает и не только кислород). Примерами таких веществ могут служить всем хорошо известные перекись водорода и озон. Эти два вещества, однако, относительно малоактивны и могут существовать долго. Другие же АФК несравненно агрессивней. В организме они живут лишь тысячные доли секунды. А потом вступают в реакцию с другими молекулами, повреждая их. Они атакуют белки, липиды клеточных мембран, ДНК.
В результате атак со стороны АФК повреждаются митохондрии. Накопление этих повреждений и является сутью старения.
Интервью
Теория клеточного старения Леонарда Хейфлика
В 1961 г. Леонард Хейфлик представил данные о том, что даже в идеальных условиях культивирования фибробласты эмбриона человека способны делиться только ограниченное число раз (50 + 10). Последняя фаза жизни клеток в культуре была уподоблена клеточному старению, а сам феномен получил по имени автора название "предела Хейфлика". Сам Хейфлик не предложил объяснение этого явления.
Теломерная теория Оловникова
развитие теории Хейфлика
В 1971 г. научный сотрудник Института биохимической физики РАН А.М. Оловников, используя данные о принципах синтеза ДНК в клетках, предложил гипотезу, по которой объясняется тем, что при каждом клеточном делении хромосомы немного укорачиваются. У хромосом имеются особые концевые участки - теломеры, которые после каждого удвоения хромосом становятся немного короче, и в какой-то момент укорачиваются настолько, что клетка уже не может делиться. Тогда она постепенно теряет жизнеспособность - именно в этом, согласно теломерной теории, и состоит старение клеток. Открытие в 1985 г. фермента теломеразы, достраивающего укороченные теломеры в половых клетках и клетках опухолей, обеспечивая их бессмертие, стало блестящим подтверждением теории Оловникова. Правда, предел в 50-60 делений справедлив далеко не для всех клеток: раковые и стволовые клетки теоретически могут делиться бесконечно долго, в живом организме стволовые клетки могут делиться не десятки, а тысячи раз, но связь старения клеток с укорочением теломер является общепризнанной.
Интервью на Радио Свобода
Элевационная теория старения
Теория расходуемой (одноразовой) сомы
Теория перекрестных сшивок
Этот механизм старения немного похож на воздействие свободных радикалов. Только роль агрессивных веществ здесь играют сахара, в первую очередь - всегда присутствующая в организме глюкоза. Сахара могут вступать в химическую реакцию с различными белками. При этом, естественно, функции этих белков могут нарушаться. Но что гораздо хуже, молекулы сахаров, соединяясь с белками, обладают способностью молекулы белков между собой. Из-за этого клетки начинают хуже работать. В них накапливается клеточный мусор.
Одно из проявлений такой сшивки белков - потеря тканями эластичности. Внешне наиболее заметным оказывается появление на коже морщин. Но гораздо больший вред приносит потеря эластичности кровеносных сосудов и лёгких. В принципе, у клеток есть механизмы для разрушения подобных сшивок. Но этот процесс требует от организма очень больших энергозатрат.
Сегодня уже существуют лекарственные препараты, которые разбивают внутренние сшивки и превращают их в питательные вещества для клетки.
Теория ошибок
Гипотеза была выдвинута в 1954 г. американским физиком М. Сциллардом. Исследуя эффекты воздействия радиации на живые организмы, он показал, что действие ионизирующего излучения существенно сокращает срок жизни людей и животных. Под воздействием радиации происходят многочисленные мутации в молекуле ДНК и инициируются некоторые симптомы старения, такие как седина или раковые опухоли. Из своих наблюдений Сцилард сделал вывод, что мутации являются непосредственной причиной старения живых организмов. Однако он не объяснил факта старения людей и животных, не подвергавшихся облучению.
Его последователь Л. Оргель считал, что мутации в генетическом аппарате клетки могут быть либо спонтанными, либо возникать в ответ на воздействие агрессивных факторов - ионизирующей радиации, ультрафиолета, воздействия вирусов и токсических (мутагенных) веществ и т.д. С течением времени система репарации ДНК изнашивается, в результате чего происходит старение организма.
Теория апоптоза (самоубийства клеток)
Академик В.П. Скулачев называет свою теорию теорией клеточного апоптоза. Апоптоз (греч. ) - процесс запрограммированной гибели клетки. Как деревья избавляются от частей, чтобы сохранить целое, так и каждая отдельная клетка, пройдя свой жизненный цикл, должна отмереть и ее место должна занять новая. Если клетка заразится вирусом, или в ней произойдет мутация, ведущая к озлокачествлению, или просто истечет срок ее существования, то, чтобы не подвергать опасности весь организм, она должна умереть. В отличие от некроза - насильственной гибели клеток из-за травмы, ожога, отравления, недостатка кислорода в результате закупоривания кровеносных сосудов и т.д., при апоптозе клетка аккуратно саморазбирается на части, и соседние клетки используют ее фрагменты в качестве строительного материала.
Самоликвидации подвергаются и митохондрии - изучив этот процесс, Скулачев назвал его митоптозом. Митоптоз происходит, если в митохондриях образуется слишком много свободных радикалов. Когда количество погибших митохондрий слишком велико, продукты их распада отравляют клетку и приводят к ее апоптозу. Старение, с точки зрения Скулачева, - результат того, что в организме гибнет больше клеток, чем рождается, а отмирающие функциональные клетки заменяются соединительной тканью. Суть его работы - поиск методов противодействия разрушению клеточных структур свободными радикалами. По мнению ученого, старость - это болезнь, которую можно и нужно лечить, программу старения организма можно вывести из строя и тем самым выключить механизм, сокращающий нашу жизнь.
По мнению Скулачева, главная из активных форм кислорода, приводящих к гибели митохондрий и клеток - перекись водорода. В настоящее время под его руководством проходит испытания препарат SKQ, предназначенный для предотвращения признаков старения.
Интервью "Новой Газете"
Адаптационно-регуляторная теория
Модель старения, разработанная выдающимся украинским физиологом и геронтологом В.В. Фролькисом в 1960-70-х гг., основана на широко распространенном представлении о том, что старость и смерть генетически запрограммированы. теории Фролькиса состоит в том, что возрастное развитие и продолжительность жизни определяются балансом двух процессов: наряду с разрушительным процессом старения развертывается процесс , для которого Фролькис предложил термин (лат. vita - жизнь, auctum - увеличивать). Этот процесс направлен на поддержание жизнеспособности организма, его адаптацию, увеличение продолжительности жизни. Представления об антистарении (витаукте) получили широкое распространение. Так, в 1995 г. в США состоялся первый международный конгресс по этой проблеме.
Существенным компонентом теории Фролькиса является разработанная им генорегуляторная гипотеза, по которой первичными механизмами старения являются нарушения в работе регуляторных генов, управляющих активностью структурных генов и, в результате, интенсивностью синтеза закодированных в них белков. Возрастные нарушения генной регуляции могут привести не только к изменению соотношения синтезируемых белков, но и к экспрессии ранее не работавших генов, появлению ранее не синтезировавшихся белков и, как результат, к старению и гибели клеток.
В.В.Фролькис полагал, что генорегуляторные механизмы старения являются основой развития распространенных видов возрастной патологии - атеросклероза, рака, диабета, болезней Паркинсона и Альцгеймера. В зависимости от активации или подавления функций тех или иных генов и будет развиваться тот или иной синдром старения, та или иная патология. На основе этих представлений была выдвинута идея генорегуляторной терапии, призванной предупреждать сдвиги, лежащие в основе развития возрастной патологии.
Редусомная теория Оловникова
Покрытая белками линейная молекула ДНК редусомы - это копия сегмента хромосомной ДНК. гнезде. Подобно теломерной ДНК линейная ДНК редусомы с течением времени укорачивается. Поэтому крошечные редусомы прогрессирующе уменьшаются в размерах; отсюда и их название. Вместе с убылью ДНК в редусоме уменьшается и количество содержащихся в ней разных генов. Укорочение молекул редусомной ДНК (и вызванное этим изменение набора генов в редусомах, меняет с возрастом уровень экспрессии различных хромосомных генов и благодаря этому служит ключевым средством измерения биологического времени в индивидуальном развитии.
Комментарии к теории
Теория соматических мутаций
Среди современных теорий старения, основанных на предположении, что ДНК является основной мишенью повреждающих агентов в клетке, доминирует теория соматических мутаций, согласно которой старение - результат взаимодействия различных эндогенных и экзогенных повреждающих агентов с генетическим материалом клетки и постепенного накопления случайных мутаций в геноме соматических клеток. Повреждения ядерной и митохондриальной ДНК соматических клеток, такие, как точечные мутации, делеции и транслокации, приводят к активации или инактивации специфических генов, вовлеченных в регуляцию клеточного цикла и контроль роста. Накопление с возрастом таких мутаций в различных органах и тканях - основной фактор, определяющий развитие возрастной патологии, включая рак.

В современном мире существуют несколько наиболее поддерживаемых концепций старения биологических организмов. Ученые в течение продолжительного периода времени пытались выяснить, по какой причине многие функции организма начинают деградировать, а вскоре – и вовсе отказывать работать, однако очень долго это не представлялось возможным, так как уровень НТП не предоставлял возможности для грамотного исследования этого таинственного процесса. Нынешняя биология уделяет механизму старения пристальное внимание, поэтому с каждым годом на свет появляются все новые факты, которые позволяют более глубоко понять особенности этого явления.
Перейдем к рассмотрению теорий.
Молекулярно-генетические теории
Гипотеза, согласно которой причиной старения являются изменения генетического аппарата клетки, является одной из наиболее авторитетных концепций в современной геронтологии. Молекулярно-генетические теории подразделяются на две обширные группы. Одни ученые придерживаются того, что возрастные изменения генома наследственно запрограммированы. Другие, в свою очередь, считают, что старение – результат накопления случайных мутаций. Таким образом, процесс старения, по мнению ученых, может являться как закономерным результатом развития организма, так и следствием накопления клетками случайных ошибок в системе хранения и передачи генетической информации.
Теория свободных радикалов
Данная концепция, выдвинутая учёными Д. Харманом(1956) и Н. Эмануэлем (1958), объясняет не только механизм старения, но и широкий спектр связанных с ним патологических явлений (ослабления иммунитета, нарушений функции мозга, сердечно-сосудистых заболеваний, рака, катаракты, и других). Согласно этой концепции, причиной нарушения функционирования клеток являются необходимые для многих биохимических процессов свободные радикалы – активные формы кислорода, синтезируемые в митохондриях – так называемых энергетических фабриках клеток. Если крайне агрессивный, химически активный свободный радикал случайно покидает то место, где его участие необходимо, он может повредить и РНК, и ДНК, и липиды, и протеины. Однако природа создала механизм защиты от избытка свободных радикалов: супероксиддисмутаза (фермент антиоксидантной защиты) и некоторые другие синтезируемые в митохондриях и клетках ферменты, многие вещества, которые попадают нам в организм с продуктами питания – в том числе витамины Е, А и С, обладают колоссальным антиоксидантным действием. Регулярное поглощение свежих фруктов и овощей, небольшое количество качественного зеленого чая или цикория в день обеспечат вам необходимую дозу полифенолов, которые являются хорошими антиоксидантами.
Однако, к сожалению, у данной медали существует обратная сторона: избыток антиоксидантов – например, при передозировке БАД – может нанести вред организму, усилив окислительные процессы в клетках живого организма.
Старение – систематическая ошибка. Данная гипотеза была выдвинута в 1954 г. американским физиком М. Сциллардом. Во время исследования эффектов воздействия радиации на живые системы он выяснил, что действие ионизирующего излучения сокращает срок жизни животных и человека. Под воздействием радиации происходят многочисленные мутации в молекуле ДНК и проявляются некоторые симптомы старения – седина или раковые опухоли. Из собственных наблюдений ученый сделал вывод, что мутации являются непосредственной причиной старения живых организмов. Однако он не объяснил факта старения людей и животных, которые не подвергались облучению. Его последователь Л. Оргель считал, что мутации в генетическом аппарате клетки могут быть либо спонтанными, либо могут возникать в ответ на воздействие опасных факторов: ультрафиолета, воздействия вирусов и токсических веществ, ионизирующей радиации. В процессе жизнедеятельности организма система репарации (особая функция клетки, которая заключается в способности исправлять химические повреждения) ДНК изнашивается, что приводит к старению организма.
Теория соматических мутаций
Многие труды ученых показали, что с возрастом число соматических мутаций и других форм повреждения ДНК возрастает. Однако они выяснили, что в клетке присутствует защитный механизм – репарация (ремонт) ДНК. Именно он играет колоссальную роль в поддержке долголетия клеток. Повреждения ДНК типичны для клеток, они вызываются жесткой радиацией и активными формами кислорода, потому целостность ДНК может поддерживаться только за счёт механизмов репарации. Действительно, существует зависимость между долголетием и репарацией ДНК, как это было продемонстрировано на примере фермента поли-АДФ-рибоза-полимеразы-1 (PARP-1), играющего немаловажную роль в клеточном ответе на вызванное стрессом повреждение ДНК. Более высокие уровни PARP-1 ассоциируются с большей продолжительностью жизни.
Теория апоптоза
Теория бактериальной интоксикации организма
Немаловажную гипотезу выдвинул авторитетный русский биолог И.И. Мечников (1845–1916). Он считал, что старение – это результат интоксикации организма продуктами обмена бактерий, которые обитают в кишечном тракте, и продуктами азотистого обмена веществ самого организма. Образуются ядовитые вещества, в числе которых индол, фенол (карболовая кислота), крезол, кадаверин (трупный яд), тирамин и другие токсины.
Теломерная теория Оловникова
В большом числе клеток живого организма потеря способности их к делению вследствие определённого количества делений связана с утратой теломер на концах хромосом. Это происходит из-за отсутствия фермента теломеразы, который обычно экспрессируется только у зародышевых и стволовых клеток. Недавно было обнаружено, что окислительный стресс также может иметь влияние на утрату теломер, значительно ускоряя этот процесс в определённых тканях.
Во многих точках мира проводятся различные эксперименты и исследования, в числе которых:
1. Манипулирование с генами
Роберт Шмуклер Рис, профессор университета Арканзаса, выключил в геноме нематоды C.elegans один ген – Age-1. Таким образом, ему удалось увеличить жизнь червя в 10 раз! Нематода довольно простой организм, поэтому ожидать такого впечатляющего результата на иных объектах не приходится. Российский исследователь Алексей Москалев таким способом продлил жизнь мухе дрозофиле всего на 10 %.
2. Надстройка теломер
Преодолеть старение органов и тканей у мышей путем надстройки теломер в стволовых клетках удалось ученым из медицинского факультета Гарварда. Заметим, они работали не с обычными мышами, а с мутантами, которые ускоренно старели. Фермент теломераза, который надстраивает теломеры до нормальной длины, у этих мышей не работал даже в стволовых клетках, там, где он должен обеспечивать длительное деление. А у самих мышей в молодом возрасте появлялись признаки старения: деградировали семенники, селезенка, мозг, нарушалось обоняние. Дегенерацию удалось повернуть вспять, когда ученые биохимически восстановили в клетках активность теломеразы. Это привело к удлинению теломер и возобновлению клеточных делений. У мышей при этом стали восстанавливаться ткани семенников, селезенки и мозга, и они снова стали ощущать запахи.
Таким образом, в настоящее время выделить основную теорию старения живых организмов довольно трудно, поскольку все они существуют в комплексе, дополняя друг друга. Современный век дает возможность миру каждый день делать удивительные открытия, так как уровень научно-технического прогресса все быстрее и быстрее постигает новые высоты, а ученые получают все более углубленные знания. Решение проблем с механизмом старения – одна из основных целей современной науки, однако, несмотря на передовые технологии, ученому миру необходимо проделать немалый путь и приложить огромное количество усилий, чтобы найти безусловно эффективные методы прекращения старения организма.
Но все же существуют некоторые принципы, с помощью которых каждый человек улучшит свое здоровье, что приведет к увеличению цикла жизни организма. Перейдем к рассмотрению данных методов.
Метод № 1
Все долгожители мира, как правило, употребляют малое количество пищи. Ученые подсчитали, что уменьшение калорийности пищи на 20–30 процентов снижает вероятность заболеть диабетом на 50 процентов, а раком – на 70 процентов. Дело в том, что сейчас мы, как правило, едим гораздо больше, чем требуется нашему организму, эволюционно формировавшемуся в условиях обилия физических нагрузок и хронической нехватки пищи.
Метод № 2
Если вы не в силах сократить калорийность ежедневного рациона, необходимо употреблять меньше соли и сахара. Исследования показали, что избыток соли вызывает гипертонию, а впоследствии – ранний инсульт. Сахар же, в свою очередь, тоже вызывает проблемы – от его чрезмерного потребления ухудшается работа головного мозга, сердца, а самое главное – чрезмерное потребление негативно сказывается на поджелудочной железе, провоцируя диабет, ожирение и раннюю смерть.
Метод № 3
Анализируя истории болезней и дневников сотен тысяч людей, учёные выяснили, что живут существенно дольше те, у кого в рационе содержатся фрукты и овощи. В них содержится несметное количество безусловно полезных витаминов и минералов, а также антиоксидантов, которые борются в организме с активными, повреждающими клетки формами кислорода. По словам ученых, лучше есть разные овощи, фрукты и ягоды, необходимо вносить разнообразие в рацион.
Метод № 4
Немаловажный пункт – это сон в полной темноте. Как выяснилось, искусственный свет, который испускается различными лампами, в вечерний период нарушает выработку в мозгу гормона мелатонина. Он крайне необходим для поддержания иммунитета. Именно благодаря ему организм обновляется и очищается ночью. Сбои в данном процессе приводят к негативным последствиям, которые неблагоприятно сказываются на организме в целом.
Метод № 5
Метод № 6
Увеличение физической активности. Подопытные мыши, которых заставляли бегать на беговой̆ дорожке и в колесе, дольше сохраняли молодость и здоровье, чем малоподвижные особи. Ученые считают, что физическая активность увеличивает количество и качество митохондрий. Исследователи из университета Макмастера (Канада), к примеру, работали с мышами, которые склонны к преждевременному старению из-за высокого уровня мутаций в ДНК митохондрий. Одна группа мышей жила в обычных условиях, другая три раза в неделю занималась интенсивным физическим трудом. Через три месяца наблюдений выяснилось, что мыши-спортсмены сохранили молодость и здоровье, сравнимое с показателями диких животных. Их митохондрии оставались функционально полноценными. Чего не скажешь об особях, которые не занимались физической активностью.
Список использованных источников
Читайте также:

