Теория молекулярных орбиталей кратко
Обновлено: 05.07.2024
В атомах электроны располагаются на атомных орбиталях (АО), а в молекулах – на молекулярных орбиталях (МО). Нахождение электронов определяется методом молекулярных орбиталей (ММО). Все отрицательные частицы располагаются на молекулярных орбиталях, единых для всей системы положительно заряженных ядер и электронов.
Теория молекулярных орбиталей
- В молекуле образуется собственная структура молекулярных орбиталей, на которой находятся все электроны данной молекулы.
- Для определения волновой функции используют сложение или вычитание атомных волновых функций.
Правила метода молекулярных орбиталей
- Молекулярная орбиталь, формирующаяся в результате сложения атомных орбиталей, имеет небольшую энергию, по сравнению с начальными атомными орбиталями. Она называется связывающей. Расположение на ней более выгодно, чем на исходных атомных орбиталях.
Молекулярная орбиталь, формирующаяся при вычитании, имеет высокую энергию. Она называется разрыхляющей.

- Количество молекулярных орбиталей определяется суммой атомных орбиталей.
- При рапределении электронами выполняется принцип наименьшей энергии, правило Гунда и принцип Паули.
Пример заполнения молекулярных орбиталей электронами
Например, необходимо заполнить молекулярные орбитали водорода Н2. Для решения этой задачи нужно изобразить на двух параллельных диаграммах энергетические уровни атомных орбиталей водорода.

Затем мысленно перекрыть две атомные орбитали, образовав две молекулярные, одна из которых обладает меньшей энергией (расположена ниже), а вторая – большей энергией (расположена выше).

Таким образом, оба электрона располагаются на связывающей орбитали.
В молекуле гелия Не2 электроны находятся как на связывающей, так и на разрыхляющей орбиталях.

Возможности метода молекулярных орбиталей
С помощью данного метода можно вычислить прочность связи. Она определяется энергией при формировании молекулы и коррелирует с величиной кратности связи. Чем больше кратность, тем выше прочность молекулы. Также метод позволяет вычислить межатомное расстояние – оно коррелирует с величиной кратности связи.
Мы уже знаем, что в атомах электроны находятся на разрешенных энергетических состояниях – атомных орбиталях (АО). Аналогичным образом, электроны в молекулах существуют в разрешенных энергетических состояниях – молекулярных орбиталях (МО).
Молекулярная орбиталь
Молекулярная орбиталь устроена намного сложнее атомной орбитали. Приведем несколько правил, которыми мы будем руководствоваться при построении МО из АО:
- При составлении МО из набора атомных орбиталей, получается такое же число МО, сколько АО в данном наборе.
- Средняя энергия МО, полученных из нескольких АО, примерно равна (но может быть больше или меньшее) средней энергии взятых АО.
- МО подчиняются принципу запрета Паули: на каждой МО не может находиться более двух электронов, которые должны иметь противоположные спины.
- АО, которые обладают сопоставимой энергией, комбинируются наиболее эффективно.
- Эффективность, с которой комбинируют две атомные орбитали, пропорциональна их перекрыванию друг с другом.
- При образовании МО при перекрывании двух неэквивалентных АО связывающая МО содержит больший вклад АО с наиболее низкой энергией, а разрыхляющая орбиталь – вклад АО с более высокой энергией.
Введем понятие порядок связи. В двухатомных молекулах, порядок связи показывает насколько число связывающих электронных пар превышает число разрыхляющих электронных пар:

Теперь на примерах рассмотрим как строить молекулярные орбитали с применением этих правил.
Молекулярно-орбитальные диаграммы элементов первого периода
Диаграмма МО молекулы Н2
Пример образования молекулы водорода из двух атомов водорода.
В результате взаимодействия 1s-орбиталей каждого из атомов водорода, образуются две молекулярные орбитали.
При взаимодействии, когда электронная плотность концентрируется в пространстве между ядрами, образуется связывающая сигма – орбиталь (σ). Эта комбинация имеет более низкую энергию, чем исходные атомы. При взаимодействии, когда электронная плотность концентрируется за пределами межъядерной области, образуется разрыхляющая сигма – орбиталь (σ * ). Эта комбинация имеет более высокую энергию, чем исходные атомы.
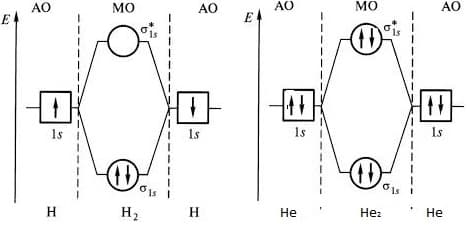
диаграммы МО молекул водорода и гелия
Электроны, в соответствии с принципом Паули, занимают сначала орбиталь с самой низкой энергией σ-орбиталь.
Диаграмма МО молекулы Не2
Теперь рассмотрим пример образования молекулы гелия He2, при сближении двух атомов гелия. В этом случае тоже происходит взаимодействие 1s-орбиталей и образование и σ * -орбиталей, при этом два электрона занимают связывающую орбиталь, а другие два электрона – разрыхляющую.
σ * — орбиталь дестабилизирована в такой же мере, насколько стабилизирована σ –орбиталь, поэтому два электрона, занимающие σ * — орбиталь, дестабилизируют молекулу He2. Действительно, экспериментально доказано, что молекула He2 очень неустойчива.
Как узнать несколько велика прочность молекулы? Чем больше разница в заполненности связывающей и разрыхляющей орбиталей, тем молекула более прочная. Как видно из диаграммы разница в заполненности орбиталей молекулы водорода больше, чем молекулы гелия, поэтому молекула водорода намного более прочная, чем молекула гелия.
Молекулярно-орбитальные диаграммы элементов второго периода
Рассмотрим, как взаимодействуют два одинаковых атома второго периода между собой, имеющие набор из s- и p-орбиталей. Следует ожидать, что 2s-орбитали будут соединяться только друг с другом, а 2p-орбитали – только с а 2p-орбиталями.
Т.к. 2p-орбитали могут взаимодействовать друг с другом двумя различными способами, то образуют σ- и π-молекулярные орбитали. Пользуясь обобщенной диаграммой, показанной ниже, можно установить электронные конфигурации двухатомных молекул второго периода , которые приведены в таблице.

Так, образование молекулы, например, фтора F2 из атомов в системе обозначений теории молекулярных орбиталей может быть записано следующим образом:
Т.к. перекрывание 1s-облаков незначительно, то участием электронов на этих орбиталях можно пренебречь. Тогда электронная конфигурация молекулы фтора будет такой:
где К — электронная конфигурация К-слоя.
В таблице приведены молекулярные орбитали двухатомных молекул элементов второго периода бора (B2), углерода (C2), азота (N2), кислорода (O2), фтора (F2)

Рассмотрим подробнее пример образования молекулы лития Li2, принимая во внимание, что 1s- и 2s-орбитали слишком сильно отличаются по энергии и поэтому между ними не возникает сильного взаимодействия.
Диаграмма энергетических уровней молекулы Li2 показана ниже, где электроны, находящиеся на 1s-связывающих и 1s-разрыхляющих орбиталях не вносят значительного вклада в связывание. Поэтому за образование химической связи в молекуле Li2 отвечают 2s-электроны.
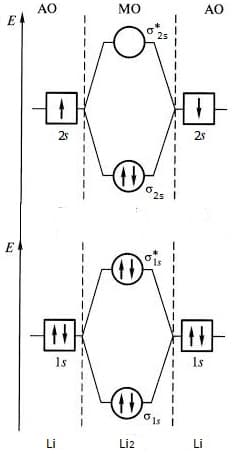
диаграмма МО молекулы лития
Это действие распространяется и на образование других молекул, в которых заполненные атомные подоболочки (s, p, d) не дают вклада в химическую связь. Таким образом, рассматриваются только валентные электроны.
В итоге, для щелочных металлов, молекулярно-орбитальная диаграмма будет иметь вид подобный рассмотренной нами диаграмме молекулы Li2.
Порядок связи n в молекуле Li2 равен 1
Молекулярные орбитали полярных двухатомных молекул
Учение о МО позволяет объяснить и образование двухатомных гетероядерных молекул. Если атомы в молекуле не слишком отличаются друг от друга (например, NO, CO, CN), то можно воспользоваться диаграммой, приведенной выше для элементов 2 периода.
При значительных различиях между атомами, входящих в состав молекулы, диаграмма видоизменяется.
Чем больше электроотрицательность атома, тем более низко на диаграмме обозначают атомные орбитали.
Диаграмма МО молекулы HF
Рассмотрим молекулу HF, в которой атомы сильно отличаются по электроотрицательности.
Энергия 1s-орбитали атома водорода выше энергии самой высокой из валентных орбиталей фтора – 2p — орбитали. Взаимодействие 1s-орбитали атома водорода и 2p — орбитали фтора приводит к образованию связывающей и разрыхляющей орбиталей, как показано на рисунке. Пара электронов, находящиеся на связывающей орбитали молекулы HF, образуют полярную ковалентную связь.
Для связывающей орбитали молекулы HF 2p — орбиталь атома фтора играет более важную роль, чем 1s — орбиталь атома водорода.
Для разрыхляющей орбитали молекулы HF наоборот: 1s — орбиталь атома водорода играет более важную роль, чем 2p — орбиталь атома фтора
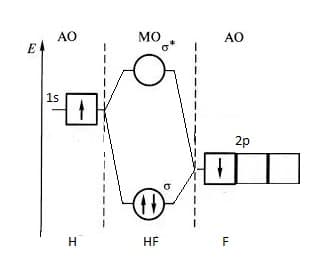
Диаграмма МО молекулы HF
Т.к. электроотрицательность фтора больше, чем электроотрицательность водорода, то на диаграмме, атомные орбитали фтора расположени ниже, чем атомная орбиталь водорода.
Определим порядок связи, т.е. кратность связи:
Т.о. в молекуле H-F связь одинарная.
Диаграмма МО молекулы СО
Электронная конфигурация внешнего слоя атомов углерода и кислорода:
С+6 1s 2 2s 2 2p 2
O+8 1s 2 2s 2 2p 4
Кислород более электроотрицательный элемент, поэтому его атомная орбиталь на диаграмме расположена ниже орбитали углерода.
Диаграмма МО молекулы СО имеет вид:

Кратность связи равна:
Диаграмма молекулы NO приведена в разделе Задачи к разделу Химическая связь и строение молекул
Согласно теории молекулярных орбиталей молекула состоит из ядер и электронов, а не представляет собой совокупность атомов, как постулирует метод валентных связей. В молекулах электроны находятся на молекулярных орбиталях (МО). Свойства молекул зависят от их электронного строения, то есть от структуры МО. МО внутренних электронов обычно совпадают с соответствующими АО, иначе говоря, внутренние электроны в молекулах сохраняют свою атомную природу и не участвуют в образовании связей. МО внешних электронов имеют более сложное строение и часто рассматриваются как линейная комбинация внешних орбиталей атомов, составляющих молекулу. Число образующихся МО равно числу АО, участвующих в их образовании, то есть из двух АО получаем две МО, из трех АО - три МО и т.д. Энергии МО могут быть ниже (связывающие МО), равны (несвязывающие МО) или выше (разрыхляющие, антисвязывающие МО), чем энергии образующих их АО. Например, взаимодействие двух АО дает две МО: одну связывающую и одну разрыхляющую.
Условия взаимодействия АО:
1. АО взаимодействуют, если имеют близкие энергии. Чем больше разница энергий АО, тем меньше их взаимодействие.
2. АО взаимодействуют, если они перекрываются. Так внутренние АО разных атомов, располагающиеся вблизи ядер, не перекрываются и не взаимодействуют, сохраняя свою атомную природу.
3. АО взаимодействуют, если имеют соответствующую симметрию. Симметрия МО характеризуется элементами симметрии, такими как ось симметрии, плоскость симметрии и т.д. Для двухатомной молекулы АВ (или любой линейной молекулы) симметрия МО может быть:
s, если данная МО имеет ось симметрии,
p, если данная МО имеет плоскость симметрии,
d, если МО имеет две перпендикулярные плоскости симметрии.
Если ось молекулы АВ совпадает с осью Z координат, то
s-, p- и d- МО образуются при взаимодействии следующих АО соответственно:
АО разной симметрии, например, s-АО и рx-АО, не взаимодействуют. Присутствие электронов на связывающих МО стабилизирует систему, так как уменьшает энергию молекулы по сравнению с энергией атомов. Стабильность молекулы характеризуется порядком связи n, равным
где nе св и nе разр - числа электронов на связывающих и разрыхляющих орбиталях.
Заполнение МО электронами происходит по тем же правилам, что и заполнение АО в атоме, а именно: правилу Паули (на МО не может быть более двух электронов), правилу Гунда (суммарный спин должен быть максимален) и т.д.
Взаимодействие 1s-АО атомов первого периода (H и Не)
приводит к образованию связывающей s-МО и разрыхляющей s*- МО:
Электронные формулы молекул, порядки связей п, экспериментальные энергии связей Е и межмолекулярные расстояния R для двухатомных молекул из атомов первого периода приведены в следующей таблице:
| Молекула | Электр. формула | n | Е (кДж) | R (нм) |
| Н2 + | s 1 | 1/2 | 0,106 | |
| H2 | s 2 | 0,074 | ||
| He2 + | s 2 s* 1 | 1/2 | 0,108 | |
| He2 | s 2 s* 2 | не существует |
Из приведенной таблицы видно, что знание электронной формулы молекулы и порядка в связи в ней позволяет правильно предвидеть закономерности в энергиях связей и межъядерных расстояниях. Аналогично могут быть построены МО для гомоядерных молекул из атомов второго периода, таких как Li2 и Be2.
Другие атомы второго периода содержат помимо 2s-АО также и 2рx-, 2py- и 2pz-АО, которые при взаимодействии могут образовывать s- и p-МО. Для атомов О, F и Ne энергии 2s и 2p АО существенно различаются и можно пренебречь взаимодействием 2s-АО одного атома и 2р-АО другого атома, рассматривая взаимодействие между 2s-АО двух атомов отдельно от взаимодействия их 2р-АО. Учитывая, что прямое перекрывание pz-pz с образованием s-связи, сильнее, чем боковое перекрывание px-px или py-py с образованием p-связей, то энергия sz- МО будет ниже, чем энергии pz- и py-МО, а энергия sz-МО выше, чем энергии px*- и py*-МО. Схема МО для молекул О2, F2, Ne2 имеет следующий вид.
Для атомов B, C, N энергии 2s- и 2р-АО близки по своим энергиям и 2s-АО одного атома взаимодействует с 2pz-АО другого атома, в результате чего энергия связывающей ss-МО понижается, а энергия sz-МО повышается настолько, что становится выше энергий px- и py-МО. Поэтому порядок МО в молекулах B2, C2 и N2 отличается от порядка МО в молекулах О2, F2 и Ne2. Ниже приведена схема МО для молекул B2, C2 и N2.

На основании приведенных схем МО можно, например, записать электронные формулы молекул О2, О2 + и О2 - .
В случае молекулы О2 теория МО позволяет предвидеть большую прочность этой молекулы, поскольку п=2, характер изменения энергий связи и межъядерных расстояний в ряду О2 + - О2 - О2 - , а также парамагнетизм молекулы О2, на верхних МО которой имеются два неспаренных электрона.
Согласно теории молекулярных орбиталей молекула состоит из ядер и электронов, а не представляет собой совокупность атомов, как постулирует метод валентных связей. В молекулах электроны находятся на молекулярных орбиталях (МО). Свойства молекул зависят от их электронного строения, то есть от структуры МО. МО внутренних электронов обычно совпадают с соответствующими АО, иначе говоря, внутренние электроны в молекулах сохраняют свою атомную природу и не участвуют в образовании связей. МО внешних электронов имеют более сложное строение и часто рассматриваются как линейная комбинация внешних орбиталей атомов, составляющих молекулу. Число образующихся МО равно числу АО, участвующих в их образовании, то есть из двух АО получаем две МО, из трех АО - три МО и т.д. Энергии МО могут быть ниже (связывающие МО), равны (несвязывающие МО) или выше (разрыхляющие, антисвязывающие МО), чем энергии образующих их АО. Например, взаимодействие двух АО дает две МО: одну связывающую и одну разрыхляющую.
Условия взаимодействия АО:
1. АО взаимодействуют, если имеют близкие энергии. Чем больше разница энергий АО, тем меньше их взаимодействие.
2. АО взаимодействуют, если они перекрываются. Так внутренние АО разных атомов, располагающиеся вблизи ядер, не перекрываются и не взаимодействуют, сохраняя свою атомную природу.
3. АО взаимодействуют, если имеют соответствующую симметрию. Симметрия МО характеризуется элементами симметрии, такими как ось симметрии, плоскость симметрии и т.д. Для двухатомной молекулы АВ (или любой линейной молекулы) симметрия МО может быть:
s, если данная МО имеет ось симметрии,
p, если данная МО имеет плоскость симметрии,
d, если МО имеет две перпендикулярные плоскости симметрии.
Если ось молекулы АВ совпадает с осью Z координат, то
s-, p- и d- МО образуются при взаимодействии следующих АО соответственно:
АО разной симметрии, например, s-АО и рx-АО, не взаимодействуют. Присутствие электронов на связывающих МО стабилизирует систему, так как уменьшает энергию молекулы по сравнению с энергией атомов. Стабильность молекулы характеризуется порядком связи n, равным
где nе св и nе разр - числа электронов на связывающих и разрыхляющих орбиталях.
Заполнение МО электронами происходит по тем же правилам, что и заполнение АО в атоме, а именно: правилу Паули (на МО не может быть более двух электронов), правилу Гунда (суммарный спин должен быть максимален) и т.д.
Взаимодействие 1s-АО атомов первого периода (H и Не)
приводит к образованию связывающей s-МО и разрыхляющей s*- МО:
Электронные формулы молекул, порядки связей п, экспериментальные энергии связей Е и межмолекулярные расстояния R для двухатомных молекул из атомов первого периода приведены в следующей таблице:
| Молекула | Электр. формула | n | Е (кДж) | R (нм) |
| Н2 + | s 1 | 1/2 | 0,106 | |
| H2 | s 2 | 0,074 | ||
| He2 + | s 2 s* 1 | 1/2 | 0,108 | |
| He2 | s 2 s* 2 | не существует |
Из приведенной таблицы видно, что знание электронной формулы молекулы и порядка в связи в ней позволяет правильно предвидеть закономерности в энергиях связей и межъядерных расстояниях. Аналогично могут быть построены МО для гомоядерных молекул из атомов второго периода, таких как Li2 и Be2.
Другие атомы второго периода содержат помимо 2s-АО также и 2рx-, 2py- и 2pz-АО, которые при взаимодействии могут образовывать s- и p-МО. Для атомов О, F и Ne энергии 2s и 2p АО существенно различаются и можно пренебречь взаимодействием 2s-АО одного атома и 2р-АО другого атома, рассматривая взаимодействие между 2s-АО двух атомов отдельно от взаимодействия их 2р-АО. Учитывая, что прямое перекрывание pz-pz с образованием s-связи, сильнее, чем боковое перекрывание px-px или py-py с образованием p-связей, то энергия sz- МО будет ниже, чем энергии pz- и py-МО, а энергия sz-МО выше, чем энергии px*- и py*-МО. Схема МО для молекул О2, F2, Ne2 имеет следующий вид.
Для атомов B, C, N энергии 2s- и 2р-АО близки по своим энергиям и 2s-АО одного атома взаимодействует с 2pz-АО другого атома, в результате чего энергия связывающей ss-МО понижается, а энергия sz-МО повышается настолько, что становится выше энергий px- и py-МО. Поэтому порядок МО в молекулах B2, C2 и N2 отличается от порядка МО в молекулах О2, F2 и Ne2. Ниже приведена схема МО для молекул B2, C2 и N2.
На основании приведенных схем МО можно, например, записать электронные формулы молекул О2, О2 + и О2 - .
В случае молекулы О2 теория МО позволяет предвидеть большую прочность этой молекулы, поскольку п=2, характер изменения энергий связи и межъядерных расстояний в ряду О2 + - О2 - О2 - , а также парамагнетизм молекулы О2, на верхних МО которой имеются два неспаренных электрона.
Связывание атомов в молекулах определяется тем, как перекрываются их волновые функции.
Атомы объединяются в молекулы благодаря химическим связям. Причем участвуют в образовании этих связей электроны, находящиеся во внешнем слое этих атомов. Существует несколько теорий, описывающих процесс связывания. Одна из них — теория валентных связей, в соответствии с которой связи между атомами образуются, когда атомы обмениваются электронными парами из перекрывающихся орбиталей. Другая — теория молекулярных орбиталей.
Такого рода приблизительные теории полезны, поскольку мы получаем простой, интуитивно понятный способ представления физических процессов. С другой стороны, современные компьютеры дают нам возможность с высокой точностью вычислить энергии связи, однако такие вычисления ничуть не приближают нас к пониманию того, что же происходит, когда атомы соединяются. Роль теорий как раз в том и состоит, чтобы дать нам это понимание.
В основе теории молекулярных орбиталей лежит представление о том, что электронная орбиталь в атоме описывается волновой функцией (см. Уравнение Шрёдингера). Теория объясняет, как при протекании химической реакции атомные орбитали преобразуются в молекулярные. Подобно большинству известных нам типов волн, волновые функции электронов в орбиталях претерпевают интерференцию. Оказывается, орбитали в молекулах можно, с хорошим приближением, представить как результат интерференции волновых функций атомов.
Например, рассмотрим, что происходит при взаимодействии двух атомных орбиталей соседних атомов. Если в области перекрывания орбиталей волновые функции претерпевают конструктивную интерференцию, электроны большую часть времени проводят между ядрами, притягивая атомы друг к другу. С другой стороны, если интерференция в области перекрывания деструктивная, электронная плотность между ядрами равна нулю, и между атомами возникает результирующая сила отталкивания. Таким образом, две атомные орбитали объединяются с образованием двух молекулярных орбиталей: одна стремится связать атомы (связывающая молекулярная орбиталь), а другая — оттолкнуть их (разрыхляющая молекулярная орбиталь). И их взаимодействие определяет, будет ли образована стабильная молекула.
Чтобы понять, как работает эта модель, попробуем разобраться, почему водород образует молекулу из двух атомов, а гелий — из одного. В образовании связи между двумя атомами водорода участвуют по одному электрону от каждого атома, а на низшей (связывающей) молекулярной орбитали как раз есть место для двух электронов. Электроны основное время находятся между ядрами, значит атомы притягиваются и молекула водорода может образоваться. У гелия же в образовании связи между двумя атомами участвуют четыре электрона, поэтому заняты как связывающая, так и разрыхляющая атомные орбитали. Численные вычисления показывают, что в этом случае будет преобладать эффект отталкивания, и, даже если молекулы гелия образуются, они будут крайне нестабильны. Поэтому молекула газа гелия состоит из одного атома.
Читайте также:

