Способы получения фенола кратко
Обновлено: 05.07.2024
Каменноугольная смола образуется при коксовании каменного угля и представляет собой смесь нескольких сотен органических веществ. Одним из продуктов переработки этой смеси и является фенол.
Фенол получают при действии гидроксида натрия на хлорбензол при повышенных температуре и давлении. Процесс протекает в две стадии. Сначала образуется фенолят натрия, так как получившийся фенол реагирует с гидроксидом натрия:
Кумольный способ получения фенола состоит из нескольких стадий. Сначала проводят реакцию бензола с пропеном и синтезируют кумол (изопропилбензол):
Потом полученный кумол окисляют кислородом воздуха и получают из него гидропероксид изопропилбензола.
Большое количество фенола расходуется для производства полимеров, из которых изготавливают пластмассы и синтетические волокна.
Фенол — ядовитое вещество. Опасны также его производные. Поэтому важной проблемой является предотвращение попадания фенола в окружающую среду.
Фенолы выделяют из каменноугольной смолы, а также из продуктов пиролиза бурых углей и древесины (деготь).
Промышленный способ получения самого фенола С6Н5ОН основан на окислении ароматического углеводорода кумола (изопропилбензол) кислородом воздуха с последующим разложением получающейся гидроперекиси, разбавленной H2SO4. Реакция проходит с высоким выходом и позволяет получить сразу два технически ценных продукта – фенол и ацетон.
Получение фенола в промышленности
1. Кумольный способ
(СССР, Сергеев П.Г., Удрис Р.Ю., Кружалов Б.Д., 1949 г.). Преимущества метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время кумольный способ используется как основной в мировом производстве фенола.
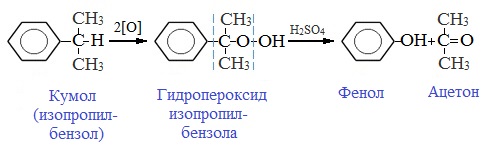
В качестве исходного сырья используют бензол и пропилен, из которых получают изопропилбензол (кумол), подвергающийся дальнейшим превращениям:
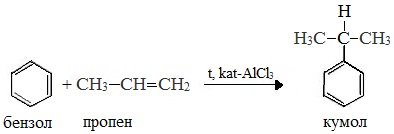
1 стадия – получение кумола
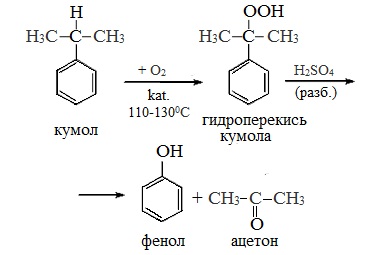
2 стадия – каталитическое окисление
2. Из каменноугольной смолы (как побочный продукт – выход небольшой)
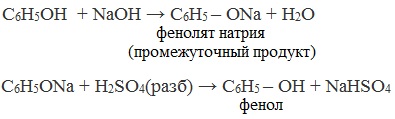
Каменноугольную смолу, содержащую в качестве одного из компонентов фенол, обрабатывают вначале раствором щелочи (образуются феноляты), а затем – кислотой:
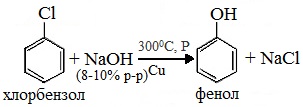
3. Взаимодействие галогенпроизводных ароматических УВ со щелочами
или с водяным паром
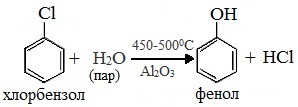
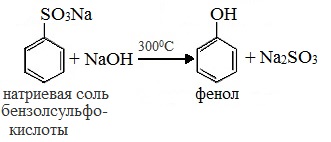
4. Сплавлением солей аренсульфокислот с твёрдыми щелочами
Рубрики: Фенолы Теги: Фенолы
В разделе получения фенолов, есть небольшая ошибка. Там напечатано разбавленная Н3SO4.

В фенолах одна из неподеленных электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца, это является главной причиной отличия свойств фенола от спиртов.

Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода.
Отличия:
- фенол не реагирует с галогеноводородами: ОН- группа очень прочно связана с бензольным кольцом, её нельзя заместить;
- фенол не вступает в реакцию этерификации, эфиры фенола получают косвенным путем;
- фенол не вступает в реакции дегидратации.
- фенол обладает более сильными кислотными свойствами и вступает в реакцию со щелочами.
1. Кислотные свойства фенолов
| Фенолы являются более сильными кислотами, чем спирты и вода, т. к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается. |
1.1. Взаимодействие с раствором щелочей
В отличие от спиртов, фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты.
| Например, фенол реагирует с гидроксидом натрия с образованием фенолята натрия |

Так как фенол – более слабая кислота, чем соляная и даже угольная, его можно получить из фенолята, вытесняя соляной или угольной кислотой:
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Фенолы взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются феноляты. При взаимодействии с металлами фенолы ведут себя, как кислоты.
| Например, фенол взаимодействует с натрием с образованием фенолята натрия и водорода . |

2. Реакции фенола по бензольному кольцу
| Наличие ОН-группы в бензольном кольце (ориентант первого рода) приводит к тому, что фенол гораздо легче бензола вступает в реакции замещения в ароматическом кольце. |
2.1. Галогенирование
| Фенол легко при комнатной температуре (без всякого катализатора) взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол). |

2.2. Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов.
| Например, при нитровании фенола избытком концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота): |

3. Поликонденсация фенола с формальдегидом
С формальдегидом фенол образует фенолоформальдегидные смолы.

4. Взаимодействие с хлоридом железа (III)
При взаимодействии фенола с хлоридом железа (III) образуются комплексные соединения железа, которые окрашивают раствор в сине-фиолетовый цвет. Это качественная реакция на фенол.
5. Гидрирование (восстановление) фенола
Присоединение водорода к ароматическому кольцу.
Продукт реакции – циклогексанол, вторичный циклический спирт.

1. Взаимодействие хлорбензола с щелочами
При взаимодействии обработке хлорбензола избытком щелочи при высокой температуре и давлении образуется водный раствор фенолята натрия.

При пропускании углекислого газа (или другой более сильной кислоты) через раствор фенолята образуется фенол.

2. Кумольный способ
Фенол в промышленности получают из каталитическим окислением кумола.
Первый этап процесса – получение кумола алкилированием бензола пропеном в присутствии фосфорной кислоты:

Второй этап – окисление кумола кислородом. Процесс протекает через образование гидропероксида изопропилбензола:

Суммарное уравнение реакции:
3. Замещение сульфогруппы в бензол-сульфокислоте
Бензол-сульфокислота реагирует с гидроксидом натрия с образованием фенолята натрия:
Фенолы – органические соединения. Они в небольших количествах есть в природе. Основную массу фенола и производных на его основе получают синтетическим путём.
Что такое фенол
К фенолам относят производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с фенил радикалом. Они могут иметь одну или несколько гидроксогрупп.

Самым простым представителем этой группы соединений считают фенол. Он и дал название классу веществ. Это же соединение называют гидроксибензолом.
Общая и структурная формулы
Состав веществ можно выразить общей формулой С6Н6-n(ОН)n.
Простейший представитель класса имеет 1 гидроксогруппу. Его молекулярная формула С6Н5ОН. Структурная формула — ОН.
Если в молекуле фенола 1 атом водорода заместить на метильный радикал, получим метилфенол. Если к нему прибавить ещё одно бензольное ядро, получим нафтол.
Химические свойства фенола
Так как гидроксибензол содержит в своём составе 2 группы атомов, выделяют две группы химических свойств.
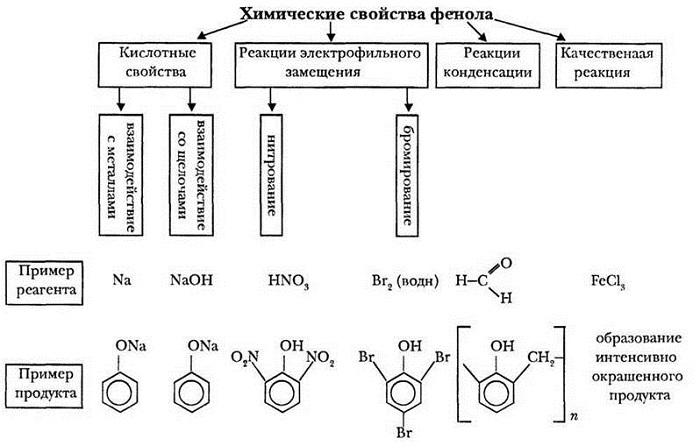
Свойства, идущие за счет фенил радикала:
Свойства, протекающие за счёт гидроксильной группы (кислотные свойства):
взаимодействие с активными металлами;
взаимодействие со щелочами.
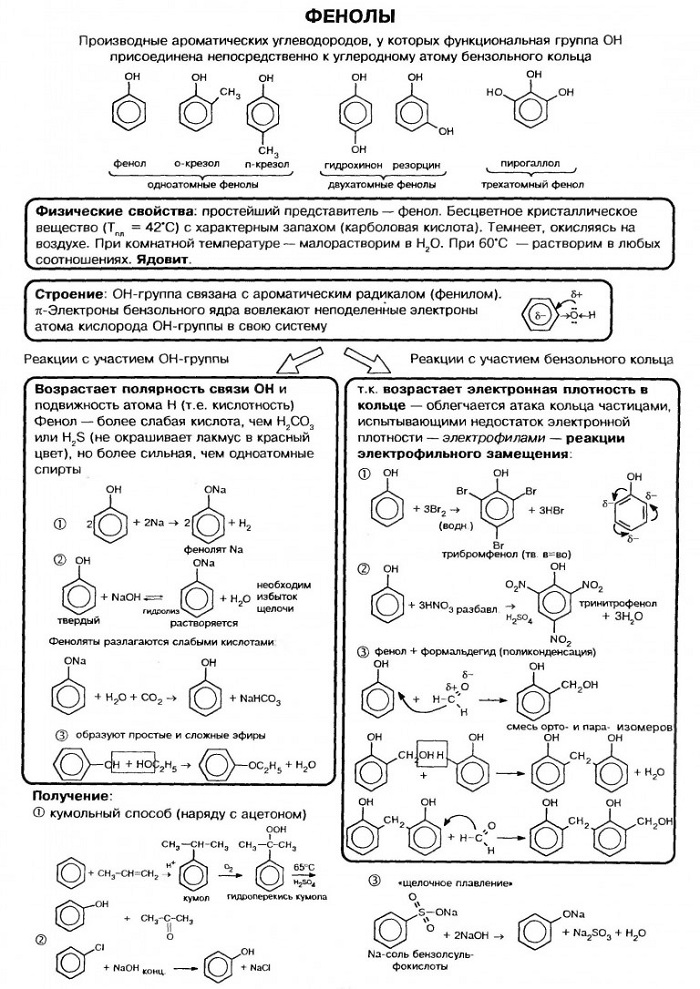
Не следует понимать, что фенол, имея в своем составе черты строения бензола и спиртов, просто повторяет их свойства. На самом деле все сложнее. Чтобы понять особенность его химических взаимодействий, необходимо знать строение вещества. В молекуле фенола наблюдается взаимное влияние атомов.
На атоме кислорода гидроксильной группы есть 2 неподелённые электронные пары. Они взаимодействуют с π – электронной системой фенил радикала.
Результат взаимодействия следующий:
Нарушается равномерное распределение электронной плотности в фенил радикале. Она возрастает на атомах 2,4,6, то есть в орто– и параположениях. Именно в этих положениях водород будет легко замещаться на другие атомы.
Атом водорода гидроксогруппы, из-за влияния фенил радикала, приобретает положительный заряд и становится более подвижным.
Результатом влияния служат своеобразные свойства фенола. Он реагирует с активными металлами и щелочами. Спирты – только с металлами. В то же время и бензол, и гидроксибензол реагируют с бромной водой. Но у фенола, в отличие от бензола, идет замещение сразу по 3 атомам.
Физические свойства
С6Н5ОН – это белое кристаллическое вещество. В результате окисления кристаллы могут приобретать розовый цвет. Температура плавления 40,9 0 С. Молярная масса 94 г/моль.

Отличается характерным резким запахом. Вещество ядовито. Проникая в организм человека, вызывает тяжёлое отравление.
С чем реагирует фенол
Гидроксибензол вступает в реакцию с активными металлами. С натрием даёт фенолят натрия. Уравнение выглядит следующим образом:
2 С6Н5ОН + 2Na = 2С6Н5ОNa + H2
В реакциях со щелочами также образует феноляты. Реагируя с гидроксидом калия, образует фенолят калия:
С6Н5ОН + KOН = С6Н5ОK +H2O
Взаимодействуя со спиртами, образует эфиры. Например, в реакции с бутанолом, получают простой эфир:
С6Н5 ОН + НО–С4Н9 = С6Н5–О–С4Н9 +Н2О
Из свойств, протекающих за счёт фенил радикала, можно отметить реакцию нитрования. Взаимодействие с HNO3 даёт 2,4,6 тринитрофенол (пикриновую кислоту):
С6Н5ОН + 3HNO3 = C6H2(NO2)3OH +3H2O
Реагируя с формальдегидом, фенол образует фенолформальдегидную смолу. Это реакция поликонденсации – получение высокомолекулярного вещества из низкомолекулярных веществ с отщеплением побочного продукта. В данном случае – это вода.
Качественные реакции на фенол
К качественным реакциям относят взаимодействие с бромной водой. В результате получают осадок белого цвета:
С6Н5ОН + 3Br2 = C6H2Br3ОН + 3HBr
Ещё одной качественной реакцией является взаимодействие с хлоридом железа(III). Получается фиолетовое окрашивание. Качественные реакции позволяют разделить и определить органические вещества.
Реакция присоединения
К реакциям присоединения относят гидрирование ароматического ядра. Гидрирование – это реакции присоединения водорода. Превращение протекает легко, в присутствии катализатора. В результате разрушается π – электронная система, образуется циклогексанол и циклогексанон:
2С6Н5ОН + 5Н2 = С6Н11ОН + С6Н10О
Окисление
Фенол не устойчив к окислению. Продукты реакции могут быть разными. Это зависит от самого окислителя и от условий, в которых протекает реакция. При окислении перекисью водорода получается двухатомный фенол:
С6Н5ОН + Н2О2 = С6Н4(ОН)2
К реакции окисления относят и реакцию горения. Образуется углекислый газ и вода.
Получение фенола
Фенол в небольшом количестве содержится в каменноугольной смоле. Но потребности в веществе настолько велики, что этого источника недостаточно.
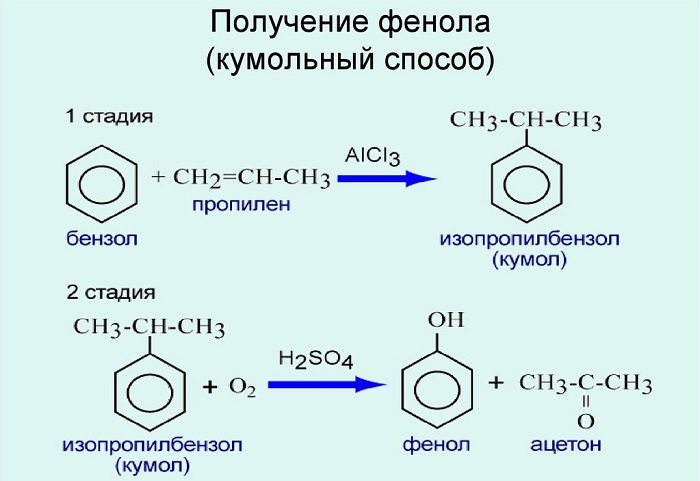
Разработаны разные способы получения:
По схеме С6Н6 ----- С6Н5Cl ----- С6Н5ОН. Минусом метода являются жёсткие условия замещения хлора на гидроксогруппу. Реакции приходится проводить при высокой температуре и давлении.
Используют для получения бензол и пропилен, в результате чего получают кумол. Затем кумол окисляют, в результате получают ценные продукты – фенол, ацетон.
Применение
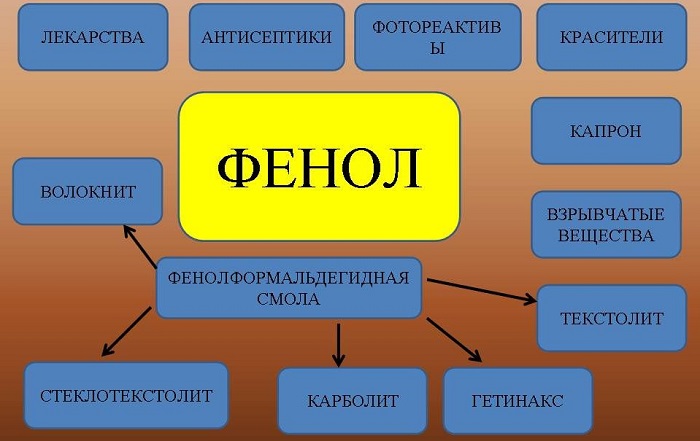
Вещество применяют для производства разнообразной продукции:
фенолформальдегидных смол и пластмасс;
раствор фенола в воде обладает антисептическими свойствами;
искусственных волокон и другой продукции.
Заключение
Фенол и фенольные соединения – очень важная группа веществ. Не следует забывать, что многие из них являются ядами. Все отходы промышленности, содержащие вещество, тщательно очищаются. Их подвергают каталитическому окислению, обработке озоном и другим способам очистки.

Фенол относится к ароматическим углеводородам и образует гомологический ряд. Вещество имеет схожее строение с бензолом, но отличается наличием группы -ОН. Главный способ получения фенола – окисление кумола.
Строение и свойства
Молекула фенола содержит бензольное кольцо. Один атом водорода замещён гидроксильной группой. Молекулярная формула фенола – C6H5OH.
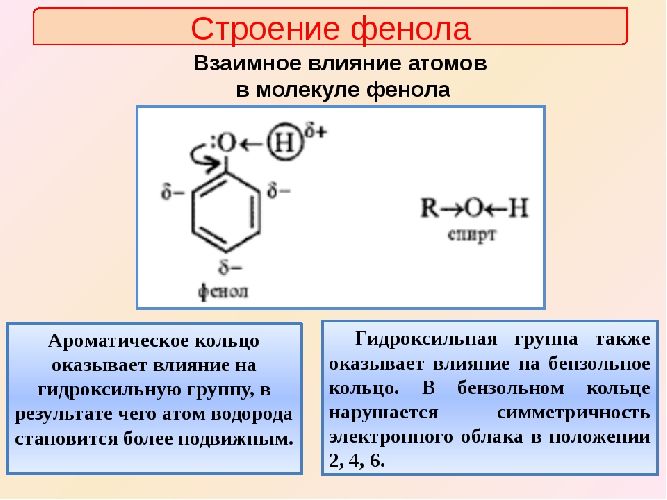
Рис. 1. Строение фенола.
При замещении атомов водорода предельными углеводородными радикалами фенол образует гомологический ряд. Общая формула гомологов – CnH2n-7OH, где n – не меньше шести.
Для гомологов фенола, как и для гомологов бензола, характерна структурная изомерия по положению углеводородного радикала в бензольном кольце и по строению заместителей.
Фенолы классифицируются по количеству гидроксильных групп на четыре вида:
Фенол – кристаллическое бесцветное вещество. Кристаллы напоминают мелкие иголки. Соединение быстро розовеет на воздухе. Фенол токсичен: оставляет ожоги на коже.
Помимо фенолов и его гомологов, содержащих одно бензольное кольцо, существуют схожие по строению и свойствам многоядерные соединения. Нафтолы содержат два бензольных кольца, антролы – три, фенантролы – четыре, бензотетролы – пять.
Получение
Фенол получают в промышленности окислением ароматических углеводородов, а также выделением из каменноугольной смолы. Основные способы получения фенола представлены в таблице.
Способ
Описание
Уравнение
Безотходная технология, позволяющая получить до 99 % полезных продуктов. Сырьём являются бензол и пропилен, из которых получают кумол. Далее кумол подвергают окислению при высокой температуре в присутствии катализатора до образования гидропероксид кумола. Это вещество подвергается разложению в кислой среде (чаще используется разбавленная серная кислота). В результате образуются фенол и ацетон. Побочным продуктом является α-метилстирол (изопренилбензол)
Получают примерно 6 % фенола. При окислении кислородом воздуха в присутствии катализатора образуется бензойная кислота. Полученное вещество окисляют солями меди (II) на воздухе в присутствии водяного пара
Например, из хлорбензола в присутствии катализатора при нагревании со щёлочью или водой образуется фенол
Из каменноугольной смолы
Небольшое количество получают из обработанной щёлочью каменноугольной смолы. В результате образуются феноляты – соли фенола. Затем их обрабатывают кислотой до выделения фенола
Из ароматических сульфокислот
Сплавление сульфокислот с твёрдыми щелочами с образованием феноксидов, которые обрабатываются сильными кислотами
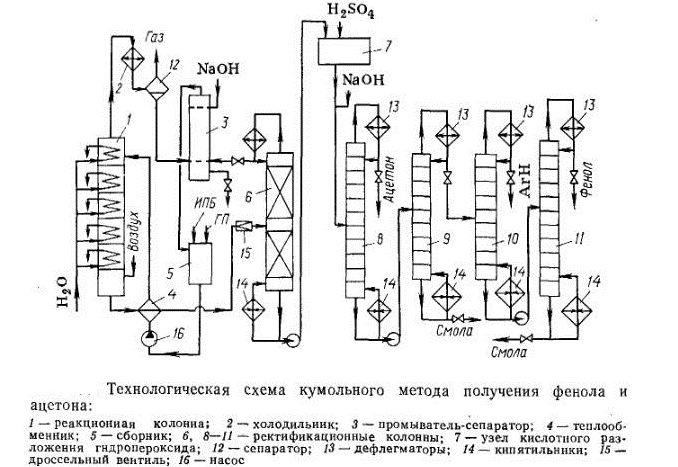
Рис. 3. Технологическая схема кумольного метода получения фенола и ацетона.
Фенол используется для производства других химических соединений, а также для дезинфекции.
Что мы узнали?
Фенол – бесцветное кристаллическое вещество с токсичными свойствами. Отличается от бензола гидроксильной группой. Имеет формулу C6H5OH. При присоединении углеводородных радикалов образует гомологический ряд с общей формулой CnH2n-7OH. Фенол получают в промышленности из кумола, толуола, галогенбензолов, каменноугольной смолы и ароматических сульфокислот. Кумольный способ самый производительный: можно получить до 99 % полезных веществ.
Читайте также:

