Специфические способы получения этилового спирта кратко
Обновлено: 05.07.2024
Характеристики и физические свойства этилового спирта
Этиловый спирт (этанол) представляет собой бесцветную жидкость со слабым запахом, легко воспламеняется.
Смешивается с водой во всех соотношениях. Этанол хорошо растворяет многие органические вещества. Безводный (абсолютный) спирт кипит при 78,37 o С. Получаемый в промышленности спирт-ректификат представляет собой смесь 95,5% этанола и 4,4% воды, которая кипит при 78,37 o С (смеси определенного состава, кипящие при постоянной температуре, называют азеотропными смесями).
Основные константы этилового спирта приведены в таблице ниже.
Таблица 1. Физические свойства этилового спирта.
Плотность, г/см 3
Температура плавления, o С
Температура кипения, o С
Молярная масса, г/моль
Получение этилового спирта
Получение этилового спирта можно осуществить следующими способами:
— гидролиз моногалогеналканов водными растворами щелочей
— гидрирование альдегидов и кетонов
Химические свойства этилового спирта
Для этанола возможны реакции, протекающие с участием:
— атома водорода гидроксильной группы;
— атома водорода гидроксильной группы и связи Cα-H;
— гидроксильной группы и связи Cβ-H.
Таким образом, все химические превращения, характерные для этилового спирта сопровождаются расщеплением связей:
— взаимодействие с активными металлами
— взаимодействие с органическими и кислородсодержашими неорганическими кислотами
— взаимодействие с галогеноводородами
— взаимодействие с тригалогенидамифосфора
— взаимодействие с аммиаком
Применение этилового спирта
Этиловый спирт широко используется в промышленном органическом синтезе. В фармации он применяется для приготовления настоек и экстрактов; в медицинской практике – как наружное антисептическое средство для дезинфекции рук и хирургических инструментов.
Примеры решения задач
| Задание | В пропанол-1 поместили металлический натрий. К реакционной смеси добавили бромэтан. Какое вещество при этом образуется. Составьте уравнения протекающих реакций. |
| Ответ | При действии металлического натрия на пропанол-1 образуется соединение подобное соли, называемое алкоголятом: |
Последующее добавление к реакционной смеси бромэтан привело к образованию простого эфира (пропилэтилового) [реакция Вильямсона]:
Этилен → Этанол →Диэтиловый эфир →Иодоэтан→ Бутан.
Укажите условия протекания реакций.
Спирты способны подвергаться межмолекулярной дегидратации в результате чего происходит образование простых эфиров. Данная реакция протекает под действие водоотнимающих реагентов, например, серной кислоты:
При действии иодоводорода на диэтиловый эфир в кислой среде происходит его расщепление на иодоэтан и этанол:

1. Щелочной гидролиз галогеналканов
При взаимодействии галогеналканов с водным раствором щелочей образуются спирты. Атом галогена в галогеналкане замещается на гидроксогруппу.
| Например, при нагревании хлорметана с водным раствором гидроксида натрия образуется метанол |

| Например, глицерин можно получить щелочным гидролизом 1,2,3-трихлорпропана: |

2. Гидратация алкенов
Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
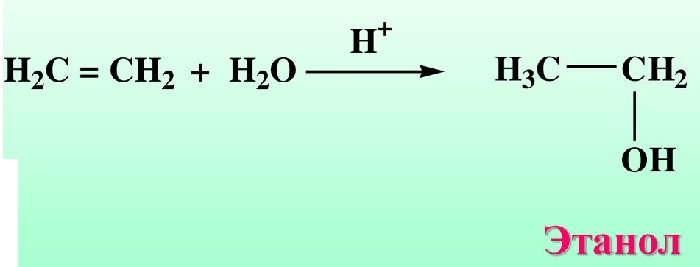
| Например, при взаимодействии этилена с водой образуется этиловый спирт. |

Гидратация алкенов также протекает по ионному (электрофильному) механизму.
Для несимметричных алкенов реакция идёт преимущественно по правилу Марковникова.
| Например, при взаимодействии пропилена с водой образуется преимущественно пропанол-2. |

3. Гидрирование карбонильных соединений
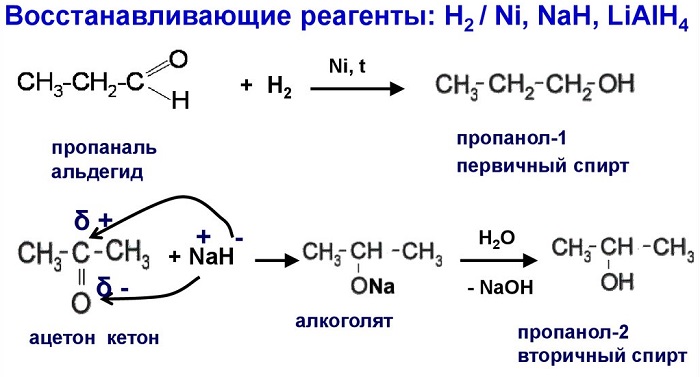
Присоединение водорода к альдегидам и кетонам протекает при нагревании в присутствии катализатора. При гидрировании альдегидов образуются первичные спирты, при гидрировании кетонов — вторичные спирты, а из формальдегида образуется метанол.
| Например, при гидрировании этаналя образуется этанол |
| Например: при гидрировании ацетона образуется изопропанол |

| Например, гидрирование диальдегида – один из способов получения этиленгликоля |

4. Окисление алкенов холодным водным раствором перманганата калия
Алкены реагируют с водным раствором перманганата калия без нагревания. При этом образуются двухатомные спирты (гликоли).

Каталитический синтез метанола из монооксида углерода и водорода при 300-400°С и давления 500 атм в присутствии смеси оксидов цинка, хрома и др.
6. Получение этанола спиртовым брожением глюкозы
Для глюкозы характерно ферментативное брожение, то есть распад молекул на части под действием ферментов. Один из вариантов — спиртовое брожение.

7. Гидролиз жиров – способ получения многоатомных спиртов
Под действием кислоты жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например: при гидролизе тристеарата глицерина образуется глицерин и стеариновая кислота |

При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
| Например: при щелочном гидролизе тристеарата глицерина образуется глицерин и соль стеариновой кислоты (стеарат) |

Добавить комментарий
Этот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев.
К наиболее часто используемым химическим способам получения спиртов относятся:
1.Гидратация алкенов (промышленный способ получения этанола для технических целей)
(t, Р, кислая среда (катализатор))
2.Щелочной гидролиз галогеналканов (лабораторный способ получения)
(водный раствор щелочи, t)
3.Восстановление альдегидов и кетонов (лабораторный способ получения)
(t, катализатор –Ni)
Особые способы получения метанола и этанола
1.Получение метанола из синтез-газа (водяной газ, генераторный газ)
(t, Р, оксидные катализаторы)
2.Получение этанола ферментативным брожением глюкозы (получение этилового спирта для пищевых и медицинских целей)
1. Гидратация алкенов
Гидратация алкенов используется в промышленности для получения спиртов из продуктов нефтепереработки.
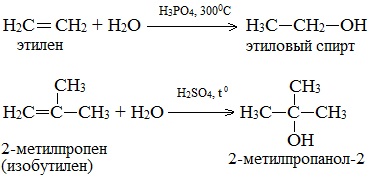
Присоединение воды к алкенам происходит в присутствии разбавленной серной или фосфорной кислот. Эта реакция протекает в соответствии с правилом Марковникова, поэтому первичный спирт можно получить только из этилена, а остальные алкены дают вторичные или третичные спирты:
Этот метод в лабораторных условиях нашел ограниченную область применения для получения третичных спиртов.
2. Гидролиз галогеналканов в водном растворе щелочи
В лабораторных условиях спирты получают действием водного раствора щелочи на алкилгалогениды при нагревании, при этом атом галогена в галогеналкане замещается группой –ОН:
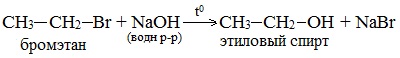
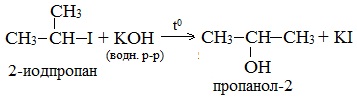
С помощью этой реакции можно получать первичные, вторичные и третичные спирты.
При действии спиртового раствора щелочи на галогеналканы происходит отщепление галогеноводорода и образование алкена.
3. Восстановление карбонильных соединений (альдегидов и кетонов)
Дегидрирование спиртов по своей химической сущности является окислением. Обратная реакция – гидрирование альдегидов, кетонов и эфиров карбоновых кислот – является, таким образом, их восстановлением.
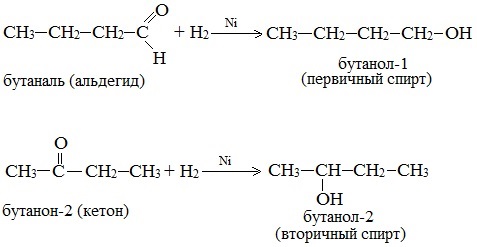
При действии водорода в присутствии катализаторов (Ni, Pt, Pd) альдегиды восстанавливаются до первичных спиртов, а кетоны – до вторичных спиртов:
4. Восстановление эфиров карбоновых кислот
Гидрирование сложных эфиров проходит через стадию образования альдегидов:
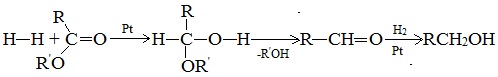
Этим методом в промышленности из метиловых эфиров высших кислот получают высшие первичные спирты, например:
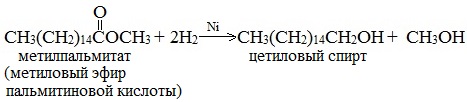
5. Гидролиз сложных эфиров карбоновых кислот в щелочной среде
Гидролиз сложных эфиров карбоновых кислот протекает как в кислой, так и в щелочной среде (водные или спиртовые растворы NaOH, КОН, а также Ba (OH)2, Ca (OH)2, Ba (OH)2, Ca (OH)2). Однако к образованию спиртов приводит гидролиз, протекающий необратимо в щелочной среде:
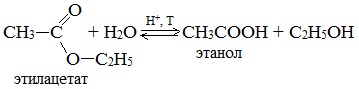
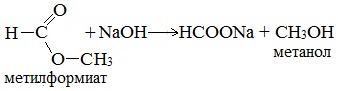
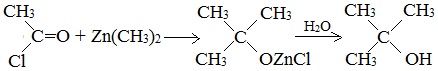
6. Синтез спиртов из карбонильных соединений с помощью магнийорганических соединений
Спирты образуются при многочисленных реакциях металлоорганических соединений с различными соединениями, содержащими карбонильную группу >С=О. Этим способом можно получать как первичные спирты, так и вторичные и третичные:
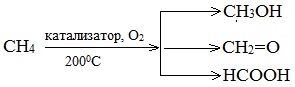
7. Окисление алканов
При мягком окислении метана кислородом воздуха в присутствии различных катализаторов образуются метанол, формальдегид или муравьиная кислота:
Специфические способы получения метанола и этанола
Производство метанола крупнотоннажное, т.к. метиловый спирт является исходным веществом для получения других продуктов органического синтеза.
В промышленности
1. Получение метанола из синтез-газа (водяной газ, генераторный газ)
а) Конверсия природного газа в синтез-газ
Его получают из метана с перегретым водяным паром:
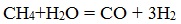
б) Каталитический синтез метанола из оксида углерода (II) и водорода
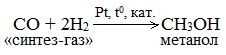
В качестве катализаторов используют смесь оксидов цинка, меди и хрома, температуру поддерживают в интервале 200-300 о С, а давление – от 40 до 150 атм.
Газ на выходе из реактора содержит 3-5% CH3OH, затем газ охлаждают и конденсируют полученный метанол, а оставшийся газ смешивают с исходным газом и направляют снова в реактор.
2. Получение этанола спиртовым брожением глюкозы
Ферментативный гидролиз крахмала – наиболее древний синтетический процесс, используемый человеком – до сих пор имеет огромное значение для получения этилового спирта.
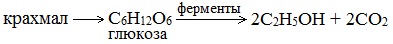
Протекает только в присутствии ферментов, которые вырабатывают некоторые микроорганизмы, например, дрожжи:
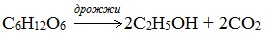
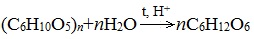
Глюкоза содержится во фруктовых соках. Глюкозу можно получить гидролизом крахмала (зерно, картофель, целлюлозные опилки):
Высокий уровень развития науки химии и инновационные технологии позволили применять различные способы получения спиртов. Статистические данные свидетельствуют о росте спроса на производство данных видов органических соединений в промышленных масштабах.
К спиртам относят вещества, химическая формула которых включает гидроксильные группы (ковалентно связанные атомы кислорода и водорода - НО).
В зависимости от количества гидроксилов выделяют:
Одноатомные спирты - получают путем преобразования предельных углеводородов (алканов). Виды одноатомных органических соединений: пропанол 1 и 2; метанол; этанол и другие.
Полиолы (многоатомные спирты), к которым относятся: двухатомные (гликоли). Диол этиленгликоль выделяют из этилена. Триол (глицерин) относится к трёхатомным спиртам.

Классифицируют органические соединения по виду углеводородных радикалов: предельные, непредельные, ароматические.
Различают по месту привязки гидроксильной группы в молекулярной цепи: первичные, вторичные и т. д.
Свойства зависят от всех элементов молекулярного строения в совокупности.
Химические способы получения спиртов
Получают двумя основными способами: химическим (синтетические спирты) и биохимическим (биоспирты).
От метода получения, исходного сырья зависят свойства вещества, его целевое использование в промышленном, пищевом производстве. Для первого вида основным сырьём служит древесина и нефтепродукты. Этанол, полученный из этих продуктов в качестве технического спирта, используют в химическом, промышленном производстве. Он содержит определённое количество вредных примесей.
Применение биохимического способа предполагает использование в качестве исходного сырья продуктов растительного происхождения. Этим способом получают медицинский, пищевой этанол.
Получение спиртов из галогеноуглеводородов
Гидролиз галогенопроизводных происходит на основе реакции нуклеофильного замещения. Реагент на внешнем уровне молекулы имеет неопределённые пары электронов, которые отрываются и перестраивают молекулярную решётку.
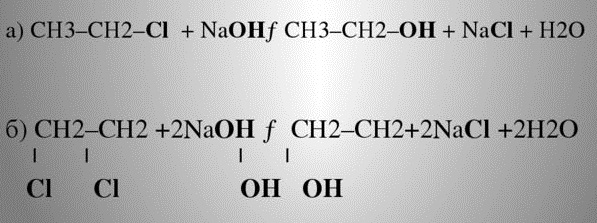
Под воздействием паров воды, щелочного раствора (реагента), температуры, галоген замещается гидроксилом, образуется спиртосодержащее органическое соединение.
Щелочной гидролиз галогеноалкенов — промышленный способ получения технического этанола из этилена.
Получение спиртов из алкенов
Алкены — этиленовые углеводороды. К ним относят бутен, этилен, пропилен и т. д. Их молекулярная цепочка включает двойную связь атомов углерода (Н₂С).
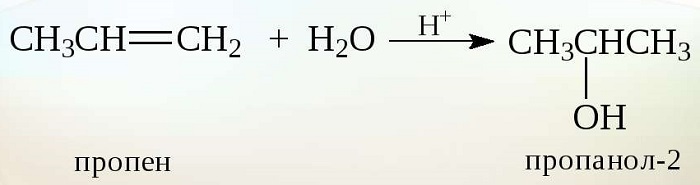
Существует два основных способа получения алкенов:
методом крекинга углеводородов (нефти и газа);
В зависимости от вида алкенов, в условиях высокой температуры (ориентировочно 300⁰С), давления (до 70 атмосфер) из водных растворов кислот образуются спирты. В промышленном производстве чаще в качестве реагента выступает ортофосфорная кислота.
Этот способ подходит для производства этилового и вторичных спиртов. К примеру из пропилена получают пропанол 2.
Получение из простых алкенов и спиртов
Спиртосодержащие органические соединения получают в результате реакции гидроборирования. Первичное сырьё (алкены) под воздействием раствора перекиси водорода гидролизуются, получают спирты.
Гидратация — процесс сложный. Он происходит в два этапа:
Промежуточное соединение вступает в реакцию со щелочным раствором перекиси водорода.
Гидроборирование — быстрый и удобный способ получения первичных спиртов. Подобный процесс происходит при нагревании вторичных спиртов, обработки их щелочными растворами перекисью водорода.
Получение спиртов из альдегидов и кетонов
Альдегиды и кетоны - вещества, в составе которых присутствует карбонильная группа (-СНО). У альдегидов –СНО связан с водородом и одним углеводородным радикалом. У кетонов 2 связи – СНО с радикалами.

Восстановление молекулы спирта происходит при нагревании с использованием никелевого катализатора. Реакция восстановления позволяет получать из альдегидов первичные спирты, из кетонов — вторичные.
Получение спиртов из карбоновых кислот и сложных эфиров
Процесс превращения карбоновых кислот, сложных эфиров в спиртоорганические соединения основан на реакции гомологизации. В результате дополнения метиленовых групп к молекулам кислот, эфиров образуются гомолог, спирт. Катализаторами процесса выступают алюмогидрид лития.
![]()
Сложный процесс проходит в несколько этапов:
Сначала в эфирную суспензию добавляется карбоновая кислота.
Её разделяют на фракции при помощи кислот, щелочных растворов.
Характерно, что это процесс взаимообратный. Из спиртосодержащих веществ синтезируют карбоновые кислоты, сложные эфирные соединения.
Получение спиртов восстановлением эпоксидов и карбонильных соединений
Оксираны (эпоксиды) или эпоксидные соединения — простые эфиры циклической формы с атомом кислорода.
Под воздействием реагентов литийдиалкилкупратов происходит разрыв кольцевой структуры молекулы, образуются молекулы органических спиртосодержащих соединений.
Получение спиртов с использованием металлорганических соединений
Исходным сырьём для получения служат карбоновые кислоты и их производные, эфиры, кетоны. Металлоорганические соединения кадмия, ртути, алюмний бромид, диалкилкупраты щелочных металлов - они вступают в реакцию с исходными компонентами (метод Гильмана). В качестве растворителя используют чаще хлористый метилен. Реакция происходит при низких температурах.
Получение спиртов окислительными методами
Используется несколько методик преобразования ненасыщенных спиртов с использованием разных реагентов и апротонных растворителей. Последние способны растворять ионные реагенты.

окисление диоксидом марганца + органический растворитель;
с использованием пентана, хлористого метилена;
окислители на основе хрома (6 валентного), марганца (6-7 валентного).
Процент выхода зависит от типа используемого реагента.
Другие способы получения спиртов
Существуют и другой способ - биохимического брожения сырья растительного происхождения. Лучше всего для этих целей подходят продукты с высоким содержанием сахара, клетчатки, крахмала. Под воздействием дрожжей, отдельных видов бактерий, плесневых грибов происходит брожение массы.
В сусле углеводы биомассы разделяются на углекислый газ, воду и этанол. Методом дистилляции выделяют его из перебродившего сусла. После ректификации (очищения), чистота этанола составляет 95-100%. Класс пищевого спирта определяет степень очистки, исходное сырьё для его производства.
Множество способов получения спиртов обусловлено широким спектром спиртосодержащих соединений и их свойствами.
Читайте также:


