Рибосомы история открытия кратко
Обновлено: 05.07.2024
Более шестидесяти лет тому назад, в 1953 г., Д. Уотсон и Ф. Крик открыли принцип строения дезоксирибонуклеиновой кислоты [1]. Структура ДНК пролила свет на механизм точного воспроизведения – удвоения генетического материала [2].
Содержание
Введение
Глава 1. Строение рибосом
Глава 2. История открытия рибосом
Глава 3. История развития методов изучения рибосом
3.1. Электронная микроскопия
3.2. Рентгеноструктурный анализ (РСА)
3.3. Футпринтинг (химическое зондирование)
3.4. Аффинная модификация
3.5. Другие методы исследования рибосом
Заключение
Список использованных источников
Введение
Более шестидесяти лет тому назад, в 1953 г., Д. Уотсон и Ф. Крик открыли принцип строения дезоксирибонуклеиновой кислоты [1]. Структура ДНК пролила свет на механизм точного воспроизведения – удвоения генетического материала [2]. Произошло становление новой науки — молекулярной биологии. Была сформулирована так называемая центральная догма молекулярной биологии: ДНК → РНК → белок, смысл которой состоит в том, что генетическая информация, записанная в ДНК, реализуется в виде белков, но не непосредственно, а через участие родственного биополимера — рибонуклеиновую кислоту (РНК), и этот путь от нуклеиновых кислот к белкам необратим. Таким образом, ДНК копируется по матрице ДНК, обеспечивая собственную репликацию, то есть воспроизведение исходного генетического материала в поколениях; РНК синтезируется по матрице ДНК, в результате чего происходит переписывание, или транскрипция, генетической информации в форму различных копий РНК; молекулы иРНК служат матрицами для синтеза белков — генетическая информация транслируется в форму полипептидных цепей.
Итак, важнейшим процессом жизнедеятельности всех организмов — от примитивных бактерий до человека, — является реализация генетической информации, закодированной в их ДНК. Завершающим этапом этого процесса является трансляция (биосинтез белков на рибосомах) – перевод последовательности нуклеотидов информационной (матричной) РНК-комплементарной копии ДНК, в последовательности аминокислотных остатков синтезируемых белков. Белки – биополимеры, ответственные практически за все биохимические реакции, происходящие в клетках живых организмов, — определяют большинство признаков организма, осуществляют регуляцию и координацию его жизнедеятельности. Трансляция осуществляется сложными клеточными надмолекулярными машинами – рибосомами. Именно они ответственны за сложный, многоэтапный процесс биосинтеза всех без исключения клеточных белков.
Глава 1. Строение рибосом
Чтобы читателю было легче воспринимать дальнейший материал, считаю необходимым привести краткую характеристику объекта, об истории открытия и изучения которого в дальнейшем пойдет речь. Итак, рибосомы – это клеточные органоиды (есть и у прокариот – одноклеточных организмов, у которых нет оформленного ядра, к которым относятся бактерии и археи, и у эукариот – настоящих ядерных – организмов, у которых в клетке есть ядро, к ним относятся как одноклеточные, так и многоклеточные представители царств грибов, растений и животных; эукариоты устроены гораздо сложнее, что влечёт за собой усложнение организации их клеточных структур, в связи с чем весьма затруднено их изучение), ответственные за биосинтез белка. Каждая рибосома состоит из двух субчастиц – большой и малой, которые в свою очередь, состоят из рибосомных РНК (рРНК) и нескольких десятков рибосомных белков. Агрегаты РНК и белков принято называть рибонуклеопротеинами.
Глава 2. История открытия рибосом
История изучения строения рибосом насчитывает более полувека со времени их открытия, и краткое описание методов, использованных для этого, представляет отдельный интерес, поскольку эти методы используются или могут быть использованы для изучения не только рибосом, но и других сложных надмолекулярных комплексов.
Итак, к 1940 г. Альберт Клод (США) сумел выделить из эукариотических клеток цитоплазматические РНК-содержащие гранулы, гораздо меньшие, чем митохондрии и лизосомы (от 50 до 200 мкм в диаметре); позже он назвал их микросомами. Результаты химических анализов показали, что микросомы Клода были рибонуклеопротеидными комплексами. В дополнение к этому, цитохимические работы Т. Касперсона (Швеция) и Ж.Браше (Бельгия) продемонстрировали, что чем интенсивнее идет белковый синтез, тем больше обнаруживается РНК в цитоплазме.
В дальнейшем, некоторым исследователям удавалось выделять из клеток бактерий, животных и растений частицы, ещё более мелкие, чем микросомы. Электронная микроскопия и седиментационный анализ в ультрацентрифуге указывали, что частицы компактны, более или менее сферичны и гомогенны по размеру, имея диаметр 100-200 Ȧ (ангстрем) и обнаруживая резкие седиментационные границы с коэффициентами седиментации от 30-40S до 80-90S (S-коэффициент седиментации, или константа Сведберга, — отражает скорость осаждения каких-либо молекулярных комплексов при скоростном ультрацентрифугировании и зависит от молекулярного веса частиц и их плотности – компактности). Пожалуй, первое ясное свидетельство, что такие частицы бактерий являются рибонуклеопротеидами было получено Г.К. Шахманом, А.Б. Парди и Р. Станиером (США) в 1952 г.
Нужна помощь в написании реферата?
Мы - биржа профессиональных авторов (преподавателей и доцентов вузов). Наша система гарантирует сдачу работы к сроку без плагиата. Правки вносим бесплатно.
Исследования функциональной роли рибосом шли параллельно с их обнаружением и структурным описанием. Первой убедительной демонстрацией того, что именно рибонуклеопротеидные частицы микросом ответственны за включение аминокислот в новосинтезированный белок, были эксперименты П. Замечника с сотрудниками (США), опубликованные в 1955 г. За этим последовали эксперименты из этой же лаборатории, показавшие, что свободные рибосомы не прикрепленные к мембранам эндоплазматического ретикулума, также включают аминокислоты и синтезируют белок, освобождающийся затем в растворимую фазу. Функции бактериальных рибосом были предметом интенсивных исследований группы Р.Б. Робертса (США); публикация К. МакКиллена, Р.Б. Робертса и Р.Дж. Бриттена [4] в 1959 г. окончательно установила, что белки синтезируются в рибосомах и затем распределяются по другим частям бактериальной клетки.
Глава 3. История развития методов изучения рибосом
3.1. Электронная микроскопия
Электромикрофотография субчастиц рибсосом (слева) и одна из первых моделей малой 30S субчастицы бактерий (справа), 1974 г.
Крио-ЭМ модели субчастиц человеческих рибосом, 2013 г. Подписаны рибосомные белки и некоторые морфологические элементы субчастиц.
Преимуществом крио-ЭМ по сравнению с РСА (рентгеноструктурный анализ) является то, что этот метод не требует выращивания кристаллов – процедуры длительной и не всегда дающей результат. Кроме того, для крио-ЭМ требуется намного меньше материала, чем для РСА. К недостаткам крио-ЭМ следует отнести то, что разрешение, которое может дать этот метод, пока не позволяет четко “видеть” неструктурированные нитевидные фрагменты рибосомных белков и рРНК, триплеты иРНК и некоторые другие важные детали.
3.2. Рентгеноструктурный анализ (РСА)
Методы рентгеноструктурного анализа позволяют судить о строении биологических макромолекул и их комплексов (в частности, эти методы помогли установить в 1953 году структуру ДНК). В основе рентгеноструктурного анализа лежит получение кристаллов макромолекул и просвечивание их рентгеновскими лучами. По характеру дифракции рентгеновских лучей, проходящих через эти кристаллы, можно судить о строении образующих кристаллы молекул. Если кристаллы хорошего качества, то такую картину можно расшифровать с помощью специальных компьютерных программ, и это в принципе позволяет определить координаты всех атомов, из которых они построены. Поэтому РСА считают одним из наиболее мощных и информативных методов для изучения строения рибосом и других сложных белково-нуклеиновых комплексов.
К недостаткам метода можно отнести, в первую очередь, трудности кристаллизации – до сих пор кристаллизация сложных рибонуклеопротеидов является скорее не наукой, а искусством, которым владеют лишь в нескольких лабораториях в мире. Даже к началу восьмидесятых годов XX века никому еще не удавалось получить пригодные для анализа кристаллы ни полных рибосом, ни их отдельных субъединиц. Вообще, кристаллизация каждого нового модельного комплекса рибосом с участниками процесса трансляции является событием.
Получить пригодные для РСА кристаллы рибосомных субчастиц даже простейших эукариот удалось впервые лишь в 2010 г. (это было сделано в группе М. Юсупова в Страсбурге). Определенные с помощью РСА координаты атомов рибосом и их модельных комплексов помещают в доступный через интернет банк данных, каждая структура имеет свой код, который известен из публикаций в научных журналах. Визуально структурную информацию можно представлять любым удобным образом. В качестве примера ниже приведена структура малой субчастицы рибосом термофильной бактерии Thermus thermophilus, полученная в 2002 г. в лаборатории В. Рамакришнана — одного из трех Нобелевских лауреатов по химии 2009 г., получивших премию за расшифровку структуры рибосомы. На этой структуре полипептидные цепи белков и полинуклеотидные цепи рРНК изображены ленточками.
Строение малой субчастицы рибосом Thermus thermophilus по данным РСА, 2002 г.
3.3. Футпринтинг (химическое зондирование)
Следует иметь в виду, что данные футпринтинга в определенной степени неоднозначны, поскольку защита любого нуклеотида рРНК от химической модификации или гидролиза может быть связана не только с тем, что он экранирован лигандом, но и с вторичными эффектами — например, структурными перестройками в рРНК, вызванными связыванием лиганда в отдаленном от этого нуклеотида участке рибосомы. Наиболее информативным оказывается применение и химического, и энзиматического пробинга одновременно. Эти методы дают взаимно дополняющую информацию, поскольку, как правило, участки, где меняется доступность нуклеотидов для химической модификации, не совпадают с участками, где меняется доступность фосфодиэфирных связей для гидролиза ферментами.
3.4. Аффинная модификация
Аффинная модификация, или аффинное химическое сшивание, основано на использовании химически активных производных лигандов рибосомы — участников процесса трансляции (тРНК, мРНК и пр.), несущих сшивающие группы в определенных положениях. Такие производные сшивают с рибосомами в составе комплексов, моделирующих ту или иную стадию трансляции, и затем определяют, к каким рибосомным белкам и/или нуклеотидам рРНК они ковалентно присоединились. В результате получают информацию о том, с какими структурными элементами рибосомы соседствует фрагмент лиганда, несущий сшивающую группу. Аффинный реагент обычно несет также метку (чаще всего радиоактивную), позволяющую следить за компонентами рибосомы, к которым он присоединился. Как правило, для изучения функциональных центров рибосом использовали аффинные реагенты на основе тРНК или фрагментов мРНК, поскольку получение аффинных реагентов на основе факторов трансляции – намного более сложная задача. Общая схема эксперимента по аффинной модификации рибосом (в качестве примера приведен реакционноспособный аналог мРНК) выглядит следующим образом:

Рибосо́ма — важнейший немембранный органоид живой клетки сферической или слегка эллипсоидной формы, диаметром от 15—20 нанометров (прокариоты) до 25—30 нанометров (эукариоты), состоящий из большой и малой субъединиц. Рибосомы служат для биосинтеза белка из аминокислот по заданной матрице на основе генетической информации, предоставляемой матричной РНК, или мРНК. Этот процесс называется трансляцией.
В эукариотических клетках рибосомы располагаются на мембранах эндоплазматической сети, хотя могут быть локализованы и в неприкрепленной форме в цитоплазме. Нередко с одной молекулой мРНК ассоциировано несколько рибосом, такая структура называется полирибосомой (полисомой). Синтез рибосом у эукариот происходит в специальной внутриядерной структуре — ядрышке.
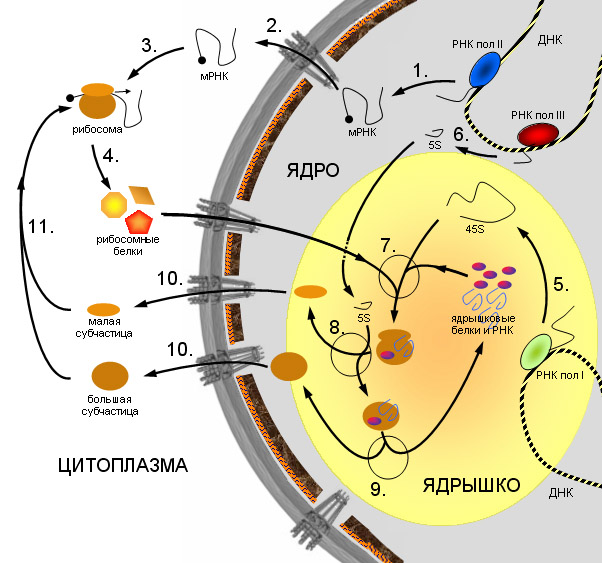

Схема синтеза рибосом в клетках эукариот.
1. Синтез мРНК рибосомных белков РНК полимеразой II. 2. Экспорт мРНК из ядра. 3. Узнавание мРНК рибосомой и 4. синтез рибосомных белков. 5. Синтез предшественника рРНК (45S — предшественник) РНК полимеразой I. 6. Синтез 5S pРНК РНК полимеразой III. 7. Сборка большой рибонуклеопротеидной частицы, включающей 45S-предшественник, импортированные из цитоплазмы рибосомные белки, а также специальные ядрышковые белки и РНК, принимающие участие в созревании рибосомных субчастиц. 8. Присоединение 5S рРНК, нарезание предшественника и отделение малой рибосомной субчастицы. 9. Дозревание большой субчастицы, высвобождение ядрышковых белков и РНК. 10. Выход рибосомных субчастиц из ядра. 11. Вовлечение их в трансляцию.
Рибосомы представляют собой нуклеопротеид, в составе которого отношение РНК/белок составляет 1:1 у высших животных и 60-65:35-40 у бактерий. Рибосомная РНК составляет около 70 % всей РНК клетки. Рибосомы эукариот включают четыре молекулы рРНК, из них 18S, 5.8S и 28S рРНК синтезируются в ядрышке РНК полимеразой I в виде единого предшественника (45S), который затем подвергается модификациям и нарезанию. 5S рРНК синтезируется РНК полимеразой III в другой части генома и не нуждаются в дополнительных модификациях. Почти вся рРНК находится в виде магниевой соли, что необходимо для поддержания структуры; при удалении ионов магния рибосома подвергается диссоциации на субъединицы.
Константа седиментации (скорость оседания в ультрацентрифуге) рибосом эукариотических клеток равняется 80S (большая и малая субъединицы 60S и 40S, соответственно), бактериальных клеток (а также митохондрий и пластид) — 70S (большая и малая субъединицы 50S и 30S, соответственно).
Содержание
История исследований рибосомы

В начале 2000-х появились атомные структуры отдельных субъединиц, а также полной рибосомы, связанной с различными субстратами, которые позволили понять механизм декодинга (распознавания антикодона тРНК, комплементарного кодону мРНК) и детали взаимодействий между рибосомой, антибиотиками, тРНК и мРНК.
Нобелевская премия по химии 2009 года получена за определение структуры прокариотической рибосомы учёным из Великобритании Венкатраманом Рамакришнаном, американцем Томасом Стейцем и израильтянкой Адой Йонат. В 2010 году в лаборатории Марата Юсупова была определена трехмерная структура эукариотической рибосомы. [3]
Механизм трансляции
Трансляция — синтез белка рибосомой на основе информации, записанной в матричной РНК (мРНК). мРНК связывается с малой субъединицей рибосомы, когда происходит узнавание 3'-концом 16S рибосомной РНК комплементарной последовательности Шайн-Далгарно, расположенной на 5'-конце мРНК (у прокариот), а также позиционирование стартового кодона (как правило, AUG) мРНК на малой субъединице. У эукариот малая субчастица рибосомы связывается также с помощью кэпа, на конце мРНК. Ассоциация малой и большой субъединиц происходит при связывании формилметионил-тРНК (fMET-тРНК) и участии факторов инициации (IF1, IF2 и IF3 у прокариот; их аналоги и дополнительные факторы участвуют в инициации трансляции у эукариотических рибосом). Таким образом, распознавание антикодона (в тРНК) происходит на малой субъединице.
После ассоциации, fMET-тРНК находится в P- (peptidyl-) сайте каталитического(пептидил-трансферазного) центра рибосомы. Следующая тРНК, несущая на 3'-конце аминокислоту и комплементарная второму кодону на мРНК, помещается с помощью фактора EF-Tu в А- (aminoacyl-) сайт каталитического центра рибосомы. Затем, образуется пептидная связь между формилметионином (связанным с тРНК, находящейся в Р-сайте) и аминокислотой, принесенной тРНК, находящейся в А-сайте. Механизм катализа образования пептидной связи в пептидил-трансферазном центре до сих пор полностью не ясен. На данный момент существует несколько гипотез, объясняющих детали этого процесса: 1. Оптимальное позиционирование субстратов (induced fit) [5] , 2. Исключение из активного центра воды, способной прервать образование пептидной цепи посредством гидролиза [6] , 3. Участие нуклеотидов рРНК (таких как А2450 и А2451) в переносе протона [7] [8] , 4. Участие 2'-гидроксильной группы 3'-концевого нуклеотида тРНК (А76) в переносе протона [9] ;. Высокая эффективность катализа достигается взаимодействием этих факторов.
После образования пептидной связи, полипептид оказывается связанным с тРНК, находящейся в А-сайте. На следующем этапе деацилированная тРНК двигается из Р-сайта в Е-сайт (exit-), а пептидил-тРНК из А- в Р-сайт. Этот процесс называется транслокацией и происходит при участии фактора EF-G. тРНК, комплементарная следующему кодону мРНК, связывается с А-центром рибосомы, что ведет к повторению описанных шагов. Стоп-кодоны (UGA, UAG и UAA) сигнализируют об окончании трансляции. Процесс окончания трансляции и освобождения готового полипетида, рибосомы и мРНК, называется терминацией. У прокариот он происходит при участии факторов терминации RF1, RF2, RF3 и RRF.

Ранее уже было показано, что рибосомные белки играют в рибосоме вспомогательную роль: они делают ее более стабильной и повышают эффективность ее работы, однако все главные действия, необходимые для синтеза белка, осуществляются не белками, а рибосомными РНК. Это значит, что изначально рибосомы могли состоять только из рРНК, а белки добавились позже. Самый главный этап трансляции — присоединение аминокислот к синтезируемой белковой молекуле (реакция транспептидации) — осуществляется молекулой 23S-рРНК. Поэтому логично предположить, что всё началось именно с этой молекулы.
Однако молекула 23S-рРНК слишком велика и сложна, чтобы появиться в готовом виде в результате случайного комбинирования нуклеотидов. Таким образом, ключевой вопрос состоит в том, могла ли 23S-рРНК произойти от более простой молекулы-предшественницы в результате постепенной эволюции, то есть путем последовательного добавления новых фрагментов. Главный вывод обсуждаемой статьи заключается в том, что структура 23S-рРНК свидетельствует именно о таком ее происхождении.
Возможность последовательной разборки молекулы без повреждения остающихся частей — факт весьма нетривиальный. Все блоки молекулы связаны друг с другом, причем связи эти имеют направленный характер: при их разрыве один блок повреждается, а другой нет. Можно представить систему блоков и связей между ними как множество точек, соединенных стрелками, причем стрелка будет указывать на тот блок, который повреждается при разрыве связи. Если бы эти стрелки образовали хотя бы одну кольцевую структуру (иными словами, если бы мы, двигаясь из какой-то точки по стрелкам, могли вернуться в ту же точку), то разобрать молекулу без повреждения остающихся частей было бы невозможно. Однако ни одной такой кольцевой структуры в молекуле 23S-рРНК не обнаружилось. Если бы направление связей было случайным, вероятность отсутствия кольцевых структур составляла бы менее одной миллиардной. Авторы делают вывод, что это вряд ли результат случайности. По-видимому, структура связей между блоками молекулы отражает последовательность добавления этих блоков в ходе постепенной эволюции молекулы.
По-видимому, проторибосома была просто устроенным рибозимом, катализирующим синтез небольших белковых молекул в РНК-организме. Специфичность синтеза поначалу была очень низкой (аминокислоты выбирались более или менее случайно). В дальнейшем к проторибосоме добавлялись новые блоки, причем добавлялись они таким образом, чтобы не нарушить структуру активного центра молекулы, а также всех тех блоков, которые присоединились ранее. Если очередная мутация приводила к нарушению уже сложившихся структур, она отсеивалась отбором.
Таким образом, 23S-рРНК, при всей ее кажущейся сложности, построена на основе довольно простого принципа. Ее блочная структура свидетельствует о том, что она могла довольно быстро развиться в ходе эволюции из проторибосомы под действием мутаций и отбора.
Источник: Konstantin Bokov, Sergey V. Steinberg. A hierarchical model for evolution of 23S ribosomal RNA // Nature. 2009. V. 457. P. 977–980.
Рибосома является органеллой живой клетки и играет важную роль в её жизнедеятельности. Выполняет биосинтез белка из аминокислот по указанной матрице, основываясь на генетической информации, полученной от матричной м-РНК (рибонуклеиновая кислота). Такой процесс носит название трансляции рибосомы.
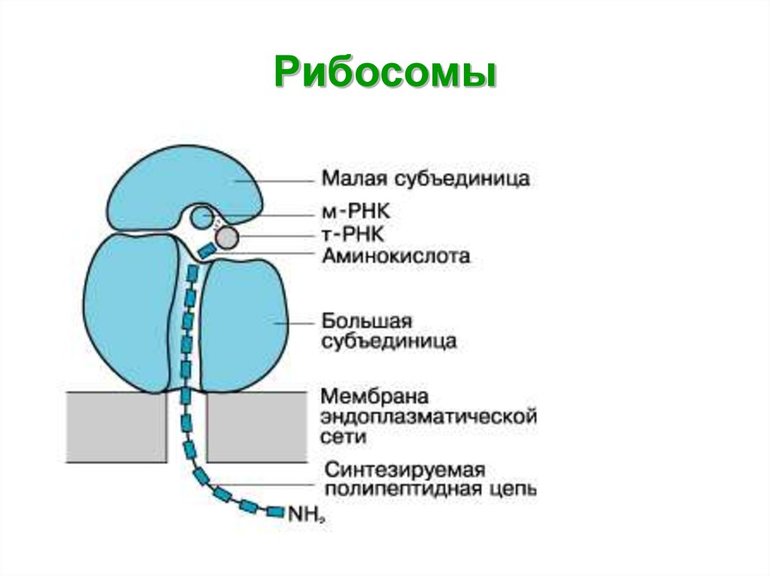
Химический состав
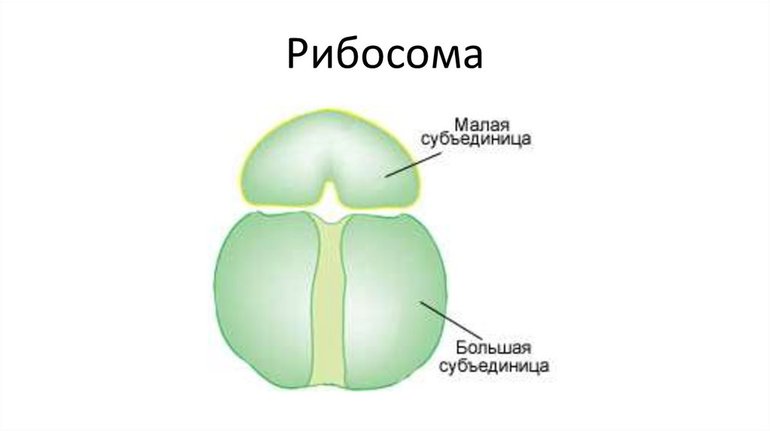
Рибосома напоминает эллипс или сферу, диаметром от пятнадцати до двадцати нанометров у прокариот и от двадцати пяти до тридцати у эукариот. Органелла состоит из маленькой и большой субъединиц.
В клетках с ядром органеллы находятся на мембране эндоплазматической сети, но могут располагаться и в отдельной форме в цитоплазме. Часто с молекулой м-РНК связано больше одной органеллы, подобная структура получила название полисомы (полирибосомы). Нужно понять, где образуются рибосомы у эукариотов. Это осуществляется в специальной структуре внутри ядра — ядрышке.
Рибосомы являются нуклеопротеидом, в котором пропорция белок/рибонуклеиновая кислота равна 50:50 у высших организмов и 65:40 у бактерий. РНК органеллы занимает почти 70% от общей РНК клетки. Органеллы эукариот содержат 4 молекулы р-РHК, из них 18 S (единица измерения Сведберга), 5 S и 28 S р-РНК синтезируются в ядрышке. Практически полностью р-РHК имеет вид магниевой соли. Это обязательное условие для стабильности структуры. Если убрать ионы магния, то органелла расщепляется на субъединицы.
Реакция оседания в центрифуге (постоянная седиментации) у органелл цитоплазмы клеток с выраженным ядром равна 80 S (маленькая и крупная частицы 40 S и 60 S, соответственно), у клеточных рибосом бактерий — 70 (для частиц 30 S и 50 S).
Строение рибосомы
В состав рибосомы входят особые РНК (рибосомные). А также своеобразные белки и малочисленные низкомолекулярные составляющие.
РНК органеллы
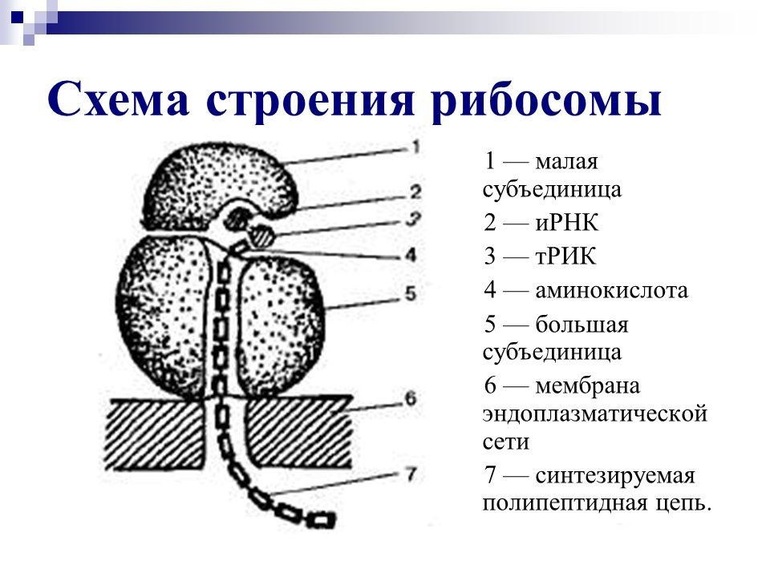
За структуру и работоспособность рибосомы в первую очередь отвечает её РHК. Рибонуклеиновая кислота органеллы или р-РНК в составе органеллы весьма компактна, обладает сложной третичной конструкцией и часто усыпана молекулами разных белков органеллы. Освобождённые от белковых соединений высокомолекулярные р-РHК в особых условиях самостоятельно скручиваются в мелкие частицы, по своей морфологии очень похожие на субчастицы рибосомы, основой которых они и являются.
Исходя из этого, общая схема структурной организации органеллы определяется свойствами р-РHК. Третичное устройство р-РНК служит каркасом для позиционирования рибосомных белков, которые в определённом понимании выполняют лишь второстепенную задачу в образовании и сохранении структуры рибосомы и её жизнедеятельности.
Есть предположение, что развитие органеллы началось ещё в добелковый период, и предшественниками рибосом были своеобразные древнейшие рибозимы. Предполагают, что в процессе эволюции (появление более сложной ступени организации живых организмов) рибозимы, способные к катализации появления амидных соединений тоже поддавались прогрессу (дополнялись различными аппаратами, а со временем и образованными ими полипептидами), вплоть до появления нынешнего модуля для синтеза белка, принимая во внимание рибосому.
Нынешняя органелла по своему содержанию до сих пор остаётся рибозимом, так как главная структурно-функциональная деятельность принадлежит её собственной кислоте, а не белкам, как считалось раньше.
В состав пептидилтрансферазного центра входит только кислота. То обстоятельство, что в то время, как почти во всех процессах жизненного функционала главную задачу выполняют белки, в образовании их самих основная роль принадлежит РНК, обеспечивает весомый аргумент в защиту гипотезы о пространстве РНК как о древнейшем добелковом периоде развития живой ткани.
РНК малой субъединицы
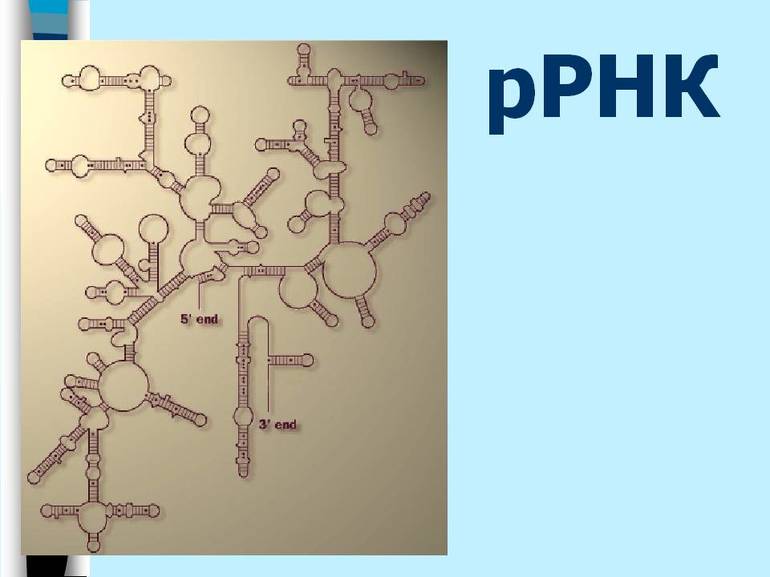
Рибосомная рибонуклеиновая кислота маленькой частицы органоида имеет маркировку 16 S р-РHК в случае органелл бактерий и 16 S -подобная р-РHК в других ситуациях. Чаще всего р-РНК маленькой субъединицы образована из одной ковалентно непрерывной полирибонуклеотидной цепочки.
Число звеньев нуклеотидов, как и постоянной величины седиментации, для экземпляров 16 S-подобных р-РHК из разных источников могут серьёзно отличаться. В рибосомах бактерий и пластидов высших представителей растительного мира эти частицы обладают размером порядка 1500 нуклеотидных остатков.
Для 16 S-подобных р-РНК цитоплазменных рибосом клеток с выраженным ядром, а также для митохондриальных рибосом высших растений и грибов типична длина до 2 тыс. нуклеотидных остатков (18 S р-РHК). Органеллы митохондрий млекопитающих животных содержат довольно короткие 16 S-подобные р-РНК (9 — 12 S), состоящие из 950 нуклеотидных остатков.
Рибонуклеиновая кислота большой частицы
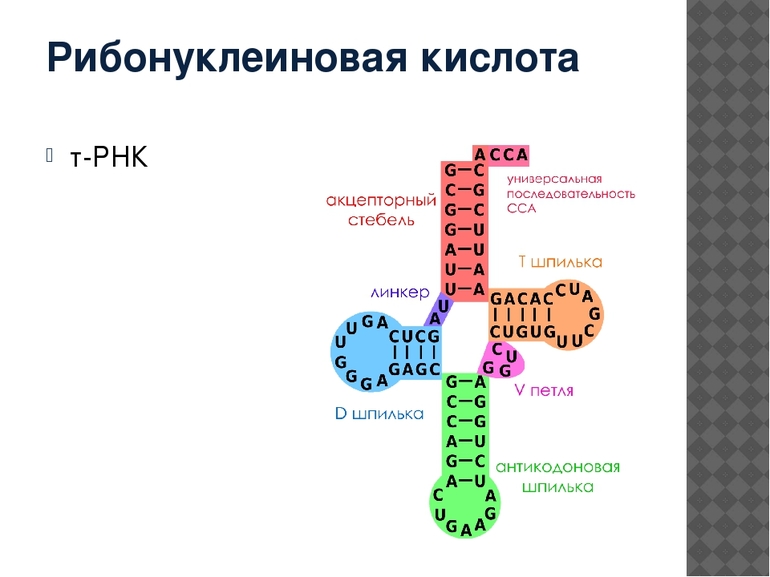
Высокомолекулярная рибонуклеиновая кислота, представляющая основу конструкции большой субъединицы рибосомы, имеет обозначение 23 S р-РHК (для бактерий) и 23 S-подобная р-РНК (для иных случаев). Бактериальная 23 S р-РНК, точно также как и 16 S р-РHК имеет вид полирибонуклеотидной ковалентно непрерывной цепочки.
Вместе с этим 23 S-подобная р-РНК органеллы цитоплазмы эукариотических клеток включает в себя две прочно сгруппированных полирибонуклеотидных цепочек — 28 S и 5,8 S р-РHК. Таким же образом 23 S-подобная р-РHК рибосом пластидов растительных видов состоит из двух крепко соединённых полирибонуклеотидных цепей и включает 4,5 S р-РНК.
Белки органоида
Кроме р-РНК, в состав органеллы входят порядка пятидесяти (прокариоты) или восьмидесяти (эукариоты) разных белков. Почти каждый из них имеет один лишь экземпляр на отдельную рибосому. Доминируют умеренно-осно̀вные белки. Бо̀льшая часть белков органоида эволюционно консервативна, а белки от разных ресурсов могут соотноситься как подобные. Это учитывается в нынешнем универсальном перечне рибосомных белков. Сама органелла состоит почти на 50% из белка.
Помимо биополимеров (белки, рибонуклеиновая кислота) составными частями рибосом являются отдельные низкомолекулярные составляющие. Это частицы воды, ионы металлов (в основном Mg 2+ ), поли- и диамины, которые могут составлять до 2,5% сухой массы рибосомы.
Механизм трансляции
Трансляция — это процесс образования белка из аминокислот на матрице информационной (матричной) кислоты (и-РНК, м-РHК), приводимый в действие рибосомой.
Основной задачей функционирования живой клетки считается биосинтез белка. Для воспроизведения этой операции абсолютно во всех клеточных организмах находятся рибосомы. Они являются рибонуклеопротеидными комплексами, в которых участвуют малая и большая субъединицы. Роль рибосомы состоит:
- в распознавании трехнуклеотидных кодонов м-РНК;
- в соотношении соответствующих им антикодонов т-РНК, переносящих аминокислоты;
- во включении этого груза в увеличивающуюся белковую цепь.
Прикрепление аминокислот к т-РНК происходит в энергозависимой реакции с помощью ферментов аминоацил-т-РHК-синтетаз, а образованная молекула носит название аминоацил-т-РНК. Следовательно, вся специфика трансляции может быть определена взаимосвязью кодона м-РНК и антикодона т-РНК, а также характерной особенностью аминоацил-т-РНК-синтетаз, прикрепляющим аминокислоты точно к соответствующим т-РНК.
Механизмы трансляции эукариотических и прокариотических клеток имеют серьезное отличие, из-за этого множество соединений, угнетающих трансляцию прокариот, в меньшей мере оказывает влияние на трансляцию высших особей. Такая особенность позволяет применять их в медицине в виде противобактериальных средств, не приносящих вред организму млекопитающих. Если кратко, то вся процедура трансляции подразделяется на три основных этапа:
- инициация — распознавание рибосомой стартового кодона и начало синтеза;
- элонгация — сама операция образования белка;
- терминация — опознавание терминирующего кодона и отделение продукта.
История исследований
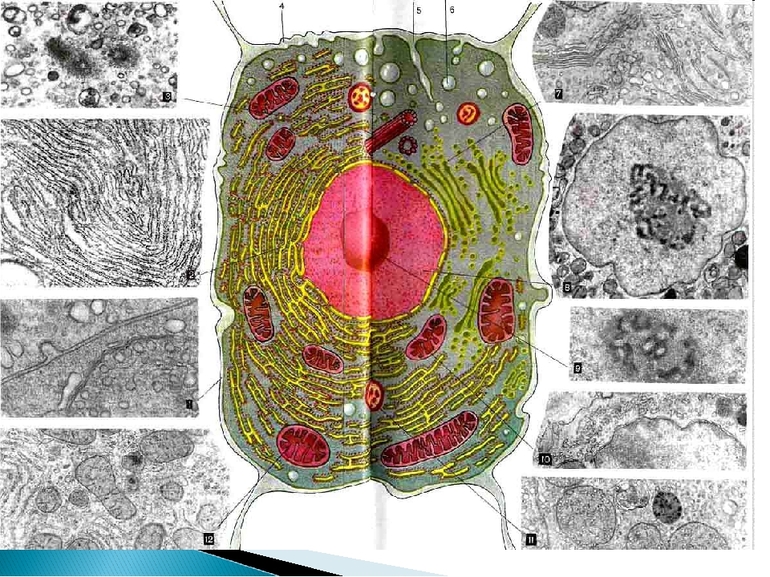
Органеллы изначально были определены как уплотнённые частички. Это сделал уроженец Румынии, гражданин Америки и клеточный биолог Джордж Паладе в 50-х гг. XIX в. В 1974 г. ему и Кристиану Де Дюву вручили Нобелевскую премию по медицине и физиологии за прорыв в знаниях о структурной и функциональной деятельности клетки.
В начале 2000-х гг. были созданы модели с атомным разрешением (до 2,4 А) конструкций отдельных субъединиц, а также полной рибосомы прокариот, связанной с разными субстратами, позволившими осознать устройство декодинга (узнавание антикода т-РНК, соответствующего кодону м-РНК) и подробности взаимосвязи рибосомы, т-РНК, м-РНК, причины трансляции и разных антибиотиков.
- американец Томас Стейц.
- британец уроженец Индии Венкатраман Рамакришнан.
- гражданка Израиля Ада Йонат.
В 2010 г. в лаборантской Марата Юсупова была открыта трёхмерная конструкция рибосомы эукариот.

В 2009 г. биохимики из Канады Сергей Штейнберг и Константин Боков из университета Монреаля, изучив третичную структуру кислоты рибосомы бактерии Escherichia coli, выдвинули обоснованную гипотезу о том, что органелла могла зародиться в результате постепенного эволюционного развития из простейшей малой молекулы РНК — проторибосомы, способной к катализации реакции соединения двух аминокислот.
Все оставшиеся конструктивные блоки рибосомы постепенно добавлялись к проторибосоме, не изменяя её строение и планомерно увеличивая продуктивность её деятельности.
Еще в школе детей начинают знакомить с рибосомой. Ее функционал перестал оставаться тайной для человека. Может показаться, что все загадки относительно этого органоида разгаданы. Однако за последние десятилетия в области исследования рибосом происходит значительный переворот.
Читайте также:

